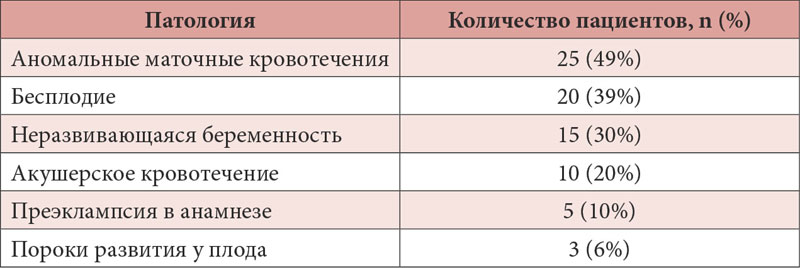
Метилфолат
Метилфолат (англ. MethylFolate) — это синтетическое производное вещество из группы фолатов. В различных источниках оно именуется как метафолин, L-метилфолат или L-5-MTHF. В последние годы это соединение активно изучается на предмет использования для лечения широкого спектра заболеваний.
Метилфолат: фолиевая кислота
Метилфолат — это ни что иное как одна из наиболее биологически активных форм фолиевой кислоты (витамина B9). Как известно, фолиевая кислота играет весьма важную роль для здоровья человека, однако в чистом виде проникнуть сквозь гематоэнцефалический барьер (барьер между кровеносной и центральной нервной системами) она неспособна. Лишь после целого ряда преобразований, под воздействием специальных ферментов эта кислота трансформируется в более доступные формы фолатов, в том числе и метилфолат. Однако эти метаболические процессы не у всех протекают одинаково. У части людей наблюдается мутация некоторых генов (например, MTHFR), нарушающих адекватное преобразование витамина B9 в биодоступную форму. Другими словами, фолиевая кислота у них усваивается очень плохо или не усваивается вовсе. Именно в таких случаях препараты с метилфолатом особенно актуальны. В отличие от фолиевой кислоты он беспрепятственно всасывается в систему кровообращения и потребляться клетками. Важным преимуществом использования метилфолата является то, что в этом случае риск накопления неизмененных фолатов в крови отсутствует, а сам он не несет токсической опасности для организма.
Метилфолат: состав
Как уже говорилось, метилфолат входит в состав группы фолатов — различных форм водорастворимой фолиевой кислоты. Эти соединения не синтезируются организмом и поступают из пищи или в виде пищевых добавок. Источником фолатов являются:
- бобовые культуры,
- зеленые листовые овощи,
- печень,
- яичный желток,
- цитрусовые.
Однако, большинство этих фолатов не являются метаболическими активными соединениями. Для того чтобы участвовать в метаболических процессах, им необходимо пройти сложных процесс преобразований и лишь метилфолат легко проникает в центральную нервную систему.
Метилфолат: свойства
Поскольку метилфолат является одной из форм фолиевой кислоты, он обладает теми же свойствами, что и она:
- участвует в процессе образования окиси азота из аргинина;
- контролирует уровень гомоцистеина в плазме крови;
- оказывает влияние на эффективность нейронных передатчиков и отвечает за осуществление когнитивных функций;
- играет значительную роль в процесс физиологического деления и роста всех клеток организма.
Таким образом, метилфолат — весьма перспективное средство для профилактики и лечения разного рода заболеваний, в том числе и психосоматических расстройств, и депрессий.
Помимо этого, метилфолат, в отличии от фолиевой кислоты, обладает способностью восстанавливать функцию эндотелиальных клеток у пациентов с гиперхолестеринемией – генетического заболевания, характеризующегося высоким уровнем холестерина в крови.
Метилфолат: гомоцистеин
По мнению ученых, важнейшей заслугой метилфолата является его способность влиять на количество аминокислоты гомоцистеина (продукта обмена метионина) в организме. Более 80 исследований доказывают, что повышение уровня гомоцистеина чревато увеличением количества свободных радикалов и развитием сердечно-сосудистых заболеваний, в том числе инсульта, инфаркта, геморрагии и тромбоза. Кроме того, отклонение показателей количест
herbhelp.ru
Фолиевая кислота 4-го поколения в составе средства Миофолик
Фолаты, фолиевая кислота и фолиевая кислота 4-го поколения: в чем разница?
Фолат (вітамін B9) — це важлива поживна речовина, необхідна для синтезу ДНК. Крім того, це субстрат, Фолаты, фолиевая кислота и фолиевая кислота 4-го поколения: в чем разница?
Фолат (витамин B9) – это важное питательное вещество, необходимое для синтеза ДНК. Кроме того, это субстрат, необходимый для целого ряда ферментативных реакций, которые происходят в процессе синтеза аминокислот и метаболизма витаминов. Потребность в фолатах в период беременности возрастает, поскольку они нужны для роста и развития плода. Дефицит фолатов связывают с развитием нарушений как у мамы (анемия, периферическая невропатия), так и у плода (врожденные аномалии развития). Фолат или витамин B9 считается одним из 13 незаменимых витаминов. Фолаты не синтезируются в организме, их нужно получать либо из пищи, либо посредством дополнительного приема
Пищевые фолаты – это питательные вещества, присутствующие в натуральных пищевых продуктах, таких как зеленые листовые овощи, бобовые, яичный желток, печень и цитрусовые.
Фолиевая кислота – цэто синтетическая пищевая добавка, которая присутствует в обогащенных пищевых продуктах и витаминных препаратах.
Фолаты и фолиевая кислота не являются метаболически активными. Чтобы участвовать в клеточном метаболизме, они должны превратиться в активную форму – 5-метилтетрагидрофолат.
5-метилтетрагидрофолат – это это фолиевая кислота 4-го поколения,является доминирующей формой фолата. Именно она циркулирует в плазме крови и участвует в биологических процессах (в 1 саше Миофолик содержится 200 мкг фолиевой кислоты 4-го поколения)).
Метаболизм фолиевой кислоты
 В пище и в большинстве препаратов содержится биологически неактивная форма фолиевой кислоты. Попадая в организм она под действием фермента метилтетрагидрофолат редуктазы (MTHFR) преобразуется в активную форму фолиевой кислоты — 5-метилтетрагидрофолат. Именно эта активная форма усваивается организмом и затем участвует в сложных биохимических процессах.
В пище и в большинстве препаратов содержится биологически неактивная форма фолиевой кислоты. Попадая в организм она под действием фермента метилтетрагидрофолат редуктазы (MTHFR) преобразуется в активную форму фолиевой кислоты — 5-метилтетрагидрофолат. Именно эта активная форма усваивается организмом и затем участвует в сложных биохимических процессах.
В Европе около 30-40% населения имеют генетическую мутацию (C677T полиморфизм), которая приводит к неспособности усваивать фолиевую кислоту из пищи или пищевых добавок.
Именно поэтому была синтезирована фолиевая кислота 4-го поколения (5-метилтетрагидрофолат), усвоение которой не зависит от возможной мутации гена MTHFR. Она обладает высокой биодоступностью и не нуждается в дополнительном метаболизме в организме.

miofolic.com
Преимущества проведения коррекции фолатного статуса с использованием метафолина — метафолин солгар — запись пользователя Kate (id925041) в сообществе ЭКО — мама в категории Библиотека: статьи, полезная информация. Стихи, видео и фильмы про ЭКО…
фолиевая кислота состав таблеткиОтличная статья, журнал "Трудный пациент" за сентябрь 2013 г. Наконец-то, не только мы, но и наши врачи убедились в преимуществах метафолина при мутации MTHFR, по сравнению с обычной фолькой (источник). Лед тронулся!
Фолиевая кислота - вещество, полученное путем химического синтеза, которое не является метаболически активным. Метафолин® - синтетической производное, созданное на базе 5-метил-тетрагидрофолата. Преимуществами метафолина являются: непосредственное поступление в организм вещества в биологически активной форме и наличие оптимального эффекта, даже в случае наличия у пациента гомозиготного и/или гетерозиготного генотипов 677C T полиморфизма метилтетрагидрофолатредуктазы (MTHFR). С учетом высокого показателя распространенности генетических полиморфизмов МТГФР (MTHFR) среди населения и проблем, связанных с пониженной активностью МТГФР, с целью профилактики и лечения различных патологических состояний, связанных с дефицитом фолатов во время беременности,
целесообразно применять витаминно-минеральные комплексы, содержащие метафолин - активную форму фолатов с высокой биодоступностью. Ключевые слова: фолиевая кислота, метафолин, МТГФР, беременность.
Сведения об авторах:
Ших Евгения Валерьевна - д.м.н., профессор, кафедра клинической фармакологии и пропедевтики внутренних болезней Первого МГМУ им. И.М. Сеченова
Махова А.А. - к.м.н., кафедра клинической фармакологии и пропедевтики внутренних болезней Первого МГМУ им. И.М. СеченоваВведение
Постоянный интерес специалистов к фолатам объясняется тем, что учеными установлена роль этого витамина в лечении широкого спектра различных заболеваний. В 1931 г. Люси Уилс описала эффективность экстракта дрожжей в борьбе с тропической макроцитарной анемией на поздних сроках беременности в условиях Индии. Это был первый в мире опыт использования фолатов для профилактики болезней. В 1991 г. группа по исследованию витаминов при Медицинском исследовательском совете подтвердила значение применения фолатов на ранних сроках беременности для предотвращения развития патологии позвоночника плода [1].
В 1995 г. был опубликован анализ 27 исследований более чем у 4000 пациентам с сосудистыми заболеваниями и таким же числом пациентов в контроле, подтвердивший, что гомоцистеин является независимым дифференцированным фактором риска в отношении атеросклероза коронарных, церебральных и периферических сосудов. Снижение уровня гомоцистеина путем образования метионина открыло новые возможности для использования фолатов в профилактике болезней [2].Фолиевая кислота в профилактике и лечении заболеваний
Фолиевая кислота, гипергомоцистеинемия и риск сердечно-сосудистых заболеваний. По результатам более чем 80 исследований показано, что даже умеренное повышение уровня гомоцистеина в крови увеличивает риск сердечно-сосудистых заболеваний. Анализ обсервационных исследований показал, что длительное снижение уровня гомоцистеина в плазме крови только лишь на 1 ммоль/л приводит к снижению сердечно-сосудистого риска на 10%. Из трех витаминов, которые регулируют уровень гомоцистеина, фолиевая кислота имеет наибольший эффект в снижении базального уровня гомоцистеина в крови, при отсутствии существенного дефицита витамина B12 или витамина В6.Диета, богатая фолиевой кислотой связана с пониженным риском сердечно-сосудистых заболеваний [3]. Исследование, проведенное в Финляндии в течение 10 лет показало, что те мужчины, которые потребляли большее количество пищевых фолатов имели на 55% более низкий риск острых коронарных событий по сравнению с теми, кто потреблял меньшее количество фолатов [4]. Увеличение потребления фолатов с пищей или продуктами, обогащенными фолиевой кислотой приводит к снижению уровня гомоцистеина [5]. Недавно проведенный метаанализе 25 рандомизированных контролируемых исследований показал, что дополнительный прием 0,8 мг фолиевой кислоты максимально уменьшает уровень гомоцистеина в плазме; в суточных дозах 0,2 и 0,4 мг фолиевой кислоты был связан с 60% и 90% снижением уровня гомоцистеина в плазме крови соответственно. Американская ассоциация Сердца рекомендует дополнительный прием 400 мкг фолиевой кислоты, 2 мг витамина В6 и 6 мкг витамина В12 в качестве стартовой терапии гипергомоцистеинемии, в случае, если диета, богатая фолатами, не приводит к адекватному снижению уровня гомоцистеина в плазме крови [6]. При этом, хотя дополнительный прием фолиевой кислоты приводит к снижению уровня гомоцистеина в плазме крови, остается не известным, снижает ли фолиевая кислота риск сердечно-сосудистых заболеваний. Онкологические заболевания. Предполагается, что рак, происходит от повреждения ДНК, когда процессы репарации замедлены или при чрезмерной экспрессии некоторых генов. Поскольку фолиевая кислота играет важную роль в синтезе ДНК и РНК и метилировании, возможно, что фолаты могут влиять на процессы репарации ДНК и экспрессии генов. Обсервационные исследования показали, что пониженный статус по фолиевой кислоте связан с повышением рака шейки матки, толстой и прямой кишки, легких, пищевода, головного мозга, поджелудочной железы и молочной железы. Интервенционные исследования по фолиевой кислоте в организме человека были проведены главным образом по отношению к раку шейки матки и колоректальному раку. Сочетание высокого потребления алкоголя с одновременным низким потреблением фолиевой кислоты приводит к повышенному риску развития рака толстой кишки [7]. Однако не следует забывать, что связь между приемом фолиевой кислоты, уровнями фолатов в крови и онкологическими заболеваниями двунаправленна: онкологический риск повышается как при дефиците, так и при избытке фолиевой кислоты [8]. Болезнь Альцгеймера и когнитивные нарушения. Роль фолиевой кислоты в синтезе нуклеиновых кислот и реакций метилирования имеет важное значение для нормального функционирования мозга. За последнее десятилетие в нескольких исследованиях описана связь между снижением уровня фолатов и когнитивными нарушениями у пожилых людей [9]. В большом перекрестном исследовании у пожилых канадцев обнаружили, что люди, имеющие низкий уровень фолиевой кислоты в сыворотке крови, имеют больший риск развития слабоумия и депрессии. В похожем исследовании, низкие сывороточные уровни фолата были связанны с проблемами с краткосрочной памятью у пожилых людей, которые не имели признаков деменции [10]. Исследования разных авторов дают противоречивые сведения относительно влияния фолиевой кислоты на риск болезни Альцгеймера. В одном из исследований у пожилых людей преимущественно испанской и афро-американской этнических групп с высоким риском сердечно-сосудистых заболеваний было обнаружено, что более высокое потребление фолиевой кислоты связано с пониженным риском развития болезни Альцгеймера [11]. Другое проспективное исследование у пожилых людей выявило, что пищевые фолаты не влияют на развитие болезни Альцгеймера [12]. Умеренное повышение уровня гомоцистеина, так же как и снижение уровня фолатов и витамина В12 ассоциировано с болезнью Альцгеймера и сосудистыми деменциями. В исследовании, проведенном у 370 пожилых мужчинах и женщинах, в течение 3 лет низкий сывороточный уровень фолатов (<10 нмоль/л) или витамина В12 (<150 пмоль/л) был ассоциирован с двойным риском развития болезни Альцгеймера [13]. Фолаты при беременности
Профилактика пороков развития плода. Частота диагностики дефектов нервной трубки (ДНТ) плода в России составляет около 0,5%; ежегодно погибают до 300 новорожденных с этим диагнозом, что составляет примерно 2% в структуре общей детской смертности [14].
Рост и развитие плода характеризуются повышенное клеточной продукцией. Адекватное поступление фолатов является критическим для синтеза ДНК и РНК. ДНТ являются врожденными пороками развития, иногда фатальными, характеризующимися анэнцефалией или расщеплением позвоночника (spina bifida). Дефекты возникают между 21 и 27 днем гестации. Это период, когда многие женщины, еще не знают о своей беременности [15].
Результаты рандомизированных исследований показали 60-100% сокращение ДНТ, в случае дополнительного потребления женщинами фолиевой кислоты на фоне полноценного разнообразного питания на протяжении одного месяца до зачатия и одного месяца после зачатия. В США рекомендуется употребление 400 мкг фолиевой кислоты ежедневно всем женщинам, репродуктивного возраста для предотвращения ДНТ, кроме этого с 1998 г. все зерновые продукты дополнительно обогащаются фолиевой кислотой, что привело к 26% снижению данных пороков развития плода. В Канаде, где так же проводится обогащение продуктов питания аналогичное США (1,5 и 1,4 мг фолиевой кислоты/кг зерна соответственно), сообщается о большем снижении частоты случаев ДНТ до 50% [16, 17].
Известным является факт, что чем ниже уровень фолатов в эритроцитах крови, тем выше риск рождения ребенка с пороком развития нервной трубки. Достаточный с точки зрения профилактики ПРНР уровень фолатов составляет >906 нмоль/л.
В вопросе преконцепционной профилактики дефектов нервной трубки, как наиболее статистически значимого осложнения фолатного дефицита, современная российская ситуация ничем не уступает таковой в странах Евросоюза. Эффективность первичной профилактики показала, что у пар, принимавших фолиевую кислоту до зачатия, частота ДНТ плода по итогам многолетних наблюдений снижается в 3 раза по сравнению с популяционной распространенностью данной группы пороков.
Фолиевая кислота напрямую участвует в формировании сосудистого русла плаценты и нарушения ангиогенеза в этой области ассоциированы с патогенезом преэклампсии и фетоплацентарной недостаточности, в том числе с задержкой роста и антенатальной гибелью плода [14].
Адекватное потребление фолиевой кислоты способствует также предотвращению возникновения других видов врожденных пороков, в том числе пороков сердца и недоразвития конечностей. Кроме того, низкий уровень потребления фолатов во время беременности ассоциируются с повышенной частотой преждевременных родов и низкой массой тела младенца при рождении. В последнее время считается, что повышенное содержание в крови гомоцистеина, является индикатором функциональной фолатной недостаточности и связывается с повышенным риском выкидыша и таким осложнениями беременности как эклампсия и преждевременная отслойка плаценты [18]
Дефицит фолиевой кислоты приводит к реализации наиболее неблагоприятных звеньев патогенеза артериальной гипертензии у беременных - к тотальной ангиопатии, микротромбозам, нарастанию инсулинорезистентности.
Согласно данным, опубликованным в зарубежной литературе, фолатный дефицит и полиморфизм метилтетрагидрофолатредуктазы связаны с отслойкой или инфарктами плаценты, спонтанными абортами, привычным невынашиванием вследствие распространенных дефектов формирования и созревания элементов трофобласта и плацентарного сосудистого русла; преэклампсией [19].
Таким образом, есть основания для продолжения дополнительного потребления фолиевой кислоты в течение всей беременности, даже после закрытия нервной трубки, чтобы уменьшить риск других возможных осложнений.
В последние годы получены многочисленные доказательства того, что среди женщин с осложненной беременностью значительно чаще встречаются гомозиготные (ТТ) и даже гетерозиготные (СТ) генотипы. Таким образом, в некоторых случаях недостаточно и неэффективно употреблять просто фолиевую кислоту. В связи с этим с целью коррекции фолатного статуса во время беременности целесообразно использовать биологически активные формы фолатов в виде 5-метилтетрагидрофолата (метафолин).Контрацепция и фолиевая кислота
Поскольку реально проходящих полноценную предгравидарную подготовку женщин гораздо меньше, чем нуждающихся в коррекции фолатного дефицита, необходимость альтернативных путей обеспечения пациенток препаратами фолиевой кислоты как для России, так и для других стран является актуальной.
На совещании Надзорного комитета по препаратам для репродуктивного здоровья FDA в 2003 г. было выдвинуто предположение о том, что комбинированные оральные контрацептивы (КОК) могут служить обоснованным методом доставки фолатных добавок в организм женщин детородного возраста.
Добавление фолата в состав современных микродозированных КОК может существенно снизить процент ДНТ в популяции - только среди женщин, принимающих гормональные контрацептивы, число незапланированных беременностей исчисляется миллионами случаев в год, что связано с погрешностями при использовании метода (пропуск таблетки и др.).
По данным Американского общества по репродуктивной медицине (2010), прием КОК с метафолином снижает частоту ДНТ на 23,7-31,4% в сравнении с пациентками, использующими обычные гормональные контрацептивы [19].Рекомендации по приему фолатов
По данным крупных исследований, включающих десятки тысяч человек, большинство взрослых людей потребляют меньше фолатов, чем это установлено нормами. В частности, изучение потребления фолатов населением Германии на протяжении 1997-2000 гг. показало, что в среднем потребление фолатов взрослыми составляет 250 мкг/сут вместо установленных для Германии 320 мкг/сут. При этом у 25% женщин детородного возраста содержание фолата в эритроцитах и плазме крови снижено.
Наибольшие количества фолиевой кислоты содержат такие продукты, как печень, дрожжи, листовые овощи (шпинат, петрушка, салат латук, перо лука и др.). Необходимый уровень фолатов может обеспечить потребление 800 г свежего салата, 500 г свежей петрушки или 500 г вареной печени в день, что маловероятно в реальной жизни. Таким образом, очевидно, что в большинстве случаев не обойтись без дополнительного приема витаминно-минеральных комплексов.
Беременным и кормящим женщинам рекомендуется употреблять 400-800 мкг/сут, а всем остальным - 400 мкг/сут фолатов, верхний предел физиологической потребности - 1000 мкг (Нормы РФ, 2008). Суточная доза потребления фолиевой кислоты для женщин репродуктивного возраста для беременных с неотягощенным акушерским анамнезом составляют 400-600 кг/сут, для кормящих - 500 мкг/сут [8].
Учитывая высокий показатель распространенности генетических полиморфизмов МТГФР (MTHFR)среди населения и проблемы, связанные с пониженной активностью фермента, и соответственно меньшим количеством биологически доступного L-метилфолата, вопросы коррекции фолатного статуса стали фокусироваться скорее на использовании L-метилфолата, а не на дополнительном приеме фолиевой кислоты в качестве средства профилактики патологий, связанных с дефицитом фолатов.Фолаты, фолиевая кислота, L-метилфолат и Метафолин
Термин фолаты обычно используется как непатентованное название для группы химически родственных соединений на основе структуры фолиевой кислоты.
Фолат или витамин B9 считается одним 13 незаменимых витаминов. Фолаты не синтезируются заново в организме, их нужно получать либо из пищи, либо посредством дополнительного приема. Пищевые фолаты - это питательные вещества, присутствующие в натуральных пищевых продуктах, таких как зеленые листовые овощи, бобовые, яичный желток, печень и цитрусовые. Фолиевая кислота - это синтетическая пищевая добавка, которая присутствует в обогащенных пищевых продуктах и витаминных препаратах. Ни фолаты, ни фолиевая кислота не являются метаболически активными. Биологической активностью обладают лишь тетрагидрофолат и его производные, а фолиевая кислота сама по себе не является биологически активным соединением.
Чтобы участвовать в клеточном метаболизме, фолиевая кислота и фолаты должны подвергнуться редуцированию. L-5-метилтетрагидрофолат (L-метилфолат) является доминирующей формой фолата, которая циркулирует в плазме крови и участвует в биологических процессах [20].
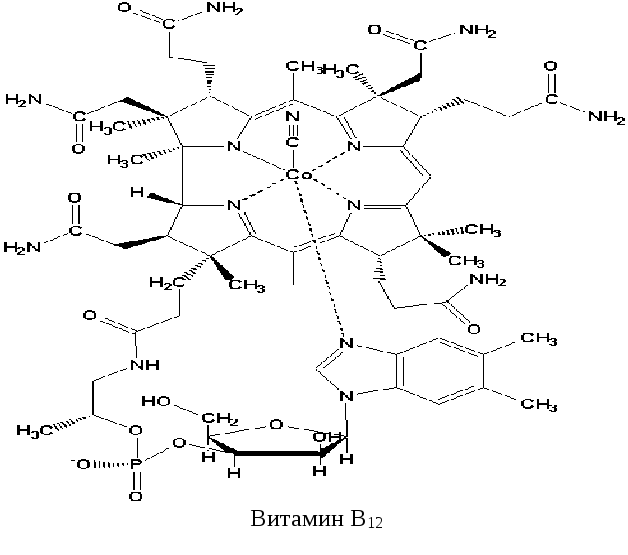
Метафолин синтетической производное, созданное на базе 5-метил-тетрагидрофолата. Единственное различие между Метафолином и 5-MТГФ - присутствие иона кальция. В организме Метафолин распадается на ионы кальция и 5-МТГФ. Метафолин (кальциевая соль L-5-метилтетрагидрофолиевой кислоты) - молекула, идентичная фолатам, содержащимся в пищевых продуктах и организме человека (рис. 1).Метафолин имеет ряд преимуществ, к которым в первую очередь относятся непосредственное поступление в организм вещества в биологически активной форме и наличие оптимального эффекта, даже в случае наличия у пациента гомозиготного и/или гетерозиготного генотипов 677C T полиморфизма MTГФР.
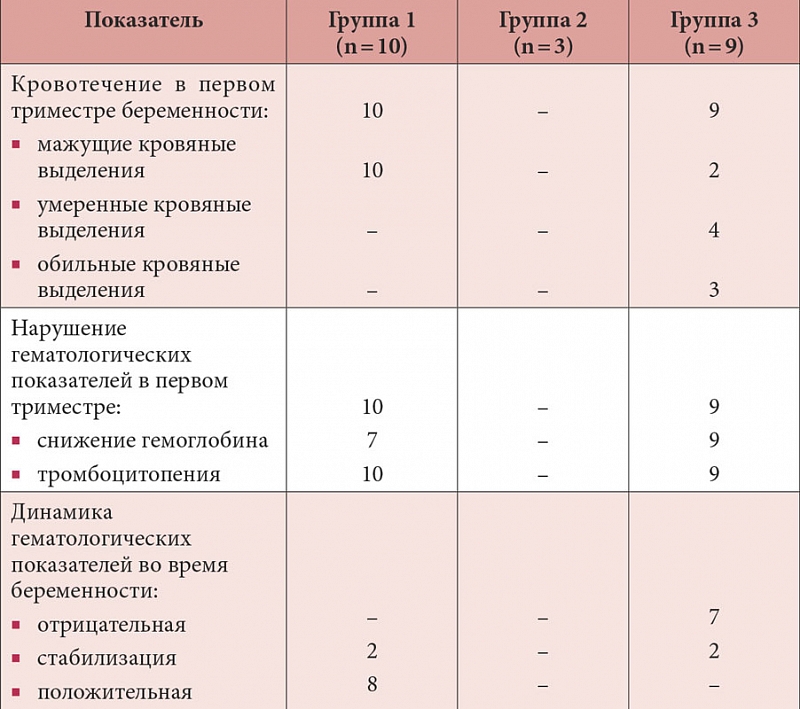
Чтобы превратиться в метаболически активную форму, фолиевая кислота должна сначала превратиться в дигидрофолат (ДГФ), а затем в тетрагидрофолат (ТГФ) посредством ферментативного восстановления, которое катализируется ферментом ДГФ редуктазой (ДГФР). Затем ТГФ с помощью фермента метилентетрагидрофолатредуктазы может превратиться в биологически активную форму L-метилфолат (МТГФР). Это ключевое превращение нужно, чтобы обеспечить L-метилфолат для реакции переноса одноуглеродных групп (передача метила), необходимого для синтеза пурина/пиримидина в процессе сборки ДНК и РНК, для метилирования ДНК и для регулирования метаболизма гомоцистеина (рис. 2) МТГФР является важнейшим ферментом практически для всех биологических процессов, которые включают метаболизм фолатов и метионина [20].
Метаболизм гомоцистеина - промежуточного звена в обмене серосодержащих аминокислот, представляет собой пример взаимосвязи питательных веществ, необходимых для оптимального физиологического функционирования организма человека. У здоровых людей работают два различных пути метаболизма гомоцистеина. Один путь синтезирует метионин из гомоцистеина и зависит от фолатных коферментов и витамин B12-зависимого фермента. Другой путь-преобразование гомоцистеина в аминокислоту-цистеин, требует двух витамин B6-зависимых ферментов. Таким образом, количество гомоцистеина в крови регулируется тремя витаминами: фолиевой кислотой, витамином B12, витамином B6 [21].
Генетические полиморфизмы и метаболизм фолиевой кислоты
В процессе метаболизма фолатов важную роль играет полиморфизм генов. В организме каждой второй женщины из-за ограниченной активности ферментов фолиевая кислота не может полностью превратиться в биологически активную форму - 5-метилтетрагидрофолат.
Фермент 5,10-метилентетрагидрофолатредуктаза (МТГФР) катализирует восстановление 5,10-метилентетрагидрофолата до 5-МТГФ, что необходимо для превращения гомоцистеина в метионин за счет присоединения углеродного остатка. Существует вариант гена МТГФР, в котором цитозин в положении 677 заменен на тимин (полиморфизм 677C/Т), в результате чего аминокислота аланин замещается валином. Среди европейцев с полиморфизмом данного гена 12% составляют гомозиготы (ТТ), 43% - гетерозиготы (СТ), а 45% - аллели "дикого типа" (СС). В условиях in vitro активность фермента в случае генотипа ТТ снижена на 75% по сравнению с аллелем "дикого типа" СС, что ассоциировано с повышением сывороточного уровня гомоцистеина как следствие подавления синтеза 5-МТГФ (это становится особенно заметным при низком содержании в крови фолиевой кислоты). Более того, установлено, что вариант гена МТГФР 677CТ служит генетическим фактором риска дефектов нервной трубки, вызывая до 19% случаев этой разновидности пороков развития [22, 23].
В ходе недавно завершенных клинических испытаний было показано, что 5-МТГФ не менее эффективен по сравнению с фолиевой кислотой с точки зрения содержания фолатов в крови и эритроцитах; он также снижает уровень гомоцистеина как у клинически здоровых лиц, так и при наличии какой-либо патологии. Ранее при проведении исследований не принималось во внимание существование мутантного генотипа МТГФР (677CТ), генотип ТТ исключался, или же работа велась в небольших группах пациентов с гомозиготным генотипом, которым назначили разное лечение. Таким образом, до последнего времени данные о влиянии [6S]-5-МТГФ и фолиевой кислоты на содержание фолатов в крови у лиц генотипом ТТ были ограничены.
В отличие от [6S]-5-МТГФ, фолиевая кислота должна быть восстановлена путем замены одного углеродного остатка. Этот процесс катализирует МТГФР. Затем продукт метаболизма в виде 5-МТГФ поступает в системный кровоток. Следовательно, в случае снижения активности МТГФР (что характерно для генотипа ТТ) эффект фолиевой кислоты относительно сывороточного уровня фолатов выражен в меньшей степени по сравнению с [6S]-5-МТГФ.
Из баз данных предыдущих исследований, проводимых Институтом питания (Университет Бонна, Германия)были отобраны с мутацией гена МТГФР 677C/Т по генотипу ТТ или СС клинически здоровые женщины репродуктивного возраста с индексом массы тела 17-25 кг/м2, нормальными показателями общего и биохимического анализов крови, соответствующим содержанием фолатов (>6,8 нМ в плазме крови и >317 нМ в эритроцитах) и витамина В12 (>110 рМ в плазме крови). Испытуемые придерживались стандартного режима питания в течение 4 недель до начала исследования и на протяжении всего срока его проведения, избегая при этом дополнительного приема витаминов или употребления пищи, обогащенной фолатами.
В соответствии с дизайном было проведено рандомизированное двойное слепое перекрестное исследование. Клиническая часть заняла три дня (скрининг, день I и день II), причем скрининг выполнялся за 12 дней до первого дня исследования. День I и день II были разделены промежутком в 6 суток (период отмывки). Испытуемым назначали таблетки немедленного высвобождения, покрытые пленчатой оболочкой, которые содержали 400 мкг фолиевой кислоты или 416 мкг [6S]-5-МТГФ. Женщин подвергли рандомизации для выбора одной из схем назначения исследуемых препаратов - [6S]-5-МТГФ - в первый день и фолиевая кислота - во второй день или фолиевая кислота - в первый день и [6S]-5-МТГФ - во второй день. Рандомизацию стратифицировали в соответствии с полиморфизмом гена МТГФР 677C/Т, чтобы обеспечить одинаковое распределение генотипов ТТ и СС в обеих группах назначения препаратов. Утром первого и второго дней исследования у пациенток брали кровь натощак (после 12-часового перерыва в приеме пищи). Сразу после взятия анализа крови испытуемые однократно принимали фолиевую кислоту или [6S]-5-МТГФ и запивали таблетку 200 мл воды. Затем кровь повторно брали на анализ в течение 8 ч после приема таблетки (через 30, 60, 90, 120, 180, 240, 360 и 480 мин).
В группе лиц с генотипом ТТ средняя AUC и Cmax для общей концентрации фолатов в крови оказались статистически достоверно выше (в два раза) после приема [6S]-5-МТГФ по сравнению с фолиевой кислотой (p<0,0001). Среднее tmax было статистически достоверно меньше для [6S]-5-МТГФ по сравнению с фолиевой кислотой.
Аналогичная картина наблюдалась и у испытуемых с генотипом СС (табл. 2). Это было справедливо как для средней AUC и Cmax (p<0,005), так и tmax (p<0,05).
Статистически достоверные различия по фармакокинетике между генотипами ТТ и СС были выявлены только для tmax на фоне применения фолиевой кислоты (среднее tmax оказалось выше в группе ТТ по сравнению с группой СС).
Результаты исследования показали, что вне зависимости от генотипа [6S]-5-МТГФ в однократной дозировке обладает большей биодоступностью, чем фолиевая кислота в такой же дозировке. Об этом можно судить по соотношениям значений AUC (для ТТ 200,95% при 95% ДИ 169,61-232,3%; для СС 159,2% при 95 ДИ 126,54-191,87%) (таблица).
Полученные в ходе настоящего исследования данные свидетельствуют о том, что при назначении на непродолжительный срок в физиологической дозировке [6S]-5-МТГФ в большей степени, чем фолиевая кислота, способствует повышению уровня фолатов в плазме крови, причем вне зависимости от генотипа мутации 677C/Т гена МТГФР. Поскольку о наличии у [6S]-5-МТГФ серьезных побочных эффектов ничего неизвестно, препараты на основе этой природной биологически активной формы фолатов могут выступать в качестве более эффективной альтернативы добавкам с фолиевой кислотой.Монокомпоненты или витаминно-минеральные комплексы?
Фолиевая кислота не является эндогенным фолатом и в дозах, превышающих рекомендованные нормы, приводит к развитию функционального дефицита фолатов. После перорального приема фолиевой кислоты происходит ее абсорбция в тонком кишечнике и в течение 2-3 часов уровни фолиевой кислоты достигают максимума в плазме крови. С током крови привнесенная фолиевая кислота поступает практически во все органы и ткани и взаимодействует с фолат-транспортерами (или так называемыми фолат-рецепторами) - белками, связанными с полисахаридами мембраны и переносящими фолаты внутрь клетки. Фолат-транспортеры имеют более высокое сродство к экзогенной фолиевой кислоте, чем к основным формам фолатов крови (тетрагидрофолатам). Следовательно, избыток экзогенной фолиевой кислоты (т.е. синтетической) в плазме крови ингибирует транспорт эндогенных фолатов, более востребованных для нужд организма. В результате на фоне избыточного приема фолиевой кислоты возникает функциональный недостаток эндогенных фолатов, которые не могут реализовать свои эффекты, так как метаболические маршруты оккупированы избытком введенной в составе препаратов фолиевой кислоты [24].
Метафолин в дозе 200 мкг входит в состав витаминно- минерального комплекса Фемибион I Наталкер, который помимо этого компонента содержит витамины С, РР, Е, В1, В2,В5, В6, В12, важная метаболическая функция которых во время беременности безусловно доказана.
Витамин B12 является кофактором фермента гомоцистеинметилтрансферазы, участвующей в превращении гомоцистеина в метионин. С метаболизмом фолиевой кислоты и цианокоболамина в период беременности очень тесно связан метаболизм пантотеновой кислоты и аскорбиновой кислоты. Тиамин - один из наиболее важных витаминов в энергетическом обмене беременной. В результате дефицита витамина В1 у беременной нарушается углеводный и другие виды обмена, следствием чего является избыточное накопление в организме альфа-кетокислот и пентозосахаров; развивается отрицательный азотистый баланс; с мочой в повышенных количествах начинают выделяться аминокислоты и креатинин. Так же в этом случае возможно повышение уровня кетокислот, сдвиг кислотно-щелочного равновесия, снижение синтеза белков. Токоферол участвует в процессах тканевого дыхания и метаболизме белков, жиров и углеводов; выступает как антиоксидант. Токоферолы так же оказывают влияние на функцию половых и других эндокринных желез, защищая их гормоны от чрезмерного окисления. Это способствует нормальному течению беременности [25].
Профессор Э.И. Цейтель, научный директор Фонда общественного контроля наследственных заболеваний, проводил сравнение эффективности поливитаминных комплексов, содержащих фолиевую кислоту, и монотерапии фолиевой кислотой. Риск дефектов нервной трубки снизился на 92% при приеме поливитаминов и лишь на 32% - при приеме монопрепаратов фолиевой кислоты. Установлено снижение распространенности пороков развития сердечно-сосудистой системы как после использования поливитаминов, так и после использования высоких доз фолиевой кислоты, однако профилактическая эффективность поливитаминов была выше. Снижение распространенности пороков развития мочевыводящих путей, врожденного пилоростеноза и пороков развития конечностей было отмечено только после использования поливитаминов как в исследованиях Э.И. Цейтеля, так и в других обсервационных исследованиях [24].Заключение
С учетом высокого показателя распространенности генетических полиморфизмов МТГФР среди населения, и проблем, связанных с пониженной активностью фермента метилтетрагидрофолатредуктазы, с целью профилактики и лечения различных патологических состояний, связанных с дефицитом фолатов во время беременности, целесообразно применять витаминно-минеральные комплексы, содержащие метафолин - активную форму фолатов с высокой биодоступностью.Мой опыт по снижению гомоцистеина с помощью метафолина/метилфолата я уже описывала ранее в посте Как я снижала гомоцистеин, результат 5,9
Еще по теме: "Роль фолатов в предупреждении осложнений беременности при MTHFR"
MTHFR и дефекты метилированияЛитература
1. Группа по исследованию витаминов при Медицинском исследовательском совете. Предотвращение дефектов нервных трубок: результаты исследования Медицинского исследовательского совета. Lancet. 1991; 338: 131-7.
2. Буши К.Дж., Берсфорд С.А., Омен Г.С., Мотульский А.Г. Количественная оценка содержания гомоцистеина в плазме как фактора риска возникновения сосудистых заболеваний: возможные преимущества повышенного потребления фолиевой кислоты. JAMA. 1995; 274: 1049-57.
3. Food and Nutrition Board, Institute of Medicine. Folate. In: Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, DC: National Academy Press. 1998; 196-305.
4. Voutilainen S., Rissanen T.H., Virtanen J., Lakka T.A. Salonen J.T.; Kuopio Ischemic Heart Disease Risk Factor Study. Low dietary folate intake is as excess incidence of acute coronary events: The Kuopio Ischemic Heart Disease Risk Factor Study. Circulation. 2001; 103 (22): 2674-2680.
5. Shane B. Folic acid, vitamin Bl2, and vitamin B6. In: Stipanuk M, ed. Biochemical and Physiological aspects of Human Nutrition. Philadelphia,PA6: WB Saunders Co.; 2000; 483-518.
6. Malinow M.R., Bostom A.G., Krauss R.M. Homocysteine, diet, and cardiovascular diseases: a healthcare professionals from the Nutrition Commitee, American Heart Associate.Circulation. 1999; 99 (1): 178-182.
7. Giovannucci E., Rimm E.B., Ascherio A., Stampfer M.J., Colditz G.A., Willett W.C. Alcohol, low-methionine-low-folate diets, and risk of colon cancer in men. J Natl Cancer Inst. 1995; 87 (4): 265-273.
8. Громова О.А., Торшин И.Ю. Наталбен - Супра витаминно-минеральный комплекс для беременных и кормящих, обогащенный омега-3 ПНЖК. Методическое пособие для врачей.
9. Weir D.G., Molloy A.M. Microvascular disease and dementia in the elderly: are they related to hyperhomocysteinemia? Am J Clin Nutr. 2000; 71 (4): 859-860.
10. Ebly E.M., Schaefer J.P., Campbell N.R., Hogan D.B. Folate status, vascular disease and cognition in elderly Canadians. Age Ageing. 1998; 27 (4): 485-491.
11. Shane B. Folic acid, vitamin B-l2, and vitamin B-6. In: Stipanuk M, ed. Biochemical and Physiological Aspects of Human Nutrition. Philadelphia, PA: W.B. Saunders Co.; 2000; 483-518.
12. Morris M.C., Evans D.A., Schneider J.A., Tangney C.C., Bienias J.L., Aggarwal N.T. Dietary folate and vitamins B-12 and B-6 not associated with incident Alzheimer's disease. J Alzheimers Dis. 2006; 9 (4): 435-443.
13. Wang H.X., Wahlin A., Basun H., Fastbom J., Winblad B., Fratiglioni L. Vitamin B(12) and folate in relation to the development of Alzheimer's disease. Neurology. 2001; 56 (9): 1188-1194.
14. Галина Т.В., Симоновская Х.Ю. Метафолин в составе КОК - инвестиция в репродуктивное благополучие. Мировые новости: современная контрацепция как новые возможности предгравидарной подготовки / Под ред. В.Е.Радзинского. М.: Редакция журнала StatusPraesens. 2013; 24.
15. McNulty H., Cuskelly G.J., Ward M. Response of red blood cell folate to intervention: implications for folate recommendations for the prevention of neuronal tube defects. Am J Clin Nutr. 2000; 71: 5 Suppl: 1308S-1311S.
16. Shane B. Folic acid, vitamin B-l2, and vitamin B-6. In: Stipanuk M, ed. Biochemical and Physiological Aspects of Human Nutrition. Philadelphia, PA: WB Saunders Co.; 2000; 483-518.
17. Centers for Disease Control and Prevention. Spina bifida and anencephaly before and after folic acid mandate-United States, 1995-1996 and 1999- 2000. MMWR Morb Mortal Wkly Rep. 2004; 53 (17): 362-365.
18. McNulty H., Cuskelly G.J., Ward M. Response of red blood cell folate to intervention: implications for folate recommendations for the prevention of neuronal tube defects. Am J Clin Nutr. 2000; 71: 5 Suppl: 1308S-1311S.
19. Centers for Disease Control and Prevention. Spina bifida and anencephaly before and after folic acid mandate-United States, 1995-1996 and 1999-2000. MMWR Morb Mortal Wkly Rep. 2004; 53 (17): 362-365.
20. Дополнительный прием фолиевой кислоты и беременность: профилактика дефектов нервной трубки и не только / Д.А.Гринберг, С.Дж.Белл, Й.Гуан, Й.Йу.
21. Gerhard G.T., Duell P.B. Homocysteine and atherosclerosis. Curr Opin Lipidol. 1999; 10 (5): 417-428.
22. Третьяк Е.Б. Реферат по материалам статьи R. Prinz-Langenohl, S. Br?mswig, O. Tobolski, et al. "[6S]-5-methyltetrahydrofolate increases plasma folate more effectively than folic acid in women with the homozygous or wild-type 677C,T polymorphism of methylenetetrahydrofolate reductase" British Journal of Pharmacology. 2009; 158: 2014-2021.
23. Мальцева Л.И., Павлова Т.В. Анализ ассоциации полиморфизма генов сосудистой системы, эндотелиальной дисфункции и системы свертывания крови с развитием гестоза у первородящих женщин. Практическая медицина. 2011 сентябрь; 4 (52).
24. Громова О.А. XIII Всероссийский научный форум "Мать и дитя". Сателлитный симпозиум компании "Д-р Редди'с Лабораторис Лтд.". Фолаты: мифы и реальность. Избыточные дозы фолиевой кислоты. Чего больше - вреда или пользы? Гинекология. 2012; 5.
25. Ших Е.В., Ильенко Л.И. Клинико-фармакологические аспекты применения витаминно-минеральных комплексов у женщин в период беременности. М: Медпрактика-М.: 2007; 80.
www.babyblog.ru
Жизнь человека и его здоровье | Фолиевая кислота и витамин В9 в чем разница?
Для вас это странный вопрос, правда? Ведь мы все знаем, что витамин В 9 называют фолиевой кислотой. Но теперь ученые установили, что есть четкие различия между ними.И нам надо знать об этих различиях, потому что они имеют не совсем одинаковые эффекты на здоровье.
В этой статье будет объяснено различие между фолиевой кислотой и витамином В 9.
Это не первая статья на блоге, которая раскрывает правду о витаминах.
Первой была «Правда о витамине Е или как нас обманывают»
Что такое витамин В 9
Витамин В9 является важным питательным веществом, и натуральной фолиевой кислотой.
Фолиевая кислота (натуральный витамин В9) выполняет много разных функций в организме.
Например, он играет ключевую роль в росте клеток и формировании ДНК.
Низкие концентрации витамина В 9 связаны с повышенным риском для здоровья.
К ним относятся:
1) Повышенный уровень гомоцистеина в крови, который связан с высоким риском сердечно- сосудистых заболеваний и инсульта.
Об этом можно прочитать в статье «Гомоцистеин – фактор риска сердечно – сосудистых заболеваний»
2) Врожденные дефекты.
Всем известно, что низкие уровни этой кислоты у беременных женщин были связаны с врожденными аномалиями.
3) Риск появления рака.
Низкие уровни этой кислоты также связаны с увеличением вероятности появления рака.
По этим причинам прием фолиевой кислоты является распространенным явлением.
Обогащение пищи этим веществом являются обязательным в некоторых странах.
Но проблема в том, что пищевые добавки и обогащенные продукты содержат синтетическую форму этой кислоты, а не ту, которая является составной частью витамина В 9.
Название этой кислоты происходит от латинского слова «лепестка», что означает лист.
На самом деле, листовые овощи являются одними из лучших диетических источников фолата.
Натуральная фолиевая кислота (витамин В 9, фолаты) – это общее название для группы родственных соединений с аналогичными питательными свойствами, то есть это не одно вещество.
Активная форма витамина В 9 фолиевой кислоты известна как levomefolic кислоты или 5- метилтетрагидрофолата (5-МТГФ).
В пищеварительной системе, большинство пищевых фолатов преобразуются в 5-МТГФ перед поступлением в кровоток.
Что такое фолиевая кислота?
Фолиевая кислота является синтетической формой витамина В9, также известной как pteroylmonoglutamic кислоты.
Она используется в пищевых добавках и добавляется к переработанным продуктам питания, таких как мука и зерновые завтраки.
На протяжении многих лет считалось, что эта фолиевая кислота поглощается в желудочно-кишечном тракте лучше, чем фолаты (витамин В9).
В отличие от большинства фолатов, синтетическая фолиевая кислота не преобразуется в активную форму витамина В9, 5 –МТГФ, в пищеварительной системе.
Вместо этого она должна быть преобразована в печени или в других тканях.
Этот процесс идет в организме, но медленно и неэффективно.
После принятия синтетической фолиевой кислоты организму требуется время, чтобы организм преобразовал это вещество в 5-МТГФ.
Даже небольшие дозы (200-400 мкг в день) не могут быть полностью преобразованы до приема следующей дозы.
Эта проблема становится еще хуже, когда человек принимает добавки синтетической фолиевой кислоты и ест продукты, содержащие эту кислоту.
В результате не преобразованная фолиевая кислота обнаруживается в кровотоке людей, даже в состоянии голодания.
Это является причиной для беспокойства, так как высокие уровни не преобразованной фолиевой кислоты связаны с несколькими проблемами со здоровьем.
Правда, в одном исследовании было показано, что прием фолиевой кислоты вместе с другими витаминами, в частности с витамином В6, делает более эффективным преобразование синтетической фолиевой кислоты в ее активную форму.
Чем вредно накопление не метаболизированной фолиевой кислоты в организме?
Некоторые исследования показывают, что хронически повышенный уровень не преобразованной фолиевой кислоты может иметь неблагоприятные последствия для здоровья.
К ним относятся:
1.Повышенный риск рака.
Высокие уровни не преобразованной фолиевой кислоты были связаны с повышенным риском рака.
Они также могут ускорить рост предраковых поражений.
2. Маскируют недостаточность витамина В 12.
Среди пожилых людей, высокий уровень фолиевой кислоты помогает скрыть недостаток витамина B12.
Не ликвидированный недостаток витамина В12 может увеличить риск развития деменции и ухудшают функции нервов. Вам может быть полезна статья «Дефицит витамина В12»
Хотя высокое потребление фолиевой кислоты является проблемой, последствия для здоровья неясны и необходимы дальнейшие исследования.
В каких продуктах содержится витамин В9
Лучше всего получать витамин B9 из цельных продуктов.
К продуктам, содержащим фолаты, относятся:
1) спаржа,
2) авокадо,
3) брюссельская капуста,
4) зелень, такие как шпинат и салат.
Тем не менее, для некоторых людей – таких как беременные женщины – добавки могут быть простым способом, чтобы убедиться, что они получают достаточно витамина В9.
В этих случаях лучше выбрать добавки, которые не содержат фолиевую кислоту.
Некоторые добавки содержат 5-метилтетрагидрофолата (5-МТГФ), который считается более здоровой альтернативой фолиевой кислоты.
Исследования показали, что 5-МТГФ равна или даже лучше, чем фолиевой кислоты.
Фолиевая кислота в виде 5-метилтетрагидрофолата (5-МТГФ) может быть связана с кальцием и известна под именем метил фолиевой кислоты или levomefolate кальция. Он также продается под марками Metafolin и Deplin.
Самые здоровые пищевые источники витамина В9 это продукты, такие как зеленые листовые овощи.
Если вам нужно принимать добавки, метил фолиевой кислоты является здоровой альтернативой фолиевой кислоты.
Выводы.
1. Настоящий Витамин В9 – это не фолиевая кислота. Есть несколько различий между витамином В9 и фолиевой кислотой.
2. Витамин В9 называют фолиевой кислотой, но витамин В9 – это комплекс нескольких природных фолиевых кислот.
Из них только одна в виде 5—метилтетрагидрофолата (5-МТГФ) является активной формой, которая и попадает в кровоток.
Все остальные природные формы фолиевой кислоты в желудочно-кишечном тракте превращаются в активную форму 5-МТГФ.
3. Фолиевая кислота является синтетической формой.
Она имеет следующие особенности:
1) Она очень медленно преобразуется в активную форму фолиевой кислоты.
2) Из-за этого она проникает в кровоток в виде не преобразованном в активную форму.
3) Не преобразованная синтетическая форма фолиевой кислоты может накапливаться в организме и приводить к негативным последствиям для здоровья.
4) К счастью, есть много альтернатив фолиевой кислоте. Они включают в себя метильные фолаты и огромное разнообразие цельных продуктов.
Делайте правильный выбор.
Больше и ежедневно употребляйте зеленые листовые овощи.
А если необходимо, то правильные добавки (метильные фолаты).
И будьте здоровы!
Но это еще не вся информация о витамине В9. Будет продолжение. Если не хотите пропустить, то подписывайтесь на рассылку.
40 голосов
Средняя оценка: 4.9 из 5
pishhaizdorove.com
Разница между L-Метилфолатом и Фолиевой кислотой
Ключевое различие между L-Метилфолатом и Фолиевой кислотой заключается в том, что L-Метилфолат является активной формой фолата в организме, тогда как Фолиевая кислота является синтетической формой фолата.
Фолат — это витамин, его называют витамином В9. Это один из 13 известных витаминов. Витамины, чтобы они имели пользу, как правило, должны быть активированы внутри организма. Активная форма фолата в организме — L-Метилфолат, а также, фолат встречается в натуральной пище. Тогда как, Фолиевая кислота является синтетической формой этого витамина.
- Содержание
- Обзор и основные отличия
- Что такое L-Метилфолат
- Что такое Фолиевая кислота
- В чем разница между L-Метилфолатом и Фолиевой кислотой
- Резюме
Что такое L-Метилфолат?
L-Метилфолат является активной формой фолата в организме человечека. Синонимом этого витамина является Левомефолиевая кислота. Он, также, может пересекать клеточные мембраны и гематоэнцефалический барьер. Основная роль этого соединения заключается в регуляции моноаминов, набора нейротрансмиттеров, таких как серотонин, дофамин и норадреналин.
 Химическая структура L-Метилфолата
Химическая структура L-МетилфолатаКроме того, L-Метилфолат используется в качестве пищевой добавки и как соединение, обладающее потенциальной противоопухолевой активностью.
 Метафолин (L-Метилфолат) в таблетках
Метафолин (L-Метилфолат) в таблеткахПри использовании этот комплекс может обеспечить метильные группы, необходимые для метилирования ДНК в вызывающих опухоль определенных генах.
Что такое Фолиевая кислота?
Фолиевая кислота является синтетической формой витамина, фолата. Она растворима в воде. Производители добавляют фолиевую кислоту в хлопья, муку, хлеб, макаронные изделия, хлебобулочные изделия, печенье, крекеры и т.д.
 Фолиевая кислота
Фолиевая кислотаЭто соединение принимают во время беременности, рекомендуемый уровень фолиевой кислоты составляет 400 микрограммов в день. Этот витамин помогает избежать врожденных дефектов головного и спинного мозга ребенка.
 Химическая структура фолиевой кислоты
Химическая структура фолиевой кислотыКроме того, он выступает в качестве основного агента для производства красных кровяных клеток. Кроме того, это соединение используют для предотвращения низкого уровня фолата в крови. Иногда люди используют этот витамин для лечения рака толстой кишки и сердечных заболеваний.
В чем разница между L-Метилфолатом и Фолиевой кислотой?
L-Метилфолат является активной формой фолата в организме человека. L-Метилфолат используется для регуляции ряда нейротрансмиттеров, называемых моноаминами, в качестве пищевой добавки, в качестве соединения, обладающего потенциальной противоопухолевой активностью, и для метилирования ДНК в некоторых генах, способствующих опухолям. Фолиевая кислота является синтетической формой витамина, фолата. Приём этого соединения помогает избежать врожденных дефектов головного и спинного мозга ребенка, вырабатывать эритроциты, предотвращать низкий уровень фолата в крови и т.д.
Заключение — L Метилфолат против Фолиевой кислоты
L-Метилфолат и Фолиевая кислота являются двумя различными формами фолата. Разница между L-Метилфолатом и Фолиевой кислотой заключается в том, что L-Метилфолат является активной формой фолата в организме, тогда как Фолиевая кислота является синтетической формой фолата.
raznisa.ru
Фолиевая кислота
Фолиевая кислота плохо растворима в воде и органических растворителях, но хорошо в щелочных растворах. Разрушается под действием света, при обработке и консервировании овощей.
Метаболизм. Витамин В9 , всасываясь в тонком кишечнике, восстанавливается в энтероцитах до тетрагидрофолиевой кислоты (ТГФК) и N5-метил-ТГФК. В крови основное количество витамина входит в состав эритроцитов. Депонируется он в печени, почках и слизистой оболочке кишечника.
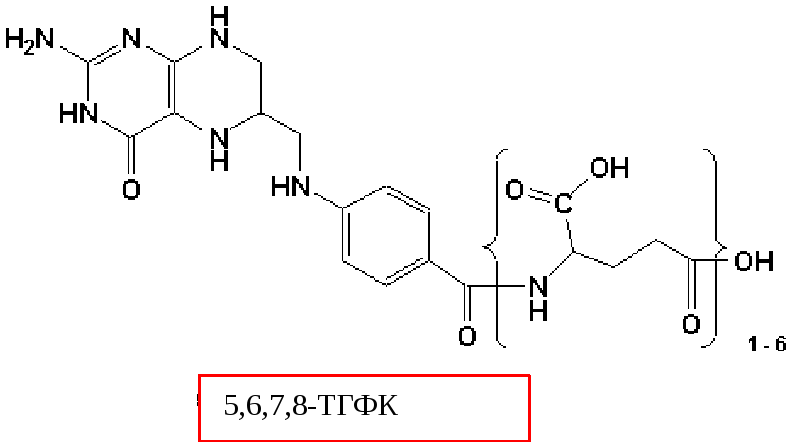
В клетках организма фолиевая кислота восстанавливается в активную форму – ТГФК – с помощью NADPH.H+ -зависимых ферментов: фолатредуктазы (1) и дигидрофолатредуктазы (2): 1. ФК + НАДФH.H+ ДГФК + НАДФ+
2. ДГФК+ НАДФH.H+ ТГФК + НАДФ+
Оба фермента нуждаются в антиоксидантной (препятствующей окислительному разрушению) защите. Эту функцию выполняет витамин С. Отсюда становится понятным, почему проявления фолиевой недостаточности могут быть ослаблены назначением аскорбиновой кислоты.
Активность дигидрофолатредуктазы блокируется конкурентными аналогами фолата – аминоптерином и метотрексатом , широко применяющимися в онкологической практике с целью угнетения размножения раковых клеток.
Избыток фолацина выводится с мочой, калом и потом.
Биохимические функции.
Коферментная форма фолиевой кислоты – ТГФК – необходима для мобилизации и использования в реакциях метаболизма одноуглеродных функциональных групп: метильной (- СН3), метиленовой (- СН2 -), метенильной (-СН =), формильной – СНО) и формиминогруппы (СН=NH). Присоединение этих групп к 5-му или 10-му атому азота ТГФК осуществляется ферментативно.
ТГФК может приобрести одноуглеродную единицу из различных источников. Например, 5-формимино-ТГФК может образоваться при распаде гистидина. Однако более типичной является активация одноуглеродных групп из серина (a), который далее трансформируется в митохондриях витамин В6-зависимой системой ферментов (б):
серингидроксиметилтрансфераза
 а)Серин + ТГФК
глицин + 5,10-метилен-ТГФК
а)Серин + ТГФК
глицин + 5,10-метилен-ТГФК
 б)Глицин ТГФК + НАД+ 5,10-метилен-ТГФК
+ СО2+NH3 +НАДН.Н+
б)Глицин ТГФК + НАД+ 5,10-метилен-ТГФК
+ СО2+NH3 +НАДН.Н+
Помимо основного своего значения – образования одноуглеродного метиленового фрагмента, эти две реакции служат как для синтеза глицина (реакция а), так и его распада (реакция б).
Метиленовая группа в составе 5,10-метилен-ТГФК может превращаться в другие одноуглеродные фрагменты:
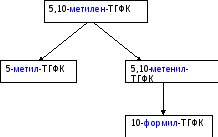
Метилен-тгфк- Метилен-тгфк-
редуктаза дегидрогеназа
метенил-ТГФК-
циклогидролаза
Важнейшими реакциями с участием одноуглеродных фрагментов, связанных с ТГФК, являются:
5,10-метенил-ТГФК и 10-формил ТГФК служат донорами соответствующих одноуглеродных радикалов при синтезе пуриновых нуклеотидов.
5-метил-ТГФК вместе с витамином В12 участвуют в переносе метильной группы в реакциях синтеза дТМФ и метионина
ТГФК вовлекается в метаболизм аминокислот: серина, глицина (см. выше) и метионина
Гиповитаминоз. Поскольку одноуглеродные группы играют исключительно важную роль в биосинтезе нуклеиновых кислот, моно- и динуклеотидов, а также в биосинтезе белков, становятся понятными те глубокие нарушения, которые наблюдаются при фолатном гиповитаминозе.
Основным клиническим проявлением недостатка фолиевой кислоты является заболевание анемией. Анемия называется мегалобластической, макроцитарной. В крови появляются большие незрелые кроветворные клетки — мегалобласты. Снижается количество эритроцитов и гемоглобина в крови, причём эритропения выражена в большей степени, чем снижение уровня гемоглобина (в отличие от железодефицитной анемии). Характерно появление в крови гиперсегментированных многоядерных лейкоцитов с большим числом тяжей между сегментами ядер.
В эритроцитарном, миелоидном и мегакариоцитарном ростках костного мозга отмечаются выраженные мегалобластические изменения. Клетки костного мозга отличаются высокой скоростью деления, поэтому они особо чувствительны к нарушению синтеза нуклеиновых кислот, возникающему при дефиците витамина В9. Схожие симптомы отмечаются и при недостатке витамина В12, так как обмен обоих витаминов взаимосвязан.
При недостаточности фолатов отмечаются слабость, головная боль, обмороки, бледность кожи, красный саднящий язык, диарея. Больные раздражительны, враждебны, у них плохая память, паранойя.
Врождённые нарушения обмена фолиевой кислоты.
Мегалобластическая анемия, сочетающаяся с нарушением психического развития, может обнаруживаться у младенцев вследствие врождённого нарушения всасывания фолатов в тонком кишечнике. Хороший клинический эффект достигается парэнтеральным введением максимальных лечебных доз витамина.
Мегалобластическая анемия вследствие дефекта фолатредуктазы. В такой ситуации нарушается превращение фолиевой кислоты в её коферментную форму – 5-формил-ТГФК. Заболевание прогрессирует медленно, неврологические нарушения обычно отсутствуют, коррегируется повышенными дозами фолиевой кислоты.
Мегалобластическая анемия из-за недостаточности формиминотрансферазы – фермента, необходимого для образования 5-формимино-ТГФК из гистидина. Заболевание обнаруживается в течение первого года жизни ребёнка и характеризуется задержкой умственного и физического развития, аномальными изменениями электроэнцефалографии. Обнаруживается по аномально высокому содержанию фолатов в крови (задержка превращения их в активную фрму) и увеличения выведения метаболитов витамина при нагрузке гистидином.
Другие разновидности анемии затрагивают иные пути метаболизма фолатов, в частности, описана мегалобластическая анемия вследствие дефекта 5,10-метилен-ТГФК-редуктазы (фермент восстанавливает 5,10-метилен-ТГФК в 5-метил-ТГФК), особую роль в заболевании мегалобластической анемией играет недостаточность витамина В12 (см. далее).Гипервитаминоз не описан. Даже при приёме доз, в 20-40 раз превышающих физиологические, токсических эффектов не отмечалось (в клинических испытаниях больные атеросклерозом принимали до 80 мг/сутки витамина В9).
Оценка обеспеченности организма фолацином. Об обеспеченности организма фолиевой кислотой можно судить по содержанию её в крови (лучше – в плазме крови). Содержание фолацина в моче, как правило, не является достоверным критерием обеспеченности организма этим витамином. Быстрое удаление витамина из крови при внутривенном его введении может указывать на недостаточную потребность организма в этом витамине (активный «захват» тканями).
Нередко об обеспеченности организма витамином Вс судят по косвенным показателям: морфологическим изменениям крови и костного мозга, а также по уровню выведения некоторых продуктов обмена витамина с мочой (формиминоглутаминовой или уроканиновой кислот).
Суточная потребность. Пищевые источники. Витамина много в лиственных овощах, например, в шпинате. Он содержится в салате, капусте, томатах, землянике. Богаты им печень и мясо, яичный желток.
При скудном питании рекомендуемая доза составляет 150- 200 мкг фолиевой кислоты ежедневно, лечебная доза – до 2 мг в сутки.
Особое значение приобретает достаточная обеспеченность фолиевой кислотой в ранние сроки беременности: на 2-й неделе (начало развития головного мозга) даже кратковременный дефицит этого витамина может привести к появлению врождённых уродств, нарушению физического и психического развития новорождённого.
Однако дефицит фолата имеет другие недавно изученные биологические последствия, включая ненормально высокий уровень урацила в ДНК. Последнее, как указывалось выше, является следствием лимита биосинтеза тиминовых нуклеотидов. Этот феномен ведёт к хромосомным поломкам, обуславливающим в значительной степени дефект нервной трубки в период эмбриогенеза. Уже не вызывает сомнений, что появление таких врождённых пороков развития, как spina bifida и анэнцефалия, патогенетически связано с дефицитом фолата. Их предупреждение, как показывает мировой опыт, достигается назначением фолиевой кислоты на протяжении всего периода беременности в дозе не менее 400 мкг в сутки, особенно важно это делать в раннем сроке, когда нервная система плода развивается особенно быстро.
Витамин В12 (кобаламин), антианемический витамин
Химическое строение и свойства.Злокачественная анемия (болезнь Аддисон-Бирмера) оставалась смертельным заболеванием до 1926 г., когда впервые для её лечения применили сырую печень. Поиски содержащегося в печени антианемического фактора привели к успеху, и в 1955 г. Дороти Ходжкин расшифровала структуру этого фактора и его пространственную конфигурацию с помощью метода рентгеноструктурного анализа.
Структура витамина В12 отличается от строения всех других витаминов своей сложностью и наличием в его молекуле иона металла – кобальта. Кобальт связан кооординационной связью с 4 атомами азота, входящими в состав порфириноподобной структуры (называемой корриновым ядром), и с атомом азота 5,6-диметилбензимидазола. Кобальтсодержащее ядро молекулы представляет собой плоскостную структуру, с перпендикулярно расположенным к ней нуклеотидом. Последний, помимо 5,6-диметилбензимидазола, содержит рибозу и фосфорную кислоту (циановая группа, связанная с кобальтом, присутствует только в очищенных препаратах витамина, в клетке она замещается водой или гидроксильной группой). Из-за присутствия в молекуле витамина кобальта и амидного азота это соединение получило название «кобаламин».
Метаболизм. Содержащийся в пище витамин В12 в желудочном соке связывается с вырабатываемым обкладочными клетками слизистой желудка белком — гликопротеином, получившим название внутреннего фактора Касла. Одна молекула этого белка избирательно связывает одну молекулу витамина; далее в подвздошной кишке этот комплекс взаимодействует со специфическими рецепторами мембран энтероцитов и всасывается путём эндоцитоза
Затем витамин освобождается в кровь воротной вены. При пероральном назначении высоких доз цианкобаламина он может абсорбироваться в тонком кишечнике путём пассивной диффузии без участия внутреннего фактора, но это медленный процесс. При заболеваниях желудка, сопровождающихся нарушением синтеза внутреннего фактора, всасывания кобаламина не происходит.
Цианкобаламин, используемый в медицинской практике, в энтероцитах превращается в оксикобаламин, являющийся транспортной формой витамина. Транспорт оксикобаламина кровью осуществляется двумя специфическими белками: транскобаламином I (α-глобулин с молекулярной массой ̴120000) и транскобаламином II (β-глобулин с молекулярной массой 35000). Второй из этих белков в транспорте витамина играет главную роль, а транскобаламин I служит своеобразным циркулирующим депо витамина. В печени и почках оксикобаламин превращается в свои коферментные формы: метилкобаламин (метил-В12) и дезоксиаденозинкобаламин (д-аденозин-В12). Коферменты с током крови разносятся по всем тканям организма.
Выводится из организма витамин с мочой.
Биохимические функции. К настоящему времени известно ~ 15 различных В12-регулируемых реакций, но только две из них протекают в клетках млекопитающих: 1/. синтез метионина из гомоцистеина (явно не удовлетворяющий потребностям организма) и 2/. изомеризация D-метилмалонил-КоА в сукцинил-КоА. Рассмотрим эти реакции.
1. В первой реакции участвует метил-В12, являющийся коферментом метионинсинтазы (гомоцистеинметилтрансферазы).. Фермент переносит метильную группу с 5-метил-ТГФК на гомоцистеин с образованием метионина:
ТГФК 5-метил-ТГФК

S
CH3-B12
H S- Ch4| В12 |
CH2 Ch3
| |
|
CH2 Ch3
| |
CH – NH2 CH – Nh3
| |
|
COOH метионинсинтаза COOH
Гомоцистеин Метионин
При уменьшении содержания в диете витамина В12 синтез метионина метионинсинтазой снижается, но поскольку при полноценном питании метионин поступает с пищей, метаболизм белков нарушается не сразу. Вместе с тем, падение активности метиоинсинтазы приводит к накоплению 5-метил-ТГФК (см. схему), который образуется при восстановлении 5,10-метилен-ТГФК, т.е. исчерпывается пул других коферментов ТГФК. Таким образом, даже при условии вполне достаточного общего уровня фолатов создаётся их функциональный дефицит – уменьшается содержание формил- и метилен-производных ТГФК. Как раз эти производные, а точнее приносимые ими одноуглеродные радикалы, необходимы для синтеза предшественников нуклеиновых кислот. Этот феномен получил название «секвестрация» пула ТГФК.
Описанная реакция служит примером тесной взаимосвязи межу двумя витаминами- фолиевой кислотой и кобаламином. Не удивительна поэтому и схожесть симптомов заболевания при дефиците какого-либо из них. При недостаточности витамина В9, а также при снижении активности метионинсинтазы – В12-зависимого фермента, функциональный пул ТГФК может быть легко исчерпан путём «секвестрации», что влечёт за собой избыточное накопление субстрата метионинсинтазной реакции – гомоцистеинаметионин. Таким образом, коферментная функция ТГФК в переносе метильной группы (ключевая реакция) зависит от доступности фолата, т.е. от адекватного его поступления в организм.
Отмечена прямая корреляция между показателями тромбоэмболических осложнений, смертностью от ишемической болезни сердца и уровнем гомоцис-теинемии у этих больных. Увеличенный уровень гомоцистеина в крови постулируется в настоящее время как независимый фактор риска развития ИБС и её тромбоэмболических осложнений. Роль гипергомоцистеинурии как пускового фактора атерогенеза связана с прооксидантным действием гомоцистеина, со способностью этой аминокислоты угнетать рост эндотелиальных клеток, оказывать митогенный эффект на гладкомышечные клетки, стимулировать адсорбцию белков в холестериновой бляшке и интенсифицировать биосинтез коллагена. Принципиально важными являются индуцированное гомоцистеином гиперкоагуляционное состояние, снижение мощности систем антиоксидантной защиты тканей, активация биосинтеза NO-синтазы.
2. Вторая реакция требует участия другой коферментной формы витамина – д-аденозин-В12. Кофермент входит в состав метималонил-КоА-мутазы. Особенностями катализа этого фермента является образование свободнорадикальных промежуточных продуктов реакции и изменение валентности кобальта. Субстратом для его действия является метилмалонил-КоА, образующийся при карбоксилировании пропионил-КоА (реакция рассматривалась в разделе «Биотин»).
О О
║ ║
С~ S KoA С ~S KoA
│ метилмалонил-КоА-мутаза │
C H2 – CH
CH2
H2 – CH
CH2
│ │
COOH CH2
│
COOH
Метилмалонил~ SKoA Сукцинил~ SkoA
Эта реакция является весьма важной в метаболизме пропионовой кислоты (точнее, пропионил~SКoA), которая образуется при окислении жирных кислот с нечётным числом атомов углерода, боковой цепи холестерина, окислительном распаде аминокислот: изолейцина, метионина и серина.
Гиповитаминоз. Недостаточность кобаламинов возникает вследствие низкого содержания их в пище при вегетарианской диете и тем более – при голодании. Но большее значение имеет нарушение всасывания витамина при гастритах с пониженной кислотностью (в случаях нарушения образования внутреннего фактора Касла), оперативном удалении желудка или подвздошной кишки.
Гиповитаминоз проявляется злокачественной мегалобластической анемией, или анемией Аддисон-Бирмера. Болезнь также называется пернициозной анемией. Нарушения кроветворной функции аналогичны наблюдаемой при недостатке фолиевой кислоты. Помимо этого, поражаются задние и боковые столбы спинного мозга вследствие нарушения синтеза миелина; дегенеративные изменения отмечаются также в периферической нервной системе и головном мозге. Неврологическая симптоматика сводится к парастезиям, ощущению онемения кистей и стоп, неустойчивости походки, ослаблению памяти вплоть до спутанности сознания.
Нарушения кроветворения при кобаламиновом гиповитаминозе трудно увязать непосредственно с дефектом коферментных функций витамина В12. Однако если учесть тесное «сотрудничество» этого витамина с фолиевой кислотой, патогенез злокачественной анемии становится более понятным. Как уже указывалось, при недостаточности витамина В12 нарушается использование 5-метил-ТГФК в реакции синтеза метионина, вследствие чего вся фолиевая кислота попадает постепенно в своеобразную ловушку («секвестируется»), создающую функциональный дефицит её коферментных производных. Это объясняет нарушение биосинтеза нуклеиновых кислот и, следовательно, угнетение костно-мозгового кроветворения.
Врождённые нарушения всасывания, транспорта и обмена витамина В12.
Анемия при врождённом дефекте образования внутреннего фактора Касла. При этом нарушается всасывание витамина. В крови его концентрация значительно снижается. Эффективно парентеральное введение препаратов витамина.
Мегалобластическая анемия при нарушении всасывания витамина В12 в кишечнике. Нарушение обусловлено врождённым дефектом механизма высвобождения витамина в кровоток и связывания его с транскортином (транскобал-амином) II. Интересно, что всасывание липидов и углеводов при этом не нарушено. Характерны стойкая протеинурия и увеличение экскреции аминокислот (валина, изолейцина, треонина и метионина).
Анемия, обусловленная врождённым дефектом транскобаламинов. При отсутствии в крови транскобаламина II развивается тяжёлая анемия с первых недель жизни ребёнка. Терапевтический эффект достигается введением мегадоз витамина В12, в 1000 раз превышающих физиологическую. Очевидно, при таких концентрациях кобаламина транспортную функцию берут на себя другие белки.
Врождённые метилмалонатацидемии. При этой патологии отмечается высокий уровень метилмалоновой кислоты в крови и повышенная экскреция её с мочой. Метилмалонатацидемия может вызываться как недостаточным поступлением с пищей витамина В12 , так и врождённым нарушением его метаболизма.
Врождённая метилмалонатацидемия проявляется в первый год жизни ребёнка упорной рвотой, кетоацидозом, нейтропенией и тромбоцитопенией, задержкой психомоторного развития, сниженной сопротивляемостью к инфекционным заболеваниям. Мегалобласты в крови тем не менее обычно не обнаруживаются. Диагноз ставится на основании обнаружения высокой концентрации метилмалоновой кислоты в моче, плазме крови или спинномозговой жидкости; уровень витамина в крови остаётся нормальным, что у
казывает на врождённый дефект его утилизации (но не всасывания). Заболевание носит выраженный семейный характер.
Метаболические нарушения при метилмалонатацидемии могут затрагивать разные аспекты функции кобаламинов, а именно:
может быть нарушено образование коферментной формы витамина – дезоксиаденозин-кобаламина, вследствие чего затрудняется превращение метилмалонил-КоА в сукцинил-КоА и метилмалоновая кислота в избыточном количестве появляется в крови.
Может нарушаться образование апофермента метилмалонил-КоА-мутазы, что также блокирует превращение метилмалонил-КоА в сукцинил-КоА.
Сочетанный дефект может затрагивать обе коферментные формы витамина – метил-В12 и д-аденозин-В12. Это сопровождается дополнительными метаболическими расстройствами, т.е. помимо нарушения обмена метилмалоновой кислоты блокируется также биосинтез метионина из гомоцистеина, следствием чего являются гомоцистинурия и снижение содержания метионина в крови и тканях. В крови обнаруживаются мегалобласты, отмечаются дегеративные изменения в нервной ткани.
Накопление метилмалоновой кислоты и метилмалонил-КоА тормозит синтез присущих клетке жирных кислот. Использование ацилсинтазой метилмалонил-КоА (вместо малонил-КоА) приводит к появлению жирных кислот необычной структуры с разветвлённой цепью; кроме того, накопление в тканях пропионил-КоА (предшественника не используемого метилмалонил-КоА) приводит к увеличению образования жирных кислот с нечётным числом атомов углерода. Всё это нарушает биосинтез сложных липидов в нервной ткани, приводит к её демиэлинизации и развитию соответствующих тяжёлых неврологических синдромов..
Лечение заключается в снижении доли принимаемого с пищей белка (либо диеты с низким содержанием изолейцина, треонина и метионина) и дополнительным назначением гомоцистеина и холина, а также высоких доз кобаламина.
Гипервитаминоз. Введение витамина даже в тысячекратной, по сравнению с физиологической, дозе не оказывало токсического эффекта.
Оценка обеспеченности организма витамином В12. Для этой цели служит определение содержания витамина в сыворотке крови, либо определение суточной экскреции метилмалоновой кислоты, которая возрастает при низкой обеспеченности организма кобаламином в десятки и сотни раз. Иногда применяется также метод нагрузки с помощью парэнтерального введения меченного по кобальту витамина В12.
Суточная потребность. Пищевые источники. Синтез кобаламинов в природе осуществляется исключительно микроорганизмами. Животные и растительные клетки такой способностью не обладают. Основные пищевые источники витамина – печень, мясо (в нём кобаламина 20 раз меньше, чем в печени), морские продукты (крабы, лососевые, сардины), молоко, яйца. У строгих вегетарианцев, исключающих из пищи не только мясные, но и молочные продукты, рано или поздно развивается В12-дефицитная анемия.
Суточная потребность – 3 мкг.
studfile.net
Роль фолатов в развитии осложнений беременности при полиморфизме MTHFR — запись пользователя Kate (id925041) в сообществе ЭКО — мама в категории Библиотека: статьи, полезная информация. Стихи, видео и фильмы про ЭКО…
Статья из журнала "ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Акушерство и гинекология", 2014, анализирует роль фолиевой кислоты при беременности, а также негативные последствия дефицита и переизбытка фолатов в период гестации. Приведены результаты наблюдения за беременными с полиморфизмом гена MTHFR, которые принимали витаминно-минеральный комплекс, содержащий активную форму фолатов - метафолин. Применение комплекса позволило качественно и количественно нормализовать гематологические показатели, а также значительно снизить риск осложнений беременности.роль активированного в процессе всасывания кальцияРоль фолиевой кислоты в организме. Дефицит фолатов и осложнения беременности
Фолаты, содержащиеся в пищевых продуктах, представляют собой химические соединения на основе фолиевой кислоты (витамина В₉). Они участвуют в важнейших обменных процессах в организме. Так, фолаты играют ключевую роль в синтезе нуклеотидов и репликации ДНК, без которых невозможны физиологическое деление и нормальный рост всех клеток. При дефиците фолатов процесс репликации нарушается, что в первую очередь отражается на быстро пролиферирующих клетках, таких как кроветворные и эпителиальные. Повреждение кроветворных клеток приводит к нарушению гемопоэза в костном мозге и формированию мегалобластного типа кроветворения, который обнаруживается фолиеводефицитной мегалобластной анемией. В результате повреждения эпителиальных клеток ухудшается регенерация кожи и слизистых оболочек .
Фолаты также принимают участие в реакциях метилирования белков, гормонов, липидов, нейромедиаторов и других субстратов обмена веществ. Нарушения цикла метилирования проявляются различными невропатиями и болезнью Альцгеймера, что обусловлено повреждением оболочки нервных окончаний и нарушением проводимости по ним нервных импульсов.
Важнейший субстрат для метилирования в организме - ДНК. Метилирование ДНК обеспечивает функционирование клеточного генома, регуляцию онтогенеза и клеточную дифференцировку. Иммунная система через реакции метилирования распознает и подавляет экспрессию чужеродных генов. Результатом дефектов метилирования становятся такие патологические состояния, как рак, атеросклероз, нейродегенеративные, аутоиммунные и аллергические заболевания.
Наряду с кроветворными и эпителиальными клетками к быстро пролифелирующим относятся ткани хориона, которые также высокочувствительны к негативному влиянию дефицита фолатов. Расстройство работы генома эмбриональных клеток во время их деления и дифференцировки приводит к нарушению эмбриогенеза и формированию пороков развития у плода.Один из тяжелейших пороков, связанных с дефицитом фолатов, - незаращение нервной трубки у плода. По данным рандомизированного плацебоконтролируемого исследования, дополнительный прием фолатов снижал частоту развития порока нервной трубки на 72% (1,0% у беременных, принимавших фолаты, и 3,5% у беременных, не принимавших фолаты). Необходимость дополнительного приема фолатов во время беременности для обеспечения нормального развития плода и рождения здорового ребенка подтверждают и другие масштабные исследования.
Существует четкая зависимость частоты порока нервной трубки у плода от уровня фолатов в эритроцитах крови беременной. Минимально достаточная концентрация фолатов для рождения здорового ребенка составляет 906 нмоль/л и встречается в популяции всего в 13% случаев, поэтому программы по дотации фолатов беременным существуют во всем мире.
Дефицит фолатов приводит не только к дефектам нервной трубки у плода, но и к целому спектру различных аномалий мозга, конечностей, ушей, мочевыделительной системы, а также формированию расщелины верхнего неба и омфалоцеле. Чаще всего (примерно у одного из 100 новорожденных) встречаются пороки сердечно-сосудистой системы. В одном из исследований было показано, что дополнительный прием фолиевой кислоты на протяжении четырех недель до зачатия и первых 12 недель беременности снижает риск развития врожденного порока сердца на 26% и дефекта сердечной перегородки - на 40%.
Кроме негативного влияния на эмбриогенез недостаточное потребление фолатов во время беременности нарушает пролиферацию клеток хориона и формирование плаценты. В дальнейшем это приводит к осложненному течению беременности: повышается риск невынашивания, плацентарной недостаточности и задержки роста плода, увеличивается количество случаев преэклампсии. Риск данных осложнений еще более возрастает при обнаружении в крови высокого уровня гомоцистеина, метаболизм которого напрямую связан с метаболизмом фолатов.
Метаболизм фолатов
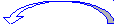
Как известно, фолаты не синтезируются в организме, поэтому их нужно получать либо из продуктов питания, либо посредством дополнительного приема. Большинство пищевых фолатов при поступлении в организм биологически не активны. Всасывается в систему кровообращения и затем потребляется клетками только одна форма фолиевой кислоты - моноглутамат 5-метилтетрагидрофолат (5-МТГФ) (рис. 1)
Рис.1 Метаболизм фолатов в кишечнике.
Остальные формы фолатов представляют собой полиглутаматы, которые в щеточной каемке слизистой кишечника преобразуются в моноглутаматы и при всасывании из кишечника в кровь под воздействием фермента метилентетрагидрофолатредуктазы (МТГФР) тоже превращаются в моноглутамат 5-МТГФ. Последний поступает в клетки организма и участвует в биологических процессах: циклах клеточной репликации и метилирования (рис. 2) .
Рис.2. Метаболизм фолатов в клетке
Цикл метилирования включает трансформацию аминокислоты метионин, поступающей в организм с продуктами животного происхождения (мясом, молоком и яйцами), в S-аденозилметионин и затем гомоцистеин. S-аденозилметионин является донором метила для всех клеточных метилтрансфераз, метилирующих различные субстраты (ДНК, белки, липиды). После потери метильной группы он преобразуется в гомоцистеин, часть которого метаболизируется при участии В₆-зависимого фермента цистатионин-синтазы и выводится почками, а часть повторно метилируется и превращается в метионин, что ведет к возобновлению клеточного цикла метилирования. Повторное метилирование гомоцистеина происходит за счет метильных групп поступившего в клетки моноглутамата 5-МТГФ, которые транспортируются с помощью В₁₂-зависимого фермента метионин-синтазы. Таким образом, фолаты обеспечивают постоянное снабжение метильными группами циклы метилирования. После участия в цикле метилирования 5-МТГФ вновь превращается в полиглутаматы фолиевой кислоты. Полиглутаматы участвуют в другом не менее важном процессе обмена веществ: обеспечивают цикл синтеза ДНК и клеточную репликацию. В результате данных реакций образуются промежуточные формы фолиевой кислоты: полиглутамат, дигидрофолат и 5,10-метилентетрагидрофолат. Дигидрофолаты с помощью фермента дегидрофолатредуктазы обратно превращаются в полиглутаматы тетрагидрофолатов и вновь используются в синтезе предшественников нуклеотидов для образования ДНК и клеточного деления. В свою очередь 5, 10-метилентетрагидрофолаты под воздействием фермента МТГФР повторно превращаются в активный моноглутамат 5-МТГФ, который наряду с поступившим из крови метилфолатом используется для повторного метилирования гомоцистеина в метионин и участия последнего в циклах метилирования.
Уровень гомоцистеина в крови строго контролируется как реметилированием, так и выведением его из организма. Исследования последних лет показывают, что любое увеличение уровня гомоцистеина в крови повышает риск тромбофилических осложнений: инфаркта миокарда, инсульта и венозной тромбоэмболии. Вместе с тем непосредственного участия в деятельности свертывающей системы крови гомоцистеин не принимает, и его эффект осуществляется опосредованно. Гипергомоцистеинемия вызывает повреждение сосудистого эндотелия, в результате чего активируются факторы свертывающей системы крови и повышается риск тромбообразования, в то время как деятельность антисвертывающего звена гемостаза ухудшается. Кроме того, в местах повреждения сосудистой стенки откладываются холестерин и кальций, образуя атеросклеротические бляшки, в результате чего просвет сосудов сужается, нарушается кровообращение и развивается ишемическая болезнь сердца.
В ряде крупномасштабных исследований было показано, что при сывороточной концентрации гомоцистеина выше 10 мкмоль/л значительно увеличивается риск развития ишемической болезни сердца, инсульта, инфаркта, а также злокачественных новообразований. Повышение уровня гомоцистеина крови всего на 5 мкмоль/л увеличивает риск атеросклеротического поражения сосудов на 80%, острого инфаркта и инсульта - на 50%. Наряду с этим значительно растет показатель общей смертности, включающий смертность как от сердечно-сосудистых заболеваний, так и от не связанных с ними причин, в том числе злокачественных новообразований.
В акушерской практике также актуален контроль уровня гомоцистеина в сыворотке крови. При повышенном содержании гомоцистеина усиливается тромбообразование в зоне плацентации, что ведет к развитию отслоек и инфарктов плаценты, нарушению кровообращения в ней с формированием плацентарной недостаточности и осложненному течению беременности. Результаты масштабного исследования, охватившего 5883 женщины и их 14 415 беременностей в период 1967-1996 гг., подтвердили достоверное повышение риска развития преэклампсии, отслойки плаценты, преждевременных родов и рождения детей с низкой массой тела (менее 1500 г) при концентрации гомоцистеина в сыворотке крови более 9 мкмоль/л. Частота осложнений беременности коррелировала со степенью повышения уровня гомоцистеина.В других исследованиях было показано достоверное снижение частоты преждевременных родов и рождения детей с экстремально низкой массой тела при дополнительном приеме фолиевой кислоты, причем с четкой зависимостью от длительности назначения фолиевой кислоты до наступления беременности.
Гипергомоцистеинемия может быть приобретенной и наследственной. Приобретенная гипергомоцистеинемия возникает при недостаточном поступлении фолатов с пищей, нарушении их всасывания в кровь на фоне заболеваний кишечника, дефиците витамина В₁₂. Алкоголизм, курение, некоторые лекарственные средства (противосудорожные, противоопухолевые, гормональные контрацептивы), гипотиреоз, сахарный диабет могут также приводить к дефициту фолатов и развитию гипергомоцистеинемии. Накопление сывороточного гомоцистеина может быть следствием нарушения его выведения, например, при заболеваниях почек и недостатке витамина В₆.
Причиной наследственной гипергомоцистеинемии является полиморфизм гена фермента МТГФР (MTHFR) - основного фермента метаболизма фолатов в организме. Он преобразует все неактивные формы фолиевой кислоты, поступившие в организм (рис. 1), а также полиглутаматы, находящиеся в клетках, в биологически активный 5-МТГФ (рис. 2). В результате генетического полиморфизма функция данного фермента снижается (при гомозиготной форме - на 75% от исходной, при гетерозиготной - на 30%), что ведет к резкому снижению поступления в кровь активных фолатов и образования их в клетках, а также развитию дефицита фолатов. Женщины с полиморфизмом гена МТГФР относятся к группе высокого риска по развитию сердечно-сосудистых заболеваний. Кроме того, у них значительно чаще регистрируются пороки развития плода и осложненное течение беременности.
Применение фолиевой кислоты во время беременности
Как показали последние исследования, традиционное назначение препаратов фолиевой кислоты при нарушении функции ферментов фолатного цикла оказалось малоэффективным. Синтетическая фолиевая кислота так же, как и большинство пищевых фолатов, биологически не активна и только с помощью фермента МТГФР преобразуется в активный моноглутамат 5-МТГФ. Следует отметить: в отличие от пищевых фолатов синтетическая фолиевая кислота даже в неметаболизированном виде может поступать в системный кровоток и захватываться клетками. Появление неметаболизированной формы в крови происходит уже при суточном потреблении фолиевой кислоты более 200 мкг, что обусловлено ограниченными возможностями ферментативной системы слизистой оболочки кишечника. Поступая в клетки, она блокирует рецепторы и ферменты, с которыми взаимодействуют эндогенные активные фолаты, и, несмотря на достаточный и даже избыточный прием фолиевой кислоты, возникает или еще больше усугубляется функциональный дефицит фолатов. Активные эндогенные фолаты не могут реализовать свои эффекты из-за избытка введенной синтетической фолиевой кислоты.
Таким образом, для организма опасен не только недостаток фолатов, но и избыток синтетической фолиевой кислоты. Эпидемиологические и клинические исследования позволили установить двунаправленную связь между приемом фолиевой кислоты, уровнем фолатов в крови и онкологическими заболеваниями. Онкологический риск повышается как при дефиците фолатов, так и при передозировке синтетической фолиевой кислоты .
Избыток синтетических фолатов при беременности также ассоциирован с неблагоприятными последствиями для плода. С ним связывают нарушение когнитивных способностей и зрения у новорожденного, ожирение в старшем возрасте. Избыток витаминов группы В, к которым относится фолиевая кислота, может вызывать тяжелые аллергические реакции в организме беременной вплоть до генерализованной токсикодермии. Нами был описан случай, когда беременная принимала по четыре таблетки, содержащие 1 мг фолиевой кислоты, в сутки в сочетании с поливитаминами (я лично видела двух врачей- одного репродуктолога и одного гематолога, которые уверенны, что 400мкг= 4 таблетки по 1 мг.). Есть данные о повышении впоследствии риска развития рака молочной железы при применении высоких доз (5 мг) фолиевой кислоты во время беременности.В этой связи отношение к фолиевой кислоте по принципу «много не бывает» в настоящее время признано ошибочным. Суточная потребность в фолатах составляет всего 400 мкг или 0,4 мг. Для беременных эта доза может быть несколько увеличена, но не должна превышать 1 мг в сутки - так называемый физиологический предел. В приказе Министерства здравоохранения РФ от 12 ноября 2012 г. № 572н «Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)"» также рекомендован ежедневный прием 400 мкг фолиевой кислоты на протяжении первого триместра беременности.
Метафолин - биологически активная форма фолатов
В последние годы исследования по профилактике осложнений, связанных с дефицитом фолатов, сфокусированы на дополнительном приеме другой формы фолиевой кислоты - 5-МТГФ, или метафолина. Это обусловлено высокой распространенностью генетического полиморфизма МТГФР среди населения, с чем связана пониженная активность основного фермента фолатного цикла. Так, гомозиготный полиморфизм встречается в 15-20% случаев, гетерозиготный - в 40-60%. В отличие от синтетической фолиевой кислоты метафолин является биологически активной формой фолатов и всасывается в кровь без участия ферментативных систем кишечника, в том числе фермента МТГФР. Он непосредственно захватывается клетками и используется в обменных процессах - репликации ДНК и циклах метилирования (рис. 1, 2). При исследовании уровня фолатов в эритроцитах крови у женщин с полиморфизмом гена МТГФР с различным типом наследования R. Prinz-Langenohl и соавт. показали, что метафолин значительно в большей степени повышает их содержание, чем фолиевая кислота. Кроме того, метафолин в большей степени, чем фолиевая кислота, влияет на сывороточный уровень гомоцистеина.
Биологически активная форма фолиевой кислоты - метафолин содержится в препарате Фемибион. В состав препарата входит 400 мкг фолатов, половина из которых представлена фолиевой кислотой и половина - метафолином. Фемибион включает другие витамины группы В (В₁, В₂, В₅, В₆ и В₁₂), а также витамины С, Е, РР и йод.
Назначать препараты, содержащие фолиевую кислоту, необходимо не менее чем за восемь недель до планируемой беременности. Именно такой срок необходим для накопления клетками минимально достаточного количества фолатов, обеспечивающего профилактику осложнений беременности и пороков развития у плода. При наступлении беременности прием фолатов необходимо продолжить до 12 недель, то есть на весь период закладки органов и систем плода и формирования плаценты.При наличии генетического полиморфизма фермента МТГФР дополнительный прием фолатов проводится не только на прегравидарном этапе и во время первого триместра беременности, но и на протяжении всей беременности, а также трех - шести месяцев послеродового периода, когда риск тромбофилических осложнений особенно высок.
Дефицит фолатов у женщин с полиморфизмом гена МТГФР связан не только с тромбофилическими и онкологическими рисками. Наши исследования показали, что при этом значительно повышается риск геморрагических осложнений, в частности аномальных маточных кровотечений.
Клиническое наблюдение женщин с полиморфизмом гена МТГФР
В период 2012-2014 гг. под нашим наблюдением находилась 51 женщина в возрасте 18-45 лет с генетическим полиморфизмом фермента МТГФР (рис. 3).
У 57% из них была выявлена гомозиготная форма полиморфизма, у 43% - гетерозиготная. Обследование проводилось в многопрофильном медицинском центре «КМ-Клиник» г. Москвы.У 54% женщин определялась тромбоцитопения - снижение количества тромбоцитов в сыворотке крови. При этом наследственные и аутоиммунные причины тромбоцитопении (идиопатическая тромбоцитопеническая пурпура, болезнь Виллебранда и др.) были исключены. Тромбоцитопения во всех случаях была умеренной - от 105-180×10⁹/л.
Следует отметить: тромбоцитопения часто сочетается с другими признаками функциональной недостаточности тромбоцитарного звена гемопоэза (нарушением агрегации тромбоцитов, удлинением активированного частичного тромбинового времени, снижением адгезивности тромбоцитов, удлинением времени кровотечения). Данные изменения наряду с большим размером и объемом клеток тромбоцитарного ростка, как правило, характеризуют мегалобластный тип кроветворения и свидетельствуют о нарушениях гемопоэза в костном мозге . Одной из причин замены нормобластного типа кроветворения на мегалобластный является недостаток фолатов. С дефицитом фолатов связывают нарушение синтеза ДНК и деления кроветворных клеток, что приводит не только к уменьшению их количества и увеличению объема, но и к функциональной недостаточности (как следствию укорочения периода жизни мегалобластов в циркулирующей крови) и более быстрому разрушению в костном мозге. При повреждении таким образом тромбоцитарного ростка повышается риск развития кровотечений.В нашем исследовании тромбоцитопатия у женщин с генетическим полиморфизмом МТГФР встречалась значительно чаще, чем гипергомоцистеинемия (высокий уровень гомоцистеина в крови определялся у 22% (n = 11)). Вместе с тем только у 12% (n = 6) имелось повышенное количество тромбоцитов в крови, которое у половины сочеталось с их функциональной недостаточностью. Данную гипотезу подтверждает высокая частота патологических маточных кровотечений у женщин с полиморфизмом гена МТГФР: почти у половины (49%) имели место аномальные маточные кровотечения преимущественно в виде обильных и/или длительных менструаций и у каждой пятой - кровотечение после родов или аборта, которое в двух случаях привело к гемотрансфузии (табл. 1).

У 37% (n = 19) женщин с полиморфизмом гена МТГФР были выявлены лабораторные признаки анемии. В абсолютном большинстве случаев (n = 16) снижался только уровень гемоглобина (до 90-110 г/л), тогда как количество эритроцитов находилось в пределах нормы. Характерные для мегалобластного пути кроветворения макроцитоз и гиперхромия эритроцитов отмечались только у трех женщин.
Таким образом, при полиморфизме гена МТГФР тромбоцитарный росток гемопоэза в сравнении с эритроцитарным подвержен большему повреждающему влиянию дефицита фолатов, что обусловливает высокую частоту гинекологических и акушерских кровотечений.
С дефицитом фолатов традиционно связывают акушерские осложнения. Так, 39% наших пациенток страдали бесплодием, у 30% была неразвивающаяся беременность, у 10% - преэклампсия в анамнезе. В 6% случаях зафиксированы пороки развития плода: дефект межжелудочковой перегородки, анэнцефалия и множественные пороки развития. Все полученные в данном исследовании показатели значительно превышали данные в общей популяции .В нашем наблюдении 22 женщины с полиморфизмом гена фермента МТГФР были беременными (табл. 2).
При этом у абсолютного большинства из них (86%) отмечалось кровотечение в первом триместре беременности, интенсивность которого варьировала от скудных мажущих кровяных выделений до 300-500 мл в сутки. Следует отметить, что все женщины получали от 0,4 до 5 мг/сут фолатов на протяжении всей беременности и трех месяцев после родов.
Десять из этих женщин с наступлением беременности начали принимать Фемибион (группа 1). Во всех случаях мы отмечали мажущие кровяные выделения из половых путей в первом триместре (использовались одна - три ежедневных прокладок в сутки). Течение беременности нормализовалось в течение пяти - десяти дней после назначения комплексной сохраняющей терапии. В ее состав входили вагинальный микронизированный прогестерон по 400-600 мг/сут до 12 недель (у пяти женщин с отягощенным акушерско-гинекологическим анамнезом вагинальный прогестерон назначался по 200 мг до 36-й недели беременности) и транексамовая кислота по 1,5-3 г/сут внутрь в течение одной-двух недель. Все беременности завершились рождением живых доношенных детей, кровотечений в родах и послеродовом периоде не наблюдалось.
Три женщины начали принимать Фемибион за шесть - восемь недель до наступления беременности (группа 2). У них кровотечений из половых путей и признаков отслойки хориона/плаценты не наблюдалось, беременность протекала без осложнений и закончилась рождением здоровых детей.
На фоне приема фолиевой кислоты у девяти беременных (группа 3), в том числе высоких доз - до 5 мг/сут, несмотря на проведение комплексной терапии микронизированным прогестероном по 400-600 мг/сут вагинально и транексамовой кислотой по 3-4 г/сут внутрь или 1-1,5 г/сут внутривенно, кровотечения в большинстве случаев были более обильными. Так, в трех случаях кровопотеря составила 300-500 мл/сут, в четырех - кровяные выделения были умеренными (до двух - трех прокладок средней впитываемости в сутки) и в двух отмечались мажущие кровяные выделения. Трех беременных с обильными и двух с умеренными кровяными выделениями перевели на прием Фемибиона вместо фолиевой кислоты, что во всех случаях позволило постепенно купировать кровотечение. В дальнейшем у двух из них произошли самопроизвольные выкидыши в 17 и 19 недель. У шести женщин беременность закончилась своевременными родами, осложнений в послеродовом периоде не отмечалось. В одном случае было произведено экстренное родоразрешение путем операции кесарева сечения в связи с развитием преэклампсии.
У абсолютного большинства беременных с полиморфизмом гена МТГФР были нарушены гематологические показатели: у 86,4% (n = 19) была обнаружена тромбоцитопения и у 72,7% (n = 16) - анемия. Снижение показателей во всех случаях было умеренным: уровень гемоглобина крови находился в пределах 88-112 г/л, количество тромбоцитов - в пределах 117-180×10⁹/л. При этом уменьшение количества эритроцитов в сыворотке крови встречалось также редко (n = 3), как и вне беременности. Следует отметить, что в половине случаев беременность наступила на фоне уже сниженных лабораторных показателей, а в половине анемия и тромбоцитопения присоединились достаточно рано - в конце первого или начале второго триместра беременности. Только у трех женщин, начавших принимать Фемибион за шесть - восемь недель до наступления беременности и продолживших его прием до родов, гематологические показатели находились в пределах нормы и сохранялись без изменений на протяжении всего периода гестации.При дотации фолиевой кислоты (группа 3), в том числе в больших дозах - до 5 мг/сут, только у двух беременных наблюдалась стабилизация показателей крови, тогда как у остальных анемия и тромбоцитопения прогрессировали, и к концу беременности уровень гемоглобина и тромбоцитов снизился на 15-30% ниже от исходных показателей.
Назначение Фемибиона на протяжении беременности, наоборот, положительно влияло на гематологический статус (группа 1). Так, у восьми беременных уровень гемоглобина и тромбоцитов достиг нормативных значений (в том числе в случаях обильных кровотечений) и только у двух остался без изменений. Нормализация показателей крови происходила в течение двух - четырех недель после назначения препарата, содержащего активную форму фолиевой кислоты.
У четырех беременных была диагностирована гипергомоцистеинемия (уровень сывороточного гомоцистеина составил 11-14,2 ммоль/л), которую также удалось нормализовать в течение месяца применения Фемибиона.
Выводы
Проведенное исследование подтвердило роль дефицита фолатов в развитии акушерских осложнений: бесплодия, невынашивания беременности, преэклампсии, пороков развития у плода. Была установлена связь нарушений в метаболизме фолатного цикла с высокой частотой аномальных гинекологических и акушерских кровотечений: у каждой второй женщины с полиморфизмом гена МТГФР (MTHFR) имелись обильные и/или длительные менструации, у каждой пятой - кровотечение в родах или после аборта и у 86% - кровотечение во время настоящей беременности. При этом у большинства обследованных женщин были изменены гематологические показатели в виде тромбоцитопении, анемии и/или гипергомоцистеинемии. Наиболее характерными, встречающимися у более половины (54%) женщин с полиморфизмом гена МТГФР и у 86,4% беременных с полиморфизмом МТГФР были повреждения тромбоцитарного звена гемопоэза - тромбоцитопатия, которая обнаруживалась снижением количества и увеличением объема тромбоцитов, а также признаками их функциональной недостаточности. У каждой третьей (37%) женщины с полиморфизмом генов ферментов фолатного цикла и у 73,7% беременных с нарушением метаболизма фолиевой кислоты выявлялась анемия.
Назначение беременным с полиморфизмом гена МТГФР препарата, содержащего активную форму фолатов - метафолин, позволило качественно и количественно нормализовать гематологические показатели, а также значительно снизить риск осложнений беременности.
www.babyblog.ru

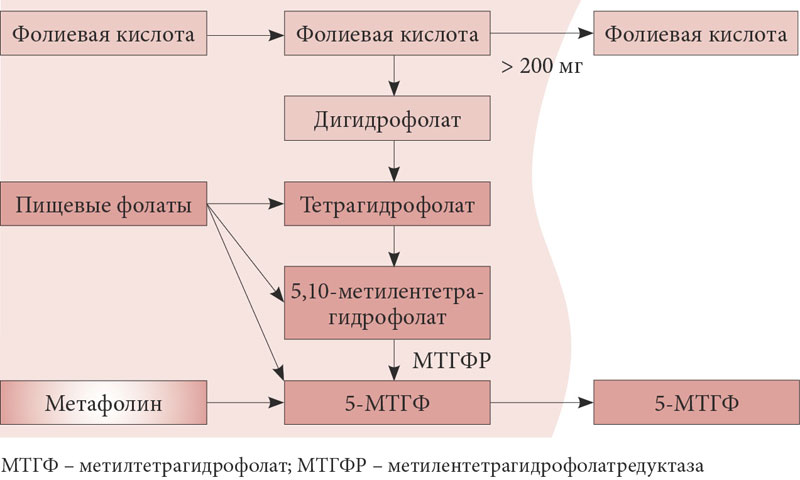
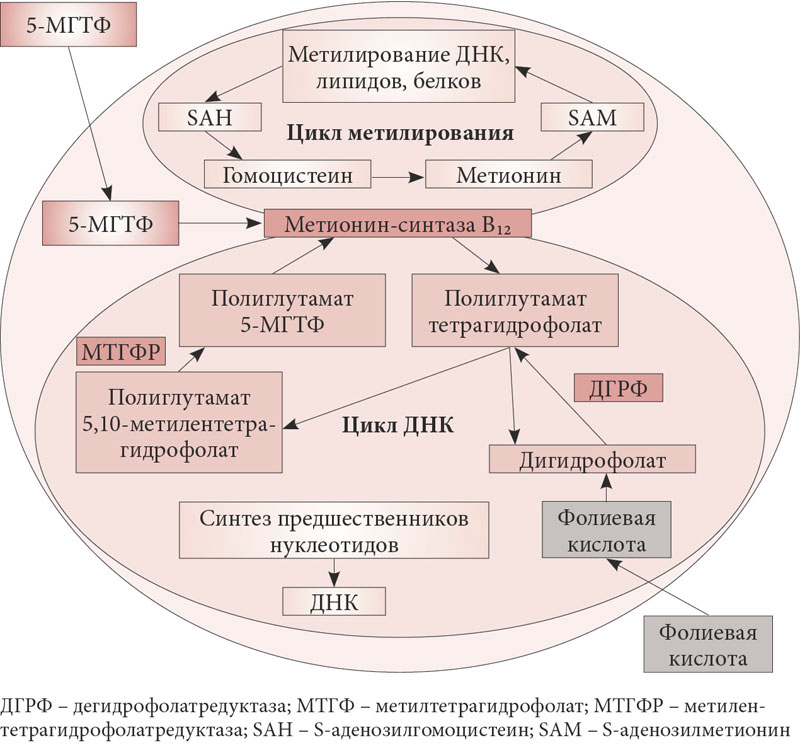 Цикл метилирования включает трансформацию аминокислоты метионин, поступающей в организм с продуктами животного происхождения (мясом, молоком и яйцами), в S-аденозилметионин и затем гомоцистеин. S-аденозилметионин является донором метила для всех клеточных метилтрансфераз, метилирующих различные субстраты (ДНК, белки, липиды). После потери метильной группы он преобразуется в гомоцистеин, часть которого метаболизируется при участии В₆-зависимого фермента цистатионин-синтазы и выводится почками, а часть повторно метилируется и превращается в метионин, что ведет к возобновлению клеточного цикла метилирования.
Повторное метилирование гомоцистеина происходит за счет метильных групп поступившего в клетки моноглутамата 5-МТГФ, которые транспортируются с помощью В₁₂-зависимого фермента метионин-синтазы. Таким образом, фолаты обеспечивают постоянное снабжение метильными группами циклы метилирования. После участия в цикле метилирования 5-МТГФ вновь превращается в полиглутаматы фолиевой кислоты.
Полиглутаматы участвуют в другом не менее важном процессе обмена веществ: обеспечивают цикл синтеза ДНК и клеточную репликацию. В результате данных реакций образуются промежуточные формы фолиевой кислоты: полиглутамат, дигидрофолат и 5,10-метилентетрагидрофолат. Дигидрофолаты с помощью фермента дегидрофолатредуктазы обратно превращаются в полиглутаматы тетрагидрофолатов и вновь используются в синтезе предшественников нуклеотидов для образования ДНК и клеточного деления. В свою очередь 5, 10-метилентетрагидрофолаты под воздействием фермента МТГФР повторно превращаются в активный моноглутамат 5-МТГФ, который наряду с поступившим из крови метилфолатом используется для повторного метилирования гомоцистеина в метионин и участия последнего в циклах метилирования.
Цикл метилирования включает трансформацию аминокислоты метионин, поступающей в организм с продуктами животного происхождения (мясом, молоком и яйцами), в S-аденозилметионин и затем гомоцистеин. S-аденозилметионин является донором метила для всех клеточных метилтрансфераз, метилирующих различные субстраты (ДНК, белки, липиды). После потери метильной группы он преобразуется в гомоцистеин, часть которого метаболизируется при участии В₆-зависимого фермента цистатионин-синтазы и выводится почками, а часть повторно метилируется и превращается в метионин, что ведет к возобновлению клеточного цикла метилирования.
Повторное метилирование гомоцистеина происходит за счет метильных групп поступившего в клетки моноглутамата 5-МТГФ, которые транспортируются с помощью В₁₂-зависимого фермента метионин-синтазы. Таким образом, фолаты обеспечивают постоянное снабжение метильными группами циклы метилирования. После участия в цикле метилирования 5-МТГФ вновь превращается в полиглутаматы фолиевой кислоты.
Полиглутаматы участвуют в другом не менее важном процессе обмена веществ: обеспечивают цикл синтеза ДНК и клеточную репликацию. В результате данных реакций образуются промежуточные формы фолиевой кислоты: полиглутамат, дигидрофолат и 5,10-метилентетрагидрофолат. Дигидрофолаты с помощью фермента дегидрофолатредуктазы обратно превращаются в полиглутаматы тетрагидрофолатов и вновь используются в синтезе предшественников нуклеотидов для образования ДНК и клеточного деления. В свою очередь 5, 10-метилентетрагидрофолаты под воздействием фермента МТГФР повторно превращаются в активный моноглутамат 5-МТГФ, который наряду с поступившим из крови метилфолатом используется для повторного метилирования гомоцистеина в метионин и участия последнего в циклах метилирования.