влияние на человека. Диоксид азота: класс опасности :: SYL.ru
Диоксид азота – один из самых распространенных загрязнителей атмосферы на сегодняшний день, играющий немалую роль в образовании смога и кислотных осадков. Давайте рассмотрим, что представляет собой это вещество и чем оно опасно для человека.
Диоксид азота: формула, характеристики
Двуокись азота – неорганическое соединение состава NO2. Представляет собой газ желто-бурого цвета. В условиях низких температур становится бесцветным. При температуре большей, чем 150°С, происходит диссоциация диоксидана оксид азота и кислород.
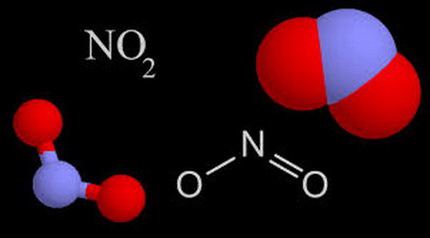
Данное соединение характеризуется специфическим запахом, который в значительных концентрациях становится удушливым. Имеет высокую химическую активность. Взаимодействует с неметаллами, в реакциях с которыми выступает окислителем. При контакте с водой превращается в азотную кислоту, со щелочной средой – образует нитриты и нитраты.
Получение диоксида азота в лабораторных условиях
В лабораториях двуокись азота в основном получают путем воздействия концентрированной азотной кислоты на медь:
Cu + 4HNO3 → (CuNO3)2 + 2NO2↑ + 2H2O.
Кроме того, соединение образуется при термическом разложении нитрата свинца.

В промышленных условиях применяется при производстве азотной и серной кислот, в качестве нитрующего агента для получения безводных нитратов и в роли окислителя в смесевых взрывчатых веществах и жидком ракетном топливе.
Антропогенные источники выбросов диоксида азота
Более 90% от общего количества выбросов оксидов азота попадают в воздушную среду при сжигании различных видов топлива. Начальной формой является NO, который, находясь в воздухе, окисляется кислородом при высокой температуре до NO2.

Основные источники, влияющие на выброс диоксида азота в атмосферу:
- автотранспортные средства, выхлопные газы которых вносят наибольший вклад в концентрацию вещества в городском воздухе;
- теплоэлектростанции;
- промышленные предприятия, в частности, нефтепромышленной и металлургической отрасли, а также заводы, производящие азотную кислоту и различные удобрения;
- сжигание твердых отходов (в частности, на мусоросжигательных заводах).

Бурый оттенок газа позволяет наблюдать его визуально в воздухе больших городов, где суточная динамика концентраций оксидов азота довольно тесно связана с интенсивностью движения автотранспортных средств и солнечного излучения. В утренние часы увеличение количества автомобилей на дорогах приводит к заметному повышению содержания монооксида азота, который с восходом солнца в результате фотохимического окисления переходит в NO2. Также бурый цвет имеют выбросы некоторых химических предприятий, из-за чего их называют «лисьими хвостами». Особенно заметны они летом.

Санитарно-гигиенические характеристики
Среди всех окислов группы NOx самым опасным для окружающей среды и человека является именно диоксид азота. Класс опасности – второй. Это значит, что NO2 относится к высокоопасным веществам. Предельно допустимая максимально-разовая концентрация (ПДК) диоксида азота в воздухе населенных пунктов равна 0,085 мг/м3, среднесуточная – 0,04.
Для воздуха рабочей зоны установлены другие нормативные значения. Так, значение предельно допустимой концентрации (ПДК р. з.) составляет 2 мг/м3 соединения (диоксид азота). Класс опасности – третий. То есть NO2 отнесен к опасным веществам.
Диоксид азота: влияние на человека
Вещество характеризуется высокой токсичностью. Диоксид азота в воздухе, даже находясь в относительно небольших концентрациях, способен приводить к существенным изменениям в организме человека. Является острым раздражителем, а также характеризуется общетоксическим действием. Воздействует в основном на органы дыхательной системы. В зависимости от концентраций наблюдаются различные последствия — от слабого раздражения слизистых оболочек глаз и носа до отека легких. Также может приводить к изменениям состава крови, в частности, способствует уменьшению содержания гемоглобина. Ниже рассмотрим подробнее некоторые из эффектов, которые способен вызывать у человека диоксид азота.

Влияние на обоняние
Даже если концентрация диоксида азота будет невысокой, люди способны ощущать его специфический запах. Пороговым значением фиксации газа в воздухе для человека считается 0,23 мг на куб. метр. Но при вдыхании диоксида азота в течение 10 минут теряется способность ощущать его запах, что говорит о негативном воздействии на обоняние, выражающемся в его ослаблении. При этом наблюдаются неприятная сухость в горле и раздражение слизистой, которые проходят при концентрации, превышающей пороговое значение обнаружения в 15 раз. Однако на смену приходят другие, более серьезные симптомы, означающие негативное воздействие двуокиси азота на органы дыхания.
Влияние диоксида азота на зрение
Одним из последствий комплексного воздействия на слизистые оболочки является ухудшение способности человека видеть в сумерках. Теряется возможность приспособления к отсутствию света. Пороговая концентрация по изменению световой чувствительности глаза составляет 0,14 мг на куб. метр. Учитывая то, что значение обонятельного восприятия почти в два раза выше, можно говорить о способности газа негативно воздействовать и при этом оставаться незамеченным.
Влияние на органы дыхания
При относительно невысоких концентрациях диоксид азота в атмосфере способен нарушать дыхание. Так, уже при содержании его в воздухе 0,056 мг на куб. метр у здорового человека наблюдается повышение сопротивления дыхательных путей. Согласно информации Всемирной Организации Здравоохранения, у людей, страдающих хроническими заболеваниями дыхательной системы, данные симптомы наблюдаются уже при содержании NO2 в воздухе, равном 0,04 мг на куб. метр.
Результатом воздействия больших концентраций оксидов азота может быть отек легких. Это объясняется следующим. При попадании в организм и взаимодействии с влагой диоксид и оксид азота образуют азотистую и азотную кислоты, разъедающие стенки альвеол легких. Они, как и кровеносные капилляры, становятся легко проницаемыми. В результате сыворотка крови попадает в полость легких. При вдыхании воздух с жидкостью образуют пену, которая нарушает нормальный газообмен, что приводит к возникновению отека легких.
При длительном воздействии окисей азота человек становится более восприимчивым к патогенам, которые вызывают болезни дыхательных путей. Ухудшается сопротивляемость легких к бактериям, расширяются альвеолы, клетки в корешках бронхов, чаще наблюдаются бронхиты, воспаление легких и пр.
У людей, страдающих сердечно-сосудистыми заболеваниями и хроническими болезнями дыхательных путей, легче развиваются осложнения в случае возникновения кратковременных респираторных инфекций, поскольку у них больше развита чувствительность к прямым воздействиям такого соединения, как диоксид азота.
Влияние на человека: другие последствия
Азотистая кислота, образующаяся при взаимодействии с влагой в дыхательных путях, вступает в реакцию со щелочными компонентами тканей, превращаясь в результате в нитриты и нитраты. Воздействие этих веществ вызывает ряд негативных последствий. Так, нитриты, всасываясь в кровь, приводят к угнетению центральной нервной системы, образованию метгемоглобина, гемолизу, билирубинемии, расширяют кровеносные сосуды, снижают артериальное давление и пр. Нитраты же при нахождении в кишечнике способны трансформироваться в канцерогенные вещества — нитрозамины.
Согласно ряду литературных источников, воздействие двуокиси азота на организм человека снижает его сопротивляемость к заболеваниям, приводит к кислородному голоданию тканей. Особенно остро это проявляется у детей. Также диоксид азота способствует повышению действия канцерогенных веществ и возникновению в результате этого злокачественных новообразований.
Некоторые из исследователей связывают повышенную смертность от раковых и сердечно-сосудистых заболеваний в определенных районах с высоким содержанием NO2 в воздушной среде.
Хроническое отравление диоксидом азота
Длительная работа в условиях присутствия диоксида азота в воздухе приводит к развитию хронических заболеваний, наиболее распространенными среди которых являются: трахеит, бронхит, перфорация носовой перегородки, пневмосклероз и др.
У людей, которые работали на протяжении 3-5 лет при содержании NO2 в воздухе рабочей зоны 0,8-5 мг на куб. метр, наблюдались хронические бронхиты, воспалительные изменения слизистой оболочки десен, осложненный астмоидными приступами пневмосклероз, бронхоэктазии. Кроме того, отмечались повышения максимальной осмотической резистентности эритроцитов, ускорение свертывания крови, тенденция к гипотонии, гранулоцитоз, снижение активности каталазы, содержания сахара и уровня глобулинов и альбуминов в крови.
У детей, проживающих на территориях, где диоксид азота присутствовал в концентрациях 0,117-0,205 мг на куб. метр, выявлены изменения объема форсированного выдоха, повышение заболеваемости. Кроме того, в мазках крови наблюдались изменения в конфигурации лимфоцитов и моноцитов, увеличение резистентности эритроцитов.
Выводы
Как видим из вышеприведенного материала, азота диоксид в атмосферном воздухе может крайне негативно сказываться на организме человека. К сожалению, превышения допустимых концентраций этого вещества в воздухе – не редкость. Поэтому довольно актуальными на сегодняшний день являются вопросы, касающиеся разработки мероприятий, направленных на снижение выбросов диоксида азота в атмосферу, которые имеют как экологическое, так и санитарно-гигиеническое значение.
www.syl.ru
Оксид азота(IV) — это… Что такое Оксид азота(IV)?
 Бурый газ
Бурый газОксид азота (IV) (диоксид азота, бурый газ) NO2 — газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона. При температуре 140 °C диоксид азота состоит только из молекул NO2, он очень тёмного, почти чёрного цвета. В точке кипения NO2 представляет собой желтоватую жидкость, содержащую около 0,1 % NO2. При температуре ниже 21°С — это бесцветная жидкость (или желтоватая из-за примеси мономера). При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Получение
В лаборатории NO2 обычно получают воздействием концентрированной азотной кислотой на медь:
Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность:
Химические свойства
Кислотный оксид, ему соответствуют азотная и азотистая кислоты. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
Жидкий NO2 применяется для получения безводных нитратов:
Применение
Физиологическое действие
Оксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
«Лисий хвост»
На фото справа — «лисий хвост» на Нижнетагильском металлургическом комбинате«Лисий хвост» — жаргонное название выбросов в атмосферу оксидов азота на химических предприятиях (иногда — из выхлопных труб автомобилей). Название происходит от оранжево-бурого цвета диоксида азота. При низких температурах диоксид азота димеризуется и становится бесцветным. В летний сезон «лисьи хвосты» наиболее заметны, так как в выбросах возрастает концентрация мономерной формы.
Вредное воздействие
Оксиды азота, улетучивающиеся в атмосферу, представляют серьёзную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек.
Двуокись азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина.
В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований.
Образующаяся в результате взаимодействия диоксида азота с водой азотная кислота является сильным коррозионным агентом.
dal.academic.ru
Окислы азота — Знаешь как
Содержание статьи
Окислы азота что это

Рис. Прибор дли демонстрации горения азота в кислороде.
Азот образует с кислородом шесть окислов: закись азота N2O, окись азота NO, двуокись азота NO2, четырехокись азота N2O4, азотистый ангидрид N2O3и азотный ангидрид N2O5. Все они могут быть получены из азотной кислоты и ее солей.
Закись азота N2O. Закись азота получается при нагревании нитрата аммония:
NH4NO3 = N2O + 2H2O
При этой реакции один из атомов азота, входящих в состав Nh5NO3, теряет электроны, а другой — приобретает их, причем оба атома азота становятся положительно одновалентными.
Закись азота представляет собой бесцветный, не имеющий запаха газ, сгущающийся в жидкость при 0° под давлением 30 ат. Она довольно хорошо растворима в воде: при 0° один объем воды растворяет 1,3, а при 25° — 0,6 объема N2O. При растворении закись азота никакого соединения с водой не образует.
Закись азота — эндотермическое соединение, легко разлагающееся при нагревании на азот и кислород:
2N2O = 2N2+ O2 + 19,5 ккал
поэтому она хорошо поддерживает горение. Тлеющая лучинка, опущенная в закись азота, вспыхивает в ней, как в чистом кислороде; фосфор, сера и другие вещества также энергично сгорают в закиси азота, освобождая азот.
Закись азота для чего
Вдыхание небольших количеств закиси азота приводит к притуплению болевой чувствительности, вследствие чего этот газ иногда применяют в смеси с кислородом для наркоза при легких операциях. Большие количества закиси азота возбуждающе действуют на нервную систему; поэтому раньше ее называли «веселящим газом».
Азот оксид
Окись азота NO. При обыкновенных условиях азот и кислород не вступают в реакцию друг с другом. Но при очень высокой температуре, например при пропускании электрических искр через воздух, азот может непосредственно соединяться с кислородом, давая окись азота. Поэтому окись азота всегда образуется в атмосфере при грозовых разрядах.
Образование окиси азота при электрическом разряде может быть иллюстрировано следующим опытом. В большую колбу (рис.) через боковые горла вставляют на пробках две толстые медные проволоки и соединяют их с полюсами большой индукционной катушки. При пропускании через катушку тока между концами проволок образуется непрерывная искра, а над ней появляется желтоватое пламя «горящего» в кислороде азота.
Реакция образования окиси азота из азота и кислорода обратима и сопровождается поглощением большого количества тепла:
N2 + О2 ⇄ 2NO — 43,2 ккал .
При низкой температуре равновесие этой реакции практически полностью сдвинуто влево, т. е, количество образующейся окиси азота ничтожно мало. С повышением температуры равновесие начинает смещаться вправо, и о так медленно, что даже при 1000° в смеси газов содержится всего лишь около 1% окиси азота. При понижении температуры окись азота снова разлагается на азот и кислород. Но если очень быстро охладить газовую смесь, то равновесие не успевает сразу сместиться, а потом уже не смещается вследствие крайне малой скорости реакции при низкой температуре, и таким образом, в смеси остается почти то же количество NO, которое образовалось при высокой температуре. В лаборатории окись азота получают обычно взаимодействием разбавленной азотной кислоты с медью:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4Н2O
или в ионной форме
3Cu + 2NO3‘ + 8H• = 3Cu•• + 2NO + 4H2O
Окись азота представляет собой бесцветный газ, очень трудно сжижаемый. Жидкая окись азота кипит при —151,8° и затвердевает при —163,7°
В воде она растворима лишь незначительно один объем воды растворяет при 0° всего 0,07 объема NO.
По химическим свойствам окись азота относится к числу безразличных окислов, так как не образует никакой кислоты.
Окись азота труднее других окислов азота отдает свой кислород. Поэтому в ней могут гореть лишь такие вещества, которые особенно энергично соединяются с кислородом, как, например, фосфор. Но зажженная свеча, лучинка, сера гаснут при внесении их в окись азота.
Наиболее характерным свойством окиси азота является ее способность легко, без всякого нагревания, соединяться с кислородом с образованием бурой двуокиси азота:
2NO + О2 = 2NO2 — 27 ккал
Если, например, открыть цилиндр, наполненный окисью азота, то у отверстия его тотчас же появляется бурое облако двуокиси азота.
Двуокись азота
Бурый ядовитый газ, обладающий характерным запахом. Он легко сгущается в красноватую жидкость (темп. кип. 21,3°), которая при охлаждении постепенно светлеет и при —10° замерзает, образуя бесцветную кристаллическую массу. Наоборот, при нагревании газообразной двуокиси азота ее окраска усиливается, а при 140° становится почти черной. Изменение окраски двуокиси азота при повышении температуры сопровождается и изменением плотности ее пара. При низкой температуре плотность пара приблизительно отвечает удвоенной формуле N2O4. С повышением температуры плотность пара уменьшается и при 140° в точности соответствует формуле NО2—Отсюда следует, что бесцветные кристаллы, существующие при —10° и ниже, состоят, вероятно, целиком из молекул N2О4 и могут быть названы четырехокисью азота. По мере нагревания бесцветная четырехокись азота постепенно диссоциирует с образованием молекул темнобурой двуокиси азота N02;полная диссоциация происходит при 140°. Поэтому при температурах от —10° до +140° всегда имеется смесь молекул NO2и N2О4, находящихся в равновесии друг с другом:
N2О4⇄ 2NО2— 13,6 ккал
Выше 140° начинается диссоциация NО2 на NO и кислород.
Двуокись азота очень энергичный окислитель. Многие вещества могут гореть в двуокиси азота, отнимая от нее кислород. Сернистый газ окисляется ею в серный ангидрид, на чем основан нитрозный метод получения серной кислоты.
Пары двуокиси азота довольно ядовиты. Вдыхание их вызывает сильное раздражение дыхательных путей и может привести к серьезному отравлению.
При растворении в воде двуокись или, вернее, четырехокись азота вступает в реакцию с водой, образуя азотную и азотистую кислоты:
N2O4 + Н2O = HNO3 + HNО2
Но азотистая кислота очень неустойчива и быстро разлагается на азотную кислоту, окись азота и воду:
3HNO2 = HNO3 + 2NO + Н2O
Поэтому практически взаимодействие двуокиси (четырех окиси) азота с водой, особенно с теплой, идет по уравнению
3N2O4 + 2Н2O = 4HNO3 + 2NO
которое легко может быть получено сложением двух предыдущих уравнений, если предварительно первое из них умножить на 3.
В присутствии воздуха образующаяся окись азота немедленно окисляется в двуокись азота, так что в этом случае NO2полностью переходит в азотную кислоту. Эта реакция имеет важное техническое значение и используется в современных способах получения азотной кислоты.
Если растворять двуокись (четырехокись) азота в щелочах, то образуется смесь солей азотной и азотистой кислот:
N2O4 + 2NaOH = NaNO3 + NaNO2 + H2O
Приведенные выше реакции взаимодействия четырехокиси азота с водой и щелочами показывают, что в молекуле этого вещества один атом азота имеет валентность +5, а другой — валентность +3. Поэтому четырехокись азота часто называют смешанным ангидридом азотистой и азотной кислот и изображают ее структурную формулу следующим образом:

Если мы подсчитаем общее число валентных электронов у всех атомов в молекулах NO и NO2, то найдем, что оно равно соответственно 11 (5 + 6) и 17 (5 + 2•6), т. е. выражается нечетными числами. Окись и двуокись азота относятся к ограниченному числу молекул с нечетным числом электронов. Такие молекулы ведут себя в химическом отношении, как свободные атомы, тоже имеющие неспаренные электроны. Молекулы с неспаренными электронами называются свободными радикалами.
Азотистый ангидрид N2O3
Представляет собой темно-синюю жидкость, кипящую при +4° и разлагающуюся при этом на окись и двуокись азота. Смесь равных объемов окиси и двуокиси азота при охлаждении вновь образует азотистый ангидрид:
N2O3 ⇄ NO + NO2
Азотистому ангидриду соответствует азотистая кислота.
Азотный ангидрид N2O5 — твердое кристаллическое вещество, плавящееся при 30°. Он может быть получен действием фосфорного ангидрида на азотную кислоту:
2HNO3 + Р205 = N2O5 + 2НРО3
Азотный ангидрид является очень сильным окислителем. Многие органические вещества при соприкосновении с ним воспламеняются. В воде азотный ангидрид легко растворяется с образованием азотной кислоты.
139 140 141
Вы читаете, статья на тему Окислы азота
znaesh-kak.com
ДВУОКИСЬ АЗОТА — это… Что такое ДВУОКИСЬ АЗОТА?
- ДВУОКИСЬ АЗОТА
ДВУОКИСЬ АЗОТА (NO2), оксид азота. Бурый газ с резким запахом. С легкостью превращается в димер (две идентичные молекулы, связанные друг с другом) четырехокиси азота (N2O4
Научно-технический энциклопедический словарь.
- ДВУЛЕТНИК
- ДВУСТВОРЧАТЫЕ
Смотреть что такое «ДВУОКИСЬ АЗОТА» в других словарях:
двуокись азота — azoto dioksidas statusas T sritis radioelektronika atitikmenys: angl. nitrogen dioxide vok. Stickstoffdioxid, n rus. двуокись азота, f pranc. bioxyde d azote, m; peroxyde d azote, m … Radioelektronikos terminų žodynas
двуокись азота — azoto dioksidas statusas T sritis apsauga nuo naikinimo priemonių apibrėžtis Dusinamoji pavojingoji cheminė medžiaga. Rusvos spalvos dujos. Lydymosi temperatūra 11,2 °C, virimo temperatūra 21,3 °C. 1,5 karto sunkesnis už orą. Gerai tirpsta… … Apsaugos nuo naikinimo priemonių enciklopedinis žodynas
двуокись азота — azoto dioksidas statusas T sritis ekologija ir aplinkotyra apibrėžtis Azoto junginys su deguonimi (NO₂) – rudos, troškios dujos. atitikmenys: angl. nitrogen dioxide vok. Stickstoffdioxid, n rus. двуокись азота, f … Ekologijos terminų aiškinamasis žodynas
Азота окислы — соединения азота с кислородом. Известны N2O, NO, N2O3, NO2 (и его димер N2O4), N2O5; есть сведения о существовании NO3, не выделенного в свободном состоянии. При высокой температуре в пламени вольтовой дуги, а в природе при электроразряде … Большая советская энциклопедия
азота двуокись — azoto(IV) oksidas statusas T sritis chemija formulė NO₂ atitikmenys: angl. nitrogen dioxide; nitrogen(IV) oxide rus. азота двуокись; азота диоксид; азота(IV) оксид ryšiai: sinonimas – azoto dioksidas … Chemijos terminų aiškinamasis žodynas
азота диоксид — azoto(IV) oksidas statusas T sritis chemija formulė NO₂ atitikmenys: angl. nitrogen dioxide; nitrogen(IV) oxide rus. азота двуокись; азота диоксид; азота(IV) оксид ryšiai: sinonimas – azoto dioksidas … Chemijos terminų aiškinamasis žodynas
азота(IV) оксид — azoto(IV) oksidas statusas T sritis chemija formulė NO₂ atitikmenys: angl. nitrogen dioxide; nitrogen(IV) oxide rus. азота двуокись; азота диоксид; азота(IV) оксид ryšiai: sinonimas – azoto dioksidas … Chemijos terminų aiškinamasis žodynas
Двуокись — Оксид (окисел, окись) соединение химического элемента с кислородом, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам… … Википедия
Двуокись — название, весьма часто применяемое для обозначения окислов (см.) состава RO2, содержащих кислорода вдвое более, чем в окисях RO. Если окисел состава RO2 принадлежит металлическому элементу, то его обыкновенно называют Д. тогда, когда он не… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
двуокись — и; ж. Химическое соединение, в котором один атом какого л. элемента соединён с двумя атомами кислорода. Д. азота … Энциклопедический словарь
dic.academic.ru
Окись азота — это… Что такое Окись азота?
Окси́д азо́та (II) NO (моноксид азота, окись азота, нитрозил-радикал) — несолеобразующий оксид азота. Он представляет собой бесцветный газ, плохо растворимый в воде. Сжижается с трудом; в жидком и твёрдом виде имеет голубой цвет.
Наличие неспаренного электрона обусловливает склонность NO к образованию слабосвязанных димеров N2O2. Это непрочные соединения с ΔH° димеризации = 17 кДж. Жидкий оксид азота (II) на 25% состоит из молекул N2O2, а твердый оксид целиком состоит из них.
Получение
- N2 + O2 → 2NO — 180,9 кДж
и тотчас же реагирует с кислородом:
- 2NO + O2 → 2NO2.
При понижении температуры оксид азота(II) разлагается на азот и кислород, но если температура падает резко, то не успевший разложиться оксид существует достаточно долго: при низкой температуре скорость распада невелика. Такое резкое охлаждение называется «закалкой» и используется при одном из способов получения азотной кислоты.
В лаборатории его обычно получают взаимодействием 30%-ной HNO3 с некоторыми металлами, например, с медью:
- 3Cu + 8HNO3 (30 %) → 3Cu(NO3)2 + 2NO↑ + 4H2O.
Более чистый, не загрязнённый примесями NO можно получить по реакциям:
- FeCl2 + NaNO2 + 2HCl → FeCl3 + NaCl + NO↑ + H2O;
- 2HNO2 + 2HI → 2NO↑ + I2↓ + 2H2O.
Промышленный способ основан на окислении аммиака при высокой температуре и давлении при участии Pt, Cr2O3 (как катализаторов):
- 4NH3 + 5O2 → 4NO + 6H2O.
Химические свойства
При комнатной температуре и атмосферном давлении окисление NO кислородом воздуха происходит мгновенно:
- 2NO + O2 → 2NO2
Для NO характерны также реакции присоединения галогенов с образованием нитрозилгалогенидов, в этой реакции NO проявляет свойства восстановителя:
- 2NO + Cl2 → 2NOCl (нитрозилхлорид).
В присутствии более сильных восстановителей NO проявляет окислительные свойства:
- 2SO2 + 2NO → 2SO3 + N2↑.
В воде NO мало растворим и с ней не реагирует, являясь несолеобразующим оксидом.
Физиологическое действие

Оксид азота (белый) в цитоплазме клеток хвойных пород деревьев через час после механического воздействия.
Как и все оксиды азота (кроме N2O), NO — токсичен, при вдыхании поражает дыхательные пути.
За два последних десятилетия было установлено, что эта молекула NO обладает широким спектром биологического действия, которое условно можно разделить на регуляторное, защитное и вредное. NO, являясь одним из мессенджеров, участвует в регуляции систем внутри- и межклеточной сигнализации. Оксид азота, производимый клетками эндотелия сосудов, отвечает за расслабление гладких мышц сосудов и их расширение(вазодилатацию), предотвращает агрегацию тромбоцитов и адгезию нейрофилов к эндотелию, участвует в различных процессах в нервной, репродуктивной и иммунной системах. NO также обладает цитотоксическими и цитостатическими свойствами. Клетки-киллеры иммунной системы используют оксид азота для уничтожения бактерий и клеток злокачественных опухолей. С нарушением биосинтеза и метаболизма NO связаны такие заболевания, как ассенциальная артериальная гипертензия, ишемическая болезнь сердца, инфаркт миокарда, первичная легочная гипертензия, бронхиальная астма, невротическая депрессия, эпилепсия, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), сахарный диабет, импотенция и др.
Оксид азота может синтезироваться несколькими путями. Растения используют неферментативную фотохимическую реакцию между NO2 и каротиноидами. У животных синтез осуществляют семейство NO-синтаз (NOS). NOS-ферменты – члены гем-содержащего суперсемейства ферментов, названных монооксигеназами. В зависимости от структуры и функций, NOS могут быть разделены на три группы: эндотелиальные (eNOS), нейрональные (nNOS) и индуцибельные (iNOS). В активный центр любой из NO-синтаз входит железопорфириновый комплекс, содержащий аксиально координированный цистеин или метионин. Хотя все изоформы NOS катализируют образование NO, все они являются продуктами различных генов, каждая из них имеет свои особенности как в механизмах действия и локализации, так и в биологическом значении для организма. Поэтому указанные изоформы принято также подразделять на конститутивную (cNOS) и индуцибельную (iNOS) синтазы оксида азота. cNOS постоянно находится в цитоплазме, зависит от концентрации ионов кальция и кальмодулина (белок, являющийся внутриклеточным посредником переноса ионов кальция) и способствует выделению небольшого количества NO на короткий период в ответ на стимуляцию рецепторов. Индуцибельная NOS появляется в клетках только после индукции их бактериальными эндотоксинами и некоторыми медиаторами воспаления, такими как гамма-интерферон, фактор некроза опухоли и др. Количество NO, образующегося под влиянием iNOS, может варьировать и достигать больших количеств (наномолей). При этом продукция NO сохраняется длительнее. Характерной особенностью NO является способность быстро (менее чем за 5 секунд) диффундировать через мембрану синтезировавшей его клетки в межклеточное пространство и легко (без участия рецепторов) проникать в клетки-мишени. Внутри клетки он активирует одни энзимы и ингибирует другие, таким образом, участвуя в регуляции клеточных функций. По сути, монооксид азота является локальным тканевым гормоном. NO играет ключевую роль в подавлении активности бактериальных и опухолевых клеток путем либо блокирования некоторых их железосодержащих ферментов, либо путем повреждения их клеточных структур оксидом азота или свободными радикалами, образующимися из оксида азота. Одновременно в очаге воспаления накапливается супероксид, который вызывает повреждение белков и липидов клеточных мембран, что и объясняет его цитотоксическое действие на клетку-мишень. Следовательно, NO, избыточно накапливаясь в клетке, может действовать двояко: с одной стороны вызывать повреждение ДНК и с другой — давать провоспалительный эффект. Оксид азота способен инициировать ангиогенез (образование кровеносных сосудов). В случае инфаркта миокарда оксид азота играет положительную роль, т.к. индуцирует новый сосудистый рост, но при раковых заболеваниях тот же самый процесс вызывает развитие опухолей, способствуя питанию и росту раковых клеток. С другой стороны, вследствие этого улучшается доставка оксида азота в опухолевые клетки. Повреждение ДНК под действием NO является одной из причин развития апоптоза (запрограммированный процесс клеточного «самоубийства», направленный на удаление клеток, утративших свои функции). В экспериментах наблюдалось дезаминирование дезоксинуклеозидов, дезоксинуклеотидов и неповрежденной ДНК при воздействии раствора, насыщенного NO. Этот процесс ответственен за повышение чувствительности клеток к алкилирующим агентам и ионизирующему излучению, что используется в антираковой терапии.
Клиренс NO (скорость очищения крови от NO в процессе его химических превращений) происходит путем образования нитритов и нитратов и составляет в среднем не более 5 секунд. В клиренс могут быть вовлечены промежуточные ступени, связанные со взаимодействием с супероксидом или с гемоглобином с образованием пероксинитрита. Оксид азота может быть восстановлен NO-редуктазой – ферментом, тесно связанным с NO-синтазой.
В 1998 году трое американцев — Фурчготт, Игнарро и Мюрад — были удостоены премии Нобелевского комитета по физиологии «за открытия, касающиеся окиси азота как сигнальной молекулы в сердечно-сосудистой системе».
Применение
Получение NO является одной из стадий получения азотной кислоты .
Wikimedia Foundation. 2010.
dikc.academic.ru
Оксиды азота — это… Что такое Оксиды азота?
Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.
Список оксидов
Известны девять соединений азота с кислородом. Кроме пяти классических оксидов азота:
-

Оксид диазота, N2O
-

Оксид азота, NO
-

Триоксид диазота , N2O3
-

Диоксид азота , NO2
-

Пентаоксид диазота, N2O5
обнаружены ещё димер диоксида азота (NO2)2 и три малостабильных соединения: нитрозилазид N4O, тринитрамид N(NO2)3 и нитратный радикал NO3.
N2O
Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.
NO
Оксид азота NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
N2O3(III)
Оксид N2O3 (триоксид диазота, азотистый ангидрид) — темно-синяя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NO2, N2O4(IV)
Оксид азота NO2 (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NO2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
и растворами щелочей:
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NO2. Этот оксид окисляет SO2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
N2O5(V)
Оксид азота N2O5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
N(NO2)3
Тринитрамид открыт в 2010 году. Является перспективным кандидатом на роль высокоэффективного ракетного топлива, однако на данный момент неизвестно, является ли устойчивой твёрдая фаза вещества.
N4O
Основная статья: Нитрозилазид
Существует при температуре ниже −50 °C как бледно-жёлтое твёрдое вещество, выше этой температуры разлагается на N2O и N2.
Воздействие на организм
Все оксиды азота физиологически активны, относятся к третьему классу опасности.
Оксид азота N2O обладает наркозным эффектом и используется в хирургической практике. Оксид азота NO — сильный яд, оказывающий влияние на ЦНС, а также вызывающий поражение крови за счёт связывания гемоглобина. Относительно высокой токсичностью (при концентрации выше 0,05 мг/л) обладает и оксид азота NO2. Он раздражает дыхательные пути и угнетает аэробное окисление в легочной ткани, что приводит к развитию токсического отёка легких.
Применение
Закись азота используется в медицине для наркоза, в пищевой промышленности в качестве пропеллента и упаковочного газа (зарегистрирована в качестве пищевой добавки E942).
См. также
Выхлопные газы
 | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 14 мая 2011. |
biograf.academic.ru
Оксиды азота — это… Что такое Оксиды азота?
Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.
Список оксидов
Известны девять соединений азота с кислородом. Кроме пяти классических оксидов азота:
-

Оксид диазота, N2O
-

Оксид азота, NO
-

Триоксид диазота , N2O3
-

Диоксид азота , NO2
-

Пентаоксид диазота, N2O5
обнаружены ещё димер диоксида азота (NO2)2 и три малостабильных соединения: нитрозилазид N4O, тринитрамид N(NO2)3 и нитратный радикал NO3.
N2O
Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.
NO
Оксид азота NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
N2O3(III)
Оксид N2O3 (триоксид диазота, азотистый ангидрид) — темно-синяя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NO2, N2O4(IV)
Оксид азота NO2 (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NO2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
и растворами щелочей:
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NO2. Этот оксид окисляет SO2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
N2O5(V)
Оксид азота N2O5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
N(NO2)3
Тринитрамид открыт в 2010 году. Является перспективным кандидатом на роль высокоэффективного ракетного топлива, однако на данный момент неизвестно, является ли устойчивой твёрдая фаза вещества.
N4O
Основная статья: Нитрозилазид
Существует при температуре ниже −50 °C как бледно-жёлтое твёрдое вещество, выше этой температуры разлагается на N2O и N2.
Воздействие на организм
Все оксиды азота физиологически активны, относятся к третьему классу опасности.
Оксид азота N2O обладает наркозным эффектом и используется в хирургической практике. Оксид азота NO — сильный яд, оказывающий влияние на ЦНС, а также вызывающий поражение крови за счёт связывания гемоглобина. Относительно высокой токсичностью (при концентрации выше 0,05 мг/л) обладает и оксид азота NO2. Он раздражает дыхательные пути и угнетает аэробное окисление в легочной ткани, что приводит к развитию токсического отёка легких.
Применение
Закись азота используется в медицине для наркоза, в пищевой промышленности в качестве пропеллента и упаковочного газа (зарегистрирована в качестве пищевой добавки E942).
См. также
Выхлопные газы
 | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 14 мая 2011. |
biograf.academic.ru