Оксиды азота
Оксиды азота
При описании свойств азота отмечалось, что при непосредственном взаимодействии азота с кислородом образуется только оксид азота (II) NO. Однако существуют оксиды азота со всеми возможными степенями окисления (от +1 до +5).
N2O — оксид азота (I), «веселящий газ»
При обычной температуре N2O — бесцветный газ со слабым приятным запахом и сладковатым вкусом; обладает наркотическим действием, вызывая сначала судорожный смех, затем — потерю сознания.
Способы получения
1. Разложение нитрата аммония при небольшом нагревании:
NH4NO3 = N2O↑ + 2Н2О
2. Действие HNO3 на активные металлы
10HNO3(конц.) + 4Са = N2O↑ + 4Ca(NO3)2 + 5Н2О
Химические свойства
N2O не проявляет ни кислотных, ни основных свойств, т. е. не взаимодействует с основаниями, с кислотами, с водой (несолеобразующий оксид).
При Т > 500’С разлагается на простые вещества. N
N2O + SO2 + Н2О = N2↑ + H2SO4
NO — оксид азота (II), монооксид азота.
При обычной температуре NO — бесцветный газ без запаха, малорастворимый в воде, очень токсичный (в больших концентрациях изменяет структуру гемоглобина).
Способы получения
1. Прямой синтез из простых веществ может быть осуществлен только при очень высокой Т:
N2 + O2 = 2NО — Q
2. Получение в промышленности (1-я стадия производства HNO3).
4NH3 + 5O2 = 4NО + 6Н2О
3. Лабораторный способ — действие разб. HNO
8HNO3 + 3Cu = 2NO + 3Cu(NO3)2 + 4Н2О
Химические свойства
NO — несолеобразующий оксид (подобно N2О). Обладает окислительно-восстановительной двойственностью.
2NO + SO2 + Н2О = N2O↑ + H2SO4
2NO + 2H2 = N2 + 2Н2О (со взрывом)
2NO + O2 = 2NO2
10NO + 6KMnO4 + 9H2SO4 = 10HNO3 + 3K2SO4 + 6MnSO4 + 4Н2О
NO2 — оксид азота (IV), диоксид азота
При обычной температуре NO2
Способы получения
I. Промышленный — окисление NO: 2NO + O2 = 2NO2
II. Лабораторные:
действие конц. HNO3 на тяжелые металлы: 4HNO3 + Сu = 2NO2↑ + Cu(NO3)2 + 2Н2О
разложение нитратов: 2Pb(NO3)2 = 4NO2↑ + O2↑ + 2РbО
Химические свойства
NO2 взаимодействует с водой, основными оксидами и щелочами. Но реакции протекают не так, как с обычными оксидами — они всегда окислительно — восстановительные. Объясняется это тем, что не существует кислоты со С.О. (N) = +4, поэтому NO
2NO2 + Н2О = HNO3 + HNO2
Если растворение происходит в присутствии O2, то образуется одна кислота — азотная:
4NO2 + 2Н2О + O2 = 4HNO3
Аналогичным образом происходит взаимодействие NO2 со щелочами:
в отсутствие O2: 2NO2 + 2NaOH = NaNO3 + NaNO2 + Н2О
в присутствии O
По окислительной способности NO2 превосходит азотную кислоту. В его атмосфере горят С, S, Р, металлы и некоторые органические вещества. При этом NO2 восстанавливается до свободного азота:
10NO2 + 8P = 5N2 + 4P2O5
2NO2 + 8HI = N2 + 4I2 + 4Н2О (возникает фиолетовое пламя)
В присутствии Pt или Ni диоксид азота восстанавливается водородом до аммиака:
2NO2 + 7Н2 = 2NH3 + 4Н2О
Как окислитель NO2 используется в ракетных топливах. При его взаимодействии с гидразином и его производными выделяется большое количество энергии:
2NO2 + 2N2H4 = 3N2 + 4Н2О + Q
N2O3 и N2O5 — неустойчивые вещества
Оба оксида имеют ярко выраженный кислотный характер, являются соответственно ангидридами азотистой и азотной кислот.
N2O3 как индивидуальное вещество существует только в твердом состоянии ниже Т пл. (-100С).
С повышением температуры разлагается: N2O3 → NO + NO2
N2O5 при комнатной температуре и особенно на свету разлагается так энергично, что иногда самопроизвольно взрывается:
2N2O5 = 4NO2
examchemistry.com
Окислы азота — это… Что такое Окислы азота?
Оксиды азота — соединения азота с кислородом.
Список оксидов
Азот образует несколько соединений с кислородом:
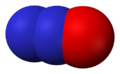 Оксид азота, N2O |  Оксид азота, NO | 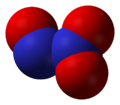 Оксид азота , N2O3 | 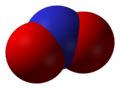 Оксид азота , NO2 |
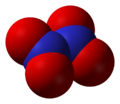 Оксид азота,(NO2)2 или N2O4 | 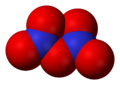 Азотный ангидрид, N2O5 |
N2O
Оксид азота N2O — бесцветный газ со слабым запахом, растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.
NO
Оксид азота NO — бесветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционноспособное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO
N2O3(III)
Оксид N2O3 (азотистый ангидрид) неустойчив при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NО2, N2O4
Оксид азота NО2 — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NО2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
2NO2 + Н2О = HNO3 + HNO2
2NO2 + 2NaOH = NaNO3 + NaNO2 + H2О
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NО2. Этот оксид окисляет SО2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
N2O5(V)
Оксид N2O5 (азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NО2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
Воздействие на организм
Все оксиды азота физиологически активны, относятся к третьему классу опасности. ПДК (оксид азота в пересчете на NO
Применение
Оксиды азота зарегистрированы в качестве пищевой добавки E918.
См.также
Выхлопные газы
Wikimedia Foundation. 2010.
dic.academic.ru
Оксид азота — это… Что такое Оксид азота?
Оксиды азота — соединения азота с кислородом.
Список оксидов
Азот образует несколько соединений с кислородом:
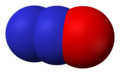 Оксид азота, N2O |  Оксид азота, NO | 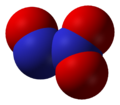 Оксид азота , N2O3 | 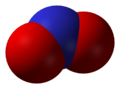 Оксид азота , NO2 |
 Оксид азота,(NO2)2 или N2O4 |  Азотный ангидрид, N2O5 |
N2O
Оксид азота N2O — бесцветный газ со слабым запахом, растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.
NO
Оксид азота NO — бесветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционноспособное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
N2O3(III)
Оксид N2O3 (азотистый ангидрид) неустойчив при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NО2, N2O4
Оксид азота NО2 — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NО2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
2NO2 + Н2О = HNO3 + HNO2 и растворами щелочей:
2NO2 + 2NaOH = NaNO3 + NaNO2 + H2О
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NО2. Этот оксид окисляет SО2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
N2O5(V)
Оксид N2O5 (азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NО2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
Воздействие на организм
Все оксиды азота физиологически активны, относятся к третьему классу опасности. ПДК (оксид азота в пересчете на NO2) – 5,0 мг/м3.
Применение
Оксиды азота зарегистрированы в качестве пищевой добавки E918.
См.также
Выхлопные газы
Wikimedia Foundation. 2010.
dik.academic.ru
Оксид азота (III) — это… Что такое Оксид азота (III)?
- Оксид азота (III)
Окси́д азо́та(III) (азотистый ангидрид, сесквиоксид азота) N2O3 — бесцветный газ (при н. у.), в твёрдом виде слабо-синего цвета. Устойчив только при температурах ниже −101 °C. Без примесей NO2 и NO он существует только в твёрдом виде.Получение
Рекомендуется капать 50%-ю азотную кислоту на твёрдый оксид мышьяка(III):
- 2HNO3 (50 %) + As2O3 → NO2↑ + NO↑ + HAsO3.
N2O3 образуется при охлаждении получающейся смеси газов.
При пропускании электрического разряда через жидкий воздух N2O3 можно получить в виде порошка голубого цвета:
- N2 + O2 → 2NO;
- 2NO + O2 → 2NO2;
- NO + 2NO2 → N2O3.
Также N2O3 можно получить действием 50%-ой азотной кислоты на крахмал.
Химические свойства
Кислотный оксид. N2O3 подвержен термической диссоциации:
- N2O3 ↔ NO2 + NO.
При 25 °C содержание N2O3 в смеси газов составляет около 10,5 %. Жидкий оксид азота (III) синего цвета, он также частично диссоциирован.
Являясь азотистым ангидридом, при взаимодействии с водой N2O3 даёт азотистую кислоту:
- N2O3 + H2O ↔ 2HNO2.
При взаимодействии с растворами щелочей образуются соответствующие нитриты:
- N2O3 + 2KOH → 2KNO2 + H2O.
Применение
Применяется в лаборатории для получения азотистой кислоты и её солей.
Физиологическое действие
Высоко токсичен. По действию на организм сравним с дымящей азотной кислотой. Вызывает тяжёлые ожоги кожи.
Wikimedia Foundation. 2010.
- Оксигенный фотосинтез
- Оксид азота (II)
Смотреть что такое «Оксид азота (III)» в других словарях:
Оксид азота(III) — Оксид азота(III) … Википедия
Оксид ниобия(III) — Общие Систематическое наименование Оксид ниобия(III) Традиционные названия Окись ниобия Химическая формула Nb2O3 Физические свойства Сос … Википедия
Оксид фосфора(III) — Оксид фосфора(III) … Википедия
Оксид азота(II) — Оксид азота(II) … Википедия
Оксид азота(IV) — Оксид азота(IV) … Википедия
Оксид азота(I) — Газ без цвета, со сладким вкусом и запахом Общие Систематическое наименование Оксонитрид азота(I) Химическая формула N2O Физические свойства … Википедия
Оксид азота(V) — Оксид азота(V) … Википедия
Оксид азота — Оксиды азота соединения азота с кислородом. Содержание 1 Список оксидов 2 N2O 3 NO 4 N2O3(III) 5 NО2, N2O4 … Википедия
азота(III) оксид — azoto(III) oksidas statusas T sritis chemija formulė N₂O₃ atitikmenys: angl. nitrogen trioxide rus. азота сесквиоксид; азота(III) оксид ryšiai: sinonimas – diazoto trioksidas … Chemijos terminų aiškinamasis žodynas
Фторид азота(III) — Фторид азота(III) … Википедия
dic.academic.ru
Оксид азота(IV) — это… Что такое Оксид азота(IV)?
 Бурый газ
Бурый газОксид азота (IV) (диоксид азота, бурый газ) NO2 — газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона. При температуре 140 °C диоксид азота состоит только из молекул NO2, он очень тёмного, почти чёрного цвета. В точке кипения NO2 представляет собой желтоватую жидкость, содержащую около 0,1 % NO2. При температуре ниже 21°С — это бесцветная жидкость (или желтоватая из-за примеси мономера). При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Получение
В лаборатории NO2 обычно получают воздействием концентрированной азотной кислотой на медь:
Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность:
Химические свойства
Кислотный оксид, ему соответствуют азотная и азотистая кислоты. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
Жидкий NO2 применяется для получения безводных нитратов:
Применение
В производстве серной и азотной кислот, в качестве окислителя в жидком ракетном топливе и смесевых взрывчатых веществах.
Физиологическое действие
Оксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
«Лисий хвост»
На фото справа — «лисий хвост» на Нижнетагильском металлургическом комбинате«Лисий хвост» — жаргонное название выбросов в атмосферу оксидов азота на химических предприятиях (иногда — из выхлопных труб автомобилей). Название происходит от оранжево-бурого цвета диоксида азота. При низких температурах диоксид азота димеризуется и становится бесцветным. В летний сезон «лисьи хвосты» наиболее заметны, так как в выбросах возрастает концентрация мономерной формы.
Вредное воздействие
Оксиды азота, улетучивающиеся в атмосферу, представляют серьёзную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек.
Двуокись азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина.
В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований.
Образующаяся в результате взаимодействия диоксида азота с водой азотная кислота является сильным коррозионным агентом.
biograf.academic.ru
Оксид азота(IV) — это… Что такое Оксид азота(IV)?
 Бурый газ
Бурый газОксид азота (IV) (диоксид азота, бурый газ) NO2 — газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона. При температуре 140 °C диоксид азота состоит только из молекул NO2, он очень тёмного, почти чёрного цвета. В точке кипения NO2 представляет собой желтоватую жидкость, содержащую около 0,1 % NO2. При температуре ниже 21°С — это бесцветная жидкость (или желтоватая из-за примеси мономера). При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Получение
В лаборатории NO2 обычно получают воздействием концентрированной азотной кислотой на медь:
Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность:
Химические свойства
Кислотный оксид, ему соответствуют азотная и азотистая кислоты. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
Жидкий NO2 применяется для получения безводных нитратов:
Применение
В производстве серной и азотной кислот, в качестве окислителя в жидком ракетном топливе и смесевых взрывчатых веществах.
Физиологическое действие
Оксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
«Лисий хвост»
На фото справа — «лисий хвост» на Нижнетагильском металлургическом комбинате«Лисий хвост» — жаргонное название выбросов в атмосферу оксидов азота на химических предприятиях (иногда — из выхлопных труб автомобилей). Название происходит от оранжево-бурого цвета диоксида азота. При низких температурах диоксид азота димеризуется и становится бесцветным. В летний сезон «лисьи хвосты» наиболее заметны, так как в выбросах возрастает концентрация мономерной формы.
Вредное воздействие
Оксиды азота, улетучивающиеся в атмосферу, представляют серьёзную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек.
Двуокись азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина.
В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований.
Образующаяся в результате взаимодействия диоксида азота с водой азотная кислота является сильным коррозионным агентом.
dik.academic.ru
АЗОТА ОКСИДЫ — это… Что такое АЗОТА ОКСИДЫ?
АЗОТА ОКСИДЫ — АЗОТА ОКСИДЫ: гемиоксид N2O и монооксид NO (бесцветные газы) сесквиоксид N2O3 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2O4), оксид N2O5 (бесцветные кристаллы). N2O и NO несолеобразующие оксиды, N2O3 с … Большой Энциклопедический словарь
АЗОТА ОКСИДЫ — АЗОТА ОКСИДЫ: гемиоксид N2O и монооксид NO (бесцветные газы), сесквиоксид N2O3 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2O4), оксид N2O5 (бесцветные кристаллы). N2O и NO несолеобразующие оксиды, N2O3… … Энциклопедический словарь
Азота оксиды — N0, Оксиды азота NO, N02 в сумме в пересчете на NOj, относящиеся к классу опасности III Источник: ГОСТ Р 51206 98: Автотранспортные средства. Содержание вредных веществ в воздух … Словарь-справочник терминов нормативно-технической документации
азота оксиды{:} — гемиоксид N2О и монооксид NO (бесцветные газы), сесквиоксид N2О3 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2О4), оксид N2О5 (бесцветные кристаллы). N2О и NO несолеобразующие оксиды, N2O3 с водой даёт… … Энциклопедический словарь
АЗОТА ОКСИДЫ — гемиоксид N2O и монооксид NO (бесцв. газы), сесквиоксид N203 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2О4), оксид N2О5 (бесцв. кристаллы). N2О и NO несолеобразующие оксиды, N2О3 с водой даёт азотистую … Естествознание. Энциклопедический словарь
АЗОТА ОКСИДЫ — Гемиоксид N2O (оксид диазота, веселящий газ ) имеет слабый приятный запах и сладковатый вкус (см. табл.). Молекула линейна (длины связей в нм): Для N2O 0,51 10 30 Кл м. Р римость в воде (г на 100 г): 0,257 (0 … Химическая энциклопедия
Азота оксиды — … Википедия
АЗОТА — ОКСИДЫ: N2O (газ, tкип 88,5шС), NO (газ, tкип 151,6шС), NO2 (красно бурый), N2O4 (газ, tкип 20,6шС, tпл 11,2шС), N2O3 (газ, tкип 40шС), N2O5 (кристаллы, tпл 41шС, возгоняется при 33шС). NO2 промежуточный продукт при получении азотной кислоты, NO2 … Современная энциклопедия
оксиды азота — оксиды азота: Смесь различных оксидов азота, образовавшихся в процессе горения топлива в цилиндре дизеля, обозначаемая символом NOx. Источник … Словарь-справочник терминов нормативно-технической документации
оксиды азота — — [http://www.eionet.europa.eu/gemet/alphabetic?langcode=en] EN nitrogen oxides Oxides formed and released in all common types of combustion; they are formed by the oxidation of atmospheric nitrogen at high temperatures. Introduced into the … Справочник технического переводчика
dic.academic.ru
