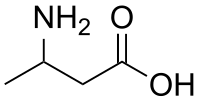
бета — аминомасляная кислота — beta-Aminobutyric acid
 | |
| имена | |
|---|---|
| название IUPAC 3-аминобутановые кислоты | |
| Другие имена 3-аминомасляная кислота | |
| Идентификаторы | |
| 3D модель ( JSmol ) | |
| ChemSpider | |
| ИКГВ InfoCard | 100.007.986 |
| |
| свойства | |
| С 4 Н 9 Н О 2 | |
| Молярная масса | 7002103121000000000 ♠103.121 г · моль -1 |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| ссылки Infobox | |
β-аминомасляная кислота (BABA) представляет собой изомер из аминокислоты аминомасляной кислоты с химической формулой C 4 H 9 NO 2 . Он имеет два изомера, альфа-аминомасляной кислоты и гамма-аминомасляная кислота (ГАМК), а медиатор у животных , который также содержится в растениях, где он может играть определенную роль в передаче сигналов. Все три не-протеиногенные аминокислоты , не найдены в белках . БАБА известна своей способностью индуцировать устойчивость к болезням растений , а также повышенную устойчивость к абиотическим стрессам, при обработке растений.
Синтез
Методы синтезируют BABA известны из , по меньшей мере , 1857 ранних методов для получения БАБА включен из аммиака и кротоновой кислоты под давлением; от ацетоуксусного эфира фенилгидразона ; или из малоновой кислоты , ацетальдегида и аммиака. В 1957 годе Zilkha сообщил новый простой метод , основанный на добавление аминов к кротоновой кислоте , а затем каталитический гидрогенолизу продукта для получения BABA. Начиная с 2000 года, способы получения только
устойчивость к болезням растений
БАБА впервые был обнаружен , чтобы увеличить устойчивость растений к болезням в 1960 году, когда было замечено , что она уменьшилась фитофторозом из помидор . Дальнейшие испытания были сделаны в 1960 — е годы, но это не было до 1990 — х годов , что интерес к соединению возобновилась. С тех пор было показано, что эффективность во многих различных pathosystems в контролируемых условиях. И многолетние и однолетние растения , как было показано , чтобы ответить, а также как однодольные и двудольные растения в пасленовых , тыквенных , сложноцветных , Fabaceae , Brassicaceae , Graminae , мальвовых , розоцветных и Vitaceae семей . Возбудитель группы, которые показали реакцию включают вирусы , бактерии, нематоды , грибки и оомицетами . Кроме того , было показано, что эффективность в области на защиту картофеля и томата растений от фитофтороза, виноградной лозы от
Вместо того , чтобы иметь прямое влияние на возбудителей болезней растений , активизирует иммунную систему растений , что позволяет им более эффективно противостоять инфекции. Эффекты , которые она широко изучена с использованием модели завод
Способ действия
БАБА вызывает защитные реакции в растениях как физических , так и биохимическими методами. Точный механизм зависит от вида растений и патогенов (The pathosystem ). Неизвестно , как БАБА взаимодействует с тканями растений для повышения устойчивости к болезням. Это не непосредственно активировать защитные гены в изоляции, но в сочетании с инфекцией, БАБА обработанных растений более быстро и сильно реагируют на возбудитель.
В некоторых pathosystems, усиливаются мозолистое и лигнин осаждение видно вокруг точки инфекции, которые действуют в качестве физического барьера , препятствующего заболевания. Связанные с патогенезом белки (PR белки) , которые выполняют множество различных функций , которые помогают предотвратить болезни накапливаются в некоторых Baba обработки растений, независимо от того, являются ли они заражают патоген или нет. При обнаружении инфицированных , однако, уровень PR — белков имеет тенденцию к дальнейшему увеличению. PR — белки не являются единственным механизмом предотвращения инфекции , однако, так как почва обливает Бабы , которые не индуцируют выработку PR белка, до сих пор придают устойчивость. Это может быть из — за различия между семействами растений, как Solanaceae (картофель, томаты, перец) реагирует путем производства PR белков без какого — либо патогена настоящего, тогда как крестоцветные (арабидопсис, цветная капуста) требует , чтобы побудить патоген PR — белки. В других pathosystems, фитоалексины (антимикробные соединения) накапливают на более высокие уровни в BABA обработанных растений , когда они инфицированы патогенными, но не тогда , когда возбудитель нет. Лиственные спреи Баб могут вызвать небольшие некротические пятна образуются на листах 1 или 2 дня после нанесения. Это было предложено быть связано с БАБА индукции гиперчувствительной реакции , которые растения обычно используют , чтобы убить инфицированные клетки , чтобы ограничить распространение инфекции.
БАБА применяется как опрыскивание растений приводит к тому , гормон , салициловая кислота (SA) для накопления, который является ключевым гормоном в борьбе с системной приобретенной устойчивости (SAR). Генетически модифицированные растения табака, которые не в состоянии аккумулировать SA по — прежнему защищены БАБА против некоторых патогенных микроорганизмов, но не другие, что указывает на механизмы pathosystem специфические , с помощью которого БАБА придает устойчивость. Arabidopsis , не в состоянии производить SA, жасмоновую кислоту или этилен (другие гормоны , участвующие в защите) все еще защищен от оомицетов
Рекомендации
« НазадАминофенилмасляная кислота14.08.2019 14:16
Содержание:
Что это такое?Что такое аминофенилмасляная кислота? Это вещество, содержащееся в медикаментах, улучшающее функциональные показатели умственной деятельности и, параллельно, дающее успокоительный и стимулирующий результат. Международное название звучит так: aminophenylbutyric acid (аминофенилбутират). По своим химическим свойствам числится производным гамма-аминомасляной кислоты и фенилэтиламина. Или гамма-амино-бета-фенилмасляной кислоты гидрохлорид. Структурная формула: C10h24ClNO2. Это массово применяемый эффективный медикамент, не вызывающий тяжелых негативных последствий. Это психостимулятор, который, кроме искоренения угнетенности, дополнительно усиливает умственную деятельность. Это средство обеспечивающее стрессоустойчивость. Седативный эффект мягок или отсутствует. Малотоксичен, без канцерогенного влияния. Действие
Аминофенилмасляная кислота производит двойной эффект:
Фармакотерапия посредством аминофенилмасляной кислоты дает положительный результат, а именно:
Это действие на организм аминофенилмасляной кислоты основано на том, что улучшается кровообращение, клетки насыщаются кислородом, оптимизируется передача импульсов, что нормализует обменные микропроцессы в тканях. Зачем применяют аминофенилмасляную кислоту? Ее предписывают для решения таких терапевтических задач как:
Форма выпуска
Оригинальный препарат аминофенилмасляной кислоты реализуется в следующих формах выпуска:
Наиболее распространенная дозировка капсул и таблеток – 250 мг и 500 мг. Где содержится?
Как уже говорилось выше, аминофенилмасляная кислота — это производное ГАМК. Где содержится эта аминокислота? Она нередко встречается в природе. Наибольшая насыщенность в чае Габа (габарон). Кроме этого, ГАМК содержится в продуктах питания:
Аналоги
Аминофенилмасляная кислота входит в состав лекарственных средств как основное действующее активное вещество. При этом вспомогательные вещества в них может немного различаться. Список препаратов, которые считаются аналогами:
Синонимы (дженерики) — это капсулы с тем же составом, либо под тем же торговым наименованием, но произведенные и выпущенные различными фармацевтическими заводами. А заменителями выступают медикаменты, имеющие похожее действие. Например, кортексин, тенотен, глицин, грандаксин и другие. Инструкция по применениюНазначения зависят от нескольких факторов, например, в зависимости от проведения лечения или профилактики, от индивидуальной переносимости, сопутствующих сбоях в здоровье, веса, тяжести ситуации. Схему и длительность приема должен определять лечащий специалист, основываясь на особенностях и ситуации. Обычно, лекарства с аминофенилмасляной кислотой применяются в течение 2-3 недель. В отдельных случаях, курс может быть продлен. Прописывается принятие аминонофенилмасляной кислоты 3 раза в сутки. Дозировка, указанная в инструкции по применению: единоразовая мера — 250-500мг, у детей до 14 лет — 250мг, малышей до 8 лет — 50-100мг. По инструкции аминофенилмасляную кислоту следует применять при:
Побочные эффекты
Побочные эффекты от аминофенилмасляной кислоты, которая содержится в препаратах, отмечаются изредка, при личной непереносимости. Это:
Противопоказание — гиперчувствительность. Под наблюдением специалиста с осторожностью принимать при заболеваниях ЖКТ и печени, при беременности и грудном вскармливании. Несоблюдение предписаний врачей, нарушения в графике приема аминофенилмасляной кислоты могут принести вред. При превышении дозировки возникают сильное желание спать, позывы к рвоте, возможны уменьшение показателей артериального давления и проблемы в функционировании почек и печени. Отзывы
Аминофенилмасляная кислота зарекомендовала себя, является эффективным лекарством. Вот некоторые из отзывов специалистов и пользователей. Отзывы врачей:
Отзывы пациентов:
Отзывы спортсменов и тренеров о приеме аминофенилмасляной кислоты:
ВыводыСпектр использования аминофенилмасляной кислоты широк, она отлично справляется с невротическими проблемами, улучшает работу мозга и организма в целом. Огромный плюс в почти полном отсутствии побочного действия. Не вызывает снижения внимания, сонливости, как многие другие транквилизаторы. Может применяться в лечении детей. Рекомендовано для спортсменов в качестве спортивного питания. За годы использования наработана обширная практика улучшения состояний пациентов, положительных итогов терапии. Где купить без рецепта?Купить аминофенилмасляную кислоту (фенибут) без рецепта можно на нашем сайте. Данный препарат относится к спортивному питанию и не требует назначения врача. |
Феномен аминофенилмасляной кислоты | Дробижев М.Ю., Федотова А.В., Кикта С.В., Антохин E.Ю.
В статье обсуждаются возможности применения аминофенилмасляной кислоты
Пожалуй, наиболее интересным из всех существующих в настоящее время в нашей стране препаратов является аминофенилмасляная кислота (АФК), известная под такими торговыми названиями, как Анвифен [1], Фенибут [2], Ноофен [3]. АФК рассматривается в качестве ноотропного, транквилизирующего, психостимулирующего, антиагрегантного и антиоксидантного средства [4, 5]. Некоторые отечественные специалисты считают, что АФК улучшает функциональное состояние мозга за счет нормализации метаболизма тканей [4].Соответственно, взрослым пациентам препарат рекомендуется для лечения ТФР (невротических) [6], астенических состояний [7] в т. ч. у больных шизофренией [8]. Но особенно широкий круг показаний у АФК в детском возрасте. Препарат рекомендуют при ТФР [9], астенических состояниях [10], негрубых тикозных расстройствах и заикании [11, 12], сенсоневральной тугоухости [4], СДВГ [13].
Наконец, обсуждаются возможности использования АФК в наркологии. Так, в некоторых зарубежных публикациях сообщается о целесообразности назначения препарата больным алкоголизмом [14]. Указывают, что АФК способствует купированию синдрома отмены, а также редукции патологического влечения к алкоголю.
Возможно представить себе препарат, который одновременно является и транквилизатором, и психостимулятором?
Более полувека назад в ЦНС был обнаружен естественный нейромедиатор торможения – γ-аминомасляная кислота (ГАМК). Ее изучение в экспериментальных условиях (например, при введении непосредственно в мозг подопытных животных) помогло выяснить, как происходят процессы естественного (физиологического) торможения (табл. 1).
![Таблица 1. Сравнительная характеристика механизмов действия ГАМК, бензодиазепинов и АФК [15–18] Таблица 1. Сравнительная характеристика механизмов действия ГАМК, бензодиазепинов и АФК [15–18]](/800/600/https/www.rmj.ru/upload/medialibrary/9a3/1657-1.png)
Оказалось, что ГАМК действует на несколько типов ГАМК-рецепторов, важнейшими из которых являются ГАМКА и ГАМКБ (табл. 1). Основная функция первых состоит в передаче сигнала от одного ГАМК-нейрона к другому (рис. 1, 2). Причем ГАМКА-рецепторы представляют собой канал, через который после воздействия естественного нейромедиатора – ГАМК быстро проникают отрицательно заряженные ионы хлора (ионотропный рецептор). При этом меняется «заряд» ГАМК-нейронов, и они теряют способность воспринимать стимулирующие электрические сигналы. Вот почему ГАМК в эксперименте на животных демонстрирует противосудорожный эффект [15].
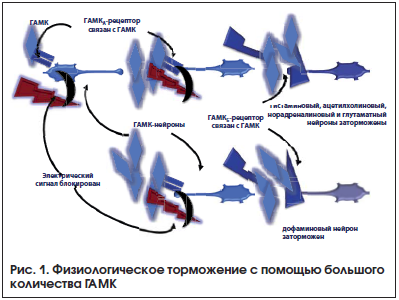

В то же время ГАМК-нейроны, в которые проникли ионы хлора, активизируются сами и начинает выделять значительное количество «новой» ГАМК (рис. 1). Этот нейромедиатор действует на ГАМКА-рецепторы других ГАМК-нейронов. При этом торможение распространяется дальше. Переходит оно и на другие нейроны: гистаминовые (ГИ), ацетилхолиновые (АЦХ), норадреналиновые (НА), глутаматные (ГЛУ), домафиновые (ДА) [17, 18].
Для этого ГАМК влияет уже на ГАМКБ-рецепторы, расположенные на этих нервных клетках (рис. 1). В отличие от ГАМКА-рецепторов они представляют собой молекулу белка, часть которой находится вне нейрона, а часть – внутри него. После того как ГАМК воздействует на «внешнюю» часть белка, запускается цепочка последовательных химических реакций, которая позволяет сигналу пройти сквозь мембрану. В дальнейшем в реакции вступают уже ферменты, расположенные внутри нейрона, и его метаболизм меняется (метаботропный рецептор). При этом нервные клетки перестают выделять свои нейромедиаторы (гистамин, ацетилхолин, норадреналин, глутамат), т. е. тормозят свою основную активность (табл. 1).
Однако влияние ГАМК на дофаминовые нейроны не столь однозначно (табл. 1). Начать с того, что ГАМК-нейроны также обладают ГАМКБ-рецепторами (рис. 1, 2). Последние необходимы для саморегуляции физиологического торможения [17, 18]. Если ГАМК влияет на указанные ГАМКБ-рецепторы, то ГАМК-нейроны тормозятся. С одной стороны, этот механизм препятствует гиперседации, но с другой – способствует тому, что ГАМК может не только снизить, но и повысить активность дофаминовых нейронов [19]. Предполагается, что это происходит из-за значительной разницы в чувствительности ГАМКБ-рецепторов.
Те из них, которые располагаются на ГАМК-нейронах, очень чувствительны к ГАМК. Эти ГАМКБ-рецепторы реагируют даже на небольшое количество «своего» нейромедиатора (рис. 2). Напротив, те рецепторы, которые располагаются на дофаминовых нейронах, менее чувствительны к ГАМК. Они реагируют только на значительное количество «чужого» нейромедиатора. Вот почему если ГАМК мало, то первоначально снижается активность ГАМК-нейронов, которые тормозят дофаминовые клетки (рис. 2). И те, напротив, повышают свою активность. И лишь когда количество ГАМК возрастает, этот нейромедиатор «добирается», наконец, до ГАМКБ-рецепторов на дофаминовых нейронах, и они перестают выделять дофамин.
Наконец, помимо процессов физиологического торможения ГАМК участвует в регуляции эндокринной системы [20]. Предполагается, что ГАМК воздействует на «свои» нейроны, расположенные в гипоталамусе и гипофизе. При этом нейромедиатор оказывает разнонаправленные влияния на секрецию гормона роста (соматотропного гормона (СТГ)), обладающего анаболическим действием, проявляющимся в усилении синтеза белка, угнетении его распада, а также в снижении отложений подкожного жира, ускорении его сгорания. В частности, действуя на ГАМК-нейроны в области гипоталамуса, ГАМК способствует выделению СТГ, а в области гипофиза – снижению его секреции.
Представленные свойства ГАМК (естественный характер торможения, его саморегуляция, противосудорожный эффект, отсутствие гиперседации) не могли не показаться обнадеживающими. Сразу же возникла идея использовать это вещество для лечения патологических процессов, сопровождающихся чрезмерным возбуждением нейронов, например, эпилепсии [21]. Вскоре ГАМК синтезировали в лабораторных условиях, и этот препарат под различными торговыми наименованиями поступил в лечебные учреждения [22, 23]. ГАМК стали назначать больным эпилепсией. И первый опыт такого лечения показался вполне успешным [21]. В дальнейшем все же выяснилось, что имел место положительный плацебо-эффект. ГАМК, будучи нелипофильным веществом, практически не проникает через ГЭБ [24], а следовательно, на больных действовал не столько сам препарат, сколько вера врачей в его впечатляющие фармакологические свойства [21].
Как только об этом стало известно, ученые всего мира обратились к поиску новых ГАМКергических препаратов, способных вызвать торможение нейронов. И в результате достаточно быстро были синтезированы первые бензодиазепины, способные легко преодолевать ГЭБ (табл. 1) [25]. Эти препараты по своей химической природе никак не походили на ГАМК и впоследствии даже получили специальное название «позитивные аллостерические модуляторы ГАМКА-рецептора» [16, 25]. Столь сложный, на первый взгляд, термин означает всего лишь, что: 1) бензодиазепины прикрепляются к ГАМКА-рецепторам на противоположной стороне от того места, где с ним взаимодействует ГАМК (аллостерический – от греч. άλλος – другой и στερεός – пространственный), 2) при этом они резко повышают способность ГАМК влиять на активность рецептора (позитивный модулятор). Представляется, однако, что эти препараты еще лучше обозначить как катализатор физиологического торможения, вызванного ГАМК. Дело в том, что бензодиазепины сами по себе не активны и в отсутствие ГАМК вообще не способны вызвать какой-то эффект [16]. Зато их добавление к ГАМК приводит к резкому усилению торможения, которое в отличие от обычного – физиологического – можно обозначить как «генерализованное».
И, действительно, бензодиазепины резко повышают способность ГАМК-нейронов сопротивляться стимулирующим электрическим сигналам (рис. 3). В результате все эти ГАМКергические препараты в той или иной мере наделены противосудорожным эффектом (табл. 1). Кроме того, бензодиазепины заставляют ГАМК-нейроны выбрасывать большое количество ГАМК, достаточное для того, чтобы быстро затормозить разные нейроны (включая и дофаминовые) и вызвать гиперседацию [26]. Наконец, было установлено, что бензодиазепины могут подавлять активность эндокринной системы и, в частности, способствовать снижению секреции СТГ [27].
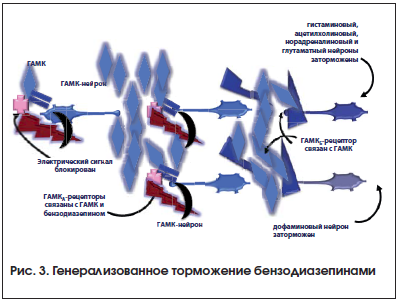
Высокая эффективность механизма действия бензодиазепинов наряду с упомянутой выше способностью проникать через ГЭБ предопределили их широкое использование в клинической практике [25]. Однако всегда существовали контингенты больных (амбулаторные пациенты, лица, управляющие автотранспортом, учащиеся, пожилые и т. д.), у которых эти ГАМКергические препараты не могли использоваться из-за серьезных проблем, связанных с выраженным характером торможения. Вот почему продолжался поиск новых лекарственных средств, обладающих иным механизмом действия.
При этом возникла вполне понятная идея – вернуться к ГАМК. Ведь если ее все же «протащить» сквозь ГЭБ, то можно будет использовать преимущества «физиологического» торможения нейронов. Тогда по инициативе профессора И.П. Лапина из института им. В.М. Бехтерева на кафедре органической химии педагогического института им. А.И. Герцена синтезировали новый ГАМКергический препарат – АФК [15]. Он был получен за счет присоединения к ГАМК фенильного кольца, добавляющего молекуле липофильных свойств. В результате АФК легко проникает через ГЭБ (табл. 1). Однако из-за изменения структуры молекулы у АФК появился собственный механизм торможения, который не похож ни на физиологический, ни на генерализованный (табл. 1, рис. 4). И этот новый вариант, пожалуй, можно обозначить как «избирательный». Действительно, в отличие от бензодиазепинов, АФК не усиливает эффекты ГАМК, а сама исполняет ее роль. Причем у АФК есть только один из двух механизмов ГАМК. Так, АФК способна оказывать влияние на ГАМКБ-рецепторы (агонист ГАМКБ-рецепторов, от греч. ἀγωνιστής – боец-противник), расположенных на различных нейронах. К тому же это влияние выражено слабее, чем у самой ГАМК [15]. В итоге избирательное торможение носит умеренный характер, уступая по силе физиологическому и уж тем более генерализованному. Вот почему АФК не обладает противосудорожным эффектом, не вызывает гиперседацию. Отсутствуют также и какие-либо научные данные, свидетельствующие о влиянии АФК на эндокринную систему и, в частности, выделение СТГ.
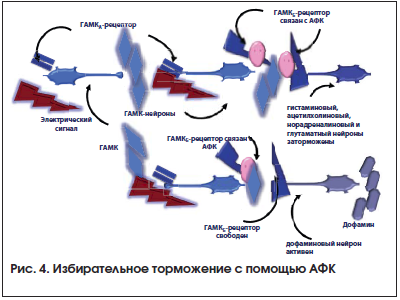
Зато избирательный вариант торможения сопряжен не только со снижением активности нейронов, но и с более ощутимым (в сравнении с ГАМК) оживлением дофаминовых нервных клеток (табл. 1). Здесь сказываются уже упоминавшиеся выше различия в чувствительности ГАМКБ-рецепторов, а также более слабое (в сравнении с ГАМК) влияние на них АФК. В результате этот препарат способен тормозить дофаминовые нейроны лишь в очень значительных дозах, которые выходят за рамки терапевтических.
Таким образом, у АФК есть два основных компонента механизма действия, которые имеют значение для клинического использования препарата: тормозящий (↓ГЛУ, ↓НА, ↓АЦХ, ↓ГИ)1 и активирующий (↑ДА) (табл. 1). Первый из них (тормозящий – ↓ГЛУ, ↓НА, ↓АЦХ, ↓ГИ) может быть востребован при многочисленных патологических состояниях, чей патогенез связан с ростом активности глутаматных, норадреналиновых, ацетилхолиновых и гистаминовых нейронов (табл. 2).
Эти расстройства никогда не изучались представителями одной медицинской специальности. Напротив, в их исследовании участвовали психиатры, неврологи, кардиологи, пульмонологи и т. д. Вот почему для обозначения рассматриваемых расстройств приходится использовать большое число медицинских терминов из разных классов МКБ 10-го пересмотра [28].
В клинической практике для лечения этих расстройств часто применяются бензодиазепины. И эта тактика представляется вполне оправданной с учетом механизма действия указанных препаратов (табл. 1). Однако выше уже упоминалось о том, что существуют многочисленные контингенты больных, у которых генерализованное торможение, часто связанное с гиперседацией, будет создавать определенные проблемы при проведении фармакотерапии. В этой ситуации представляется предпочтительным использовать умеренный тормозящий компонент механизма действия АФК.
Лучшей переносимости терапии будет способствовать и то, что АФК (в отличие от бензодиазепинов) обладает активирующим компонентом механизма действия (↑ДА). Между тем дофаминовая активность необходима для реализации функций интеллектуальной и моторной сферы как взрослых, так и детей [16]. Именно дофаминовые нейроны отвечают за развитие мотивации, системы подкрепления, а следовательно, целенаправленного поведения в процессе обучения любым новым навыкам. Кроме того, дофаминовые нейроны чрезвычайно важны для переключения с одной задачи на другую. Наконец, они же отвечают за эмоции, организацию точных движений и их плавность, а также регулируют эндокринную систему.
Вот почему показаниями для назначения АФК могут быть различные расстройства, связанные с повышением активности глутаматных, норадреналиновых, ацетилхолиновых и гистаминовых нейронов (табл. 2) у «проблемных» контингентов пациентов. К этим контингентам можно отнести больных: 1) детского или пожилого возраста; 2) получающих лечение амбулаторно, 3) занятых учебой или работой, сопряженной с интеллектуальной и/или моторной активностью.
![Таблица 2. Патогенез и клиника расстройств, являющихся терапевтической мишенью для тормозящего компонента механизма действия АФК [38, 39] Таблица 2. Патогенез и клиника расстройств, являющихся терапевтической мишенью для тормозящего компонента механизма действия АФК [38, 39]](/800/600/https/www.rmj.ru/upload/medialibrary/1b5/1657-6.png)
Очевидно, что все представленные показания отнюдь не являются новыми и лишь уточняют имеющиеся в справочниках [1]. К тому же они широко обсуждаются в литературе. Но существуют и другие патологические состояния, при которых целесообразно прибегнуть к назначению препарата. К сожалению, эти расстройства практически не отражены в показаниях, их гораздо реже упоминают в публикациях. Возможно, это объясняется сложным патогенезом таких патологических состояний, возникающих из-за понижения активности одних нейронов (дофаминовых) и повышения – других (норадреналиновых и/или ацетилхолиновых) (табл. 3).
![Таблица 3. Патогенез и клиника расстройств, являющихся терапевтической мишенью для активирую- щего и тормозящего компонентов механизма действия АФК [16, 40] Таблица 3. Патогенез и клиника расстройств, являющихся терапевтической мишенью для активирую- щего и тормозящего компонентов механизма действия АФК [16, 40]](/800/600/https/www.rmj.ru/upload/medialibrary/a2a/1657-7.png)
К тому же для лечения указанных расстройств зачастую необходим как активирующий (↑ДА), так и тормозящий (↓ГЛУ, ↓НА, ↓АЦХ, ↓ГИ) компоненты механизма действия АФК. В качестве примера приведем СДВГ, патогенез которого связан со снижением активности дофаминовых нейронов и повышением – норадреналиновых.
Традиционные подходы к терапии этого синдрома, к сожалению, далеки от рациональных. В частности, в нашей стране при лечении СДВГ надеются на «активизацию» неких «резервов» ЦНС [29] за счет пирацетама, винпоцетина и даже полипептидов, извлеченных из «коры головного мозга крупного рогатого скота, а также свиней» [30]. Между тем не совсем ясно, как эти очень разнородные препараты влияют на обмен дофамина и норадреналина. Напротив, активирующий компонент механизма действия АФК прямо предусматривает повышение активности дофаминовых нейронов, а тормозящий – снижение норадреналиновых (табл. 1).
Достаточно сложный патогенез и у осложнений фармакотерапии шизофрении (табл. 3), которые в нашей стране усугубляются многолетним назначением высокопотентных нейролептиков (например, галоперидола) [31]. Между тем эти препараты осуществляют торможение различных дофаминовых нейронов, что в некоторых случаях сопровождается реципрокным повышением активности других нервных клеток: ацетилхолиновых и норадреналиновых (табл. 3). В результате у больных отмечаются разнообразные нарушения, связанные с эмоциями, моторикой и эндокринной системой. Для борьбы с этими осложнениями обычно рекомендуют отменять препараты, заменять одно лекарственное средство на другое, более переносимое, а также назначать на непродолжительное время корректоры (холинолитики) [32]. К сожалению, в нашей стране такой модификации нейролептической терапии предпочитают постоянное (как правило, многолетнее) использование мощного холинолитика – тригексифенидила. Между тем это ведет к развитию еще более тяжелых и некурабельных побочных эффектов, таких как поздняя дискинезия [33].
Возможность хотя бы частично улучшить описанную ситуацию связана с достаточно распространенной практикой назначения транквилизаторов при шизофрении [32] – как правило, это бензодиазепины, использующиеся для лечения психопато- и неврозоподобных симптомов. Представляется, однако, что назначение АФК в рассматриваемых случаях будет способствовать не только реализации указанных «тактических» задач терапии, но и профилактике поздней дискинезии. Ведь, в отличие от бензодиазепинов, механизм действия АФК (табл. 1) позволяет повысить активность дофаминовых нейронов (активирующий компонент) и понизить ее у ацетилхолиновых и норадреналиновых (тормозящий компонент). В результате АФК будет способствовать купированию побочных эффектов нейролептиков. При этом появится возможность снизить дозы тригексифенидила, а следовательно, и риск развития поздней дискинезии (табл. 3).
Таким образом, показаниями для назначения АФК могут быть и некоторые расстройства, связанные со снижением активности дофаминовых нейронов и повышением – норадреналиновых и ацетилхолиновых (табл. 3). Причем при СДВГ этот препарат может использоваться для проведения монотерапии. Что же касается разнообразных побочных эффектов нейролептиков, то здесь АФК целесообразно применять в качестве дополнительного медикаментозного средства.
Интересно, однако, что свойственное АФК избирательное торможение в значительной мере препятствует ее использованию не по медицинским показаниям. Действительно, исходя из представленного выше механизма действия, препарат способен активировать дофаминовые нейроны, но только в терапевтических дозах [15]. Именно при соблюдении этих условий АФК будет действовать на ГАМКБ-рецепторы ГАМК-нейронов, которые тормозят дофаминовые нервные клетки. Но если доза препарата возрастет, он «доберется» и до ГАМКБ-рецепторов, расположенных на дофаминовых нейронах. В результате они затормозятся и перестанут выделять дофамин.
Между тем одним из наиболее важных механизмов формирования зависимости является возможность повышения дозы вещества, для того, чтобы преодолеть толерантность к нему или привыкание к его эффектам. Очевидно, что попытка увеличить дозировку АФК неминуемо приведет не к увеличению активности дофаминовых нейронов, а к их торможению. Вот почему, по данным зарубежных исследователей, лица, использующие этот препарат не по медицинским показаниям, фактически не могут выйти за пределы терапевтического диапазона [34]. В свою очередь это приводит к тому, что АФК, даже в условиях полного отсутствия какого-либо врачебного контроля, остается безопасным препаратом. Случаи развития серьезных осложнений (гиперседация, синдром отмены) при использовании АФК не по медицинским показаниям достаточно редки, а смертельные исходы не встречаются вовсе [34–40].
Представленные данные о механизме действия АФК позволяют высказать и некоторые соображения относительно преимуществ и недостатков различных препаратов, содержащих рассматриваемое действующее вещество. Так, преимущества избирательного торможения позволяют использовать АФК у больных самого разного возраста (включая детей с 3-х лет), а также при большом числе патологических состояний. Вот почему представляется весьма удобным пользоваться таблетками, которые содержат разное количество АФК. В этом случае создаются оптимальные возможности для индивидуального подбора доз. Именно таким требованиям соответствует препарат Анвифен [1]. Он выпускается в дозах 50 и 250 мг. В то же время остальные препараты, содержащие АФК в качестве действующего вещества, доступны только в самой высокой из перечисленных дозировок (250 мг).
Завершая настоящий обзор литературы, целесообразно подчеркнуть, что в условиях сосуществования множества мнений относительно клинического использования препарата всегда можно прибегнуть к анализу его механизмов действия. Сопоставление фармакологических свойств лекарственного средства с современными данными о патогенезе расстройств вполне позволяет с большой долей уверенности судить об обоснованности тех или иных показаний для назначения медикаментозного средства.
гамма — аминомасляная кислота — gamma-Aminobutyric acid
«GABA» перенаправляется сюда. Для использования в других целях, см ГАМК (значения) .  | |
| имена | |
|---|---|
| Предпочтительное название IUPAC 4-аминобутановые кислоты | |
| Идентификаторы | |
| 3D модель ( JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ИКГВ InfoCard | 100.000.235 |
| Номер EC | 200-258-6 |
| KEGG | |
| MeSH | гамма-аминомасляная кислота + |
| номер RTECS | ES6300000 |
| UNII | |
| |
| свойства | |
| С 4 Н 9 NO 2 | |
| Молярная масса | 103,120 г / моль |
| Внешность | белый микрокристаллический порошок |
| плотность | 1,11 г / мл |
| Температура плавления | 203,7 ° С (398,7 ° F, 476,8 К) |
| Точка кипения | 247,9 ° С (478,2 ° F, 521,0 К) |
| 130 г / 100 мл | |
| войти P | -3,17 |
| Кислотность (р К ) |
|
| опасности | |
| Основные опасности | Раздражает, Вредный |
| Смертельная доза или концентрация ( LD , LC ): | |
| 12680 мг / кг (мыши, перорально) | |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
 N проверить ( что ?) N проверить ( что ?)  Y Y N N | |
| ссылки Infobox | |
гамма- аминомасляная кислота , или γ-аминомасляная кислота ɡ æ м ə
функция
медиатор
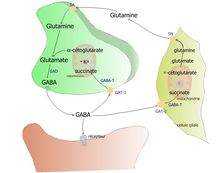 ГАМК обмен веществ, вовлечение глиальных клеток
ГАМК обмен веществ, вовлечение глиальных клетокВ позвоночных , ГАМК действует на ингибирующих синапсов в мозге путем связывания со специфическими трансмембранных рецепторов в плазматической мембране обоих пре- и постсинаптические нейрональных процессов. Это связывание вызывает открытие ионных каналов , чтобы обеспечить поток либо отрицательно заряженных хлоридных ионов в клетке или положительно заряженных калиевых ионов из клетки. Это действие приводит к отрицательному изменению трансмембранного потенциала , как правило , вызывает гиперполяризацию . Два общих класса рецепторов ГАМК известны:
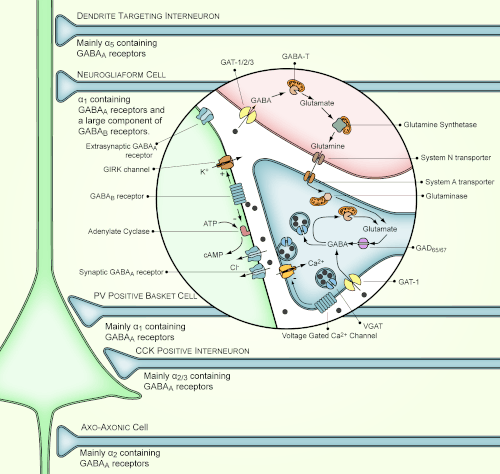 Производство, выпуск, действие и деградация ГАКА на стереотипный ГАМКергический синапсе
Производство, выпуск, действие и деградация ГАКА на стереотипный ГАМКергический синапсеНейроны , которые производят ГАМК в качестве своей продукции, называются ГАМКергических нейронов, и имеют в основном тормозящее действие на рецепторы взрослого позвоночного. Средние колючие клетки являются типичным примером ингибирующих центральной нервной системы ГАМК клеток. В противоположность этому , ГАМК проявляет как возбуждающие и ингибирующие действия в насекомых , опосредующие мышечной активации в синапсах между нервов и мышечных клеток, а также стимуляция некоторых желез . У млекопитающих, некоторые ГАМКергические нейроны, такие как люстры клетка , также способны возбуждать их глутаматергические аналоги.
ГАМК А рецепторы представляют собой лиганд-активированный хлорид каналов: при активации ГАМК, они позволяют поток хлоридных ионов через мембрану клетки. Является ли этот поток хлорид деполяризации (делает напряжение на мембране клетки менее отрицательный), маневровый (не оказывает никакого влияния на мембранного потенциала клетки), или ингибирующий / гиперпол (делает мембрану ячейки более отрицательное) зависит от направления потока хлористый. Когда сетка хлорида течет из клетки, ГАМК деполяризации; когда хлорид поступает в клетку, ГАМК ингибирующее или гиперпол. Когда чистый поток хлорида близка к нулю, то действие ГАМК шунтирования. Шунтирование ингибирование не имеет непосредственного влияния на мембранный потенциал клетки; Однако, это уменьшает эффект любого совпадающей синаптической вход за счет уменьшения электрического сопротивления мембраны клетки. Шунтирование ингибирование может «отменить» раздражительный эффект деполяризации ГАМК, что приводит к общему торможению , даже если мембранный потенциал становится менее отрицательным. Считалось , что переключатель развития молекулярной машины , контролирующей концентрацию хлорида внутри клетки изменяет функциональную роль ГАМК между неонатальных и взрослых стадий. Так как мозг развивается в зрелом возрасте, роль изменения ГАМК от возбуждающих к ингибирующих.
развитие мозга
В то время как ГАМК является тормозным передатчик в зрелом мозге, как думали его действия , в первую очередь возбуждающим в развивающемся мозге. Градиент хлорида , как сообщалось, обращенными в незрелых нейронах, с его разворотом потенциальным выше , чем покой мембранного потенциала клетки; активация ГАКА-А рецептора , таким образом , приводит к оттоку Cl — ионы из клетки (то есть, деполяризующий ток). Дифференциальный градиент хлорида в незрелых нейронов было показано, что в первую очередь за счет более высокой концентрации NKCC1 со-транспортеров по отношению к KCC2 со-переносчики в незрелых клеток. ГАМКергические интернейроны созревают быстрее в гиппокампе и сигнализация машины ГАКА появляется раньше , чем глутаматергическая передача. Таким образом, ГАМК считается главным возбуждающим нейромедиатором во многих областях мозга до созревания в глутаматэргических синапсов.
В стадиях развития , предшествующих образованию синаптических контактов, ГАМК синтезируется нейронами и действует как в качестве АУТОКРИННОЙ (действующего на одной и той же клетке) и паракринной (действующего на соседних клетках) медиатор сигнализации. В ганглионарном бугорке также в значительной степени способствовать укреплению населения кортикальных клеток ГАМКергических.
ГАМК регулирует пролиферацию нервных клеток — предшественников миграцию и дифференцировку Удлинение невритов и образование синапсов.
ГАМК также регулирует рост эмбриональных и стволовых нервных клеток . ГАМК может в фло uence развития нейронных клеток — предшественников с помощью нейротрофического фактора головного мозга , полученного выражения (BDNF). ГАМК активирует GABA A — рецептор , вызывая остановку клеточного цикла в S-фазе, что ограничивает рост.
Вне нервной системы
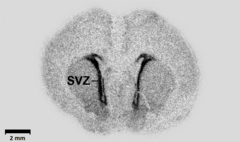 экспрессия мРНК зародышевой варианта ГАМК-продуцирующих фермента GAD67 в корональной секции мозга в один-дневных Wistar крыс , с самой высокой экспрессии в субвентрикулярной зоне (SVZ)
экспрессия мРНК зародышевой варианта ГАМК-продуцирующих фермента GAD67 в корональной секции мозга в один-дневных Wistar крыс , с самой высокой экспрессии в субвентрикулярной зоне (SVZ)Кроме нервной системы, ГАМК также производится на относительно высоком уровне в инсулин -продуцирующих бета-клеток на поджелудочной железе . Эти бета-клетки секретируют ГАМК наряду с инсулином и ГАМК связывается с ГАМК — рецепторами на соседних островковых альфа-клеток и ингибирует их от секретирующих глюкагон (который будет противодействовать эффекты инсулина в).
ГАМК может способствовать репликации и выживание бета-клеток , а также способствовать превращению альфа-клеток к бета-клетки, которые могут привести к новым методам лечения для диабета .
ГАМК был также обнаружен в других периферических тканях, включая кишечник, желудок, маточные трубы, матка, яичники, семенники, почки, мочевой пузырь, легкие и печень, хотя и на гораздо более низких уровнях, чем в нейронах или бета-клетках. механизмы ГАМКергические были продемонстрированы в различных периферических тканей и органов, которые включают в кишечник, желудок, поджелудочная железа, фаллопиевы трубы, матка, яичники, яички, почки, мочевого пузыря, легких и печени.
Иммунные клетки экспрессируют рецепторы для GABA и введение ГАМК может подавлять воспалительные иммунные реакции и содействовать «регуляторные» иммунные реакции, такие , что введение ГАМК было показано, ингибирует аутоиммунных заболеваний , в некоторых моделях животных.
В 2018 году, GABA показала регулировать секрецию большего числа цитокинов. В плазме СД1 пациентов, уровни 26 цитокинов увеличены и тех, 16 ингибируются ГАМК в клеточных анализах.
В 2007 годе возбуждающая система ГАКА была описана в дыхательных путях эпителия . Система активируется под воздействием аллергенов и может участвовать в механизмах астмы . Системы ГАМКергические также были найдены в яичках и в хрусталике глаза.
GABA происходит в растениях.
Структура и конформации
ГАМК находится в основном в виде цвиттера — ионе (т.е. с карбоксильной группой депротонированной и аминогруппами протонированными). Ее конформации зависит от его окружения. В газовой фазе, высоко сложенный конформации сильно выступает за счет электростатического притяжения между двумя функциональными группами. Стабилизации составляет около 50 ккал / моль, в соответствии с квантовой химии расчетов. В твердом состоянии, расширенный конформация найден, с транс — конформации в конце аминокислоты и гош конформации на карбоксильном конце. Это связанно с упаковочным взаимодействием с соседними молекулами. В растворе, пяти различные конформации, некоторые сложенные и некоторые расширенные, обнаружены в результате сольватации эффектов. Конформационная гибкость ГАКА имеет важное значение для его биологической функции, как это было установлено, связывается с различными рецепторами с различными конформациями. Многие аналоги ГАМК с фармацевтической промышленности имеют более жесткие структуры для того , чтобы контролировать связывание лучше.
история
В 1883 году, ГАКА были впервые синтезированы, и она была известна только как продукт метаболизма растений и микроорганизмов.
В 1950 году ГАМК был обнаружен в качестве составной части млекопитающих центральной нервной системы .
В 1959 г. было показано , что на тормозящий синапс на раки мышечных волокон ГАКА действуют как стимуляция ингибирующего нерва. И ингибирование стимуляции нерва и прикладной ГАМК блокируется пикротоксином .
Биосинтез
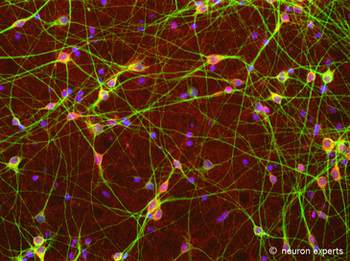 ГАМКергические нейроны, которые производят ГАМК
ГАМКергические нейроны, которые производят ГАМКГАМК синтезируется из глутамата с помощью фермента глутамат декарбоксилазы (GAD) с пиридоксальфосфата (активная форма витамина B6 ) в качестве кофактора . Этот процесс преобразует глутамат (основные возбуждающие нейротрансмиттер) в ГАКА (главный ингибирующий нейромедиатор).
Традиционно считалось , что экзогенный ГАМК не проникает через гематоэнцефалический барьер, однако , более современные исследования показывают , что это может быть возможным, или что экзогенный ГАМК (например , в виде пищевых добавок) может оказывать воздействие ГАМКергических на энтеральной нервной системы , которая в свою очередь , стимулируют выработку эндогенного GABA. Непосредственное участие ГАМК в глутамат-глютамина цикла делает вопрос о том, может ли ГАМК проникать через гематоэнцефалический барьер несколько вводит в заблуждение, потому что оба глутамата и глутамина может свободно пересечь барьер и преобразовать в GABA в мозге.
катаболизм
ГАМК — трансаминазы фермент катализирует превращение 4-аминобутановой кислоты (ГАМК) и 2-оксоглутарата (α-кето) в янтарной полуальдегида и глутамата. Янтарная полуальдегида затем окисляется в янтарную кислоту с помощью янтарной полуальдегиддегидрогеназы и как таковой входит в цикл лимонной кислоты в качестве полезного источника энергии.
Фармакология
Лекарственные средства , которые действуют как аллостерические модуляторы из ГАМК — рецепторов (известные как аналоги ГАМК или ГАМКергических препаратов), или увеличить доступное количество ГАМК, как правило , имеют расслабляющий, анти-беспокойство, и противосудорожным эффектами. Многие из перечисленных ниже веществ , как известно, вызывают антероградную амнезия и ретроградная амнезия .
В общем, ГАМК не пересекает гематоэнцефалический барьер , хотя некоторые участки мозга , которые не имеют никакого эффективного гематоэнцефалического барьера, такие как перивентрикулярного ядра , может быть достигнуто с помощью препаратов , таких как системно впрыскиваемого ГАМК. По крайней мере , одно исследование предполагает , что перорально ГАМК увеличивает количество гормона роста человека (HGH). ГАМК впрыскивается непосредственно в мозг, как сообщается, имеет как стимулирующее и ингибирующее действие на производстве гормона роста, в зависимости от физиологии человека. Некоторые пролекарства ГАМК (напр. Пикамилона ) были разработаны , чтобы проникать через гематоэнцефалический барьер, а затем разделить на ГАМК и молекулой — носителем , как только внутри мозга. Это позволяет для прямого повышения уровня ГАКА на протяжении всех областей мозга, таким образом , следующего характера распределения пролекарства уровня метаболизма.
ГАМК усиливается катаболизм серотонина в N -acetylserotonin (предшественник мелатонина ) у крыс. Таким образом , подозревают , что ГАМК участвует в синтезе мелатонина и , таким образом , может оказывать регуляторные эффекты на сон и репродуктивных функций.
Химия
Хотя в химических терминах, ГАМК является аминокислота (как это имеет как первичный амин и карбоксильную функциональную группу), оно редко упоминается как таковой в профессиональной, научной или медицинской общественности. По соглашению термин «аминокислота», когда используется без спецификатора , относится конкретно к альфа — аминокислоты . ГАМК не является альфа — аминокислота, а это означает аминогруппу не присоединен к альфа — углерод , так что не включена в белки .
- ГАМК А рецепторов лиганды.
- Агонисты / положительные аллостерические модуляторы : спирт ( этанол ), барбитураты , бензодиазепины , Carisoprodol , хлоралгидрат , etaqualone , Etomidate , glutethimide , кава , метаквалон , Мусцимол , нейроактивные стероиды , Z-препараты , пропофол , шлемник , валериана , Theanine , летучие и ингаляционные анестетика .
- Антагонисты / отрицательные модуляторы аллостерические : бикукуллин , цикутоксин , флумазенил , фуросемид , габазин , oenanthotoxin , пикротоксин , Ro15-4513 , туйон , Аментофлавон .
- GABA B лиганды рецепторов.
- Ингибиторы обратного захвата ГАМК : дерамциклан , Гиперфорин , тиагабина .
- ГАМК-трансаминазы ингибиторы: gabaculine , фенелзин , вальпроат , Vigabatrin , мелиссы ( Melissa лекарственный ).
- Аналоги ГАМК : прегабалин , габапентин , пикамилона , progabide
Пищевые добавки
ГАМК продается как пищевая добавка .
В растениях
GABA также встречается в растениях. Это наиболее распространенная аминокислота в апопласте томатов. Данные также указывают на роль в клеточной сигнализации в растениях.
Смотрите также
Рекомендации
Список используемой литературы
внешняя ссылка
Гамма-аминомасляная кислота — Википедия
| Гамма-аминомасляная кислота | |
|---|---|
| Систематическое наименование | 4-аминобутановая кислота |
| Хим. формула | C4H9O2N |
| Состояние | твёрдое |
| Молярная масса | 103,120 г/моль |
| Плотность | 1,11 г/см³ |
| Т. плав. | 203 °C |
| Т. кип. | 247,9 °C |
| pKa | 4,05 |
| Растворимость в воде | 130 г/100 мл |
| Рег. номер CAS | 56-12-2 |
| PubChem | 119 |
| Рег. номер EINECS | 200-258-6 |
| SMILES | |
| InChI | |
| RTECS | ES6300000 |
| ChEBI | 16865 |
| ChemSpider | 116 |
| ЛД50 | 12 680 мг/кг (мыши, перорально) |
| Токсичность | слаботоксичное вещество, ирритант |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
γ-Аминомасляная кислота (сокр. ГАМК, GABA) — органическое соединение, непротеиногенная аминокислота, важнейший тормозной нейромедиатор центральной нервной системы (ЦНС) человека и других млекопитающих. Аминомасляная кислота является биогенным веществом. Содержится в ЦНС и принимает участие в нейромедиаторных и метаболических процессах в мозге.
Получение
Гамма-аминомасляная кислота в организме образуется из другой аминокислоты — глутаминовой с помощью фермента глутаматдекарбоксилазы.
Биологическая активность
В нервной системе
γ-Аминомасляная кислота выполняет в организме функцию ингибирующего медиатора центральной нервной системы. При выбросе ГАМК в синаптическую щель происходит активация ионных каналов ГАМКA— и ГАМКC-рецепторов, приводящая к ингибированию нервного импульса. Лиганды рецепторов ГАМК рассматриваются как потенциальные средства для лечения различных расстройств психики и центральной нервной системы, к которым относятся болезни Паркинсона и Альцгеймера, расстройства сна (бессонница, нарколепсия), эпилепсия.
Установлено, что ГАМК является основным нейромедиатором, участвующим в процессах центрального торможения.
Вместе с этим ГАМК проявляет также и свойства нейромедиатора, участвующего в возбуждающих процессах в ЦНС на ранних этапах развития мозга у человека. ГАМК не связана исключительно с синаптическим торможением в ЦНС. На ранних этапах развития мозга ГАМК опосредует преимущественно синаптическое возбуждение[2]. В незрелых нейронах ГАМК проявляет возбуждающие и деполяризующие свойства в синергичном взаимодействии с глутаматом. Возбуждающее поведение ГАМК обусловлено высокой внутриклеточной концентрацией ионов хлора, накапливаемого при помощи транспортного белка NKCC, таким образом, открытие ГАМК-рецепторов приводит к потере этих анионов и возникновению ВПСП на мембране нейрона. Во взрослом мозге возбуждающая функция ГАМК сохраняется лишь частично, уступая место синаптическому торможению[3].
Под влиянием ГАМК активируются также энергетические процессы мозга, повышается дыхательная активность тканей, улучшается утилизация мозгом глюкозы, улучшается кровоснабжение.
Действие ГАМК в ЦНС осуществляется путём её взаимодействия со специфическими ГАМКергическими рецепторами, которые в последнее время подразделяют на ГАМКA— и ГАМКB-рецепторы и др. В механизме действия целого ряда центральных нейротропных веществ (снотворных, противосудорожных, судорожных и др.) существенную роль играет их агонистическое или антагонистическое взаимодействие с ГАМК-рецепторами. Бензодиазепины потенцируют действие ГАМК.
Наличие ГАМК в ЦНС было обнаружено в середине 1950-х годов, в 1963 году осуществлён её синтез (Krnjević K., Phillis J. W.[4][5]). В конце 1960-х годов под названием «Гаммалон» ГАМК была предложена для применения в качестве лекарственного средства за рубежом, затем — под названием «Аминалон» — в России.
По экспериментальным данным, ГАМК при введении в организм плохо проникает через гематоэнцефалический барьер, однако есть свидетельства того, что ГАМК транспортируется в мозг с помощью специфических мембранных транспортеров GAT2 и BGT-1[6].
За пределами нервной системы
В 2007 году была впервые описана ГАМКергическая система в эпителии дыхательных путей. Система активируется под воздействием аллергенов и может играть роль в механизмах астмы[7].
Другая ГАМКергическая система описана в яичках, она может влиять на работу клеток Лейдига[8].
Исследователи больницы St. Michael, Торонто, Канада, установили в июле 2011 года, что ГАМК играет роль в предотвращении и возможно обратном развитии сахарного диабета у мышей[9].
ГАМК обнаружена в бета-клетках поджелудочной железы в концентрациях, сопоставимых с таковыми в ЦНС. Секреция ГАМК в бета-клетках происходит совместно с секрецией инсулина. ГАМК опосредованно ингибирует секрецию глюкагона, связанную с повышением концентрации глюкозы в крови.[10]
Пищевая добавка
ГАМК в виде пищевых добавок применяется при умственной отсталости, после инсульта и травм мозга, для лечения энцефалопатии и ДЦП.[11] Нет достаточных доказательств эффективности таких препаратов.[12]
См. также
Примечания
- ↑ Popp A., Urbach A., Witte O.W., Frahm C. Adult and embryonic GAD transcripts are spatiotemporally regulated during postnatal development in the rat brain (англ.) // PLoS ONE (англ.)русск. : journal / Reh, Thomas A.. — 2009. — Vol. 4, no. 2. — P. e4371. — DOI:10.1371/journal.pone.0004371. — Bibcode: 2009PLoSO…4.4371P. — PMID 19190758.
- ↑ Yehezkel Ben-Ari. Excitatory actions of gaba during development: the nature of the nurture // Nature Reviews. Neuroscience. — 2002-9. — Т. 3, вып. 9. — С. 728—739. — ISSN 1471-003X. — DOI:10.1038/nrn920.
- ↑ Frontiers | Excitatory actions of GABA during development (неопр.). www.frontiersin.org. Дата обращения 13 декабря 2018.
- ↑ Krnjević K., Phillis J. W. Iontophoretic studies of neurones in the mammalian cerebral cortex // The Journal of Physiology. — 1963. — Vol. 165(2). — P. 274—304. — PMID 14035891.
- ↑ Krnjević Krešimir. From ‘soup physiology’ to normal brain science // The Journal of Physiology. — 2005. — Vol. 569. — P. 1—2. — DOI:10.1113/jphysiol.2005.096883. [исправить]
- ↑ Diegel J. G., Pintar M. M. A possible improvement in the resolution of proton spin relaxation for the study of cancer at low frequency (англ.) // J. Natl. Cancer Inst. — 1975. — Vol. 55, no. 3. — P. 725—726. — PMID 1159850.
- ↑ Xiang Y. Y. et al. A GABAergic system in airway epithelium is essential for mucus overproduction in asthma (англ.) // Nat. Med. — 09 июля 2007. — Vol. 13, no. 7. — P. 862—867. — DOI:10.1038/nm1604. — PMID 17589520.
- ↑ Mayerhofer A. Neuronal Signaling Molecules and Leydig Cells // The Leydig cell in health and disease (англ.) / Eds.: Payne A. H., Hardy M. P. — Humana Press, 2007. — С. 299. — (Contemporary Endocrinology). — ISBN 1-58829-754-3, 978-1-58829-754-9. — DOI:10.1007/978-1-59745-453-7.
- ↑ Soltani N. et al. GABA exerts protective and regenerative effects on islet beta cells and reverses diabetes (англ.) // Proceedings of the National Academy of Sciences. — 2011. — Vol. 108. — P. 11692—11697. — DOI:10.1073/pnas.1102715108. [исправить]
- ↑ P. Rorsman, P. O. Berggren, K. Bokvist, H. Ericson, H. Möhler. Glucose-inhibition of glucagon secretion involves activation of GABAA-receptor chloride channels (англ.) // Nature. — 1989-09-21. — Vol. 341, iss. 6239. — P. 233—236. — ISSN 0028-0836. — DOI:10.1038/341233a0.
- ↑ Машковский М.Д. «Лекарственные средства» (16-е изд.),Новая волна, 2012, ISBN: 978-5-7864-0218-7, стр. 117
- ↑ Gaba (Gamma-Aminobutyric Acid) Effectiveness, Safety, and Drug Interactions on RxList (англ.). RxList. Дата обращения 14 января 2019.
Литература
Ссылки
альфа — аминомасляная кислота — alpha-Aminobutyric acid
 | |
 | |
| имена | |
|---|---|
| название IUPAC 2-аминобутановые кислоты | |
| Другие имена 2-аминомасляная кислота; α-аминобутанов кислота; этилглицин; гомоаланина | |
| Идентификаторы | |
| 3D модель ( JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ИКГВ InfoCard | 100.018.742 |
| UNII | |
| |
| свойства | |
| С 4 Н 9 NO 2 | |
| Молярная масса | 103,12 г / моль |
| Кислотность (р К ) | 2,55 (карбоксильной), 9,60 (амино) |
| -62,1 · 10 -6 см 3 / моль | |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
 Y проверить ( что ?) Y проверить ( что ?)  Y Y N N | |
| ссылки Infobox | |
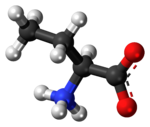
α-аминомасляная кислота (AABA), также известная как гомоаланин в области биохимии, является не-протеиногенным альфа — аминокислотой с химической формулой C 4 H 9 NO 2 . Прямые два углерода боковой цепи один атом углерода длиннее , чем аланин, следовательно, префикс гомо- .
Homoalaine является biosynthesised по transaminating оксобутирата метаболита в изолейцин биосинтеза. Он используется нерибосомальным пептидный синтазом. Одним из примеров нерибосомальных пептида , содержащего гомоаланин является офтальмологической кислоты , который был впервые выделен из линзы теленка.
альфа-аминомасляная кислота является одним из трех изомеров из аминомасляной кислоты . Два других являются нейромедиатором γ-аминомасляной кислоты (GABA) и β-аминомасляная кислота (BABA) , которая , как известно , для индукции устойчивости к болезням растений .
Рекомендации
<img src=»https://en.wikipedia.org//en.wikipedia.org/wiki/Special:CentralAutoLogin/start?type=1×1″ alt=»» title=»»>Гамма-аминомасляная кислота (ГАМК) — КиберПедия
Серотонин
Рис. 1. Серотонин
Серотонин (Рис. 1)– нейромедиатор, обеспечивающий чувство счастья. Большое количество серотонина вырабатывается в ядрах шва головного мозга. [3]
Увеличение концентрации данного вещества создает ощущение подъема настроения.
Есть люди, предрасположенные к более интенсивной выработке серотонина, их называют сангвиниками.
У людей с пониженным уровнем серотонина малейшие проблемы вызывают сильную депрессию. Данное свойство характерно для меланхоликов.
Гамма-аминомасляная кислота (ГАМК)
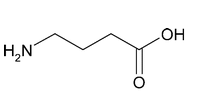
Рис. 2. Гамма-аминомасляная кислота
ГАМК (Рис. 2)– это тормозной нейромедиатор центральной нервной системы человека
Механизм функционирования нейронов основан на изменении концентрации ионов снаружи мембраны клетки и внутри нее. Изнутри мембрана заряжена отрицательно по отношению к внешней среде. Чем меньше заряд внутри мембраны, тем менее чувствительной становится клетка. ГАМК увеличивает проницаемость клеточной мембраны для ионов хлора, которые несут в себе отрицательный заряд, как следствие – снижение возбудимости самого нейрона. [4]
ГАМК обладает успокаивающим эффектом, придавая человеку чувство гармонии и спокойствия.
Дофамин
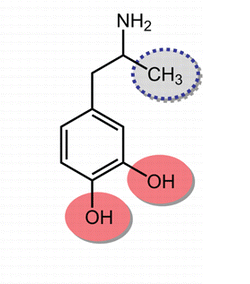
Рис. 3. Дофамин
Дофамин (Рис. 3)– это нейромедиатор адаптации и удовольствия. [5]
Дофамин способен придавать человеку уверенность в себе, стремление к самосовершенствованию. Доказано, что у людей с низкой самооценкой снижено содержание дофамина.
Когда мы попробовали новый вкусный торт, раздражаются нейроны, расположенные в центре удовольствия в мозгу. Порцией поощрения со стороны нашей нервной системы является выработка дофамина. На положительную реакцию вырабатывается рефлекс. Человек будет стремиться попробовать этот торт снова и снова для того, чтобы вновь получить порцию поощрения в виде удовольствия.
Всем нам знакомо чувство предвкушения. Почему, когда мы думаем о чем-либо приятном, о вкусной еде, например, это вызывается у нас приятное ощущение и еще большее желание?
Дело в том, что выработка дофамина начинается еще в процессе ожидания удовольствия. Это схоже с рефлексом собаки Павлова.
Широко известный эксперимент на крысах, основанный на вживлении им электродов в мозг, раздражающих центр удовольствия. Рычаг, установленный в клетке, активировал электрод. Крысы наступали на рычаг до тех пор, пока не доводили себя до смерти изнеможением. Они не ели и не спали, получая удовольствия от раздражения простым нажатием лапы на рычаг. [6]
Рассмотрим влияние гормонов на поведение человека.
Мелатонин
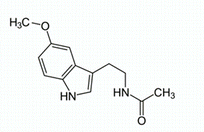
Рис. 4. Мелатонин
Мелатонин (Рис. 4) — антагонист серотонина, что синтезируется в эпифизе из серотонина. Секреция мелатонина напрямую зависит от общего уровня освещенности: избыток света тормозит его секрецию, а снижение освещенности – повышает синтез мелатонина.
Мелатонин является катализатором синтеза гамма-аминомасляной кислоты, что является тормозным медиатором ЦНС, которая тормозит синтез серотонина. [7]
Мелатонин ответственен за циркадные ритмы – внутренние биологические часы человека, что отвечают за сон и бодрствование. Его основная секреция приходится на период сна человека.
Вы замечали, что “жаворонки” (люди, что просыпаются рано утром и их максимальная активность приходится на первую половину дня) обычно люди активные. Они любят большое количество света в помещениях и прогулки в ясную погоду.
В то время как “совы” (люди, чья активность приходится на вторую половину дня) — любители поспать до обеда. Это обычно люди домашние и усидчивые. Они любят спать с занавешенными шторами.
Именно низкая освещённость и, как следствие, высокая выработка мелатонина являются основными причинами сезонной депрессии.
Мелатонин, вырабатываясь из серотонина, в то же время, сам притупляет его выработку. Этот факт представляет собой воплощение закона и единстве, и борьбе противоположностей. На этом принципе и устроен механизм саморегуляции сна и бодрствования. Именно поэтому в состоянии депрессии, люди страдают бессонницей — для того, чтобы погрузиться в сон нужен мелатонин, а без серотонина его никак не получить, а в состоянии депрессии его секреция снижена. [6]
Эндорфины
Рис. 5. Бета – эндорфин
Эндорфины (Рис. 5): данная группа гормонов выделяется после стрессовых ситуаций, обладает сильным обезболивающим, противошоковым и антистрессовым действием. Действуя, как блокаторы, эндорфины понижают чувствительность некоторых отделов центральной нервной системы. Вот почему у людей после стрессовых ситуаций снижен болевой порог.
Но стресс – это не единственная причина, запускающая механизм выработки эндорфинов. Опытным путём установлено, что выброс данных гормонов у человека напрямую связан с ощущением счастья.
Интересно, что эндорфины обладают мощным репаративным действием. Значит, утверждение: “Счастливые люди выздоравливают быстрее” — это научно доказанный факт. Так как выработка эндорфинов напрямую зависит от секреции серотонина. [8]
Эйфория — это один из «побочных эффектов» борьбы со стрессом. После успешно преодоленного стресса, организм получает вознаграждение в виде положительных эмоций.
Было установлено, что удовольствие от занятия спортом также имеет эндокринную природу: после перенесенных нагрузок, выброс эндорфинов увеличивается и у человека повышается настроение.[6]
Еще одна интересная особенность эндорфинов — это опиоидная система организма. Наркотические вещества сходны по структуре с эндорфинами и способны связываться с опиоидными рецепторами, вызывая чувство удовольствия. [2]
Однако, при постоянном раздражении клеток, запускается механизм привыкания: организм приспосабливается к высокой концентрации наркотических веществ в крови с помощью уменьшение количества рецепторов на клеточной мембране. Именно поэтому наркоманам для получения желаемого результата необходимо увеличивать дозу употребляемых наркотических веществ.
Адреналин

Рис. 6. Адреналин
Адреналин (Рис. 6) . В состоянии спокойствия, клетки мозгового слоя надпочечников все время вырабатывают небольшое количество адреналина вместе с норадреналином. В случае воздействия на организм человека какого-либо внешнего либо стрессового фактора, происходит скачок выработки адреналина и норадреналина. Данные биологически активные вещества помогают человеку успешно справляться со стрессами, придавая уверенности в себе. Однако, есть одно “но”. Адреналин повышает чувство страха и тревоги человека.[9].
Тиреоидные гормоны
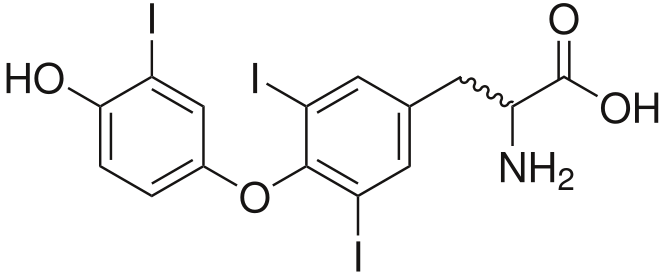
Рис. 7. Трийодтиронин
Рис. 8. Тироксин
Тиреоидные гормоны (Рис. 7,8)– это гормоны раздражительности. Если их слишком много, то у человека наблюдается взвинченность, нервное состояние, но при этом, тироксин помогает справиться со стрессом, участвуя в адаптации и в лучшем усвоении новой информации.
Тиреоидные гормоны контролируют распределение Na+ и К+ внутри клетки и во внеклеточном пространстве. Повышение уровня тетрайодтиронина или трийодтиронина сопровождается повышением уровня Na+ внутри клетки и выходом некоторой части ионов К+ из клетки. Такое изменение в распределении Na+ и К+ ведет к понижению порога возбудимости нервных клеток, это говорит о том, что нервным клеткам будет нужен раздражитель меньшей силы, чтобы перейти в состояние возбуждения. [10]
Тиреоидные гормоны способны проникать в мозг через гематоэнцефалический барьер и обнаруживаются в сером веществе различных отделах мозга.
Экспериментально доказано, что при гипотиреозе у людей замедляется скорость мыслительных процессов, понижается эмоциональный тонус, снижается память, возможности обучения
При гипертиреоидизме, наоборот, увеличивается скорость и амплитуда рефлекторных реакций, возбудимость, скорость мыслительных процессов, улучшается память и возможности обучения. [2]
Пролактин
Рис. 9. Пролактин.
Основной эффект пролактина (рис 9) – выработка молока в молочных железах.
Экспериментально было установлено, что уровень пролактина влияет на материнскую привязанность: лабораторные макаки, которым вводили ингибиторы пролактина, обособлялись от своих детенышей, предпочитая больше времени проводить в одиночестве.
Установлено, что адреналин является ингибитором выработки окситоцина и пролактина. Поэтому у женщин, испытывающих частый стресс во время беременности и вскармливания, наблюдаются проблемы, связанные с нехваткой молока [11].
Таким образом, все выше указанное подтверждает существенное влияние гормонов и нейромедиаторов на поведение человека, вызывая ярко выраженную перемену эмоционального состояния. Часто поведение людей основываются на импульсивных порывах, что в стрессовых ситуациях является эволюционно выработанной приспособительной реакцией.
Человек, обладая самосознанием, способен подвергать мысленному анализу свою психоэмоциональную реакцию и с помощью высшей нервной деятельности корректировать ее.
Настроение: серотонин
Серотонин — это нейромедиатор — одно из веществ, являющихся химическим передатчиком импульсов между нервными клетками человеческого мозга. Восприимчивые к серотонину нейроны расположены практически по всему мозгу.
Больше всего их в так называемых «ядрах шва» — участках ствола мозга. Именно там и происходит синтез серотонина в головном мозге. Кроме головного мозга, большое количество серотонина вырабатывается слизистыми оболочками желудочно-кишечного тракта.
Направления распространения серотониновых импульсов из этих ядер затрагивают многие области как головного, так и спинного мозга.
Трудно переоценить ту роль, которую выполняет серотонин в человеческом организме:
• В передней части мозга под воздействием серотонина стимулируются области, ответственные за процесс познавательной активности.
• Поступающий в спинной мозг серотонин, положительно влияет на двигательную активность и тонус мышц. Это состояние можно охарактеризовать фразой «горы сверну».
• И наконец самое главное — повышение серотонинэргической активности создает в коре головного мозга ощущение подъема настроения. Пока ограничимся именно таким термином, хотя в различных сочетаниях серотонина с другими гормонами — мы получаем весь спектр эмоций «удовлетворения» и «эйфории» — но об этом мы поговорим чуть позже.
Недостаток серотонина, напротив — вызывает снижение настроения и депрессию.
Кроме настроения, серотонин ответственен за самообладание или эмоциональную устойчивость (Mehlman et al., 1994). Серотонин контролирует восприимчивость мозговых рецепторов к стрессовым гормонам адреналину и норадреналину (о которых будет рассказано далее). У людей с пониженным уровнем серотонина, малейшие поводы вызывают обильную стрессовую реакцию. Отдельные исследователи считают, что доминирование особи в социальной иерархии обусловлено именно высоким уровнем серотонина.
Для того чтобы серотонин вырабатывался в нашем организме, необходимы две вещи:
• поступление с пищей аминокислоты триптофана — так как именно она нужна для непосредственного синтеза серотонина в синапсах
• поступление глюкозы с углеводной пищей => стимуляция выброса инсулина в кровь => стимуляция катаболизма белка в тканях => повышение уровня триптофана в крови.
С этими фактами напрямую связаны такие явления: булимия и так называемый «синдром сладкоежки». Всё дело в том, что серотонин способен вызвать субъективное ощущение сытости. Когда в организм поступает пища, в том числе содержащая триптофан — увеличивается выработка серотонина, что повышает настроение. Мозг быстро улавливает связь между этими явлениями — и в случае депрессии (серотонинового голодания), незамедлительно «требует» дополнительного поступления пищи с триптофаном или глюкозой.
Как ни странно, наиболее богаты триптофаном продукты, которые почти целиком состоит из углеводов,- такие, например, как хлеб, бананы, шоколад или чистые углеводы: столовый сахар или фруктозу. Это косвенно подтверждает бытующее в обществе утверждение, что сладкоешки / полные люди — более добрые, чем худые.
Серотонин метаболизируется в организме с помощью моноаминоксидазы-А (МАО-А) до 5-гидроксииндолуксусной кислоты, которая затем выводится с мочой. Первые Антидепрессанты являлись ингибиторами моноаминоксидазы.
Однако из-за большого количества побочных эффектов, вызванных широким биологическим действием моноаминоксидазы, в настоящее время в качестве андипепрессантов применяются «ингибиторы обратного захвата серотонина». Эти вещества затрудняют обратный захват серотонина в синапсах, тем самым повышая его концентрацию в крови. Например флуоксетин (препарат «Прозак»).
День и ночь: мелатонин
Мы ужели выяснили, что серотонин во-первых, вырабатывается за счёт обогащенной триптофаном и глюкозой пищей, а во-вторых — сам притупляет чувство голода. Мы выяснили, почему серотонин даёт прилив физических сил.
У серотонина в организме есть антипод — это мелатонин. Они синтезируется в эпифизе («шишковидной железе») из серотонина. Секреция мелатонина напрямую зависит от общего уровня освещенности — избыток света тормозит его образование, а снижение освещённости, напротив — повышает синтез мелатонина.
Именно под влиянием мелатонина в вырабатывается гамма-аминомасляная кислота, которая, в свою очередь тормозит синтез серотонина. 70% суточной продукции мелатонина приходится на ночные часы.
Именно синтезирующийся в эпифизе мелатонин ответственен за циркадные ритмы — внутренние биологические часы человека. Как правильно замечено, циркадный ритм напрямую не определяется внешними причинами, такими как солнечный свет и температура, но зависит от них — так как зависит от них синтез мелатонина.
Именно низкая освещённость и, как следствие, высокая выработка мелатонина, являются основными причинами сезонной депрессии. Вспомните эмоциональный подъём, когда зимой выдаётся ясный погожий день. Теперь вы знаете, почему это происходит — в этот день у вас снижается мелатонин, и повышается серотонин.
Замечу, что мелатонин вырабатывается не сам по себе — а из серотонина. И в то же время, сам притупляет его выработку. На этих, почти диалектических «единстве и борьбе противоположностей» и устроен внутренний механизм саморегуляции циркадных ритмов. Именно поэтому в состоянии депрессии, люди страдают бессонницей — для того, чтобы погрузиться в сон нужен мелатонин, а без серотонина его никак не получить.
Удовольствие: дофамин
Рассмотрим ещё один нейромедиатор — дофамин (или допамин) — вещество группы фенилэтиламинов. Тяжело переоценить роль дофамина в организме человека — как и серотонин, он выступает в качестве нейромедиатора и гормона одновременно. От него косвенно зависят и сердечная деятельность, и двигательная активность, и даже рвотный рефлекс.
Дофамин-гормон вырабатывается мозговым веществом надпочечников, а дофамин-нейромедиатор — областью среднего мозга, называемой «черным телом«.
Нас интересует дофамин-нейромедиатор. Известны четыре «дофаминовых пути» — проводящих пути мозга, в которых роль переносчика нервного имульса играет дофамин. Один из них — мезолимбический путь — считается ответственным за продуцирование чувств удовольствия.
Уровень дофамина достигает максимума во время таких действий, как еда и секс.
Почему нам приятно от мыслей о предстоящем удовольствии? Почему мы можем часами смаковать предстоящее наслаждение? Последние исследования показывают, что выработка дофамина начинается ещё в процессе ожидания удовольствия. Этот эффект схож с рефлексом предварительного слюноотделения у «собаки Павлова».
Считается, что дофамин также участвует в процессе принятия человеком решений. По крайней мере, среди людей с нарушением синтеза/транспорта дофамина многие испытывают затруднения с принятием решений. Это связано с тем, что дофамин отвечает за «чувство награды«, которое зачастую позволяет принять решение, обдумывая то или иное действие ещё на подсознательном уровне.
К сожалению, нейробиология ещё только развивается. В частности, относительно недавняя нобелевская премия за 2000 год в области биологии была присуждена за открытия в области «передачи сигналов в нервной системе». Поэтому, получить из русскоязычного интернета более подробную информацию по нейромедиаторам, на данный момент не представляется возможным.
Влюблённость: фенилэтиламин
2-фенилэтиламин (или PEA) — является нейротрансмиттером и нейромодулятором энергии межличностных отношений. Выделение РЕА повышает эмоциональную теплоту, симпатию, сексуальность
Хотя фенилэтиламин является начальным соединением для других нейромедиаторов, и сам он часто выделяется вместе дофамином и серотонином, тем не менее, его действие в эмоциональной области единственно в своем роде. Для РЕА совсем недавно был идентифицирован специфический рецептор, локализованный в миндалевидном теле — ядре мозга.
Своеобразно также короткое время жизни фенилэтиламина (минуты) и его разрушение под действием энзима моноамин-оксигеназы. Короткое время жизни свидетельствует о специальной биодинамической роли РЕА, связанной с очень кратко действующим эффектом раздражения. Напротив, другие нейроамины (допамин, серотонин и норадреналин) обладают большими временами жизни (часы).
Влияние фенилэтиламина на поведение человека принято объяснять на основе гипотезы М. Либовица (называемой ещё «психохимической гипотезой») о влюбленности. Несмотря на спекулятивность этой гипотезы, она позволяет хотя бы объяснить роль фенилэтиламина в регулировании аффектов. Если мы встречаем кого-либо, кто нам нравится, в мозгу начинает вырабатываться фенилэтиламин. Мы, люди, судим о привлекательности партнера или партнерши в первую очередь по оптическому впечатлению, а не по запаху или осязанию, как большинство млекопитающих. Романтическая любовь может вспыхнуть буквально с первого взгляда. Синтез фенилэтиламина в мозгу и его распределение по всей нервной системе играют роль при возникновении возбуждения, охватывающего нас при взгляде на любимого человека, и стремления к нему, когда его нет с нами.
Фенилэтиламин содержится в шоколаде, в сладостях (содержащих аспартам), в диэтических напитках. И всё же все эти источники не дают того результата, какой дает фенилэтиламин, выделяемый мозгом (то есть эндогенный). Главная причина – быстрое разрушение фенилэтиламина под действием энзима моноаминоксидазы-Б (МАО-Б) — основное его количество расщепляется еще на начальной стадии потребления. Любовные напитки существуют в сказании о Тристане и Изольде или в драме Шекспира «Сон в летнюю ночь», в действительности же наша химическая система ревниво охраняет свое исключительное право контроля наших эмоций.
В Интернете практически нет русскоязычных научных статей, в которых бы описывался механизм действия фенилэтиламина как нейромедиатора. Зато полно популярно-бытовых заметок сомнительного наполнения. Если бы не эта и эта статьи, и их англоязычные аналоги — я вообще бы усомнился в научности действия фенилэтиламина. Тем не менее, не следует забывать, что «на нашем современном уровне знаний эта гипотеза М.Либовица полностью не подтверждена».
Доверие: окситоцин
Окситоцин — ещё один гормон и нейротрансмиттер гипофиза. Физиологическое действие окситоцина-гормона заключается в увеличении частоты сокращений матки и альвеолы молочных желез у женщин. В медицине, окситоцин используется для стимуляции родовой деятельности.
Окситоцин также участвует в реакции сексуального возбуждения. Именно окситоцин участвует в эрекции сосков (как у мужчин, так и у женщин). Благодаря окситоцину у женщины в период лактации увеличивается выработка грудного молока, при близком контакте с новорождённым ребёнком или при раздражении сосков.
Отдельные исследователи считают, что окситоцин участвует в механизме мужской эрекции — по крайней мере, положительный эффект давала инъекция его в отдельные участки мозга. Однако, смело можно утверждать, что роль окситоцина в механизме эрекции — не определяющая.
Сравнительно недавно (2005 год) была открыто психо-физиологическая роль окситоцина-нейромодулятора. В ходе нескольких экспериментов, выяснилось, что окситоцин увеличивает степень доверия к конкретному человеку.
В опыте приняли участие 178 студентов цюрихских университетов (исключительно мужчины). Им предложили стать партнерами в игре, где одни выполняли роль инвесторов, а другие — брокеров. В начале эксперимента каждый участник получил личный финансовый фонд. Инвестор мог оставить все эти условные деньги себе, или же передать их (все или частично) своему брокеру. По условиям игры брокер на каждой такой операции наваривал 200% прибыли, то есть вклад «инвестора» до него доходил в тройном размере. При этом брокер мог либо оставить у себя все эти деньги, либо возвратить инвестору любую их часть. На этом игра заканчивалась, и партнеры приступали к подсчету выигрышей и потерь. Чтобы создать настоящий азарт и корыстный интерес, экспериментаторы в конце опыта выдавали за каждую «денежную единицу» 40 вполне реальных швейцарских сантимов.
Ключевой аспект эксперимента заключался в том, что одним инвесторам давали вдыхать аэрозольный препарат окситоцина, а остальным — нейтральный спрей. Оказалось, что инвесторы, которые получали окситоцин, много больше доверяли своим брокерам. 45% из них предпочли вложить в дело все 12 единиц своего капитала. 21% не сделали никаких вложений или проявили минимум доверия. А вот среди «плацебников» все обстояло точно наоборот: максимум доверия — 21%, минимум — 45%.
Однако из этих результатов отнюдь не следует, что окситоцин действительно увеличивает степень доверия к партнеру по «деловой операции». Чтобы исключить интерпретацию опыта, якобы «под воздействием окситоцина люди перестают бояться рисковать» был поставлен дополнительный эксперимент, с прежними условиями. Однако, размер получаемой инвестором выплаты определял уже не брокер, а генератор случайных чисел. В этой ситуации обе группы «инвесторов» действовали одинаково, так что окситоцин не оказал на них никакого влияния. Этот контрольный опыт продемонстрировал, что окситоцин увеличивает степень доверия к конкретному человеку, но отнюдь не подталкивает играть наудачу.
В настоящий момент считается, что уровень окситоцина повышается при близком контакте с человеком, особенно при прикосновениях и поглаживаниях. Ещё больше окситоцина выделяется в процессе полового акта, и непосредственно в момент оргазма — как у мужчин, так и у женщин.
Окситоцин участвует в формировании связей между людьми, в том числе связей между матерью и ребёнком. Окситоцин понижает уровень тревожности и напряжения человека при контактах с другими людьми. Окситоцин стимулирует выработку эндорфинов, вызывающих ощущение «счастья». Кошка, которая мурлыкает в ответ на ваши поглаживания — типичный пример действия окситоцина.
Интересный эксперимент был проведён в 2005 году. Исследования касались детей-сирот, которые провели первые месяцы или годы жизни в приюте, а потом были усыновлены благополучными семьями. Дети играли в компьютерную игру, сидя на коленях у своей матери (родной или приемной), после этого измерялся уровень окситоцина и сравнивался с уровнем, измеренным перед началом эксперимента. В другой раз те же дети играли в ту же игру, сидя на коленях у незнакомой женщины.
Оказалось, что у домашних детей после общения с мамой уровень окситоцина заметно повышается, тогда как совместная игра с незнакомой женщиной такого эффекта не вызывала. У бывших сирот окситоцин не повышался ни от контакта с приемной матерью, ни от общения с незнакомкой. Эти печальные результаты показывают, что способность радоваться общению с близким человеком, по-видимому, формируется в первые месяцы жизни.
Привязанность: вазопрессин
Вазопрессин — гормон гипофиза, по молекулярному строению схожий с окситоцином. Основная физиологическая функция вазопрессина — увеличение реабсорбции воды почками, тем самым повышая концентрацию мочи и уменьшая её объём.
В 1999 на примере мышей-полёвок было неожиданно открыто ещё одно свойство вазопрессина. Дело в том, что существует два вида мышей: полёвка-степная и полёвка-горная. При этом степные полёвки относятся к 3% млекопитающих, реализующих моногамные отношения. Когда степные полевки спариваются, выделяются два гормона: окситоцин и вазопрессин. Если выделение этих гормонов блокировать, половые отношения между степными полевками становятся такими же мимолетными, как и у их «распутных» горных родственников. Наибольший эффект приносит именно блокировка вазопрессина.
В данном случае отличительный признак — запах. Крысы и мыши узнают друг друга по запаху. Учёные утверждают, что степные полёвки привязываются друг к другу благодаря действию механизма полового импринтинга, опосредованного запахом. Более того, ученые предполагают, что у других моногамных животных, включая человека, эволюция механизма поощрения, участвующего в формировании этой привязанности, протекала схожим образом, в том числе с целью регулирования моногамии.
Среди исследованных человекоподобных обезьян уровень вазопрессина в центрах поощрения мозга у моногамных мартышек был выше, чем у немоногамных макак-резусов. Считается, что животные, устанавливающие прочные социальные отношения, поступают так благодаря наличию и особому расположению их рецепторов для восприятия вазопрессина и окситоцина. Чем больше рецепторов находится в областях, связанных с поощрением, тем большее удовольствие доставляет социальное взаимодействие.
По альтернативной гипотезе, считается что моногамия полёвок вызывается изменениями в структуре и количестве дофаминовых рецепторов.
Подготовка к зачатию: прогестины (прогестерон)
Прогестины, и в частности прогестерон — исключительно женские половые гормоны. Основная их функция — обеспечение возможности наступления, а затем = поддержание беременности.
Если пик эстрогенов приходится на овуляцию (это повышает половое влечение, уровень феромонов и увеличивает вероятность полового акта, необходимого для зачатия) — то наибольший уровень прогестерона приходится на вторую стадию цикла — идёт подготовка организма к возможной беременности.
На данный момент существует несколько теорий о причинах возникновения предменструального синдрома.
Обычно, симптомы ПМС связывают с резким уменьшением количества прогестерона на фоне существенно возросшей концентрации эстрогенов. Прогестерон обладает обезболивающим действием, а избыток эстрогенов приводит к задержке жидкости и солей натрия в межклеточном пространстве. Именно с чрезмерной гидратацией организма и его солевой интоксикацией и связано явление ПМС. Характер симптомов определяется заинтересованностью тканей, где развивается отек (мозг — головная боль, кишечник — вздутие живота,тошнота и т.д.).
Кстати: доказано, что уровень прогестерона повышается в организме женщины при одном взгляде на ребенка. Младенческая схема, запускающая женское родительское поведение, таким образом, имеет гормональную базу. Пухлое тельце, коротенькие ножки и ручки, большая голова и большие глаза — стимулирует мощный выброс прогестерона у женщины. Ничего подобного при контакте с младенцами у мужчин не происходит.
Предрасположенность к гормональному ответу на младенческую схему у женщин столь сильна, что механизм этот запускается даже тогда, когда женщина видит котенка, щенка или просто игрушечного плюшевого мишку (см. рисунок).
Именно особенностями женского восприятия, связанными с врожденными материнскими инстинктами объясняется тот факт, что многие девушки и молодые женщины приходят в восторг от мягких плюшевых игрушек с пропорциями младенческого тела, тогда как длинные и тощие игрушки не вызывают у них никакой положительной реакции.
У мужчин прогестерон не вырабатывается, и им просто непонятны взрывы умиления, которые взрослая женщина, исторгает при виде маленькой плюшевой зверушки.
Эрекция : монооксид азота
Сам механизм эрекции довольно сложен. Упрощённо, его можно разбить на следующие этапы:
• Мозг получает сексуальную стимуляцию: зрительную / тактильную / мысленную — кому какая нравится 😉 С помощью нейромедиаторов норадреналина, ацетилхолина и окситоцина сигнал передаётся к гладкой мускулатуре пещеристых тел.
• Под действием нервных импульсов и тестостерона в синапсах гладкой мускалатуры начинает выделяться.. монооксид азота NO. Будучи неорганическим, это соединение играет существенную роль в физиологии человека. NO — нейротрансмиттер с сосудорасширяющим действием, кроме обеспечения эрекции, участвует в механизме долговременной памяти.
• Окись азота, в свою очередь, приводит к образованию другого химического вещества — циклический гуанозин монофосфат (цГМФ) которое приводит к расслаблению гладкой мускулатуры пещеристых тел и позволяет крови заполнить их.
•Поступление богатой кислородом артериальной крови способствует образованию еще большего количества окиси азота. А это, опять же, ведет к увеличению производства цГМФ.
• По мере заполнения кровью, пещеристые тела начинают пережимать вены, отводящие кровь от пениса. Это задерживает ее внутри кавернозных тел и поддерживает пенис в эрегированном состоянии.
• Эрекция продолжается до тех пор, пока гладкие мышцы пещеристых тел снова не сократятся. При этом кровь, находящаяся в них, изгоняется, а венозные сосуды раскрываются и отводят ее избыток от пениса.
Такие препараты, как Виагра, Сиалис Левитра (и др.) содержат силденафил — ингибитор фосфодиэстеразы–5 (ФДЭ–5), вещества расщепляющего цГМФ. При этом в организме происходит накопление цГМФ, в результате чего поддерживается длительная эрекция.
Следующее поколение препаратов — препараты, содержащие сверхмалые дозы антител к NO-синтазе (Импаза). Такие препараты повышают активность NO-синтаз (источников NO в пещеристых телах), и обладают не только разовым эффектом, но и приводят к долгосрочным улучшениям.
Опьянение: этанол
К сожалению, нельзя ни съесть, ни даже ввести себе внутривенно — ни серотонин, ни дофамин. Они должны вырабатываться внутри головного мозга. Будучи введенными извне, эти вещества не способны преодолеть гематоэнцефалический барьер, защищающий мозг от поступления чужеродных веществ.
Зато гематоэнцефалический барьер замечательно преодолевают никотин, опиаты, и конечно же алкоголь.
В отличие от наркотиков, имеющих к соответствующим рецепторам высокое сродство (например, наркотики опийной группы) молекулы этанола не воздействуют непосредственно на рецепторы, а пропитывают липидный слой мембраны нейрона, разжижают её, вызывая процесс флюидизации. В разрыхлённой мембране рецептор утрачивает опору, его конформация изменяется и возникает ощущение опьянения.
Прием этанола усиливает оборот серотонина. Повышение проницаемости мембран-везикул способствует утечке медиатора в пресинаптическую щель и реализации его эффекта. Оказав действие, он интенсивно расщепляется до 5-оксииндолуксусной кислоты. Уменьшение концентрации серотонина в гипоталамусе служит фактором, усиливающим стремление к выпивке.
Однократный прием алкоголя приводит к активизации процессов образования и использования норадреналина. Содержание его снижается за счет усиления выброса нейромедиатора из везикул и ускоренного его распада. Усилением кругооборота норадреналина в среднем мозге и гипоталамусе объясняется фаза двигательного, вегетативного и эмоционального возбуждения, связанного с употреблением алкоголя. Истощение запасов норадреналина приводит к подавленному состоянию, психической и двигательной заторможенности.
Всем известный синдром алкогольного похмелья вызван интоксикацией организма продуктом окисления этанола — ацетальдегидом, который печень не успевает окончательно расщепить в безвредную уксусную кислоту.
Серотонин

Рис. 1. Серотонин
Серотонин (Рис. 1)– нейромедиатор, обеспечивающий чувство счастья. Большое количество серотонина вырабатывается в ядрах шва головного мозга. [3]
Увеличение концентрации данного вещества создает ощущение подъема настроения.
Есть люди, предрасположенные к более интенсивной выработке серотонина, их называют сангвиниками.
У людей с пониженным уровнем серотонина малейшие проблемы вызывают сильную депрессию. Данное свойство характерно для меланхоликов.
Гамма-аминомасляная кислота (ГАМК)

Рис. 2. Гамма-аминомасляная кислота
ГАМК (Рис. 2)– это тормозной нейромедиатор центральной нервной системы человека
Механизм функционирования нейронов основан на изменении концентрации ионов снаружи мембраны клетки и внутри нее. Изнутри мембрана заряжена отрицательно по отношению к внешней среде. Чем меньше заряд внутри мембраны, тем менее чувствительной становится клетка. ГАМК увеличивает проницаемость клеточной мембраны для ионов хлора, которые несут в себе отрицательный заряд, как следствие – снижение возбудимости самого нейрона. [4]
ГАМК обладает успокаивающим эффектом, придавая человеку чувство гармонии и спокойствия.
Дофамин

Рис. 3. Дофамин
Дофамин (Рис. 3)– это нейромедиатор адаптации и удовольствия. [5]
Дофамин способен придавать человеку уверенность в себе, стремление к самосовершенствованию. Доказано, что у людей с низкой самооценкой снижено содержание дофамина.
Когда мы попробовали новый вкусный торт, раздражаются нейроны, расположенные в центре удовольствия в мозгу. Порцией поощрения со стороны нашей нервной системы является выработка дофамина. На положительную реакцию вырабатывается рефлекс. Человек будет стремиться попробовать этот торт снова и снова для того, чтобы вновь получить порцию поощрения в виде удовольствия.
Всем нам знакомо чувство предвкушения. Почему, когда мы думаем о чем-либо приятном, о вкусной еде, например, это вызывается у нас приятное ощущение и еще большее желание?
Дело в том, что выработка дофамина начинается еще в процессе ожидания удовольствия. Это схоже с рефлексом собаки Павлова.
Широко известный эксперимент на крысах, основанный на вживлении им электродов в мозг, раздражающих центр удовольствия. Рычаг, устан