КАЛИЯ — это… Что такое КАЛИЯ?
калия — суп potage calia à l estragon. кулин. Суп калия с астрагоном. Радецкий 1853 2 15 … Исторический словарь галлицизмов русского языка
Калия — Кришна танцует на головах змея Калия. У этого термина существуют и другие значения, см. Калия (значения) … Википедия
Калия — (Санскр.) Пятиголовый змий, убитый Кришной в детстве Мистическое чудовище, символизирующее страсти человека река или вода будучи символом материи. Источник: Теософский словарь … Религиозные термины
КАЛИЯ ХЛОРИД — Действующее вещество ›› Калия хлорид* (Potassium chloride*) Латинское название Potassium chloride АТХ: ›› A12BA01 Калия хлорид Фармакологическая группа: Макро и микроэлементы Нозологическая классификация (МКБ 10) ›› E87.6 Гипокалиемия ›› I47.2… … Словарь медицинских препаратов
КАЛИЯ ЙОДИД — Действующее вещество ›› Калия йодид (Potassium iodide) Латинское название Kalii iodidum АТХ: ›› H03CA Препараты йода Фармакологические группы: Гормоны щитовидной железы, их аналоги и антагонисты (включая антитиреоидные средства) ›› Макро и… … Словарь медицинских препаратов
КАЛИЯ ЙОДИД — Kalii iodidum. Синоним: калий йодистый. Свойства. Калия йодид представляет собой бесцветные или белые кубические кристаллы или белый мелкокристаллический порошок без запаха, солено горького вкуса, легко растворимый в воде и спирте. Гигроскопичен … Отечественные ветеринарные препараты
КАЛИЯ АЦЕТАТ — ( Кalii асеtas ). Синоним: Каlium aceticum. Белый кристаллический порошок без запаха или со слабым запахом уксусной кислоты, солоноватого вкуса. Гигроскопичен, расплывается на воздухе. Очень легко растворим в воде (2,5 : 1), легко в спирте (1 :… … Словарь медицинских препаратов
КАЛИЯ ОРОТАТ — Действующее вещество ›› Оротовая кислота* (Orotic acid*) Латинское название Potassium orotate АТХ: ›› A05BA Препараты для лечения заболеваний печени Фармакологическая группа: Анаболики Нозологическая классификация (МКБ 10) ›› D64 Другие анемии… … Словарь медицинских препаратов
КАЛИЯ ГИДРООКИСЬ — Kalii hydroxydum. Синонимы: кали едкое, гидрат окиси калия плавленый (очищенный). Свойства. Белые с желтоватым оттенком куски или цилиндрические палочки с кристаллической структурой на изломе. Гигроскопична, на воздухе расплавляется и быстро пог … Отечественные ветеринарные препараты
КАЛИЯ ПЕРМАНГАНАТ — Kalii permanganas. Свойства. Калия перманганат (марганцовокислый калий) кристаллический порошок или ромбовидные кристаллы темно фиолетового цвета с металлическим опенком. Хорошо растворим в воде (1:18), в зависимости от концентрации растворы окр … Отечественные ветеринарные препараты
Калия — Википедия. Что такое Калия
 Кришна танцует на головах змея Калия.
Кришна танцует на головах змея Калия.Калия (санскр. कालिया, Kāliyā
Согласно древнему обычаю, наги регулярно приносили Гаруде в дар пищу.[1] Однажды Калия возгордился и съел подношение, принесённое другими нагами для царя пернатых.[1] Гаруда пришёл в ярость и набросился на Калию, намереваясь убить его за проявленную дерзость.[1] Калия уставился на Гаруду множеством своих немигающих глаз, распахнул свои пасти и обнажив острые клыки, полные смертельного яда, всячески пытался укусить противника, бросаясь на него подобно молнии.
Однажды Гаруда поймал в Ямуне рыбу, и, намереваясь утолить голод, приготовился съесть её.[1] В этот момент к нему подошёл благочестивый риши и попросил его пощадить рыбе жизнь, отпустив её назад в реку.[1] Однако Гаруду терзал такой жестокий голод, что он не смог удержаться и съел пойманную им рыбу.[1] Мудрец сильно разгневался и проклял Гаруду, сказав, что если тот когда-либо ещё коснется вод Ямуны, то в тот же час и погибнет.
Однажды Кришна пригнал на водопой к Ямуне стадо телят.[1] На песчаном берегу реки он увидел мёртвые тела своих друзей, мальчиков-пастушков, а рядом с ними — павшее коровье стадо.
В это самое время во Вриндаване появились дурные предзнаменования, предвещавшие беду.[2] Жители Вриндавана пришли в великое беспокойство и отправились на поиски Кришны.[2] Его следы привели их к берегу Ямуны.[3] Узрев любимого Кришну недвижимым в смертельных объятиях змея, они горько заплакали и собрались было броситься в реку на помощь Кришне, но Баларама остановил их.[3] Вдруг тело Кришны стало расширяться и разомкнуло кольца Калии.[3] При виде оказавшегося на свободе Кришны, Калия пришёл в неистовую ярость.[3] Описывается, что его смрадное дыхание жгло как огонь, смертельный яд вытекал из его ртов и капал в воду, языки его алчно шевелились, и множество немигающих глаз с ненавистью уставились на Кришну, стремясь лишить его всякой силы.
См. также
Примечания
Ссылки
Цианид калия — это… Что такое Цианид калия?
Циани́д ка́лия, или циа́нистый ка́лий — калиевая соль циановодородной кислоты, химическая формула KCN. Бесцветные кристаллы, по фактуре и размерам напоминающие сахарный песок. Хорошо растворим в воде (41,7 % по массе при 25 °C, 55 % при 100 °C). Плохо растворим в этаноле, не растворяется в углеводородах.
Водный раствор цианида калия для некоторых людей имеет запах горького миндаля, для некоторых остается без запаха. Предполагается, что это различие обусловлено генетически.[1]
Получение
Цианид калия в лаборатории получают взаимодействием циановодорода с гидроксидом калия:
Также цианид калия можно получить из хлороформа, аммиака и гидроксида калия:
Легко получить прокаливанием жёлтой кровяной соли при температуре выше 650 градусов.
Цианистый калий выделил шведский аптекарь Карл Вильгельм Шееле в 1762 году.
Применение
Применяется в процессе добычи золота и серебра из руд (цианирование):
- ,
а также в гальванотехнике цинка, кадмия, меди, серебра и золота, в том числе для ювелирного дела.
Химические свойства
Так как синильная кислота, соответствующая цианид-иону, очень слабая, то цианид калия легко вытесняется из солей более сильными кислотами. Так, например, на воздухе цианид калия со временем превращается в нетоксичный карбонат калия (поташ) в результате реакции с углекислым газом и водой:
Формально, в этом процессе принимает участие нестабильная слабая угольная кислота, которая вытесняет из соли синильную кислоту.
Токсичность
 Потенциально смертельная доза цианистого калия (140 мг)
Потенциально смертельная доза цианистого калия (140 мг)Сильнейший неорганический яд. При попадании через пищеварительный тракт смертельная доза для человека 1,7 мг/кг. Иногда переносятся бо́льшие дозы, замедление действия возможно при заполнении желудка пищей. Антидотными свойствами обладают метгемоглобинообразующие вещества и вещества, содержащие серу и углеводы. К метгемоглобинообразователям относятся антициан, амилнитрит, азотистокислый натрий, метиленовый синий. Они окисляют железо гемоглобина, превращая его в метгемоглобин.
В организме человека цианид калия оказывает мощное ингибирующее воздействие. Он блокирует клеточный фермент цитохром с-оксидазы, в результате чего клетки теряют способность усваивать кислород из крови и организм погибает от внутритканевой гипоксии.
Примечания
Ссылки
Чрезвычайно опасные вещества | |
|---|---|
Нитрат калия — это… Что такое Нитрат калия?
| Нитрат калия | |
 | |
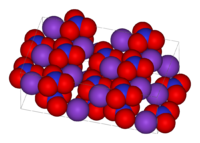 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат калия |
| Сокращения | в народе КС, НК |
| Традиционные названия | Ка́лиевая селитра, кали́йная селитра, индийская селитра, Соль Петра (Salt of Peter)[источник?] |
| Химическая формула | KNO3 |
| Эмпирическая формула | KNO3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Отн. молек. масса | 101,1032 а. е. м. |
| Молярная масса | 101,1032 г/моль |
| Плотность | 2,109 (16 °C) г/см³ |
| Твёрдость | 2 |
| Термические свойства | |
| Температура плавления | 334 °C |
| Температура кипения | с разложением °C |
| Температура разложения | 400 °C |
| Тройная точка | отсутствует |
| Молярная теплоёмкость (ст. усл.) | 95,06 Дж/(моль·К) |
| Энтальпия образования (ст. усл.) | -494,00 кДж/моль |
| Энтальпия плавления | 9,80 кДж/моль |
| Энтальпия сублимации | 181,00 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 13,3 (0 °C) 36 (25 °C) 247 (100 °C) |
| Классификация | |
| Рег. номер CAS | 7757-79-1 |
| RTECS | TT3700000 |
| Безопасность | |
| ЛД50 | 3750 мг/кг |
| Токсичность | малотоксичен |
| NFPA 704 |  |
Нитра́т ка́лия, азотноки́слый ка́лий (ка́лиевая сели́тра, кали́йная селитра, индийская селитра и др.) — неорганическое бинарное соединение, калиевая соль азотной кислоты с формулой KNO3. В кристаллическом состоянии — бесцветное вещество, нелетучее, слегка гигроскопичное, без запаха. Нитрат калия хорошо растворим в воде. Практически не токсичен для живых организмов.
Встречается в природе в виде минерала нитрокалита, в Ост-Индии находятся одно из крупнейших месторождений, отсюда второе название — индийская селитра. В очень малых количествах содержится в растениях и животных[1].
Форма кристаллов игольчатая, сами кристаллы очень длинные. Легко поддается очистке перекристаллизацией с минимальными потерями.
Основное применение находит в пиротехнике (до XX века особенно широко, как компонент основного в то время взрывчатого вещества — дымного (черного) пороха) и как калий-азотное удобрение (очень удобный комплекс двух обычно плохо сочетающихся при усваивании растениями элементов).
Физические свойства
Нитрат калия в нормальных условиях представляет собой бесцветные кристаллы (в измельченном состоянии белый порошок) с ионной структурой и ромбической или гексагональной кристаллической решеткой. Слегка гигроскопичен, склонен несильно слеживаться со временем. Не имеет запаха, нелетуч.
Хорошо растворим в воде, в средней степени в глицерине, жидком аммиаке, гидразине, нерастворим в чистом этаноле и эфире (в разбавленных водой растворяется плохо). Таблица растворимости в некоторых растворителях, в граммах KNO3 на 100 г H2O[2][3]:
| Растворитель / Температура | 0 °С | 10 °С | 20 °С | 25 °С | 30 °С | 40 °С | 50 °С | 60 °С | 70 °С | 80 °С | 90 °С | 100 °С |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Вода | 13,9 | 21,2 | 31,6 | 37,9 | 46,0 | 61,3 | 106,2 | 166,6 | 245,0 | |||
| Жидкий аммиак | 10,52 | 10,4 | ||||||||||
| Гидразин | 14 | |||||||||||
| Диэтиловый эфир | ||||||||||||
| Этанол | ||||||||||||
| Метанол | ||||||||||||
| Глицерин |
При медленной кристаллизации вырастают очень длинные игольчатые кристаллы. Нитрат калия хорошо поддается очистке перекристаллизацией, причем с небольшими потерями, благодаря сильному повышению растворимости с ростом температуры.
Химические свойства
Разлагается при 400 °C с образованием нитрита калия KNO2 и кислорода O2 (выделение последнего увеличивает пожароопасность нитрата калия):
Является сильным окислителем, реагирует с горючими материалами и восстановителями, при измельчении активно и нередко со взрывом. В смеси с некоторыми органическими материалами склонен самовоспламенять их.
Расплав может быть использован для получения калия электролизом, однако из-за высоких окислительных способностей нитрата калия в этом состоянии предпочтительнее гидроксид калия.
Получение
В Средние Века и Новое Время (когда активно использовали порох) для получения нитрата калия служили селитря́ницы — кучи из смеси навоза (и других перегнивающих компонентов) с известняком, строительным мусором и прочим известняковым материалом с прослойками из соломы или хвороста, накрытые дерном для удерживания образующихся газов. При гниении навоза образовывался аммиак, который накапливаясь в прослойках из соломы, подвергался нитрификации и превращался вначале в азотистую, а затем в азотную кислоту. Последняя, взаимодействуя с известняком, давала Ca(NO3)2, который выщелачивался водой. Добавка древесной золы (состоящей в основном из поташа) приводила к осаждению CaCO3 и получению раствора нитрата калия; нередко золу добавляли сразу в кучу вместо известняка, тогда калиевая селитра получалась сразу. Реакция поташа с кальциевой селитрой (нитратом кальция)
является самой древней из используемых человеком для получения нитрата калия и популярна до сих пор. Вместо поташа впрочем, сейчас в лабораториях чаще всего используют сульфат калия, реакция очень похожа:
Первый способ применялся до 1854 г., когда немецкий химик К. Нёльнер изобрел производство нитрата калия, основанное на реакции более доступных и дешевых хлорида калия и нитрата натрия:
Существует несколько других способов получения нитрата калия. Это взаимодействие нитрата аммония и хлорида калия с образованием нитрата калия и хлорида аммония, последний легко отделяется:
- — популярнейшая после реакции нитрата кальция с карбонатом или сульфатом калия
- — в основном демонстративная реакция соответствующей кислоты и основания
- — тоже демонстративная реакция соответствующих кислоты и металла
- — демонстр. реакция соотв. щелочного оксида с соотв. кислотой
Природные источники и месторождения
В природе калия нитрат распространен в виде минерала нитрокалита. Крупнейшие его месторождения находятся в Ост-Индии и в Чили (вместе с основным минералов — нитронатритом). Природный нитрат калия является результатом разложения азотистых веществ с последующим связыванием медленно выделяющегося аммиака нитробактериями, чему способствует влага и тепло, поэтому наиболее крупные залежи находятся в странах с жарким климатом[4].
В очень малых количествах содержится в растениях и животных[1], является промежуточным продуктом при переработке ими почвенных сульфата и карбоната калия.
Применение
Основное применение на сегодняшний день нитрат калия находит в качестве ценного удобрения, так как совмещает в себе два частично блокирующих усвоение друг друга растениями элемента.
Незаменим он при изготовлении дымного пороха и некоторых других составов (например, карамельного ракетного топлива), которые почти полностью сейчас идут на производство пиротехники.
Применяется также в электровакуумной промышленности и оптическом стекловарении для обесцвечивания и осветления технических хрустальных стекол и придания прочности изделиям из стекла[5].
Расплав часто используется в лабораториях и у любителей для получения элементарного калия электролизом, наряду с гидроксидом калия.
Используется в качестве сильного окислителя в металлургии, в частности при переработке никелевых руд.
См. также
Примечания
Ссылки
КАЛИЙ — это… Что такое КАЛИЙ?
Калий-40 — Калий 40 … Википедия
КАЛИЙ — новолатинск. kalium, от араб. kali, щелочь. Мягкий и легкий металл, составляющий основание кали. Открыт Деви в 1807 году. Объяснение 25000 иностранных слов, вошедших в употребление в русский язык, с означением их корней. Михельсон А.Д., 1865.… … Словарь иностранных слов русского языка
КАЛИЙ — (Kalium), K, химический элемент I группы периодической системы, атомный номер 19, атомная масса 39,0983; относится к щелочным металлам; tпл 63,51шC. В живых организмах калий основной внутриклеточный катион, участвует в генерации биоэлектрических… … Современная энциклопедия
КАЛИЙ — (Kalium, s. Potassium), хим. элемент, симв. К, порядковый номер 19, серебристо белый, блестящий металл, имеющий при обыкновенной ta плотность воска; открыт Деви в 1807 г. Уд. в. при 20° 0,8621, атомный вес 39,1, одновалентен; t° плавления … Большая медицинская энциклопедия
Калий — (Kalium), K, химический элемент I группы периодической системы, атомный номер 19, атомная масса 39,0983; относится к щелочным металлам; tпл 63,51°C. В живых организмах калий основной внутриклеточный катион, участвует в генерации биоэлектрических… … Иллюстрированный энциклопедический словарь
КАЛИЙ — муж. потасий, металл, составляющий основанье кали, весьма сходный с натрием (содием). Кали ср., нескл., растительная щелочь или щелочная соль; углекислый калий, чистый поташ. Калиевый, к калию относящийся. Калистый, содержащий кали. Толковый… … Толковый словарь Даля
калий — потассий, поташ Словарь русских синонимов. калий сущ., кол во синонимов: 4 • металл (86) • потассий … Словарь синонимов
КАЛИЙ — (лат. Kalium) К, химический элемент I группы периодической системы, атомный номер 19, атомная масса 39,0983, относится к щелочным металлам. Название от араб. аль кали поташ (давно известное соединение калия, добывающееся из древесной золы).… … Большой Энциклопедический словарь
Калий — K (от араб, аль кали поташ * a. Potassium, potash; н. Kalium; ф. potassium; и. potasio), хим. элемент I группы периодич. системы Mенделеева, ат.н. 19, ат. м. 39,102. Природный K. состоит из двух стабильных изотопов 39K (93,08%), 41K… … Геологическая энциклопедия
КАЛИЙ — КАЛИЙ, калия, мн. нет, муж., и кали, нескл., ср. (араб. поташ) (хим.). Химический элемент щелочный металл серебристо белого цвета, добываемый из углекалиевой соли. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
