Глюкозамин и хондроитин в лечении остеоартроза: данные литературы и результаты собственных исследований | Поворознюк В.В.
Остеоартроз (ОА) – хроническое прогрессирующее дегенеративное заболевание суставов, характеризующееся деградацией суставного хряща с последующими изменениями в субхондральной кости и развитием краевых остеофитов, приводящее к потере хряща и сопутствующему поражению других компонентов сустава (синовиальная оболочка, связки). Отметим, что в иностранной литературе остеоартрит выступает аналогом остеоартроза: тем самым, исследователи подчеркивают роль воспалительного процесса в патогенезе заболевания.
При проведении Международной декады заболеваний костей и суставов (2000-2010) выделены следующие заболевания, имеющие наиболее важное медико-социальное значение для общества: остеоартрит (остеоартроз), остеопороз, боль в нижней части спины, ревматоидный артрит, травматические повреждения. По влиянию на состояние здоровья ОА занимает среди всех заболеваний 4-е место у женщин и 8-е у мужчин. Среди основных факторов риска заболевания – возраст, ожирение и травматическое повреждение сустава.Отличительной особенностью данных рекомендаций является то, что впервые указано модифицирующее действие на суставной хрящ таких лекарственных средств, как глюкозамин и ходроитин [8,15].
1. Симптоматические средства быстрого действия (НПВП, ацетоминофен, опиоидные анальгетики, кортикостероиды и др.), которые оказывают влияние на клинические симптомы заболевания (боль, воспаление и др.).
2. Модифицирующие средства замедленного действия (глюкозамин, диацереин, хондроитин, гиалуроновая кислота, неомыляемые соединения авокадо и сои), эффект которых проявляется более медленно по сравнению с симптоматическими средствами и длится после окончания их применения. Данные фармакологические агенты обладают хондромодифицирующим действием, предупреждая деградацию суставного хряща.
глюкозамина и хондроитина
Глюкозамин (ГК), образующийся в организме в виде глюкозамина 6-фосфата (ГК6-Ф), является фундаментальным строительным блоком, необходимым для биосинтеза таких соединений, как гликолипиды, гликопротеины, гликозоаминогликаны, гиалуронат и протеогликаны. В связи с этим ГК – компонент клеточных мембран и клеточных поверхностных белков, а также промежуточных структурных молекул, соединяющих клетки. Непосредственно или косвенно глюкозамин играет роль в формировании суставных поверхностей, сухожилий, связок, синовиальной жидкости, кожи, костной ткани, ногтей, клапанов сердца, кровеносных сосудов и слизистой секреции пищеварительных, дыхательных и мочевых трактов.
Первичная биологическая роль ГК в прекращении или предупреждении дегенерации сустава непосредственно обусловлена его способностью действовать как эссенциальный субстрат для стимулирования биосинтеза гликозоаминогликанов и гиалуроновой кислоты, необходимых для формирования протеогликанов, находящихся в структурной матрице сустава. Хондроитин сульфат, абсорбируется ли он неповрежденным или в виде компонентов, обеспечивает дополнительный субстрат для формирования здоровой суставной матрицы.
Механизм действия ХС подобен ГК, так как он может также обеспечить субстрат для синтеза протеогликанов. ГК и ХС оказывали in vitro стимулирующее влияние на продукцию протеогликанов культурой дифференцированных человеческих хондроцитов, на рост и метаболизм гликозоаминогликанов. В условиях эксперимента глюкозамин гидрохлорид, глюкозамин гидройодид и глюкозамин сульфат способствовали существенному увеличению гликозоаминогликанов во внеклеточном матриксе хряща. Хотя хондроитин сульфат также способен положительно влиять на метаболизм гликозоаминогликанов, его эффект был менее существенным.
Глюкозамин и хондроитин в лечении остеоартроза
Проведено много исследований по изучению эффективности глюкозамина и хондроитина в лечении остеоартроза коленных и тазобедренных суставов. Результаты исследований были обобщены в обзорах и мета-анализах Leeb B.F. et al. [10], McAlindon T.E. et al. [11], Richi F. et al. [17], Towheed T.E. et al., [18]. Вехой в исследовании эффективности глюкозамина в лечении ОА коленных суставов называют результаты исследования профессора Jean Reginster и его коллег из Льежского университета (Бельгия), опубликованные в журнале Lancet в 2001 году [16]. В трехлетнем исследовании принимали участие 212 пациентов с ОА коленных суставов, рандомизированных в две группы: принимающих 1500 мг в день глюкозамина сульфата или плацебо. Через три года в группе плацебо отмечали существенное ухудшение клинико-рентгенологических признаков, в то время как в группе пациентов, принимающих глюкозамина сульфат, наблюдалось достоверное снижение выраженности болевого синдрома по шкале WOMAC. Измерение величины межсуставной щели показало прогрессивное ее сужение (на 0,31 мм) в группе плацебо и отсутствие изменений в группе больных, принимавших глюкозамин сульфат (- 0,06 мм).
Симптоматическая эффективность глюкозамина и хондроитина была доказана в обзорах Leeb B.F. et al. [10], McAlindon T.E. et al. [11]. В мета-анализе Richi F. et al. [17] показано, что глюкозамин обладает структурно-модифицирующим (при трехлетнем приеме замедляет дегенеративный процесс в суставном хряще) и симптоматическим действием, хондроитин – симптоматическим (оказывает положительное влияние на индекс Лекена, показатели ВАШ). При этом безопасность при приеме была превосходной как для глюкозамина, так и хондроитина.
Пациенты и врачи часто задавали вопрос: что является более зффективным в лечении остеоартроза – глюкозамин, хондроитин или их комбинация? Ответ был получен после завершения первого этапа мультицентрового, двойного слепого плацебо- и целекоксиб-контролируемого исследования (GAIT – Glucosamine/chondroitin Arthritis Intervention Trial) [6], результаты которого были доложены на X Мировом конгрессе OARSI по остеоартрозу (Бостон, 8-11 декабря 2005 год). Исследование проводилось в 16 центрах США под эгидой Национального института здоровья, спонсировалось Национальным центром комплементарной и альтернативной медицины и Национальным институтом артрита, скелетно-мышечных и кожных заболеваний. Было рандомизировано 1583 пациента (средний возраст составил 59 лет) с симптоматическим остеоартрозом коленных суставов. Пациенты были разделены на пять групп: I – 317 больных, принимавших 1500 мг в день (по 500 мг три раза) глюкозамина гидрохлорида, II – 318 больных, принимавших 1200 мг в день (по 400 мг три раза) хондроитин сульфата, III – 317 больных, принимавших комбинацию (1500 мг глюкозамина гидрохлорида и 1200 мг хондроитин сульфата в день), IV – 318 больных, принимавших 200 мг целекоксиба ежедневно, V – 313 больных группы плацебо. Прием препаратов длился в течение 24 недель. Всем пациентам разрешалось принимать до 4000 мг в день ацетаминофена в качестве анальгезирующего средства. Первичным критерием оценки эффективности лечения было 20%-ное снижение выраженности болевого синдрома в коленных суставах через 6 месяцев. По выраженности болевого синдрома пациенты были разделены на две группы: незначительный (по шкале WOMAC 125-300 мм) – 1229 человек, от умеренного до выраженного (по шкале WOMAC 300-400 мм) – 354 человека.
По результатам проведенного исследования в целом в группе обследованных глюкозамин, хондроитин и их комбинация не были достоверно лучше по сравнению с влиянием плацебо на выраженность болевого синдрома. Однако в группе больных с выраженностью болевого синдрома от умеренного до выраженного прием глюкозамина гидрохлорида в комбинации с хондроитин сульфатом приводил через 6 месяцев к достоверному снижению выраженности болевого синдрома по сравнению с группой плацебо (20% снижение боли у 79,2% пациентов по сравнению с 54,3% пациентами в группе плацебо, p=0,002). Только глюкозамин гидрохлорид (65,7% и 54,3%, p=0,17), хондроитин сульфат (61,4% и 54,3%, p=0,39 и целекоксиб (69,4% и 54,3%, p=0,06) достоверно не превышали эффективность плацебо в лечении болевого синдрома в коленных суставах у больных с остеоартрозом. Подобные результаты были получены и при использовании критериев OMERACT-OARSI. Побочные эффекты были незначительны и равномерно распределялись между обследуемыми группами.
Таким образом, исследование GAIT продемонстрировало, что только глюкозамина гидрохлорид в комбинации с хондроитин сульфатом является эффективным средством в лечении болевого синдрома в коленных суставах от умеренного до выраженного [6]. Через 12 месяцев ожидаются результаты оценки структурно-модифицирующего действия на хрящевую ткань указанных средств в исследовании GAIT.
В отделе клинической физиологии и патологии опорно-двигательного аппарата Института геронтологии АМН Украины проведено исследование эффективности препарата Терафлекс, который содержит 500 мг глюкозамина гидрохлорида и 400 мг хондроитин сульфата [Поворознюк В.В., Григорьева Н.В., 2004]. В исследуемую группу вошли 38 женщин в возрасте 52,7±8,4 года с остеоартрозом коленных суставов II-III степени (по классификации Келгрена-Лоуренса). Все пациентки жаловались на боли в коленных суставах, у 23 из них (60,5%) отмечалось ограничение подвижности в суставах. Группу контроля составили 25 пациенток с аналогичным диагнозом в возрасте 51,8±6,2 года, леченные по традиционной схеме, включающей НПВП (диклофенак) в течение первых 2 недель, индивидуальный комплекс лечебной физкультуры, физиотерапевтические мероприятия. В исследуемой группе традиционная схема лечения была дополнена приемом Терафлекса. Препарат назначался в течение первого месяца по одной капсуле три раза в день, затем по одной капсуле два раза в день. Общая длительность курса лечения составляла 6 мес. Оценка эффективности проводилась с использованием Мак-Гилловского опросника боли, ВАШ, альгофункционального индекса Лекена. У больных, принимавших Терафлекс, отмечено достоверное снижение выраженности болевого синдрома, показателей альгофункционального индекса Лекена через 3 мес. лечения, которое сохранялось при продолжении курса терапии до 6 мес. (рис. 1,2). После приема препарата не выявлено побочных эффектов .
Таким образом, длительный прием Терафлекса способствует снижению выраженности болевого синдрома при остеоартрозе коленных суставов, повышению их функциональных возможностей, улучшению качества жизни.
Открытое рандомизированное исследование эффективности препарата Терафлекс у больных с остеоартрозом коленных и тазобедренных суставов, проведенное в Институте ревматологии РАМН также показало, что препарат является эффективным средством для лечения ОА крупных суставов [1]. В указанном исследовании подтверждено симптом-модифицирующее действие Терафлекса: препарат в дозе две капсулы в сутки эффективно уменьшал боль, сохранял и улучшал функцию суставов, позволял снизить дозу применяемых НПВП.
Существенное постарение населения предопределяет увеличение числа больных с остеоартрозом. Своевременная диагностика, целенаправленное лечение и использование модифицирующих средств (глюкозамина и хондроитина) будут способствовать предотвращению инвалидизации, улучшению качества жизни, активному долголетию.
Литература
1. Беневоленская Л.И., Алексеева Л.И., Зайцева Е.М. Эффективность препарата Терафлекс у больных с остеоартрозом коленных и тазобедренных суставов (открытое рандомизированное исследование) // Русский медицинский журнал – 2005. – 13 (8). – С 525-527.
2. Поворознюк В.В. Остеоартроз: современные принципы лечения //Здоровье Украины – 2003 (ноябрь).
3. Поворознюк В.В., Григорьева Н.В. Менопауза и костно-мышечная система – Київ, 2004 – С 512.
4. American College of Rheumatology Subcommittee on Osteoarthritis Guidelines. Recommendations for the medical management of osteoarthritis of the hip and knee: 2000 update // Arthritis Rheum – 2000. – 43. – P 1905-1915.
5. Berman B.M., Bausell R.B., Lee W.L. Use and referral patterns for 22 complementary and alternative medical therapies by members of the American College of Rheumatology: results of a national survey //Arch Intern Med – 2002. – 162. – P 766-770.
6. Clegg D.O., Reda D.J., Harris C. et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis// N Engl J Med. – 2006. – 354. – P 795-808.
7. Hochberg M.C., Altman R.D., Brandt K.D. et al. Guidelines for the medical management of osteoarthritis. II. Osteoarthritis of the knee // Arthritis Rheum – 199. – 38. – P 1541-1546.
8. Jordan K.M., Arden N.K., Doherty M. EULAR recommendations 2003: an evidence based approach to the management of knee osteoarthritis: report of a task force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT) // Ann Rheum Dis — 2003. – 62. – P 1145-1155.
9. Lawrence R.C., Helmick C.G., Arnett F.C. et al. Estimates of the prevalence of arthritis and selected musculoskeletal disorders in the United States // Arthritis Rheum – 1998. – 41. – P 778-799.
10. Leeb B.F., Schweitzer H., Montag K., Smolen J.S. A meta-analysis of chondroitin sulfate in the treatment of osteoarthritis // J Rheumatol – 2000. – 27. – P 205-211.
11. McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis //JAMA – 2000. – 283. – P 1469-1475.
12. Michel B.A., Stucki G., Frey D. Chondroitins 4 and 6 sulfate in osteoarthritis of the knee: a randomized, controlled trial // Arthritis Rheum – 2005. – 52. – P. 779-786
13. Palmer T., Toombs J.D. Managing joint pain in primary care //J Am Board Fam Pract – 2004. – 17. – P 832 – 842.
14. Pavelka K., Gatterova J., Olejarova M. Glucosamine sulfate use and delay of progression of knee osteoarthritis: a 3-year, randomized, placebo-controlled, double-blind study // Arch Intern Med – 2002. – 162. – P 2113-2123.
15. Pendleton A., Arden N., Dougados M. EULAR recommendations for the management of knee osteoarthritis: report of a task force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT) // Ann Rheum Dis – 2000 – 59. – P 936-944.
16. Reginster J.Y., Deroisy R., Rovati L.C. Long-term effects of glucosamine sulphate on osteoarthritis progression: a randomised, placebo-controlled clinical trial //Lancet — 2001. – 357 – P 251-256.
17. Richy F., Bruyere O., Ethgen O. Structural and symptomatic efficacy of glucosamine and chondroitin in knee osteoarthritis: a comprehensive meta-analysis // Arch Intern Med – 2003. – 163. – P 1514-1522.
18. Towheed T.E., Maxwell L., Anastassiades T.P. Glucosamine therapy for treating osteoarthritis // Cochrane Database Syst Rev – 2005. — CD002946-CD002946.
19. Verbruggen G. Chondroprotective drugs in degenerative joint diseases //Rheumatology – 2005. – 45. – P 129-138.
20. Felson D.T. Osteoarthritis of the knee // N Engl J Med – 2006. – 354. – P 841-848.
www.rmj.ru
ИССЛЕДОВАНИЕ: ЭФФЕКТИВНОСТЬ ГЛЮКОЗАМИНА-ХОНДРОИТИНА ДЛЯ СУСТАВОВ
Многоцентровое рандомизированное двойное слепое исследование для сравнения эффективности комбинации хондроитин сульфата и глюкозамина с эффективностью целекоксиба в лечении остеоартрита коленного сустава с болью средней и тяжелой степени.

Целекоксиб относится к группе НПВП (НПВС) — нестероидных противовоспалительных препаратов. Действие НПВП направлено на снятие симптомов воспаления, однако НПВП могут оказывать неблагоприятное воздействие на сердечно-сосудистую систему и желудочно-кишечный тракт, что вызывает опасения относительно их длительного применения. Комбинация глюкозамин-хондроитин десятилетиями применялась как натуральная альтернатива лекарственным препаратам, применяемым в терапии артрита.
Исследование опубликовано 14 января 2015 г. Проводилось во Франции, Германии, Польше, Испании, Канаде, США, Англии, Бельгии.
606 пациентов были разделены 2 группы. Первая группа принимала 400 мг хондроитин сульфата плюс 500 мг глюкозамина гидрохлорида три раза в день. Вторая группа принимала 200 мг целекоксиба. 6 месяцев.
Оценивались: уровень боли, скованность сустава, подвижность сустава, выпот (скопление биологической жидкости в зоне воспаления) и потребность в обезболивающих препаратах.
В конце испытания в обеих группах показатели боли снизились на 50%. Все анализы чувствительности соответствовали этому результату. Скованность сустава снизилась на 46,9% в группе глюкозамина-хондроитина и на 49,2% в группе целекоксиба. В обеих группах наблюдалось уменьшение отека и выпота в суставах на 50% и более.
ВЫВОДЫ:
Комбинация хондроитин сульфат и глюкозамин обладает эффективностью сравнимой с целекоксибом в снижении боли, ригидности (снижении подвижности сустава в результате образования рубцовых тканей), функциональных ограничений и отека/выпота в суставах через 6 месяцев у пациентов с болезненным остеоартритом коленного сустава. Глюкозамин-хондроитин имеют хороший профиль безопасности.
«Эти результаты подтверждают, что сочетание хондроитин сульфата и глюкозамина гидрохлорида оказалось не уступающим целекоксибу в возможности снижения боли», — заключают авторы исследования Марк Хохберг из Университета Мэриленда и его коллеги.
Как принимать глюкозамин-хондроитин
Согласно указаниям на упаковке (эталонные дозы — у таких мировых производителей как Now Foods, Doctor’s Best, MRM).
Продолжительность приема глюкозамина-хондроитина
Для профилактики заболеваний: 3 месяца. Через 3 месяца перерыва курс повторять, и так постоянно (2 курса в год).
В лечебных целях: 3-6 месяцев. Курсы повторять. При необходимости можно принимать практически постоянно.
Глюкозамин-хондроитин хорошо сочетается с любыми другими добавками (бадами). Также можно применять одновременно с НПВП.

Купить глюкозамин-хондроитин на iHerb



В моей АВТОРСКОЙ БАЗОВОЙ СХЕМЕ БАДОВ можно найти лучшие, на мой взгляд, препараты глюкозамина-хондроитина и пример их сочетаемости с другими добавками для суставов). Я выбрала для своей схемы препараты глюкозамина-хондроитина с MSM (метилсульфонилметаном). MSM – это сероорганическое соединение с выраженным противовоспалительным действием.
Можно усилить позиции серы в препаратах глюкозамина-хондроитина с MSM, принимая серу дополнительно. В профилактических и лечебных целях можно принимать до 2-3 граммов MSM. Считается, что 3 грамма MSM — оптимальная цифра, чтобы почувствовать эффект на суставах.

Купить MSM (МСМ, метилсульфонилметан) на iHerb

Также находим мои посты с добавками и наружными средствами для суставов:
ЧТО ЕЩЕ Я ПРИНИМАЮ, КРОМЕ БАЗОВОЙ СХЕМЫ БАДОВ (ЦЕЛАДРИН, ХОНДРОПРОТЕКТОРЫ 4 В 1)
ДОБАВКИ ДЛЯ КОСТЕЙ, СУСТАВОВ И КРАСОТЫ. А ТАКЖЕ АНАЛОГ ГЕПТРАЛА
БОМБОВОЕ ИССЛЕДОВАНИЕ: КОЛЛАГЕН ДЛЯ СИНТЕЗА СОБСТВЕННОГО КОЛЛАГЕНА И КАК АНТИОКСИДАНТ. КАК РАБОТАЕТ КОЛЛАГЕН
ЗЕЛЕНЫЕ МИДИИ ДЛЯ СУСТАВОВ
ЛЮБИМЕЦ ГОМЕОПАТОВ, ИСПОЛЬЗУЕМЫЙ ДОКАЗАТЕЛЬНОЙ МЕДИЦИНОЙ. ПРОТИВ БОЛИ И АРТРИТОВ
КРЕМ ДЛЯ СУСТАВОВ И МЫШЦ
Обсуждения на моей стене в ВКонтакте глюкозамина в контексте сахарного диабета


© Данная публикация является объектом авторских прав. Использование разрешено только с указанием автора и источника в виде активной ссылки.
Публикация ссылается на исследование:
Combined chondroitin sulfate and glucosamine for painful knee osteoarthritis: a multicentre, randomised, double-blind, non-inferiority trial versus celecoxib.
 Обо мне: МАРИНА ХАЙФА И БЛОГ «ВЕЧНАЯ МОЛОДОСТЬ».
Обо мне: МАРИНА ХАЙФА И БЛОГ «ВЕЧНАЯ МОЛОДОСТЬ».Другие мои публикации на тему исследований.
marinahaifa.com
Систематический анализ исследований противоопухолевых эффектов хондропротекторов глюкозамина сульфата и хондроитина сульфата | Громова О.А., Торшин И.Ю., Лила А.М., Романов И.С., Назаренко А.Г.
В работе представлены результаты систематического анализа фундаментальных и клинических исследований противоопухолевых эффектов глюкозамина сульфата и хондроитина сульфата.
Введение
Стандартизированные фармацевтические формы хондроитина сульфата (ХС) и глюкозамина сульфата (ГС) являются эффективными и безопасными хондропротекторами, позволяющими осуществлять долговременную терапию остеоартрита и других патологий суставов. ХС и ГС способствуют реконструкции соединительнотканной основы хряща и обладают анальгетическим и противовоспалительным действием. Взаимодействуя с рецепторами CD44, TLR4 и ICAM1 на поверхности различных клеток, ХС и ГС ингибируют провоспалительный транскрипционный фактор NF-kB и цитокиновый сигнальный путь JAK/STAT. Поэтому стандартизированные формы ХС/ГС наряду нестероидными противовоспалительными препаратами (НПВП) могут использоваться в терапии не только патологии суставов [1], но и других заболеваний, в патогенезе которых имеется компонент хронического воспаления.Важными перспективными направлениями применения ХС/ГС являются долговременная профилактика и адъювантная терапия опухолевых заболеваний. Эти фармакологические эффекты ХС/ГС известны достаточно давно: первые работы, посвященные ингибированию роста опухолей глюкозамином, были опубликованы еще в начале 1950-х гг. [2–4]. Противоопухолевое действие ХС/ГС обусловлено, в частности, тем, что ХС и ГС способствуют снижению хронического воспаления, в т. ч. опосредованного фактором некроза опухолей (ФНО).
Хемореактомный анализ молекулы показал, что ГС и самостоятельно, и в сочетании с НПВП проявляет следующие биологически активные свойства: 1) ингибирует белки метаболизма простагландинов и лейкотриенов,
2) ингибирует провоспалительный эффект транскрипционного фактора NF-kB, участвующего в осуществлении действия ФНО-α, 3) снижает экспрессию провоспалительных цитокинов в культуре клеток, 4) ингибирует различные матриксные металлопротеиназы, 5) обладает вазодинамическими и антидиабетическими эффектами в отношении культуры клеток [5]. Эти эффекты важны для профилактики и терапии опухолевых заболеваний.
Хемотранскриптомный анализ молекулы ГС при воздействии на фибробласты линии FIBRNPC показал, что ГС не только ингибирует активность NF-kB и других провоспалительных белков, но и способствует снижению транскрипции генов, вовлеченных в провоспалительный сигнальный каскад NF-kB (NFKB2, TNFRSF1B, PYCARD, TRAF2, TNFSF12 и др.) и генов белков, осуществляющих передачу сигнала на разных уровнях каскада NF-kB (CD44, TLR4, ICAM1, NF-kB, JAK/STAT и др.). ГС может в существенной мере снижать экспрессию генов, вовлеченных в процесс деления клетки и транскрипцию генов [6]. Комплексное противовоспалительное и цитостатическое действие ГС является патогенетическим при лечении не только остеоартрита, но и коморбидных заболеваний, сопровождающихся хроническим воспалением, в т. ч. опухолевых заболеваний.
В настоящей работе представлен систематический анализ противоопухолевых эффектов ХС/ГС. Количество публикаций по данному вопросу достаточно велико: например, только по запросу «(Cancer OR cancers OR tumor OR tumors OR tumour OR tumours) AND (glucosamine OR chondroitin)» в базе данных биомедицинских публикаций PUBMED найдено 5129 ссылок, из них по эффектам ГС — 2659 ссылок. В рамках настоящей работы мы осуществили компьютеризованный анализ данного массива публикаций с использованием современных методов анализа больших данных [7, 8], развиваемых в рамках топологического [9] и метрического [10, 11] подходов к задачам распознавания/классификации [12, 13]. В качестве контрольной выборки публикаций использовались 5129 случайно выбранных статей из 4 226 339 найденных по запросу «(Cancer OR cancers OR tumor OR tumors OR tumour OR tumours) NOT glucosamine NOT chondroitin» в базе данных PUBMED. В результате проведенного анализа текстов были отобраны наиболее информативные ключевые слова, описывающие взаимосвязь ХС/ГС с патофизиологий и клиникой опухолевых патологий (табл. 1).
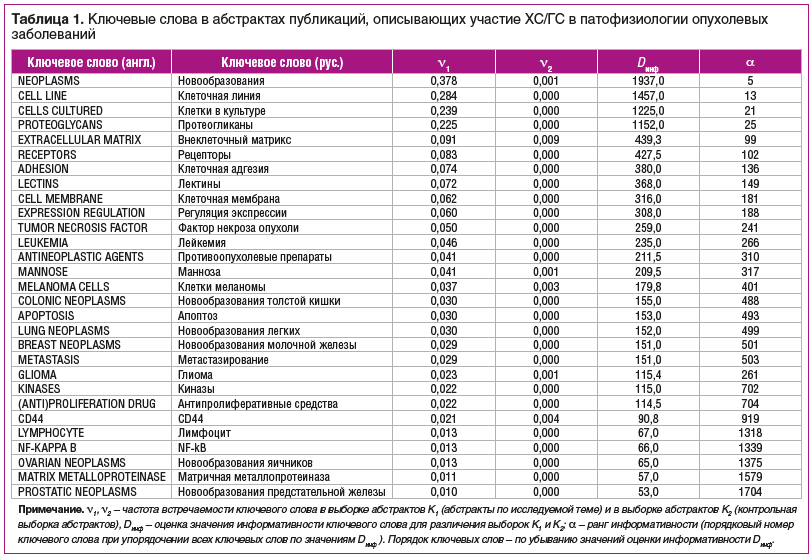
Анализ полученного списка наиболее информативных ключевых слов (табл. 1), составленного на основе анализа всего массива публикаций результатов клинических, биохимических, экспериментальных исследований ХС/ГС, позволяет утверждать, что ХС/ГС, участвуя в формировании протеогликанов внеклеточного матрикса, лектинов и в клеточной адгезии, также влияют на формирование новообразований и метастазирование опухолей различных типов (лейкемия, меланома, глиома, новообразования толстой кишки, легких, молочной железы, яичников, предстательной железы).
Важными молекулярными механизмами противоопухолевого действия ХС/ГС, приводящими к апоптозу линий опухолевых клеток, являются активация рецептора CD44 (приводящая к ингибированию эффектов NF-kB, фактора некроза опухоли, матричных металлопротеиназ), гликозилирование рецепторов, регуляция экспрессии генов. Поэтому ХС/ГС могут являться ценным дополнением к адъювантной терапии с использованием противоопухолевых препаратов, в т. ч. антипролиферативных средств и ингибиторов различных киназ.
Дальнейший анализ информативных ключевых слов с последующей рубрикацией текстов исследований по диагнозам МКБ-10 позволил охарактеризовать опухолевые патологии, ассоциированные с нарушениями обмена ХС/ГС и описанные в исследуемый выборке из 5129 публикаций (рис. 1).
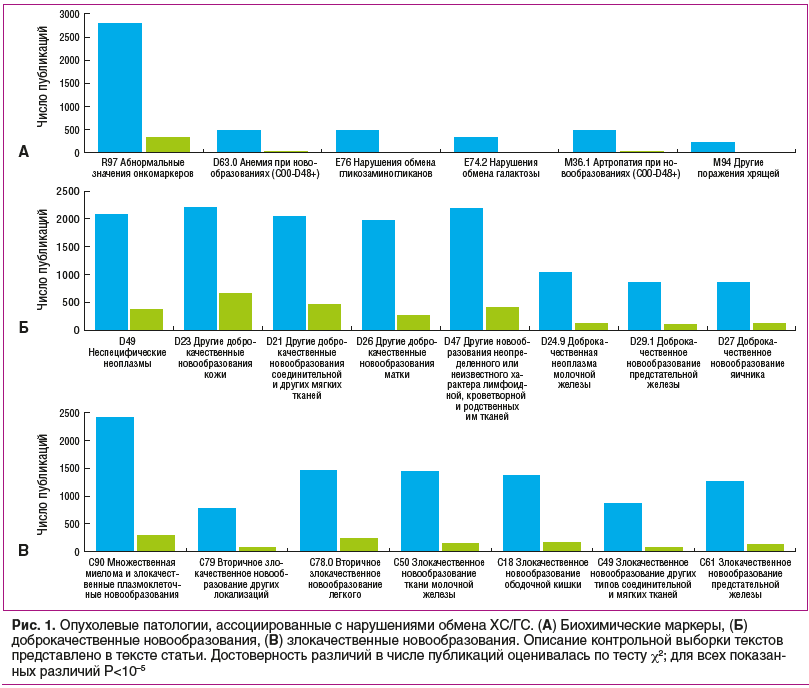
Далее мы последовательно рассмотрим молекулярные механизмы противоопухолевого действия ГС, механизмы противоопухолевого действия ХС (в частности, роли паттернов сульфатирования ХС) и результаты нескольких крупномасштабных клинико-эпидемиологических исследований противоопухолевых эффектов ХС/ГС.
Молекулярные механизмы противоопухолевого действия ГС: воздействие на провоспалительные цитокины
В эксперименте пероральный прием олигомеров ГС и N-ацетил-D-глюкозамина приводил к торможению развития опухолей. По сравнению с контролем олигомеры ГС значительно подавляли рост опухоли у мышей и стимулировали выраженный апоптоз опухолевых клеток на фоне более высоких уровней интерлейкина-12 и интерферона-гамма, что указывает на активацию врожденного противоопухолевого иммунитета [14].ГС ингибирует экспрессию ЦОГ-2 и провоспалительного интерлейкина ИЛ-8 в клетках линии MCF-7 рака молочной железы человека. ГС эффективно подавляет активацию экспрессии генов ЦОГ-2 и ИЛ-8, вызываемую протеинкиназой С (РКС), синтез простагландина Е2 и ИЛ-8. ГС также способствовал деградации белков ЦОГ-2 и ИЛ-8 кальпаин-зависимым и протеасом-зависимым образом при участии сигнального пути NF-kB. ГС ослаблял PKC-опосредованное фосфорилирование, снижая активацию NF-kB через рецептор CD44, что значительно ингибировало рост трансплантатов рака молочной железы в эксперименте [15]. ГС также ингибирует опосредованную IL-1-бета продукцию IL-8 в клеточных линиях DU-145 и PC-3 рака предстательной железы [16].
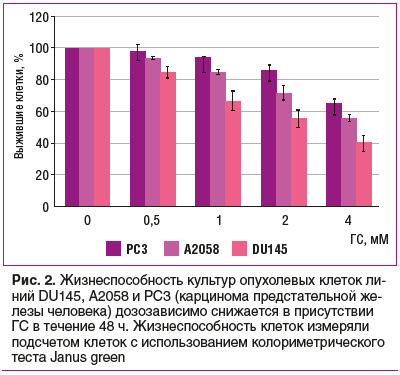
Противоопухолевая активность ГС проявляется посредством ингибирования глобального N-связанного гликозилирования — посттрансляционной модификации, которая важна для стабильности и функции внутриклеточных белков. Клетки линии DU145 (карцинома предстательной железы человека) экспрессируют IL-6, что активирует передачу сигналов по каскаду IL-6/STAT3. Субъединицы рецептора IL-6 (белок gp130) подвергаются N-гликозилированию. ГС уменьшал N-гликозилирование рецепторов gp130, связывание IL-6 с клетками и фосфорилирование сигнальных белков JAK2, SHP2 и STAT3 [17], что способствовало снижению популяции опухолевых клеток 3 исследованных линий (рис. 2). Инактивируя белок STAT3, ГС также снижает жизнеспособность клеток — предшественников рака молочной железы человека [18].
Противораковое действие ГС также проявляется посредством индуцированной глюкозамином модификации O-гликозилирования, что приводит к ингибированию фосфорилирования сигнальным белком FOXO и, как результат, ингибированию активности сигнальных путей PI3K/AKT и MAPK/ERK [19].
Молекулярные механизмы противоопухолевого действия ГС: другие механизмы
Помимо воздействия на гликозилирование и ингибирования NF-kB, приводящего к ослаблению эффектов ФНО-α и других провоспалительных цитокинов, противоопухолевые эффекты ГС могут осуществляться и посредством других молекулярных механизмов.Например, ГС ингибирует метаболизм тимидина в опухолевых клетках. Глюкозамин ингибирует поглощение тимидина, фосфорилирование тимидина и увеличивает утечку тимидина во внеклеточное пространство. Глюкозамин также напрямую ингибирует фермент тимидинкиназу [20]. Уменьшая доступный для опухоли пул уридиновых нуклеотидов, эти эффекты ГС способствуют гибели опухолевых клеток [21].
Антипролиферативное действие ГС в опухолевых клетках связано с остановкой цикла клеточного деления в фазе G0/G1. ГС дозозависимо ингибировал пролиферацию опухолевых клеток линий 786-O и Caki-1 рака почки (рис. 3) и стимулировал апоптоз опухолевых клеток. Экспрессия регуляторных белков Cyclin D1, CDK4 и CDK6, которые способствуют фазовому переходу G1/S во время пролиферации, была значительно подавлена на фоне повышения уровней ингибиторов клеточного цикла p21 и p53 [22].

Производное глюкозамина (молекула NCPA) индуцирует экспрессию ингибитора сериновой протеазы Maspin — белка-супрессора опухолей при различных типах рака, в т. ч. при раке простаты. Производное глюкозамина блокирует пролиферацию клеток линии PC3, не чувствительных к андрогенам, ингибируя продукцию циклина-D1 и индуцируя апоптоз опухолевых клеток [23].
ГС стимулирует гибель опухолевых клеток посредством ингибирования протеасом. В клетках рака предстательной железы человека линии ALVA41 ингибирование протеасомной активности приводило к накоплению убиквитинированных белков с последующей индукцией апоптоза. ГС снижал активность PA28 — белка — активатора протеасом через O-гликозилирование белков [24].
ГС вызывает аутофагическую гибель опухолевых клеток посредством стимуляции стресса в эндоплазматическом ретикулуме (ЭР-стресс) опухолевых клеток. В экспериментах на культуре клеток глиомы человека линии U87MG ЭР-стресс, вызванный ГС, проявлялся в индукции экспрессии генов BiP, IRE1-альфа и фосфо-eIF2-альфа, что соответствует торможению пролиферации и инициации апоптоза опухолевых клеток [25].
Производное ГС, фенилглюкозамин, инактивирует рецептор андрогенов в опухолевых клетках мочевого пузыря при участии микроРНК mir-449a, что снижает пролиферацию андроген-зависимых клеток карциномы мочевого пузыря [26].
В клетках линий DU145 (рак предстательной железы) и MDA-MB-231 (рак молочной железы) ГС тормозит пролиферацию посредством ингибирования p70S6K —
сигнального белка, участвующего в трансляции всех белков. Глюкозамин уменьшал фосфорилирование белка p70S6K и его субстратов RPS6 и eIF-4B. Кроме того, глюкозамин усиливал эффекты ингибирования пролиферации рапамицином, специфическим ингибитором белка mTOR [27].
N-ацетилглюкозамин стимулирует апоптоз клеток опухолей легкого посредством фактора TRAIL и активации белка DR-5. Белок TRAIL является потенциальным противораковым агентом. Однако многие клетки немелкоклеточного рака легких (NSCLC) частично устойчивы к TRAIL, что ограничивает его клиническое применение. В эксперименте совместное применение белка TRAIL и N-ацетилглюкозамина увеличивало накопление и кластеризацию DR5, что, в свою очередь, активировало проапоптотическую каспазу-8. N-ацетилглюкозамин способствовал кластеризации рецептора DR5 путем улучшения его O-гликозилирования [28].
Молекулярные механизмы противоопухолевого действия ХС
ХС ингибирует пролиферацию клеток посредством (1) увеличения экспрессии ингибитора циклин-зависимой киназы (CDKN1, белок p21), (2) увеличения апоптоза за счет активации каспазы-3, (3) подавления экспрессии фактора роста эндотелия сосудов (VEGF), (4) увеличения экспрессии тканевого ингибитора металлопротеиназы-1 (TIMP-1) и подавления матриксных металлопротеиназ. Эти эффекты, сопровождающиеся значительным ингибированием сигнального пути NF-kB [29], характерны и для ГС, и для ХС.Одним из важных аспектов противоопухолевого действия ХС является инкапсуляция опухолей. Микроокружение опухоли является привлекательной терапевтической мишенью для лечения рака. Эндогенный ХС как часть клеточной микросреды состоит из длинных линейных цепочек повторяющихся дисахаридных звеньев, ковалентно связанных с белками с образованием ХС-протеогликанов [30].
Резко повышенные уровни ХС наблюдаются в стромальном компартменте многих солидных опухолей, включая рак молочной железы. Это обусловлено, по всей видимости, тем, что ХС ингибирует инвазию опухоли и защищает окружающие ткани от метастазирования. Например, в моделях опухолей мозга ХС-протеогликаны вызывают выход реактивных астроцитов из опухолевой массы, что приводит к инкапсуляции опухолевых поражений. Формирующаяся астроглиотическая капсула ингибирует инвазию опухоли [31].
В эксперименте было показано, что разрушение капсулы, сформированной из ХС вокруг новообразований, ускоряет рост опухолей и способствует метастазированию. Например, ферментативная элиминация эндогенного ХС, проводимая посредством внутриопухолевых инъекций хондроитиназы ABC, приводила к увеличению метастазирования и ускоренному росту вторичных опухолей [30].
Эксперименты на культуре клеток также подтверждают противоопухолевые эффекты ХС. Дисахариды ХС показали противоопухолевый потенциал по отношению к клеткам рака толстой кишки человека [32]. В экспериментах на клетках линии HT-1376 (опухоли мочевого пузыря) ХС усиливает противоопухолевую активность гемцитабина и митомицина-С. ХС приводил к ингибированию роста опухолевых клеток на 50% через 72 ч. Комбинация ХС + гемцитабин в соотношении 1:1 индуцировала апоптоз опухолевых клеток посредством активации каспазы-9 и каспазы-3 [33].
Паттерны сульфатирования и противоопухолевое действие ХС
Противоопухолевые эффекты эндогенных и экзогенных ХС могут зависеть от паттернов сульфатирования ХС. Начальная стадия инвазии состоит в прикреплении опухолевой клетки к внеклеточному матриксу через эндогенные молекулы ХС. При этом образуется С-концевой внутриклеточный фрагмент N-кадгерина, взаимодействующий с бета-катенином. Эти эффекты существенно зависят от длины цепи и характера сульфатирования молекулы ХС. Делеция гена хондроитин-4-O-сульфотрансферазы-1 (C4ST-1), который увеличивает 4-O-сульфатирование ХС и длину цепи ХС, подавляет активацию пути N-кадгерин /бета-катенин посредством эндоцитоза N-кадгерина и значительно уменьшает инвазию клеток BT-549 [34].Следует отметить, что во время прогрессирования и метастазирования рака эндогенные ХС в строме опухолей претерпевают аномальные изменения в составе и в структуре: уменьшается соотношение между дерматансульфатом и ХС, изменяется паттерн сульфатирования ХС [35]. В опухолевых клетках наблюдаются нарушения экспрессии различных ферментов, синтезирующих эндогенные ХС и дерматан сульфаты. В частности, повышается экспрессия дерматансульфат-эпимеразы, хондроитин-синтазы I, хондроитин-4-сульфотрансфераз CHST11, CHST12 и CHST15 [36], фактора полимеризации хондроитина в опухолях и снижается экспрессия хондроитин-6-сульфотрансферазы 3 [37].
Клинические исследования показали, что пациенты с опухолями шеи выделяют с мочой ХС низкой степени сульфатирования [38]. Отмечена корреляция между содержанием несульфатированных дисахаридов и стадией прогрессирования опухолей [39]. Повышенная экспрессия несульфатированного хондроитина коррелирует с неблагоприятными клинико-патологическими параметрами при раке предстательной железы, включая более тяжелую стадию заболевания, более высокий балл по шкале Глисона и более высокий уровень простатспецифического антигена (ПСА) [40].
Таким образом, особенности сульфатирования ХС связаны с состоянием пациентов с опухолевыми заболеваниями. Систематический экспериментальный анализ дисахаридов ХС, проведенный в исследовании [41], позволил выявить паттерны сульфатирования ХС, которые способствуют ингибированию опухолей молочной железы. Для этого были синтезированы молекулы дисахаридов ХС, соответствующие 16 возможным паттернам сульфатирования, затем было изучено их влияние на опухолевые клетки [41]. Результаты показали достоверное увеличение активности каспазы-3 и каспазы-7 при обработке клеток линии MDA-MB-231 (рак молочной железы) ди- и трисульфатированными дисахаридами ХС.
Первичные карциномы яичников и их метастазы содержат 4,6-дисульфатированные ХС, которые способствуют адгезии опухолевых клеток [42]. В то же время эксперименты на культуре клеток показали, что хондроитин-4,6-сульфат (известен также как ХС-Е, ХС-4,6) снижает подвижность опухолевых клеток (рис. 4) и ингибирует проонкогенную передачу сигналов по каскаду Wnt/бета-катенин [43].

Торможение активности каскада Wnt — важный механизм противоопухолевого действия дисульфатированного ХС-4,6. В отсутствие стимуляции Wnt3a уровни бета-катенина были низкими и наблюдались в основном в мембране опухолевых клеток линий EMT6 и 4T1 (рак молочной железы, рис. 5). Активация каскада Wnt3a приводила к резкому увеличению уровня бета-катенина в клеточном ядре. Добавление ХС-4,6 к среде значительно снижает уровни бета-катенина, подтверждая, что ХС-4,6 является мощным ингибитором передачи сигналов Wnt/бета-катенин в клетках рака молочной железы [43].
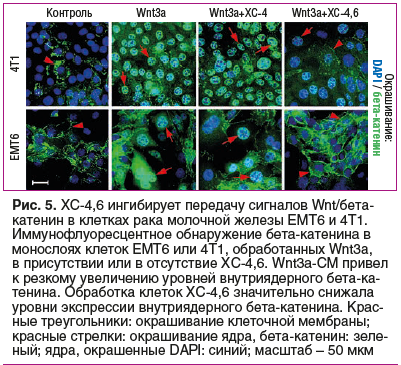
В целом различия в длине цепи и паттерне сульфатирования ХС оказывают влияние на проявление противоопухолевых свойств ХС. Оптимальная длина цепей ХС в высокоочищенной фармацевтической субстанции CS Bioactive© (Биоиберика, С.А.У., Испания) обеспечивает медленное высвобождение коротких олигосахаридов. Соотношение различных форм сульфатирования ХС в фармацевтической субстанции CS Bioactive© (Биоиберика, С.А.У., Испания) (60% ХС-4, 30% ХС-6) [44] обеспечивает эффективную работу хондроитиназы, карбогидрат сульфотрансферазы и других ферментов, которые диверсифицируют паттерн сульфатирования синтезируемых из ХС олигосахаридов (способствуя в т. ч. синтезу ХС-4,6). Синтезируемые таким образом дисахариды ХС избирательно накапливаются в опухолевой ткани, проявляя описанные выше эффекты.
Клинико-эпидемиологические исследования противоопухолевых эффектов ХС/ГС
Разносторонние молекулярные механизмы противоопухолевого действия ГС, установленные в ходе фундаментальных исследований, указывают на перспективность использования ХС и ГС в профилактике и терапии опухолевых заболеваний. Очень важной характеристикой молекул ГС и ХС является их таргетное накопление в опухолевой ткани. Например, наногели ХС-метотрексат значительно повышают растворимость и улучшают эффективность доставки метотрексата к опухоли благодаря связыванию ХС с рецептором CD44 [45]. ГС и N-ацетилглюкозамин являются перспективными контрастными веществами для проведения МРТ при визуализации опухолей, т. к. оба вещества нетоксичны и имеют тенденцию дозозависимо накапливаться и удерживаться в области опухоли [46].Результаты крупномасштабного клинического эпидемиологического «Исследования по профилактике рака II» (Cancer Prevention Study II Nutrition Cohort, n=113 067) показали, что регулярное употребление ГС снижает риск развития колоректального рака. За группой наблюдали в течение 10 лет, за этот период было зарегистрировано 1440 случаев заболевания. Прием ГС был ассоциирован с более низким риском заболевания (ОР 0,83; 95% ДИ 0,71–0,97), чем в контрольной группе [47].
Регулярное использование ГС/ХС в крупномасштабном исследовании здоровья медсестер (n=65 000) было ассоциировано с более низким риском заболеваемости колоректальным раком. За 8 лет наблюдений было зарегистрировано 672 случая заболевания. Регулярное потребление ГС было связано с 21% снижением риска (ОР 0,79; 95% ДИ: 0,63–1,00), ХС — с 23% снижением риска (ОР 0,77; 95% ДИ: 0,59–1,01). Ассоциации сохранялись после поправок на пол, использование аспирина, ИМТ, физическую активность, что указывает на антипролиферативный и онкопрофилактический потенциал ХС/ГС [48].
Все описанные выше противоопухолевые эффекты ХС и ГС подразумевают, что используются высокоочищенные формы ХС/ГС. Кроме того, препараты ХС должны быть стандартизированы по молекулярной массе и по паттернам сульфатирования. Наличие в препаратах ХС/ГС посторонних примесей (особенно белкового происхождения) будет провоцировать развитие аутоиммунных реакций, препятствующих развитию противовоспалительного и противоопухолевого эффектов ХС и ГС [49], приводить к вторичному синовиту [50] и др.
Посторонние белковые примеси в составе нестандартизированных экстрактов ХС природного происхождения будут провоцировать развитие провоспалительных реакций. Воспалительные клетки и медиаторы воспаления являются ключевым компонентом микроокружения опухоли и способствуют ее развитию [51]. Собственно, именно поэтому ингибиторы провоспалительных киназ и используются как противоопухолевые средства [52].
Наглядной иллюстрацией опасности использования нестандартизированных препаратов ХС, содержащих посторонние белковые примеси, является опубликованный в литературе случай из практики. Инъекции гликозамингликан-пептидного комплекса (Арумалон) пациентке 62 лет с дегенеративными изменениями тазобедренного сустава привели к тяжелым осложнениям: температура до 39 °С, отеки пальцев, суставов рук и колен, сыпь на коже, повышение уровней лейкоцитов и 2–3-кратное повышение уровней печеночных ферментов в крови. Эффект нестандартизированного препарата ХС был подтвержден положительным тестом на трансформацию лимфоцитов в культуре и наличием специфических антител в культивируемой жидкости лимфоцитов, в то время как сыворотка была отрицательной для антител. Только через 1 год после приема поддерживающей дозы преднизона (15 мг/сут) пациентка полностью избавилась от описанной симптоматики. Таким образом, нестандартизированные препараты ХС, особенно с нестандартизированными белковыми примесями животного происхождения, имеют повышенный риск системных побочных эффектов [53].
Заключение
Такие микронутриенты, как ХС и ГС, оказывают многогранное воздействие на организм. Молекулы ХС и ГС вырабатываются хондроцитами и являются одними из основных структурных компонентов хряща и синовиальной жидкости. Кроме восстановления соединительной ткани ХС и ГС проявляют противоболевой, противовоспалительный, иммуномодулирующий, антипролиферативный и другие эффекты. Противоопухолевое действие ХС/ГС распространяется на различные типы опухолей (глиома, рак толстой кишки, легких, молочной железы, яичников, предстательной железы, почек, мочевого пузыря и др.). И ХС, и ГС взаимодействуют с рецептором CD44, способствуя снижению хронического воспаления, торможению пролиферации и стимулированию апоптоза опухолевых клеток.Кроме того, молекула ГС ингибирует метаболизм тимидина в опухолевых клетках, модулирует процессы гликозилирования белков, тормозит цикл клеточного деления, ингибирует протеасомы, вызывает аутофагическую гибель опухолевых клеток посредством стимуляции стресса в эндоплазматическом ретикулуме, инактивирует рецептор андрогенов, что также способствует специфической противоопухолевой активности.
Молекулы ХС стимулируют апоптоз опухолевых клеток, подавляют экспрессию фактора роста эндотелия сосудов фактор (VEGF) и активность матриксных металлопротеиназ, ингибируют активность каскада Wnt/бета-катенин. Способствуя инкапсуляции опухолевых образований, молекулы ХС тормозят процесс метастазирования. Имеющиеся данные крупномасштабных клинических исследований указывают на перспективность использования ХС/ГС для долговременной профилактики опухолевых заболеваний.
Перспективными направлениями дальнейших исследований являются (1) хемокиномный анализ свойств молекулы ГС, который позволит соотнести эффекты ГС с эффектами известных противоопухолевых препаратов — ингибиторов киназ, (2) хемотранскриптомное исследование эффектов ГС в отношении опухолевых клеток (например, клеток линии MCF7 рака молочной железы), которое позволяет рассмотреть противоопухолевое воздействие ГС на транскриптом опухолевых клеток человека, (3) хемореактомное моделирование эффектов воздействия ГС и молекул сравнения на различные линии опухолевых клеток в культуре.
Работа выполнена при поддержке грантов РФФИ 18–07–01022, 18–07–00944, 16–29–12936.
www.rmj.ru
Новые данные о глюкозамине сульфате Текст научной статьи по специальности «Клиническая медицина»
НОВЫЕ ДАННЫЕ О ГЛКЖОЗАМИНЕ СУЛЬФАТЕ ПРИ ОСТЕОАРТРОЗЕ
М.Аннефельд Rotta Reesearch Laboratorium, Монза, Италия
Остеоартроз и роль глюкозамине сульфата
Остеоартроз (ОА) — дегенеративное заболевание суставов, развивающееся практически во всех периферических (синовиальных) суставах чел. ОА считается органным заболеванием, в развитии которого участвуют дегенеративные процессы, затрагивающие различные ткани сустава, включая субхондраль-ную кость, синовиальную оболочку и особенно — суставной хрящ, являющийся основным объектом развития данного заболевания, при этом патогенетические механизмы ОА (биомеханические, биохимические и др.) остаются относительно малоизученными.
Основными проявлениями ОА являются боль и ограничение функции сустава, а также патологические изменения его структуры. К сожалению, корреляция между клиническими проявлениям и морфологическими изменениями при ОА выражена слабо, особенно на ранних стадиях заболевания. Однако на конечных стадиях оба фактора приобретают степень крайней выраженности, определяющей исход ОА, требующий хирургического лечения — обычно эндопротезирования сустава.
Наиболее правильным при оценке выраженности ОА является учет не только субъективных показателей (в частности, боли при движениях), но и состояния структур, образующих сустав.
Среди взрослых американцев (старше 30 лет) симптомы поражения коленного сустава фиксируется приблизительно у 6%, а тазобедренного — приблизительно у 3%[1).Таккак ОА является заболеванием, распространенность которого увеличивается с возрастом, по мере старения населения его частота нарастает. Результаты эпидемиологических исследований показывают, что заболеваемость и распространенность ОА возрастают в 2-10 раз в возрастных группах от 30 до 64 лет, при этом рост не прекращается и в более старшем возрасте (2]. В целом, частота артроза коленного сустава (гона-ртроза) выше, чем тазобедренного; характерные для ОА рентгенографические изменения в коленном суставе обнаруживаются у 5-15% американцев и европейцев в возрасте 35-74 лет [3]. В плане инвалидизации населения вклад гона-ртроза сопоставим с сердечно-сосудистыми заболеваниями и выше вклада других болезней, характерных для пожилого возраста [4].
В течение последнего десятилетия исследования в области фармакотерапии ОА велись в двух основных направлениях:!) разработка сильнодействующих и относительно безопасных симптоматических препаратов, которые могут неспецифически контролировать некоторые симптомы заболевания, но которые не устраняют прогрессирования болезни (например селективные нестероидные противовоспалительные препараты (НПВП), включая коксибы) и 2) разработка препаратов, влияющих на симптомы заболевания и структурные изменения в суставе. Оиокозамин сульфат является одним из препаратов второй группы.
В ходе исследований был выяснен механизм действия глюкозаминосульфата при ОА. Установлено, что глюкозамино-сульфат биодоступен для суставных тканей, включая хрящ, после системного (орального) введения препарата [5]. Именно глюкозамин сульфат встраивается хондроцитами в компоненты глюкозаминосульфатных цепей непораженной хрящевой ткани [6]. Кроме того, глюкозамин сульфат стимулирует синтез физиологических протеогликанов и снижает активность катаболических ферментов, включая металлопротеина-зы [7,8,9].
Показано, что под влиянием глюкозамина сульфата оказывается обратимым процесс интерлейкин-1 (ИЛ-1) ингибиции синтеза суставного хряща 110]. Этот цитокиновый антагонизм является результатом ингибирования ИЛ-1-зависимой внутриклеточной передачи сигнала в хондроцитах, в частности, через подавление активации NF-kВ [11], вследствие мощной антиоксидантной активности глюкозамина 112]. Таким образом снижается ИЛ-1-зависимая экспрессия ферментов, участвующих в воспалении и деструкции суставных тканей, таких как металлопротеиназы, индуцированная окись азота и цик-лооксигеназа-2 (СОХ-2) |11|. Неорганические сульфаты в составе глюкозаминосульфата, вероятно, вносят свой вклад в проявление его фармакологических эффектов, так как необходимы для регуляции синтеза хрящевых глюкозаминогликанов и протеогликанов, при этом их уровни в сыворотке крови после введения глюкозаминосульфата возрастают 113].
Клинические данные по применению глюкозамине сульфата при ОА
Эффективность и безопасность применения глюкозаминосульфата при лечении ОА обоснованы данными трех обширных обзоров, а также результатами нескольких мета-анализов.
Входе анализа, проведенного Т.Е. McAlindon с соавт. ] 14] при финансовой поддержке Национального института здоровья США, оценивались эффективность и безопасность глюкозам иносульфата и хондроитинсульфата при лечении ОА. Авторы ограничили свои поиски материалов июнем 1999 г и включили в анализ испытания, в которых проводилось сравнение с больными, получавшими плацебо по крайней мере в течение 4 недель, вследствие чего они рассмотрели в своем обзоре результаты только 6 испытаний. Несмотря на эти относительные ограничения, ученые обнаружили умеренный терапевтический эффект глюкозаминосульфата на течение ОА , причем величина этого эффекта возрастала по мере продления периода лечения (более 4 недель).
Авторы обсуждают общие вопросы качества оценки результатов анализируемых испытаний, но их средняя расчетная оценка качества испытаний глюкозамин сульфата, как и, вероятно, других препаратов, применяемых при лечении ОА, аналогична стандартам, которые они используют при рецензировании медицинских статей на эту тему. Кроме того, они утверждают, что 38% асимметрия, которую они обнаружили при анализе воронкообразного графика результатов испытаний (funnel plot analysis), указывает на наличие систематической ошибки в опубликованных работах 115, 16]. и полагают, что эта асимметрия является обычной для мета-анализов, опубликованных в ведущих медицинских журналах, а ее причиной могут быть различные факторы, в том числе истинная гетерогенность (т.е. действительное различие эффектов в разных испытаниях). Последнее представляется весьма вероятным при ОА из-за различных критериев отбора больных, тяжести заболевания и методов оценки. Но при всем этом признается, что не было обнаружено отрицательных результатов испытаний глюкозамина сульфата.
Несмотря на вышеуказанные недостатки проанализированных исследований, авторы смогли прийти к выводу, что глюкозаминосульфат действительно оказывает эффект на симптомы ОА, причем степень положительного действия колеблется от умеренной до высокой, при этом обеспечивается хорошая безопасность препарата.
Более точный и подробный мета-анализ, который охва-
тывает период с 1966г по ноябрь 1999г. был опубликован в начале 2001г в виде Кохрейновского обзора [17]. В данном анализе были рассмотрены 16 рандомизированных контролируемых испытаний глюкозами на сульфата, включая все испытания (в сравнении с плацебо), которые были рассмотрены в более ранней публикации Т.Е. McAlindon с соавт. |14|, с добавлением данных ряда новых работ. Кроме того, в анализ были включены 4 клинических испытания глюкозами-носульфата, в которых проводилось сравнение с другим препаратом, а не с плацебо. Этот момент очень важен, так как стандартная симптоматическая фармакотерапия ОА подразумевает использование неспецифических симптоматических препаратов, например, аналгетиков и особенно НПВП: во включенных испытаниях в качестве препарата в контрольной группе использовались именно НПВП.
Все испытания были рандомизированными, проводились с использованием двойной слепой оценки, большого общего количества больных — 2029 (992 получали глюкозамин и 1037 -препараты сравнения). Средняя продолжительность испытаний составила 6,25 недели, поэтому обзор отражает кратковременные симптоматические результаты лечения ОА. В подавляющем большинстве испытаний глюкозаминосульфат назначали per os, в дневной дозе, обычно эквивалентной 1500 мг препарата. В большинстве испытаний изучался эффект лечения тонартроза. В ходе качественной оценки согласно утвержденной методики были получены результаты, которые привели к противоположным выводам, сделанным авторами в предыдущем обзоре, где утверждалось, что в общем качество испытаний глюкозамина сульфата про ОА было так же высоко (если не выше), как и уровень испытаний НПВП, при суммарных медианных баллах качества равных 9 (из 16 возможных баллов). Важно отметить выраженную тенденцию улучшения качества для большинства недавних исследований, проведенных в 90-х годах, по сравнению с исследованиями, выполненными в 80-е: медиана качества у первых составила 12 баллов против 7.5.
В качестве критерия величины эффекта использовали стандартизованные разности средних (СРС), интерпретируя их следующим образом: 0,20 — низкий эффект, 0,50 — умеренный и 0,8 или выше — выраженный. Величина объединенных СРС для оценки степени уменьшения боли по сравнению с плацебо была очень высокой — 1,40. Для оценки улучшения функциональной активности, которую оценивали по индексу Lequesne, она составила 0,63 и соответствовала разнице в отклонении от базального уровня по сравнению с плацебо, равной 3,5 баллам, т.е. была равна смещению на один класс в тяжести заболевания по индексу Lequesne.
В испытаниях, где глюкозамин сульфат сравнивали с различными НПВП,он оказался равным по эффективности двум и превышал два других противовоспалительных препарата. При этом значение объединенных ССР составило 0,86 (3 испытания) и 0,32 (2 испытания) по индексу Lequesne, что указывало на тенденцию к преимуществу со стороны глюкозами носульфата, что по мнению авторов является основополагающим моментом, тем более учитывая очень высокую степень безопасности глюкозамин сульфата.
Авторы Кохрейновского обзора сделали общее заключение о том, что имеются веские доказательства эффективности и безопасности глюкоза ми носульфата при лечении ОА. В частности, они отметили, что все испытания, кроме одного, выполнены с применением препарата гпюкозаминосульфата, а результаты одного испытания с использованием глюкозами-ногидрохлорида, которые были менее или, по крайней мере, не столь обнадеживающими (установлена более высокая вариабельность), говорят о том, что применение оригинального препарата глюкозамина и наличие в нем сульфатов могут играть решающую роль. В заключение было указано, что необходимо провести долгосрочные клинические испытания для оценки долговременной эффективности и безопасности глюкозамин сульфата.
Недавно были опубликованы данные третьего мета-анализа [19], в котором отдельно оценивались эффективность и
безопасность глюкозамин сульфата и хондроитинсульфата. Анализировались данные только рандомизированых испытаний с использованием двойного слепого метода и плацебо в качестве контроля (таким образом исключался контроль по препарату сравнения). Глюкозамин сульфат назначался орально больным с гонартрозом, результаты испытаний оценивали новейшими методами. Поэтому в данный мета-анализ оказалось возможным включить данные только 7-и испытаний глюкозаминосульфата, 3-и из которых были включены в ранее выполнявшиеся мета-анализы JAMA и Кохрейновского обзора. Преимуществом данного анализа является то,что в нем учтены проблемы, обозначенные в вышеупомянутых работах, а именно, в период их проведения были даны рекомендации о том, что необходимы а) дальнейшие высококачественные крупномасштабные испытания и б) долговременные клинические испытания. Эти рекомендации были полностью учтены в ходе двух независимых, высококачественных, долговременных испытаний глюкозамина сульфата, результаты которых были опубликованы в 2001 г в журналах Lancet [20] и Archives of internal Medicine [21],
Проанализированы данные, полученные при лечении 1020 бальных ОА глюкозаминосульфатом. Средний балл качества этих испытаний был высоким — 90% согласно принятому для них методу оценки качества.
В ходе долговременных (3 года) испытаний глюкозаминосульфата [20, 211 были получены данные, которые с высокой статистической достоверностью говорят о том, что данный препарат является высокоэффективным в плане торможения структурных изменений (по данным радиографического измерения степени сужения суставной щели), причем данные обоих крупномасштабных испытаний согласуются. Величина воздействия на данный параметр варьировала от низкой до умеренной и сопровождалось статистически значимым клиническим эффектом. Данные для оценки клинического эффекта хондроитинсульфата оказались недостаточными,
Согласно совокупным критериям оценки, которые применялись в этом мета-анализе, глюкозаминосульфат оказывает благоприятный симптоматический эффект при ОА как в кратковременных, так и в долговременных испытаниях. Соответствующая величина эффекта оказалась ниже приведенной в обзоре JAMA и Кохрейновском обзоре, так как, по мнению авторов, были приняты более строгие условия включения результатов исследования в мета-анализ и более консервативная модель анализа.
В отличие от предшествующего мета-анализа , представленного в JAMA, авторы исключили любое влияние систематической ошибки, связанной с преимущественной публикацией положительных результатов исследований, на достоверность полученных результатов.
Ниже приводятся результаты долговременных испытаний.
В первом испытании [20] принимали участие 212 больных (средний возраст 66 лет, 76% — женщины) с гонартозом, которые составили случайную выборку; больные получали орально глюкозамин сульфат в дозе 1500мг/сут. в течение 3-х лет. Полученные данные оценивались двойным слепым методом. Оценка ОА по выраженности симптомов и структурных изменений в коленных суставах варьировала от низкой до умеренной степени. По истечении 3 лет отмечалось значительное симптоматическое улучшение (оценка по индексу WOMAC степени выраженности болевого синдрома и функции сустава) у больных, получавших глюкозамин сульфат, по сравнению с группой плацебо. Изменение глобального индекса состояния здоровья соответствовали 10% ухудшению симптомов у больных, получавших плацебо. У больных, получавших глюкозаминосульфат, по глобальному индексу достигнуто 25% улучшение.
В данной работе впервые было показано, что достоверный симптоматический эффект глюкозамина сульфата сопровождался столь же убедительным структурным эффектом. Основным критерием оценки структурного эффекта являлась ширина суставной щели (ШСЩ). Ее сужение (ССЩ) определяли методом цифрового анализа изображения ШСЩ медиальной
тибио-феморальной области сустава, а также методом визуальной оценки (при помощи лупы) на рентгенограмме в точке максимального сужения. Стандартизованные рентгенограммы передне-задней области нагруженного сустава при полном разгибании ноги были сделаны в начале испытания и по истечении 1-3 лет в процессе его проведения. В группе плацебо отмечено ежегодное уменьшение ШСЩ в среднем на 0,1 мм, что согласуется с опубликованными данными о структурном прогрессировании ОА. В целом по группе пациентов, получавших глюкозаминосульфат, ССЩ к концу испытания не отмечалось, и межгрупповые различия оказались статистически достоверными. Более того, у 30% больных на плацебо обнаружено значительное ССЩ, в среднем более чем на 0,5 мм, что может грозить развитием инвалидности в будущем. В основной группе такой эффект отмечен лишь у 15% больных (р=0,013).
Статистически значимых различий по частоте или характеру побочных эффектов в группах больных, получавших глюкозамин сульфат или плацебо, не обнаружено. В ходе клинических и лабораторных исследований по ходу испытания у пациентов не выявлено достоверных органных или функциональных нарушений.
Согласно четким требованиям редактора и рецензентов журнала Lancet, где были опубликованы данные результаты, авторы статьи предупреждают о том, что их не следует распространять на нестандатизированные препараты, состав которых варьирует в широких пределах и которые, как утверждают производители, содержат глюкозамин.
Вышеприведенное исследование относится только к стандартному препарату глюкозаминосульфата.
В сопровождающей редакторской статье глюкозаминосульфат был назван возможным началом новой эры в лечении ОА, а испытание, проведенное J.Y. Reginster с со-авт.), — вехой в изучении данной болезни (22|.
O.Buyere с соавт. опубликовали два полных отчета, основанных на результатах испытаний, выполненных JJ. Reginster с соавт. В первом [23] они показали слабую корреляцию между симптомами гонартроза и структурными параметрами сустава, измеряемыми по радиограммам, что широко освещалось ранее в литературе, посвященной проблемам ОА. Однако установлена умеренная степень корреляции между интенсивностью боли в колене и ССЩ. Интересно отметить, что симптоматический эффект глюкозамина сульфата оказался значимым независимо от базального уровня структурного поражения сустава и степени прогрессирования гонартроза. Последний факт был представлен во втором отчете [24]: у больных с наименее выраженными структурными повреждениями сустава на базальном уровне, находящихся в течение 3-х лет на плацебо, отмечалось наиболее существенное ССЩ к концу исследования. У таких же больных основной группы, наоборот, положительный структурный эффект глюкозаминосульфата оказался максимальным.
Во втором независимом испытании, которое провели K.Pavelka с соавт. [21], были фактически подтверждены результаты работы JJ. Reginster с соавт., причем протоколы обоих испытаний были практически идентичным и. Включено 202 больных с ОА коленного сустава, средний возраст 62 года, 78% — женщины. На протяжении 3-х лет испытания отмечалось постоянное симптоматическое улучшение (согласно индексу Lequesne — от слабовыраженного до умеренного — 8-9 баллов) у больных, которые получали глюкозаминосульфат. Это улучшение достигалось в течение первого года лечения и сохранялось на постоянном уровне до его окончания. По истечении 3-х лет уменьшение боли, снижение ограничения функции и подвижности сустава по индексу WOMAC и его субшкалам, а также по индексу Lequesne у больных, получавших глюкозамин сульфат, были достоверными по сравнению с аналогичными показателями у больных, находившихся на плацебо, при этом величина эффекта была сопоставима с отмеченной в испытании J.J. Reginster с соавт.
В работе K.Pavelka с соавт. также подтверждена высокая структурная активность глюкозамин сульфата, причем выра-
женность эффекта была аналогичной: отмечено ежегодное прогрессирующее ССЩ в группе плацебо, в то время как в группе глюкозамин сульфата в среднем ШСЩ не уменьшилась. Количество больных с уменьшением ШСЩ более чем на 0,5 мм составило 14% в группе плацебо и только 5% в группе, получавшей глюкозамин сульфат (р=0,05). При анализе данных динамического радиографического исследования коленных суставов установлено, что число пациентов с плохими конечными показателями по числу остеофитов (ин-дентификация по стандартному радиографическому атласу) в группе плацебо было в 3 раза больше, чем в основной группе больных.
Показатели безопасности, подробно представленные в работе, были аналогичными в обеих группах исследованных больных. Подобно предостережению, прозвучавшему в статье .и. Reg¡nster с соавт., авторы подчеркивают неправомочность экстраполяции полученных результатов на препараты глюкозамина, отличные от оригинального глюкозамина сульфата, который использовался в данной работе.
Интересно отметить, что данные по структурному эффекту препарата, полученные в обеих разобранных выше работах, были подвергнуты сомнению, так как в них проводился анализ рентгенограмм коленного сустава, выполненных в положении стоя (полное выпрямление). Однако такой метод являлся «золотым стандартом», рекомендованным в научных руководствах, в то время как корректность ни одной из позднее предложенных методик еще не оценивалась в соответствующих испытаниях. Оппонентами была выдвинута гипотеза о том, что в результате уменьшения боли под воздействием глюкозаминосульфата по сравнению с плацебо изменяется положение костей в коленном суставе (особенно при полном выпрямлении ноги), что может привести к искажению оценки ССЩ и преувеличению межгрупповых различий. При этом критики сами признавали выраженный долговременный симптоматический эффект глюкозаминосульфата, который до этого не наблюдался при лечении другими препаратами. Авторы обоих долговременных испытаний эффектов глюкозами-носульфата, сначала К.Рауе1ка (работа которого после появления критических замечаний была опубликована в полном объеме), а затем и обе группы исследователей, в совместном реферате [25] в ходе дальнейшей обработки своих результатов по структурному эффекту глюкозаминосульфата убедительно показали, что только уменьшение боли никак не объясняет снижение степени ССЩ.
Согласно данным испытаний и мета-анализов степень безопасности глюкозаминоа сульфата довольно высокая. В ходе кратковременных клинических испытаний нежелательные побочные эффекты наблюдались лишь у 6-12% больных, препарат был отменен по этой причине менее чем у 4% испытуемых. По частоте и характеру нежелательных побочных эффектов не отмечено достоверной разницы между плацебо и глюкозам и ном сульфатом, как и по частоте случаев отмены препарата, связанных с обеспечением безопасности. Напротив, в сравнительных клинических испытаниях, частота нежелательных побочных эффектов особенно относительно желудочно-кишечного тракта была всегда достоверно выше в группах сравнения, получавших НПВП, чем в группе больных, лечившихся глюкозамин сульфатом.
Во всех испытаниях характер нежелательных эффектов был аналогичным в группах плацебо и глюкозаминосульфата, и в большинстве отмеченных случаев побочные эффекты были невыраженными и преходящими.
Долговременные базовые клинические испытания особенно важны, так как в их ходе оценивается безопасность глюкозаминосульфата при длительном применении, которое очень редко или вообще никогда не рассматривается при оценке препаратов, используемых при лечении ОА. Степень безопасности глюкозаминосульфата при долговременном применении была аналогична установленной при краткосрочных испытаниях, при этом слабое, умеренное и преходящее побочное действие в группе больных, получавших глюкозаминосульфат, отмечалось с такой же частотой, как и в
группе плацебо. Во всех проведенных кратковременных и долговременных испытаниях значимых изменений в результатах общих лабораторных анализов не было выявлено.
Механизм действия глюкозамина не предполагает его токсичности. В отличие от НПВП, глюкозамин не ингибирует циклооксигеназу первого типа (СОХ-1), что объясняет гораздо более высокую степень безопасности глюкозамино-сульфата в отношении желудочно-кишечного тракта.
Так как глюкозамин является аминомоносахаридом, следовательно, с точки зрения безопасности следует обратить внимание на обмен глюкозы. В недавно проведенных экспериментах на животных, которым внутривенного вводили дозы глюкозамина гораздо выше фармакологических, было показано, что препарат может повышать инсулиновую резистентность в результате сложных взаимодействий с так называемой гексозаминовой последовательностью реакции, которая представляет собой альтернативный путь метаболизма глюкозы (26). Однако в двух недавних испытаниях, в которых очень высокие дозы глюкозамин сульфата вводились людям внутривенно |27| или даже внутриартериально [28), было установлено, что данный механизм, вероятно, не работает в человеческом организме, т.е. глюкозаминосульфат не оказывал влияния на чувствительность, секрецию и активность инсулина. Действительно, в работе 1999г [291 было показано, что глюкозамин сульфат при кратковременном приеме препарата не влияет на уровень глюкозы в плазме крови, взятой натощак, даже у больных с высоким базальным содержанием глюкозы. В ходе долговременного испытания, проведенного J J. Reginster с соавт., даже была отмечена тенденция к снижению данного показателя в среднем. В ходе испытания K.Pavelka с соавт. у 4-х больных развился диабет, но 3-е из них относились к группе плацебо и только один получал глюкозамин сульфат.
В самом последнем испытании [30] принимали участие 26 пожилых пациентов с диабетом 2 типа, которые в течение
ЛИТЕРАТУРА
1. Felson D.T., Zhand Y. Ап update on the epidemiology of knee and hip osteoarthritis with a view to prevention. Arthr.Reum., 1998,41, 1343-1355
2. Oliveira S.A., Felson D.T., ReedJ.l. Incidence of symptomatic hand, hip and knee osteoarthritis among patients in a health maintenance organization. Arthr.Reum.,1995, 38. 1134-1141
3. Pendleton A., Arden N.. Dougados M. et al. EULAR recommendations for the management of knee osteoarthritis: report of a task of the Standing Committee Гог International Clinical Studies Including Therapeutic Trials (ESCISIT). Ann. Reum.Dis., 2000,59,936-944
4. Guccione A.A., Felson D.T., Anderson J.J. et al. The effects of specific medical conditions on the functional limitations of elders in the Framingham Study. Am.J.Public Health, 1994,84, 351-358
5. Setnikar I., Rovati L.C., Absorption, distribution, metabolism
and excretion of glucosamine sulfate: a review.
Arzneimittelforschung, 2001,51, 699-725
6 Noyszewski E.A., Wroblewski K., Dodge G.R. et al. Preferential incorporation of glucosamine into the galactosamine moieties of chondroitin sulfates in articular cartilage expiants. Arthr.Reum., 2001, 44, 1089-1095
7. Bassleer C., Rovati L.C., Franchimont P. Glucosamine sulfate stimulates proteoglycan production in human chondrocytes in vitro. Osteoarthr. Cartil., 1998, 6, 427-434
8. Piperno М., Reboul P., Helio Le Graverand M.P. et al. Glucosamine sulfate modulates dysregulater activities of human osteoarthritis chondrocytes in vitro. Osteoarthr. Cartil., 2000. 8, 207-212
9. Dodge G.R., Jimenez SA. Glucosamine sulfate modulates the levels ofaggrecan and matrix metallopteinase-3 synthesized by cultured humanosteoarthritis articular chondrocytes, Osteoarthr. Cartil., 2003, 11, 424-432
10. Yaron I., Shirasi I., Judovich R., Yaron M. Glucosamine sul
90 дней получали ежедневно 1500 мг глюкозамина сульфата и 1200 мг хондроитинсульфата или плацебо (рандомизированная выборка, двойной слепой метод). В течение испытания терапия диабета не менялась ни у одного больного. Не отмечено достоверных различий между группами по уровню гемоглобина А 1с после лечения, а также других значимых внутригрупповых различий до и после лечения.
ОА является хроническим заболеванием, которое развивается преимущественно у пожилых людей с полиморбидной патологией, часто требующей соответствующего лечения. Глюкозамин не конкурирует с другими препаратами в процессе всасывания, а после всасывания не связывается с белками плазмы. Метаболически данное вещество встраивается преимущественно в протеогликаны или деградирует вне системы цитохромных ферментов. Таким образом, предполагается, что в силу своих физико-химических, фармакокинетических и метаболических особенностей глюкозамин обладает низким потенциалом для взаимодействия с другими лекарственными средствами.
Выводы
Полученные к настоящему времени клинические данные говорято том, что глюкозамин сульфат дает реальные возможности в лечении ОА, особенно у пожилых пациентов. Впервые появился лекарственный препарат, который безопасен при долговременном приеме и который способен замедлить прогрессирование заболевания как в отношении уменьшения симптоматических проявлений, так и в плане структурных изменений тканей сустава. Эти свойства препарата способны радикально изменяить представление врачей и больных о возможностях долговременного лечения ОА, когда реально проводить одновременное лечение одного или нескольких сопутствующих заболеваний. При этом и врач, и пациент приобретают уверенность, что с помощью глюкозами-носульфата обеспечивается долговременный контроль над болезнью у отвечающих на лечение больных.
fate inhibits nitric oxide and stromelusin production in cartilage cultures and reverses IL-1 inhibition of osteoarthritis articular cartilage sintetasis. Ann. Reum.Dis., 2001,60, suppl., 50
II. Lardo R., Alvares-Soria M.A., Diez-Ortego J. et al. Glucosamine ingibits IL-l(i- induced NF[?B frticulation et al. in human osteoarthritic chondrocytes. Osteoarthr. Cartil., 2003,11, 290-298
12 SethikarL. Cereda R., Pacini M.A., Revel L, Antireactive properties of glucosamine sulfate. Arzneimittelforschung, 1991,41,157-161.
13. Hoffer L.J., Kaplan L.N., Hamadeh M.J. et al. Sulfate could mediate the therapeutic effect of glucosamine sulfate. Metabolism, 2001, 50, 767-770.
14. McAlindon T.E., La Valley M.P., Gulin J.P., Felson D.T. Glucosamine and chondroitin for treatment of osteoarthritis: a ssystematic quality assessment and tneta-analysis. JAMA, 2000, 283, 1469-1475
15. Egger M., Davey Smith G., Scheneider M., MinderC. Bias in meta analysis detected bi a simple, graphical test. BMJ, 1997,315,629-634
16. Sterne J.A., Egger M., Smith G.D. Systematic reviews in health care: investigating and dealing with publicación and other biases in meta analysis. BMJ, 2001., 323, 101-105
17. Towheend T.E.. Anastassiades T.P., Shea B. et al. Glucosamine therapy for treating osteoarthritis (Cochrane Review). ln:The Cochrane Library, Issue 2, 2001. Oxford: Update Software
18. Lequesne M.G., Mery C., Samson M., Gerard P. Indexes of severity for osteoarthritis of the hip knee. \&lidation-value in comparison with other assessment tests. Scand. J. Reumotol., 1987,65, suppl., 85-89
19. RichyF., Bruyere O., Ethgen et al. Structural and symptomatic efficacy of glucosamine and chondroitin in knee osteoarthritis. A comprehensive Meta-analysis. Arch, Int. Med., 2003,163,1514-1522
20. Reginster J.Y., Deroisy R., Rovati L.C. et al. Long-term effects of glucosamine sulfate on osteoarthritis progression: a randomized, placebo controlled clinical trial. Lancet, 2001,357,251-256
21. Pavelka K., Gatterova J.OIejarova M. et al. Glucosamine sulfate use and delay of progression of knee osteoarthritis: 3-year, randomized, placebo-controlled, duble-blind study. Arch. Int. Med.,2002., 162,2113-2123
22. McAlindon T.E. Glucosamine for osteoarthritis: dawn of a new era? Lancet, 2001,357,247-248
23. Bruyere O..Honoré A., Rovati L.C. et al. Radililogic features poorly predict clinical outcomes in knee osteoarthritis. Scand. J. Reumotol., 2002,31,13-16
24. Bruyere O.,Honoré A., Ethgen O. et al. Correlation between radiographic severity of knee osteoarthritis and future disease progression. Results from a 3-year, prospective, placebo-controlled, study evaluating the of glucosamine sulfate. Osteoarthr. Cartil., 2003, 12, 1-5
25. Pavelka K., Rovati L.C., Gatterova J. et al. Pain relief is not a
confounder in joint space narrowing assessment of full exten-
sion knee radiographs. Osteoarthr. Cartil., 2002, 10 (suppl. A), S 16-17
26. Baron A.D., Zhu J.S, Zhu J.H. et al. Glucosamine induces insulin resistance in vivo by affecting GLUT 4 translocacion in skeletal muscle. Implications for glucose toxicity. J. Clin. Invest., 1995,96, 2792-2801
27. MonauniT., Zenti M.G., Cretti A. et al. Effects of glucosamine infusion on insulin secretion and insulin action in humans. Diabetes, 2000,49,926-935
28. Pouwels M.J., Jacobs J.R., Span P.N. et al. Short-term glucosamine infusion does not affect insulin sensitivity in humans. J. Clin. Endocrinol. Metab., 2001, 86, 2099-2103.
29. Rovati L.C., Annefeld М., Giacovelli G. et al. Glucosamine in osteoarthritis. Lancet, 1999,354,1640
30. Scroggie D.A., Albright A., Harris M. The effect of glu-cosamine-chondroitin supplementation on glycosylated hemoglobin levels in patiens with type2 diabetes mellitus. A placebocontrolled, duble-blinded, randomized clinical trial. Arch.Int.Med., 2003, 163, 1587-1590
Поступила 25.12.04
cyberleninka.ru
Эффективность глюкозамина и хондроитина при остеоартроза, артрозе и остеоартрите
Подборка исследований по эффективности глюкозамина и хондроитина при терапии остеоартроза (артроз, остеоартрит). В данной статье приведены только заключения исследований, с полным текстом можно ознакомиться по приведенным ссылкам.
Американская Академия Хирургов-ортопедов — Лечение остеоартрита колена, 2-e издание
American Academy of Orthopaedic Surgeons — Treatment of Osteoarthritis of the Knee – 2nd Edition
Мы не можем рекомендовать использование глюкозамина и хондроитина для пациентов с клиническими признаками остеоартрита колена.
…
В настоящее время глюкозамин и хондроитин сульфат широко изучены. Нет никаких существенных доказательств того, что минимальные клинически важные результаты были достигнуты по сравнению с плацебо, независимо от того, оценивались ли глюкозамин и хондроитин сульфат раздельно или в комбинации. Рекомендация основана на недостаточной эффективности, а не на потенциальный вреде.
Воздействие глюкозамина, хондроитина или плацебо на пациентов с остеоартрозом тазобедренного или коленного суставов: сетевой мета-анализ
Effects of glucosamine, chondroitin, or placebo in patients with osteoarthritis of hip or knee: network meta-analysis
BMJ. 2010; 341: c4675.
По сравнению с плацебо, глюкозамин, хондроитин и их комбинация не приводят к снижению боли в суставах и не оказывают влияния на сужение суставной щели. Органы здравоохранения и медицинского страхования не должны покрывать затраты на эти препараты, не следует рекомендовать их пациентам, которым еще не назначен курс лечения.
Глюкозамин и хондроитин для лечения остеоартроза: систематическая оценка качества и мета-анализ
Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis.
JAMA. 2000 Mar 15;283(11):1469-75.
Испытания препаратов глюкозамина и хондроитина для симптомов остеоартроза демонстрируют эффективность от умеренной до большой, но вопросы качества и вероятные систематические ошибки в публикациях дают возможность предположить, что эти эффекты являются преувеличенными. Тем не менее, некоторая степень эффективности представляется вероятной для этих препаратов.
Воздействие глюкозамина, хондроитина и метилсульфонилметана при спондилопатии и остеохондрозе: систематический обзор
Efficacy of glucosamine, chondroitin, and methylsulfonylmethane for spinal degenerative joint disease and degenerative disc disease: a systematic review.
J Can Chiropr Assoc. 2011 March; 55(1): 47–55.
Существует мало литературы обосновывающей использование обычных пищевых добавок для терапии спондилопатии, в следствии чего трудно установить, должны ли врачи рекомендовать их.
Мета-анализ: хондроитин при остеоартрозе тазобедренного или коленного суставов
Meta-analysis: chondroitin for osteoarthritis of the knee or hip.
Ann Intern Med. 2007 Apr 17;146(8):580-90.
Крупномасштабные, методологически обоснованные исследования показывают, что симптоматическая польза хондроитина минимальна или отсутствует. По этой причине использованию хондроитина в установившейся клинической практике следует препятствовать.
Глюкозамин от боли при остеоартрозе: почему результаты испытаний различаются?
Glucosamine for pain in osteoarthritis: why do trial results differ?
Arthritis Rheum. 2007 Jul;56(7):2267-77.
Неоднородность множества испытаний глюкозамина больше, чем это ожидается в силу случайности. Глюкозамин гидрохлорид не является эффективным. Среди испытаний, к которым причастна индустрия, величина эффекта была неизменно выше. Потенциальные объяснения включают в себя различия в приготовлении глюкозамина, неадекватное скрытое отнесение участников испытаний к той или иной группе и предвзятость индустрии.
Три типа терапии при остеоартрозе коленного сустава: факты показывают отсутствие пользы
Three Treatments for Osteoarthritis of the Knee: Evidence Shows Lack of Benefit
Eisenberg Center at Oregon Health & Science University.
Issued: April 8, 2009.
Лучшие доказательства эффективности лечения глюкозамином и хондроитином идут от Glucosamine/ Chondroitin Arthritis Intervention Trial (GAIT).
Исследование GAIT — рандомизированное клиническое исследование, в котором сравнивались группы людей, получающие один из пяти способов лечения: глюкозамин гидрохлорид, хондроитин сульфат, комбинация обоих, целекоксиб (НПВП), либо плацебо. В исследовании принимали участие в общей сложности 1583 пациента с остеоартрозаом коленного сустава. В этом исследовании глобальные улучшения в боли и функции суставов наблюдались во всех группах — глюкозамин, хондроитин, глюкозамин и хондроитин вместе взятых и плацебо. Однако, не было никакого клинически значимого эффекта на симптомы остеоартроза коленного сустава обусловленного применением добавок глюкозамина и / или хондроитина. В исследовании также проанализированы подгруппы людей с умеренной и тяжелой формой остеоартроза и было обнаружено, что глюкозамин и хондроитин повлияли на боль и улучшили функцию суставов лучше, чем лечение плацебо в этой подгруппе.
В целом, люди с остеоартрозом коленного сустава не получили большего облегчения симптомов при использовании глюкозамина и хондроитина, чем при приеме плацебо.
Тематические ресурсы
Вы можете следить за комментариями к этой записи через ленту RSS 2.0.
amigoacid.ru
