Хондроитина сульфат — это… Что такое Хондроитина сульфат?
Хондроитинсульфаты — полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами хряща. Вырабатываются хрящевой тканью суставов, входят в состав синовиальной жидкости. Необходимым строительным компонентом хондроитинсульфата является глюкозамин, при недостатке глюкозамина в составе синовиальной жидкости образуется недостаток хондроитинсульфата, что ухудшает качество синовиальной жидкости и может вызвать хруст в суставах[1].
В медицине хондроитина сульфат применяется в качестве лекарственного средства группы нестероидных противовоспалительных препаратов.
Биологическая роль
Хондроитинсульфат обладает тропностью к хрящевой ткани, инициирует процесс фиксации серы в процессе синтеза хондроитин-серной кислоты, что, в свою очередь, способствует отложению кальция в костях. Стимулирует синтез гиалуроновой кислоты, укрепляя соединительнотканные структуры: хряща, сухожилий, связок, кожи.
Особенностью хондроитина среди протеогликанов является его способность сохранять воду в толще хряща в виде водных полостей, создающих хорошую амортизацию и поглощающих удары, что в итоге повышает прочность соединительной ткани. Важным действием хондроитина является его способность угнетать действие специфических ферментов, разрушающих соединительную ткань, в том числе лизосомальных ферментов, высвобождающихся в результате разрушения хондроцитов (эластаза, пептидаза, катепсин, интерлейкин-1 и др.)[1].
Естественное потребление хондроитинсульфата и других хондропротекторных веществ осуществлялось с употреблением в пищу сухожилий, кожи и хрящей животных, особенно рыб. В связи с уменьшением доли этих продуктов в рационе современного человека (иногда и с полным исключением), а также при метаболических нарушениях, чрезмерных функциональных нагрузках и особенно возрастном снижении активности синтетических процессов хондроитинсульфат должен поступать уже в готовом виде (или в виде предшественников синтеза) извне, в том числе с пищей
Фармакология
По данным разработчиков лекарственных средств[2], хондроитина сульфат замедляет резорбцию костной ткани и снижает потерю Ca
Биологически активные добавки

Хондроитинсульфат состоит из нескольких фракций с разной молекулярной массой, притом высокомолекулярные фракции разлагаются в желудочно-кишечном тракте. В связи с этим первые препараты хондроитинсульфата были пригодны только для внутривенного применения. Однако со временем были разработаны технологии получения низкомолекулярных фракций хондроитинсульфата, которые почти полностью всасываются в желудочно-кишечном тракте, сохраняя свою структуру, и встраиваются в хрящевую ткань. Современные биологически активные пищевые добавки содержат низкомолекулярные фракции хондроитинсульфата, получаемые в основном из хряща лососёвых рыб
Многочисленные клинические исследования (в том числе слепые и плацебо-контролируемые) показали, что курсовое назначение препаратов хондроитинсульфата в течение 1-3 месяцев сопровождается увеличением подвижности суставов, уменьшением их отёчности и болезненности, а также улучшением объективных показателей, включая рентгенологические. Положительная динамика рентгенологических показателей, таких как ширина суставной щели, свидетельствуют о стойком восстановлении структуры суставного хряща, чего не наблюдается при применении одних только нестероидных противовоспалительных средств (диклофенак, пироксикам, индометацин и др.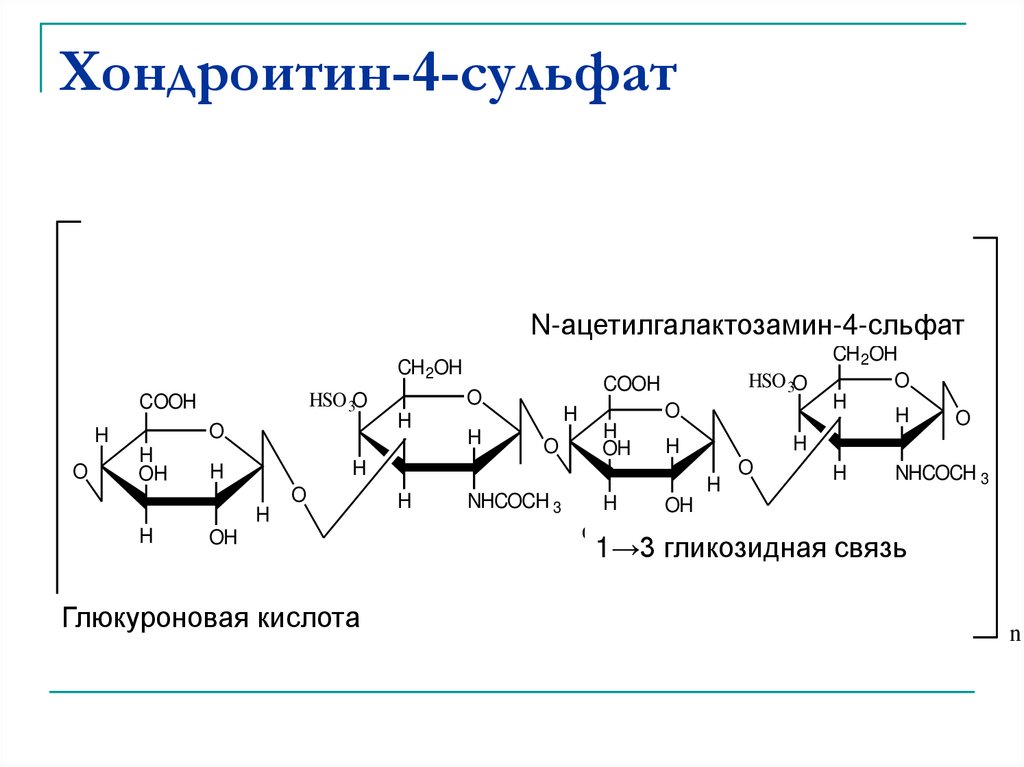
При приёме внутрь хондроитинсульфат блокирует активность панкреатической липазы и замедляет всасывание жиров в кишечнике. В результате длительного применения хондроитинсульфата может наблюдаться снижение уровней гиперлипидемии и гиперхолистеринемии и даже снижение массы тела[1].
Принимается в лечебных целях по 500—1500 мг в день в два или три приёма. Стандартная суточная доза составляет 400 мг 3 раза в день. Точная дозировка зависит от веса пациента и степени выраженности заболевания. Противопоказаниями к приёму лекарства служат нарушения свёртывающей системы крови и тромбофлебит. К самым частым побочным реакциям относится аллергия, так как препарат в сущности своей является белком животного происхождения. Длительный и стойкий результат от применения хондроитинсульфата можно получить только от приёма не менее 2-3 месяцев подряд. В целом отличается хорошей переносимостью и безопасностью
Доктор медицинских наук Стивен Барретт предупреждает о том, что потребители должны внимательно относиться к рекламе препаратов хондроитина и не доверять обещаниям чудодейственного излечения артрита[5], которые часто даются производителями[6].
См. также
Примечания
- ↑ 1 2 3 4 5 6 7 8 Гичев Ю. Ю., Гичев Ю. П. Руководство по микронутриентологии. Роль и значение биологически активных добавок к пище. — М.:»Триада-Х», 2006. — 264 с. — С. 151
- ↑ Поиск по базе данных ЛС, опции поиска: МНН —
- ↑ Mucopolysaccharides (Chondroitin Sulfates) As Dietary Supplements: Sources, Production and Comparative Bioavailability (англ.
 )
) - ↑ http://www.fasebj.org/cgi/reprint/20/7/803.pdf (англ.)
- ↑ Елена Малышева Передача «Здоровье» от 31 марта 2007 г. (рус.) (c 15 минуты). Архивировано из первоисточника 6 апреля 2012.
- ↑ Simon Wandel, Peter Jüni, Britta Tendal, Eveline Nüesch Effects of glucosamine, chondroitin, or placebo in patients with osteoarthritis of hip or knee: network meta-analysis (англ.). BMJ Publishing Group Ltd. (5.07.2010). Архивировано из первоисточника 6 апреля 2012. Проверено 25 апреля 2011.
- ↑ Clegg DO, Reda DJ, Harris CL, et al. (February 2006). «Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis».
 N. Engl. J. Med. 354 (8): 795—808. doi:10.1056/NEJMoa052771. PMID 16495392.
N. Engl. J. Med. 354 (8): 795—808. doi:10.1056/NEJMoa052771. PMID 16495392. - ↑ Rozendaal RM, Koes BW, van Osch GJ, et al. (February 2008). «Effect of glucosamine sulfate on hip osteoarthritis: a randomized trial». Ann. Intern. Med. 148 (4): 268-77. PMID 18283204.
Ссылки
Иследование: хондроитин сульфат эффективнее плацебо при лечении остеоартрита — Пресс-релизы
ЛОНДОН, June 13, 2016/PRNewswire/. Новое клиническое исследование, проведенное в полном соответствии с последними нормативами Европейского агентства лекарственных средств EMeA, показывает, что отпускаемый по рецепту препарат хондроитина сульфата устраняет боль и функциональные нарушения у пациентов, страдающих остеоартрозом коленных суставов (ОА), значительно более эффективен по сравнению с плацебо.
Компания IBSA в рамках Европейского конгресса ревматологов (European Congress of Rheumatology, EULAR 2016) представила результаты нового многоцентрового рандомизированного клинического исследования фазы III двойной анонимности и двойной имитации, названного «CONCEPT» (ChONdroitin ― CElecoxib ― Placebo T rial).
(Logo: http://photos.prnewswire.com/prnh/20160607/376534LOGO )
Исследование проводилось в полном соответствии с большинством последних нормативов EMeA в 16 центрах, расположенных в Бельгии, Чехии, Италии, Польше и Швейцарии. В нем принимали участие 603 пациента, страдающие ОА коленных суставов. Исследование было направлено на подтверждение эффективности и безопасности отпускаемого по рецепту высокоочищенного хондроитина сульфата по сравнению с плацебо и целекоксибом в качестве золотого стандарта в течение периода шести месяцев.
Результаты, представленные профессором Регинстером, доктором медицины, доктором наук, процессором кафедры эпидемиологии, здравоохранения и экономики здравоохранения Льежского университета (Бельгия) в рамках саттелитного симпозиума IBSA на тему «Какие методы лечения нам следует принять в качестве долгосрочной терапии ОА коленного сустава» (http://www.ibsa-international.com/eular2016), показывают, что два начальных пункта оценки эффективности терапии ― снижение алгофункционального индекса Лекена и снижение болевых ощущений по визуальной аналоговой шкале ― оказались статистически значимыми (p<0,05) по сравнению с плацебо, что подтверждает наличие эффекта SYSADOA (Sympomatic Slow Acting Drug in OsteoArthritis, симптоматический препарат замедленного действия в терапии остеоартроза) при использовании хондроитина сульфата.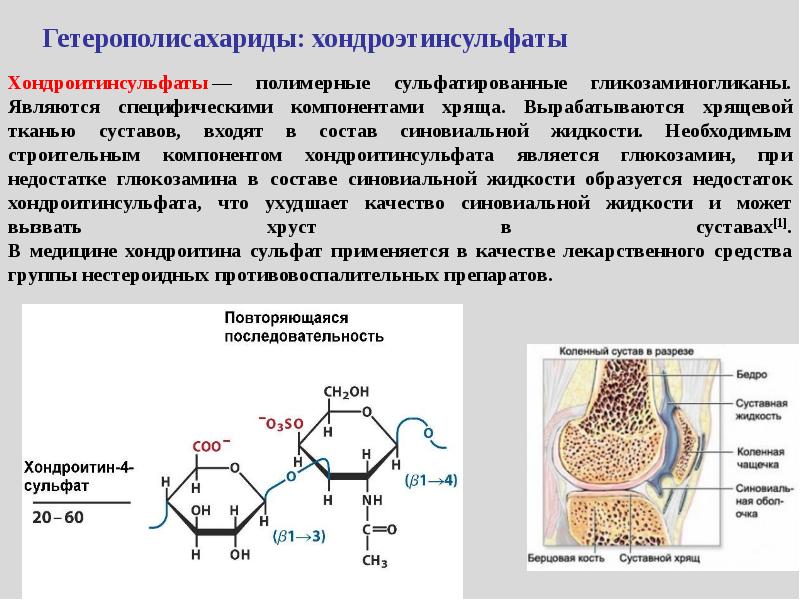 Кроме того, хондроитин сульфат оказался таким же эффективным, как и активно применяемый препарат сравнения (целекоксиб), а также показал приемлемое соотношение пользы и риска.
Кроме того, хондроитин сульфат оказался таким же эффективным, как и активно применяемый препарат сравнения (целекоксиб), а также показал приемлемое соотношение пользы и риска.
«Мы очень удовлетворены результатами испытаний, ― комментирует глава научно-исследовательского отдела компании IBSA Джузеппе Маутоне (Giuseppe Mautone), ― поскольку эти свидетельства подтверждают прогресс в поиске лекарственных средств для долгосрочной терапии ОА».
Об остеоартрозе (OA)
На сегодняшний день OA страдают около 40 млн европейцев; заболевание является условием для значительного числа медицинских консультаций и основным показателем для использования препаратов, отпускаемых по рецепту. На фоне продолжающегося старения населения к 2020 году ОА может стать четвертой по распространенности причиной инвалидности [1], [2].
Снятие болевых ощущений, восстановление функциональности и повышение качества жизни ― основные цели лечения ОА [2]. В ходе лечения чаще всего применяются болеутоляющие и противовоспалительные препараты, которые являются эффективными, но часто вызывают серьезные побочные реакции на гастроинтестиальном и сердечно-сосудистом уровне.
На данный момент были изучены свойства нескольких составов по снятию клинических симптомов и положительному воздействию на структурные изменения суставов, однако до сих пор ведутся широкие споры вокруг включения тех или иных методов лечения/препаратов в долгосрочную терапию ОА коленных суставов.
О хондроитине сульфате
Хондроитин сульфат IBSA* представляет собой препарат, отпускаемый по рецепту, с положительным и консолидированным соотношением пользы и риска. Его эффективность и безопасность при лечении ОА доказана в ходе клинических испытаний с участием более 3900 пациентов.
Препарат доступен в 13 странах ЕС, и с начала продаж (1983 г., Швейцария) лечение получили более 55 млн пациентов.
*Самые известные торговые марки: Condrosulf(R), Chondrosulf(R).
О компании IBSA
IBSA ― фармацевтическая компания средней величины, штаб-квартира которой находится в Лугано, Швейцария.
http://www.ibsa-international.com/home
На сегодняшний день в группе IBSA работает более 1800 человек, а ее деятельность ведется более чем в 80 странах мира через партнерства и местные представительства в Италии, Франции, Венгрии, Словакии, Польше, Турции, Китае и Скандинавии.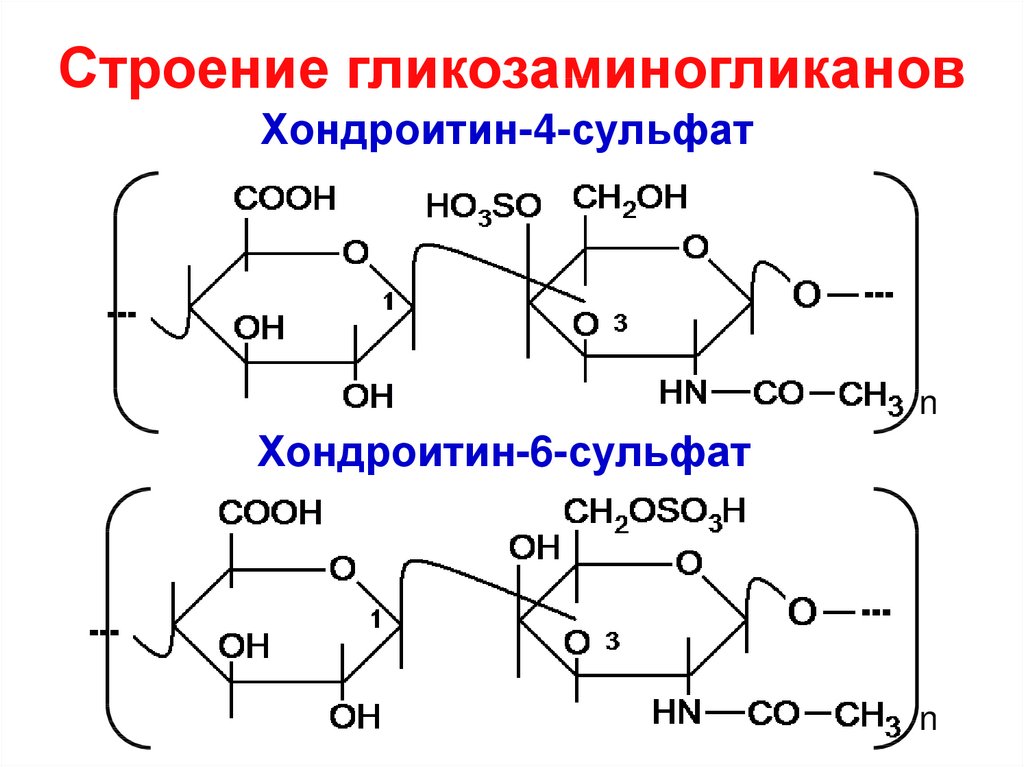 Деятельность компании охватывает восемь основных направлений лечения (боли/воспаления, ревматология, репродукция и фертильность, эндокринология, урология, дерматология и лечебная косметология, респираторные и сердечно-сосудистые заболевания), компания имеет более 60 эксклюзивных патентов.
Деятельность компании охватывает восемь основных направлений лечения (боли/воспаления, ревматология, репродукция и фертильность, эндокринология, урология, дерматология и лечебная косметология, респираторные и сердечно-сосудистые заболевания), компания имеет более 60 эксклюзивных патентов.
Библиографический список
1) Conaghan P.G. et al. Ann Rheum Dis. 2014; 73 (8): 1442-5.
2) Bruyère O. et al. Semin Arthritis Rheum. 2015; 45: S3-S11.
Для получения подробной информации:
Michele Fasola (Мишель Фазола)
менеджер по медицинскому маркетингу
Медицинское управление
IBSA Institut Biochimique SA
Тел.: +41-(0)-58-360-10-00
http://www.ibsa-international.com
Photo: http://photos.prnewswire.com/prnh/20160607/376534LOGO Source: IBSA
Хондроитин 0,25г капсулы 300мг 50 шт.
Краткое описание
Хондроитин сульфат улучшает фосфорно-кальциевый обмен в хрящевой ткани, ускоряет процессы ее восстановления.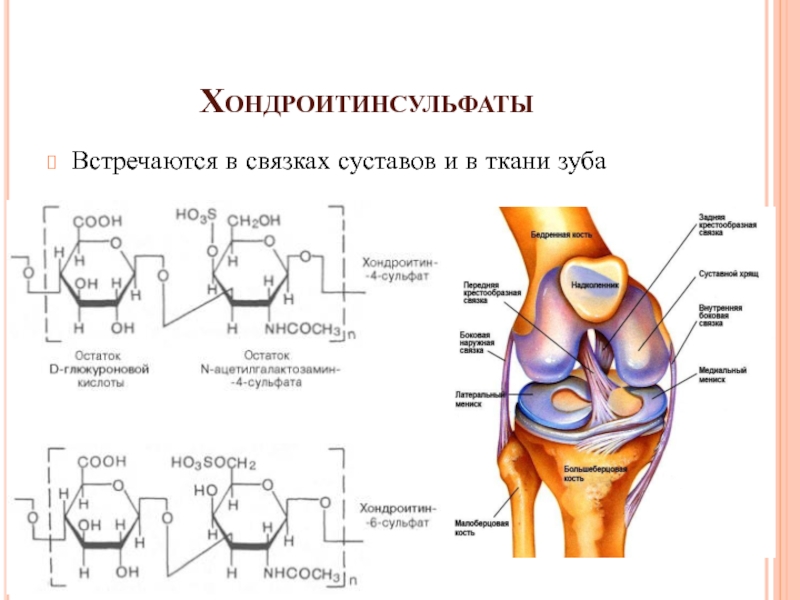 Это важный структурный компонент хрящевой ткани и связок. Входя в состав хряща, он придает ему упругость и амортизирующие свойства за счет удержания воды в ткани.
Это важный структурный компонент хрящевой ткани и связок. Входя в состав хряща, он придает ему упругость и амортизирующие свойства за счет удержания воды в ткани.
Состав
Хондроитина сульфат, лактоза, капсула (желатин, краситель диоксид титана), агент антислеживающий — кальция стеарат.
Фармакологическое действие
Стимулятор регенерации хрящевой ткани (хондропротектор). Высокомолекулярный мукополисахарид, получаемый из хрящей трахеи крупного рогатого скота. Влияет на обменные процессы в гиалиновом и волокнистом хрящах, уменьшает дегенеративные изменения в хрящевой ткани суставов, стимулирует биосинтез гликозаминогликанов. Способствует регенерации хрящевых поверхностей суставов и суставной сумки, увеличивает продукцию внутрисуставной жидкости. Замедляет резорбцию костной ткани и снижает потери кальция, ускоряет процессы восстановления костной ткани.
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. Терапевтический эффект сохраняется длительное время после окончания курса лечения.
Замедляет резорбцию костной ткани и снижает потери кальция, ускоряет процессы восстановления костной ткани.
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. Терапевтический эффект сохраняется длительное время после окончания курса лечения.
Показания
Рекомендуется в качестве биологически активной добавки к пище — источника хондроитинсульфата.
Способ применения и дозировка
Взрослым и детям старше 14 лет по 2 капсулы 2 раза в день во время еды, запивая не менее чем 1/2 стакана воды.
Побочные действия
Симптомы: редко — тошнота, рвота, диарея; при длительном приеме в чрезмерно высоких дозах (более 3 г/сут) возможны геморрагические высыпания. Лечение: проведение симптоматической терапии.
Лечение: проведение симптоматической терапии.
Противопоказания
Индивидуальная непереносимость компонентов продукта, беременность, период грудного вскармливания.
Передозировка
При одновременном применении препарата Хондроитин-АКОС с другими лекарственными средствами возможно усиление действия непрямых антикоагулянтов, антиагрегантов, фибринолитиков.
Особые указания
Препарат принимают внутрь, во время или после еды, запивая не менее чем 1/2 стакана воды. Взрослым и подросткам в возрасте 15 лет и старше назначают в дозе 1 г/сут — по 2 капсулы 2 раза/сут. Рекомендуемая продолжительность начального курса лечения составляет 6 месяцев. Период действия препарата после его отмены — 3-5 месяцев в зависимости от локализации и стадии заболевания. Продолжительность повторных курсов лечения врач устанавливает индивидуально.
Период действия препарата после его отмены — 3-5 месяцев в зависимости от локализации и стадии заболевания. Продолжительность повторных курсов лечения врач устанавливает индивидуально.
Взаимодействие с другими препаратами
Противопоказано применение у детей младше 15 лет ввиду отсутствия точных данных об эффективности и безопасности препарата у данной категории пациентов.
Chondroitin Sulfate (CS) — Хондроитинсульфат
Московский государственный университет
Исследовательский центр им.Алмазова
НЦ вирусологии и биотехнологии «Вектор»
Институт медико-биологических проблем РАН
Институт Цитологии и Генетики СО РАН
Институт физиологии им. Павлова
Сеченовский Университет
МНТК Микрохирургии глаза им. Федорова
Федорова
МФТИ
Институт экспериментальной медицины
Исследовательский центр им. Дмитрия Рогачева
НИЦ Курчатовский институт
Петербургский институт ядерной физики им. Б.П.Константинова
НИИ глазных болезней им. Гельмгольца
НЦ акушерства, гинекологии и перинатологии им.Кулакова
ИЭФБ РАН им.Сеченова
Национальный исследовательский университет Лобачевского
Томский научный исследовательский медицинский центр
Казанский Федеральный Университет
СЗГМУ им.Мечникова
Балтийский федеральный университет
Научный центр неврологии
Северо-Кавказский федеральный университет
Дальневосточный федеральный университет
ФНКЦ физико-химической медицины
ФНКЦ реаниматологии и реабилитологии
Сибирский федеральный университет
Институт биологии гена РАН
ФИЦ Питания и биотехнологий
Сибирский медицинский университет
Институт биофизики клетки РАН
НИПИ им. Бехтерева
Бехтерева
Институт Фундаментальных Проблем Биологии РАН
Институт токсикологии ФМБА России
НИИ Акушерства и гинекологии им. Отта
НИИ Психического здоровья
РМАПО
Красноярский медицинский университет им. Войно-Ясенецкого
Алтайский медицинский университет
Ниармедик
Волгоградский медицинский университет
Новосибирский медицинский университет
РНИОИ
ИБХ РАН им. акад. Шемякина и Овчинникова
Петровакс Фарм
Южно-Уральский государственный университет
ПИМУ
ФНЦ Пищевых систем им.Горбатова РАН
Найден способ вернуть памяти молодость
Британские ученые предложили инновационный метод лечения возрастной потери памяти. Доклинические исследования показывают, что снижение памяти у стареющих мышей можно обратить вспять, манипулируя составом структур мозга, известных как перинейрональные сети.
Доклинические исследования показывают, что снижение памяти у стареющих мышей можно обратить вспять, манипулируя составом структур мозга, известных как перинейрональные сети.
Перинейрональными сетями (PNN) называют структуры в головном мозге, которые помогают стабилизировать синаптическую активность – основной механизм памяти и обучения. По сути, они тормозят нейропластичность – способность человеческого мозга изменяться под действием опыта и восстанавливать утраченные по разным причинам связи между нейронами.
Предыдущие исследования на животных показали, что с возрастом PNN могут все более тормозить нейропластичность и нарушать формирование новых воспоминаний. Поэтому ученые предположили, что возрастную потерю памяти можно обратить вспять, воздействуя на PNN.
Стимулировать либо подавлять функцию PNN могут химические вещества под названием хондроитинсульфаты. Существуют несколько их разновидностей, и они действуют на клетки мозга по-разному – к примеру, хондроитин-6-сульфат и хондроитин-4-сульфат.
С возрастом баланс между этими двумя видами хондроитинсульфатов меняется. Исследователи подозревают, что в нарушении их баланса и скрыт механизм влияния PNN на возрастное снижение памяти.
Исследуя эту гипотезу, ученые изменили состав хондроитинсульфата у старых мышей. Уровни хондроитин-6-сульфата в PNN были восстановлены до уровней, наблюдаемых у молодых мышей. Результаты оказались впечатляющими. Память у старых мышей восстановилась до уровня их более молодых собратьев.
«Мы увидели замечательные результаты, когда лечили старых мышей этим препаратом, – утверждает Джессика Квок (Jessica Kwok), исследователь из Университета Лидса. – Память и способность к обучению были восстановлены до уровня, который у них был в далекой молодости».
Специально для эксперимента ученые вырастили генетически модифицированных мышей, у которых с рождения уровень хондроитин-6-сульфата был низким. Эти животные показали преждевременное ухудшение возрастной памяти по сравнению с их нормальными ровесниками. Когда генетически модифицированным мышам с помощью инъекции восстановили естественный уровень хондроитин-6-сульфата, их память улучшилась до уровня их нормальных ровесников.
Когда генетически модифицированным мышам с помощью инъекции восстановили естественный уровень хондроитин-6-сульфата, их память улучшилась до уровня их нормальных ровесников.
«Хотя наше исследование проводилось только на мышах, тот же механизм должен действовать и у людей – молекулы и структуры в человеческом мозге такие же, как и у грызунов, – отмечает Джеймс Фосетт (James Fawcett) из Кембриджского университета. – Это говорит о том, что можно предотвратить развитие потери памяти в пожилом возрасте».
Исследование британских ученых опубликовал журнал Molecular Psychiatry.
Ранее мы рассказывали, как некоторые люди сохраняют прекрасную память до самой старости. Еще мы писали, что продолжительность жизни мышей увеличили на 30% и что биологический возраст организма покажет хроническое воспаление.
Больше новостей из мира науки и медицины вы найдёте в разделах «Наука» и «Медицина» на медиаплатформе «Смотрим».
ХОНДРОИТИН СУЛЬФАТ лиофилизат — инструкция по применению, цена, дозировки, аналоги, противопоказания
Действующее вещество
— хондроитина сульфат (chondroitine sulfate sodium)
Состав и форма выпуска препарата
| Лиофилизат для приготовления раствора для в/м введения | 1 амп. |
| хондроитина сульфат | 100 мг |
100 мг — ампулы (10) — пачки картонные.
100 мг — ампулы (5) — пачки картонные.
100 мг — ампулы (5) — упаковки контурные пластиковые (1) — пачки картонные.
100 мг — ампулы (5) — упаковки контурные пластиковые (2) — пачки картонные.
100 мг — ампулы (5) — поддоны (2) — пачки картонные.
100 мг — ампулы (10) — коробки картонные.
Фармакологическое действие
Средство, влияющее на фосфорно-кальциевый обмен в хрящевой ткани, является высокомолекулярным мукополисахаридом. Оказывает хондростимулирующее, регенерирующее, противовоспалительное и анальгезирующее действие. Хондроитина сульфат участвует в построении основного вещества хрящевой и костной ткани. Обладает хондропротекторными свойствами, усиливает обменные процессы в гиалиновом и волокнистом хрящах, субхондриальной кости; ингибирует ферменты, вызывающие деградацию (разрушение) суставного хряща; стимулирует выработку хондроцитами протеогликанов. Способствует снижению выброса в синовиальную жидкость медиаторов воспаления и болевых факторов, подавляет секрецию лейкотриенов и простагландинов. Замедляет резорбцию костной ткани и снижает потери кальция, ускоряет процессы восстановления костной ткани. Хондроитина сульфат замедляет прогрессирование остеоартроза и остеохондроза. Способствует восстановлению суставной сумки и хрящевых поверхностей суставов, препятствует коллапсу соединительной ткани, нормализует продукцию суставной жидкости.
Способствует снижению выброса в синовиальную жидкость медиаторов воспаления и болевых факторов, подавляет секрецию лейкотриенов и простагландинов. Замедляет резорбцию костной ткани и снижает потери кальция, ускоряет процессы восстановления костной ткани. Хондроитина сульфат замедляет прогрессирование остеоартроза и остеохондроза. Способствует восстановлению суставной сумки и хрящевых поверхностей суставов, препятствует коллапсу соединительной ткани, нормализует продукцию суставной жидкости.
Обладая структурной схожестью с гепарином, потенциально может препятствовать образованию фибриновых тромбов в синовиальном и субхондриальном микроциркуляторном русле.
Новости по теме
Фармакокинетика
После в/м введения хондроитина сульфат натрия легко всасывается. Уже через 30 мин после инъекции он обнаруживается в крови в значительных концентрациях. Cmax хондроитина сульфат натрия в плазме достигается через 1 ч, затем постепенно снижается в течение 2 сут. Хондроитина сульфат натрия накапливается, главным образом, в хрящевой ткани, образующей суставы. Синовиальная оболочка не является препятствием для проникновения средства в полость сустава. Через 15 мин после в/м инъекции хондроитина сульфат натрия обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч.
Хондроитина сульфат натрия накапливается, главным образом, в хрящевой ткани, образующей суставы. Синовиальная оболочка не является препятствием для проникновения средства в полость сустава. Через 15 мин после в/м инъекции хондроитина сульфат натрия обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч.
Показания
Дегенеративно-дистрофические заболевания суставов и позвоночника (остеоартроз периферических суставов, межпозвонковый остеоартроз и остеохондроз), для ускорения формирования костной мозоли при переломах.
Противопоказания
Повышенная чувствительность к хондроитина сульфату, склонность к кровоточивости, тромбофлебиты; детский и подростковый возраст до 18 лет; беременность, период грудного вскармливания.
С осторожностью
Одновременное применение с антикоагулянтами прямого действия.
Дозировка
В/м назначают в дозе 100 мг через день. При хорошей переносимости дозу увеличивают до 200 мг, начиная с четвертой инъекции. Курс лечения — 25-30 инъекций. При необходимости возможно проведение повторных курсов лечения через 6 месяцев.
Курс лечения — 25-30 инъекций. При необходимости возможно проведение повторных курсов лечения через 6 месяцев.
Побочные действия
Аллергические реакции: нечасто — кожный зуд, эритема, крапивница, дерматит, ангионевротический отек.
Со стороны пищеварительной системы: часто — диарея, боли в животе, тошнота; частота неизвестна — рвота.
Местные реакции: боль и геморрагии в месте инъекции.
Лекарственное взаимодействие
Возможно усиление действия непрямых антикоагулянтов, антиагрегантов, фибринолитиков, что требует более частого контроля показателей свертывания крови при совместном применении.
Особые указания
При аллергических реакциях или геморрагиях лечение следует прекратить.
Беременность и лактация
Противопоказано применение при беременности и в период грудного вскармливания.
Применение в детском возрасте
Противопоказано применение у детей и подростков в возрасте до 18 лет.
Применение в пожилом возрасте
Специальные указания по применению у пациентов пожилого возраста отсутствуют.
Описание препарата ХОНДРОИТИН СУЛЬФАТ основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Хондроитин сульфат в лечении остеоартроза
Остеоартроз (ОА) представляет собой гетерогенную группу заболеваний различной этиологии, которые имеют сходные биологические, морфологические и клинические проявления и исход, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондрального участка кости, синовиальной оболочки, связок, капсулы, периартикулярных мышц.
Рентгенографические признаки заболевания выявляются приблизительно у 50 % людей в возрасте 55 лет и у 80 % лиц старше 75 лет. При этом ОА остается основной причиной нетрудоспособности в США и других развитых странах.
Наиболее важным клиническим симптомом ОА является боль, обычно небольшая в начале, от легкой до умеренной по интенсивности, усиливается при нагрузке на сустав и уменьшается в покое. Появление боли в течение ночи свидетельствует о более тяжелой форме заболевания. Интересно, что боль при ОА — это не просто результат структурных изменений в пораженном суставе, но скорее исход комплексного взаимодействия между структурными изменениями, механизмами периферической и центральной боли и субъективными составляющими боли, на которые, в свою очередь, влияют образование, пол и психосоциальные факторы.
Диагностика ОА в подавляющем большинстве случаев не вызывает больших трудностей и основывается на клинических и рентгенологических (сужение суставной щели, краевые остеофиты) признаках. Исключение составляют больные с признаками воспаления суставов (например, при генерализованном ОА, поражающем мелкие суставы кистей). Кроме того, иногда возникают проблемы при дифференциальной диагностике первичного и вторичного ОА, связанного с метаболическими и другими заболеваниями.
Исключение составляют больные с признаками воспаления суставов (например, при генерализованном ОА, поражающем мелкие суставы кистей). Кроме того, иногда возникают проблемы при дифференциальной диагностике первичного и вторичного ОА, связанного с метаболическими и другими заболеваниями.
Фармакотерапия ОА до недавнего времени была направлена скорее на уменьшение симптомов болезни, нежели на ее причину. Анальгетики, нестероидные противовоспалительные препараты (НПВП) и стероиды составляли основу лечения ОА. Однако побочные эффекты большинства этих лекарственных средств заставили пересмотреть показания к их широкому назначению больным ОА и способствовали разработке препаратов, способных контролировать течение болезни. К таким препаратам относится хондроитин сульфат (ХС).
ХС является основным компонентом большинства тканей и присутствует преимущественно в экстрацеллюлярном матриксе. Наиболее богаты им соединительная ткань, хрящ, кожа, стенки сосудов и костная ткань, а также связки и сухожилия.
ХС представляет собой гликозаминогликан. Это полисахаридная цепь, построенная из дисахаридов, образованных уроновыми кислотами (глюкуроновой, галактуроновой и идуроновой), N-ацетилгексозаминами и нейтральными сахаридами. Данные полисахаридные цепи не способны к самостоятельному существованию в тканях и соединяются ковалентной связью с белками, образуя протеогликаны.
ХС используется в лечебной практике свыше 20 лет. За это время проведено более 20 контролируемых исследований эффективности препарата при ОА, в которых доказан симптоматический эффект ХС при ОА коленных, тазобедренных суставов и суставов кистей (табл. 1).
В 1992 г. B. Mazieres c соавт. было проведено двойное слепое плацебо-контролируемое исследование, в которое вошли 120 пациентов с ОА коленных суставов, принимавших ХС в дозе 1 г/сут по интермиттирующей схеме (3 месяца приема, 2 месяца наблюдения). Основным критерием эффективности была потребность больных в НПВП. По завершении 3-месячной терапии пациенты, принимавшие ХС, испытывали значительно меньшую потребность в НПВП, причем эта тенденция сохранялась в течение последующего наблюдения. Помимо этого, отмечено достоверное снижение интенсивности боли в коленных суставах по визуальной аналоговой шкале (ВАШ), уменьшение функционального индекса Лекена и улучшение оценки общего состояния здоровья пациентами. Переносимость препарата была хорошей, и все больные закончили исследование [10].
Помимо этого, отмечено достоверное снижение интенсивности боли в коленных суставах по визуальной аналоговой шкале (ВАШ), уменьшение функционального индекса Лекена и улучшение оценки общего состояния здоровья пациентами. Переносимость препарата была хорошей, и все больные закончили исследование [10].
В 1998 г. симптом-модифицирующие свойства ХС были подтверждены в другом рандомизированном двойном слепом плацебо-контролируемом исследовании L. Bucsi и G. Poor, в котором проводилось сравнение эффективности ХС в дозе 800 мг/сут (40 больных) с плацебо (40 больных) в течение 6 месяцев. В исследование вошли пациенты с 1–3-й рентгенологическими стадиями гонартроза по Келлгрену. Клинические симптомы оценивались в начале, через 1, 3 и 6 месяцев терапии. У больных, получавших ХС, отмечено достоверное улучшение по индексу Лекена, выраженности боли по ВАШ и времени прохождения 20 метров. Потребность в приеме парацетамола была ниже в группе больных, принимавших ХС, но различия не были достоверными [11].
P. Bourgeois с соавт. провели многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. В исследование вошли 127 больных с гонартрозом 1–3-й стадий по Келлгрену: 40 больных принимали ХС в дозе 1200 мг/сут в виде геля per os, 43 больных — аналогичную дозу ХС в капсулах (400 мг 3 раза в сутки) и 44 больных получали плацебо. Длительность терапии составила 3 месяца. В обеих группах больных, принимавших ХС, отмечалось значительное снижение интенсивности боли (оцененной по ВАШ) и индекса Лекена (р < 0,01) по сравнению с группой плацебо. Переносимость терапии была хорошей, все больные закончили исследование. Авторы заключили, что ХС уменьшает клинические симптомы ОА и улучшает функциональную способность суставов. Эффективность ХС, принимаемого в дозе 1200 мг/сут однократно, не отличалась от эффективности 3-кратного приема 400 мг ХС [12].
Способность ХС влиять на симптомы ОА была доказана в исследовании P. Morreale с соавт., которые оценили эффективность ХС у 146 пациентов с гонартрозом. 74 больных получали ХС по 400 мг 3 раза в сутки в течение 3 месяцев с последующим 3-месячным наблюдением. 72 больных принимали диклофенак 150 мг/сут, на фоне которого отмечалось уменьшение боли в коленных суставах к 10-му дню терапии и возобновление ее через очень короткий промежуток времени после прерывания лечения . В группе ХС симптоматический эффект отмечался через 1 месяц от начала терапии и сохранялся в течение 3 месяцев после ее окончания. Индекс Лекена через 3 месяца лечения снизился на 78 % от исходного, по окончании 3 месяцев наблюдения он оставался на 64,4 % ниже первоначального значения. В группе диклофенака снижение индекса составило 62,6 %, через 3 месяца после прекращения приема диклофенака — только 29,7 %. Таким образом, в этом исследовании авторы показали не только более высокую эффективность ХС, но и выраженный эффект последействия препарата по сравнению с традиционной терапией НПВП [13].
74 больных получали ХС по 400 мг 3 раза в сутки в течение 3 месяцев с последующим 3-месячным наблюдением. 72 больных принимали диклофенак 150 мг/сут, на фоне которого отмечалось уменьшение боли в коленных суставах к 10-му дню терапии и возобновление ее через очень короткий промежуток времени после прерывания лечения . В группе ХС симптоматический эффект отмечался через 1 месяц от начала терапии и сохранялся в течение 3 месяцев после ее окончания. Индекс Лекена через 3 месяца лечения снизился на 78 % от исходного, по окончании 3 месяцев наблюдения он оставался на 64,4 % ниже первоначального значения. В группе диклофенака снижение индекса составило 62,6 %, через 3 месяца после прекращения приема диклофенака — только 29,7 %. Таким образом, в этом исследовании авторы показали не только более высокую эффективность ХС, но и выраженный эффект последействия препарата по сравнению с традиционной терапией НПВП [13].
Способность ХС контролировать течение ОА продемонстрировано в ходе годичного рандомизированного плацебо-контролируемого исследования, которое включало 42 больных обоих полов в возрасте 35–78 лет с симптоматическим ОА коленных суставов [14]. Для оценки ширины суставной щели коленного сустава использовался компьютеризированный анализ. Группа ХС принимала препарат в дозе 800 мг/сут. Помимо клинической оценки ОА (выраженность боли и функциональная недостаточность), проводилась оценка ширины суставной щели в медиальном отделе тибиофеморального сустава, а также уровень биохимических маркеров костного и хрящевого метаболизма. Исследование подтвердило, что ХС вызывает достоверное уменьшение болевого синдрома и функциональной недостаточности. Через год изменения ширины суставной щели в группе ХС не наблюдалось, в то время как в группе плацебо отмечено заметное ее сужение. Отмечалась стабилизация костного и хрящевого обмена на фоне приема ХС. И хотя исследование было пилотным и включало небольшое число больных, авторам удалось показать, что ХС способен не только влиять на симптомы ОА, но и оказывать структурно-модифицирующее действие, то есть стабилизировать ширину суставной щели в тибиофеморальном суставе.
Для оценки ширины суставной щели коленного сустава использовался компьютеризированный анализ. Группа ХС принимала препарат в дозе 800 мг/сут. Помимо клинической оценки ОА (выраженность боли и функциональная недостаточность), проводилась оценка ширины суставной щели в медиальном отделе тибиофеморального сустава, а также уровень биохимических маркеров костного и хрящевого метаболизма. Исследование подтвердило, что ХС вызывает достоверное уменьшение болевого синдрома и функциональной недостаточности. Через год изменения ширины суставной щели в группе ХС не наблюдалось, в то время как в группе плацебо отмечено заметное ее сужение. Отмечалась стабилизация костного и хрящевого обмена на фоне приема ХС. И хотя исследование было пилотным и включало небольшое число больных, авторам удалось показать, что ХС способен не только влиять на симптомы ОА, но и оказывать структурно-модифицирующее действие, то есть стабилизировать ширину суставной щели в тибиофеморальном суставе.
В другом РКИ после 1 года лечения 100 пациентов с остеоартрозом коленных суставов в виде 2 трехмесячных курсов приема хондроитина сульфата 800 мг/сут отмечено снижение индекса Лекена на 36 % против 23 % в группе плацебо. Подобное же соотношение получено и по другим вторичным показателям. В группе хондроитина сульфата не отмечено рентгенологических признаков сужения суставной щели, в то время как в группе плацебо сужение было значительным. Таким образом, получены доказательства того, что хондроитин сульфат уменьшает боль и улучшает функцию коленного сустава. Замедление рентгенологического прогрессирования сужения суставной щели при использовании хондроитина сульфата расценено как дополнительное доказательство в пользу его структурно-модифицирующих свойств [15].
Подобное же соотношение получено и по другим вторичным показателям. В группе хондроитина сульфата не отмечено рентгенологических признаков сужения суставной щели, в то время как в группе плацебо сужение было значительным. Таким образом, получены доказательства того, что хондроитин сульфат уменьшает боль и улучшает функцию коленного сустава. Замедление рентгенологического прогрессирования сужения суставной щели при использовании хондроитина сульфата расценено как дополнительное доказательство в пользу его структурно-модифицирующих свойств [15].
Важные результаты получены в процессе 6-месячного открытого рандомизированного многоцентрового (9 центров) исследования эффективности и безопасности ХС в России, в которое были включены 555 пациентов с ОА коленного или тазобедренного суставов 1–3-й стадий. Основную группу составили 192 пациента, контрольную группу — 363 пациента. Препарат назначали в дозе 1,5 г/сут в течение первых 3 недель, затем 1 г/сут. На фоне лечения отмечена достоверная положительная динамика индекса Лекена (в 2 раза при гонартрозе и в 2,5 раза при коксартрозе, p < 0,05), боли в покое (в 3,8 раза при гонартрозе и в 3 раза при коксартрозе, p < 0,05) и при ходьбе (p < 0,05) и потребности в НПВП (в 5,7 раза при гонартрозе и в 4,6 раза при коксартрозе). В целом клиническое улучшение отмечено у 90,2 % пациентов. После завершения исследования лечебный эффект сохранялся в течение 4,1 мес. при коксартрозе и 4,6 мес. при гонартрозе. Интересные данные были получены при анализе динамики ОА за год после окончания лечения ХС, свидетельствующие о том, что терапия ХС в течение даже относительно короткого периода времени способствовала в дальнейшем снижению частоты обострений заболевания, а следовательно, госпитализаций и обращений больных в поликлиники, что, безусловно, имеет важное значение с точки зрения улучшения качества жизни больных ОА [16].
В целом клиническое улучшение отмечено у 90,2 % пациентов. После завершения исследования лечебный эффект сохранялся в течение 4,1 мес. при коксартрозе и 4,6 мес. при гонартрозе. Интересные данные были получены при анализе динамики ОА за год после окончания лечения ХС, свидетельствующие о том, что терапия ХС в течение даже относительно короткого периода времени способствовала в дальнейшем снижению частоты обострений заболевания, а следовательно, госпитализаций и обращений больных в поликлиники, что, безусловно, имеет важное значение с точки зрения улучшения качества жизни больных ОА [16].
Метаанализ 7 исследований, включавших 372 пациента с ОА коленных суставов, леченных ХС в дозе 800–1600 мг/сут в течение 6 месяцев и более, показал достоверное уменьшение боли и функционального индекса Лекена по сравнению с плацебо [17].
В другом метаанализе 15 рандомизированных контролируемых исследований за период 1966–1999 гг. (404 больных ОА с преимущественным поражением коленных и тазобедренных суставов) свидетельствуют об эффективности препарата по сравнению с плацебо по влиянию на болевой синдром, функциональный индекс Лекена, уменьшению дозы принимаемых НПВП и анальгетиков. Кроме того, отмечена хорошая переносимость хондроитина сульфата [18], также исследовалось применение ХС и глюкозамина при остеоартрозе коленных суставов, получен обобщенный эффект: для глюкозамина — 0,44 (95 % ДИ, 0,24–0,64), для хондроитина сульфата — 0,78 (95% ДИ, 0,60–0,95) [9].
Кроме того, отмечена хорошая переносимость хондроитина сульфата [18], также исследовалось применение ХС и глюкозамина при остеоартрозе коленных суставов, получен обобщенный эффект: для глюкозамина — 0,44 (95 % ДИ, 0,24–0,64), для хондроитина сульфата — 0,78 (95% ДИ, 0,60–0,95) [9].
В 1998 г. опубликованы результаты рандомизированного двойного слепого плацебо-контролируемого проспективного исследования хондроитина сульфата у больных ОА суставов кистей. В исследование вошли 119 больных, 34 больных принимали ХС 1200 мг/сут, 85 больных — плацебо. Длительность терапии составила 3 года, в течение которых ежегодно проводилась рентгенография кистей. В группе ХС за 3-летний период выявлено достоверное уменьшение числа новых эрозий в суставах кистей [19]. Эти данные были подтверждены исследованиями G. Rovetta с соавт. на основании лечения 24 больных ХС в дозе 800 мг/сут в течение 2 лет [20].
Дальнейшие исследования ХС были направлены на изучение структурно-модифицирующих свойств препарата при ОА коленных суставов. Исследование, проведенное B.A. Michel с соавт., было первым, в котором использовалась структурная конечная точка (динамика изменения ширины суставной щели) в качестве главного критерия оценки действия ХС. Было показано, что терапия ХС в дозе 800 мг/сут в течение 2 лет оказывала статистически достоверное стабилизирующее влияние на ширину суставной щели у больных гонартрозом [21]. В 2006 г. на сессии EULAR A. Kahan c соавт. доложили результаты исследования STOPP, согласующиеся с результатами предыдущей работы. На основании анализа результатов лечения ХС в течение 2 лет 622 больных гонартрозом было показано замедление прогрессирования заболевания у пациентов, леченных ХС, по сравнению с плацебо-группой.
Исследование, проведенное B.A. Michel с соавт., было первым, в котором использовалась структурная конечная точка (динамика изменения ширины суставной щели) в качестве главного критерия оценки действия ХС. Было показано, что терапия ХС в дозе 800 мг/сут в течение 2 лет оказывала статистически достоверное стабилизирующее влияние на ширину суставной щели у больных гонартрозом [21]. В 2006 г. на сессии EULAR A. Kahan c соавт. доложили результаты исследования STOPP, согласующиеся с результатами предыдущей работы. На основании анализа результатов лечения ХС в течение 2 лет 622 больных гонартрозом было показано замедление прогрессирования заболевания у пациентов, леченных ХС, по сравнению с плацебо-группой.
Как известно, ХС является нетоксичной субстанцией, поскольку это природный компонент, входящий в состав соединительной ткани человека и животных. Результаты многочисленных проведенных исследований свидетельствуют о хорошей переносимости препарата. Более того, длительное использование ХС в некоторых европейских странах (во Франции с 1969 г. , в Швейцарии с 1982 г., в Италии с 1990 г.) не выявило развития каких-либо токсических реакций.
, в Швейцарии с 1982 г., в Италии с 1990 г.) не выявило развития каких-либо токсических реакций.
Таким образом, экспериментальные и клинические исследования свидетельствуют о статистически достоверном уменьшении болевого синдрома у больных ОА коленных, тазобедренных суставов и суставов кистей на фоне терапии ХС по сравнению с плацебо. При ОА коленных суставов отмечено улучшение функционального индекса Лекена и уменьшение суточной потребности в НПВП и анальгетиках. Кроме того, эффект после отмены ХС сохраняется в среднем в течение 3 месяцев в отношении болевого синдрома и функции суставов. Чрезвычайно интересны данные по влиянию ХС на прогрессирование ОА суставов кистей (образование новых эрозий) и коленных суставов (рентгенологическая динамика суставной щели), вместе с тем они требуют дальнейших подтверждений. И хотя механизм действия препарата на различные патогенетические звенья заболевания до конца не ясен, приведенные данные доказывают эффективность ХС при ОА, на основании чего он внесен в рекомендации EULAR по лечению ОА коленных, тазобедренных суставов и суставов кистей.
Впервые опубликована в «Русском медицинском журнале» (т. 15, № 8, 2007)
От исследований in vitro к клиническим рекомендациям
Ther Adv Musculoskelet Dis. 2010 Dec; 2 (6): 335–348.
Мариан Мати
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Кристель Санчес
2 Исследовательское отделение костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Cecile Lambert
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
2 Кости и Отделение исследования хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
1 Отделение исследования костей и хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия eb.ca.glu@nitornehyЭта статья цитируется другими статьями в PMC.
Abstract
Хондроитинсульфат (CS) рекомендуется в качестве терапевтического вмешательства при мультимодальном подходе к лечению остеоартрита (OA). CS был тщательно изучен для описания его фармакологии (фармакокинетических эффектов, эффектов in vitro и in vivo) и клинической эффективности. Сообщалось о различных результатах в зависимости от системы оценки (модель, дозировка и продолжительность) и источника CS (происхождение и качество).Целью этого обзора было собрать большую часть доступной информации о CS и обсудить его эффективность в управлении OA.
Ключевые слова: хрящ, хондроитинсульфат, остеоартрит, механизм действия, фармакокинетика
Введение
Хондроитинсульфат (CS) является основным компонентом внеклеточного матрикса (ECM) многих соединительных тканей, включая хрящ, кость, кожу , связки и сухожилия. Остеоартрит (ОА) характеризуется прогрессирующими структурными и метаболическими изменениями в тканях суставов, в основном деградацией хряща, склерозом субхондральной кости и воспалением синовиальной оболочки. Лечение остеоартрита включает мультимодальное терапевтическое вмешательство, поскольку на сегодняшний день лечения не найдено. Для лечения ОА необходимы препараты, которые могут замедлить, остановить или даже избежать деградации суставов. Многие из рекомендуемых вмешательств представляют только эффекты, изменяющие симптомы, и несколько эффектов, изменяющих структуру.
Лечение остеоартрита включает мультимодальное терапевтическое вмешательство, поскольку на сегодняшний день лечения не найдено. Для лечения ОА необходимы препараты, которые могут замедлить, остановить или даже избежать деградации суставов. Многие из рекомендуемых вмешательств представляют только эффекты, изменяющие симптомы, и несколько эффектов, изменяющих структуру.
CS и другие соединения, такие как глюкозамин, используются в медицинских целях более 40 лет. CS продается как безрецептурная пищевая добавка в Северной Америке и отпускается по рецепту в соответствии с правилами Европейского медицинского агентства (EMEA) в Европе.В последние десятилетия CS вызывал много интересов в качестве потенциального терапевтического средства против ОА. CS является частью рекомендаций Международного общества исследований остеоартрита (OARSI) по лечению остеоартрита коленного сустава [Zhang et al. 2010, 2008] и рекомендаций Европейской лиги против ревматизма (EULAR) по лечению тазобедренного и коленного суставов OA Zhzang et al. 2005; Jordan et al. 2003]. ХС и глюкозамин могут стать отличной альтернативой для пациентов с ОА.
2005; Jordan et al. 2003]. ХС и глюкозамин могут стать отличной альтернативой для пациентов с ОА.
CS, как естественный компонент ЕСМ, представляет собой сульфатированный гликозаминогликан (ГАГ), состоящий из длинной неразветвленной полисахаридной цепи с повторяющейся дисахаридной структурой N-ацетилга-лактозамина и глюкуроновой кислоты.Большинство остатков N-ацетилгалактозамина () сульфатированы, особенно в положениях 4 и 6, что делает CS сильно заряженным полианионом. CS отвечает за многие важные биомеханические свойства хряща, такие как сопротивление и эластичность. Его высокое содержание в аггрекане играет важную роль в обеспечении устойчивости хряща к давлению при различных условиях нагрузки. Профиль сульфатации хондроитина был описан в хрящах [Mourao, 1988]. Изменения в структуре CS описаны в тканях OA [Caterson et al. 1990] и пониженное соотношение CS-6: CS-4 были обнаружены в синовиальной жидкости и хрящах пациентов с ОА [Shinmei et al. 1992]. Более трех десятилетий назад было предложено [Schwartz and Dorfman, 1975], что поставка CS в качестве терапевтического вмешательства при повреждении хряща может обеспечить строительные блоки для синтеза нового компонента матрикса, поскольку повышение концентрации CS может действовать в пользу матрикса. регенерация и учитывать ее благотворное влияние.
Более трех десятилетий назад было предложено [Schwartz and Dorfman, 1975], что поставка CS в качестве терапевтического вмешательства при повреждении хряща может обеспечить строительные блоки для синтеза нового компонента матрикса, поскольку повышение концентрации CS может действовать в пользу матрикса. регенерация и учитывать ее благотворное влияние.
Химическая структура хондроитинсульфата, где R — Na или H, а X — SO 3 R или H.
Однако с тех пор механизм действия CS как терапевтического вмешательства все еще требует выяснения, а его эффективность остается предметом дискуссий.
Общая цель этого обзора состояла в том, чтобы собрать большую часть доступной информации о CS, его фармакокинетике, его эффектах in vitro, и in vivo, и его клинической эффективности. Цель этого обзора — обсудить клиническую полезность CS и перспективы использования CS при лечении остеоартрита.
Фармакокинетика
Natural CS имеет молекулярную массу 50–100 кДа. После процесса экстракции молекулярная масса составляет 10-40 кДа в зависимости от сырья. CS в основном получают из бычьего, свиного или морского (акульего) хряща.
После процесса экстракции молекулярная масса составляет 10-40 кДа в зависимости от сырья. CS в основном получают из бычьего, свиного или морского (акульего) хряща.
CS чаще всего вводят перорально в дозах от 800 до 1200 мг / день. CS быстро всасывается в желудочно-кишечном тракте. Поглощенный CS достигает компартмента крови в виде 10% CS и 90% деполимеризованных низкомолекулярных производных.
Сообщалось о различной биодоступности и фармакокинетических переменных в зависимости от характеристик и происхождения CS [Malavaki et al. 2008]. О некоторых из них сообщили в. Биодоступность CS обсуждается. Данные зависят от системы, используемой для оценки, структуры и характеристик CS, таких как молекулярная масса, плотность заряда и кластер дисульфатированных дисахаридов, используемой концентрации и вида животных, использованных для проведения исследования [Volpi, 2003]. В большинстве исследований использовался CS из трахеи крупного рогатого скота (чистота 95%), который представляет собой тот же материал, который использовался в клинических испытаниях [Barnhill et al.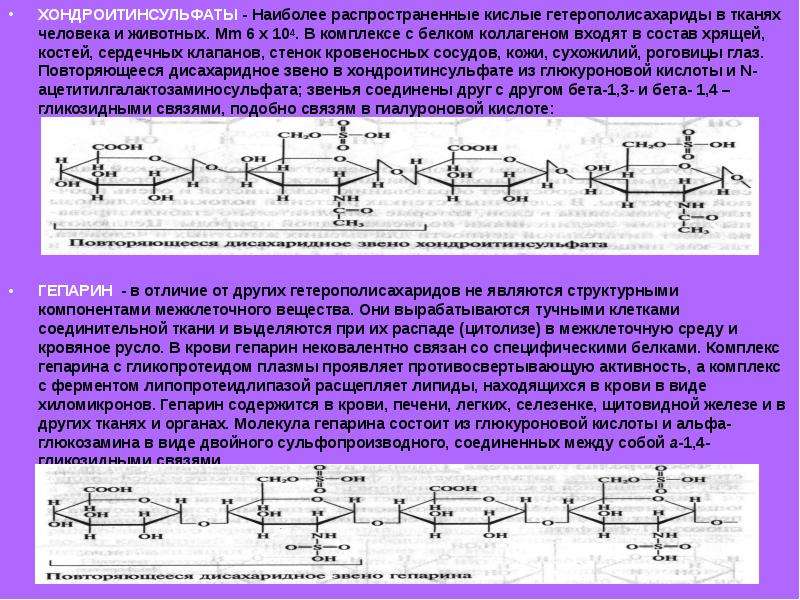 2006].
2006].
Таблица 1.
Различные фармакокинетические параметры в зависимости от системы исследования и источника CS.
| Исследование | Источник хондроитина | Система | Результаты | |
|---|---|---|---|---|
| Conte et al. [1995] | Трахея крупного рогатого скота 16 мг / кг перорально | Крысы Wistar | ||
| Трахея крупного рогатого скота 16 мг / кг перорально | Молодые собаки породы бигль | |||
Трахея крупного рогатого скота Разовая доза 0. 8 г или две дозы по 0,4 г 8 г или две дозы по 0,4 г | Здоровые добровольцы ( N = 12; 6 мужчин и 6 женщин) | Разовая доза: | Две дозы: | |
| Трахея крупного рогатого скота Разовая доза 0,8 г / день | Пациенты с ОА ( N = 18) | Концентрация в плазме:
| ||
| Ronca . [1998] | Смесь CS-6 и CS-4 (1: 1) Пероральное введение 16 мг / кг (4 мг / крыса) | Крысы ( N = 10) |
| |
| Volpi [2002] | Хондросульф® однократная доза (4 г) | Мужчина здоровый волонтеры ( N = 20) | ||
| Volpi [2003] | Shark CS Однократная доза (4 г) | Здоровые добровольцы мужского пола ( N = 20) |
Биодоступность CS после перорального приема колеблется от 10% до 20% [Lauder, 2009].
Поглощение CS может зависеть от статуса сульфатации. Положение и процентное содержание сульфатных групп обычно варьируется в зависимости от конкретных источников животного происхождения [Volpi, 2006a, 2006b]. Действительно, десульфатированный хондроитин у мышей [Kusano et al. 2007] имеет очень быстрое поглощение, с пиком в течение 15 минут и очень быстрым возвращением к исходному уровню через 3 часа, тогда как CS у акул у здоровых добровольцев мужского пола поглощается медленнее (пик через 8,7 часа) и медленнее выведение (уровни поддерживаются). до 16 часов после администрирования) [Volpi, 2003].CS из трахеи крупного рогатого скота демонстрирует быстрое увеличение плазмы здоровых добровольцев мужского пола с пиком в пределах 1–5 часов после введения и возвращением к исходному уровню через 10 часов [Volpi, 2002].
Фармакокинетические параметры CS, определенные у здоровых добровольцев мужского пола [Volpi, 2002], после перорального приема показали значительное увеличение уровней CS в плазме (более чем на 200%) по сравнению с уровнями перед дозой в течение 24 часов. Пиковые концентрации наблюдались через 2 часа после дозирования, и увеличение значимо через 2-6 часов после дозирования.Кинетика первого порядка наблюдалась для доз до 3000 мг. Многократные дозы 800 мг для пациентов с ОА не изменяют кинетику CS. Недавно, используя флуорофорный углеводный электрофорез и хроматографию наложения 6, Джексон и его коллеги не наблюдали никаких изменений эндогенной концентрации (20 (мкг / мл) и состава дисахаридов CS после перорального приема однократной дозы 1200 мг CS. Одно объяснение может быть, что небольшое количество проглоченного CS достигает циркуляции в неизмененной форме или состоит из дисахаридов более крупных фрагментов [Jackson et al. 2010]; в качестве альтернативы, могло случиться так, что анализ был недостаточно чувствителен для обнаружения более низких концентраций. Это еще предстоит продемонстрировать другими методами анализа. Другой характеристикой CS является его способность накапливаться в суставных тканях. Высокое содержание меченого CS было обнаружено в тканях суставов, включая синовиальную жидкость и хрящ, после перорального введения людям [Ronca et al.
Пиковые концентрации наблюдались через 2 часа после дозирования, и увеличение значимо через 2-6 часов после дозирования.Кинетика первого порядка наблюдалась для доз до 3000 мг. Многократные дозы 800 мг для пациентов с ОА не изменяют кинетику CS. Недавно, используя флуорофорный углеводный электрофорез и хроматографию наложения 6, Джексон и его коллеги не наблюдали никаких изменений эндогенной концентрации (20 (мкг / мл) и состава дисахаридов CS после перорального приема однократной дозы 1200 мг CS. Одно объяснение может быть, что небольшое количество проглоченного CS достигает циркуляции в неизмененной форме или состоит из дисахаридов более крупных фрагментов [Jackson et al. 2010]; в качестве альтернативы, могло случиться так, что анализ был недостаточно чувствителен для обнаружения более низких концентраций. Это еще предстоит продемонстрировать другими методами анализа. Другой характеристикой CS является его способность накапливаться в суставных тканях. Высокое содержание меченого CS было обнаружено в тканях суставов, включая синовиальную жидкость и хрящ, после перорального введения людям [Ronca et al. 1998].
1998].
Трудно оценить релевантность максимальной концентрации, достигнутой в компартменте крови (Cmax) для этого типа лекарственного средства, поскольку in vivo ответ может быть результатом воздействия CS и дисахаридов.Более того, CS — это препарат замедленного действия, в результате чего действие начинается медленно, а максимальный эффект достигается через несколько месяцев. Кроме того, CS — это лекарство биологического происхождения, что означает, что его измерение в биологических жидкостях не позволяет отличить лекарство от эндогенных молекул. Максимальный эффект (Emax) был предсказан с использованием альтернативного метода [du Souich and Verges, 2001]. Эффект Emax рассчитывали на основании клинической эффективности. Было подсчитано, что 50% Emax достигается за 35 дней у пациентов с легким ОА.Примерный период полураспада CS и его производных в плазме крови человека составляет 15 часов. Стабильное состояние достигается через 3–4 дня, и для получения максимального эффекта может потребоваться 3–6 месяцев лечения.
CS не метаболизируется цитохромом P450. Это говорит в пользу очень низкого риска взаимодействия с другими лекарствами.
Наконец, для CS был описан эффект переноса. Действительно, после отсроченного начала действия максимальный эффект сохраняется после прекращения терапии.
Механизм действия
Многие эффекты были описаны для CS в различных исследованиях in vitro, и in vivo, с использованием различных типов и концентраций CS и различных моделей.Точный механизм действия еще предстоит уточнить. In vitro эффекты на суставные клетки и эффекты in vivo на моделях артрита описаны в и, соответственно.
Таблица 2.
In vitro эффекты хондроитинсульфата.
| Исследование | Хондроитин | Система и продолжительность | Результаты | ||||
|---|---|---|---|---|---|---|---|
Verbruggen et al. [1977] [1977] | 10–400 мкг / мл | Однослойные синовиальные клетки | Стимуляция 11% синтеза гиалуроната во время фазы роста | ||||
| Увеличение на 88% во время стационарной фазы | |||||||
| Bassleer et al. [1998] | КРС 100–1000 мкг / мл | Суставные хондроциты человека в кластерах, стимулированные IL-1β До 32 дней | Значительное снижение продукции PGE, стимулированной IL-1β 2 | ||||
| Увеличение выработки коллагена PG и типа II | |||||||
Wang et al. [2002] [2002] | C poly S 10 мкг / мл | Человеческие суставные хондроциты в агарозном геле, стимулированные IL-1β 1 неделя | Стимуляция аггрекана, гиалуронана и коллагена типа II из-за подавления ММП | ||||
| Campo et al. al. [2004] | CS-4 1,0 и 2,0 мг / мл | Фибробласт кожи человека | Антиоксидантное действие CS-4 за счет повышения жизнеспособности клеток и ингибирования фрагментации ДНК | ||||
| Chan et al. [2005a] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Снижение IL-1β-индуцированной MMP-13 | ||||
Chan et al. [2005b] [2005b] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Подавление индуцированной IL-1β экспрессии NO-синтазы, COX-2 и mPGES-1 | ||||
| Монфорт и др. [2005] | 10–1000 мкг / мл | Хондроциты ОА человека, стимулированные IL-1β 48 ч | Ингибирование MMP-3 | ||||
| Holzmann et al. [2006] | 25 мкг / мл | Человеческие суставные хондроциты, стимулированные LPS До 72 часов | Ингибирование MMP-13 за счет снижения активации p38 и Erk1 / 2 | ||||
Tat et al. [2007] [2007] | 200 мкг / мл | Остеобласты субхондральной кости человека ОА До 48 ч | Снижение прорезорбтивных агентов | ||||
| Обратное действие витамина D3 на соотношение OPG: RANK9584 | Tahiri et al. [2008] | Хондросульф® или свинья 10 или 100 мкг / мл | Хондроциты суставов кролика, стимулированные IL-1β 20 ч | Повышение синтеза PG | |||
| Ингибирование экспрессии AD10AMTS-5 | |||||||
Jomphe et al. [2008] [2008] | Очищенные бычьи CS-4 и CS-6 200 мг / мл | Хондроциты кролика, стимулированные IL-1β 48 ч | Снижение ядерной транслокации NF-κB | ||||
| Профилактика активации Erk1 / 2 и p38 | |||||||
| Снижение апоптоза, индуцированного нитропруссидом | |||||||
| Legendre et al. [2008] | Avian CS −100 мкг / мл | Бычьи суставные хондроциты в гипоксических альгинатных гранулах 24–48 часов | Снижение IL-1β-индуцированных MMP-1, −3, −13 и ADAMTS-4 и — 5 | ||||
| Снижение IL-1β-индуцированного COX-2 и iNOS | |||||||
| Снижение продукции PGE 2 , но не NO | Незначительное увеличение синтеза ГАГ | ||||||
| Противодействие подавлению IL-1β рецепторов TGFβ | |||||||
Katta et al. [2009] [2009] | Смесь CS A, CS B и CS C 10–50 мг / мл | Эксплантаты бычьего хряща 24 ч | Эффективная смазка для суставов | ||||
| Распространение в хрящ | |||||||
| Давид-Рауди et al. [2009] | Avian CS 100 мкг / мл | OA фибробластоподобные синвиоциты человека 48 часов с предварительной обработкой | Регулирование гиалуронансинтазы | ||||
| Campo et al. [2009a] | CS-4 крупного рогатого скота и CS-6 акулы 0,5 и 1,0 мг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Антиапоптотический эффект обоих CS | ||||
| Ингибирование медиаторов воспаления, iNOS и MMP более очевидно с CS-4, чем с CS-6 | |||||||
Campo et al. [2009b] [2009b] | CS-4 крупного рогатого скота и CS-6 акулы 25 и 50 мкг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Ингибирование воспалительных цитокинов (MyD88 и TRAF-6), ингибирование активации NF -kB и iNOS обоими CS | ||||
| Эффект через TLR4 (подтвержден экспериментом со специфическими антителами) | |||||||
| Bian et al. [2009] | CS-6 и CS-4 акульего происхождения 10–100 мг / мл | Эксплантаты бычьего хряща 4 недели | Снижение содержания ГАГ | ||||
| Imada et al. | Акула (в основном CS-6) и свинья (в основном CS-4) 1–100 мкг / мл | Суставные хондроциты человека в альгинатных шариках и синовиальный фибробласт, стимулированные IL-1β 6 или 4 дня | Разные эффект обеих CS | ||||
| Подавление индуцированных IL-1b ADAMTS-4 и -5 в обоих типах клеток | |||||||
| Подавление индуцированных IL-1β MMP- 13 и увеличить экспрессию аггрекана в хондроцитах | |||||||
| Восстановление TIMP-3 в хондроцитах и TIMP-1 в синовиоцитах CS свиньи |
Таблица 3.

In vivo эффекты хондроитинсульфата.
| Исследование | Хондроитин | Модель | Результаты |
|---|---|---|---|
| Uebelhart et al. [1998] | 80 мг / день перорально или i. м. | Кроличья модель повреждения хряща, вызванного химопапаином | Значительное увеличение продукции PG |
| Omata et al. [2000] | 1000 мг / кг | Коллаген-индуцированный артрит у мышей | Снижение параметров синовита: клеточная инфильтрация, фиброз и пролиферация выстилающих клеток |
Campo et al. [2003] [2003] | 1 мл / кг (внутрибрюшинно) | Коллаген-индуцированный артрит у крыс | Лечение начинали после начала артрита (день 10) |
| Защита от окислительного стресса | |||
| 25 мг / кг (перорально) | Снижение уровней TNF-α и миелопероксидазы в плазме | ||
| Cho et al. [2004] | 1200 мг / кг | Коллаген-индуцированный артрит у крыс | Снижение уровней IL-6 |
Caraglia et al.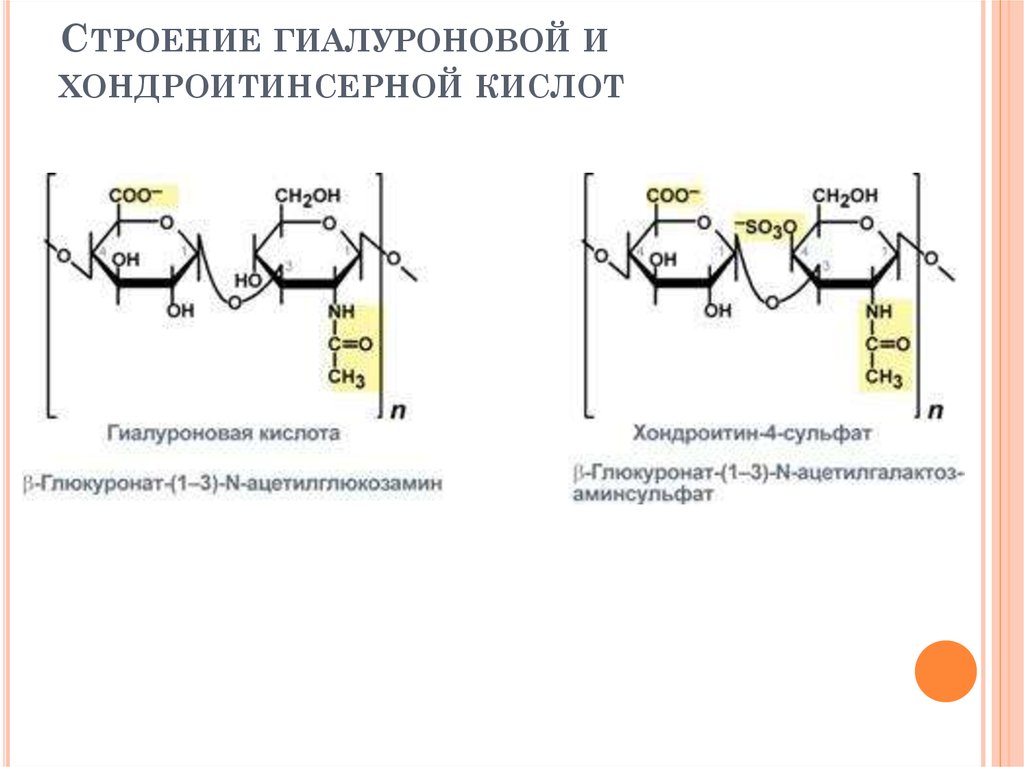 [2005] [2005] | 0,3 мг / день | Спонтанный ОА у мышей 12 дней | Значительное уменьшение апоптозных хондроцитов через 30 дней |
| Chou et al. [2005] | Пищевая добавка (18 мг / г) | Адъювант-индуцированный артрит Фрейнда у крыс | Предотвращение увеличения MMP-9 Снижение уровня IL-1β в тканях суставов, но не в сыворотке |
| Campo et al. al. [2008] | CS-4 (трахея крупного рогатого скота) 30–120 мг / кг (т.е.p.) | Коллаген-индуцированный артрит у мышей В течение 25 дней | Ингибирование активации NF-κB Ингибирование MMP-13 ингибирование активации каспаз-3 и -7 |
Противовоспалительный эффект
CS. сообщалось, что он обладает противовоспалительным действием. Было показано, что он ингибирует in vitro синтез различных промежуточных продуктов воспаления, таких как синтаза оксида азота (NO), циклооксигеназа (COX) -2, микросомальная простагландин-синтаза (mPGES) -1 и простагландин (PG) E 2 [Campo и другие. 2009a; Legendre et al. 2008; Чан и др. 2005b; Bassleer et al. 1998]. Также было показано, что CS может действовать на toll-подобный рецептор (TLR) -4, ингибируя воспалительные цитокины, MyD88 и фактор, связанный с рецептором фактора некроза опухоли (TNF) (TRAF) -6, посредством ингибирования ядерного фактора (NF ) -kB активация [Campo et al. 2009b].
Противовоспалительный эффект CS был также продемонстрирован in vivo. Было показано, что CS снижает синовит при коллаген-индуцированном артрите у мышей [Omata et al. 2000]. Он также был способен снижать провоспалительный цитокин, интерлейкин (IL) -6, в той же модели [Cho et al. 2004]. CS также снижает уровень IL-1b в суставной ткани при адъювантном артрите Фрейнда при введении в качестве пищевой добавки [Chou et al. 2005] и TNF-α и миелопероксидаза в плазме крови крыс с коллаген-индуцированным артритом и после перорального введения [Campo et al. 2003].
Антикатаболические и анаболические эффекты
Первый анаболический эффект CS был описан более 30 лет назад.CS увеличивал синтез гиалуроната в синовиальных клетках [Verbruggen and Veys, 1977]. С тех пор было также продемонстрировано увеличение синтеза коллагена типа II и протеогликана (PG) в хондроцитах человека [Wang et al. 2002; Bassleer et al. 1998] и ГАГ в хондроцитах крупного рогатого скота [Legendre et al. 2008]. Этот эффект также может быть вторичным по отношению к подавлению регуляции матриксной металлопротеиназы (ММП) [Wang et al. 2002]. Было также показано, что CS ингибирует MMP-1, -3 и -13, а также ADAMTS-4 и -5 (аггреканазы) в хондроцитах человека, свиньи и крупного рогатого скота [Imada et al. 2010; Legendre et al. 2008; Tahiri et al. 2008; Чан и др. 2005a; Монфорт и др. 2005]. Ингибирование MMP-13 может происходить через ингибирование активации p38 и Erk1 / 2 [Holzmann et al. 2006]. Для CS-4 и CS-6 были продемонстрированы различные ингибирующие способности против ММП в хондроцитах мышей [Campo et al. 2009a]. Различия между CS-6 и CS-4 недавно были также показаны на человеческих клетках. Действительно, CS-6 (акульего происхождения) может противодействовать ингибированию IL-1b тканевым ингибитором металлопротеаз (TIMP) -3 в хондроцитах человека и TIMP-1 в синовиальных фибробластах, тогда как CS-4 (происхождение из трахеи свиньи) не дает того же эффект [Imada et al. 2010]. CS может активировать гиалуронансинтазу в фибробластоподобных клетках [David-Raoudi et al. 2009] и может быть эффективным в качестве смазки для суставов, как было показано на эксплантатах бычьего хряща [Katta et al. 2009]. Также сообщалось, что CS может влиять на процесс резорбции, происходящий в субхондральной кости во время ОА. CS действительно может увеличивать соотношение остеопротегерин (OPG): активатор рецептора для лиганда NF-κB (RANKL) в остеобластах OA в пользу гомеостаза субхондральной кости [Tat et al. 2007]. Было продемонстрировано, что CS действует на большинство суставных тканей, участвующих в патофизиологии ОА. Наконец, недавнее исследование in vitro на эксплантатах бычьего хряща, обработанных CS-4 и CS-6 в течение 4 недель, выявило отрицательный эффект CS, показывающий, что он снижает содержание GAG [Bian et al. 2009]. Важно отметить, что это исследование было проведено с самой высокой концентрацией CS из когда-либо протестированных (10–100 мг / мл).
Анаболический и антикатаболический эффект CS также был продемонстрирован in vivo. CS может увеличивать продукцию PG на кроличьей модели деградации хряща [Uebelhart et al. 1998], предотвращают повышение уровня ММР-9 при адъювантном артрите Фрейнда у крыс при введении в качестве пищевой добавки [Chou et al. 2005] или ингибируют ММР-13 при коллаген-индуцированном артрите у мышей [Campo et al. 2008].
Антиапоптотический эффект
CS продемонстрировал антиапоптотические свойства как in vitro, так и in vivo. Было показано, что CS (200 (мкг / мл) снижает чувствительность хондроцитов кролика к апоптозу [Jomphe et al. 2008]. Этот эффект был связан с уменьшением транслокации NF-κB и со снижением пути передачи сигналов киназы MAP через p38 и Erk1 / 2. Другое исследование указало на антиапоптотический эффект CS-4 и CS-6 в суставных хондроцитах мыши [Campo et al. 2009a]. In vivo, на мышиной модели спонтанного ОА было показано, что 12-дневное лечение CS (0,3 мг / день) снижает количество апоптозных хондроцитов при оценке через 30 дней [Caraglia et al. 2005]. Также было продемонстрировано, что он способен ингибировать активацию каспазы-3 и -7 при коллаген-индуцированном артрите у мышей [Campo et al. 2008]. Эти результаты свидетельствуют в пользу хондропротекторного действия CS.
Антиоксидантный эффект
Антиоксидантные эффекты были рассмотрены [Campo et al. 2006a, 2006b]. Было показано, что CS обладает антиоксидантными свойствами in vitro в фибробластах кожи человека [Campo et al. 2004] и in vivo при коллаген-индуцированном артрите у крыс [Campo et al. 2003]. CS обеспечивает защиту от перекиси водорода и супероксид-анионов. Действительно, эти исследования продемонстрировали, что он может ограничивать гибель клеток, уменьшать фрагментацию ДНК и окисление белков, уменьшать образование свободных радикалов и действовать как поглотитель свободных радикалов. Он снижает перекисное окисление липидов и улучшает антиоксидантную защиту за счет восстановления эндогенных антиоксидантов, восстановленного глутатиона (GSH) и супероксиддисмутазы (SOD).
Регуляция клеточного сигнального пути
CS, как было обнаружено, действует на основные клеточные сигнальные пути.Было показано, что он ингибирует активацию пути киназы MAP, p38 и Erk ½, а также ингибирование трансактивации NF-κB в хондроцитах кролика [Jomphe et al. 2008; Verge’s et al. 2004]. Было также показано, что CS действует на другие промежуточные продукты клеточной передачи сигналов [Egea et al. 2010]. CS был способен индуцировать путь протеинкиназы C (PKC) / PI3K / Akt в клетках нейробластомы. Многие эффекты, описанные для CS на патофизиологию ОА, могут быть связаны с его действием на передачу сигналов в клетках.
Важно помнить, что большинство эффектов in vitro было получено с использованием высоких концентраций CS, которые не соответствуют ожидаемым концентрациям в плазме. Более того, учитывая медленное действие препарата на человека, системы in vitro и in vivo использовались в течение довольно короткого времени. Различные авторы предположили, что высокая концентрация, используемая in vitro, использовалась для компенсации этих проблем [Tat et al. 2010; Монфорт и др. 2008b]. Различия в чистоте и свойствах CS могут быть причиной несоответствия эффектов. Это было недавно рассмотрено в двух всеобъемлющих обзорах [Rainsford, 2009; Вольпи, 2009]. Это было подтверждено даже в суставных хондроцитах [Tat et al. 2010], когда три разных типа CS были протестированы в одной и той же системе и оказали различное воздействие на ключевые медиаторы OA. Это исследование продемонстрировало, что ХС бычьего происхождения гораздо эффективнее ингибирует катаболические медиаторы, чем ХС свиного происхождения.Также важно отметить, что эффекты CS in vivo в основном наблюдались на животных моделях артрита. Только одно исследование было проведено на модели спонтанного ОА [Caraglia et al. 2005].
Точный механизм действия CS еще предстоит выяснить. Взятые вместе, эти данные предполагают вмешательство CS на разных уровнях патофизиологии ОА, как показано в.
Схематическое изображение мишеней хондроитинсульфата (CS) в хондроцитах во время остеоартрита, как было предложено исследованиями in vitro: CS действует на сигнальные пути клеток, воспалительные и катаболические пути и на окислительный стресс (как показано черными стрелками).CS нацелен на различные промежуточные соединения в этих путях (как показано серыми стрелками). CS, хондроитинсульфат; ИЛ, интерлейкин; ECM, внеклеточный матрикс; ПГЕ 2 , простагландин E 2 ; PG, протеогликан; ММП, матриксная металлопротеиназа; NO, оксид азота; ADAMTS, дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами; NF-κB, ядерный фактор kB; ЦОГ, циклоосигеназа, iNOS, индуцируемая синтаза оксида азота.
Клинический эффект хондроитинсульфата
Терапевтическая эффективность CS изучалась и сообщалась в различных клинических исследованиях у пациентов с ОА.Влияние CS на пациентов с ОА оценивалось либо по симптомам ОА (боль и функция), чтобы определить его симптоматическое лекарство замедленного действия для эффекта ОА (SYSADOA), либо по модификации заболевания (эффект структуры, сужение суставной щели (JSN)) для определения его модифицирующий болезнь эффект препарата ОА (DMOAD).
Симптоматическое лекарство замедленного действия для лечения ОА
Различные мета-анализы [Reichenbach et al. 2007; Richy et al. 2003; Leeb et al. 2000; McAlindon et al. 2000] сообщили о различной величине эффекта (ES) на боль и функцию CS в диапазоне от 0,9 до всего 0,3.
Недавно были разработаны и опубликованы три исследования, посвященных влиянию CS на SYSADOA, то есть исследование GAIT [Hochberg and Clegg, 2008; Clegg et al. 2006], исследование STOPP [Kahan et al. 2009] и еще одно рандомизированное контролируемое исследование (РКИ) [Mazieres et al. 2007; Mazieres et al. 2006] (). Совсем недавно рекомендации Международного общества исследований остеоартрита (OARSI) по лечению ОА определили умеренный или большой ES (0.75, 95% ДИ 0,50–0,99) [Zhang et al. 2010], но подчеркнул систематическую ошибку публикации, неоднородность результатов и кумулятивное снижение ES (1,85, 95% ДИ 1,47–2,22, в 1992 г. до 0,75, 95% ДИ 0,50–1,01, в 2006 г.).
Таблица 4.
| Исследование | Результат | Вмешательство | Население и продолжительность | Размер результата / эффекта | |||||
|---|---|---|---|---|---|---|---|---|---|
| Глобальная оценка | 900 Maziéres et al. [2007] | Глобальная оценка исследователями клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 3,1 (CS) и 2,5 (Плацебо), p = 0,044 Благоприятствует CS | ||||
| Общая оценка пациентом клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец обработки) | NS | ||||||
| Качество жизни | |||||||||
| Maziéres et al. [2007] | Физический компонент SF-12 (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 5,8 (CS) и 3,8 (плацебо), p = 0,021 Благоприятствует CS | |||||
| SF-12 Психический компонент | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Pain | |||||||||
| Clegg et al. [2006] | Боль | CS против плацебо | РКИ, N = 1583, 24 недели | CS не лучше, чем плацебо | |||||
| Maziéres et al. [2007] | Боль во время активности, ВАШ (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | −41% (CS ) и -32% (плацебо), p = 0,029 Поддерживает CS | |||||
| Боль в покое, ВАШ (изменение от исходного уровня) | CS vs. плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Reichenbach et al. [2007] | Исходы, связанные с болью | CS по сравнению с плацебо / без лечения | MA, 20 РКИ, n = 3846, ОА коленного или тазобедренного сустава, продолжительность испытаний от 6 до 132 недель | Значительная неоднородность | |||||
| Kahan et al. [2009] | Подшкала VAS и WOMAC | CS vs. плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Значительно более быстрое уменьшение боли в целевом колене с помощью CS | |||||
| Функция | |||||||||
| Clegg et al. [2006] | Припухлость сустава, выпот или и то, и другое при клиническом обследовании | CS по сравнению с плацебо | РКИ, N = 1583, 24 недели | CS значительно лучше | |||||
| Maziéres et al. [2007] | Индекс Лекена (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | |||||
| Изменение структуры | |||||||||
| Reichenbach et al. [2007] | Минимум JSW | CS по сравнению с плацебо / без лечения | MA, 5 РКИ, N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | ES средняя разница 0 .16 мм, 95% ДИ 0,08–0,24 | |||||
| Благоприятствует хондроитину | |||||||||
| Среднее значение JSW | CS по сравнению с плацебо / без лечения | MA, 5 N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследования от 6 до 132 недель | ES средняя разница 0,23, 95% ДИ 0,09–0,37 | ||||||
| Поддерживает хондроитин | |||||||||
| Кахан и другие. [2009] | Минимальный JSW | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Повышение эффекта лечения со временем | |||||
| CS значительно лучше для JSW | |||||||||
| Lee et al. [2010] | Минимальный JSN | CS по сравнению с плацебо | MA, 4 РКИ, N = 1088, ОА коленного сустава, период наблюдения от 1 до 2 лет | Небольшой, но значительный защитный эффект CS через 2 лет на минимуме JSN | |||||
| Hochberg [2010] | Минимум JSW | MA, 3 РКИ, N = 1179, Коленный остеоартрит, последующее наблюдение 2 года | Значительное снижение скорости уменьшения суставной щели ширина с CS | ||||||
| ES 0.23 (95% ДИ 0,11–0,35) | |||||||||
| Неблагоприятные события | |||||||||
| Maziéres et al. [2007] | Количество пациентов по крайней мере с одним НЯ, связанным с лечением | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | NS | |||||
| Всего количество НЯ | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | N = 18 (CS) и N = 20 (плацебо) NS | ||||||
| Reichenbach et al. [2007] | Пациенты с НЯ | CS по сравнению с плацебо / без лечения | MA, 12 РКИ, N = 1929, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | |||||
| Исключение из-за НЯ | Хондроитин по сравнению с плацебо / отсутствие лечения | МА, 9 РКИ, N = 1781, ОА коленного и тазобедренного суставов, диапазон продолжительности исследований от 6 до 132 недель | NS | ||||||
| Пациенты с тяжелыми НЯ | Хондроитин vs. плацебо / без лечения | MA, 2 РКИ, N = 217, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | ||||||
| Kahan et al. [2009] | Исключение из-за НЯ | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | NS |
Сообщалось о глобальных клинических испытаниях a благотворное влияние CS на боль и функцию (). Однако в самом крупном исследовании GAIT не сообщалось о влиянии на эти конечные точки.
Эффекты модификации структуры
Эффекты модификации структуры CS были описаны и проанализированы в двух недавних метаанализах [Hochberg, 2010; Ли и др. 2010]. Ранее сообщалось, что не было неоднородности в результатах РКИ по эффектам модификации структуры [Hochberg et al. 2008]. Результаты показали небольшое, но значительное снижение ухудшения JSN (ES = 0,26, 95% ДИ 0,16–0,36). Недавно при наблюдении за пациентами в течение 2 лет было выявлено значительное влияние CS на JSN у пациентов, получавших CS, по сравнению с плацебо [Kahan et al. 2009].
Безопасность и переносимость
В большинстве клинических испытаний сообщалось о прекрасном профиле безопасности и хорошей переносимости CS. Частота побочных эффектов и частота отказов были эквивалентны в группах CS и плацебо. При применении CS не наблюдалось серьезных серьезных побочных эффектов. Спасательные препараты (парацетамол или нестероидные противовоспалительные препараты [НПВП]) разрешены во время клинических испытаний. Этот факт может уменьшить разницу между группами CS и плацебо [Monfort et al. 2008a] ().
Хондроитинсульфат в рекомендациях
CS рекомендован в руководствах, опубликованных OARSI и Европейской лигой против ревматизма (EULAR) для лечения ОА коленного сустава [Zhang et al. 2008; Jordan et al. 2003]. OARSI рекомендует CS из-за его симптоматического и структурно-модифицирующего эффекта при ОА коленного сустава, но также рекомендует прекратить его через 6 месяцев, если симптоматическая реакция отсутствует. Что касается ОА бедра и кисти, EULAR рекомендует SYSADOA, включая CS, из-за их симптоматических эффектов и низкой токсичности, но подчеркивает тот факт, что ES небольшие, подходящие пациенты не определены должным образом, а клинически значимая модификация структуры и фармакоэкономический аспект не очень хорошо установлено.
Обсуждение
CS используется уже несколько десятилетий, и было важно описать его фармакокинетику, механизм действия и описать его клиническую эффективность.
CS обладает различными эффектами, от противовоспалительных и антикатаболических до антиапоптотических, а также антиоксидантных свойств. Все эти результаты были получены в разных системах с разными дозировками. Во многих обзорах говорится о важности источника CS и чистоты [Lauder, 2009; Рейнсфорд, 2009 г .; Вольпи, 2009; Лаудер и др. 2000]. Кроме того, сульфатированный CS в разных положениях (например, 4 или 6) может иметь разные эффекты. Например, CS-4 более эффективен как антиоксидант, чем CS-6 [Albertini et al. 2000; Volpi, Tarugi, 1999]. Исследования in vitro и in vivo имеют ограничения, в основном из-за используемой концентрации и продолжительности исследования. CS используется в концентрациях, которые значительно превосходят плазменную концентрацию после перорального введения терапевтической дозы CS. Действительно, CS достиг концентрации в плазме примерно 2.0 мкг / мл у пациентов с ОА после перорального введения 0,8 г CS [Conte et al. 1995]. Это исследование также показало, что CS может достигать 2,7 мг / мл в синовиальной жидкости пациентов с ОА. Другой эксперимент на крысах после перорального введения (16 мг / кг) показал концентрацию 3,3 мг / г в хрящах [Ronca et al. 1998]. В большинстве исследований in vitro использовалось от 10 мг / мл CS до 1000 мг / мл (см.). При интерпретации данных необходимо учитывать условия исследования. Наконец, недавно был проведен обзор эффективности КС при воспалительных состояниях, отличных от ОА, и в основном более тяжелых, чем ОА [Vallières and du Souich, 2010; du Souich et al. 2009]. Было показано, что CS эффективен при патологии, включая псориаз [Möller et al. 2010; Verges et al. 2005]. Это предполагает сильную противовоспалительную активность CS. К сожалению, отсутствие inivo демонстрации влияния CS на прогрессирование ОА. Только в одном исследовании изучалось влияние хондроитина на модель ОА. Для лучшего понимания клинической эффективности CS необходимы дальнейшие исследования, изучающие влияние CS на деградацию хряща, ремоделирование субхондральной кости и воспаление синовиальной оболочки.
CS рекомендуется OARSI в качестве вмешательства SYSADOA для лечения ОА [Zhang et al. 2010, 2008] и EULAR [Jordan et al. 2003]. Обе организации признали его симптоматические и структурно-модифицирующие эффекты. OARSI рекомендует прекратить лечение через 6 месяцев при отсутствии эффективности [Zhang et al. 2008]. В то время, когда EULAR опубликовал свои рекомендации, они предложили растущие доказательства эффективности CS. Однако ко времени последнего обновления OARSI [Zhang et al. 2010], ES снизился, что свидетельствует о нестабильности эффективности, что, по крайней мере частично, может быть связано с повышением качества исследований. Несоответствие эффективности, показанное в нескольких клинических испытаниях, имеет большое значение. Этот метаанализ [Zhang et al. 2010] также продемонстрировал серьезную предвзятость публикации. Эти наблюдения также сделаны для других соединений класса SYSADOA, включая сульфат глюкозамина (GS). Напротив, ES для ацетаминофена, хотя и очень маленький, по-видимому, со временем стабилизировался, что позволяет предположить, что дальнейших РКИ для проверки его анальгетической эффективности не требовалось.В целом, этот обзор указывает на то, что существует потребность в клинических испытаниях хорошего качества с продолжительностью и количеством пациентов, соответствующих этому виду соединений. Также уместно сравнить ES для боли основных фармакологических методов, обычно используемых при лечении ОА. Для сравнения, ЭС CS — одна из самых важных. Например, болевой синдром ES (2010 г.) для ацетаминофена составил 0,14 (95% 0,05–0,23), для НПВП 0,29 (95% 0,22–0,35) и для CS 0,75 (95% 0,50–1,01). Это говорит о клинической значимости использования CS для лечения ОА, учитывая его низкую токсичность. ОА является долгосрочным прогрессирующим заболеванием, для которого перед применением каждого лечения должна быть проведена оценка соотношения риск / польза.
В некоторых исследованиях оценивалась эффективность использования CS в сочетании с GS. Это было сделано in vitro [Chan et al. 2006, 2007, 2005a, 2005b], а также в клинических испытаниях [Vangsness et al. 2009; Sawitzke et al. 2008; Clegg et al. 2006, 2005]. Синергетический эффект обоих соединений еще предстоит продемонстрировать, но многие авторы рекомендуют использовать комбинацию.
Одна из причин для оптимизма в отношении использования CS отдельно или в сочетании со связанным продуктом, таким как GS, — это профиль безопасности.CS не взаимодействует с другими лекарствами и не вызывает серьезных побочных эффектов. Это говорит в пользу положительного соотношения риск / польза.
Заключение
Несмотря на умеренное влияние CS на боль и функцию, CS представляет собой интересный продукт для лечения ОА коленного сустава. Клинические данные свидетельствуют в пользу медленного действия на симптомы умеренного ОА коленного сустава. CS рекомендуется по самым популярным рекомендациям. Его профиль безопасности, несомненно, является одним из основных преимуществ при лечении стареющих пациентов с некоторыми сопутствующими заболеваниями.Таким образом, нет никаких ограничений для его использования у пациентов с ОА, если не учитывать экономический эффект. Тем не менее, следует проявлять осторожность в отношении типа и состава CS. Конечно, остаются вопросы относительно механизма его действия. Эффект CS на воспаление субхондральной кости и синовиальной оболочки может быть лучше документирован.
Благодарности
Авторы благодарят L. Montell Bonaventura и J. Verges из Bioiberica, любезно предоставившие документацию по хондроитинсульфату.К. Санчес — научный сотрудник Национального фонда научных исследований (FNRS, Бельгия).
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Проф. Хенротин получил образовательные и исследовательские гранты от Bioiberica, Expanscience, Danone, Nestec и BioXtract.
Ссылки
- Альбертини Р., Пасси А., Абуджа П.М., Де Лука Г. (2000) Влияние гликозаминогликанов и протеогликанов на перекисное окисление липидов.Инт Дж Мол Мед 6: 129–136 [PubMed] [Google Scholar]
- Barnhill J.G., Fye C.L., Williams D.W., Reda D.J., Harris C.L., Clegg D.O. (2006) Выбор хондроитинового продукта для интервенционного исследования артрита глюкозамином / хондроитином. J Am Pharm Assoc (Вашингтон, Вашингтон) 46: 14–24 [PubMed] [Google Scholar]
- Bassleer C.T., Combal J.P., Bougaret S., Malaise M. (1998) Влияние хондроитинсульфата и интерлейкина-1 бета на суставные хондроциты человека, культивируемые в кластерах. Остеоартроз Хрящ 6: 196–204 [PubMed] [Google Scholar]
- Биан Л., Каплун М., Уильямс Д.Ю., Сюй Д., Атешян Г.А., Хунг С.Т. (2009) Влияние хондроитинсульфата на биохимические, механические и фрикционные свойства хрящевых эксплантатов при длительном культивировании. J Биомеханика 42: 286–290 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Ferlazzo AM, Calatroni A. (2004) Уменьшение фрагментации ДНК и производство гидроксильных радикалов гиалуроновой кислотой и хондроитин-4-сульфатом в железе плюс индуцированный аскорбатом окислительный стресс в культурах фибробластов.Free Radic Res 38: 601–611 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Traina P., Calatroni A. (2008) Хондроитин-4-сульфат ингибирует NF-kB транслокация и активация каспаз при коллаген-индуцированном артрите у мышей. Остеоартроз Хрящ 16: 1474–1483 [PubMed] [Google Scholar]
- Кампо Г.М., Авенозо А., Кампо С., Д’Аскола А., Трэйна П., Сама Д. и др. (2009a) Гликозаминогликаны модулируют воспаление и апоптоз в хондроцитах, обработанных LPS.J Cell Biochem 106: 83–92 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Ferlazzo AM, Altavilla D., Calatroni A. (2003) Эффективность лечения гликозаминогликанами экспериментального коллаген-индуцированного артрита в крысы. Артрит Res Ther 5: R122 – R131 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006a) Антиоксидантная активность хондроитинсульфата. Adv Pharmacol 53: 417–431 [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006b) Хондроитинсульфат: антиоксидантные свойства и положительные эффекты. Мини Рев Мед Хим 6: 1311–1320 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Traina P., D’Ascola A., Calatroni A. (2009b) Гликозаминогликаны снижают воспалительную реакцию, модулируя толл-подобные рецептор-4 в хондроцитах, стимулированных ЛПС. Arch Biochem Biophys 491: 7–15 [PubMed] [Google Scholar]
- Caraglia M., Beninati S., Giuberti G., Д’Алессандро А.М., Лентини А., Аббруззезе А. и др. (2005) Альтернативная терапия земными элементами усиливает хондрозащитные эффекты хондроитинсульфата у мышей. Exp Mol Med 37: 476–481 [PubMed] [Google Scholar]
- Катерсон Б., Махмудиан Ф., Соррелл Дж. М., Хардингем Т. Э., Бейлисс М. Т., Карни С. Л. и др. (1990) Модуляция структуры нативного хондроитинсульфата в развитии тканей и при заболеваниях. J Cell Sci 97: 411–417 [PubMed] [Google Scholar]
- Чан П.С., Кэрон Дж.P., Orth M.W. (2005a) Влияние глюкозамина и хондроитинсульфата на регуляцию экспрессии генов протеолитических ферментов и их ингибиторов в эксплантатах суставного хряща быка, зараженных интерлейкином-1. Am J Vet Res 66: 1870–1876 [PubMed] [Google Scholar]
- Chan P.S., Caron J.P., Orth M.W. (2006) Кратковременные изменения экспрессии генов в хрящевых эксплантатах, стимулированные интерлейкином бета, глюкозамином и хондроитинсульфатом. J Ревматол 33: 1329–1340 [PubMed] [Google Scholar]
- Чан П.С., Карон Дж. П., Орт М. В. (2007) Влияние глюкозамина и хондроитинсульфата на эксплантаты бычьего хряща в условиях длительного культивирования. Am J Vet Res 68: 709–715 [PubMed] [Google Scholar]
- Chan PS, Caron JP, Rosa GJ, Orth MW (2005b) Глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простагландина E (2) в эксплантатах суставного хряща. . Остеоартроз Хрящ 13: 387–394 [PubMed] [Google Scholar]
- Чо С. Ю., Сим Дж.С., Чжон С. С., Чанг С. Ю., Чой Д. В., Тойда Т. и др. (2004) Влияние низкомолекулярного хондроитинсульфата на индуцированный коллагеном артрит типа II у мышей DBA / 1J. Биол Фарм Булл 27: 47–51 [PubMed] [Google Scholar]
- Chou M.M., Vergnolle N., McDougall J.J., Wallace J.L., Marty S., Teskey V. и др. (2005) Влияние хондроитина и сульфата глюкозамина в составе диетического батончика на воспаление, интерлейкин-1бета, матриксную металлопротеазу-9 и повреждение хряща при артрите. Эксп Биол Мед 230: 255–262 [PubMed] [Google Scholar]
- Клегг Д.О., Реда Д.Дж., Харрис К.Л., Кляйн М.А. (2005) Эффективность глюкозамина и хондроитинсульфата у пациентов с болезненным остеоартритом (ОА) коленного сустава: исследование вмешательства глюкозамина / хондроитина. Ревматоидный артрит 52 (9S): S256, (Аннотация). [Google Scholar]
- Clegg D.O., Reda D.J., Harris C.L., Klein M.A., O’Dell J.R., Hooper M.M., et al. (2006) Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med 354: 795–808 [PubMed] [Google Scholar]
- Конте А., Volpi N., Palmieri L., Bahous I., Ronca G. (1995) Биохимические и фармакокинетические аспекты перорального лечения хондроитинсульфатом. Arzneimittelforschung 45: 918–925 [PubMed] [Google Scholar]
- David-Raoudi M., Deschrevel B., Leclercq S., Galera P., Boumediene K., Pujol JP (2009) Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальная регуляция гиалуронансинтаз: роль p38 и Akt. Ревматоидный артрит 60: 760–770 [PubMed] [Google Scholar]
- du Souich P., Гарсия А.Г., Верджес Дж., Монтелл Э. (2009) Иммуномодулирующие и противовоспалительные эффекты хондроитинсульфата. J Cell Mol Med 13 (8A): 1451–1463 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- du Souich P., Verges J. (2001) Простой подход для прогнозирования максимального эффекта, вызываемого лекарством, когда концентрации в плазме недоступны или диссоциируют от воздействия, как показано на данных по хондроитинсульфату. Clin Pharmacol Ther 70: 5–9 [PubMed] [Google Scholar]
- Эгеа Дж., Гарсия А.Г., Верджес Дж., Монтелл Э., Лопес М.Г. (2010) Антиоксидантное, противовоспалительное и нейропротекторное действие хондроитинсульфата и протеогликанов. Остеоартроз Хрящ 18 (Приложение 1): S24 – S28 [PubMed] [Google Scholar]
- Hochberg M.C. (2010) Структурно-модифицирующие эффекты хондроитинсульфата при остеоартрите коленного сустава: обновленный метаанализ рандомизированных плацебо-контролируемых исследований продолжительностью 2 года. Остеоартроз Хрящ 18 (Приложение 1): 528–531 [PubMed] [Google Scholar]
- Hochberg M.К., Клегг Д.О. (2008) Потенциальные эффекты хондроитинсульфата на отек суставов: отчет GAIT. Остеоартроз Хрящ 16 (Приложение 3): S22 – S24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hochberg MC, Zhan M., Langenberg P. (2008) Скорость уменьшения ширины суставной щели у пациентов с остеоартритом колено: систематический обзор и метаанализ рандомизированных плацебо-контролируемых исследований хондроитинсульфата. Curr Med Res Opin, в печати. [PubMed] [Google Scholar]
- Holzmann J., Брандл Н., Земанн А., Шабус Р., Марловиц С., Коуберн Р. и др. (2006) Различные эффекты TGFbeta и хондроитинсульфата на уровни активации p38 и ERK1 / 2 в суставных хондроцитах человека, стимулированных LPS. Остеоартроз Хрящ 14: 519–525 [PubMed] [Google Scholar]
- Имада К., Ока Х., Кавасаки Д., Миура Н., Сато Т., Ито А. (2010) Механизмы антиартритного действия природного хондроитинсульфата у человека суставные хондроциты и синовиальные фибробласты. Биол Фарм Булл 33: 410–414 [PubMed] [Google Scholar]
- Джексон К.Г., Плаас А.Х., Сэнди Дж. Д., Хуа С., Ким-Роландс С., Барнхилл Дж. Г. и др. (2010) Фармакокинетика перорального приема глюкозамина и хондроитинсульфата у человека по отдельности или в комбинации. Остеоартроз Хрящ 18: 297–302 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Jomphe C.j, Gabriac M., Hale T.M., Heroux L., Trudeau L.E., Deblois D., et al. (2008) Хондроитинсульфат ингибирует ядерную транслокацию ядерного фактора-каппаВ в хондроцитах, стимулированных интерлейкином-1бета.Базовый Clin Pharmacol Toxicol 102: 59–65 [PubMed] [Google Scholar]
- Jordan K.M., Arden N.K., Doherty M., Bannwarth B., Bijlsma J.W., Dieppe P., et al. (2003) Рекомендации EULAR 2003: научно обоснованный подход к лечению остеоартрита коленного сустава: отчет рабочей группы Постоянного комитета по международным клиническим исследованиям, включая терапевтические испытания (ESCISIT). Энн Рум Дис 62: 1145–1155 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Kahan A., Uebelhart D., De Vathaire F., Дельмас П.Д., Регинстер Дж. (2009) Долгосрочные эффекты хондроитинов 4 и 6 сульфата на остеоартрит коленного сустава: исследование по предотвращению прогрессирования остеоартрита, двухлетнее рандомизированное двойное слепое плацебо-контролируемое исследование. Ревматоидный артрит 60: 524–533 [PubMed] [Google Scholar]
- Катта Дж., Джин З., Ингам Э., Фишер Дж. (2009) Хондроитинсульфат: эффективная смазка для суставов? Остеоартроз Хрящ 17: 1001–1008 [PubMed] [Google Scholar]
- Кусано С., Отани А., Сакаи С., Игараси Н., Такегучи А., Тойода Х. и др. (2007) Определение хондрозина в плазме крови мышей с помощью ВЭЖХ после внутривенной или пероральной дозы. Биол Фарм Булл 30: 1365–1368 [PubMed] [Google Scholar]
- Лаудер Р.М. (2009) Хондроитинсульфат: сложная молекула с потенциальным воздействием на широкий спектр биологических систем. Комплемент Терапии Мед 17: 56–62 [PubMed] [Google Scholar]
- Лаудер Р.М., Хакерби Т.Н., Недушинский Л.А. (2000) Метод снятия отпечатков пальцев на хондроитин / дерматансульфат и гиалуронановые олигосахариды.Гликобиология 10: 393–401 [PubMed] [Google Scholar]
- Ли Й.Х., Ву Дж.Х., Чой С.Дж., Джи Дж.Д., Сон Г.Г. (2010) Влияние глюкозамина или хондроитинсульфата на прогрессирование остеоартрита: метаанализ. Ревматол Инт 30: 357–363 [PubMed] [Google Scholar]
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. (2000) Метаанализ хондроитинсульфата в лечении остеоартрита. J Ревматол 27: 205–211 [PubMed] [Google Scholar]
- Legendre F., Bauge C, Roche R., Saurel A.S., Pujol J.P. (2008) Хондроитинсульфатная модуляция матрикса и экспрессия воспалительных генов в IL-lbeta-стимулированных хондроцитах — исследование в культурах гипоксических альгинатных гранул. Остеоартроз Хрящ 16: 105–114 [PubMed] [Google Scholar]
- Малаваки С.Дж., Асимакопулу А.П., Ламари Ф.Н., Теохарис А.Д., Цанакакис Г.Н., Караманос Н.К. (2008) Капиллярный электрофорез для контроля качества хондроитинсульфатов в сырье и рецептурах. Анальный биохим 374: 213–220 [PubMed] [Google Scholar]
- Mazieres B., Хучер М., Заим М., Гарнеро П. (2007) Эффект хондроитинсульфата при симптоматическом остеоартрите коленного сустава: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. Энн Рум Дис 66: 639–645 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mazieres B., Hucher M.M.H., Zam M.M.Z. (2006) Хондроитинсульфат в лечении остеоартрита коленного сустава: рандомизированное двойное слепое многоцентровое плацебо-контролируемое исследование. Энн Рум Дис 65 (Дополнение II): 398. [Google Scholar]
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. (2000) Глюкозамин и хондроитин для лечения остеоартрита: систематическая оценка качества и метаанализ. JAMA 283: 1469–1475 [PubMed] [Google Scholar]
- Möller I., Pérez M., Monfort J., Benito P., Cuevas J., Perna C., et al. (2010) Эффективность хондроитинсульфата у пациентов с сопутствующим остеоартритом коленного сустава и псориазом: рандомизированное двойное слепое плацебо-контролируемое исследование. Остеоартроз Хрящ 18 (Приложение 1): 532–540 [PubMed] [Google Scholar]
- Monfort J., Martel-Pelletier J., Pelletier J.P. (2008a) Хондроитинсульфат при симптоматическом остеоартрите: критическая оценка метаанализов. Curr Med Res Opin 24: 1303–1308 [PubMed] [Google Scholar]
- Monfort J., Nacher M., Montell E., Vila J., Verges J., Benito P. (2005) Хондроитинсульфат и гиалуроновая кислота (500–730 кДа ) подавляют синтез стромелизина-1 в хондроцитах человека, страдающих остеоартритом. Наркотики Exp Clin Res 31: 71–76 [PubMed] [Google Scholar]
- Monfort J., Pelletier J.P., Garcia-Giralt N., Martel-Pelletier J. (2008b) Биохимические основы действия хондроитинсульфата на суставные ткани при остеоартрозе. Энн Рум Дис 67: 735–740 [PubMed] [Google Scholar]
- Mourao P.A. (1988) Распределение хондроитин-4-сульфата и хондроитин-6-сульфата в суставном и ростовом хряще человека. Ревматоидный артрит 31: 1028–1033 [PubMed] [Google Scholar]
- Omata T., Itokazu Y., Inoue N., Segawa Y. (2000) Эффекты хондроитинсульфата-C на разрушение суставного хряща при артрите, индуцированном мышиным коллагеном.Arzneimittelforschung 50: 148–153 [PubMed] [Google Scholar]
- Rainsford K.D. (2009) Важность фармацевтического состава и данных клинических испытаний и фармакологических исследований в определении эффективности хондроитинсульфата и других гликозаминогликанов: критический анализ. J Pharm Pharmacol 61: 1263–1270 [PubMed] [Google Scholar]
- Reichenbach S., Sterchi R., Scherer M., Trelle S., Burgi E., Burgi U., et al. (2007) Мета-анализ: хондроитин при остеоартрите коленного или тазобедренного суставов.Энн Интерн Мед 146: 580–590 [PubMed] [Google Scholar]
- Ричи Ф., Брюйер О., Этген О., Кучерат М., Хенротин Ю., Регинстер Дж. Я. (2003) Структурная и симптоматическая эффективность глюкозамина и хондроитина при остеоартрите коленного сустава: всесторонний метаанализ. Arch Intern Med 163: 1514–1522 [PubMed] [Google Scholar]
- Ronca F., Palmieri L., Panicucci P., Ronca G. (1998) Противовоспалительная активность хондроитинсульфата. Остеоартроз Хрящ 6 (Приложение A): 14–21 [PubMed] [Google Scholar]
- Sawitzke A.Д., Ши Х., Финко М.Ф., Данлоп Д.Д., Бингем С.О., III, Харрис К.Л. и др. (2008) Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Ревматоидный артрит 58: 3183–3191 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Шварц Н.Б., Дорфман А. (1975) Стимуляция продукции хондроитинсульфат-протеогликана хондроцитами в монослое. Подключите ткань Res 3: 115–122 [PubMed] [Google Scholar]
- Shinmei M., Мияучи С., Мачида А., Миядзаки К. (1992) Количественное определение хондроитин-4-сульфата и хондроитин-6-сульфата в патологической суставной жидкости. Ревматоидный артрит 35: 1304–1308 [PubMed] [Google Scholar]
- Тахири К., Корвин-Змиевска С., Ришетт П., Херо Ф., Шевалье Х., Савуре Дж. Ф. и др. (2008) Природные хондроитинсульфаты увеличивают агрегацию протеогликановых комплексов и снижают экспрессию ADAMTS-5 в хондроцитах, обработанных интерлейкином 1 бета. Энн Рум Дис 67: 696–702 [PubMed] [Google Scholar]
- Тат С.K., Pelletier J.P., Mineau F., Duval N., Martel-Pelletier J. (2010) Различные эффекты 3 различных соединений хондроитинсульфата на хрящ / хондроциты человека при остеоартрите: важность чистоты и производственного процесса. J Ревматол 37: 656–664 [PubMed] [Google Scholar]
- Tat S.K., Pelletier J.P., Verges J., Montell E., Lajeunesse D., Fahmi H., et al. (2007) Хондроитин и сульфат глюкозамина в комбинации снижают прорезорбтивные свойства субхондральных костных остеобластов человека.Артрит Res Ther 9: R117. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Uebelhart D., Thonar EJ, Zhang J., Williams JM (1998) Защитный эффект экзогенного хондроитин-4,6-сульфата при острой деградации суставного хряща у кролика . Остеоартроз Хрящ 6 (Suppl. A): 6–13 [PubMed] [Google Scholar]
- Валлиер М., дю Суич П. (2010) Модуляция воспаления с помощью хондроитинсульфата. Остеоартроз Хрящ 18 (Приложение 1): S1 – S6 [PubMed] [Google Scholar]
- Вангснесс К.Т., младший, Спайкер В., Эриксон Дж. (2009) Обзор доказательной медицины использования глюкозамина и хондроитинсульфата при остеоартрите коленного сустава. Артроскопия: J Arthroscopic Relat Surg 25: 86–94 [PubMed] [Google Scholar]
- Verbruggen G., Veys E.M. (1977) Влияние сульфатированных гликозаминогликанов на метаболизм протеогликанов в клетках синовиальной оболочки. Acta Rhumatol Belg 1: 75–92 [PubMed] [Google Scholar]
- Verges J., Montell E., Herrero M., Perna C, Cuevas J., Perez M., et al.(2005) Клиническое и гистопатологическое улучшение псориаза при пероральном приеме хондроитинсульфата: случайная находка. Дерматол Интернет J 11: 31. [PubMed] [Google Scholar]
- Vergés J., Montell E., Martinez G., Heroux L., du Souich P. (2004) Хондроитинсульфат снижает фактор ядерной транслокации NF-kappaB и не изменяет состояние активации активирующего белка-1 (AP-1). Остеоартроз Хрящ 12: 194, (Аннотация). [Google Scholar]
- Volpi N. (2002) Пероральная биодоступность хондроитинсульфата (Кондросульф) и его компонентов у здоровых добровольцев мужского пола.Остеоартроз Хрящ 10: 768–777 [PubMed] [Google Scholar]
- Volpi N. (2003) Пероральное всасывание и биодоступность хондроитинсульфата ихтикового происхождения у здоровых добровольцев мужского пола. Остеоартроз Хрящ 11: 433–441 [PubMed] [Google Scholar]
- Volpi N. (2006a) Достижения в анализе хондроитинсульфата: применение при физиологических и патологических состояниях соединительной ткани и при фармакологическом лечении остеоартрита. Curr Pharm Des 12: 639–658 [PubMed] [Google Scholar]
- Volpi N.(2006b) Хондроитинсульфат: структура, роль и фармакологическая активность, Elsevier: Amsterdam [Google Scholar]
- Volpi N. (2009) Качество различных препаратов хондроитинсульфата в зависимости от их терапевтической активности. J Pharm Pharmacol 61: 1271–1280 [PubMed] [Google Scholar]
- Volpi N., Tarugi P. (1999) Влияние плотности заряда хондроитинсульфата, положения сульфатной группы и молекулярной массы на Cu2 + -опосредованное окисление липопротеинов низкой плотности человека: действие нормального человеческого хондроитинсульфата плазмы.J Biochem 125: 297–304 [PubMed] [Google Scholar]
- Wang L., Wang J., Almqvist KF, Veys EM, Verbruggen G. (2002) Влияние полисульфатированных полисахаридов и гидрокортизона на метаболизм внеклеточного матрикса суставных хондроцитов человека в пробирка. Clin Exp Rheumatol 20: 669–676 [PubMed] [Google Scholar]
- Zhang W., Doherty M., Arden N., Bannwarth B., Bijlsma J., Gunther K.P., et al. (2005) Основанные на фактических данных рекомендации EULAR по лечению остеоартрита тазобедренного сустава: отчет рабочей группы Постоянного комитета EULAR по международным клиническим исследованиям, включая терапию (ESCISIT).Энн Рум Дис 64: 669–681 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Чжан В., Московиц Р. В., Нуки Г., Абрамсон С., Альтман Р. Д., Арден Н. и др. (2008) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, Часть II: Основанные на фактах, согласованные экспертные рекомендации OARSI. Остеоартроз Хрящ 16: 137–162 [PubMed] [Google Scholar]
- Чжан В., Нуки Г., Московиц Р. В., Абрамсон С., Альтман Р. Д., Арден Н. К. и др. (2010) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г.Остеоартроз Хрящ 18 (4): 476–499 [PubMed] [Google Scholar]
От исследований in vitro к клиническим рекомендациям
Ther Adv Musculoskelet Dis. 2010 Dec; 2 (6): 335–348.
Мариан Мати
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Кристель Санчес
2 Исследовательское отделение костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Cecile Lambert
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
2 Кости и Отделение исследования хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
1 Отделение исследования костей и хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия eb.ca.glu@nitornehyЭта статья цитируется другими статьями в PMC.Abstract
Хондроитинсульфат (CS) рекомендуется в качестве терапевтического вмешательства при мультимодальном подходе к лечению остеоартрита (OA). CS был тщательно изучен для описания его фармакологии (фармакокинетических эффектов, эффектов in vitro и in vivo) и клинической эффективности. Сообщалось о различных результатах в зависимости от системы оценки (модель, дозировка и продолжительность) и источника CS (происхождение и качество).Целью этого обзора было собрать большую часть доступной информации о CS и обсудить его эффективность в управлении OA.
Ключевые слова: хрящ, хондроитинсульфат, остеоартрит, механизм действия, фармакокинетика
Введение
Хондроитинсульфат (CS) является основным компонентом внеклеточного матрикса (ECM) многих соединительных тканей, включая хрящ, кость, кожу , связки и сухожилия. Остеоартрит (ОА) характеризуется прогрессирующими структурными и метаболическими изменениями в тканях суставов, в основном деградацией хряща, склерозом субхондральной кости и воспалением синовиальной оболочки.Лечение остеоартрита включает мультимодальное терапевтическое вмешательство, поскольку на сегодняшний день лечения не найдено. Для лечения ОА необходимы препараты, которые могут замедлить, остановить или даже избежать деградации суставов. Многие из рекомендуемых вмешательств представляют только эффекты, изменяющие симптомы, и несколько эффектов, изменяющих структуру.
CS и другие соединения, такие как глюкозамин, используются в медицинских целях более 40 лет. CS продается как безрецептурная пищевая добавка в Северной Америке и отпускается по рецепту в соответствии с правилами Европейского медицинского агентства (EMEA) в Европе.В последние десятилетия CS вызывал много интересов в качестве потенциального терапевтического средства против ОА. CS является частью рекомендаций Международного общества исследований остеоартрита (OARSI) по лечению остеоартрита коленного сустава [Zhang et al. 2010, 2008] и рекомендаций Европейской лиги против ревматизма (EULAR) по лечению тазобедренного и коленного суставов OA Zhzang et al. 2005; Jordan et al. 2003]. ХС и глюкозамин могут стать отличной альтернативой для пациентов с ОА.
CS, как естественный компонент ЕСМ, представляет собой сульфатированный гликозаминогликан (ГАГ), состоящий из длинной неразветвленной полисахаридной цепи с повторяющейся дисахаридной структурой N-ацетилга-лактозамина и глюкуроновой кислоты.Большинство остатков N-ацетилгалактозамина () сульфатированы, особенно в положениях 4 и 6, что делает CS сильно заряженным полианионом. CS отвечает за многие важные биомеханические свойства хряща, такие как сопротивление и эластичность. Его высокое содержание в аггрекане играет важную роль в обеспечении устойчивости хряща к давлению при различных условиях нагрузки. Профиль сульфатации хондроитина был описан в хрящах [Mourao, 1988]. Изменения в структуре CS описаны в тканях OA [Caterson et al. 1990] и пониженное соотношение CS-6: CS-4 были обнаружены в синовиальной жидкости и хрящах пациентов с ОА [Shinmei et al. 1992]. Более трех десятилетий назад было предложено [Schwartz and Dorfman, 1975], что поставка CS в качестве терапевтического вмешательства при повреждении хряща может обеспечить строительные блоки для синтеза нового компонента матрикса, поскольку повышение концентрации CS может действовать в пользу матрикса. регенерация и учитывать ее благотворное влияние.
Химическая структура хондроитинсульфата, где R — Na или H, а X — SO 3 R или H.
Однако с тех пор механизм действия CS как терапевтического вмешательства все еще требует выяснения, а его эффективность остается предметом дискуссий.
Общая цель этого обзора состояла в том, чтобы собрать большую часть доступной информации о CS, его фармакокинетике, его эффектах in vitro, и in vivo, и его клинической эффективности. Цель этого обзора — обсудить клиническую полезность CS и перспективы использования CS при лечении остеоартрита.
Фармакокинетика
Natural CS имеет молекулярную массу 50–100 кДа.После процесса экстракции молекулярная масса составляет 10-40 кДа в зависимости от сырья. CS в основном получают из бычьего, свиного или морского (акульего) хряща.
CS чаще всего вводят перорально в дозах от 800 до 1200 мг / день. CS быстро всасывается в желудочно-кишечном тракте. Поглощенный CS достигает компартмента крови в виде 10% CS и 90% деполимеризованных низкомолекулярных производных.
Сообщалось о различной биодоступности и фармакокинетических переменных в зависимости от характеристик и происхождения CS [Malavaki et al. 2008]. О некоторых из них сообщили в. Биодоступность CS обсуждается. Данные зависят от системы, используемой для оценки, структуры и характеристик CS, таких как молекулярная масса, плотность заряда и кластер дисульфатированных дисахаридов, используемой концентрации и вида животных, использованных для проведения исследования [Volpi, 2003]. В большинстве исследований использовался CS из трахеи крупного рогатого скота (чистота 95%), который представляет собой тот же материал, который использовался в клинических испытаниях [Barnhill et al. 2006].
Таблица 1.
Различные фармакокинетические параметры в зависимости от системы исследования и источника CS.
| Исследование | Источник хондроитина | Система | Результаты | |
|---|---|---|---|---|
| Conte et al. [1995] | Трахея крупного рогатого скота 16 мг / кг перорально | Крысы Wistar | ||
| Трахея крупного рогатого скота 16 мг / кг перорально | Молодые собаки породы бигль | |||
| Трахея крупного рогатого скота Разовая доза 0.8 г или две дозы по 0,4 г | Здоровые добровольцы ( N = 12; 6 мужчин и 6 женщин) | Разовая доза: | Две дозы: | |
| Трахея крупного рогатого скота Разовая доза 0,8 г / день | Пациенты с ОА ( N = 18) | Концентрация в плазме:
| ||
| Ronca . [1998] | Смесь CS-6 и CS-4 (1: 1) Пероральное введение 16 мг / кг (4 мг / крыса) | Крысы ( N = 10) |
| |
| Volpi [2002] | Хондросульф® однократная доза (4 г) | Мужчина здоровый волонтеры ( N = 20) | ||
| Volpi [2003] | Shark CS Однократная доза (4 г) | Здоровые добровольцы мужского пола ( N = 20) |
Биодоступность CS после перорального приема колеблется от 10% до 20% [Lauder, 2009].
Поглощение CS может зависеть от статуса сульфатации. Положение и процентное содержание сульфатных групп обычно варьируется в зависимости от конкретных источников животного происхождения [Volpi, 2006a, 2006b]. Действительно, десульфатированный хондроитин у мышей [Kusano et al. 2007] имеет очень быстрое поглощение, с пиком в течение 15 минут и очень быстрым возвращением к исходному уровню через 3 часа, тогда как CS у акул у здоровых добровольцев мужского пола поглощается медленнее (пик через 8,7 часа) и медленнее выведение (уровни поддерживаются). до 16 часов после администрирования) [Volpi, 2003].CS из трахеи крупного рогатого скота демонстрирует быстрое увеличение плазмы здоровых добровольцев мужского пола с пиком в пределах 1–5 часов после введения и возвращением к исходному уровню через 10 часов [Volpi, 2002].
Фармакокинетические параметры CS, определенные у здоровых добровольцев мужского пола [Volpi, 2002], после перорального приема показали значительное увеличение уровней CS в плазме (более чем на 200%) по сравнению с уровнями перед дозой в течение 24 часов. Пиковые концентрации наблюдались через 2 часа после дозирования, и увеличение значимо через 2-6 часов после дозирования.Кинетика первого порядка наблюдалась для доз до 3000 мг. Многократные дозы 800 мг для пациентов с ОА не изменяют кинетику CS. Недавно, используя флуорофорный углеводный электрофорез и хроматографию наложения 6, Джексон и его коллеги не наблюдали никаких изменений эндогенной концентрации (20 (мкг / мл) и состава дисахаридов CS после перорального приема однократной дозы 1200 мг CS. Одно объяснение может быть, что небольшое количество проглоченного CS достигает циркуляции в неизмененной форме или состоит из дисахаридов более крупных фрагментов [Jackson et al. 2010]; в качестве альтернативы, могло случиться так, что анализ был недостаточно чувствителен для обнаружения более низких концентраций. Это еще предстоит продемонстрировать другими методами анализа. Другой характеристикой CS является его способность накапливаться в суставных тканях. Высокое содержание меченого CS было обнаружено в тканях суставов, включая синовиальную жидкость и хрящ, после перорального введения людям [Ronca et al. 1998].
Трудно оценить релевантность максимальной концентрации, достигнутой в компартменте крови (Cmax) для этого типа лекарственного средства, поскольку in vivo ответ может быть результатом воздействия CS и дисахаридов.Более того, CS — это препарат замедленного действия, в результате чего действие начинается медленно, а максимальный эффект достигается через несколько месяцев. Кроме того, CS — это лекарство биологического происхождения, что означает, что его измерение в биологических жидкостях не позволяет отличить лекарство от эндогенных молекул. Максимальный эффект (Emax) был предсказан с использованием альтернативного метода [du Souich and Verges, 2001]. Эффект Emax рассчитывали на основании клинической эффективности. Было подсчитано, что 50% Emax достигается за 35 дней у пациентов с легким ОА.Примерный период полураспада CS и его производных в плазме крови человека составляет 15 часов. Стабильное состояние достигается через 3–4 дня, и для получения максимального эффекта может потребоваться 3–6 месяцев лечения.
CS не метаболизируется цитохромом P450. Это говорит в пользу очень низкого риска взаимодействия с другими лекарствами.
Наконец, для CS был описан эффект переноса. Действительно, после отсроченного начала действия максимальный эффект сохраняется после прекращения терапии.
Механизм действия
Многие эффекты были описаны для CS в различных исследованиях in vitro, и in vivo, с использованием различных типов и концентраций CS и различных моделей.Точный механизм действия еще предстоит уточнить. In vitro эффекты на суставные клетки и эффекты in vivo на моделях артрита описаны в и, соответственно.
Таблица 2.
In vitro эффекты хондроитинсульфата.
| Исследование | Хондроитин | Система и продолжительность | Результаты | ||||
|---|---|---|---|---|---|---|---|
| Verbruggen et al. [1977] | 10–400 мкг / мл | Однослойные синовиальные клетки | Стимуляция 11% синтеза гиалуроната во время фазы роста | ||||
| Увеличение на 88% во время стационарной фазы | |||||||
| Bassleer et al. [1998] | КРС 100–1000 мкг / мл | Суставные хондроциты человека в кластерах, стимулированные IL-1β До 32 дней | Значительное снижение продукции PGE, стимулированной IL-1β 2 | ||||
| Увеличение выработки коллагена PG и типа II | |||||||
| Wang et al. [2002] | C poly S 10 мкг / мл | Человеческие суставные хондроциты в агарозном геле, стимулированные IL-1β 1 неделя | Стимуляция аггрекана, гиалуронана и коллагена типа II из-за подавления ММП | ||||
| Campo et al. al. [2004] | CS-4 1,0 и 2,0 мг / мл | Фибробласт кожи человека | Антиоксидантное действие CS-4 за счет повышения жизнеспособности клеток и ингибирования фрагментации ДНК | ||||
| Chan et al. [2005a] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Снижение IL-1β-индуцированной MMP-13 | ||||
| Chan et al. [2005b] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Подавление индуцированной IL-1β экспрессии NO-синтазы, COX-2 и mPGES-1 | ||||
| Монфорт и др. [2005] | 10–1000 мкг / мл | Хондроциты ОА человека, стимулированные IL-1β 48 ч | Ингибирование MMP-3 | ||||
| Holzmann et al. [2006] | 25 мкг / мл | Человеческие суставные хондроциты, стимулированные LPS До 72 часов | Ингибирование MMP-13 за счет снижения активации p38 и Erk1 / 2 | ||||
| Tat et al. [2007] | 200 мкг / мл | Остеобласты субхондральной кости человека ОА До 48 ч | Снижение прорезорбтивных агентов | ||||
| Обратное действие витамина D3 на соотношение OPG: RANK9584 | Tahiri et al. [2008] | Хондросульф® или свинья 10 или 100 мкг / мл | Хондроциты суставов кролика, стимулированные IL-1β 20 ч | Повышение синтеза PG | |||
| Ингибирование экспрессии AD10AMTS-5 | |||||||
| Jomphe et al. [2008] | Очищенные бычьи CS-4 и CS-6 200 мг / мл | Хондроциты кролика, стимулированные IL-1β 48 ч | Снижение ядерной транслокации NF-κB | ||||
| Профилактика активации Erk1 / 2 и p38 | |||||||
| Снижение апоптоза, индуцированного нитропруссидом | |||||||
| Legendre et al. [2008] | Avian CS −100 мкг / мл | Бычьи суставные хондроциты в гипоксических альгинатных гранулах 24–48 часов | Снижение IL-1β-индуцированных MMP-1, −3, −13 и ADAMTS-4 и — 5 | ||||
| Снижение IL-1β-индуцированного COX-2 и iNOS | |||||||
| Снижение продукции PGE 2 , но не NO | Незначительное увеличение синтеза ГАГ | ||||||
| Противодействие подавлению IL-1β рецепторов TGFβ | |||||||
| Katta et al. [2009] | Смесь CS A, CS B и CS C 10–50 мг / мл | Эксплантаты бычьего хряща 24 ч | Эффективная смазка для суставов | ||||
| Распространение в хрящ | |||||||
| Давид-Рауди et al. [2009] | Avian CS 100 мкг / мл | OA фибробластоподобные синвиоциты человека 48 часов с предварительной обработкой | Регулирование гиалуронансинтазы | ||||
| Campo et al. [2009a] | CS-4 крупного рогатого скота и CS-6 акулы 0,5 и 1,0 мг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Антиапоптотический эффект обоих CS | ||||
| Ингибирование медиаторов воспаления, iNOS и MMP более очевидно с CS-4, чем с CS-6 | |||||||
| Campo et al. [2009b] | CS-4 крупного рогатого скота и CS-6 акулы 25 и 50 мкг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Ингибирование воспалительных цитокинов (MyD88 и TRAF-6), ингибирование активации NF -kB и iNOS обоими CS | ||||
| Эффект через TLR4 (подтвержден экспериментом со специфическими антителами) | |||||||
| Bian et al. [2009] | CS-6 и CS-4 акульего происхождения 10–100 мг / мл | Эксплантаты бычьего хряща 4 недели | Снижение содержания ГАГ | ||||
| Imada et al. [2010] | Акула (в основном CS-6) и свинья (в основном CS-4) 1–100 мкг / мл | Суставные хондроциты человека в альгинатных шариках и синовиальный фибробласт, стимулированные IL-1β 6 или 4 дня | Разные эффект обеих CS | ||||
| Подавление индуцированных IL-1b ADAMTS-4 и -5 в обоих типах клеток | |||||||
| Подавление индуцированных IL-1β MMP- 13 и увеличить экспрессию аггрекана в хондроцитах | |||||||
| Восстановление TIMP-3 в хондроцитах и TIMP-1 в синовиоцитах CS свиньи |
Таблица 3.
In vivo эффекты хондроитинсульфата.
| Исследование | Хондроитин | Модель | Результаты |
|---|---|---|---|
| Uebelhart et al. [1998] | 80 мг / день перорально или i. м. | Кроличья модель повреждения хряща, вызванного химопапаином | Значительное увеличение продукции PG |
| Omata et al. [2000] | 1000 мг / кг | Коллаген-индуцированный артрит у мышей | Снижение параметров синовита: клеточная инфильтрация, фиброз и пролиферация выстилающих клеток |
| Campo et al. [2003] | 1 мл / кг (внутрибрюшинно) | Коллаген-индуцированный артрит у крыс | Лечение начинали после начала артрита (день 10) |
| Защита от окислительного стресса | |||
| 25 мг / кг (перорально) | Снижение уровней TNF-α и миелопероксидазы в плазме | ||
| Cho et al. [2004] | 1200 мг / кг | Коллаген-индуцированный артрит у крыс | Снижение уровней IL-6 |
| Caraglia et al. [2005] | 0,3 мг / день | Спонтанный ОА у мышей 12 дней | Значительное уменьшение апоптозных хондроцитов через 30 дней |
| Chou et al. [2005] | Пищевая добавка (18 мг / г) | Адъювант-индуцированный артрит Фрейнда у крыс | Предотвращение увеличения MMP-9 Снижение уровня IL-1β в тканях суставов, но не в сыворотке |
| Campo et al. al. [2008] | CS-4 (трахея крупного рогатого скота) 30–120 мг / кг (т.е.p.) | Коллаген-индуцированный артрит у мышей В течение 25 дней | Ингибирование активации NF-κB Ингибирование MMP-13 ингибирование активации каспаз-3 и -7 |
Противовоспалительный эффект
CS. сообщалось, что он обладает противовоспалительным действием. Было показано, что он ингибирует in vitro синтез различных промежуточных продуктов воспаления, таких как синтаза оксида азота (NO), циклооксигеназа (COX) -2, микросомальная простагландин-синтаза (mPGES) -1 и простагландин (PG) E 2 [Campo и другие. 2009a; Legendre et al. 2008; Чан и др. 2005b; Bassleer et al. 1998]. Также было показано, что CS может действовать на toll-подобный рецептор (TLR) -4, ингибируя воспалительные цитокины, MyD88 и фактор, связанный с рецептором фактора некроза опухоли (TNF) (TRAF) -6, посредством ингибирования ядерного фактора (NF ) -kB активация [Campo et al. 2009b].
Противовоспалительный эффект CS был также продемонстрирован in vivo. Было показано, что CS снижает синовит при коллаген-индуцированном артрите у мышей [Omata et al. 2000]. Он также был способен снижать провоспалительный цитокин, интерлейкин (IL) -6, в той же модели [Cho et al. 2004]. CS также снижает уровень IL-1b в суставной ткани при адъювантном артрите Фрейнда при введении в качестве пищевой добавки [Chou et al. 2005] и TNF-α и миелопероксидаза в плазме крови крыс с коллаген-индуцированным артритом и после перорального введения [Campo et al. 2003].
Антикатаболические и анаболические эффекты
Первый анаболический эффект CS был описан более 30 лет назад.CS увеличивал синтез гиалуроната в синовиальных клетках [Verbruggen and Veys, 1977]. С тех пор было также продемонстрировано увеличение синтеза коллагена типа II и протеогликана (PG) в хондроцитах человека [Wang et al. 2002; Bassleer et al. 1998] и ГАГ в хондроцитах крупного рогатого скота [Legendre et al. 2008]. Этот эффект также может быть вторичным по отношению к подавлению регуляции матриксной металлопротеиназы (ММП) [Wang et al. 2002]. Было также показано, что CS ингибирует MMP-1, -3 и -13, а также ADAMTS-4 и -5 (аггреканазы) в хондроцитах человека, свиньи и крупного рогатого скота [Imada et al. 2010; Legendre et al. 2008; Tahiri et al. 2008; Чан и др. 2005a; Монфорт и др. 2005]. Ингибирование MMP-13 может происходить через ингибирование активации p38 и Erk1 / 2 [Holzmann et al. 2006]. Для CS-4 и CS-6 были продемонстрированы различные ингибирующие способности против ММП в хондроцитах мышей [Campo et al. 2009a]. Различия между CS-6 и CS-4 недавно были также показаны на человеческих клетках. Действительно, CS-6 (акульего происхождения) может противодействовать ингибированию IL-1b тканевым ингибитором металлопротеаз (TIMP) -3 в хондроцитах человека и TIMP-1 в синовиальных фибробластах, тогда как CS-4 (происхождение из трахеи свиньи) не дает того же эффект [Imada et al. 2010]. CS может активировать гиалуронансинтазу в фибробластоподобных клетках [David-Raoudi et al. 2009] и может быть эффективным в качестве смазки для суставов, как было показано на эксплантатах бычьего хряща [Katta et al. 2009]. Также сообщалось, что CS может влиять на процесс резорбции, происходящий в субхондральной кости во время ОА. CS действительно может увеличивать соотношение остеопротегерин (OPG): активатор рецептора для лиганда NF-κB (RANKL) в остеобластах OA в пользу гомеостаза субхондральной кости [Tat et al. 2007]. Было продемонстрировано, что CS действует на большинство суставных тканей, участвующих в патофизиологии ОА. Наконец, недавнее исследование in vitro на эксплантатах бычьего хряща, обработанных CS-4 и CS-6 в течение 4 недель, выявило отрицательный эффект CS, показывающий, что он снижает содержание GAG [Bian et al. 2009]. Важно отметить, что это исследование было проведено с самой высокой концентрацией CS из когда-либо протестированных (10–100 мг / мл).
Анаболический и антикатаболический эффект CS также был продемонстрирован in vivo. CS может увеличивать продукцию PG на кроличьей модели деградации хряща [Uebelhart et al. 1998], предотвращают повышение уровня ММР-9 при адъювантном артрите Фрейнда у крыс при введении в качестве пищевой добавки [Chou et al. 2005] или ингибируют ММР-13 при коллаген-индуцированном артрите у мышей [Campo et al. 2008].
Антиапоптотический эффект
CS продемонстрировал антиапоптотические свойства как in vitro, так и in vivo. Было показано, что CS (200 (мкг / мл) снижает чувствительность хондроцитов кролика к апоптозу [Jomphe et al. 2008]. Этот эффект был связан с уменьшением транслокации NF-κB и со снижением пути передачи сигналов киназы MAP через p38 и Erk1 / 2. Другое исследование указало на антиапоптотический эффект CS-4 и CS-6 в суставных хондроцитах мыши [Campo et al. 2009a]. In vivo, на мышиной модели спонтанного ОА было показано, что 12-дневное лечение CS (0,3 мг / день) снижает количество апоптозных хондроцитов при оценке через 30 дней [Caraglia et al. 2005]. Также было продемонстрировано, что он способен ингибировать активацию каспазы-3 и -7 при коллаген-индуцированном артрите у мышей [Campo et al. 2008]. Эти результаты свидетельствуют в пользу хондропротекторного действия CS.
Антиоксидантный эффект
Антиоксидантные эффекты были рассмотрены [Campo et al. 2006a, 2006b]. Было показано, что CS обладает антиоксидантными свойствами in vitro в фибробластах кожи человека [Campo et al. 2004] и in vivo при коллаген-индуцированном артрите у крыс [Campo et al. 2003]. CS обеспечивает защиту от перекиси водорода и супероксид-анионов. Действительно, эти исследования продемонстрировали, что он может ограничивать гибель клеток, уменьшать фрагментацию ДНК и окисление белков, уменьшать образование свободных радикалов и действовать как поглотитель свободных радикалов. Он снижает перекисное окисление липидов и улучшает антиоксидантную защиту за счет восстановления эндогенных антиоксидантов, восстановленного глутатиона (GSH) и супероксиддисмутазы (SOD).
Регуляция клеточного сигнального пути
CS, как было обнаружено, действует на основные клеточные сигнальные пути.Было показано, что он ингибирует активацию пути киназы MAP, p38 и Erk ½, а также ингибирование трансактивации NF-κB в хондроцитах кролика [Jomphe et al. 2008; Verge’s et al. 2004]. Было также показано, что CS действует на другие промежуточные продукты клеточной передачи сигналов [Egea et al. 2010]. CS был способен индуцировать путь протеинкиназы C (PKC) / PI3K / Akt в клетках нейробластомы. Многие эффекты, описанные для CS на патофизиологию ОА, могут быть связаны с его действием на передачу сигналов в клетках.
Важно помнить, что большинство эффектов in vitro было получено с использованием высоких концентраций CS, которые не соответствуют ожидаемым концентрациям в плазме. Более того, учитывая медленное действие препарата на человека, системы in vitro и in vivo использовались в течение довольно короткого времени. Различные авторы предположили, что высокая концентрация, используемая in vitro, использовалась для компенсации этих проблем [Tat et al. 2010; Монфорт и др. 2008b]. Различия в чистоте и свойствах CS могут быть причиной несоответствия эффектов. Это было недавно рассмотрено в двух всеобъемлющих обзорах [Rainsford, 2009; Вольпи, 2009]. Это было подтверждено даже в суставных хондроцитах [Tat et al. 2010], когда три разных типа CS были протестированы в одной и той же системе и оказали различное воздействие на ключевые медиаторы OA. Это исследование продемонстрировало, что ХС бычьего происхождения гораздо эффективнее ингибирует катаболические медиаторы, чем ХС свиного происхождения.Также важно отметить, что эффекты CS in vivo в основном наблюдались на животных моделях артрита. Только одно исследование было проведено на модели спонтанного ОА [Caraglia et al. 2005].
Точный механизм действия CS еще предстоит выяснить. Взятые вместе, эти данные предполагают вмешательство CS на разных уровнях патофизиологии ОА, как показано в.
Схематическое изображение мишеней хондроитинсульфата (CS) в хондроцитах во время остеоартрита, как было предложено исследованиями in vitro: CS действует на сигнальные пути клеток, воспалительные и катаболические пути и на окислительный стресс (как показано черными стрелками).CS нацелен на различные промежуточные соединения в этих путях (как показано серыми стрелками). CS, хондроитинсульфат; ИЛ, интерлейкин; ECM, внеклеточный матрикс; ПГЕ 2 , простагландин E 2 ; PG, протеогликан; ММП, матриксная металлопротеиназа; NO, оксид азота; ADAMTS, дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами; NF-κB, ядерный фактор kB; ЦОГ, циклоосигеназа, iNOS, индуцируемая синтаза оксида азота.
Клинический эффект хондроитинсульфата
Терапевтическая эффективность CS изучалась и сообщалась в различных клинических исследованиях у пациентов с ОА.Влияние CS на пациентов с ОА оценивалось либо по симптомам ОА (боль и функция), чтобы определить его симптоматическое лекарство замедленного действия для эффекта ОА (SYSADOA), либо по модификации заболевания (эффект структуры, сужение суставной щели (JSN)) для определения его модифицирующий болезнь эффект препарата ОА (DMOAD).
Симптоматическое лекарство замедленного действия для лечения ОА
Различные мета-анализы [Reichenbach et al. 2007; Richy et al. 2003; Leeb et al. 2000; McAlindon et al. 2000] сообщили о различной величине эффекта (ES) на боль и функцию CS в диапазоне от 0,9 до всего 0,3.
Недавно были разработаны и опубликованы три исследования, посвященных влиянию CS на SYSADOA, то есть исследование GAIT [Hochberg and Clegg, 2008; Clegg et al. 2006], исследование STOPP [Kahan et al. 2009] и еще одно рандомизированное контролируемое исследование (РКИ) [Mazieres et al. 2007; Mazieres et al. 2006] (). Совсем недавно рекомендации Международного общества исследований остеоартрита (OARSI) по лечению ОА определили умеренный или большой ES (0.75, 95% ДИ 0,50–0,99) [Zhang et al. 2010], но подчеркнул систематическую ошибку публикации, неоднородность результатов и кумулятивное снижение ES (1,85, 95% ДИ 1,47–2,22, в 1992 г. до 0,75, 95% ДИ 0,50–1,01, в 2006 г.).
Таблица 4.
| Исследование | Результат | Вмешательство | Население и продолжительность | Размер результата / эффекта | |||||
|---|---|---|---|---|---|---|---|---|---|
| Глобальная оценка | 900 Maziéres et al. [2007] | Глобальная оценка исследователями клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 3,1 (CS) и 2,5 (Плацебо), p = 0,044 Благоприятствует CS | ||||
| Общая оценка пациентом клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец обработки) | NS | ||||||
| Качество жизни | |||||||||
| Maziéres et al. [2007] | Физический компонент SF-12 (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 5,8 (CS) и 3,8 (плацебо), p = 0,021 Благоприятствует CS | |||||
| SF-12 Психический компонент | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Pain | |||||||||
| Clegg et al. [2006] | Боль | CS против плацебо | РКИ, N = 1583, 24 недели | CS не лучше, чем плацебо | |||||
| Maziéres et al. [2007] | Боль во время активности, ВАШ (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | −41% (CS ) и -32% (плацебо), p = 0,029 Поддерживает CS | |||||
| Боль в покое, ВАШ (изменение от исходного уровня) | CS vs. плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Reichenbach et al. [2007] | Исходы, связанные с болью | CS по сравнению с плацебо / без лечения | MA, 20 РКИ, n = 3846, ОА коленного или тазобедренного сустава, продолжительность испытаний от 6 до 132 недель | Значительная неоднородность | |||||
| Kahan et al. [2009] | Подшкала VAS и WOMAC | CS vs. плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Значительно более быстрое уменьшение боли в целевом колене с помощью CS | |||||
| Функция | |||||||||
| Clegg et al. [2006] | Припухлость сустава, выпот или и то, и другое при клиническом обследовании | CS по сравнению с плацебо | РКИ, N = 1583, 24 недели | CS значительно лучше | |||||
| Maziéres et al. [2007] | Индекс Лекена (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | |||||
| Изменение структуры | |||||||||
| Reichenbach et al. [2007] | Минимум JSW | CS по сравнению с плацебо / без лечения | MA, 5 РКИ, N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | ES средняя разница 0 .16 мм, 95% ДИ 0,08–0,24 | |||||
| Благоприятствует хондроитину | |||||||||
| Среднее значение JSW | CS по сравнению с плацебо / без лечения | MA, 5 N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследования от 6 до 132 недель | ES средняя разница 0,23, 95% ДИ 0,09–0,37 | ||||||
| Поддерживает хондроитин | |||||||||
| Кахан и другие. [2009] | Минимальный JSW | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Повышение эффекта лечения со временем | |||||
| CS значительно лучше для JSW | |||||||||
| Lee et al. [2010] | Минимальный JSN | CS по сравнению с плацебо | MA, 4 РКИ, N = 1088, ОА коленного сустава, период наблюдения от 1 до 2 лет | Небольшой, но значительный защитный эффект CS через 2 лет на минимуме JSN | |||||
| Hochberg [2010] | Минимум JSW | MA, 3 РКИ, N = 1179, Коленный остеоартрит, последующее наблюдение 2 года | Значительное снижение скорости уменьшения суставной щели ширина с CS | ||||||
| ES 0.23 (95% ДИ 0,11–0,35) | |||||||||
| Неблагоприятные события | |||||||||
| Maziéres et al. [2007] | Количество пациентов по крайней мере с одним НЯ, связанным с лечением | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | NS | |||||
| Всего количество НЯ | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | N = 18 (CS) и N = 20 (плацебо) NS | ||||||
| Reichenbach et al. [2007] | Пациенты с НЯ | CS по сравнению с плацебо / без лечения | MA, 12 РКИ, N = 1929, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | |||||
| Исключение из-за НЯ | Хондроитин по сравнению с плацебо / отсутствие лечения | МА, 9 РКИ, N = 1781, ОА коленного и тазобедренного суставов, диапазон продолжительности исследований от 6 до 132 недель | NS | ||||||
| Пациенты с тяжелыми НЯ | Хондроитин vs. плацебо / без лечения | MA, 2 РКИ, N = 217, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | ||||||
| Kahan et al. [2009] | Исключение из-за НЯ | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | NS |
Сообщалось о глобальных клинических испытаниях a благотворное влияние CS на боль и функцию (). Однако в самом крупном исследовании GAIT не сообщалось о влиянии на эти конечные точки.
Эффекты модификации структуры
Эффекты модификации структуры CS были описаны и проанализированы в двух недавних метаанализах [Hochberg, 2010; Ли и др. 2010]. Ранее сообщалось, что не было неоднородности в результатах РКИ по эффектам модификации структуры [Hochberg et al. 2008]. Результаты показали небольшое, но значительное снижение ухудшения JSN (ES = 0,26, 95% ДИ 0,16–0,36). Недавно при наблюдении за пациентами в течение 2 лет было выявлено значительное влияние CS на JSN у пациентов, получавших CS, по сравнению с плацебо [Kahan et al. 2009].
Безопасность и переносимость
В большинстве клинических испытаний сообщалось о прекрасном профиле безопасности и хорошей переносимости CS. Частота побочных эффектов и частота отказов были эквивалентны в группах CS и плацебо. При применении CS не наблюдалось серьезных серьезных побочных эффектов. Спасательные препараты (парацетамол или нестероидные противовоспалительные препараты [НПВП]) разрешены во время клинических испытаний. Этот факт может уменьшить разницу между группами CS и плацебо [Monfort et al. 2008a] ().
Хондроитинсульфат в рекомендациях
CS рекомендован в руководствах, опубликованных OARSI и Европейской лигой против ревматизма (EULAR) для лечения ОА коленного сустава [Zhang et al. 2008; Jordan et al. 2003]. OARSI рекомендует CS из-за его симптоматического и структурно-модифицирующего эффекта при ОА коленного сустава, но также рекомендует прекратить его через 6 месяцев, если симптоматическая реакция отсутствует. Что касается ОА бедра и кисти, EULAR рекомендует SYSADOA, включая CS, из-за их симптоматических эффектов и низкой токсичности, но подчеркивает тот факт, что ES небольшие, подходящие пациенты не определены должным образом, а клинически значимая модификация структуры и фармакоэкономический аспект не очень хорошо установлено.
Обсуждение
CS используется уже несколько десятилетий, и было важно описать его фармакокинетику, механизм действия и описать его клиническую эффективность.
CS обладает различными эффектами, от противовоспалительных и антикатаболических до антиапоптотических, а также антиоксидантных свойств. Все эти результаты были получены в разных системах с разными дозировками. Во многих обзорах говорится о важности источника CS и чистоты [Lauder, 2009; Рейнсфорд, 2009 г .; Вольпи, 2009; Лаудер и др. 2000]. Кроме того, сульфатированный CS в разных положениях (например, 4 или 6) может иметь разные эффекты. Например, CS-4 более эффективен как антиоксидант, чем CS-6 [Albertini et al. 2000; Volpi, Tarugi, 1999]. Исследования in vitro и in vivo имеют ограничения, в основном из-за используемой концентрации и продолжительности исследования. CS используется в концентрациях, которые значительно превосходят плазменную концентрацию после перорального введения терапевтической дозы CS. Действительно, CS достиг концентрации в плазме примерно 2.0 мкг / мл у пациентов с ОА после перорального введения 0,8 г CS [Conte et al. 1995]. Это исследование также показало, что CS может достигать 2,7 мг / мл в синовиальной жидкости пациентов с ОА. Другой эксперимент на крысах после перорального введения (16 мг / кг) показал концентрацию 3,3 мг / г в хрящах [Ronca et al. 1998]. В большинстве исследований in vitro использовалось от 10 мг / мл CS до 1000 мг / мл (см.). При интерпретации данных необходимо учитывать условия исследования. Наконец, недавно был проведен обзор эффективности КС при воспалительных состояниях, отличных от ОА, и в основном более тяжелых, чем ОА [Vallières and du Souich, 2010; du Souich et al. 2009]. Было показано, что CS эффективен при патологии, включая псориаз [Möller et al. 2010; Verges et al. 2005]. Это предполагает сильную противовоспалительную активность CS. К сожалению, отсутствие inivo демонстрации влияния CS на прогрессирование ОА. Только в одном исследовании изучалось влияние хондроитина на модель ОА. Для лучшего понимания клинической эффективности CS необходимы дальнейшие исследования, изучающие влияние CS на деградацию хряща, ремоделирование субхондральной кости и воспаление синовиальной оболочки.
CS рекомендуется OARSI в качестве вмешательства SYSADOA для лечения ОА [Zhang et al. 2010, 2008] и EULAR [Jordan et al. 2003]. Обе организации признали его симптоматические и структурно-модифицирующие эффекты. OARSI рекомендует прекратить лечение через 6 месяцев при отсутствии эффективности [Zhang et al. 2008]. В то время, когда EULAR опубликовал свои рекомендации, они предложили растущие доказательства эффективности CS. Однако ко времени последнего обновления OARSI [Zhang et al. 2010], ES снизился, что свидетельствует о нестабильности эффективности, что, по крайней мере частично, может быть связано с повышением качества исследований. Несоответствие эффективности, показанное в нескольких клинических испытаниях, имеет большое значение. Этот метаанализ [Zhang et al. 2010] также продемонстрировал серьезную предвзятость публикации. Эти наблюдения также сделаны для других соединений класса SYSADOA, включая сульфат глюкозамина (GS). Напротив, ES для ацетаминофена, хотя и очень маленький, по-видимому, со временем стабилизировался, что позволяет предположить, что дальнейших РКИ для проверки его анальгетической эффективности не требовалось.В целом, этот обзор указывает на то, что существует потребность в клинических испытаниях хорошего качества с продолжительностью и количеством пациентов, соответствующих этому виду соединений. Также уместно сравнить ES для боли основных фармакологических методов, обычно используемых при лечении ОА. Для сравнения, ЭС CS — одна из самых важных. Например, болевой синдром ES (2010 г.) для ацетаминофена составил 0,14 (95% 0,05–0,23), для НПВП 0,29 (95% 0,22–0,35) и для CS 0,75 (95% 0,50–1,01). Это говорит о клинической значимости использования CS для лечения ОА, учитывая его низкую токсичность. ОА является долгосрочным прогрессирующим заболеванием, для которого перед применением каждого лечения должна быть проведена оценка соотношения риск / польза.
В некоторых исследованиях оценивалась эффективность использования CS в сочетании с GS. Это было сделано in vitro [Chan et al. 2006, 2007, 2005a, 2005b], а также в клинических испытаниях [Vangsness et al. 2009; Sawitzke et al. 2008; Clegg et al. 2006, 2005]. Синергетический эффект обоих соединений еще предстоит продемонстрировать, но многие авторы рекомендуют использовать комбинацию.
Одна из причин для оптимизма в отношении использования CS отдельно или в сочетании со связанным продуктом, таким как GS, — это профиль безопасности.CS не взаимодействует с другими лекарствами и не вызывает серьезных побочных эффектов. Это говорит в пользу положительного соотношения риск / польза.
Заключение
Несмотря на умеренное влияние CS на боль и функцию, CS представляет собой интересный продукт для лечения ОА коленного сустава. Клинические данные свидетельствуют в пользу медленного действия на симптомы умеренного ОА коленного сустава. CS рекомендуется по самым популярным рекомендациям. Его профиль безопасности, несомненно, является одним из основных преимуществ при лечении стареющих пациентов с некоторыми сопутствующими заболеваниями.Таким образом, нет никаких ограничений для его использования у пациентов с ОА, если не учитывать экономический эффект. Тем не менее, следует проявлять осторожность в отношении типа и состава CS. Конечно, остаются вопросы относительно механизма его действия. Эффект CS на воспаление субхондральной кости и синовиальной оболочки может быть лучше документирован.
Благодарности
Авторы благодарят L. Montell Bonaventura и J. Verges из Bioiberica, любезно предоставившие документацию по хондроитинсульфату.К. Санчес — научный сотрудник Национального фонда научных исследований (FNRS, Бельгия).
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Проф. Хенротин получил образовательные и исследовательские гранты от Bioiberica, Expanscience, Danone, Nestec и BioXtract.
Ссылки
- Альбертини Р., Пасси А., Абуджа П.М., Де Лука Г. (2000) Влияние гликозаминогликанов и протеогликанов на перекисное окисление липидов.Инт Дж Мол Мед 6: 129–136 [PubMed] [Google Scholar]
- Barnhill J.G., Fye C.L., Williams D.W., Reda D.J., Harris C.L., Clegg D.O. (2006) Выбор хондроитинового продукта для интервенционного исследования артрита глюкозамином / хондроитином. J Am Pharm Assoc (Вашингтон, Вашингтон) 46: 14–24 [PubMed] [Google Scholar]
- Bassleer C.T., Combal J.P., Bougaret S., Malaise M. (1998) Влияние хондроитинсульфата и интерлейкина-1 бета на суставные хондроциты человека, культивируемые в кластерах. Остеоартроз Хрящ 6: 196–204 [PubMed] [Google Scholar]
- Биан Л., Каплун М., Уильямс Д.Ю., Сюй Д., Атешян Г.А., Хунг С.Т. (2009) Влияние хондроитинсульфата на биохимические, механические и фрикционные свойства хрящевых эксплантатов при длительном культивировании. J Биомеханика 42: 286–290 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Ferlazzo AM, Calatroni A. (2004) Уменьшение фрагментации ДНК и производство гидроксильных радикалов гиалуроновой кислотой и хондроитин-4-сульфатом в железе плюс индуцированный аскорбатом окислительный стресс в культурах фибробластов.Free Radic Res 38: 601–611 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Traina P., Calatroni A. (2008) Хондроитин-4-сульфат ингибирует NF-kB транслокация и активация каспаз при коллаген-индуцированном артрите у мышей. Остеоартроз Хрящ 16: 1474–1483 [PubMed] [Google Scholar]
- Кампо Г.М., Авенозо А., Кампо С., Д’Аскола А., Трэйна П., Сама Д. и др. (2009a) Гликозаминогликаны модулируют воспаление и апоптоз в хондроцитах, обработанных LPS.J Cell Biochem 106: 83–92 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Ferlazzo AM, Altavilla D., Calatroni A. (2003) Эффективность лечения гликозаминогликанами экспериментального коллаген-индуцированного артрита в крысы. Артрит Res Ther 5: R122 – R131 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006a) Антиоксидантная активность хондроитинсульфата. Adv Pharmacol 53: 417–431 [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006b) Хондроитинсульфат: антиоксидантные свойства и положительные эффекты. Мини Рев Мед Хим 6: 1311–1320 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Traina P., D’Ascola A., Calatroni A. (2009b) Гликозаминогликаны снижают воспалительную реакцию, модулируя толл-подобные рецептор-4 в хондроцитах, стимулированных ЛПС. Arch Biochem Biophys 491: 7–15 [PubMed] [Google Scholar]
- Caraglia M., Beninati S., Giuberti G., Д’Алессандро А.М., Лентини А., Аббруззезе А. и др. (2005) Альтернативная терапия земными элементами усиливает хондрозащитные эффекты хондроитинсульфата у мышей. Exp Mol Med 37: 476–481 [PubMed] [Google Scholar]
- Катерсон Б., Махмудиан Ф., Соррелл Дж. М., Хардингем Т. Э., Бейлисс М. Т., Карни С. Л. и др. (1990) Модуляция структуры нативного хондроитинсульфата в развитии тканей и при заболеваниях. J Cell Sci 97: 411–417 [PubMed] [Google Scholar]
- Чан П.С., Кэрон Дж.P., Orth M.W. (2005a) Влияние глюкозамина и хондроитинсульфата на регуляцию экспрессии генов протеолитических ферментов и их ингибиторов в эксплантатах суставного хряща быка, зараженных интерлейкином-1. Am J Vet Res 66: 1870–1876 [PubMed] [Google Scholar]
- Chan P.S., Caron J.P., Orth M.W. (2006) Кратковременные изменения экспрессии генов в хрящевых эксплантатах, стимулированные интерлейкином бета, глюкозамином и хондроитинсульфатом. J Ревматол 33: 1329–1340 [PubMed] [Google Scholar]
- Чан П.С., Карон Дж. П., Орт М. В. (2007) Влияние глюкозамина и хондроитинсульфата на эксплантаты бычьего хряща в условиях длительного культивирования. Am J Vet Res 68: 709–715 [PubMed] [Google Scholar]
- Chan PS, Caron JP, Rosa GJ, Orth MW (2005b) Глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простагландина E (2) в эксплантатах суставного хряща. . Остеоартроз Хрящ 13: 387–394 [PubMed] [Google Scholar]
- Чо С. Ю., Сим Дж.С., Чжон С. С., Чанг С. Ю., Чой Д. В., Тойда Т. и др. (2004) Влияние низкомолекулярного хондроитинсульфата на индуцированный коллагеном артрит типа II у мышей DBA / 1J. Биол Фарм Булл 27: 47–51 [PubMed] [Google Scholar]
- Chou M.M., Vergnolle N., McDougall J.J., Wallace J.L., Marty S., Teskey V. и др. (2005) Влияние хондроитина и сульфата глюкозамина в составе диетического батончика на воспаление, интерлейкин-1бета, матриксную металлопротеазу-9 и повреждение хряща при артрите. Эксп Биол Мед 230: 255–262 [PubMed] [Google Scholar]
- Клегг Д.О., Реда Д.Дж., Харрис К.Л., Кляйн М.А. (2005) Эффективность глюкозамина и хондроитинсульфата у пациентов с болезненным остеоартритом (ОА) коленного сустава: исследование вмешательства глюкозамина / хондроитина. Ревматоидный артрит 52 (9S): S256, (Аннотация). [Google Scholar]
- Clegg D.O., Reda D.J., Harris C.L., Klein M.A., O’Dell J.R., Hooper M.M., et al. (2006) Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med 354: 795–808 [PubMed] [Google Scholar]
- Конте А., Volpi N., Palmieri L., Bahous I., Ronca G. (1995) Биохимические и фармакокинетические аспекты перорального лечения хондроитинсульфатом. Arzneimittelforschung 45: 918–925 [PubMed] [Google Scholar]
- David-Raoudi M., Deschrevel B., Leclercq S., Galera P., Boumediene K., Pujol JP (2009) Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальная регуляция гиалуронансинтаз: роль p38 и Akt. Ревматоидный артрит 60: 760–770 [PubMed] [Google Scholar]
- du Souich P., Гарсия А.Г., Верджес Дж., Монтелл Э. (2009) Иммуномодулирующие и противовоспалительные эффекты хондроитинсульфата. J Cell Mol Med 13 (8A): 1451–1463 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- du Souich P., Verges J. (2001) Простой подход для прогнозирования максимального эффекта, вызываемого лекарством, когда концентрации в плазме недоступны или диссоциируют от воздействия, как показано на данных по хондроитинсульфату. Clin Pharmacol Ther 70: 5–9 [PubMed] [Google Scholar]
- Эгеа Дж., Гарсия А.Г., Верджес Дж., Монтелл Э., Лопес М.Г. (2010) Антиоксидантное, противовоспалительное и нейропротекторное действие хондроитинсульфата и протеогликанов. Остеоартроз Хрящ 18 (Приложение 1): S24 – S28 [PubMed] [Google Scholar]
- Hochberg M.C. (2010) Структурно-модифицирующие эффекты хондроитинсульфата при остеоартрите коленного сустава: обновленный метаанализ рандомизированных плацебо-контролируемых исследований продолжительностью 2 года. Остеоартроз Хрящ 18 (Приложение 1): 528–531 [PubMed] [Google Scholar]
- Hochberg M.К., Клегг Д.О. (2008) Потенциальные эффекты хондроитинсульфата на отек суставов: отчет GAIT. Остеоартроз Хрящ 16 (Приложение 3): S22 – S24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hochberg MC, Zhan M., Langenberg P. (2008) Скорость уменьшения ширины суставной щели у пациентов с остеоартритом колено: систематический обзор и метаанализ рандомизированных плацебо-контролируемых исследований хондроитинсульфата. Curr Med Res Opin, в печати. [PubMed] [Google Scholar]
- Holzmann J., Брандл Н., Земанн А., Шабус Р., Марловиц С., Коуберн Р. и др. (2006) Различные эффекты TGFbeta и хондроитинсульфата на уровни активации p38 и ERK1 / 2 в суставных хондроцитах человека, стимулированных LPS. Остеоартроз Хрящ 14: 519–525 [PubMed] [Google Scholar]
- Имада К., Ока Х., Кавасаки Д., Миура Н., Сато Т., Ито А. (2010) Механизмы антиартритного действия природного хондроитинсульфата у человека суставные хондроциты и синовиальные фибробласты. Биол Фарм Булл 33: 410–414 [PubMed] [Google Scholar]
- Джексон К.Г., Плаас А.Х., Сэнди Дж. Д., Хуа С., Ким-Роландс С., Барнхилл Дж. Г. и др. (2010) Фармакокинетика перорального приема глюкозамина и хондроитинсульфата у человека по отдельности или в комбинации. Остеоартроз Хрящ 18: 297–302 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Jomphe C.j, Gabriac M., Hale T.M., Heroux L., Trudeau L.E., Deblois D., et al. (2008) Хондроитинсульфат ингибирует ядерную транслокацию ядерного фактора-каппаВ в хондроцитах, стимулированных интерлейкином-1бета.Базовый Clin Pharmacol Toxicol 102: 59–65 [PubMed] [Google Scholar]
- Jordan K.M., Arden N.K., Doherty M., Bannwarth B., Bijlsma J.W., Dieppe P., et al. (2003) Рекомендации EULAR 2003: научно обоснованный подход к лечению остеоартрита коленного сустава: отчет рабочей группы Постоянного комитета по международным клиническим исследованиям, включая терапевтические испытания (ESCISIT). Энн Рум Дис 62: 1145–1155 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Kahan A., Uebelhart D., De Vathaire F., Дельмас П.Д., Регинстер Дж. (2009) Долгосрочные эффекты хондроитинов 4 и 6 сульфата на остеоартрит коленного сустава: исследование по предотвращению прогрессирования остеоартрита, двухлетнее рандомизированное двойное слепое плацебо-контролируемое исследование. Ревматоидный артрит 60: 524–533 [PubMed] [Google Scholar]
- Катта Дж., Джин З., Ингам Э., Фишер Дж. (2009) Хондроитинсульфат: эффективная смазка для суставов? Остеоартроз Хрящ 17: 1001–1008 [PubMed] [Google Scholar]
- Кусано С., Отани А., Сакаи С., Игараси Н., Такегучи А., Тойода Х. и др. (2007) Определение хондрозина в плазме крови мышей с помощью ВЭЖХ после внутривенной или пероральной дозы. Биол Фарм Булл 30: 1365–1368 [PubMed] [Google Scholar]
- Лаудер Р.М. (2009) Хондроитинсульфат: сложная молекула с потенциальным воздействием на широкий спектр биологических систем. Комплемент Терапии Мед 17: 56–62 [PubMed] [Google Scholar]
- Лаудер Р.М., Хакерби Т.Н., Недушинский Л.А. (2000) Метод снятия отпечатков пальцев на хондроитин / дерматансульфат и гиалуронановые олигосахариды.Гликобиология 10: 393–401 [PubMed] [Google Scholar]
- Ли Й.Х., Ву Дж.Х., Чой С.Дж., Джи Дж.Д., Сон Г.Г. (2010) Влияние глюкозамина или хондроитинсульфата на прогрессирование остеоартрита: метаанализ. Ревматол Инт 30: 357–363 [PubMed] [Google Scholar]
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. (2000) Метаанализ хондроитинсульфата в лечении остеоартрита. J Ревматол 27: 205–211 [PubMed] [Google Scholar]
- Legendre F., Bauge C, Roche R., Saurel A.S., Pujol J.P. (2008) Хондроитинсульфатная модуляция матрикса и экспрессия воспалительных генов в IL-lbeta-стимулированных хондроцитах — исследование в культурах гипоксических альгинатных гранул. Остеоартроз Хрящ 16: 105–114 [PubMed] [Google Scholar]
- Малаваки С.Дж., Асимакопулу А.П., Ламари Ф.Н., Теохарис А.Д., Цанакакис Г.Н., Караманос Н.К. (2008) Капиллярный электрофорез для контроля качества хондроитинсульфатов в сырье и рецептурах. Анальный биохим 374: 213–220 [PubMed] [Google Scholar]
- Mazieres B., Хучер М., Заим М., Гарнеро П. (2007) Эффект хондроитинсульфата при симптоматическом остеоартрите коленного сустава: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. Энн Рум Дис 66: 639–645 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mazieres B., Hucher M.M.H., Zam M.M.Z. (2006) Хондроитинсульфат в лечении остеоартрита коленного сустава: рандомизированное двойное слепое многоцентровое плацебо-контролируемое исследование. Энн Рум Дис 65 (Дополнение II): 398. [Google Scholar]
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. (2000) Глюкозамин и хондроитин для лечения остеоартрита: систематическая оценка качества и метаанализ. JAMA 283: 1469–1475 [PubMed] [Google Scholar]
- Möller I., Pérez M., Monfort J., Benito P., Cuevas J., Perna C., et al. (2010) Эффективность хондроитинсульфата у пациентов с сопутствующим остеоартритом коленного сустава и псориазом: рандомизированное двойное слепое плацебо-контролируемое исследование. Остеоартроз Хрящ 18 (Приложение 1): 532–540 [PubMed] [Google Scholar]
- Monfort J., Martel-Pelletier J., Pelletier J.P. (2008a) Хондроитинсульфат при симптоматическом остеоартрите: критическая оценка метаанализов. Curr Med Res Opin 24: 1303–1308 [PubMed] [Google Scholar]
- Monfort J., Nacher M., Montell E., Vila J., Verges J., Benito P. (2005) Хондроитинсульфат и гиалуроновая кислота (500–730 кДа ) подавляют синтез стромелизина-1 в хондроцитах человека, страдающих остеоартритом. Наркотики Exp Clin Res 31: 71–76 [PubMed] [Google Scholar]
- Monfort J., Pelletier J.P., Garcia-Giralt N., Martel-Pelletier J. (2008b) Биохимические основы действия хондроитинсульфата на суставные ткани при остеоартрозе. Энн Рум Дис 67: 735–740 [PubMed] [Google Scholar]
- Mourao P.A. (1988) Распределение хондроитин-4-сульфата и хондроитин-6-сульфата в суставном и ростовом хряще человека. Ревматоидный артрит 31: 1028–1033 [PubMed] [Google Scholar]
- Omata T., Itokazu Y., Inoue N., Segawa Y. (2000) Эффекты хондроитинсульфата-C на разрушение суставного хряща при артрите, индуцированном мышиным коллагеном.Arzneimittelforschung 50: 148–153 [PubMed] [Google Scholar]
- Rainsford K.D. (2009) Важность фармацевтического состава и данных клинических испытаний и фармакологических исследований в определении эффективности хондроитинсульфата и других гликозаминогликанов: критический анализ. J Pharm Pharmacol 61: 1263–1270 [PubMed] [Google Scholar]
- Reichenbach S., Sterchi R., Scherer M., Trelle S., Burgi E., Burgi U., et al. (2007) Мета-анализ: хондроитин при остеоартрите коленного или тазобедренного суставов.Энн Интерн Мед 146: 580–590 [PubMed] [Google Scholar]
- Ричи Ф., Брюйер О., Этген О., Кучерат М., Хенротин Ю., Регинстер Дж. Я. (2003) Структурная и симптоматическая эффективность глюкозамина и хондроитина при остеоартрите коленного сустава: всесторонний метаанализ. Arch Intern Med 163: 1514–1522 [PubMed] [Google Scholar]
- Ronca F., Palmieri L., Panicucci P., Ronca G. (1998) Противовоспалительная активность хондроитинсульфата. Остеоартроз Хрящ 6 (Приложение A): 14–21 [PubMed] [Google Scholar]
- Sawitzke A.Д., Ши Х., Финко М.Ф., Данлоп Д.Д., Бингем С.О., III, Харрис К.Л. и др. (2008) Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Ревматоидный артрит 58: 3183–3191 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Шварц Н.Б., Дорфман А. (1975) Стимуляция продукции хондроитинсульфат-протеогликана хондроцитами в монослое. Подключите ткань Res 3: 115–122 [PubMed] [Google Scholar]
- Shinmei M., Мияучи С., Мачида А., Миядзаки К. (1992) Количественное определение хондроитин-4-сульфата и хондроитин-6-сульфата в патологической суставной жидкости. Ревматоидный артрит 35: 1304–1308 [PubMed] [Google Scholar]
- Тахири К., Корвин-Змиевска С., Ришетт П., Херо Ф., Шевалье Х., Савуре Дж. Ф. и др. (2008) Природные хондроитинсульфаты увеличивают агрегацию протеогликановых комплексов и снижают экспрессию ADAMTS-5 в хондроцитах, обработанных интерлейкином 1 бета. Энн Рум Дис 67: 696–702 [PubMed] [Google Scholar]
- Тат С.K., Pelletier J.P., Mineau F., Duval N., Martel-Pelletier J. (2010) Различные эффекты 3 различных соединений хондроитинсульфата на хрящ / хондроциты человека при остеоартрите: важность чистоты и производственного процесса. J Ревматол 37: 656–664 [PubMed] [Google Scholar]
- Tat S.K., Pelletier J.P., Verges J., Montell E., Lajeunesse D., Fahmi H., et al. (2007) Хондроитин и сульфат глюкозамина в комбинации снижают прорезорбтивные свойства субхондральных костных остеобластов человека.Артрит Res Ther 9: R117. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Uebelhart D., Thonar EJ, Zhang J., Williams JM (1998) Защитный эффект экзогенного хондроитин-4,6-сульфата при острой деградации суставного хряща у кролика . Остеоартроз Хрящ 6 (Suppl. A): 6–13 [PubMed] [Google Scholar]
- Валлиер М., дю Суич П. (2010) Модуляция воспаления с помощью хондроитинсульфата. Остеоартроз Хрящ 18 (Приложение 1): S1 – S6 [PubMed] [Google Scholar]
- Вангснесс К.Т., младший, Спайкер В., Эриксон Дж. (2009) Обзор доказательной медицины использования глюкозамина и хондроитинсульфата при остеоартрите коленного сустава. Артроскопия: J Arthroscopic Relat Surg 25: 86–94 [PubMed] [Google Scholar]
- Verbruggen G., Veys E.M. (1977) Влияние сульфатированных гликозаминогликанов на метаболизм протеогликанов в клетках синовиальной оболочки. Acta Rhumatol Belg 1: 75–92 [PubMed] [Google Scholar]
- Verges J., Montell E., Herrero M., Perna C, Cuevas J., Perez M., et al.(2005) Клиническое и гистопатологическое улучшение псориаза при пероральном приеме хондроитинсульфата: случайная находка. Дерматол Интернет J 11: 31. [PubMed] [Google Scholar]
- Vergés J., Montell E., Martinez G., Heroux L., du Souich P. (2004) Хондроитинсульфат снижает фактор ядерной транслокации NF-kappaB и не изменяет состояние активации активирующего белка-1 (AP-1). Остеоартроз Хрящ 12: 194, (Аннотация). [Google Scholar]
- Volpi N. (2002) Пероральная биодоступность хондроитинсульфата (Кондросульф) и его компонентов у здоровых добровольцев мужского пола.Остеоартроз Хрящ 10: 768–777 [PubMed] [Google Scholar]
- Volpi N. (2003) Пероральное всасывание и биодоступность хондроитинсульфата ихтикового происхождения у здоровых добровольцев мужского пола. Остеоартроз Хрящ 11: 433–441 [PubMed] [Google Scholar]
- Volpi N. (2006a) Достижения в анализе хондроитинсульфата: применение при физиологических и патологических состояниях соединительной ткани и при фармакологическом лечении остеоартрита. Curr Pharm Des 12: 639–658 [PubMed] [Google Scholar]
- Volpi N.(2006b) Хондроитинсульфат: структура, роль и фармакологическая активность, Elsevier: Amsterdam [Google Scholar]
- Volpi N. (2009) Качество различных препаратов хондроитинсульфата в зависимости от их терапевтической активности. J Pharm Pharmacol 61: 1271–1280 [PubMed] [Google Scholar]
- Volpi N., Tarugi P. (1999) Влияние плотности заряда хондроитинсульфата, положения сульфатной группы и молекулярной массы на Cu2 + -опосредованное окисление липопротеинов низкой плотности человека: действие нормального человеческого хондроитинсульфата плазмы.J Biochem 125: 297–304 [PubMed] [Google Scholar]
- Wang L., Wang J., Almqvist KF, Veys EM, Verbruggen G. (2002) Влияние полисульфатированных полисахаридов и гидрокортизона на метаболизм внеклеточного матрикса суставных хондроцитов человека в пробирка. Clin Exp Rheumatol 20: 669–676 [PubMed] [Google Scholar]
- Zhang W., Doherty M., Arden N., Bannwarth B., Bijlsma J., Gunther K.P., et al. (2005) Основанные на фактических данных рекомендации EULAR по лечению остеоартрита тазобедренного сустава: отчет рабочей группы Постоянного комитета EULAR по международным клиническим исследованиям, включая терапию (ESCISIT).Энн Рум Дис 64: 669–681 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Чжан В., Московиц Р. В., Нуки Г., Абрамсон С., Альтман Р. Д., Арден Н. и др. (2008) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, Часть II: Основанные на фактах, согласованные экспертные рекомендации OARSI. Остеоартроз Хрящ 16: 137–162 [PubMed] [Google Scholar]
- Чжан В., Нуки Г., Московиц Р. В., Абрамсон С., Альтман Р. Д., Арден Н. К. и др. (2010) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г.Остеоартроз Хрящ 18 (4): 476–499 [PubMed] [Google Scholar]
От исследований in vitro к клиническим рекомендациям
Ther Adv Musculoskelet Dis. 2010 Dec; 2 (6): 335–348.
Мариан Мати
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Кристель Санчес
2 Исследовательское отделение костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Cecile Lambert
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
2 Кости и Отделение исследования хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
1 Отделение исследования костей и хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия eb.ca.glu@nitornehyЭта статья цитируется другими статьями в PMC.Abstract
Хондроитинсульфат (CS) рекомендуется в качестве терапевтического вмешательства при мультимодальном подходе к лечению остеоартрита (OA). CS был тщательно изучен для описания его фармакологии (фармакокинетических эффектов, эффектов in vitro и in vivo) и клинической эффективности. Сообщалось о различных результатах в зависимости от системы оценки (модель, дозировка и продолжительность) и источника CS (происхождение и качество).Целью этого обзора было собрать большую часть доступной информации о CS и обсудить его эффективность в управлении OA.
Ключевые слова: хрящ, хондроитинсульфат, остеоартрит, механизм действия, фармакокинетика
Введение
Хондроитинсульфат (CS) является основным компонентом внеклеточного матрикса (ECM) многих соединительных тканей, включая хрящ, кость, кожу , связки и сухожилия. Остеоартрит (ОА) характеризуется прогрессирующими структурными и метаболическими изменениями в тканях суставов, в основном деградацией хряща, склерозом субхондральной кости и воспалением синовиальной оболочки.Лечение остеоартрита включает мультимодальное терапевтическое вмешательство, поскольку на сегодняшний день лечения не найдено. Для лечения ОА необходимы препараты, которые могут замедлить, остановить или даже избежать деградации суставов. Многие из рекомендуемых вмешательств представляют только эффекты, изменяющие симптомы, и несколько эффектов, изменяющих структуру.
CS и другие соединения, такие как глюкозамин, используются в медицинских целях более 40 лет. CS продается как безрецептурная пищевая добавка в Северной Америке и отпускается по рецепту в соответствии с правилами Европейского медицинского агентства (EMEA) в Европе.В последние десятилетия CS вызывал много интересов в качестве потенциального терапевтического средства против ОА. CS является частью рекомендаций Международного общества исследований остеоартрита (OARSI) по лечению остеоартрита коленного сустава [Zhang et al. 2010, 2008] и рекомендаций Европейской лиги против ревматизма (EULAR) по лечению тазобедренного и коленного суставов OA Zhzang et al. 2005; Jordan et al. 2003]. ХС и глюкозамин могут стать отличной альтернативой для пациентов с ОА.
CS, как естественный компонент ЕСМ, представляет собой сульфатированный гликозаминогликан (ГАГ), состоящий из длинной неразветвленной полисахаридной цепи с повторяющейся дисахаридной структурой N-ацетилга-лактозамина и глюкуроновой кислоты.Большинство остатков N-ацетилгалактозамина () сульфатированы, особенно в положениях 4 и 6, что делает CS сильно заряженным полианионом. CS отвечает за многие важные биомеханические свойства хряща, такие как сопротивление и эластичность. Его высокое содержание в аггрекане играет важную роль в обеспечении устойчивости хряща к давлению при различных условиях нагрузки. Профиль сульфатации хондроитина был описан в хрящах [Mourao, 1988]. Изменения в структуре CS описаны в тканях OA [Caterson et al. 1990] и пониженное соотношение CS-6: CS-4 были обнаружены в синовиальной жидкости и хрящах пациентов с ОА [Shinmei et al. 1992]. Более трех десятилетий назад было предложено [Schwartz and Dorfman, 1975], что поставка CS в качестве терапевтического вмешательства при повреждении хряща может обеспечить строительные блоки для синтеза нового компонента матрикса, поскольку повышение концентрации CS может действовать в пользу матрикса. регенерация и учитывать ее благотворное влияние.
Химическая структура хондроитинсульфата, где R — Na или H, а X — SO 3 R или H.
Однако с тех пор механизм действия CS как терапевтического вмешательства все еще требует выяснения, а его эффективность остается предметом дискуссий.
Общая цель этого обзора состояла в том, чтобы собрать большую часть доступной информации о CS, его фармакокинетике, его эффектах in vitro, и in vivo, и его клинической эффективности. Цель этого обзора — обсудить клиническую полезность CS и перспективы использования CS при лечении остеоартрита.
Фармакокинетика
Natural CS имеет молекулярную массу 50–100 кДа.После процесса экстракции молекулярная масса составляет 10-40 кДа в зависимости от сырья. CS в основном получают из бычьего, свиного или морского (акульего) хряща.
CS чаще всего вводят перорально в дозах от 800 до 1200 мг / день. CS быстро всасывается в желудочно-кишечном тракте. Поглощенный CS достигает компартмента крови в виде 10% CS и 90% деполимеризованных низкомолекулярных производных.
Сообщалось о различной биодоступности и фармакокинетических переменных в зависимости от характеристик и происхождения CS [Malavaki et al. 2008]. О некоторых из них сообщили в. Биодоступность CS обсуждается. Данные зависят от системы, используемой для оценки, структуры и характеристик CS, таких как молекулярная масса, плотность заряда и кластер дисульфатированных дисахаридов, используемой концентрации и вида животных, использованных для проведения исследования [Volpi, 2003]. В большинстве исследований использовался CS из трахеи крупного рогатого скота (чистота 95%), который представляет собой тот же материал, который использовался в клинических испытаниях [Barnhill et al. 2006].
Таблица 1.
Различные фармакокинетические параметры в зависимости от системы исследования и источника CS.
| Исследование | Источник хондроитина | Система | Результаты | |
|---|---|---|---|---|
| Conte et al. [1995] | Трахея крупного рогатого скота 16 мг / кг перорально | Крысы Wistar | ||
| Трахея крупного рогатого скота 16 мг / кг перорально | Молодые собаки породы бигль | |||
| Трахея крупного рогатого скота Разовая доза 0.8 г или две дозы по 0,4 г | Здоровые добровольцы ( N = 12; 6 мужчин и 6 женщин) | Разовая доза: | Две дозы: | |
| Трахея крупного рогатого скота Разовая доза 0,8 г / день | Пациенты с ОА ( N = 18) | Концентрация в плазме:
| ||
| Ronca . [1998] | Смесь CS-6 и CS-4 (1: 1) Пероральное введение 16 мг / кг (4 мг / крыса) | Крысы ( N = 10) |
| |
| Volpi [2002] | Хондросульф® однократная доза (4 г) | Мужчина здоровый волонтеры ( N = 20) | ||
| Volpi [2003] | Shark CS Однократная доза (4 г) | Здоровые добровольцы мужского пола ( N = 20) |
Биодоступность CS после перорального приема колеблется от 10% до 20% [Lauder, 2009].
Поглощение CS может зависеть от статуса сульфатации. Положение и процентное содержание сульфатных групп обычно варьируется в зависимости от конкретных источников животного происхождения [Volpi, 2006a, 2006b]. Действительно, десульфатированный хондроитин у мышей [Kusano et al. 2007] имеет очень быстрое поглощение, с пиком в течение 15 минут и очень быстрым возвращением к исходному уровню через 3 часа, тогда как CS у акул у здоровых добровольцев мужского пола поглощается медленнее (пик через 8,7 часа) и медленнее выведение (уровни поддерживаются). до 16 часов после администрирования) [Volpi, 2003].CS из трахеи крупного рогатого скота демонстрирует быстрое увеличение плазмы здоровых добровольцев мужского пола с пиком в пределах 1–5 часов после введения и возвращением к исходному уровню через 10 часов [Volpi, 2002].
Фармакокинетические параметры CS, определенные у здоровых добровольцев мужского пола [Volpi, 2002], после перорального приема показали значительное увеличение уровней CS в плазме (более чем на 200%) по сравнению с уровнями перед дозой в течение 24 часов. Пиковые концентрации наблюдались через 2 часа после дозирования, и увеличение значимо через 2-6 часов после дозирования.Кинетика первого порядка наблюдалась для доз до 3000 мг. Многократные дозы 800 мг для пациентов с ОА не изменяют кинетику CS. Недавно, используя флуорофорный углеводный электрофорез и хроматографию наложения 6, Джексон и его коллеги не наблюдали никаких изменений эндогенной концентрации (20 (мкг / мл) и состава дисахаридов CS после перорального приема однократной дозы 1200 мг CS. Одно объяснение может быть, что небольшое количество проглоченного CS достигает циркуляции в неизмененной форме или состоит из дисахаридов более крупных фрагментов [Jackson et al. 2010]; в качестве альтернативы, могло случиться так, что анализ был недостаточно чувствителен для обнаружения более низких концентраций. Это еще предстоит продемонстрировать другими методами анализа. Другой характеристикой CS является его способность накапливаться в суставных тканях. Высокое содержание меченого CS было обнаружено в тканях суставов, включая синовиальную жидкость и хрящ, после перорального введения людям [Ronca et al. 1998].
Трудно оценить релевантность максимальной концентрации, достигнутой в компартменте крови (Cmax) для этого типа лекарственного средства, поскольку in vivo ответ может быть результатом воздействия CS и дисахаридов.Более того, CS — это препарат замедленного действия, в результате чего действие начинается медленно, а максимальный эффект достигается через несколько месяцев. Кроме того, CS — это лекарство биологического происхождения, что означает, что его измерение в биологических жидкостях не позволяет отличить лекарство от эндогенных молекул. Максимальный эффект (Emax) был предсказан с использованием альтернативного метода [du Souich and Verges, 2001]. Эффект Emax рассчитывали на основании клинической эффективности. Было подсчитано, что 50% Emax достигается за 35 дней у пациентов с легким ОА.Примерный период полураспада CS и его производных в плазме крови человека составляет 15 часов. Стабильное состояние достигается через 3–4 дня, и для получения максимального эффекта может потребоваться 3–6 месяцев лечения.
CS не метаболизируется цитохромом P450. Это говорит в пользу очень низкого риска взаимодействия с другими лекарствами.
Наконец, для CS был описан эффект переноса. Действительно, после отсроченного начала действия максимальный эффект сохраняется после прекращения терапии.
Механизм действия
Многие эффекты были описаны для CS в различных исследованиях in vitro, и in vivo, с использованием различных типов и концентраций CS и различных моделей.Точный механизм действия еще предстоит уточнить. In vitro эффекты на суставные клетки и эффекты in vivo на моделях артрита описаны в и, соответственно.
Таблица 2.
In vitro эффекты хондроитинсульфата.
| Исследование | Хондроитин | Система и продолжительность | Результаты | ||||
|---|---|---|---|---|---|---|---|
| Verbruggen et al. [1977] | 10–400 мкг / мл | Однослойные синовиальные клетки | Стимуляция 11% синтеза гиалуроната во время фазы роста | ||||
| Увеличение на 88% во время стационарной фазы | |||||||
| Bassleer et al. [1998] | КРС 100–1000 мкг / мл | Суставные хондроциты человека в кластерах, стимулированные IL-1β До 32 дней | Значительное снижение продукции PGE, стимулированной IL-1β 2 | ||||
| Увеличение выработки коллагена PG и типа II | |||||||
| Wang et al. [2002] | C poly S 10 мкг / мл | Человеческие суставные хондроциты в агарозном геле, стимулированные IL-1β 1 неделя | Стимуляция аггрекана, гиалуронана и коллагена типа II из-за подавления ММП | ||||
| Campo et al. al. [2004] | CS-4 1,0 и 2,0 мг / мл | Фибробласт кожи человека | Антиоксидантное действие CS-4 за счет повышения жизнеспособности клеток и ингибирования фрагментации ДНК | ||||
| Chan et al. [2005a] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Снижение IL-1β-индуцированной MMP-13 | ||||
| Chan et al. [2005b] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Подавление индуцированной IL-1β экспрессии NO-синтазы, COX-2 и mPGES-1 | ||||
| Монфорт и др. [2005] | 10–1000 мкг / мл | Хондроциты ОА человека, стимулированные IL-1β 48 ч | Ингибирование MMP-3 | ||||
| Holzmann et al. [2006] | 25 мкг / мл | Человеческие суставные хондроциты, стимулированные LPS До 72 часов | Ингибирование MMP-13 за счет снижения активации p38 и Erk1 / 2 | ||||
| Tat et al. [2007] | 200 мкг / мл | Остеобласты субхондральной кости человека ОА До 48 ч | Снижение прорезорбтивных агентов | ||||
| Обратное действие витамина D3 на соотношение OPG: RANK9584 | Tahiri et al. [2008] | Хондросульф® или свинья 10 или 100 мкг / мл | Хондроциты суставов кролика, стимулированные IL-1β 20 ч | Повышение синтеза PG | |||
| Ингибирование экспрессии AD10AMTS-5 | |||||||
| Jomphe et al. [2008] | Очищенные бычьи CS-4 и CS-6 200 мг / мл | Хондроциты кролика, стимулированные IL-1β 48 ч | Снижение ядерной транслокации NF-κB | ||||
| Профилактика активации Erk1 / 2 и p38 | |||||||
| Снижение апоптоза, индуцированного нитропруссидом | |||||||
| Legendre et al. [2008] | Avian CS −100 мкг / мл | Бычьи суставные хондроциты в гипоксических альгинатных гранулах 24–48 часов | Снижение IL-1β-индуцированных MMP-1, −3, −13 и ADAMTS-4 и — 5 | ||||
| Снижение IL-1β-индуцированного COX-2 и iNOS | |||||||
| Снижение продукции PGE 2 , но не NO | Незначительное увеличение синтеза ГАГ | ||||||
| Противодействие подавлению IL-1β рецепторов TGFβ | |||||||
| Katta et al. [2009] | Смесь CS A, CS B и CS C 10–50 мг / мл | Эксплантаты бычьего хряща 24 ч | Эффективная смазка для суставов | ||||
| Распространение в хрящ | |||||||
| Давид-Рауди et al. [2009] | Avian CS 100 мкг / мл | OA фибробластоподобные синвиоциты человека 48 часов с предварительной обработкой | Регулирование гиалуронансинтазы | ||||
| Campo et al. [2009a] | CS-4 крупного рогатого скота и CS-6 акулы 0,5 и 1,0 мг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Антиапоптотический эффект обоих CS | ||||
| Ингибирование медиаторов воспаления, iNOS и MMP более очевидно с CS-4, чем с CS-6 | |||||||
| Campo et al. [2009b] | CS-4 крупного рогатого скота и CS-6 акулы 25 и 50 мкг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Ингибирование воспалительных цитокинов (MyD88 и TRAF-6), ингибирование активации NF -kB и iNOS обоими CS | ||||
| Эффект через TLR4 (подтвержден экспериментом со специфическими антителами) | |||||||
| Bian et al. [2009] | CS-6 и CS-4 акульего происхождения 10–100 мг / мл | Эксплантаты бычьего хряща 4 недели | Снижение содержания ГАГ | ||||
| Imada et al. [2010] | Акула (в основном CS-6) и свинья (в основном CS-4) 1–100 мкг / мл | Суставные хондроциты человека в альгинатных шариках и синовиальный фибробласт, стимулированные IL-1β 6 или 4 дня | Разные эффект обеих CS | ||||
| Подавление индуцированных IL-1b ADAMTS-4 и -5 в обоих типах клеток | |||||||
| Подавление индуцированных IL-1β MMP- 13 и увеличить экспрессию аггрекана в хондроцитах | |||||||
| Восстановление TIMP-3 в хондроцитах и TIMP-1 в синовиоцитах CS свиньи |
Таблица 3.
In vivo эффекты хондроитинсульфата.
| Исследование | Хондроитин | Модель | Результаты |
|---|---|---|---|
| Uebelhart et al. [1998] | 80 мг / день перорально или i. м. | Кроличья модель повреждения хряща, вызванного химопапаином | Значительное увеличение продукции PG |
| Omata et al. [2000] | 1000 мг / кг | Коллаген-индуцированный артрит у мышей | Снижение параметров синовита: клеточная инфильтрация, фиброз и пролиферация выстилающих клеток |
| Campo et al. [2003] | 1 мл / кг (внутрибрюшинно) | Коллаген-индуцированный артрит у крыс | Лечение начинали после начала артрита (день 10) |
| Защита от окислительного стресса | |||
| 25 мг / кг (перорально) | Снижение уровней TNF-α и миелопероксидазы в плазме | ||
| Cho et al. [2004] | 1200 мг / кг | Коллаген-индуцированный артрит у крыс | Снижение уровней IL-6 |
| Caraglia et al. [2005] | 0,3 мг / день | Спонтанный ОА у мышей 12 дней | Значительное уменьшение апоптозных хондроцитов через 30 дней |
| Chou et al. [2005] | Пищевая добавка (18 мг / г) | Адъювант-индуцированный артрит Фрейнда у крыс | Предотвращение увеличения MMP-9 Снижение уровня IL-1β в тканях суставов, но не в сыворотке |
| Campo et al. al. [2008] | CS-4 (трахея крупного рогатого скота) 30–120 мг / кг (т.е.p.) | Коллаген-индуцированный артрит у мышей В течение 25 дней | Ингибирование активации NF-κB Ингибирование MMP-13 ингибирование активации каспаз-3 и -7 |
Противовоспалительный эффект
CS. сообщалось, что он обладает противовоспалительным действием. Было показано, что он ингибирует in vitro синтез различных промежуточных продуктов воспаления, таких как синтаза оксида азота (NO), циклооксигеназа (COX) -2, микросомальная простагландин-синтаза (mPGES) -1 и простагландин (PG) E 2 [Campo и другие. 2009a; Legendre et al. 2008; Чан и др. 2005b; Bassleer et al. 1998]. Также было показано, что CS может действовать на toll-подобный рецептор (TLR) -4, ингибируя воспалительные цитокины, MyD88 и фактор, связанный с рецептором фактора некроза опухоли (TNF) (TRAF) -6, посредством ингибирования ядерного фактора (NF ) -kB активация [Campo et al. 2009b].
Противовоспалительный эффект CS был также продемонстрирован in vivo. Было показано, что CS снижает синовит при коллаген-индуцированном артрите у мышей [Omata et al. 2000]. Он также был способен снижать провоспалительный цитокин, интерлейкин (IL) -6, в той же модели [Cho et al. 2004]. CS также снижает уровень IL-1b в суставной ткани при адъювантном артрите Фрейнда при введении в качестве пищевой добавки [Chou et al. 2005] и TNF-α и миелопероксидаза в плазме крови крыс с коллаген-индуцированным артритом и после перорального введения [Campo et al. 2003].
Антикатаболические и анаболические эффекты
Первый анаболический эффект CS был описан более 30 лет назад.CS увеличивал синтез гиалуроната в синовиальных клетках [Verbruggen and Veys, 1977]. С тех пор было также продемонстрировано увеличение синтеза коллагена типа II и протеогликана (PG) в хондроцитах человека [Wang et al. 2002; Bassleer et al. 1998] и ГАГ в хондроцитах крупного рогатого скота [Legendre et al. 2008]. Этот эффект также может быть вторичным по отношению к подавлению регуляции матриксной металлопротеиназы (ММП) [Wang et al. 2002]. Было также показано, что CS ингибирует MMP-1, -3 и -13, а также ADAMTS-4 и -5 (аггреканазы) в хондроцитах человека, свиньи и крупного рогатого скота [Imada et al. 2010; Legendre et al. 2008; Tahiri et al. 2008; Чан и др. 2005a; Монфорт и др. 2005]. Ингибирование MMP-13 может происходить через ингибирование активации p38 и Erk1 / 2 [Holzmann et al. 2006]. Для CS-4 и CS-6 были продемонстрированы различные ингибирующие способности против ММП в хондроцитах мышей [Campo et al. 2009a]. Различия между CS-6 и CS-4 недавно были также показаны на человеческих клетках. Действительно, CS-6 (акульего происхождения) может противодействовать ингибированию IL-1b тканевым ингибитором металлопротеаз (TIMP) -3 в хондроцитах человека и TIMP-1 в синовиальных фибробластах, тогда как CS-4 (происхождение из трахеи свиньи) не дает того же эффект [Imada et al. 2010]. CS может активировать гиалуронансинтазу в фибробластоподобных клетках [David-Raoudi et al. 2009] и может быть эффективным в качестве смазки для суставов, как было показано на эксплантатах бычьего хряща [Katta et al. 2009]. Также сообщалось, что CS может влиять на процесс резорбции, происходящий в субхондральной кости во время ОА. CS действительно может увеличивать соотношение остеопротегерин (OPG): активатор рецептора для лиганда NF-κB (RANKL) в остеобластах OA в пользу гомеостаза субхондральной кости [Tat et al. 2007]. Было продемонстрировано, что CS действует на большинство суставных тканей, участвующих в патофизиологии ОА. Наконец, недавнее исследование in vitro на эксплантатах бычьего хряща, обработанных CS-4 и CS-6 в течение 4 недель, выявило отрицательный эффект CS, показывающий, что он снижает содержание GAG [Bian et al. 2009]. Важно отметить, что это исследование было проведено с самой высокой концентрацией CS из когда-либо протестированных (10–100 мг / мл).
Анаболический и антикатаболический эффект CS также был продемонстрирован in vivo. CS может увеличивать продукцию PG на кроличьей модели деградации хряща [Uebelhart et al. 1998], предотвращают повышение уровня ММР-9 при адъювантном артрите Фрейнда у крыс при введении в качестве пищевой добавки [Chou et al. 2005] или ингибируют ММР-13 при коллаген-индуцированном артрите у мышей [Campo et al. 2008].
Антиапоптотический эффект
CS продемонстрировал антиапоптотические свойства как in vitro, так и in vivo. Было показано, что CS (200 (мкг / мл) снижает чувствительность хондроцитов кролика к апоптозу [Jomphe et al. 2008]. Этот эффект был связан с уменьшением транслокации NF-κB и со снижением пути передачи сигналов киназы MAP через p38 и Erk1 / 2. Другое исследование указало на антиапоптотический эффект CS-4 и CS-6 в суставных хондроцитах мыши [Campo et al. 2009a]. In vivo, на мышиной модели спонтанного ОА было показано, что 12-дневное лечение CS (0,3 мг / день) снижает количество апоптозных хондроцитов при оценке через 30 дней [Caraglia et al. 2005]. Также было продемонстрировано, что он способен ингибировать активацию каспазы-3 и -7 при коллаген-индуцированном артрите у мышей [Campo et al. 2008]. Эти результаты свидетельствуют в пользу хондропротекторного действия CS.
Антиоксидантный эффект
Антиоксидантные эффекты были рассмотрены [Campo et al. 2006a, 2006b]. Было показано, что CS обладает антиоксидантными свойствами in vitro в фибробластах кожи человека [Campo et al. 2004] и in vivo при коллаген-индуцированном артрите у крыс [Campo et al. 2003]. CS обеспечивает защиту от перекиси водорода и супероксид-анионов. Действительно, эти исследования продемонстрировали, что он может ограничивать гибель клеток, уменьшать фрагментацию ДНК и окисление белков, уменьшать образование свободных радикалов и действовать как поглотитель свободных радикалов. Он снижает перекисное окисление липидов и улучшает антиоксидантную защиту за счет восстановления эндогенных антиоксидантов, восстановленного глутатиона (GSH) и супероксиддисмутазы (SOD).
Регуляция клеточного сигнального пути
CS, как было обнаружено, действует на основные клеточные сигнальные пути.Было показано, что он ингибирует активацию пути киназы MAP, p38 и Erk ½, а также ингибирование трансактивации NF-κB в хондроцитах кролика [Jomphe et al. 2008; Verge’s et al. 2004]. Было также показано, что CS действует на другие промежуточные продукты клеточной передачи сигналов [Egea et al. 2010]. CS был способен индуцировать путь протеинкиназы C (PKC) / PI3K / Akt в клетках нейробластомы. Многие эффекты, описанные для CS на патофизиологию ОА, могут быть связаны с его действием на передачу сигналов в клетках.
Важно помнить, что большинство эффектов in vitro было получено с использованием высоких концентраций CS, которые не соответствуют ожидаемым концентрациям в плазме. Более того, учитывая медленное действие препарата на человека, системы in vitro и in vivo использовались в течение довольно короткого времени. Различные авторы предположили, что высокая концентрация, используемая in vitro, использовалась для компенсации этих проблем [Tat et al. 2010; Монфорт и др. 2008b]. Различия в чистоте и свойствах CS могут быть причиной несоответствия эффектов. Это было недавно рассмотрено в двух всеобъемлющих обзорах [Rainsford, 2009; Вольпи, 2009]. Это было подтверждено даже в суставных хондроцитах [Tat et al. 2010], когда три разных типа CS были протестированы в одной и той же системе и оказали различное воздействие на ключевые медиаторы OA. Это исследование продемонстрировало, что ХС бычьего происхождения гораздо эффективнее ингибирует катаболические медиаторы, чем ХС свиного происхождения.Также важно отметить, что эффекты CS in vivo в основном наблюдались на животных моделях артрита. Только одно исследование было проведено на модели спонтанного ОА [Caraglia et al. 2005].
Точный механизм действия CS еще предстоит выяснить. Взятые вместе, эти данные предполагают вмешательство CS на разных уровнях патофизиологии ОА, как показано в.
Схематическое изображение мишеней хондроитинсульфата (CS) в хондроцитах во время остеоартрита, как было предложено исследованиями in vitro: CS действует на сигнальные пути клеток, воспалительные и катаболические пути и на окислительный стресс (как показано черными стрелками).CS нацелен на различные промежуточные соединения в этих путях (как показано серыми стрелками). CS, хондроитинсульфат; ИЛ, интерлейкин; ECM, внеклеточный матрикс; ПГЕ 2 , простагландин E 2 ; PG, протеогликан; ММП, матриксная металлопротеиназа; NO, оксид азота; ADAMTS, дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами; NF-κB, ядерный фактор kB; ЦОГ, циклоосигеназа, iNOS, индуцируемая синтаза оксида азота.
Клинический эффект хондроитинсульфата
Терапевтическая эффективность CS изучалась и сообщалась в различных клинических исследованиях у пациентов с ОА.Влияние CS на пациентов с ОА оценивалось либо по симптомам ОА (боль и функция), чтобы определить его симптоматическое лекарство замедленного действия для эффекта ОА (SYSADOA), либо по модификации заболевания (эффект структуры, сужение суставной щели (JSN)) для определения его модифицирующий болезнь эффект препарата ОА (DMOAD).
Симптоматическое лекарство замедленного действия для лечения ОА
Различные мета-анализы [Reichenbach et al. 2007; Richy et al. 2003; Leeb et al. 2000; McAlindon et al. 2000] сообщили о различной величине эффекта (ES) на боль и функцию CS в диапазоне от 0,9 до всего 0,3.
Недавно были разработаны и опубликованы три исследования, посвященных влиянию CS на SYSADOA, то есть исследование GAIT [Hochberg and Clegg, 2008; Clegg et al. 2006], исследование STOPP [Kahan et al. 2009] и еще одно рандомизированное контролируемое исследование (РКИ) [Mazieres et al. 2007; Mazieres et al. 2006] (). Совсем недавно рекомендации Международного общества исследований остеоартрита (OARSI) по лечению ОА определили умеренный или большой ES (0.75, 95% ДИ 0,50–0,99) [Zhang et al. 2010], но подчеркнул систематическую ошибку публикации, неоднородность результатов и кумулятивное снижение ES (1,85, 95% ДИ 1,47–2,22, в 1992 г. до 0,75, 95% ДИ 0,50–1,01, в 2006 г.).
Таблица 4.
| Исследование | Результат | Вмешательство | Население и продолжительность | Размер результата / эффекта | |||||
|---|---|---|---|---|---|---|---|---|---|
| Глобальная оценка | 900 Maziéres et al. [2007] | Глобальная оценка исследователями клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 3,1 (CS) и 2,5 (Плацебо), p = 0,044 Благоприятствует CS | ||||
| Общая оценка пациентом клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец обработки) | NS | ||||||
| Качество жизни | |||||||||
| Maziéres et al. [2007] | Физический компонент SF-12 (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 5,8 (CS) и 3,8 (плацебо), p = 0,021 Благоприятствует CS | |||||
| SF-12 Психический компонент | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Pain | |||||||||
| Clegg et al. [2006] | Боль | CS против плацебо | РКИ, N = 1583, 24 недели | CS не лучше, чем плацебо | |||||
| Maziéres et al. [2007] | Боль во время активности, ВАШ (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | −41% (CS ) и -32% (плацебо), p = 0,029 Поддерживает CS | |||||
| Боль в покое, ВАШ (изменение от исходного уровня) | CS vs. плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Reichenbach et al. [2007] | Исходы, связанные с болью | CS по сравнению с плацебо / без лечения | MA, 20 РКИ, n = 3846, ОА коленного или тазобедренного сустава, продолжительность испытаний от 6 до 132 недель | Значительная неоднородность | |||||
| Kahan et al. [2009] | Подшкала VAS и WOMAC | CS vs. плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Значительно более быстрое уменьшение боли в целевом колене с помощью CS | |||||
| Функция | |||||||||
| Clegg et al. [2006] | Припухлость сустава, выпот или и то, и другое при клиническом обследовании | CS по сравнению с плацебо | РКИ, N = 1583, 24 недели | CS значительно лучше | |||||
| Maziéres et al. [2007] | Индекс Лекена (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | |||||
| Изменение структуры | |||||||||
| Reichenbach et al. [2007] | Минимум JSW | CS по сравнению с плацебо / без лечения | MA, 5 РКИ, N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | ES средняя разница 0 .16 мм, 95% ДИ 0,08–0,24 | |||||
| Благоприятствует хондроитину | |||||||||
| Среднее значение JSW | CS по сравнению с плацебо / без лечения | MA, 5 N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследования от 6 до 132 недель | ES средняя разница 0,23, 95% ДИ 0,09–0,37 | ||||||
| Поддерживает хондроитин | |||||||||
| Кахан и другие. [2009] | Минимальный JSW | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Повышение эффекта лечения со временем | |||||
| CS значительно лучше для JSW | |||||||||
| Lee et al. [2010] | Минимальный JSN | CS по сравнению с плацебо | MA, 4 РКИ, N = 1088, ОА коленного сустава, период наблюдения от 1 до 2 лет | Небольшой, но значительный защитный эффект CS через 2 лет на минимуме JSN | |||||
| Hochberg [2010] | Минимум JSW | MA, 3 РКИ, N = 1179, Коленный остеоартрит, последующее наблюдение 2 года | Значительное снижение скорости уменьшения суставной щели ширина с CS | ||||||
| ES 0.23 (95% ДИ 0,11–0,35) | |||||||||
| Неблагоприятные события | |||||||||
| Maziéres et al. [2007] | Количество пациентов по крайней мере с одним НЯ, связанным с лечением | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | NS | |||||
| Всего количество НЯ | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | N = 18 (CS) и N = 20 (плацебо) NS | ||||||
| Reichenbach et al. [2007] | Пациенты с НЯ | CS по сравнению с плацебо / без лечения | MA, 12 РКИ, N = 1929, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | |||||
| Исключение из-за НЯ | Хондроитин по сравнению с плацебо / отсутствие лечения | МА, 9 РКИ, N = 1781, ОА коленного и тазобедренного суставов, диапазон продолжительности исследований от 6 до 132 недель | NS | ||||||
| Пациенты с тяжелыми НЯ | Хондроитин vs. плацебо / без лечения | MA, 2 РКИ, N = 217, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | ||||||
| Kahan et al. [2009] | Исключение из-за НЯ | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | NS |
Сообщалось о глобальных клинических испытаниях a благотворное влияние CS на боль и функцию (). Однако в самом крупном исследовании GAIT не сообщалось о влиянии на эти конечные точки.
Эффекты модификации структуры
Эффекты модификации структуры CS были описаны и проанализированы в двух недавних метаанализах [Hochberg, 2010; Ли и др. 2010]. Ранее сообщалось, что не было неоднородности в результатах РКИ по эффектам модификации структуры [Hochberg et al. 2008]. Результаты показали небольшое, но значительное снижение ухудшения JSN (ES = 0,26, 95% ДИ 0,16–0,36). Недавно при наблюдении за пациентами в течение 2 лет было выявлено значительное влияние CS на JSN у пациентов, получавших CS, по сравнению с плацебо [Kahan et al. 2009].
Безопасность и переносимость
В большинстве клинических испытаний сообщалось о прекрасном профиле безопасности и хорошей переносимости CS. Частота побочных эффектов и частота отказов были эквивалентны в группах CS и плацебо. При применении CS не наблюдалось серьезных серьезных побочных эффектов. Спасательные препараты (парацетамол или нестероидные противовоспалительные препараты [НПВП]) разрешены во время клинических испытаний. Этот факт может уменьшить разницу между группами CS и плацебо [Monfort et al. 2008a] ().
Хондроитинсульфат в рекомендациях
CS рекомендован в руководствах, опубликованных OARSI и Европейской лигой против ревматизма (EULAR) для лечения ОА коленного сустава [Zhang et al. 2008; Jordan et al. 2003]. OARSI рекомендует CS из-за его симптоматического и структурно-модифицирующего эффекта при ОА коленного сустава, но также рекомендует прекратить его через 6 месяцев, если симптоматическая реакция отсутствует. Что касается ОА бедра и кисти, EULAR рекомендует SYSADOA, включая CS, из-за их симптоматических эффектов и низкой токсичности, но подчеркивает тот факт, что ES небольшие, подходящие пациенты не определены должным образом, а клинически значимая модификация структуры и фармакоэкономический аспект не очень хорошо установлено.
Обсуждение
CS используется уже несколько десятилетий, и было важно описать его фармакокинетику, механизм действия и описать его клиническую эффективность.
CS обладает различными эффектами, от противовоспалительных и антикатаболических до антиапоптотических, а также антиоксидантных свойств. Все эти результаты были получены в разных системах с разными дозировками. Во многих обзорах говорится о важности источника CS и чистоты [Lauder, 2009; Рейнсфорд, 2009 г .; Вольпи, 2009; Лаудер и др. 2000]. Кроме того, сульфатированный CS в разных положениях (например, 4 или 6) может иметь разные эффекты. Например, CS-4 более эффективен как антиоксидант, чем CS-6 [Albertini et al. 2000; Volpi, Tarugi, 1999]. Исследования in vitro и in vivo имеют ограничения, в основном из-за используемой концентрации и продолжительности исследования. CS используется в концентрациях, которые значительно превосходят плазменную концентрацию после перорального введения терапевтической дозы CS. Действительно, CS достиг концентрации в плазме примерно 2.0 мкг / мл у пациентов с ОА после перорального введения 0,8 г CS [Conte et al. 1995]. Это исследование также показало, что CS может достигать 2,7 мг / мл в синовиальной жидкости пациентов с ОА. Другой эксперимент на крысах после перорального введения (16 мг / кг) показал концентрацию 3,3 мг / г в хрящах [Ronca et al. 1998]. В большинстве исследований in vitro использовалось от 10 мг / мл CS до 1000 мг / мл (см.). При интерпретации данных необходимо учитывать условия исследования. Наконец, недавно был проведен обзор эффективности КС при воспалительных состояниях, отличных от ОА, и в основном более тяжелых, чем ОА [Vallières and du Souich, 2010; du Souich et al. 2009]. Было показано, что CS эффективен при патологии, включая псориаз [Möller et al. 2010; Verges et al. 2005]. Это предполагает сильную противовоспалительную активность CS. К сожалению, отсутствие inivo демонстрации влияния CS на прогрессирование ОА. Только в одном исследовании изучалось влияние хондроитина на модель ОА. Для лучшего понимания клинической эффективности CS необходимы дальнейшие исследования, изучающие влияние CS на деградацию хряща, ремоделирование субхондральной кости и воспаление синовиальной оболочки.
CS рекомендуется OARSI в качестве вмешательства SYSADOA для лечения ОА [Zhang et al. 2010, 2008] и EULAR [Jordan et al. 2003]. Обе организации признали его симптоматические и структурно-модифицирующие эффекты. OARSI рекомендует прекратить лечение через 6 месяцев при отсутствии эффективности [Zhang et al. 2008]. В то время, когда EULAR опубликовал свои рекомендации, они предложили растущие доказательства эффективности CS. Однако ко времени последнего обновления OARSI [Zhang et al. 2010], ES снизился, что свидетельствует о нестабильности эффективности, что, по крайней мере частично, может быть связано с повышением качества исследований. Несоответствие эффективности, показанное в нескольких клинических испытаниях, имеет большое значение. Этот метаанализ [Zhang et al. 2010] также продемонстрировал серьезную предвзятость публикации. Эти наблюдения также сделаны для других соединений класса SYSADOA, включая сульфат глюкозамина (GS). Напротив, ES для ацетаминофена, хотя и очень маленький, по-видимому, со временем стабилизировался, что позволяет предположить, что дальнейших РКИ для проверки его анальгетической эффективности не требовалось.В целом, этот обзор указывает на то, что существует потребность в клинических испытаниях хорошего качества с продолжительностью и количеством пациентов, соответствующих этому виду соединений. Также уместно сравнить ES для боли основных фармакологических методов, обычно используемых при лечении ОА. Для сравнения, ЭС CS — одна из самых важных. Например, болевой синдром ES (2010 г.) для ацетаминофена составил 0,14 (95% 0,05–0,23), для НПВП 0,29 (95% 0,22–0,35) и для CS 0,75 (95% 0,50–1,01). Это говорит о клинической значимости использования CS для лечения ОА, учитывая его низкую токсичность. ОА является долгосрочным прогрессирующим заболеванием, для которого перед применением каждого лечения должна быть проведена оценка соотношения риск / польза.
В некоторых исследованиях оценивалась эффективность использования CS в сочетании с GS. Это было сделано in vitro [Chan et al. 2006, 2007, 2005a, 2005b], а также в клинических испытаниях [Vangsness et al. 2009; Sawitzke et al. 2008; Clegg et al. 2006, 2005]. Синергетический эффект обоих соединений еще предстоит продемонстрировать, но многие авторы рекомендуют использовать комбинацию.
Одна из причин для оптимизма в отношении использования CS отдельно или в сочетании со связанным продуктом, таким как GS, — это профиль безопасности.CS не взаимодействует с другими лекарствами и не вызывает серьезных побочных эффектов. Это говорит в пользу положительного соотношения риск / польза.
Заключение
Несмотря на умеренное влияние CS на боль и функцию, CS представляет собой интересный продукт для лечения ОА коленного сустава. Клинические данные свидетельствуют в пользу медленного действия на симптомы умеренного ОА коленного сустава. CS рекомендуется по самым популярным рекомендациям. Его профиль безопасности, несомненно, является одним из основных преимуществ при лечении стареющих пациентов с некоторыми сопутствующими заболеваниями.Таким образом, нет никаких ограничений для его использования у пациентов с ОА, если не учитывать экономический эффект. Тем не менее, следует проявлять осторожность в отношении типа и состава CS. Конечно, остаются вопросы относительно механизма его действия. Эффект CS на воспаление субхондральной кости и синовиальной оболочки может быть лучше документирован.
Благодарности
Авторы благодарят L. Montell Bonaventura и J. Verges из Bioiberica, любезно предоставившие документацию по хондроитинсульфату.К. Санчес — научный сотрудник Национального фонда научных исследований (FNRS, Бельгия).
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Проф. Хенротин получил образовательные и исследовательские гранты от Bioiberica, Expanscience, Danone, Nestec и BioXtract.
Ссылки
- Альбертини Р., Пасси А., Абуджа П.М., Де Лука Г. (2000) Влияние гликозаминогликанов и протеогликанов на перекисное окисление липидов.Инт Дж Мол Мед 6: 129–136 [PubMed] [Google Scholar]
- Barnhill J.G., Fye C.L., Williams D.W., Reda D.J., Harris C.L., Clegg D.O. (2006) Выбор хондроитинового продукта для интервенционного исследования артрита глюкозамином / хондроитином. J Am Pharm Assoc (Вашингтон, Вашингтон) 46: 14–24 [PubMed] [Google Scholar]
- Bassleer C.T., Combal J.P., Bougaret S., Malaise M. (1998) Влияние хондроитинсульфата и интерлейкина-1 бета на суставные хондроциты человека, культивируемые в кластерах. Остеоартроз Хрящ 6: 196–204 [PubMed] [Google Scholar]
- Биан Л., Каплун М., Уильямс Д.Ю., Сюй Д., Атешян Г.А., Хунг С.Т. (2009) Влияние хондроитинсульфата на биохимические, механические и фрикционные свойства хрящевых эксплантатов при длительном культивировании. J Биомеханика 42: 286–290 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Ferlazzo AM, Calatroni A. (2004) Уменьшение фрагментации ДНК и производство гидроксильных радикалов гиалуроновой кислотой и хондроитин-4-сульфатом в железе плюс индуцированный аскорбатом окислительный стресс в культурах фибробластов.Free Radic Res 38: 601–611 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Traina P., Calatroni A. (2008) Хондроитин-4-сульфат ингибирует NF-kB транслокация и активация каспаз при коллаген-индуцированном артрите у мышей. Остеоартроз Хрящ 16: 1474–1483 [PubMed] [Google Scholar]
- Кампо Г.М., Авенозо А., Кампо С., Д’Аскола А., Трэйна П., Сама Д. и др. (2009a) Гликозаминогликаны модулируют воспаление и апоптоз в хондроцитах, обработанных LPS.J Cell Biochem 106: 83–92 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Ferlazzo AM, Altavilla D., Calatroni A. (2003) Эффективность лечения гликозаминогликанами экспериментального коллаген-индуцированного артрита в крысы. Артрит Res Ther 5: R122 – R131 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006a) Антиоксидантная активность хондроитинсульфата. Adv Pharmacol 53: 417–431 [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006b) Хондроитинсульфат: антиоксидантные свойства и положительные эффекты. Мини Рев Мед Хим 6: 1311–1320 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Traina P., D’Ascola A., Calatroni A. (2009b) Гликозаминогликаны снижают воспалительную реакцию, модулируя толл-подобные рецептор-4 в хондроцитах, стимулированных ЛПС. Arch Biochem Biophys 491: 7–15 [PubMed] [Google Scholar]
- Caraglia M., Beninati S., Giuberti G., Д’Алессандро А.М., Лентини А., Аббруззезе А. и др. (2005) Альтернативная терапия земными элементами усиливает хондрозащитные эффекты хондроитинсульфата у мышей. Exp Mol Med 37: 476–481 [PubMed] [Google Scholar]
- Катерсон Б., Махмудиан Ф., Соррелл Дж. М., Хардингем Т. Э., Бейлисс М. Т., Карни С. Л. и др. (1990) Модуляция структуры нативного хондроитинсульфата в развитии тканей и при заболеваниях. J Cell Sci 97: 411–417 [PubMed] [Google Scholar]
- Чан П.С., Кэрон Дж.P., Orth M.W. (2005a) Влияние глюкозамина и хондроитинсульфата на регуляцию экспрессии генов протеолитических ферментов и их ингибиторов в эксплантатах суставного хряща быка, зараженных интерлейкином-1. Am J Vet Res 66: 1870–1876 [PubMed] [Google Scholar]
- Chan P.S., Caron J.P., Orth M.W. (2006) Кратковременные изменения экспрессии генов в хрящевых эксплантатах, стимулированные интерлейкином бета, глюкозамином и хондроитинсульфатом. J Ревматол 33: 1329–1340 [PubMed] [Google Scholar]
- Чан П.С., Карон Дж. П., Орт М. В. (2007) Влияние глюкозамина и хондроитинсульфата на эксплантаты бычьего хряща в условиях длительного культивирования. Am J Vet Res 68: 709–715 [PubMed] [Google Scholar]
- Chan PS, Caron JP, Rosa GJ, Orth MW (2005b) Глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простагландина E (2) в эксплантатах суставного хряща. . Остеоартроз Хрящ 13: 387–394 [PubMed] [Google Scholar]
- Чо С. Ю., Сим Дж.С., Чжон С. С., Чанг С. Ю., Чой Д. В., Тойда Т. и др. (2004) Влияние низкомолекулярного хондроитинсульфата на индуцированный коллагеном артрит типа II у мышей DBA / 1J. Биол Фарм Булл 27: 47–51 [PubMed] [Google Scholar]
- Chou M.M., Vergnolle N., McDougall J.J., Wallace J.L., Marty S., Teskey V. и др. (2005) Влияние хондроитина и сульфата глюкозамина в составе диетического батончика на воспаление, интерлейкин-1бета, матриксную металлопротеазу-9 и повреждение хряща при артрите. Эксп Биол Мед 230: 255–262 [PubMed] [Google Scholar]
- Клегг Д.О., Реда Д.Дж., Харрис К.Л., Кляйн М.А. (2005) Эффективность глюкозамина и хондроитинсульфата у пациентов с болезненным остеоартритом (ОА) коленного сустава: исследование вмешательства глюкозамина / хондроитина. Ревматоидный артрит 52 (9S): S256, (Аннотация). [Google Scholar]
- Clegg D.O., Reda D.J., Harris C.L., Klein M.A., O’Dell J.R., Hooper M.M., et al. (2006) Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med 354: 795–808 [PubMed] [Google Scholar]
- Конте А., Volpi N., Palmieri L., Bahous I., Ronca G. (1995) Биохимические и фармакокинетические аспекты перорального лечения хондроитинсульфатом. Arzneimittelforschung 45: 918–925 [PubMed] [Google Scholar]
- David-Raoudi M., Deschrevel B., Leclercq S., Galera P., Boumediene K., Pujol JP (2009) Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальная регуляция гиалуронансинтаз: роль p38 и Akt. Ревматоидный артрит 60: 760–770 [PubMed] [Google Scholar]
- du Souich P., Гарсия А.Г., Верджес Дж., Монтелл Э. (2009) Иммуномодулирующие и противовоспалительные эффекты хондроитинсульфата. J Cell Mol Med 13 (8A): 1451–1463 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- du Souich P., Verges J. (2001) Простой подход для прогнозирования максимального эффекта, вызываемого лекарством, когда концентрации в плазме недоступны или диссоциируют от воздействия, как показано на данных по хондроитинсульфату. Clin Pharmacol Ther 70: 5–9 [PubMed] [Google Scholar]
- Эгеа Дж., Гарсия А.Г., Верджес Дж., Монтелл Э., Лопес М.Г. (2010) Антиоксидантное, противовоспалительное и нейропротекторное действие хондроитинсульфата и протеогликанов. Остеоартроз Хрящ 18 (Приложение 1): S24 – S28 [PubMed] [Google Scholar]
- Hochberg M.C. (2010) Структурно-модифицирующие эффекты хондроитинсульфата при остеоартрите коленного сустава: обновленный метаанализ рандомизированных плацебо-контролируемых исследований продолжительностью 2 года. Остеоартроз Хрящ 18 (Приложение 1): 528–531 [PubMed] [Google Scholar]
- Hochberg M.К., Клегг Д.О. (2008) Потенциальные эффекты хондроитинсульфата на отек суставов: отчет GAIT. Остеоартроз Хрящ 16 (Приложение 3): S22 – S24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hochberg MC, Zhan M., Langenberg P. (2008) Скорость уменьшения ширины суставной щели у пациентов с остеоартритом колено: систематический обзор и метаанализ рандомизированных плацебо-контролируемых исследований хондроитинсульфата. Curr Med Res Opin, в печати. [PubMed] [Google Scholar]
- Holzmann J., Брандл Н., Земанн А., Шабус Р., Марловиц С., Коуберн Р. и др. (2006) Различные эффекты TGFbeta и хондроитинсульфата на уровни активации p38 и ERK1 / 2 в суставных хондроцитах человека, стимулированных LPS. Остеоартроз Хрящ 14: 519–525 [PubMed] [Google Scholar]
- Имада К., Ока Х., Кавасаки Д., Миура Н., Сато Т., Ито А. (2010) Механизмы антиартритного действия природного хондроитинсульфата у человека суставные хондроциты и синовиальные фибробласты. Биол Фарм Булл 33: 410–414 [PubMed] [Google Scholar]
- Джексон К.Г., Плаас А.Х., Сэнди Дж. Д., Хуа С., Ким-Роландс С., Барнхилл Дж. Г. и др. (2010) Фармакокинетика перорального приема глюкозамина и хондроитинсульфата у человека по отдельности или в комбинации. Остеоартроз Хрящ 18: 297–302 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Jomphe C.j, Gabriac M., Hale T.M., Heroux L., Trudeau L.E., Deblois D., et al. (2008) Хондроитинсульфат ингибирует ядерную транслокацию ядерного фактора-каппаВ в хондроцитах, стимулированных интерлейкином-1бета.Базовый Clin Pharmacol Toxicol 102: 59–65 [PubMed] [Google Scholar]
- Jordan K.M., Arden N.K., Doherty M., Bannwarth B., Bijlsma J.W., Dieppe P., et al. (2003) Рекомендации EULAR 2003: научно обоснованный подход к лечению остеоартрита коленного сустава: отчет рабочей группы Постоянного комитета по международным клиническим исследованиям, включая терапевтические испытания (ESCISIT). Энн Рум Дис 62: 1145–1155 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Kahan A., Uebelhart D., De Vathaire F., Дельмас П.Д., Регинстер Дж. (2009) Долгосрочные эффекты хондроитинов 4 и 6 сульфата на остеоартрит коленного сустава: исследование по предотвращению прогрессирования остеоартрита, двухлетнее рандомизированное двойное слепое плацебо-контролируемое исследование. Ревматоидный артрит 60: 524–533 [PubMed] [Google Scholar]
- Катта Дж., Джин З., Ингам Э., Фишер Дж. (2009) Хондроитинсульфат: эффективная смазка для суставов? Остеоартроз Хрящ 17: 1001–1008 [PubMed] [Google Scholar]
- Кусано С., Отани А., Сакаи С., Игараси Н., Такегучи А., Тойода Х. и др. (2007) Определение хондрозина в плазме крови мышей с помощью ВЭЖХ после внутривенной или пероральной дозы. Биол Фарм Булл 30: 1365–1368 [PubMed] [Google Scholar]
- Лаудер Р.М. (2009) Хондроитинсульфат: сложная молекула с потенциальным воздействием на широкий спектр биологических систем. Комплемент Терапии Мед 17: 56–62 [PubMed] [Google Scholar]
- Лаудер Р.М., Хакерби Т.Н., Недушинский Л.А. (2000) Метод снятия отпечатков пальцев на хондроитин / дерматансульфат и гиалуронановые олигосахариды.Гликобиология 10: 393–401 [PubMed] [Google Scholar]
- Ли Й.Х., Ву Дж.Х., Чой С.Дж., Джи Дж.Д., Сон Г.Г. (2010) Влияние глюкозамина или хондроитинсульфата на прогрессирование остеоартрита: метаанализ. Ревматол Инт 30: 357–363 [PubMed] [Google Scholar]
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. (2000) Метаанализ хондроитинсульфата в лечении остеоартрита. J Ревматол 27: 205–211 [PubMed] [Google Scholar]
- Legendre F., Bauge C, Roche R., Saurel A.S., Pujol J.P. (2008) Хондроитинсульфатная модуляция матрикса и экспрессия воспалительных генов в IL-lbeta-стимулированных хондроцитах — исследование в культурах гипоксических альгинатных гранул. Остеоартроз Хрящ 16: 105–114 [PubMed] [Google Scholar]
- Малаваки С.Дж., Асимакопулу А.П., Ламари Ф.Н., Теохарис А.Д., Цанакакис Г.Н., Караманос Н.К. (2008) Капиллярный электрофорез для контроля качества хондроитинсульфатов в сырье и рецептурах. Анальный биохим 374: 213–220 [PubMed] [Google Scholar]
- Mazieres B., Хучер М., Заим М., Гарнеро П. (2007) Эффект хондроитинсульфата при симптоматическом остеоартрите коленного сустава: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. Энн Рум Дис 66: 639–645 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mazieres B., Hucher M.M.H., Zam M.M.Z. (2006) Хондроитинсульфат в лечении остеоартрита коленного сустава: рандомизированное двойное слепое многоцентровое плацебо-контролируемое исследование. Энн Рум Дис 65 (Дополнение II): 398. [Google Scholar]
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. (2000) Глюкозамин и хондроитин для лечения остеоартрита: систематическая оценка качества и метаанализ. JAMA 283: 1469–1475 [PubMed] [Google Scholar]
- Möller I., Pérez M., Monfort J., Benito P., Cuevas J., Perna C., et al. (2010) Эффективность хондроитинсульфата у пациентов с сопутствующим остеоартритом коленного сустава и псориазом: рандомизированное двойное слепое плацебо-контролируемое исследование. Остеоартроз Хрящ 18 (Приложение 1): 532–540 [PubMed] [Google Scholar]
- Monfort J., Martel-Pelletier J., Pelletier J.P. (2008a) Хондроитинсульфат при симптоматическом остеоартрите: критическая оценка метаанализов. Curr Med Res Opin 24: 1303–1308 [PubMed] [Google Scholar]
- Monfort J., Nacher M., Montell E., Vila J., Verges J., Benito P. (2005) Хондроитинсульфат и гиалуроновая кислота (500–730 кДа ) подавляют синтез стромелизина-1 в хондроцитах человека, страдающих остеоартритом. Наркотики Exp Clin Res 31: 71–76 [PubMed] [Google Scholar]
- Monfort J., Pelletier J.P., Garcia-Giralt N., Martel-Pelletier J. (2008b) Биохимические основы действия хондроитинсульфата на суставные ткани при остеоартрозе. Энн Рум Дис 67: 735–740 [PubMed] [Google Scholar]
- Mourao P.A. (1988) Распределение хондроитин-4-сульфата и хондроитин-6-сульфата в суставном и ростовом хряще человека. Ревматоидный артрит 31: 1028–1033 [PubMed] [Google Scholar]
- Omata T., Itokazu Y., Inoue N., Segawa Y. (2000) Эффекты хондроитинсульфата-C на разрушение суставного хряща при артрите, индуцированном мышиным коллагеном.Arzneimittelforschung 50: 148–153 [PubMed] [Google Scholar]
- Rainsford K.D. (2009) Важность фармацевтического состава и данных клинических испытаний и фармакологических исследований в определении эффективности хондроитинсульфата и других гликозаминогликанов: критический анализ. J Pharm Pharmacol 61: 1263–1270 [PubMed] [Google Scholar]
- Reichenbach S., Sterchi R., Scherer M., Trelle S., Burgi E., Burgi U., et al. (2007) Мета-анализ: хондроитин при остеоартрите коленного или тазобедренного суставов.Энн Интерн Мед 146: 580–590 [PubMed] [Google Scholar]
- Ричи Ф., Брюйер О., Этген О., Кучерат М., Хенротин Ю., Регинстер Дж. Я. (2003) Структурная и симптоматическая эффективность глюкозамина и хондроитина при остеоартрите коленного сустава: всесторонний метаанализ. Arch Intern Med 163: 1514–1522 [PubMed] [Google Scholar]
- Ronca F., Palmieri L., Panicucci P., Ronca G. (1998) Противовоспалительная активность хондроитинсульфата. Остеоартроз Хрящ 6 (Приложение A): 14–21 [PubMed] [Google Scholar]
- Sawitzke A.Д., Ши Х., Финко М.Ф., Данлоп Д.Д., Бингем С.О., III, Харрис К.Л. и др. (2008) Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Ревматоидный артрит 58: 3183–3191 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Шварц Н.Б., Дорфман А. (1975) Стимуляция продукции хондроитинсульфат-протеогликана хондроцитами в монослое. Подключите ткань Res 3: 115–122 [PubMed] [Google Scholar]
- Shinmei M., Мияучи С., Мачида А., Миядзаки К. (1992) Количественное определение хондроитин-4-сульфата и хондроитин-6-сульфата в патологической суставной жидкости. Ревматоидный артрит 35: 1304–1308 [PubMed] [Google Scholar]
- Тахири К., Корвин-Змиевска С., Ришетт П., Херо Ф., Шевалье Х., Савуре Дж. Ф. и др. (2008) Природные хондроитинсульфаты увеличивают агрегацию протеогликановых комплексов и снижают экспрессию ADAMTS-5 в хондроцитах, обработанных интерлейкином 1 бета. Энн Рум Дис 67: 696–702 [PubMed] [Google Scholar]
- Тат С.K., Pelletier J.P., Mineau F., Duval N., Martel-Pelletier J. (2010) Различные эффекты 3 различных соединений хондроитинсульфата на хрящ / хондроциты человека при остеоартрите: важность чистоты и производственного процесса. J Ревматол 37: 656–664 [PubMed] [Google Scholar]
- Tat S.K., Pelletier J.P., Verges J., Montell E., Lajeunesse D., Fahmi H., et al. (2007) Хондроитин и сульфат глюкозамина в комбинации снижают прорезорбтивные свойства субхондральных костных остеобластов человека.Артрит Res Ther 9: R117. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Uebelhart D., Thonar EJ, Zhang J., Williams JM (1998) Защитный эффект экзогенного хондроитин-4,6-сульфата при острой деградации суставного хряща у кролика . Остеоартроз Хрящ 6 (Suppl. A): 6–13 [PubMed] [Google Scholar]
- Валлиер М., дю Суич П. (2010) Модуляция воспаления с помощью хондроитинсульфата. Остеоартроз Хрящ 18 (Приложение 1): S1 – S6 [PubMed] [Google Scholar]
- Вангснесс К.Т., младший, Спайкер В., Эриксон Дж. (2009) Обзор доказательной медицины использования глюкозамина и хондроитинсульфата при остеоартрите коленного сустава. Артроскопия: J Arthroscopic Relat Surg 25: 86–94 [PubMed] [Google Scholar]
- Verbruggen G., Veys E.M. (1977) Влияние сульфатированных гликозаминогликанов на метаболизм протеогликанов в клетках синовиальной оболочки. Acta Rhumatol Belg 1: 75–92 [PubMed] [Google Scholar]
- Verges J., Montell E., Herrero M., Perna C, Cuevas J., Perez M., et al.(2005) Клиническое и гистопатологическое улучшение псориаза при пероральном приеме хондроитинсульфата: случайная находка. Дерматол Интернет J 11: 31. [PubMed] [Google Scholar]
- Vergés J., Montell E., Martinez G., Heroux L., du Souich P. (2004) Хондроитинсульфат снижает фактор ядерной транслокации NF-kappaB и не изменяет состояние активации активирующего белка-1 (AP-1). Остеоартроз Хрящ 12: 194, (Аннотация). [Google Scholar]
- Volpi N. (2002) Пероральная биодоступность хондроитинсульфата (Кондросульф) и его компонентов у здоровых добровольцев мужского пола.Остеоартроз Хрящ 10: 768–777 [PubMed] [Google Scholar]
- Volpi N. (2003) Пероральное всасывание и биодоступность хондроитинсульфата ихтикового происхождения у здоровых добровольцев мужского пола. Остеоартроз Хрящ 11: 433–441 [PubMed] [Google Scholar]
- Volpi N. (2006a) Достижения в анализе хондроитинсульфата: применение при физиологических и патологических состояниях соединительной ткани и при фармакологическом лечении остеоартрита. Curr Pharm Des 12: 639–658 [PubMed] [Google Scholar]
- Volpi N.(2006b) Хондроитинсульфат: структура, роль и фармакологическая активность, Elsevier: Amsterdam [Google Scholar]
- Volpi N. (2009) Качество различных препаратов хондроитинсульфата в зависимости от их терапевтической активности. J Pharm Pharmacol 61: 1271–1280 [PubMed] [Google Scholar]
- Volpi N., Tarugi P. (1999) Влияние плотности заряда хондроитинсульфата, положения сульфатной группы и молекулярной массы на Cu2 + -опосредованное окисление липопротеинов низкой плотности человека: действие нормального человеческого хондроитинсульфата плазмы.J Biochem 125: 297–304 [PubMed] [Google Scholar]
- Wang L., Wang J., Almqvist KF, Veys EM, Verbruggen G. (2002) Влияние полисульфатированных полисахаридов и гидрокортизона на метаболизм внеклеточного матрикса суставных хондроцитов человека в пробирка. Clin Exp Rheumatol 20: 669–676 [PubMed] [Google Scholar]
- Zhang W., Doherty M., Arden N., Bannwarth B., Bijlsma J., Gunther K.P., et al. (2005) Основанные на фактических данных рекомендации EULAR по лечению остеоартрита тазобедренного сустава: отчет рабочей группы Постоянного комитета EULAR по международным клиническим исследованиям, включая терапию (ESCISIT).Энн Рум Дис 64: 669–681 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Чжан В., Московиц Р. В., Нуки Г., Абрамсон С., Альтман Р. Д., Арден Н. и др. (2008) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, Часть II: Основанные на фактах, согласованные экспертные рекомендации OARSI. Остеоартроз Хрящ 16: 137–162 [PubMed] [Google Scholar]
- Чжан В., Нуки Г., Московиц Р. В., Абрамсон С., Альтман Р. Д., Арден Н. К. и др. (2010) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г.Остеоартроз Хрящ 18 (4): 476–499 [PubMed] [Google Scholar]
От исследований in vitro к клиническим рекомендациям
Ther Adv Musculoskelet Dis. 2010 Dec; 2 (6): 335–348.
Мариан Мати
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Кристель Санчес
2 Исследовательское отделение костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
Cecile Lambert
2 Отделение исследований костей и хрящей, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
2 Кости и Отделение исследования хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия
1 Отделение исследования костей и хряща, Институт патологии, уровень 5, CHU Sart-Tilman, 4000 Льеж, Бельгия eb.ca.glu@nitornehyЭта статья цитируется другими статьями в PMC.Abstract
Хондроитинсульфат (CS) рекомендуется в качестве терапевтического вмешательства при мультимодальном подходе к лечению остеоартрита (OA). CS был тщательно изучен для описания его фармакологии (фармакокинетических эффектов, эффектов in vitro и in vivo) и клинической эффективности. Сообщалось о различных результатах в зависимости от системы оценки (модель, дозировка и продолжительность) и источника CS (происхождение и качество).Целью этого обзора было собрать большую часть доступной информации о CS и обсудить его эффективность в управлении OA.
Ключевые слова: хрящ, хондроитинсульфат, остеоартрит, механизм действия, фармакокинетика
Введение
Хондроитинсульфат (CS) является основным компонентом внеклеточного матрикса (ECM) многих соединительных тканей, включая хрящ, кость, кожу , связки и сухожилия. Остеоартрит (ОА) характеризуется прогрессирующими структурными и метаболическими изменениями в тканях суставов, в основном деградацией хряща, склерозом субхондральной кости и воспалением синовиальной оболочки.Лечение остеоартрита включает мультимодальное терапевтическое вмешательство, поскольку на сегодняшний день лечения не найдено. Для лечения ОА необходимы препараты, которые могут замедлить, остановить или даже избежать деградации суставов. Многие из рекомендуемых вмешательств представляют только эффекты, изменяющие симптомы, и несколько эффектов, изменяющих структуру.
CS и другие соединения, такие как глюкозамин, используются в медицинских целях более 40 лет. CS продается как безрецептурная пищевая добавка в Северной Америке и отпускается по рецепту в соответствии с правилами Европейского медицинского агентства (EMEA) в Европе.В последние десятилетия CS вызывал много интересов в качестве потенциального терапевтического средства против ОА. CS является частью рекомендаций Международного общества исследований остеоартрита (OARSI) по лечению остеоартрита коленного сустава [Zhang et al. 2010, 2008] и рекомендаций Европейской лиги против ревматизма (EULAR) по лечению тазобедренного и коленного суставов OA Zhzang et al. 2005; Jordan et al. 2003]. ХС и глюкозамин могут стать отличной альтернативой для пациентов с ОА.
CS, как естественный компонент ЕСМ, представляет собой сульфатированный гликозаминогликан (ГАГ), состоящий из длинной неразветвленной полисахаридной цепи с повторяющейся дисахаридной структурой N-ацетилга-лактозамина и глюкуроновой кислоты.Большинство остатков N-ацетилгалактозамина () сульфатированы, особенно в положениях 4 и 6, что делает CS сильно заряженным полианионом. CS отвечает за многие важные биомеханические свойства хряща, такие как сопротивление и эластичность. Его высокое содержание в аггрекане играет важную роль в обеспечении устойчивости хряща к давлению при различных условиях нагрузки. Профиль сульфатации хондроитина был описан в хрящах [Mourao, 1988]. Изменения в структуре CS описаны в тканях OA [Caterson et al. 1990] и пониженное соотношение CS-6: CS-4 были обнаружены в синовиальной жидкости и хрящах пациентов с ОА [Shinmei et al. 1992]. Более трех десятилетий назад было предложено [Schwartz and Dorfman, 1975], что поставка CS в качестве терапевтического вмешательства при повреждении хряща может обеспечить строительные блоки для синтеза нового компонента матрикса, поскольку повышение концентрации CS может действовать в пользу матрикса. регенерация и учитывать ее благотворное влияние.
Химическая структура хондроитинсульфата, где R — Na или H, а X — SO 3 R или H.
Однако с тех пор механизм действия CS как терапевтического вмешательства все еще требует выяснения, а его эффективность остается предметом дискуссий.
Общая цель этого обзора состояла в том, чтобы собрать большую часть доступной информации о CS, его фармакокинетике, его эффектах in vitro, и in vivo, и его клинической эффективности. Цель этого обзора — обсудить клиническую полезность CS и перспективы использования CS при лечении остеоартрита.
Фармакокинетика
Natural CS имеет молекулярную массу 50–100 кДа.После процесса экстракции молекулярная масса составляет 10-40 кДа в зависимости от сырья. CS в основном получают из бычьего, свиного или морского (акульего) хряща.
CS чаще всего вводят перорально в дозах от 800 до 1200 мг / день. CS быстро всасывается в желудочно-кишечном тракте. Поглощенный CS достигает компартмента крови в виде 10% CS и 90% деполимеризованных низкомолекулярных производных.
Сообщалось о различной биодоступности и фармакокинетических переменных в зависимости от характеристик и происхождения CS [Malavaki et al. 2008]. О некоторых из них сообщили в. Биодоступность CS обсуждается. Данные зависят от системы, используемой для оценки, структуры и характеристик CS, таких как молекулярная масса, плотность заряда и кластер дисульфатированных дисахаридов, используемой концентрации и вида животных, использованных для проведения исследования [Volpi, 2003]. В большинстве исследований использовался CS из трахеи крупного рогатого скота (чистота 95%), который представляет собой тот же материал, который использовался в клинических испытаниях [Barnhill et al. 2006].
Таблица 1.
Различные фармакокинетические параметры в зависимости от системы исследования и источника CS.
| Исследование | Источник хондроитина | Система | Результаты | |
|---|---|---|---|---|
| Conte et al. [1995] | Трахея крупного рогатого скота 16 мг / кг перорально | Крысы Wistar | ||
| Трахея крупного рогатого скота 16 мг / кг перорально | Молодые собаки породы бигль | |||
| Трахея крупного рогатого скота Разовая доза 0.8 г или две дозы по 0,4 г | Здоровые добровольцы ( N = 12; 6 мужчин и 6 женщин) | Разовая доза: | Две дозы: | |
| Трахея крупного рогатого скота Разовая доза 0,8 г / день | Пациенты с ОА ( N = 18) | Концентрация в плазме:
| ||
| Ronca . [1998] | Смесь CS-6 и CS-4 (1: 1) Пероральное введение 16 мг / кг (4 мг / крыса) | Крысы ( N = 10) |
| |
| Volpi [2002] | Хондросульф® однократная доза (4 г) | Мужчина здоровый волонтеры ( N = 20) | ||
| Volpi [2003] | Shark CS Однократная доза (4 г) | Здоровые добровольцы мужского пола ( N = 20) |
Биодоступность CS после перорального приема колеблется от 10% до 20% [Lauder, 2009].
Поглощение CS может зависеть от статуса сульфатации. Положение и процентное содержание сульфатных групп обычно варьируется в зависимости от конкретных источников животного происхождения [Volpi, 2006a, 2006b]. Действительно, десульфатированный хондроитин у мышей [Kusano et al. 2007] имеет очень быстрое поглощение, с пиком в течение 15 минут и очень быстрым возвращением к исходному уровню через 3 часа, тогда как CS у акул у здоровых добровольцев мужского пола поглощается медленнее (пик через 8,7 часа) и медленнее выведение (уровни поддерживаются). до 16 часов после администрирования) [Volpi, 2003].CS из трахеи крупного рогатого скота демонстрирует быстрое увеличение плазмы здоровых добровольцев мужского пола с пиком в пределах 1–5 часов после введения и возвращением к исходному уровню через 10 часов [Volpi, 2002].
Фармакокинетические параметры CS, определенные у здоровых добровольцев мужского пола [Volpi, 2002], после перорального приема показали значительное увеличение уровней CS в плазме (более чем на 200%) по сравнению с уровнями перед дозой в течение 24 часов. Пиковые концентрации наблюдались через 2 часа после дозирования, и увеличение значимо через 2-6 часов после дозирования.Кинетика первого порядка наблюдалась для доз до 3000 мг. Многократные дозы 800 мг для пациентов с ОА не изменяют кинетику CS. Недавно, используя флуорофорный углеводный электрофорез и хроматографию наложения 6, Джексон и его коллеги не наблюдали никаких изменений эндогенной концентрации (20 (мкг / мл) и состава дисахаридов CS после перорального приема однократной дозы 1200 мг CS. Одно объяснение может быть, что небольшое количество проглоченного CS достигает циркуляции в неизмененной форме или состоит из дисахаридов более крупных фрагментов [Jackson et al. 2010]; в качестве альтернативы, могло случиться так, что анализ был недостаточно чувствителен для обнаружения более низких концентраций. Это еще предстоит продемонстрировать другими методами анализа. Другой характеристикой CS является его способность накапливаться в суставных тканях. Высокое содержание меченого CS было обнаружено в тканях суставов, включая синовиальную жидкость и хрящ, после перорального введения людям [Ronca et al. 1998].
Трудно оценить релевантность максимальной концентрации, достигнутой в компартменте крови (Cmax) для этого типа лекарственного средства, поскольку in vivo ответ может быть результатом воздействия CS и дисахаридов.Более того, CS — это препарат замедленного действия, в результате чего действие начинается медленно, а максимальный эффект достигается через несколько месяцев. Кроме того, CS — это лекарство биологического происхождения, что означает, что его измерение в биологических жидкостях не позволяет отличить лекарство от эндогенных молекул. Максимальный эффект (Emax) был предсказан с использованием альтернативного метода [du Souich and Verges, 2001]. Эффект Emax рассчитывали на основании клинической эффективности. Было подсчитано, что 50% Emax достигается за 35 дней у пациентов с легким ОА.Примерный период полураспада CS и его производных в плазме крови человека составляет 15 часов. Стабильное состояние достигается через 3–4 дня, и для получения максимального эффекта может потребоваться 3–6 месяцев лечения.
CS не метаболизируется цитохромом P450. Это говорит в пользу очень низкого риска взаимодействия с другими лекарствами.
Наконец, для CS был описан эффект переноса. Действительно, после отсроченного начала действия максимальный эффект сохраняется после прекращения терапии.
Механизм действия
Многие эффекты были описаны для CS в различных исследованиях in vitro, и in vivo, с использованием различных типов и концентраций CS и различных моделей.Точный механизм действия еще предстоит уточнить. In vitro эффекты на суставные клетки и эффекты in vivo на моделях артрита описаны в и, соответственно.
Таблица 2.
In vitro эффекты хондроитинсульфата.
| Исследование | Хондроитин | Система и продолжительность | Результаты | ||||
|---|---|---|---|---|---|---|---|
| Verbruggen et al. [1977] | 10–400 мкг / мл | Однослойные синовиальные клетки | Стимуляция 11% синтеза гиалуроната во время фазы роста | ||||
| Увеличение на 88% во время стационарной фазы | |||||||
| Bassleer et al. [1998] | КРС 100–1000 мкг / мл | Суставные хондроциты человека в кластерах, стимулированные IL-1β До 32 дней | Значительное снижение продукции PGE, стимулированной IL-1β 2 | ||||
| Увеличение выработки коллагена PG и типа II | |||||||
| Wang et al. [2002] | C poly S 10 мкг / мл | Человеческие суставные хондроциты в агарозном геле, стимулированные IL-1β 1 неделя | Стимуляция аггрекана, гиалуронана и коллагена типа II из-за подавления ММП | ||||
| Campo et al. al. [2004] | CS-4 1,0 и 2,0 мг / мл | Фибробласт кожи человека | Антиоксидантное действие CS-4 за счет повышения жизнеспособности клеток и ингибирования фрагментации ДНК | ||||
| Chan et al. [2005a] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Снижение IL-1β-индуцированной MMP-13 | ||||
| Chan et al. [2005b] | 20 мкг / мл | Эксплантаты бычьего суставного хряща, стимулированные IL-1β от 24 до 48 часов | Подавление индуцированной IL-1β экспрессии NO-синтазы, COX-2 и mPGES-1 | ||||
| Монфорт и др. [2005] | 10–1000 мкг / мл | Хондроциты ОА человека, стимулированные IL-1β 48 ч | Ингибирование MMP-3 | ||||
| Holzmann et al. [2006] | 25 мкг / мл | Человеческие суставные хондроциты, стимулированные LPS До 72 часов | Ингибирование MMP-13 за счет снижения активации p38 и Erk1 / 2 | ||||
| Tat et al. [2007] | 200 мкг / мл | Остеобласты субхондральной кости человека ОА До 48 ч | Снижение прорезорбтивных агентов | ||||
| Обратное действие витамина D3 на соотношение OPG: RANK9584 | Tahiri et al. [2008] | Хондросульф® или свинья 10 или 100 мкг / мл | Хондроциты суставов кролика, стимулированные IL-1β 20 ч | Повышение синтеза PG | |||
| Ингибирование экспрессии AD10AMTS-5 | |||||||
| Jomphe et al. [2008] | Очищенные бычьи CS-4 и CS-6 200 мг / мл | Хондроциты кролика, стимулированные IL-1β 48 ч | Снижение ядерной транслокации NF-κB | ||||
| Профилактика активации Erk1 / 2 и p38 | |||||||
| Снижение апоптоза, индуцированного нитропруссидом | |||||||
| Legendre et al. [2008] | Avian CS −100 мкг / мл | Бычьи суставные хондроциты в гипоксических альгинатных гранулах 24–48 часов | Снижение IL-1β-индуцированных MMP-1, −3, −13 и ADAMTS-4 и — 5 | ||||
| Снижение IL-1β-индуцированного COX-2 и iNOS | |||||||
| Снижение продукции PGE 2 , но не NO | Незначительное увеличение синтеза ГАГ | ||||||
| Противодействие подавлению IL-1β рецепторов TGFβ | |||||||
| Katta et al. [2009] | Смесь CS A, CS B и CS C 10–50 мг / мл | Эксплантаты бычьего хряща 24 ч | Эффективная смазка для суставов | ||||
| Распространение в хрящ | |||||||
| Давид-Рауди et al. [2009] | Avian CS 100 мкг / мл | OA фибробластоподобные синвиоциты человека 48 часов с предварительной обработкой | Регулирование гиалуронансинтазы | ||||
| Campo et al. [2009a] | CS-4 крупного рогатого скота и CS-6 акулы 0,5 и 1,0 мг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Антиапоптотический эффект обоих CS | ||||
| Ингибирование медиаторов воспаления, iNOS и MMP более очевидно с CS-4, чем с CS-6 | |||||||
| Campo et al. [2009b] | CS-4 крупного рогатого скота и CS-6 акулы 25 и 50 мкг / мл | Хондроциты суставов мыши, стимулированные LPS 24 ч | Ингибирование воспалительных цитокинов (MyD88 и TRAF-6), ингибирование активации NF -kB и iNOS обоими CS | ||||
| Эффект через TLR4 (подтвержден экспериментом со специфическими антителами) | |||||||
| Bian et al. [2009] | CS-6 и CS-4 акульего происхождения 10–100 мг / мл | Эксплантаты бычьего хряща 4 недели | Снижение содержания ГАГ | ||||
| Imada et al. [2010] | Акула (в основном CS-6) и свинья (в основном CS-4) 1–100 мкг / мл | Суставные хондроциты человека в альгинатных шариках и синовиальный фибробласт, стимулированные IL-1β 6 или 4 дня | Разные эффект обеих CS | ||||
| Подавление индуцированных IL-1b ADAMTS-4 и -5 в обоих типах клеток | |||||||
| Подавление индуцированных IL-1β MMP- 13 и увеличить экспрессию аггрекана в хондроцитах | |||||||
| Восстановление TIMP-3 в хондроцитах и TIMP-1 в синовиоцитах CS свиньи |
Таблица 3.
In vivo эффекты хондроитинсульфата.
| Исследование | Хондроитин | Модель | Результаты |
|---|---|---|---|
| Uebelhart et al. [1998] | 80 мг / день перорально или i. м. | Кроличья модель повреждения хряща, вызванного химопапаином | Значительное увеличение продукции PG |
| Omata et al. [2000] | 1000 мг / кг | Коллаген-индуцированный артрит у мышей | Снижение параметров синовита: клеточная инфильтрация, фиброз и пролиферация выстилающих клеток |
| Campo et al. [2003] | 1 мл / кг (внутрибрюшинно) | Коллаген-индуцированный артрит у крыс | Лечение начинали после начала артрита (день 10) |
| Защита от окислительного стресса | |||
| 25 мг / кг (перорально) | Снижение уровней TNF-α и миелопероксидазы в плазме | ||
| Cho et al. [2004] | 1200 мг / кг | Коллаген-индуцированный артрит у крыс | Снижение уровней IL-6 |
| Caraglia et al. [2005] | 0,3 мг / день | Спонтанный ОА у мышей 12 дней | Значительное уменьшение апоптозных хондроцитов через 30 дней |
| Chou et al. [2005] | Пищевая добавка (18 мг / г) | Адъювант-индуцированный артрит Фрейнда у крыс | Предотвращение увеличения MMP-9 Снижение уровня IL-1β в тканях суставов, но не в сыворотке |
| Campo et al. al. [2008] | CS-4 (трахея крупного рогатого скота) 30–120 мг / кг (т.е.p.) | Коллаген-индуцированный артрит у мышей В течение 25 дней | Ингибирование активации NF-κB Ингибирование MMP-13 ингибирование активации каспаз-3 и -7 |
Противовоспалительный эффект
CS. сообщалось, что он обладает противовоспалительным действием. Было показано, что он ингибирует in vitro синтез различных промежуточных продуктов воспаления, таких как синтаза оксида азота (NO), циклооксигеназа (COX) -2, микросомальная простагландин-синтаза (mPGES) -1 и простагландин (PG) E 2 [Campo и другие. 2009a; Legendre et al. 2008; Чан и др. 2005b; Bassleer et al. 1998]. Также было показано, что CS может действовать на toll-подобный рецептор (TLR) -4, ингибируя воспалительные цитокины, MyD88 и фактор, связанный с рецептором фактора некроза опухоли (TNF) (TRAF) -6, посредством ингибирования ядерного фактора (NF ) -kB активация [Campo et al. 2009b].
Противовоспалительный эффект CS был также продемонстрирован in vivo. Было показано, что CS снижает синовит при коллаген-индуцированном артрите у мышей [Omata et al. 2000]. Он также был способен снижать провоспалительный цитокин, интерлейкин (IL) -6, в той же модели [Cho et al. 2004]. CS также снижает уровень IL-1b в суставной ткани при адъювантном артрите Фрейнда при введении в качестве пищевой добавки [Chou et al. 2005] и TNF-α и миелопероксидаза в плазме крови крыс с коллаген-индуцированным артритом и после перорального введения [Campo et al. 2003].
Антикатаболические и анаболические эффекты
Первый анаболический эффект CS был описан более 30 лет назад.CS увеличивал синтез гиалуроната в синовиальных клетках [Verbruggen and Veys, 1977]. С тех пор было также продемонстрировано увеличение синтеза коллагена типа II и протеогликана (PG) в хондроцитах человека [Wang et al. 2002; Bassleer et al. 1998] и ГАГ в хондроцитах крупного рогатого скота [Legendre et al. 2008]. Этот эффект также может быть вторичным по отношению к подавлению регуляции матриксной металлопротеиназы (ММП) [Wang et al. 2002]. Было также показано, что CS ингибирует MMP-1, -3 и -13, а также ADAMTS-4 и -5 (аггреканазы) в хондроцитах человека, свиньи и крупного рогатого скота [Imada et al. 2010; Legendre et al. 2008; Tahiri et al. 2008; Чан и др. 2005a; Монфорт и др. 2005]. Ингибирование MMP-13 может происходить через ингибирование активации p38 и Erk1 / 2 [Holzmann et al. 2006]. Для CS-4 и CS-6 были продемонстрированы различные ингибирующие способности против ММП в хондроцитах мышей [Campo et al. 2009a]. Различия между CS-6 и CS-4 недавно были также показаны на человеческих клетках. Действительно, CS-6 (акульего происхождения) может противодействовать ингибированию IL-1b тканевым ингибитором металлопротеаз (TIMP) -3 в хондроцитах человека и TIMP-1 в синовиальных фибробластах, тогда как CS-4 (происхождение из трахеи свиньи) не дает того же эффект [Imada et al. 2010]. CS может активировать гиалуронансинтазу в фибробластоподобных клетках [David-Raoudi et al. 2009] и может быть эффективным в качестве смазки для суставов, как было показано на эксплантатах бычьего хряща [Katta et al. 2009]. Также сообщалось, что CS может влиять на процесс резорбции, происходящий в субхондральной кости во время ОА. CS действительно может увеличивать соотношение остеопротегерин (OPG): активатор рецептора для лиганда NF-κB (RANKL) в остеобластах OA в пользу гомеостаза субхондральной кости [Tat et al. 2007]. Было продемонстрировано, что CS действует на большинство суставных тканей, участвующих в патофизиологии ОА. Наконец, недавнее исследование in vitro на эксплантатах бычьего хряща, обработанных CS-4 и CS-6 в течение 4 недель, выявило отрицательный эффект CS, показывающий, что он снижает содержание GAG [Bian et al. 2009]. Важно отметить, что это исследование было проведено с самой высокой концентрацией CS из когда-либо протестированных (10–100 мг / мл).
Анаболический и антикатаболический эффект CS также был продемонстрирован in vivo. CS может увеличивать продукцию PG на кроличьей модели деградации хряща [Uebelhart et al. 1998], предотвращают повышение уровня ММР-9 при адъювантном артрите Фрейнда у крыс при введении в качестве пищевой добавки [Chou et al. 2005] или ингибируют ММР-13 при коллаген-индуцированном артрите у мышей [Campo et al. 2008].
Антиапоптотический эффект
CS продемонстрировал антиапоптотические свойства как in vitro, так и in vivo. Было показано, что CS (200 (мкг / мл) снижает чувствительность хондроцитов кролика к апоптозу [Jomphe et al. 2008]. Этот эффект был связан с уменьшением транслокации NF-κB и со снижением пути передачи сигналов киназы MAP через p38 и Erk1 / 2. Другое исследование указало на антиапоптотический эффект CS-4 и CS-6 в суставных хондроцитах мыши [Campo et al. 2009a]. In vivo, на мышиной модели спонтанного ОА было показано, что 12-дневное лечение CS (0,3 мг / день) снижает количество апоптозных хондроцитов при оценке через 30 дней [Caraglia et al. 2005]. Также было продемонстрировано, что он способен ингибировать активацию каспазы-3 и -7 при коллаген-индуцированном артрите у мышей [Campo et al. 2008]. Эти результаты свидетельствуют в пользу хондропротекторного действия CS.
Антиоксидантный эффект
Антиоксидантные эффекты были рассмотрены [Campo et al. 2006a, 2006b]. Было показано, что CS обладает антиоксидантными свойствами in vitro в фибробластах кожи человека [Campo et al. 2004] и in vivo при коллаген-индуцированном артрите у крыс [Campo et al. 2003]. CS обеспечивает защиту от перекиси водорода и супероксид-анионов. Действительно, эти исследования продемонстрировали, что он может ограничивать гибель клеток, уменьшать фрагментацию ДНК и окисление белков, уменьшать образование свободных радикалов и действовать как поглотитель свободных радикалов. Он снижает перекисное окисление липидов и улучшает антиоксидантную защиту за счет восстановления эндогенных антиоксидантов, восстановленного глутатиона (GSH) и супероксиддисмутазы (SOD).
Регуляция клеточного сигнального пути
CS, как было обнаружено, действует на основные клеточные сигнальные пути.Было показано, что он ингибирует активацию пути киназы MAP, p38 и Erk ½, а также ингибирование трансактивации NF-κB в хондроцитах кролика [Jomphe et al. 2008; Verge’s et al. 2004]. Было также показано, что CS действует на другие промежуточные продукты клеточной передачи сигналов [Egea et al. 2010]. CS был способен индуцировать путь протеинкиназы C (PKC) / PI3K / Akt в клетках нейробластомы. Многие эффекты, описанные для CS на патофизиологию ОА, могут быть связаны с его действием на передачу сигналов в клетках.
Важно помнить, что большинство эффектов in vitro было получено с использованием высоких концентраций CS, которые не соответствуют ожидаемым концентрациям в плазме. Более того, учитывая медленное действие препарата на человека, системы in vitro и in vivo использовались в течение довольно короткого времени. Различные авторы предположили, что высокая концентрация, используемая in vitro, использовалась для компенсации этих проблем [Tat et al. 2010; Монфорт и др. 2008b]. Различия в чистоте и свойствах CS могут быть причиной несоответствия эффектов. Это было недавно рассмотрено в двух всеобъемлющих обзорах [Rainsford, 2009; Вольпи, 2009]. Это было подтверждено даже в суставных хондроцитах [Tat et al. 2010], когда три разных типа CS были протестированы в одной и той же системе и оказали различное воздействие на ключевые медиаторы OA. Это исследование продемонстрировало, что ХС бычьего происхождения гораздо эффективнее ингибирует катаболические медиаторы, чем ХС свиного происхождения.Также важно отметить, что эффекты CS in vivo в основном наблюдались на животных моделях артрита. Только одно исследование было проведено на модели спонтанного ОА [Caraglia et al. 2005].
Точный механизм действия CS еще предстоит выяснить. Взятые вместе, эти данные предполагают вмешательство CS на разных уровнях патофизиологии ОА, как показано в.
Схематическое изображение мишеней хондроитинсульфата (CS) в хондроцитах во время остеоартрита, как было предложено исследованиями in vitro: CS действует на сигнальные пути клеток, воспалительные и катаболические пути и на окислительный стресс (как показано черными стрелками).CS нацелен на различные промежуточные соединения в этих путях (как показано серыми стрелками). CS, хондроитинсульфат; ИЛ, интерлейкин; ECM, внеклеточный матрикс; ПГЕ 2 , простагландин E 2 ; PG, протеогликан; ММП, матриксная металлопротеиназа; NO, оксид азота; ADAMTS, дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами; NF-κB, ядерный фактор kB; ЦОГ, циклоосигеназа, iNOS, индуцируемая синтаза оксида азота.
Клинический эффект хондроитинсульфата
Терапевтическая эффективность CS изучалась и сообщалась в различных клинических исследованиях у пациентов с ОА.Влияние CS на пациентов с ОА оценивалось либо по симптомам ОА (боль и функция), чтобы определить его симптоматическое лекарство замедленного действия для эффекта ОА (SYSADOA), либо по модификации заболевания (эффект структуры, сужение суставной щели (JSN)) для определения его модифицирующий болезнь эффект препарата ОА (DMOAD).
Симптоматическое лекарство замедленного действия для лечения ОА
Различные мета-анализы [Reichenbach et al. 2007; Richy et al. 2003; Leeb et al. 2000; McAlindon et al. 2000] сообщили о различной величине эффекта (ES) на боль и функцию CS в диапазоне от 0,9 до всего 0,3.
Недавно были разработаны и опубликованы три исследования, посвященных влиянию CS на SYSADOA, то есть исследование GAIT [Hochberg and Clegg, 2008; Clegg et al. 2006], исследование STOPP [Kahan et al. 2009] и еще одно рандомизированное контролируемое исследование (РКИ) [Mazieres et al. 2007; Mazieres et al. 2006] (). Совсем недавно рекомендации Международного общества исследований остеоартрита (OARSI) по лечению ОА определили умеренный или большой ES (0.75, 95% ДИ 0,50–0,99) [Zhang et al. 2010], но подчеркнул систематическую ошибку публикации, неоднородность результатов и кумулятивное снижение ES (1,85, 95% ДИ 1,47–2,22, в 1992 г. до 0,75, 95% ДИ 0,50–1,01, в 2006 г.).
Таблица 4.
| Исследование | Результат | Вмешательство | Население и продолжительность | Размер результата / эффекта | |||||
|---|---|---|---|---|---|---|---|---|---|
| Глобальная оценка | 900 Maziéres et al. [2007] | Глобальная оценка исследователями клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 3,1 (CS) и 2,5 (Плацебо), p = 0,044 Благоприятствует CS | ||||
| Общая оценка пациентом клинического улучшения (колено) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец обработки) | NS | ||||||
| Качество жизни | |||||||||
| Maziéres et al. [2007] | Физический компонент SF-12 (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | 5,8 (CS) и 3,8 (плацебо), p = 0,021 Благоприятствует CS | |||||
| SF-12 Психический компонент | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Pain | |||||||||
| Clegg et al. [2006] | Боль | CS против плацебо | РКИ, N = 1583, 24 недели | CS не лучше, чем плацебо | |||||
| Maziéres et al. [2007] | Боль во время активности, ВАШ (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | −41% (CS ) и -32% (плацебо), p = 0,029 Поддерживает CS | |||||
| Боль в покое, ВАШ (изменение от исходного уровня) | CS vs. плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | ||||||
| Reichenbach et al. [2007] | Исходы, связанные с болью | CS по сравнению с плацебо / без лечения | MA, 20 РКИ, n = 3846, ОА коленного или тазобедренного сустава, продолжительность испытаний от 6 до 132 недель | Значительная неоднородность | |||||
| Kahan et al. [2009] | Подшкала VAS и WOMAC | CS vs. плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Значительно более быстрое уменьшение боли в целевом колене с помощью CS | |||||
| Функция | |||||||||
| Clegg et al. [2006] | Припухлость сустава, выпот или и то, и другое при клиническом обследовании | CS по сравнению с плацебо | РКИ, N = 1583, 24 недели | CS значительно лучше | |||||
| Maziéres et al. [2007] | Индекс Лекена (изменение от исходного уровня) | CS по сравнению с плацебо | РКИ ( n = 307) ОА коленного сустава 6 месяцев (конец лечения) | NS | |||||
| Изменение структуры | |||||||||
| Reichenbach et al. [2007] | Минимум JSW | CS по сравнению с плацебо / без лечения | MA, 5 РКИ, N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | ES средняя разница 0 .16 мм, 95% ДИ 0,08–0,24 | |||||
| Благоприятствует хондроитину | |||||||||
| Среднее значение JSW | CS по сравнению с плацебо / без лечения | MA, 5 N = 1192, ОА коленного и тазобедренного суставов, продолжительность исследования от 6 до 132 недель | ES средняя разница 0,23, 95% ДИ 0,09–0,37 | ||||||
| Поддерживает хондроитин | |||||||||
| Кахан и другие. [2009] | Минимальный JSW | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | Повышение эффекта лечения со временем | |||||
| CS значительно лучше для JSW | |||||||||
| Lee et al. [2010] | Минимальный JSN | CS по сравнению с плацебо | MA, 4 РКИ, N = 1088, ОА коленного сустава, период наблюдения от 1 до 2 лет | Небольшой, но значительный защитный эффект CS через 2 лет на минимуме JSN | |||||
| Hochberg [2010] | Минимум JSW | MA, 3 РКИ, N = 1179, Коленный остеоартрит, последующее наблюдение 2 года | Значительное снижение скорости уменьшения суставной щели ширина с CS | ||||||
| ES 0.23 (95% ДИ 0,11–0,35) | |||||||||
| Неблагоприятные события | |||||||||
| Maziéres et al. [2007] | Количество пациентов по крайней мере с одним НЯ, связанным с лечением | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | NS | |||||
| Всего количество НЯ | CS по сравнению с плацебо | РКИ, N = 307, ОА коленного сустава, 24 недели | N = 18 (CS) и N = 20 (плацебо) NS | ||||||
| Reichenbach et al. [2007] | Пациенты с НЯ | CS по сравнению с плацебо / без лечения | MA, 12 РКИ, N = 1929, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | |||||
| Исключение из-за НЯ | Хондроитин по сравнению с плацебо / отсутствие лечения | МА, 9 РКИ, N = 1781, ОА коленного и тазобедренного суставов, диапазон продолжительности исследований от 6 до 132 недель | NS | ||||||
| Пациенты с тяжелыми НЯ | Хондроитин vs. плацебо / без лечения | MA, 2 РКИ, N = 217, ОА коленного и тазобедренного суставов, продолжительность исследований от 6 до 132 недель | NS | ||||||
| Kahan et al. [2009] | Исключение из-за НЯ | CS по сравнению с плацебо | РКИ ( N = 622), ОА коленного сустава, последующее наблюдение 2 года | NS |
Сообщалось о глобальных клинических испытаниях a благотворное влияние CS на боль и функцию (). Однако в самом крупном исследовании GAIT не сообщалось о влиянии на эти конечные точки.
Эффекты модификации структуры
Эффекты модификации структуры CS были описаны и проанализированы в двух недавних метаанализах [Hochberg, 2010; Ли и др. 2010]. Ранее сообщалось, что не было неоднородности в результатах РКИ по эффектам модификации структуры [Hochberg et al. 2008]. Результаты показали небольшое, но значительное снижение ухудшения JSN (ES = 0,26, 95% ДИ 0,16–0,36). Недавно при наблюдении за пациентами в течение 2 лет было выявлено значительное влияние CS на JSN у пациентов, получавших CS, по сравнению с плацебо [Kahan et al. 2009].
Безопасность и переносимость
В большинстве клинических испытаний сообщалось о прекрасном профиле безопасности и хорошей переносимости CS. Частота побочных эффектов и частота отказов были эквивалентны в группах CS и плацебо. При применении CS не наблюдалось серьезных серьезных побочных эффектов. Спасательные препараты (парацетамол или нестероидные противовоспалительные препараты [НПВП]) разрешены во время клинических испытаний. Этот факт может уменьшить разницу между группами CS и плацебо [Monfort et al. 2008a] ().
Хондроитинсульфат в рекомендациях
CS рекомендован в руководствах, опубликованных OARSI и Европейской лигой против ревматизма (EULAR) для лечения ОА коленного сустава [Zhang et al. 2008; Jordan et al. 2003]. OARSI рекомендует CS из-за его симптоматического и структурно-модифицирующего эффекта при ОА коленного сустава, но также рекомендует прекратить его через 6 месяцев, если симптоматическая реакция отсутствует. Что касается ОА бедра и кисти, EULAR рекомендует SYSADOA, включая CS, из-за их симптоматических эффектов и низкой токсичности, но подчеркивает тот факт, что ES небольшие, подходящие пациенты не определены должным образом, а клинически значимая модификация структуры и фармакоэкономический аспект не очень хорошо установлено.
Обсуждение
CS используется уже несколько десятилетий, и было важно описать его фармакокинетику, механизм действия и описать его клиническую эффективность.
CS обладает различными эффектами, от противовоспалительных и антикатаболических до антиапоптотических, а также антиоксидантных свойств. Все эти результаты были получены в разных системах с разными дозировками. Во многих обзорах говорится о важности источника CS и чистоты [Lauder, 2009; Рейнсфорд, 2009 г .; Вольпи, 2009; Лаудер и др. 2000]. Кроме того, сульфатированный CS в разных положениях (например, 4 или 6) может иметь разные эффекты. Например, CS-4 более эффективен как антиоксидант, чем CS-6 [Albertini et al. 2000; Volpi, Tarugi, 1999]. Исследования in vitro и in vivo имеют ограничения, в основном из-за используемой концентрации и продолжительности исследования. CS используется в концентрациях, которые значительно превосходят плазменную концентрацию после перорального введения терапевтической дозы CS. Действительно, CS достиг концентрации в плазме примерно 2.0 мкг / мл у пациентов с ОА после перорального введения 0,8 г CS [Conte et al. 1995]. Это исследование также показало, что CS может достигать 2,7 мг / мл в синовиальной жидкости пациентов с ОА. Другой эксперимент на крысах после перорального введения (16 мг / кг) показал концентрацию 3,3 мг / г в хрящах [Ronca et al. 1998]. В большинстве исследований in vitro использовалось от 10 мг / мл CS до 1000 мг / мл (см.). При интерпретации данных необходимо учитывать условия исследования. Наконец, недавно был проведен обзор эффективности КС при воспалительных состояниях, отличных от ОА, и в основном более тяжелых, чем ОА [Vallières and du Souich, 2010; du Souich et al. 2009]. Было показано, что CS эффективен при патологии, включая псориаз [Möller et al. 2010; Verges et al. 2005]. Это предполагает сильную противовоспалительную активность CS. К сожалению, отсутствие inivo демонстрации влияния CS на прогрессирование ОА. Только в одном исследовании изучалось влияние хондроитина на модель ОА. Для лучшего понимания клинической эффективности CS необходимы дальнейшие исследования, изучающие влияние CS на деградацию хряща, ремоделирование субхондральной кости и воспаление синовиальной оболочки.
CS рекомендуется OARSI в качестве вмешательства SYSADOA для лечения ОА [Zhang et al. 2010, 2008] и EULAR [Jordan et al. 2003]. Обе организации признали его симптоматические и структурно-модифицирующие эффекты. OARSI рекомендует прекратить лечение через 6 месяцев при отсутствии эффективности [Zhang et al. 2008]. В то время, когда EULAR опубликовал свои рекомендации, они предложили растущие доказательства эффективности CS. Однако ко времени последнего обновления OARSI [Zhang et al. 2010], ES снизился, что свидетельствует о нестабильности эффективности, что, по крайней мере частично, может быть связано с повышением качества исследований. Несоответствие эффективности, показанное в нескольких клинических испытаниях, имеет большое значение. Этот метаанализ [Zhang et al. 2010] также продемонстрировал серьезную предвзятость публикации. Эти наблюдения также сделаны для других соединений класса SYSADOA, включая сульфат глюкозамина (GS). Напротив, ES для ацетаминофена, хотя и очень маленький, по-видимому, со временем стабилизировался, что позволяет предположить, что дальнейших РКИ для проверки его анальгетической эффективности не требовалось.В целом, этот обзор указывает на то, что существует потребность в клинических испытаниях хорошего качества с продолжительностью и количеством пациентов, соответствующих этому виду соединений. Также уместно сравнить ES для боли основных фармакологических методов, обычно используемых при лечении ОА. Для сравнения, ЭС CS — одна из самых важных. Например, болевой синдром ES (2010 г.) для ацетаминофена составил 0,14 (95% 0,05–0,23), для НПВП 0,29 (95% 0,22–0,35) и для CS 0,75 (95% 0,50–1,01). Это говорит о клинической значимости использования CS для лечения ОА, учитывая его низкую токсичность. ОА является долгосрочным прогрессирующим заболеванием, для которого перед применением каждого лечения должна быть проведена оценка соотношения риск / польза.
В некоторых исследованиях оценивалась эффективность использования CS в сочетании с GS. Это было сделано in vitro [Chan et al. 2006, 2007, 2005a, 2005b], а также в клинических испытаниях [Vangsness et al. 2009; Sawitzke et al. 2008; Clegg et al. 2006, 2005]. Синергетический эффект обоих соединений еще предстоит продемонстрировать, но многие авторы рекомендуют использовать комбинацию.
Одна из причин для оптимизма в отношении использования CS отдельно или в сочетании со связанным продуктом, таким как GS, — это профиль безопасности.CS не взаимодействует с другими лекарствами и не вызывает серьезных побочных эффектов. Это говорит в пользу положительного соотношения риск / польза.
Заключение
Несмотря на умеренное влияние CS на боль и функцию, CS представляет собой интересный продукт для лечения ОА коленного сустава. Клинические данные свидетельствуют в пользу медленного действия на симптомы умеренного ОА коленного сустава. CS рекомендуется по самым популярным рекомендациям. Его профиль безопасности, несомненно, является одним из основных преимуществ при лечении стареющих пациентов с некоторыми сопутствующими заболеваниями.Таким образом, нет никаких ограничений для его использования у пациентов с ОА, если не учитывать экономический эффект. Тем не менее, следует проявлять осторожность в отношении типа и состава CS. Конечно, остаются вопросы относительно механизма его действия. Эффект CS на воспаление субхондральной кости и синовиальной оболочки может быть лучше документирован.
Благодарности
Авторы благодарят L. Montell Bonaventura и J. Verges из Bioiberica, любезно предоставившие документацию по хондроитинсульфату.К. Санчес — научный сотрудник Национального фонда научных исследований (FNRS, Бельгия).
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Проф. Хенротин получил образовательные и исследовательские гранты от Bioiberica, Expanscience, Danone, Nestec и BioXtract.
Ссылки
- Альбертини Р., Пасси А., Абуджа П.М., Де Лука Г. (2000) Влияние гликозаминогликанов и протеогликанов на перекисное окисление липидов.Инт Дж Мол Мед 6: 129–136 [PubMed] [Google Scholar]
- Barnhill J.G., Fye C.L., Williams D.W., Reda D.J., Harris C.L., Clegg D.O. (2006) Выбор хондроитинового продукта для интервенционного исследования артрита глюкозамином / хондроитином. J Am Pharm Assoc (Вашингтон, Вашингтон) 46: 14–24 [PubMed] [Google Scholar]
- Bassleer C.T., Combal J.P., Bougaret S., Malaise M. (1998) Влияние хондроитинсульфата и интерлейкина-1 бета на суставные хондроциты человека, культивируемые в кластерах. Остеоартроз Хрящ 6: 196–204 [PubMed] [Google Scholar]
- Биан Л., Каплун М., Уильямс Д.Ю., Сюй Д., Атешян Г.А., Хунг С.Т. (2009) Влияние хондроитинсульфата на биохимические, механические и фрикционные свойства хрящевых эксплантатов при длительном культивировании. J Биомеханика 42: 286–290 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Ferlazzo AM, Calatroni A. (2004) Уменьшение фрагментации ДНК и производство гидроксильных радикалов гиалуроновой кислотой и хондроитин-4-сульфатом в железе плюс индуцированный аскорбатом окислительный стресс в культурах фибробластов.Free Radic Res 38: 601–611 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., D’Ascola A., Traina P., Calatroni A. (2008) Хондроитин-4-сульфат ингибирует NF-kB транслокация и активация каспаз при коллаген-индуцированном артрите у мышей. Остеоартроз Хрящ 16: 1474–1483 [PubMed] [Google Scholar]
- Кампо Г.М., Авенозо А., Кампо С., Д’Аскола А., Трэйна П., Сама Д. и др. (2009a) Гликозаминогликаны модулируют воспаление и апоптоз в хондроцитах, обработанных LPS.J Cell Biochem 106: 83–92 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Ferlazzo AM, Altavilla D., Calatroni A. (2003) Эффективность лечения гликозаминогликанами экспериментального коллаген-индуцированного артрита в крысы. Артрит Res Ther 5: R122 – R131 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006a) Антиоксидантная активность хондроитинсульфата. Adv Pharmacol 53: 417–431 [PubMed] [Google Scholar]
- Кампо Г.М., Авеносо А., Кампо С., Ферлаццо А.М., Калатрони А. (2006b) Хондроитинсульфат: антиоксидантные свойства и положительные эффекты. Мини Рев Мед Хим 6: 1311–1320 [PubMed] [Google Scholar]
- Campo GM, Avenoso A., Campo S., Traina P., D’Ascola A., Calatroni A. (2009b) Гликозаминогликаны снижают воспалительную реакцию, модулируя толл-подобные рецептор-4 в хондроцитах, стимулированных ЛПС. Arch Biochem Biophys 491: 7–15 [PubMed] [Google Scholar]
- Caraglia M., Beninati S., Giuberti G., Д’Алессандро А.М., Лентини А., Аббруззезе А. и др. (2005) Альтернативная терапия земными элементами усиливает хондрозащитные эффекты хондроитинсульфата у мышей. Exp Mol Med 37: 476–481 [PubMed] [Google Scholar]
- Катерсон Б., Махмудиан Ф., Соррелл Дж. М., Хардингем Т. Э., Бейлисс М. Т., Карни С. Л. и др. (1990) Модуляция структуры нативного хондроитинсульфата в развитии тканей и при заболеваниях. J Cell Sci 97: 411–417 [PubMed] [Google Scholar]
- Чан П.С., Кэрон Дж.P., Orth M.W. (2005a) Влияние глюкозамина и хондроитинсульфата на регуляцию экспрессии генов протеолитических ферментов и их ингибиторов в эксплантатах суставного хряща быка, зараженных интерлейкином-1. Am J Vet Res 66: 1870–1876 [PubMed] [Google Scholar]
- Chan P.S., Caron J.P., Orth M.W. (2006) Кратковременные изменения экспрессии генов в хрящевых эксплантатах, стимулированные интерлейкином бета, глюкозамином и хондроитинсульфатом. J Ревматол 33: 1329–1340 [PubMed] [Google Scholar]
- Чан П.С., Карон Дж. П., Орт М. В. (2007) Влияние глюкозамина и хондроитинсульфата на эксплантаты бычьего хряща в условиях длительного культивирования. Am J Vet Res 68: 709–715 [PubMed] [Google Scholar]
- Chan PS, Caron JP, Rosa GJ, Orth MW (2005b) Глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простагландина E (2) в эксплантатах суставного хряща. . Остеоартроз Хрящ 13: 387–394 [PubMed] [Google Scholar]
- Чо С. Ю., Сим Дж.С., Чжон С. С., Чанг С. Ю., Чой Д. В., Тойда Т. и др. (2004) Влияние низкомолекулярного хондроитинсульфата на индуцированный коллагеном артрит типа II у мышей DBA / 1J. Биол Фарм Булл 27: 47–51 [PubMed] [Google Scholar]
- Chou M.M., Vergnolle N., McDougall J.J., Wallace J.L., Marty S., Teskey V. и др. (2005) Влияние хондроитина и сульфата глюкозамина в составе диетического батончика на воспаление, интерлейкин-1бета, матриксную металлопротеазу-9 и повреждение хряща при артрите. Эксп Биол Мед 230: 255–262 [PubMed] [Google Scholar]
- Клегг Д.О., Реда Д.Дж., Харрис К.Л., Кляйн М.А. (2005) Эффективность глюкозамина и хондроитинсульфата у пациентов с болезненным остеоартритом (ОА) коленного сустава: исследование вмешательства глюкозамина / хондроитина. Ревматоидный артрит 52 (9S): S256, (Аннотация). [Google Scholar]
- Clegg D.O., Reda D.J., Harris C.L., Klein M.A., O’Dell J.R., Hooper M.M., et al. (2006) Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med 354: 795–808 [PubMed] [Google Scholar]
- Конте А., Volpi N., Palmieri L., Bahous I., Ronca G. (1995) Биохимические и фармакокинетические аспекты перорального лечения хондроитинсульфатом. Arzneimittelforschung 45: 918–925 [PubMed] [Google Scholar]
- David-Raoudi M., Deschrevel B., Leclercq S., Galera P., Boumediene K., Pujol JP (2009) Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальная регуляция гиалуронансинтаз: роль p38 и Akt. Ревматоидный артрит 60: 760–770 [PubMed] [Google Scholar]
- du Souich P., Гарсия А.Г., Верджес Дж., Монтелл Э. (2009) Иммуномодулирующие и противовоспалительные эффекты хондроитинсульфата. J Cell Mol Med 13 (8A): 1451–1463 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- du Souich P., Verges J. (2001) Простой подход для прогнозирования максимального эффекта, вызываемого лекарством, когда концентрации в плазме недоступны или диссоциируют от воздействия, как показано на данных по хондроитинсульфату. Clin Pharmacol Ther 70: 5–9 [PubMed] [Google Scholar]
- Эгеа Дж., Гарсия А.Г., Верджес Дж., Монтелл Э., Лопес М.Г. (2010) Антиоксидантное, противовоспалительное и нейропротекторное действие хондроитинсульфата и протеогликанов. Остеоартроз Хрящ 18 (Приложение 1): S24 – S28 [PubMed] [Google Scholar]
- Hochberg M.C. (2010) Структурно-модифицирующие эффекты хондроитинсульфата при остеоартрите коленного сустава: обновленный метаанализ рандомизированных плацебо-контролируемых исследований продолжительностью 2 года. Остеоартроз Хрящ 18 (Приложение 1): 528–531 [PubMed] [Google Scholar]
- Hochberg M.К., Клегг Д.О. (2008) Потенциальные эффекты хондроитинсульфата на отек суставов: отчет GAIT. Остеоартроз Хрящ 16 (Приложение 3): S22 – S24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hochberg MC, Zhan M., Langenberg P. (2008) Скорость уменьшения ширины суставной щели у пациентов с остеоартритом колено: систематический обзор и метаанализ рандомизированных плацебо-контролируемых исследований хондроитинсульфата. Curr Med Res Opin, в печати. [PubMed] [Google Scholar]
- Holzmann J., Брандл Н., Земанн А., Шабус Р., Марловиц С., Коуберн Р. и др. (2006) Различные эффекты TGFbeta и хондроитинсульфата на уровни активации p38 и ERK1 / 2 в суставных хондроцитах человека, стимулированных LPS. Остеоартроз Хрящ 14: 519–525 [PubMed] [Google Scholar]
- Имада К., Ока Х., Кавасаки Д., Миура Н., Сато Т., Ито А. (2010) Механизмы антиартритного действия природного хондроитинсульфата у человека суставные хондроциты и синовиальные фибробласты. Биол Фарм Булл 33: 410–414 [PubMed] [Google Scholar]
- Джексон К.Г., Плаас А.Х., Сэнди Дж. Д., Хуа С., Ким-Роландс С., Барнхилл Дж. Г. и др. (2010) Фармакокинетика перорального приема глюкозамина и хондроитинсульфата у человека по отдельности или в комбинации. Остеоартроз Хрящ 18: 297–302 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Jomphe C.j, Gabriac M., Hale T.M., Heroux L., Trudeau L.E., Deblois D., et al. (2008) Хондроитинсульфат ингибирует ядерную транслокацию ядерного фактора-каппаВ в хондроцитах, стимулированных интерлейкином-1бета.Базовый Clin Pharmacol Toxicol 102: 59–65 [PubMed] [Google Scholar]
- Jordan K.M., Arden N.K., Doherty M., Bannwarth B., Bijlsma J.W., Dieppe P., et al. (2003) Рекомендации EULAR 2003: научно обоснованный подход к лечению остеоартрита коленного сустава: отчет рабочей группы Постоянного комитета по международным клиническим исследованиям, включая терапевтические испытания (ESCISIT). Энн Рум Дис 62: 1145–1155 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Kahan A., Uebelhart D., De Vathaire F., Дельмас П.Д., Регинстер Дж. (2009) Долгосрочные эффекты хондроитинов 4 и 6 сульфата на остеоартрит коленного сустава: исследование по предотвращению прогрессирования остеоартрита, двухлетнее рандомизированное двойное слепое плацебо-контролируемое исследование. Ревматоидный артрит 60: 524–533 [PubMed] [Google Scholar]
- Катта Дж., Джин З., Ингам Э., Фишер Дж. (2009) Хондроитинсульфат: эффективная смазка для суставов? Остеоартроз Хрящ 17: 1001–1008 [PubMed] [Google Scholar]
- Кусано С., Отани А., Сакаи С., Игараси Н., Такегучи А., Тойода Х. и др. (2007) Определение хондрозина в плазме крови мышей с помощью ВЭЖХ после внутривенной или пероральной дозы. Биол Фарм Булл 30: 1365–1368 [PubMed] [Google Scholar]
- Лаудер Р.М. (2009) Хондроитинсульфат: сложная молекула с потенциальным воздействием на широкий спектр биологических систем. Комплемент Терапии Мед 17: 56–62 [PubMed] [Google Scholar]
- Лаудер Р.М., Хакерби Т.Н., Недушинский Л.А. (2000) Метод снятия отпечатков пальцев на хондроитин / дерматансульфат и гиалуронановые олигосахариды.Гликобиология 10: 393–401 [PubMed] [Google Scholar]
- Ли Й.Х., Ву Дж.Х., Чой С.Дж., Джи Дж.Д., Сон Г.Г. (2010) Влияние глюкозамина или хондроитинсульфата на прогрессирование остеоартрита: метаанализ. Ревматол Инт 30: 357–363 [PubMed] [Google Scholar]
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. (2000) Метаанализ хондроитинсульфата в лечении остеоартрита. J Ревматол 27: 205–211 [PubMed] [Google Scholar]
- Legendre F., Bauge C, Roche R., Saurel A.S., Pujol J.P. (2008) Хондроитинсульфатная модуляция матрикса и экспрессия воспалительных генов в IL-lbeta-стимулированных хондроцитах — исследование в культурах гипоксических альгинатных гранул. Остеоартроз Хрящ 16: 105–114 [PubMed] [Google Scholar]
- Малаваки С.Дж., Асимакопулу А.П., Ламари Ф.Н., Теохарис А.Д., Цанакакис Г.Н., Караманос Н.К. (2008) Капиллярный электрофорез для контроля качества хондроитинсульфатов в сырье и рецептурах. Анальный биохим 374: 213–220 [PubMed] [Google Scholar]
- Mazieres B., Хучер М., Заим М., Гарнеро П. (2007) Эффект хондроитинсульфата при симптоматическом остеоартрите коленного сустава: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. Энн Рум Дис 66: 639–645 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mazieres B., Hucher M.M.H., Zam M.M.Z. (2006) Хондроитинсульфат в лечении остеоартрита коленного сустава: рандомизированное двойное слепое многоцентровое плацебо-контролируемое исследование. Энн Рум Дис 65 (Дополнение II): 398. [Google Scholar]
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. (2000) Глюкозамин и хондроитин для лечения остеоартрита: систематическая оценка качества и метаанализ. JAMA 283: 1469–1475 [PubMed] [Google Scholar]
- Möller I., Pérez M., Monfort J., Benito P., Cuevas J., Perna C., et al. (2010) Эффективность хондроитинсульфата у пациентов с сопутствующим остеоартритом коленного сустава и псориазом: рандомизированное двойное слепое плацебо-контролируемое исследование. Остеоартроз Хрящ 18 (Приложение 1): 532–540 [PubMed] [Google Scholar]
- Monfort J., Martel-Pelletier J., Pelletier J.P. (2008a) Хондроитинсульфат при симптоматическом остеоартрите: критическая оценка метаанализов. Curr Med Res Opin 24: 1303–1308 [PubMed] [Google Scholar]
- Monfort J., Nacher M., Montell E., Vila J., Verges J., Benito P. (2005) Хондроитинсульфат и гиалуроновая кислота (500–730 кДа ) подавляют синтез стромелизина-1 в хондроцитах человека, страдающих остеоартритом. Наркотики Exp Clin Res 31: 71–76 [PubMed] [Google Scholar]
- Monfort J., Pelletier J.P., Garcia-Giralt N., Martel-Pelletier J. (2008b) Биохимические основы действия хондроитинсульфата на суставные ткани при остеоартрозе. Энн Рум Дис 67: 735–740 [PubMed] [Google Scholar]
- Mourao P.A. (1988) Распределение хондроитин-4-сульфата и хондроитин-6-сульфата в суставном и ростовом хряще человека. Ревматоидный артрит 31: 1028–1033 [PubMed] [Google Scholar]
- Omata T., Itokazu Y., Inoue N., Segawa Y. (2000) Эффекты хондроитинсульфата-C на разрушение суставного хряща при артрите, индуцированном мышиным коллагеном.Arzneimittelforschung 50: 148–153 [PubMed] [Google Scholar]
- Rainsford K.D. (2009) Важность фармацевтического состава и данных клинических испытаний и фармакологических исследований в определении эффективности хондроитинсульфата и других гликозаминогликанов: критический анализ. J Pharm Pharmacol 61: 1263–1270 [PubMed] [Google Scholar]
- Reichenbach S., Sterchi R., Scherer M., Trelle S., Burgi E., Burgi U., et al. (2007) Мета-анализ: хондроитин при остеоартрите коленного или тазобедренного суставов.Энн Интерн Мед 146: 580–590 [PubMed] [Google Scholar]
- Ричи Ф., Брюйер О., Этген О., Кучерат М., Хенротин Ю., Регинстер Дж. Я. (2003) Структурная и симптоматическая эффективность глюкозамина и хондроитина при остеоартрите коленного сустава: всесторонний метаанализ. Arch Intern Med 163: 1514–1522 [PubMed] [Google Scholar]
- Ronca F., Palmieri L., Panicucci P., Ronca G. (1998) Противовоспалительная активность хондроитинсульфата. Остеоартроз Хрящ 6 (Приложение A): 14–21 [PubMed] [Google Scholar]
- Sawitzke A.Д., Ши Х., Финко М.Ф., Данлоп Д.Д., Бингем С.О., III, Харрис К.Л. и др. (2008) Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Ревматоидный артрит 58: 3183–3191 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Шварц Н.Б., Дорфман А. (1975) Стимуляция продукции хондроитинсульфат-протеогликана хондроцитами в монослое. Подключите ткань Res 3: 115–122 [PubMed] [Google Scholar]
- Shinmei M., Мияучи С., Мачида А., Миядзаки К. (1992) Количественное определение хондроитин-4-сульфата и хондроитин-6-сульфата в патологической суставной жидкости. Ревматоидный артрит 35: 1304–1308 [PubMed] [Google Scholar]
- Тахири К., Корвин-Змиевска С., Ришетт П., Херо Ф., Шевалье Х., Савуре Дж. Ф. и др. (2008) Природные хондроитинсульфаты увеличивают агрегацию протеогликановых комплексов и снижают экспрессию ADAMTS-5 в хондроцитах, обработанных интерлейкином 1 бета. Энн Рум Дис 67: 696–702 [PubMed] [Google Scholar]
- Тат С.K., Pelletier J.P., Mineau F., Duval N., Martel-Pelletier J. (2010) Различные эффекты 3 различных соединений хондроитинсульфата на хрящ / хондроциты человека при остеоартрите: важность чистоты и производственного процесса. J Ревматол 37: 656–664 [PubMed] [Google Scholar]
- Tat S.K., Pelletier J.P., Verges J., Montell E., Lajeunesse D., Fahmi H., et al. (2007) Хондроитин и сульфат глюкозамина в комбинации снижают прорезорбтивные свойства субхондральных костных остеобластов человека.Артрит Res Ther 9: R117. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Uebelhart D., Thonar EJ, Zhang J., Williams JM (1998) Защитный эффект экзогенного хондроитин-4,6-сульфата при острой деградации суставного хряща у кролика . Остеоартроз Хрящ 6 (Suppl. A): 6–13 [PubMed] [Google Scholar]
- Валлиер М., дю Суич П. (2010) Модуляция воспаления с помощью хондроитинсульфата. Остеоартроз Хрящ 18 (Приложение 1): S1 – S6 [PubMed] [Google Scholar]
- Вангснесс К.Т., младший, Спайкер В., Эриксон Дж. (2009) Обзор доказательной медицины использования глюкозамина и хондроитинсульфата при остеоартрите коленного сустава. Артроскопия: J Arthroscopic Relat Surg 25: 86–94 [PubMed] [Google Scholar]
- Verbruggen G., Veys E.M. (1977) Влияние сульфатированных гликозаминогликанов на метаболизм протеогликанов в клетках синовиальной оболочки. Acta Rhumatol Belg 1: 75–92 [PubMed] [Google Scholar]
- Verges J., Montell E., Herrero M., Perna C, Cuevas J., Perez M., et al.(2005) Клиническое и гистопатологическое улучшение псориаза при пероральном приеме хондроитинсульфата: случайная находка. Дерматол Интернет J 11: 31. [PubMed] [Google Scholar]
- Vergés J., Montell E., Martinez G., Heroux L., du Souich P. (2004) Хондроитинсульфат снижает фактор ядерной транслокации NF-kappaB и не изменяет состояние активации активирующего белка-1 (AP-1). Остеоартроз Хрящ 12: 194, (Аннотация). [Google Scholar]
- Volpi N. (2002) Пероральная биодоступность хондроитинсульфата (Кондросульф) и его компонентов у здоровых добровольцев мужского пола.Остеоартроз Хрящ 10: 768–777 [PubMed] [Google Scholar]
- Volpi N. (2003) Пероральное всасывание и биодоступность хондроитинсульфата ихтикового происхождения у здоровых добровольцев мужского пола. Остеоартроз Хрящ 11: 433–441 [PubMed] [Google Scholar]
- Volpi N. (2006a) Достижения в анализе хондроитинсульфата: применение при физиологических и патологических состояниях соединительной ткани и при фармакологическом лечении остеоартрита. Curr Pharm Des 12: 639–658 [PubMed] [Google Scholar]
- Volpi N.(2006b) Хондроитинсульфат: структура, роль и фармакологическая активность, Elsevier: Amsterdam [Google Scholar]
- Volpi N. (2009) Качество различных препаратов хондроитинсульфата в зависимости от их терапевтической активности. J Pharm Pharmacol 61: 1271–1280 [PubMed] [Google Scholar]
- Volpi N., Tarugi P. (1999) Влияние плотности заряда хондроитинсульфата, положения сульфатной группы и молекулярной массы на Cu2 + -опосредованное окисление липопротеинов низкой плотности человека: действие нормального человеческого хондроитинсульфата плазмы.J Biochem 125: 297–304 [PubMed] [Google Scholar]
- Wang L., Wang J., Almqvist KF, Veys EM, Verbruggen G. (2002) Влияние полисульфатированных полисахаридов и гидрокортизона на метаболизм внеклеточного матрикса суставных хондроцитов человека в пробирка. Clin Exp Rheumatol 20: 669–676 [PubMed] [Google Scholar]
- Zhang W., Doherty M., Arden N., Bannwarth B., Bijlsma J., Gunther K.P., et al. (2005) Основанные на фактических данных рекомендации EULAR по лечению остеоартрита тазобедренного сустава: отчет рабочей группы Постоянного комитета EULAR по международным клиническим исследованиям, включая терапию (ESCISIT).Энн Рум Дис 64: 669–681 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Чжан В., Московиц Р. В., Нуки Г., Абрамсон С., Альтман Р. Д., Арден Н. и др. (2008) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, Часть II: Основанные на фактах, согласованные экспертные рекомендации OARSI. Остеоартроз Хрящ 16: 137–162 [PubMed] [Google Scholar]
- Чжан В., Нуки Г., Московиц Р. В., Абрамсон С., Альтман Р. Д., Арден Н. К. и др. (2010) Рекомендации OARSI по лечению остеоартроза тазобедренного и коленного суставов, часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г.Остеоартроз Хрящ 18 (4): 476–499 [PubMed] [Google Scholar]
Хондроитинсульфат — обзор
4.3.2.2 Производные CS и их сочетание с другими полимерами
CS представляет собой водорастворимый полимер. Ранние попытки использования CS в качестве носителя для доставки лекарств в толстую кишку сшивали полимер в разной степени для получения биоразлагаемой системы для контролируемого высвобождения модельных лекарств, индометацина. Возникла линейная корреляция между степенью перекрестного сшивания и скоростью высвобождения лекарственного средства, что указывает на то, что уровень перекрестного сшивания CS может использоваться для регулирования кинетики доставки лекарственного средства [69,70].Тем не менее, поперечное сшивание CS используется как стратегия уменьшения растворения CS в воде. Например, обработка водорастворимого полимера CS с различными пропорциями триметафосфата натрия приводит к сшиванию CS и снижению растворимости при использовании полимера для доставки лекарств [71].
В основном из-за своей водорастворимой природы и отсутствия механической стабильности CS был модифицирован или использован вместе с другими полимерами для доставки лекарств и тканевой инженерии.Пористая губка из CS-хитозана использовалась для доставки тромбоцитарного фактора роста (PDGF), направленного на достижение большей регенерации кости. Водный раствор CS-хитозана подвергали сублимационной сушке с последующим сшиванием с образованием пористой губки с размером пор 100-150 мкм. PDGF-BB вводили в губку из CS-хитозана путем замачивания губки из CS-хитозана в растворе PDGF-BB. Количество CS может действовать как фактор, контролирующий высвобождение PDGF-BB из губки [72]. Также было замечено, что присутствие CS увеличивало остеокондуктивные характеристики материала.Следовательно, биоактивный CS можно использовать в сочетании с другими полимерами в составе материалов для доставки факторов роста.
Поскольку CS выполняет полезные биологические функции и представляет собой водорастворимый и ферментативно биоразлагаемый полисахарид, его использовали в сочетании с такими материалами, как коллаген, при приготовлении матриц каркасов. Добавление CS к матрице коллагена I типа было достигнуто с использованием 1-этил-3- (3-диметиламинопропил) карбодиимида в качестве сшивающего агента.Связанная с CS матрица обладает повышенной способностью связывать воду с уменьшением прочности на разрыв и температуры денатурации [72]. Помимо придания каркасу полезных биологических свойств, CS также предоставил возможность контролировать механические характеристики каркаса и характеристики разложения.
Как объяснялось в предыдущем разделе, CS является важным компонентом суставного ECM и, как известно, играет решающую роль в развитии и улучшении патологий суставов / хрящей. Следовательно, он широко используется в инженерии костно-хрящевой ткани.Здесь снова ряд вариантов CS, таких как модифицированный CS или CS в комбинации с другими природными и / или синтетическими полимерами, был использован для составления каркасов. Использовались строительные леса разных форматов. Как волокнистые губчатые каркасы, так и каркасы из гидрогеля были созданы с использованием CS. При использовании CS в сочетании с коллагеном I типа в виде волокнистого губчатого матрикса было замечено явное преимущество в пролиферации хондроцитов и поддержании фенотипа [73]. Аналогичным образом были синтезированы губки с диаметром пор 180 мкм с использованием вместе природных полимеров желатина, CS и HA.Когда эти каркасы были засеяны хондроцитами, они сохраняли свою морфологию до 5 недель и демонстрировали более высокие уровни продукции аггрекана, чем каркасы, которые не содержали компонентов CS и HA. Эти исследования in vitro и ясно указывают на потенциал каркасов, включающих CS, для инженерии хрящевой ткани [74,75].
Ряд гидрогелевых каркасов был также разработан с использованием CS для хрящей. Хондроциты имеют округлую морфологию, и это, как видно, лучше всего сохраняется в гидрогелях, поэтому гидрогелевые каркасы являются идеальным вариантом для регенерации хряща.Полимеры, такие как PEG, поливиниловый спирт (PVA) и поли (3-гидроксибутират) (PHB), были использованы с CS для создания гидрогелей. Хотя гидрогели PVA сами по себе не могут поддерживать адгезию клеток, добавление CS снижает крайнюю гидрофильность гидрогеля и способствует большему прикреплению клеток к каркасу [76]. Когда CS, содержащий гидрогель коллагена, был конъюгирован с тканью PHB, он показал больший остеогенный потенциал, чем исходная ткань, на засеянных остеобластах [77]. Присутствие CS в гидрогелях PEG способствовало хондрогенной дифференцировке засеянных мезенхимальных стволовых клеток костного мозга, но не позволяло им перейти в гипертрофическое состояние.Это был оптимальный результат, подходящий для дифференцировки хондроцитов и достижения регенерации хряща [78]. В недавнем исследовании основная цепь полисахарида была модифицирована метакрилатными и альдегидными группами с образованием адгезивного геля. Эта модификация привела к лучшей интеграции гидрогеля с имплантированной тканью in vivo , как видно на модели крысы. Это произошло из-за большего взаимодействия каркас-белок, вызванного добавлением модифицированного CS [79]. Были предприняты усилия по доставке CS с использованием принципов строительных лесов в суставы, пораженные остеоартрозом.Например, каркас с 40% хитозана и 60% CS был разработан, чтобы служить носителем CS, который оказался эффективным [80]. Следовательно, CS сам по себе после определенных модификаций и в сочетании с другими синтетическими и природными полимерами имеет большой потенциал в качестве каркаса и доставки лекарств для костно-хрящевой регенерации.
Для внутрисуставной доставки хондроитинсульфата | Гликобиология
На данный момент не существует эффективного лечения, которое могло бы остановить патологический процесс остеоартрита (ОА), и лечение болезни в основном основано на облегчении клинических симптомов с помощью нестероидных противовоспалительных препаратов (НПВП) и анальгетиков.Тем не менее, некоторые натуральные продукты были предложены в качестве симптоматического лечения и названы симптоматическими лекарствами, модифицирующими болезнь с медленным действием (SYSADOA). Они включают сульфат глюкозамина (GS), сульфат хондроитина (CS), гиалуронан (внутрисуставная инъекция), диацереин и неомыляемые экстракты авокадо / сои. GS и CS продаются без рецепта в Соединенных Штатах, но в некоторых европейских странах они клинически используются как противоартрозные препараты. Однако их клиническая эффективность никогда не была четко продемонстрирована, и недавнее крупномасштабное многоцентровое исследование Glucosamine / chondroitin Arthritis Intervention Trial (GAIT) не показало значительного эффекта CS по сравнению с плацебо (Clegg et al.2006 г.). Также были опубликованы недавние данные, которые ясно демонстрируют, что диетический глюкозамин не может быть непосредственно эффективным в стимуляции синтеза хондроитинсульфата в суставном хряще (Silbert 2009).
CS представляет собой гликозаминогликан (ГАГ), в основном присутствующий в суставном хряще. Он состоит из повторяющихся дисахаридных единиц глюкуроновой кислоты (GlcA) и N, -ацетил-d-галактозамина (GalNAc). Эти анионные компоненты, входящие в состав протеогликанов (PG), способствуют гидратации хряща и его устойчивости к механическому сжатию.Использование КС для улучшения клинических симптомов ОА исторически основывалось на расплывчатых предположениях о том, что введение компонента хрящевого матрикса поможет хондроцитам восполнить утраченную среду (Uebelhart et al. 2006). Некоторые сульфатированные полисахариды также использовались для стимуляции процесса восстановления тканей (Verbruggen and Veys 1977).
Механизмы действия CS на метаболизм хряща изучены недостаточно. Несколько исследований in vitro продемонстрировали, что CS имеет большое влияние как на эксплантаты хряща, так и на изолированные суставные хондроциты.CS стимулирует синтез протеогликанов в хондроцитах крупного рогатого скота и человека (Bassleer et al. 1998; Legendre et al. 2008), тогда как он снижает индуцированную интерлейкином-1β (IL-1β) экспрессию матриксных металлопротеиназ-1, -3 и -13. и аггреканазы-1 и -2 (Chan, Caron, Orth 2005; Montfort et al. 2005; Legendre et al. 2008). Кроме того, CS были приписаны некоторые противовоспалительные свойства, основанные на его способности ингибировать хемотаксис и фагоцитоз лейкоцитов человека, защищать плазматическую мембрану от активных форм кислорода (Ronca et al.1998) и для снижения экспрессии циклооксигеназы-2 (COX-2) и продукции простагландина E 2 хондроцитами (Chan, Caron, Rosa, et al. 2005; Legendre et al. 2008). Недавно было обнаружено, что CS противодействует подавлению экспрессии IL-1β рецепторов трансформирующего фактора роста-β (TGF-β) в хондроцитах (Legendre et al. 2008).
Однако маловероятно, что эти ограниченные хондрозащитные и противовоспалительные свойства могут проявляться in vivo CS на суставной хрящ после перорального введения гликозаминогликана.Фактически, полисахариды плохо всасываются через пищеварительную систему (Baici et al. 1992), и только 12–13% проглоченного CS всасывается в кровоток без изменений (Sakai et al. 2002). Кроме того, период полувыведения CS в кровеносной системе составляет 3-15 минут после внутривенного введения (Sakai et al. 2002). Когда CS вводили пациентам перорально в виде однократной дозы 1200 мг / день, пик времени наблюдался через 4 часа, и была измерена максимальная концентрация в плазме 3,8 ± 0,6 мкг / мл (Ronca et al.1998). Этот уровень ниже концентраций CS, обычно используемых в большинстве опубликованных исследований in vitro. В совокупности эти данные указывают на то, что перорально введенный CS не распределяется систематически на суставной хрящ и что механизм эффекта CS при пероральном лечении ОА, если таковой имеется, может быть опосредован другими путями.
С другой стороны, мы можем предположить, что приведение CS в контакт с суставными клетками может имитировать хондропротекторные и противовоспалительные эффекты CS, наблюдаемые in vitro.Эта точка зрения была недавно подтверждена нашим исследованием, показывающим, что CS также способен увеличивать продукцию высокомолекулярного гиалуронана культивированными синовиальными фибробластами при остеоартрите (рис. 1) (David-Raoudi et al. 2009). Следовательно, разумно предположить, что CS, введенный в синовиальную жидкость, будет находиться в прямом контакте как с синовиоцитами, так и с поверхностными хондроцитами, и, следовательно, будет оказывать такое же действие, что и in vitro. Предоставляя местный источник, можно также исключить необходимость в большом количестве CS.Таким образом, достаточное количество CS может быть доступно и не потеряно при абсорбции в кровоток. В поддержку такого подхода недавно было показано, что внутрисуставная доставка CS эффективна для восстановления дефектов суставов на модели кролика (Hui et al. 2007). Более того, может быть интересно связать CS с уже существующей внутрисуставной доставкой HA. Комбинируя эти два гликозаминогликана, оба из которых обладают умеренными противовоспалительными свойствами (Morreale et al. 1996; Ronca et al.1998; Kydd et al. 2007; Yasuda 2007), возможно дальнейшее улучшение терапевтической эффективности. Более того, этот CS может активировать локальный синтез гиалуронана суставными клетками, вероятно, обеспечит поступление гиалуронана в течение более длительного периода времени, чем однократная инъекция экзогенного гиалуронана, который, как известно, имеет короткий период жизни.
Рис. 1
Типичный хроматографический профиль гиалуронана, продуцируемого фибробластоподобными синовиоцитами ОА (FLS), инкубированных с IL-113 и CS / IL-1R.Культуры FLS предварительно обрабатывали 100 мкг / мл птичьего CS (MW> 18 × 10 3 Да, Pierre Fabre Laboratories, Кастр, Франция) в 10% FCS / DMEM в течение 4 дней, со сменой среды через 2 дня. Затем клетки инкубировали в течение 48 ч с CS в DMEM / 1% ITS (инсулин / трансферрин / селен) и 1 нг / мл IL-1β. Фракционирование и характеризация высвобожденной в среду НА выполняли с использованием 2 колонок Shodex 0Hpak (KB806-KB805) от Showa Denko (Токио, Япония), элюированных 0,15 М NaCl при 35 ° C.Содержание HA во фракциях ВЭЖХ определяли в каждой фракции ВЭЖХ с помощью ELISA, используя HABP (белок, связывающий гиалуроновую кислоту).
Рис. 1
Типичный хроматографический профиль гиалуронана, продуцируемого фибробластоподобными синовиоцитами ОА (FLS), инкубированных с IL-113 и CS / IL-1R. Культуры FLS предварительно обрабатывали 100 мкг / мл птичьего CS (MW> 18 × 10 3 Да, Pierre Fabre Laboratories, Кастр, Франция) в 10% FCS / DMEM в течение 4 дней, со сменой среды через 2 дня. Затем клетки инкубировали в течение 48 ч с CS в DMEM / 1% ITS (инсулин / трансферрин / селен) и 1 нг / мл IL-1β.Фракционирование и характеризация высвобожденной в среду НА выполняли с использованием 2 колонок Shodex 0Hpak (KB806-KB805) от Showa Denko (Токио, Япония), элюированных 0,15 М NaCl при 35 ° C. Содержание HA во фракциях ВЭЖХ определяли в каждой фракции ВЭЖХ с помощью ELISA, используя HABP (белок, связывающий гиалуроновую кислоту).
Однако сначала необходимо решить проблему чистоты и химического строения промышленных образцов ХС. В отличие от гиалуронана, CS не может быть получен инженерным путем, и экстракты животных (бычий, ихтиевый, птичий) по-прежнему являются единственными доступными источниками.Также требуется дополнительная информация о последовательном расположении дисахаридных единиц в цепи, поскольку это может повлиять на биологическую функцию CS. Сегодня требования к качеству производства нейтрацевтиков не такие строгие, как для фармацевтических (Адебовале и др., 2000; Саад и др., 2005; Сим и др., 2005; Барнхилл и др., 2006; Малаваки и др., 2007; Ламари, 2008). . Были обнаружены большие различия в составе коммерческих препаратов CS, особенно в соотношении 0-, 4- и 6-сульфатированных дисахаридов, что отражает большие различия в видовом или тканевом происхождении (Malawaki et al.2007).
В заключение, для повышения эффективности CS в качестве терапевтического средства при лечении ОА коленного сустава было бы очень интересно доставлять растворы этого гликозаминогликана непосредственно в синовиальную полость, отдельно или в сочетании с гиалуронаном. Этот новый подход позволит CS оказывать хондропротекторное и противовоспалительное действие на суставные клетки с помощью механизмов, уже описанных в системах in vitro.
Финансирование
Часть нашей работы по хондроитинсульфату финансировалась лабораторией Пьера Фабра (Кастр, Франция).
Заявление о конфликте интересов
Не объявлено.
Сокращения
CS
GAG
GS
НПВП
нестероидные противовоспалительные препараты
- 000
OA 9014AD
000 PG медленное действие модифицирующие препараты
Аббревиатуры
Список литературы
,,,.Анализ содержания глюкозамина и хондроитинсульфата в продаваемых продуктах и проницаемости хондроитинсульфатного сырья по Caco-2
,J Am Nutraceutical Assoc
,2000
, vol.3
(стр.37
—44
),,,,,.Анализ гликозаминогликанов в сыворотке крови человека после перорального приема хондроитинсульфата
,Rheumatol Int
,1992
, vol.12
(стр.81
—88
),,,,,.Выбор хондроитиновых препаратов для интервенционного исследования артрита глюкозамином / хондроитином
,J Am Pharm Assoc.
,2006
, т.46
(стр.14
—24
),,,.Влияние хондроитинсульфата и интерлейкина-1β на суставные хондроциты человека, культивируемые в кластерах
,Остеоартрит Хрящ
,1998
, vol.6
(стр.196
—204
),,.Влияние глюкозамина и хондроитинсульфата на регуляцию экспрессии генов протеолитических ферментов и их ингибиторов в суставных эксплантатах крупного рогатого скота, зараженных интерлейкином-1
,Am J Vet Res.
,2005
, т.66
(стр.1870
—1876
),,,.Глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простангландина E 2 в эксплантатах суставного хряща
,Остеоартрит Хрящ.
,2005
, т.13
(стр.387
—394
),,,,,,,,, и др.Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава
,N Engl J Med.
,2006
, т.354
(стр.795
—808
),,,,,.Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальной регуляции гиалуронансинтаз. Роль p38 и Akt
,Arthritis Rheum.
,2009
, т.60
(стр.760
—770
),,.Внутрисуставная доставка хондроитинсульфата для лечения дефектов суставов у кроликов модель
,J Mol Hist.
,2007
, т.38
(стр.483
—489
),,,.Ранний воспалительный артрит у кролика: влияние внутрисуставных и системных кортикостероидов на уровни мРНК в соединительной ткани колена
,J Rheumatol.
,2007
, т.34
(стр.130
—139
).Потенциал хондроитинсульфата как терапевтического агента
,Connect Tissue Res.
,2008
, т.49
(стр.289
—292
),,,,.Хондроитинсульфатная модуляция матрикса и экспрессия воспалительных генов в IL-1β-стимулированных хондроцитах — Исследование на культурах гипоксических альгинатных гранул
,Остеоартрит Хрящ
,2008
, vol.16
(стр.105
—114
),,,,,.Капиллярный электрофорез для контроля качества хондроитинсульфатов в сырье и препаратах
,Anal Biochem.
,2007
, т.374
(стр.213
—220
),,,,,.Хондроитинсульфат и гиалуроновая кислота (500–730 кДа) ингибируют синтез стромелизина-1 в хондроцитах человека, страдающих остеоартритом
,Drug Exp Clin Res.
,2005
, т.31
(стр.71
—76
),,,,,.Сравнение противовоспалительной эффективности хондроитинсульфата и диклофенака натрия у пациентов с остеоартритом коленного сустава
,J Ревматол.
,1996
, т.23
(стр.1385
—1391
),,,.Противовоспалительная активность хондроитинсульфата
,Остеоартроз Хрящ.
,1998
, т.6
(стр.14
—21
),,,.Анализ содержания гиалуронана в препаратах хондроитинсульфата с использованием селективного ферментативного расщепления и масс-спектрометрии с ионизацией электрораспылением
,Anal Biochem.
,2005
, т.344
(стр.232
—239
),,,,, и др.Предварительная процедура для микроопределения хондроитинсульфата в плазме и моче
,Anal Biochem.
,2002
, т.302
(стр.169
—174
).Диетический глюкозамин под вопросом
,Glycobiology
,2009
, vol.19
(стр.564
—667
),,,,,,,.Количественный анализ хондроитинсульфата в сырье, офтальмологических растворах, мягких капсулах и жидких препаратах
,J Chromatogr B Analyt Technol Biomed Life Sci.
,2005
, т.818
(стр.133
—139
),,,.Хондроитинсульфат как модифицирующий структуру агент
,Ad Pharmacol.
,2006
, т.53
(стр.475
—488
),.Влияние сульфатированных гликозаминогликанов на метаболизм протеогликанов в клетках синовиальной оболочки
,Acta Rhumatol Belg.
,1977
, т.1
(стр.75
—92
).Гиалуронан подавляет выработку цитокинов стимулированными липополисахаридом макрофагами U937 путем подавления NF-κB через ICAM-1
,Inflamm Res.
,2007
, т.56
(стр.246
—253
)© Автор 2009. Опубликовано Oxford University Press. Все права защищены. Для получения разрешений обращайтесь по электронной почте: [email protected]
Oxford University Press
Фармакопротеомическое исследование действия хондроитина и сульфата глюкозамина на суставные хондроциты человека | Исследования и терапия артрита
Беренбаум Ф .: Новые горизонты и перспективы в лечении остеоартроза. Arthritis Res Ther. 2008, 10: S1-10.1186 / ar2462.
PubMed Central Статья PubMed Google ученый
Reginster JY, Deroisy R, Rovati LC, Lee RL, Lejeune E, Bruyere O, Giacovelli G, Henrotin Y, Dacre JE, Gossett C: Долгосрочные эффекты сульфата глюкозамина на прогрессирование остеоартрита: рандомизированные, плацебо-контролируемое клиническое исследование.Ланцет. 2001, 357: 251-256. 10.1016 / S0140-6736 (00) 03610-2.
CAS Статья PubMed Google ученый
Pavelka K, Gatterova J, Olejarova M, Machacek S, Giacovelli G, Rovati LC: Использование глюкозамина сульфата и замедление прогрессирования остеоартрита коленного сустава: трехлетнее рандомизированное плацебо-контролируемое двойное слепое исследование . Arch Intern Med. 2002, 162: 2113-2123. 10.1001 / archinte.162.18.2113.
CAS Статья PubMed Google ученый
Towheed TE, Maxwell L, Anastassiades TP, Shea B, Houpt J, Robinson V, Hochberg MC, Wells G: терапия глюкозамином для лечения остеоартрита. Кокрановская база данных Syst Rev.2005, CD002946-
Google ученый
Leeb BF, Schweitzer H, Montag K, Smolen JS: метаанализ хондроитинсульфата в лечении остеоартрита. J Rheumatol. 2000, 27: 205-211.
CAS PubMed Google ученый
Kahan A, Uebelhart D, De Vathaire F, Delmas PD, Reginster JY: Долгосрочные эффекты хондроитинов 4 и 6 сульфата на остеоартрит коленного сустава: исследование профилактики прогрессирования остеоартрита, двухлетнее рандомизированное двойное слепое плацебо -контролируемое судебное разбирательство. Ревматоидный артрит. 2009, 60: 524-533. 10.1002 / арт.24255.
CAS Статья PubMed Google ученый
McAlindon TE, LaValley MP, Gulin JP, Felson DT: Глюкозамин и хондроитин для лечения остеоартрита: систематическая оценка качества и метаанализ.ДЖАМА. 2000, 283: 1469-1475. 10.1001 / jama.283.11.1469.
CAS Статья PubMed Google ученый
Reichenbach S, Sterchi R, Scherer M, Trelle S, Bürgi E, Bürgi U, Dieppe PA, Jüni P: Мета-анализ: хондроитин при остеоартрозе колена или бедра. Ann Intern Med. 2007, 146: 580-590.
Артикул PubMed Google ученый
Clegg DO, Reda DJ, Harris CL, Klein MA, O’Dell JR, Hooper MM, Bradley JD, Bingham CO, Weisman MH, Jackson CG, Lane NE, Cush JJ, Moreland LW, Schumacher HR, Oddis CV, Wolfe F, Molitor JA, Yocum DE, Schnitzer TJ, Furst DE, Sawitzke AD, Shi H, Brandt KD, Moskowitz RW, Williams HJ: глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава.N Engl J Med. 2006, 354: 795-808. 10.1056 / NEJMoa052771.
CAS Статья PubMed Google ученый
Gouze JN, Gouze E, Popp MP, Bush ML, Dacanay EA, Kay JD, Levings PP, Patel KR, Saran JP, Watson RS, Ghivizzani SC: экзогенный глюкозамин глобально защищает хондроциты от артритогенных эффектов IL. -1бета. Arthritis Res Ther. 2006, 8: R173-10.1186 / ar2082.
PubMed Central Статья PubMed Google ученый
Чапал Н., Молина Л., Молина Ф, Лапланш М., Пау Б., Пети П.: Фармакопротеомический подход к изучению механизма действия, токсичности и устойчивости лекарств: применение при диабете и раке. Fundam Clin Pharmacol. 2004, 18: 413-422. 10.1111 / j.1472-8206.2004.00258.x.
CAS Статья PubMed Google ученый
Gorg A, Weiss W, Dunn MJ: Современная технология двумерного электрофореза для протеомики. Протеомика.2004, 4: 3665-3685. 10.1002 / pmic.200401031.
Артикул PubMed Google ученый
Руис-Ромеро С., Лопес-Армада М.Дж., Бланко Ф.Дж.: Протеомная характеристика нормальных суставных хондроцитов человека: новый инструмент для изучения остеоартрита и других ревматических заболеваний. Протеомика. 2005, 5: 3048-3059. 10.1002 / pmic.200402106.
CAS Статья PubMed Google ученый
Руис-Ромеро С., Каррейра В., Рего I, Ремесейро С., Лопес-Армада М.Дж., Бланко Ф.Дж.: Протеомный анализ хондроцитов человека, страдающих остеоартритом, выявляет белковые изменения при стрессе и гликолизе. Протеомика. 2008, 8: 495-507. 10.1002 / pmic.200700249.
CAS Статья PubMed Google ученый
Cillero-Pastor B, Ruiz-Romero C, Caramés B, López-Armada MJ, Blanco FJ: Протеомный анализ двумерного электрофореза для идентификации нормального протеома хондроцитов человека, стимулированного фактором некроза опухоли альфа и интерлейкином. 1бета.Ревматоидный артрит. 2010, 62: 802-814. 10.1002 / арт.27265.
CAS Статья PubMed Google ученый
Фернандес Дж., Мартель-Пеллетье Дж., Пеллетье Дж. П.: Роль цитокинов в патофизиологии остеоартрита. Биореология. 2002, 39: 237-246. Обзор
CAS PubMed Google ученый
Laemmli UK: Расщепление структурных белков во время сборки головки бактериофага Т4.Природа. 1970, 227: 680-685. 10.1038 / 227680a0.
CAS Статья PubMed Google ученый
Rabilloud T, Brodard V, Peltre G, Righetti PG, Ettori C: модифицированное окрашивание серебром для иммобилизованных градиентов pH. Электрофорез. 1992, 13: 264-266. 10.1002 / elps.1150130154.
CAS Статья PubMed Google ученый
Sechi S, Chait BT: Модификация остатков цистеина путем алкилирования.Инструмент для картирования пептидов и идентификации белков. Anal Chem. 1998, 70: 5150-5158. 10.1021 / ac9806005.
CAS Статья PubMed Google ученый
Матрица. [http://www.matrixscience.com]
Сервер протеомики ExPASy. [http://www.expasy.ch/sprot]
База знаний UniProt. [http://www.ebi.ac.uk/trembl]
Прогнозирование PSORT II.[http://www.psort.org/]
Универсальная библиотека зондов. [http://www.roche-applied-science.com]
Ливак К.Дж., Шмитген Т.Д .: Анализ данных относительной экспрессии генов с использованием количественной ПЦР в реальном времени и 2 (-Delta Delta C (T) ) Метод. Методы. 2001, 25: 402-408. 10.1006 / meth.2001.1262.
CAS Статья PubMed Google ученый
Ruiz-Romero C, Calamia V, Mateos J, Carreira V, Martinez-Gomariz M, Fernandez M, Blanco FJ: Митохондриальная дисрегуляция остеоартрозных суставных хондроцитов человека, проанализированная с помощью протеомики: снижение митохондриальных дисмаксидных точек окислительно-восстановительный дисбаланс.Протеомика клеток Mol. 2009, 8: 172-189. 10.1074 / mcp.M800292-MCP200.
PubMed Central CAS Статья PubMed Google ученый
Shikhman AR, Kuhn K, Alaaeddine N, Lotz M: N-ацетилглюкозамин предотвращает опосредованную IL-1 бета активацию хондроцитов человека. J Immunol. 2001, 166: 5155-5160.
CAS Статья PubMed Google ученый
Gouze JN, Bianchi A, Becuwe P, Dauca M, Netter P, Magdalou J, Terlain B, Bordji K: глюкозамин модулирует индуцированную IL-1 активацию хондроцитов крысы на уровне рецепторов и путем ингибирования пути NF-kappa B . FEBS Lett. 2002, 510: 166-170. 10.1016 / S0014-5793 (01) 03255-0.
CAS Статья PubMed Google ученый
Tat SK, Pelletier JP, Vergés J, Lajeunesse D, Montell E, Fahmi H, Lavigne M, Martel-Pelletier J: Хондроитин и сульфат глюкозамина в комбинации снижают прорезорбтивные свойства субхондральных костных хрящей при остеоартрозе человека. : исследование фундаментальных наук.Arthritis Res Ther. 2007, 9: R117-10.1186 / ar2325.
PubMed Central Статья PubMed Google ученый
Iovu M, Dumais G, du Souich P: Противовоспалительная активность хондроитинсульфата. Хрящевой артроз. 2008, 16: S14-18. 10.1016 / j.joca.2008.06.008.
Артикул PubMed Google ученый
Улдри М., Ибберсон М., Хосокава М., Торенс Б. GLUT2 представляет собой высокоаффинный переносчик глюкозамина.FEBS Lett. 2002, 524: 199-203. 10.1016 / S0014-5793 (02) 03058-2.
CAS Статья PubMed Google ученый
Windhaber RA, Wilkins RJ, Meredith D: Функциональная характеристика транспорта глюкозы в суставных хондроцитах крупного рогатого скота. Pflugers Arch. 2003, 446: 572-577. 10.1007 / s00424-003-1080-5.
CAS Статья PubMed Google ученый
Дэвид-Рауди М., Мендичи Р., Пуйоль Дж. П. Для внутрисуставной доставки хондроитинсульфата. Гликобиология. 2009, 19: 813-815. 10.1093 / гликоб / cwp069.
CAS Статья PubMed Google ученый
Wei F, Haut RC: Высокие уровни глюкозамин-хондроитинсульфата могут изменять циклическую преднагрузку и реакцию острой перегрузки хондральных эксплантатов. J Orthop Res. 2009, 27: 353-359. 10.1002 / jor.20757.
Артикул PubMed Google ученый
d’Abusco AS, Calamia V, Cicione C, Grigolo B, Politi L, Scandurra R: Глюкозамин влияет на внутриклеточную передачу сигналов посредством ингибирования фосфорилирования митоген-активированной протеинкиназы в хондроцитах человека. Arthritis Res Ther. 2007, 9: R104-10.1186 / ar2307.
Артикул Google ученый
Чан П.С., Карон Дж. П., Орт М.В.: Влияние глюкозамина и хондроитинсульфата на эксплантаты бычьего хряща в условиях длительного культивирования.Am J Vet Res. 2007, 68: 709-715. 10.2460 / ajvr.68.7.709.
CAS Статья PubMed Google ученый
Piperno M, Reboul P, Hellio Le Graverand MP, Peschard MJ, Annefeld M, Richard M, Vignon E: Сульфат глюкозамина модулирует дисрегулируемую активность остеоартритических хондроцитов человека in vitro. Хрящевой артроз. 2000, 8: 207-212. 10.1053 / joca.1999.0291.
CAS Статья PubMed Google ученый
Ronca F, Palmieri L, Panicucci P, Ronca G: Противовоспалительная активность хондроитинсульфата. Хрящевой артроз. 1998, 6: 14-21. 10.1016 / С1063-4584 (98) 80006-Х.
Артикул PubMed Google ученый
Chan PS, Caron JP, Orth MW: Кратковременные изменения экспрессии генов в хрящевых эксплантатах, стимулированные интерлейкином бета плюс глюкозамин и хондроитинсульфат. J Rheumatol. 2006, 33: 1329-1340.
CAS PubMed Google ученый
Орт М.В., Петерс Т.Л., Хокинс Дж. Н.: Ингибирование деградации суставного хряща глюкозамином-HCl и хондроитинсульфатом. Equine Vet J Suppl. 2002, 34: 224-229. 10.1111 / j.2042-3306.2002.tb05423.x.
Артикул PubMed Google ученый
Chou MM, Vergnolle N, McDougall JJ, Wallace JL, Marty S, Teskey V, Buret AG: Влияние хондроитина и сульфата глюкозамина в составе диетического батончика на воспаление, интерлейкин-1бета, матриксную металлопротеазу-9, и повреждение хряща при артрите.Exp Biol Med (Maywood). 2005, 230: 255-262.
CAS Google ученый
Chan PS, Caron JP, Rosa GJ, Orth MW: глюкозамин и хондроитинсульфат регулируют экспрессию генов и синтез оксида азота и простагландина E (2) в эксплантатах суставного хряща. Хрящевой артроз. 2005, 13: 387-394. 10.1016 / j.joca.2005.01.003.
CAS Статья PubMed Google ученый
Campo GM, Avenoso A, Campo S, Ferlazzo AM, Altavilla D, Calatroni A: Эффективность лечения гликозаминогликанами экспериментального коллаген-индуцированного артрита у крыс. Arthritis Res Ther. 2003, 5: R122-131. 10.1186 / ar748.
PubMed Central CAS Статья PubMed Google ученый
Legendre F, Baugé C, Roche R, Saurel AS, Pujol JP: Модуляция хондроитинсульфатом матрикса и экспрессия воспалительных генов в хондроцитах, стимулированных IL-1beta — исследование на культурах гипоксических альгинатных гранул.Хрящевой артроз. 2008, 16: 105-114. 10.1016 / j.joca.2007.05.020.
CAS Статья PubMed Google ученый
Дэвид-Рауди М., Дешревель Б., Леклерк С., Галера П., Бумедиен К., Пуйоль Дж. П. Хондроитинсульфат увеличивает выработку гиалуронана синовиоцитами человека за счет дифференциальной регуляции гиалуронансинтаз: роль p38 и Akt. Ревматоидный артрит. 2009, 60: 760-770. 10.1002 / арт.24302.
CAS Статья PubMed Google ученый
Grimmer C, Balbus N, Lang U, Aigner T, Cramer T, Müller L, Swoboda B, Pfander D: Регулирование синтеза коллагена типа II во время остеоартрита пролил-4-гидроксилазами. Am J Pathol. 2006, 169: 491-502. 10.2353 / ajpath.2006.050738.
PubMed Central CAS Статья PubMed Google ученый
Элльгаард Л., Фрикель Е.М.: кальнексин, кальретикулин и ERp57: товарищи по команде в сворачивании гликопротеина. Cell Biochem Biophys.2003, 39: 223-247. 10.1385 / CBB: 39: 3: 223.
CAS Статья PubMed Google ученый
Кивирикко К.И., Пихлаяниеми Т. Коллаген-гидроксилазы и протеин-дисульфидизомеразная субъединица пролил-4-гидроксилаз. Adv Enzymol Relat Areas Mol Biol. 1998, 72: 325-398.
CAS PubMed Google ученый
Alexopoulos LG, Youn I, Bonaldo P, Guilak F: Изменения развития и остеоартрита у мышей с нокаутом Col6a1: биомеханика коллагена типа VI в перицеллюлярном матриксе хряща.Ревматоидный артрит. 2009, 60: 771-779. 10.1002 / арт.24293.
PubMed Central CAS Статья PubMed Google ученый
Корригалл В.М., Бодман-Смит, доктор медицины, Файф М.С., Канас Б., Майерс Л.К., Вули П., Сох С., Стейнс Н.А., Паппин Д.Д., Берло С.Е., ван Эден В., ван Дер Зи Р., Ланчбери Дж.С., Панайи Г.С.: Молекулярный шаперон эндоплазматического ретикулума человека BiP является аутоантигеном ревматоидного артрита и предотвращает индукцию экспериментального артрита.J Immunol. 2001, 166: 1492-1498.
CAS Статья PubMed Google ученый
Панайи Г.С., Корригалл В.М.: BiP регулирует аутоиммунное воспаление и повреждение тканей. Autoimmun Rev.2006, 5: 140-142. 10.1016 / j.autrev.2005.08.006.
CAS Статья PubMed Google ученый
Мэтьюз Дж. А., Белоф Дж. Л., Асеведо-Дункан М., Поттер Р. Л.: Индуцированное глюкозамином увеличение фосфорилирования Akt соответствует усилению стресса эндоплазматического ретикулума в астроглиальных клетках.Mol Cell Biochem. 2007, 298: 109-123. 10.1007 / s11010-006-9358-5.
CAS Статья PubMed Google ученый
Marshall KW, Zhang H, Yager TD, Nossova N, Dempsey A, Zheng R, Han M, Tang H, Chao S, Liew CC: Биомаркеры на основе крови для обнаружения легкого остеоартрита коленного сустава человека. Хрящевой артроз. 2005, 13: 861-871. 10.1016 / j.joca.2005.06.002.
CAS Статья PubMed Google ученый
Афонсу В., Чампи Р., Митрович Д., Коллин П., Ломри А.: Активные формы кислорода и супероксиддисмутазы: роль в заболеваниях суставов.

 )
) N. Engl. J. Med. 354 (8): 795—808. doi:10.1056/NEJMoa052771. PMID 16495392.
N. Engl. J. Med. 354 (8): 795—808. doi:10.1056/NEJMoa052771. PMID 16495392.