Мышечные белки
Впервые А. Я. Данилевский (1881) разделил экстрагируемые из мышц белки на три класса: растворимые в воде, экстрагируемые 8 — 12% раствором хлорида аммония и белки, извлекаемые разбавленными растворами кислот и щелочей. В настоящее время белки мышечной ткани делят на три основные группы: саркоплазматические белки, миофибриллярные белки, белки стромы. На долю первых приходится около 35%, вторых —45% и третьих-20% всего мышечного белка. Эти группы белков резко отличаются друг от друга по растворимости в воде и солевых средах с различной ионной силой.
Белки, входящие в состав саркоплазмы, принадлежат к числу протеинов, растворимых в солевых средах с низкой ионной силой.
К числу саркоплазматических белков относятся также дыхательный пигмент миоглобин и разнообразные белки-ферменты, локализованные главным образом в митохондриях и катализирующие процессы тканевого дыхания, окислительного фосфорилирования, а также многие стороны азотистого и липидного обменов. Недавно была открыта группа саркоплазматических белков — парвальбумины, которые способны связывать ионы кальция.
К группе миофибриллярных белков относятся миозин, актин и актомиозин — белки, растворимые в солевых средах с высокой ионной силой, и так называемые регуляторные белки: тропомиозин, тропонин, α- и β-актинин, образующие в мышце с актомиозином единый комплекс. Перечисленные миофибриллярные белки тесно связаны с сократительной функцией мышц.
 Толстые
нити (толстые
миофиламенты) в саркомере получены
путем соединения большого ппчисла
определенным образом ориентированных
в ппппппппппппппппппппппппппппппппппппространстве
молекул миозина.
Толстые
нити (толстые
миофиламенты) в саркомере получены
путем соединения большого ппчисла
определенным образом ориентированных
в ппппппппппппппппппппппппппппппппппппространстве
молекул миозина.
Актин, составляющий ~20% от сухой массы миофибрилл. Известны две формы актина: глобулярный (Г-актин) и фибриллярный (Ф-актин) актин. Молекула Г-актина состоит из одной полипептидной цепочки, в образовании которой принимают участие 374 аминокислотных остатка. Ф-актин является продуктом полимеризации Г-актина и имеет структуру двухцепочечной спирали.
Актомиозин образуется при соединении миозина с Ф-актином. Актомиозин, как обладает АТФазной активностью. Однако АТФазная активность актомиозина отличается от АТФазной активности миозина. Фермент актомиозин активируется ионами магния и ингибируется этилен-диаминтетраацетатом (ЭДТА) и высокой концентрацией АТФ, тогда как миозиновая АТФаза ингибируется ионами Mg2+, активируется ЭДТА и не ингибируется высокой концентрацией АТФ. Оптимальные значения рН для обоих ферментов также различны.
Тропомиозин был открыт К. Бейли в 1946 г. Молекула тропомиозина состоит из двух α-спиралей и имеет вид стержня. На долю тропомиозина приходится около 4 — 7% всех белков миофибрилл.
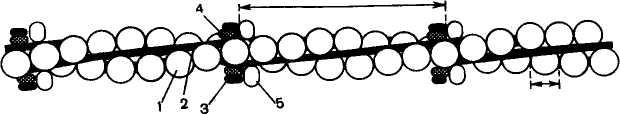 Т
Т
Структура тонкого филамента.
1 — актин; 2 — тропомиозин; 3 — тропонин С;
4 — тропонин
I; 5 — тропонин Тропонин — глобулярный белок, открытый С. Эбаси в 1963 г. В скелетных мышцах взрослых животных и человека тропонин (Тн) составляет лишь около 2% от всех миофибриллярных белков. В его состав входят три субъединицы (Тн-I, Тн-С, Тн-Т). Тн-I (ингибирующий) может ингибировать АТФазную активность, Тн-С (кальцийсвязывающий) обладает значительным сродством к ионам кальция, Тн-Т (тропомиозинсвязывающий) обеспечивает связь с тропомиозином. Тропонин, соединяясь с тропомиозином, образует комплекс, названный нативным тропомиозином. Этот комплекс прикрепляется к актиновым филаментам и придает актомиозину скелетных мышц позвоночных чувствительность к ионам кальция.Небелковые азотистые экстрактивные вещества
В скелетных мышцах содержится ряд важных азотистых экстрактивных веществ: адениновые нуклеотиды (АТФ, АДФ и АМФ), нуклеотиды неаденинового ряда, креатин-фосфат, креатин, креатинин, карнозин, ансерин, свободные аминокислоты и др.
На долю креатина и креатинфосфата приходится до 60% небелкового азота мышц. Креатинфосфат и креатин относятся к тем азотистым экстрактивным веществам мышц, которые участвуют в химических процессах, связанных с мышечным сокращением.
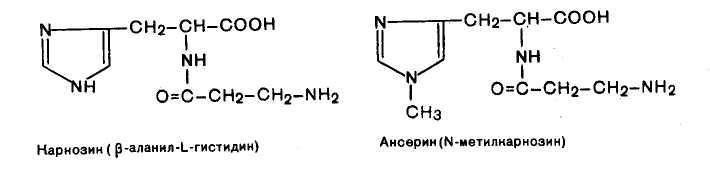
Карнозин и ансерин — специфические азотистые вещества скелетной мускулатуры позвоночных — увеличивают амплитуду мышечного сокращения, предварительно сниженную утомлением. Имидазолсодержащие дипептиды не влияют непосредственно на сократительный аппарат, но увеличивают эффективность работы ионных насосов мышечной клетки.
Среди свободных аминокислот в мышцах наиболее высокую концентрацию имеет глутаминовая кислота (до 1,2 г/кг) и ее амид — глутамин (0,8-1,0 г/кг). В состав различных клеточных мембран мышечной ткани входит ряд фосфоглицеридов: фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин и др. Другие азотсодержащие вещества: мочевина, мочевая кислота, аденин, гуанин, ксантин и гипоксантин — встречаются в мышечной ткани в небольшом количестве.
studfile.net
Мышечные белки. «БИОЛОГИЧЕСКАЯ ХИМИЯ», Березов Т.Т., Коровкин Б.Ф.
Белки, входящие в состав саркоплазмы, относятся к протеинам, растворимым в солевых средах с
низкой ионной силой. Принятое ранее подразделение саркоплазматических белков на
миоген, глобулин X, миоальбумин и белки-пигменты в значительной мере утратило
смысл, поскольку существование глобулина X и миогена как индивидуальных белков
в настоящее время отрицается. Установлено, что глобулин X представляет собой
смесь различных белковых веществ со свойствами глобулинов. Термин «миоген»
также является собирательным понятием. В частности, в состав белков группы
миогена входит ряд протеинов, наделенных ферментативной активностью: например,
ферменты гликолиза. К числу саркоплазмати-ческих белков относятся также
дыхательный пигмент миоглобин и разнообразные белки-ферменты, локализованные
главным образом в митохондриях и катализирующие процессы тканевого дыхания,
окислительного фосфорилирования, а также многие стороны азотистого и липидного
обмена. Недавно была открыта группа саркоплазматических белков –
пар-вальбумины, которые способны связывать ионы Са
К группе миофибриллярных белков относятся миозин, актин и актомио-зин – белки, растворимые в солевых средах с высокой ионной силой, и так называемые регуляторные белки: тропомиозин, тропонин, α- и β-актинин, образующие в мышце с актомиозином единый комплекс. Перечисленные миофибриллярные белки тесно связаны с сократительной функцией мышц.
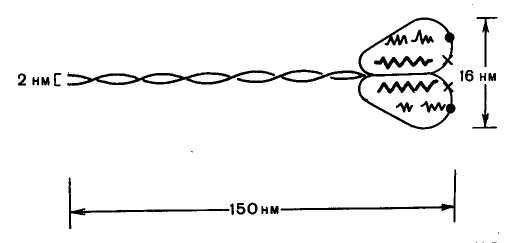
Рис. 20.3. Строение молекулы миозина. Объяснение в тексте.
Миозин составляет 50–55% от сухой массы миофибрилл. Представление о миозине как о главном белке миофибрилл сложилось в результате работ А.Я. Данилевского, О. Фюрта, Э. Вебера и ряда других исследователей. Однако всеобщее внимание к миозину было привлечено лишь после опубликования работ В.А. Энгельгардта и М.Н. Любимовой (1939– 1942). В этих работах впервые было показано, что миозин обладает АТФазной активностью, т.е. способностью катализировать расщепление АТФ на АДФ и Н3РО4. Химическая энергия АТФ, освобождающаяся в ходе данной ферментативной реакции, превращается в механическую энергию сокращающейся мышцы. Молекулярная масса миозина скелетных мышц около 500000 (для миозина кролика 470000). Молекула миозина (рис. 20.3) имеет сильно вытянутую форму, длину 150 нм. Она может быть расщеплена без разрыва ковалентных связей на субъединицы: две тяжелые полипептидные цепи с мол. массой 205000–210000 и несколько коротких легких цепей, мол. масса которых около 20000. Тяжелые цепи образуют длинную закрученную α-спираль («хвост» молекулы), конец каждой тяжелой цепи совместно с легкими цепями создает глобулу («головка» молекулы), способную соединяться с актином. Эти «головки» выдаются из основного стержня молекулы. Легкие цепи, находящиеся в «головке» миозиновой молекулы и принимающие участие в проявлении АТФазной активности миозина, гетерогенны по своему составу. Количество легких цепей в молекуле миозина у различных видов животных и в разных типах мышц неодинаково.
Кратковременная обработка трипсином расщепляет молекулу миозина на два фрагмента. Из хвостового участка (С-концевой участок молекулы) образуется легкий меромиозин (ЛММ) - фрагмент длиной 90 нм, а из остальной части, включающей «головки»,- тяжелый меромиозин (ТММ). ЛММ, подобно миозину, образует нити, однако он не обладает АТФазной активностью и не связывает актин. ТММ катализирует гидролиз АТФ и связывает актин. ТММ можно расщепить далее путем более длительной обработки трипсином или папаином, в результате чего получается один S2-фрагмент длиной 40 нм с мол. массой 62000 и два S1-фрагмента с мол. массой 110000, представляющие собой «головки» миозина.
Толстые нити (толстые миофиламенты) в саркомере надо понимать как образование, полученное путем соединения большого числа определенным образом ориентированных в пространстве молекул миозина (рис. 20.4).
Актин, составляющий 20% от сухой массы миофибрилл, был открыт Ф. Штраубом в 1942 г. Известны две формы актина: глобулярный актин (G-актин) и фибриллярный актин (F-актин). Молекула G-актина с мол. массой 42000 состоит из одной полипептидной цепочки (глобула), в обра-
Рис. 20.4. Строение толстого миозинового филамента.
зовании которой принимают участие 374 аминокислотных остатка. При повышении ионной силы до физиологического уровня G-актин полиме-ризуется в F-актин (фибриллярная форма). На электронных микрофотографиях волокна F-актина выглядят как две нити бус, закрученных одна вокруг другой (рис. 20.5).
Актомиозин образуется при соединении миозина с F-актином. Ак-томиозин, как естественный, так и искусственный, т.е. полученный путем соединения in vitro высокоочищенных препаратов миозина и F-актина, обладает АТФазной активностью, которая отличается от таковой миозина, АТФазная активность миозина значительно возрастает в присутствии стехиометрических количеств F-актина. Фермент актомиозин активируется ионами Mg2+и ингибируется этилендиаминтетраацетатом (ЭДТА) и высокой концентрацией АТФ, тогда как миозиновая АТФаза ингибируется ионами Mg2+, активируется ЭДТА и не ингибируется высокой концентрацией АТФ. Оптимальные значения рН для обоих ферментов также различны.
Как отмечалось, кроме рассмотренных основных белков, в миофибрил-лах содержатся также тропомиозин, тропонин и некоторые другие ре-гуляторные белки.
Тропомиозин был открыт К. Бейли в 1946 г. Молекула тропомиозина состоит из двух α-спиралей и имеет вид стержня длиной 40 нм; его мол. масса 65000. На долю тропомиозина приходится около 4–7% всех белков миофибрилл.
Тропонин – глобулярный белок, открытый С. Эбаси в 1963 г.; его мол. масса 80000. В скелетных мышцах взрослых животных и человека тропонин (Тн) составляет лишь около 2% от всех миофибриллярных белков. В его состав входят три субъединицы (Тн-I, Тн-С, Тн-Т). Тн-I (ингибирующий) может ингибировать АТФазную активность, ТН-С (кальцийсвязывающий) обладает значительным сродством к ионам кальция, Тн-Т (тропомиозин-связывающий) обеспечивает связь с тропомиозином. Тропонин, соединяясь с тропомиозином, образует комплекс, названный нативным тропомиози-ном. Этот комплекс прикрепляется к актиновым филаментам и придает актомиозину скелетных мышц позвоночных чувствительность к ионам Са2+ (рис. 20.6).
Установлено, что тропонин (его субъединицы Тн-Т и Тн-I) способен фосфорилироваться при участии цАМФ-зависимых протеинкиназ. Вопрос о том, имеет ли отношение фосфорилирование тропонина in vitro к регуляции мышечного сокращения, остается пока открытым.
Белки стромы в поперечно-полосатой мускулатуре представлены в основном коллагеном и эластином. Известно, что строма скелетных мышц, остающаяся после исчерпывающей экстракции мышечной кашицы солевыми растворами с высокой ионной силой, состоит в значительной мере из соединительнотканных элементов стенок сосудов и нервов, а также сарколеммы и некоторых других структур.
Рис. 20.6. Структура тонкого филамента.
1 — актин; 2 - тропомиозин; 3 — тропонин С; 4 — тропонин I; 5 — тропонин Т.
Предыдущая страница | Следующая страница
СОДЕРЖАНИЕ
www.xumuk.ru
1.2. Химический состав мышечной ткани
Химический состав мышц млекопитающих представлен в таблице 1. Как видно из таблицы 72-80% массы мышцы составляет вода. Большую часть сухого остатка (16-21%) образуют белки, остальное — органические вещества и минеральные соли.
Таблица 1
Химический состав мышц млекопитающих (по Збарскому)
Вещество | Содержание в мышцах, % |
Вода | 72 — 80 |
Белки | 16,3 – 20,9 |
Гликоген | 0,3 — 2 |
Фосфатиды | 0,4 – 1,0 |
Холестерин | 0,03 – 0,23 |
Креатин и креатинфосфат | 0,2 – 0,55 |
Азотсодержащие вещества (креатинин, карнозин, ансерин, карнитин) | 0,383 – 0,535 |
Свободные аминокислоты | 0,1 – 0,7 |
Мочевина | 0,002 – 0,2 |
Молочная кислота | 0,01 – 0,2 |
Основные неорганические ионы: | |
К | 0,32 |
Na | 0,08 |
Са | 0,007 |
Mg | 0,02 |
Fe | 0,026 |
Cl | 0,02 |
Распределение белков в клетке выглядит так: в миофибриллах — 4% всех мышечных белков, в саркоплазме — 30%, в митохондриях — 14%, в сарколемме — 15%, в ядрах и других клеточных органеллах — около 1%.
Кроме основных сократительных белков, характеристика которых была дана выше, следует отметить еще два: миостромин и миоглобин. Миостромин участвует в образовании сарколеммы и линии Z. Миоглобин — белок, по строению и функции подобный гемоглобину; первичная структура миоглобина приведена выше. В отличие от гемоглобина он не обладает четвертичной структурой; однако сродство миоглобина к кислороду намного выше, чем у гемоглобина.
B мышцах человека содержится дипептид карнозин (аланилгистидин), который принимает участие в ферментативном переносе фосфатных групп и оказывает стимулирующее влияние на передачу импульсов с нерва на мышцу, а также участвует в восстановлении утомленных мышц.
Из органических веществ небелковой природы отметим АТФ, креатинфосфат и гликоген. АТФ является главным источником энергии для мышечного сокращения, креатинфосфат — первый резерв ресинтеза АТФ; гликоген — основной запасной источник энергии в мышце.
Фосфатиды и холестерин входят в состав различных мембран мышечного волокна. Свободные аминокислоты используются биосинтезе мышечных белков.
B мышце содержится ряд промежуточных продуктов обмена углеводов. К ним относятся, прежде всего, пировиноградная и молочная кислоты, а также ферменты гликолиза.
Из минеральных
веществ в мышцах имеются главным образом
катионы К ,
Na
,
Na ,
Mg
,
Mg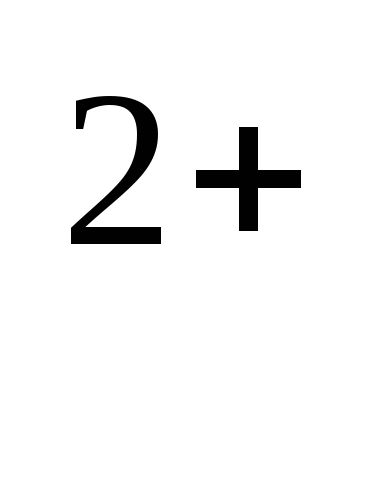 ,
Са
,
Са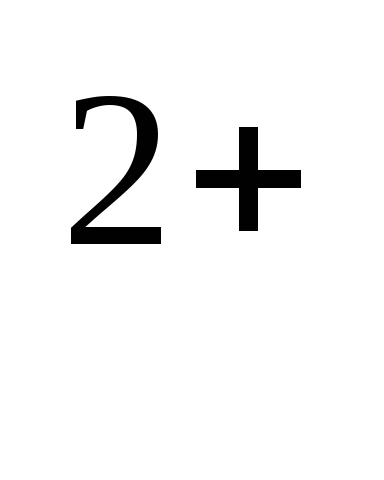 ,
анионы Cl
,
анионы Cl ,
Н
,
Н РО
РО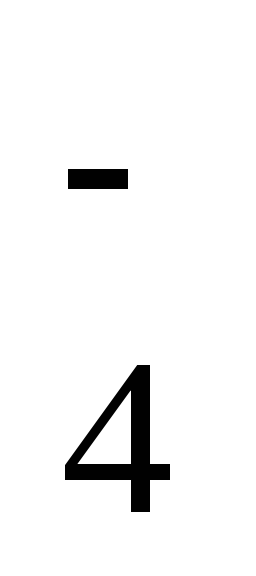 , HPО
, HPО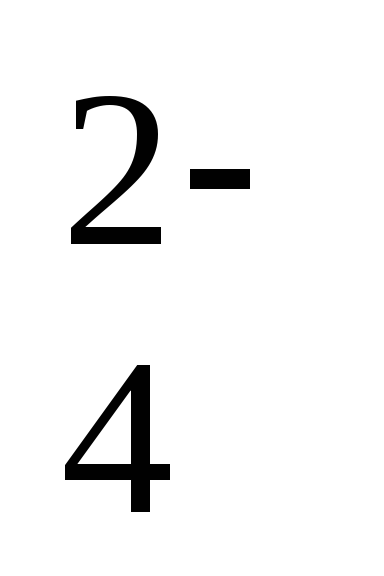 .
Перечисленные ионы играют важную роль
в регуляции биохимических процессов
в сокращающихся мышцах.
.
Перечисленные ионы играют важную роль
в регуляции биохимических процессов
в сокращающихся мышцах.
1.3. Мышечное сокращение
B основе мышечного сокращения лежат два процесса:
• спиральное скручивание сократительных белков;
• циклически повторяющееся образование и диссоциация комплекса между цепью миозина и актином.
Мышечное сокращение
инициируется приходом потенциала
действия на концевую пластинку
двигательного нерва, где выделяется
нейрогормон ацетилхолин, функцией
которого является передача импульсов.
Сначала ацетилхолин взаимодействует
с ацетилхолиновыми рецепторами, что
приводит к распространению потенциала
действия вдоль сарколеммы. Все это
вызывает увеличение проницаемости
сарколеммы для катионов Na ,
которые устремляются внутрь мышечного
волокна, нейтрализуя отрицательный
заряд на внутренней поверхности
сарколеммы. С сарколеммой связаны
поперечные трубочки саркоплазматического
ретикулума, по которым распространяется
волна возбуждения. От трубочек волна
возбуждения передается мембранам
пузырьков и цистерн, которые оплетают
миофибриллы на участках, где происходит
взаимодействие актиновых и миозиновых
нитей. При передаче сигнала на цистерны
саркоплазматического ретикулума,
последние начинают освобождать
находящийся в них Са
,
которые устремляются внутрь мышечного
волокна, нейтрализуя отрицательный
заряд на внутренней поверхности
сарколеммы. С сарколеммой связаны
поперечные трубочки саркоплазматического
ретикулума, по которым распространяется
волна возбуждения. От трубочек волна
возбуждения передается мембранам
пузырьков и цистерн, которые оплетают
миофибриллы на участках, где происходит
взаимодействие актиновых и миозиновых
нитей. При передаче сигнала на цистерны
саркоплазматического ретикулума,
последние начинают освобождать
находящийся в них Са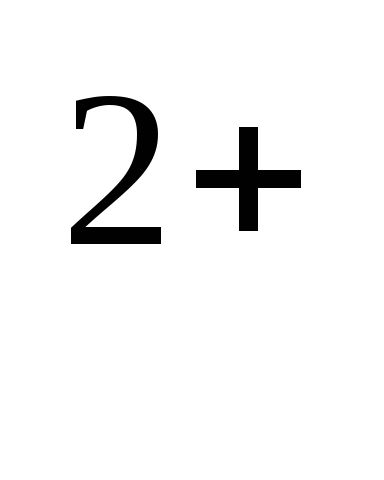 .
Высвобожденный Са
.
Высвобожденный Са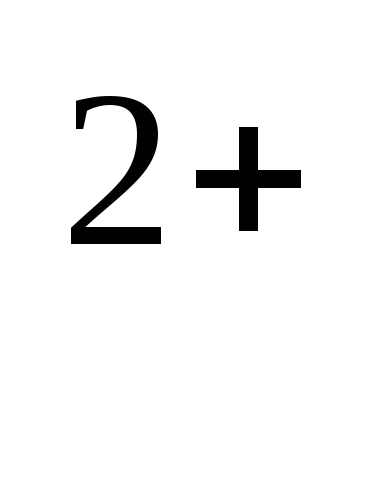 связывается с Тн-С, что вызывает
конформационные сдвиги, передающиеся
на тропомиозин и далее на актин. Актин
как бы освобождается из комплекса с
компонентами тонких филаментов, в
котором он находился. Далее актин
взаимодействует с миозином, и результатом
такого взаимодействия является
образование спайки, что делает
возможным движение тонких нитей вдоль
толстых.
связывается с Тн-С, что вызывает
конформационные сдвиги, передающиеся
на тропомиозин и далее на актин. Актин
как бы освобождается из комплекса с
компонентами тонких филаментов, в
котором он находился. Далее актин
взаимодействует с миозином, и результатом
такого взаимодействия является
образование спайки, что делает
возможным движение тонких нитей вдоль
толстых.
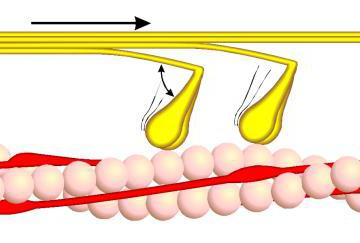
Генерация силы (укорочение) обусловлена характером взаимодействия между миозином и актином. На миозиновом стержне имеется подвижный шарнир, в области которого происходит поворот при связывании глобулярной головки миозина с определенным участком актина. Именно такие повороты, происходящие одновременно в многочисленны участках взаимодействия миозина и актина, являются причиной втягивания актиновых филаментов (тонких нитей) в H-зону. Здесь они контактируют (при максимальном укорочении) или даже перекрываются друг с другом, как это показано на рисунке 6.
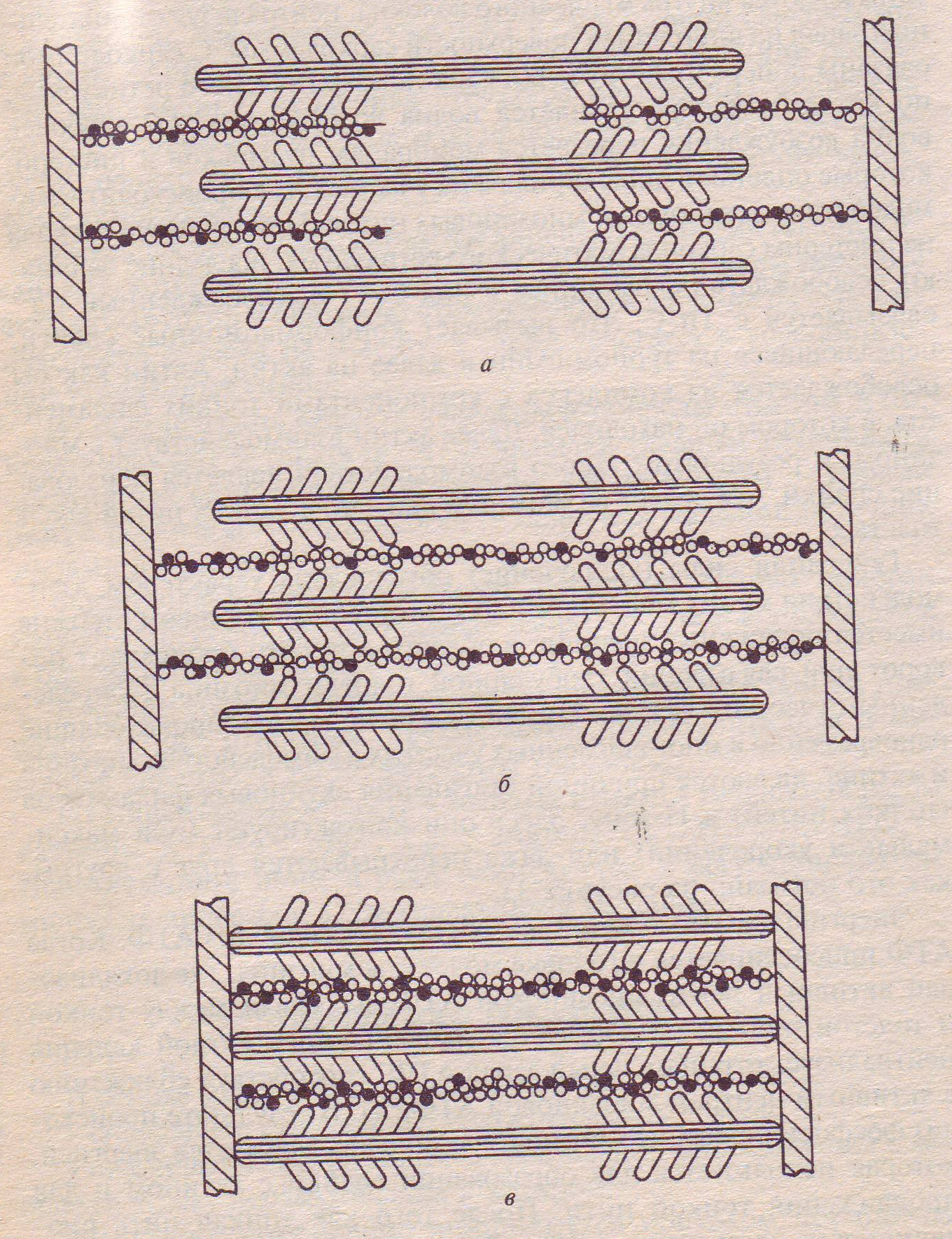
Рис. 6. Механизм сокращения: а – состояние покоя; б – умеренное сокращение; в – максимальное сокращение
Энергию для этого процесса поставляет гидролиз АТФ. Когда АТФ присоединяется к головке молекулы миозина, где локализован активный центр миозиновой АТФазы, связи между тонкой и толстой нитями не образуется. Появившийся катион кальция нейтрализует отрицательный заряд АТФ, способствуя сближению с активным центром миозиновой АТФазы. В результате происходит фосфорилирование миозина, т. e. миозин заряжается энергией, которая используется для образования спайки с активом и для продвижения тонкой нити. После того как тонкая нить продвинется на один «шаг», АДФ и фосфорная кислота отщепляются от актомиозинового комплекса. Затем к миозиновой головке присоединяется новая молекула АТФ, и весь процесс повторяется со следующей головкой молекулы миозина.
Затрата АТФ
необходима и для расслабления мышц.
После прекращения действия двигательного
импульса Са переходит в цистерны саркоплазматического
ретикулума. Тн-С теряет связанный с
ним кальций, следствием этого являются
конформационные сдвиги в комплексе
тропонин-тропомиозин, и Тн-I снова
закрывает активные центры актина, делая
их неспособными взаимодействовать с
миозином. Концентрация Са
переходит в цистерны саркоплазматического
ретикулума. Тн-С теряет связанный с
ним кальций, следствием этого являются
конформационные сдвиги в комплексе
тропонин-тропомиозин, и Тн-I снова
закрывает активные центры актина, делая
их неспособными взаимодействовать с
миозином. Концентрация Са в области сократительных белков
становится ниже пороговой, и мышечные
волокна теряют способность образовывать
актомиозин.
в области сократительных белков
становится ниже пороговой, и мышечные
волокна теряют способность образовывать
актомиозин.
B этих условиях эластические силы стромы, деформированной в момент сокращения, берут верх, и мышца расслабляется. При этом тонкие нити извлекаются из пространства между толстыми нитями диска A, зона H и диск I приобретают первоначальную длину, линии Z отдаляются друг от друга на прежнее расстояние. Мышца становится тоньше и длиннее.
Скорость гидролиза АТФ при мышечной работе огромна: до 10 мк моль на 1 г мышцы за 1 мин. Общие запасы АТФ невелики, поэтому для обеспечения нормальной работы мышц АТФ должна восстанавливаться с той же скоростью, с какой она расходуется.
studfile.net
Сократительные белки: функции, примеры
Белки (полипептиды, протеины) представляют собой высокомолекулярные вещества, в состав которых входят альфа-аминокислоты, соединенные пептидной связью. Состав протеинов определяется в живых организмах генетическим кодом. Как правило, при синтезе используется набор из 20 стандартных аминокислот.
Классификация белков
Разделение протеинов осуществляется по разным признакам:
- Форме молекулы.
- Составу.
- Функциям.
По последнему критерию белки классифицируются:
- На структурные.
- Питательные и запасные.
- Транспортные.
- Сократительные.
Структурные белки
К ним относят эластин, коллаген, кератин, фиброин. Структурные полипептиды участвуют в процессе формирования мембран клеток. Они могут создавать в них каналы или осуществлять иные функции.
Питательные, запасные протеины
Питательным полипептидом является казеин. За счет него растущий организм обеспечивается кальцием, фосфором и аминокислотами.
Запасными являются белки семян культурных растений, яичный белок. Они потребляются на этапе развития зародышей. В человеческом организме, как и у животных, протеины не откладываются в запас. Их необходимо регулярно получать с пищей, иначе вероятно развитие дистрофии.
Транспортные полипептиды
Классическим примером таких белков является гемоглобин. В крови обнаруживаются и другие полипептиды, участвующие в перемещении гормонов, липидов и других веществ.
В мембранах клетки находятся протеины, обладающие способностью транспортировать ионы, аминокислоты, глюкозу и прочие соединения через клеточную мембрану.
Сократительные белки
Функции этих полипептидов связаны с работой мышечных волокон. Кроме того, они обеспечивают движение ресничек и жгутиков у простейших. Сократительные белки выполняют функцию транспортировки органелл внутри клетки. За счет их наличия обеспечивается изменение клеточных форм.
Примерами сократительных белков являются миозин и актин. Стоит сказать, что эти полипептиды обнаруживаются не только в клетках мышечных волокон. Сократительные белки выполняют свои задачи практически во всех тканях животных.
Особенности
В клетках обнаруживается индивидуальный полипептид – тропомиозин. Сократительный мышечный белок миозин является его полимером. Он образует комплекс с актином.
Сократительные белки мышц не растворяются в воде.
Скорость синтеза полипептидов
Ее регулируют тиреоидные и стероидные гормоны. Проникая в клетку, они связываются со специфическими рецепторами. Образованный комплекс проникает в клеточное ядро и связывается с хроматином. За счет этого повышается скорость синтеза полипептидов на генном уровне.
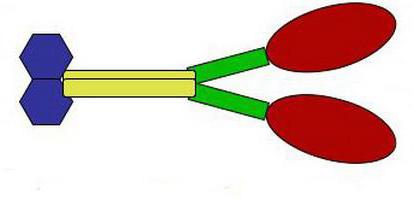
Активные гены обеспечивают усиление синтеза определенной РНК. Она выходит из ядра, направляется к рибосомам и активирует синтез новых структурных либо сократительных белков, ферментов или гормонов. В этом заключается анаболическое действие генов.
Между тем белковый синтез в клетках – процесс достаточно медленный. Он требует больших энергетических затрат и пластического материала. Соответственно, гормоны не в состоянии оперативно контролировать метаболизм. Ключевая их задача состоит в регуляции роста, дифференциации и развития клеток в организме.
Мышечное сокращение
Оно является ярким примером сократительной функции белков. В ходе исследований было установлено, что в основе сокращения мускулатуры лежит изменение физических свойств полипептида.
Сократительную функцию выполняет белок актомиозин, взаимодействующий с аденозинтрифосфорной кислотой. Эта связь сопровождается сокращением миофибрилл. Такое взаимодействие можно наблюдать вне организма.
К примеру, если на вымоченные в воде (мацерированные) волокна мышц, лишенные возбудимости, воздействовать раствором аденозинтрифосфата, начнется их резкое сокращение, аналогичное сокращению живой мускулатуры. Этот опыт имеет важнейшее практическое значение. Он доказывает тот факт, что для мышечного сокращения необходима химическая реакция сократительных белков с веществом, богатым энергией.
Действие витамина Е
С одной стороны, он является главным внутриклеточным антиоксидантом. Витамин Е обеспечивает защиту жиров и прочих легкоокисляемых соединений от окисления. Вместе с тем он выступает в качестве переносчика электронов и участвует в окислительно-восстановительных реакциях, которые связаны с запасанием высвобождаемой энергии.
Дефицит витамина Е вызывает атрофию мышечной ткани: содержание сократительного белка миозина резко уменьшается, и его заменяет коллаген – инертный полипептид.
Специфика миозина
Он считается одним из ключевых сократительных белков. На его долю приходится порядка 55 % от общего содержания полипептидов в мышечной ткани.
Из миозина состоят филаменты (толстые нити) миофибрилл. В молекуле присутствует длинная фибриллярная часть, имеющая двуспиральную структуру, и головки (глобулярные структуры). В составе миозина выделяют 6 субъединиц: 2 тяжелые и 4 легкие цепи, находящиеся в глобулярной части.
В качестве основной задачи фибриллярного участка выступает способность формировать пучки филаментов миозина или толстые протофибриллы.
На головках находятся активный участок АТФ-азы и актинсвязывающий центр. За счет этого обеспечивается гидролиз АТФ и связь с актиновыми филаментами.
Разновидности
Подвидами актина и миозина считаются:
- Динеин жгутиков и ресничек простейших.
- Спектрин в мембранах эритроцитов.
- Нейростенин перисинаптических мембран.
К разновидностям актина и миозина можно также отнести полипептиды бактерий, ответственные за перемещение различных веществ в градиенте концентраций. Этот процесс называется также хемотаксисом.
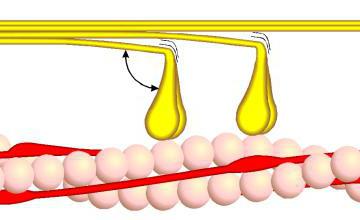
Роль аденозинтрифосфорной кислоты
Если поместить нити актомиозина в раствор кислоты, добавить ионы калия и магния, можно увидеть, что они укорачиваются. При этом наблюдается расщепление АТФ. Это явление свидетельствует о том, что распад аденозинтрифосфорной кислоты имеет определенную связь с изменением физико-химических свойств сократительного белка и, следовательно, с работой мышц. Впервые этот феномен был выявлен Сцент-Дьиордьи и Энгельгардтом.
Синтез и распад АТФ имеют важнейшее значение в процессе превращения химической энергии в механическую. При распаде гликогена, сопровождающегося выработкой молочной кислоты, как и при дефосфорилировании аденозинтрифосфорной и креатинфосфорной кислот, участие кислорода не требуется. Этим объясняется способность изолированной мышцы функционировать в анаэробных условиях.
В волокнах мускулатуры, утомленных при работе в анаэробной среде, накапливаются молочная кислота и продукты, образовавшиеся при распаде аденозинтрифосфорной и креатинфосфорной кислот. В результате исчерпываются запасы веществ, при расщеплении которых выделяется необходимая энергия. Если поместить утомленную мышцу в условия, содержащие кислород, она будет его потреблять. Некоторое количество молочной кислоты начнет окисляться. В результате образуются вода и углекислый газ. Высвобождающаяся энергия будет использоваться для ресинтеза креатинфосфорной, аденозинтрифосфорной кислот и гликогена из продуктов распада. За счет этого мышца снова приобретет способность работать.
Скелетная мышца
Отдельные свойства полипептидов можно объяснить только на примере их функций, т. е. их вклада в сложную деятельность. Среди немногочисленных структур, в отношении которых была установлена корреляция между функциями белков и органа, особого внимания заслуживает скелетная мышца.
Ее клетка активируется за счет нервных импульсов (мембранно-направленных сигналов). В молекулярном плане сокращение основывается на циклическом формировании поперечных мостиков благодаря периодическим взаимодействиям между актином, миозином и Mg-АТР. Кальцийсвязывающие белки и ионы Са выступают в качестве посредников между эффекторами и нервными сигналами.
Посредничество ограничивает скорость ответа на импульсы «включение/выключение» и предотвращает самопроизвольные сокращения. Вместе с тем некоторые осцилляции (колебания) маховых мышечных волокон крылатых насекомых контролируют не ионы или аналогичные низкомолекулярные соединения, а непосредственно сократительные белки. За счет этого возможны очень быстрые сокращения, которые после активации протекают самостоятельно.
Жидкокристаллические свойства полипептидов
При укорочении мышечных волокон изменяется период решетки, образованной протофибриллами. При вхождении решетки из тонких нитей в структуру из толстых элементов тетрагональную симметрию сменяет гексагональная. Это явление можно считать полиморфным переходом в жидкокристаллической системе.
Особенности механохимических процессов
Они сводятся к трансформации химической энергии в механическую. АТФ-азная активность митохондриальных клеточных мембран имеют сходство с актом иозиновой системы скелетной мускулатуры. Общие черты отмечаются и в их механохимических свойствах: они сокращаются под влиянием АТФ.
Следовательно, в мембранах митохондрий должен присутствовать сократительный белок. И он действительно там присутствует. Установлено, что сократительные полипептиды задействованы в митохондриальной механохимии. Однако выяснилось также, что значительную роль в процессах играет и фосфатидилинозитол (липид мембран).
Дополнительно
Молекула белка миозина не только способствует сокращению разных мышц, но и может участвовать в других внутриклеточных процессах. Речь, в частности, о перемещении органелл, прикреплении актиновых нитей к мембранам, формировании и функционировании цитоскелета и пр. Почти всегда молекула так или иначе взаимодействует с актином, являющимся вторым ключевым сократительным белком.
Было доказано, что молекулы актомиозина могут изменять длину под воздействием химической энергии, высвобождаемой при отщеплении от АТФ остатка фосфорной кислоты. Другими словами, именно этот процесс обуславливает сокращение мышц.
Система АТФ, таким образом, выступает как своего рода аккумулятор химической энергии. По мере надобности она превращается непосредственно в механическую при посредничестве актомиозина. При этом отсутствует промежуточный этап, характерный для процессов взаимодействия других элементов, — переход в тепловую энергию.
fb.ru
Белки. Вся правда о главном строительном элементе мышц. [Часть 1].


Э-ге-гей, уважаемые! Рад Вас снова приветствовать на страницах проекта “Азбука Бодибилдинга”! Наконец-то совершилось! Мы добрались до одной из самых фундаментальных тем, касающихся питания бодибилдеров – белки. Фундаментальных потому, что это основной строительный кирпичик мышц, именно благодаря ему мы и видим (или не видим) тот объем мускулов, которые нам удалось накачать. Сразу скажу, что хоть тема и довольно сложная, но если в ней разобраться вдоль и поперек, то рельефные мышцы – это как минимум Ваш диагноз.
Если копнуть, то в действительности довольно мало начинающих бодибилдеров (да и просто людей, занимающихся в тренажерном зале), обладают всей полнотой знаний относительно белков. Зачастую им только известно, что белки – это хорошо, их надо есть, да и все пожалуй. Мы же с Вами будем последовательно разбираться как в теоретических вопросах – строение и функции, механизмы синтеза белка, так и в практических – как они строят наши мышцы и т.п. В общем, уделим самое пристальное внимание этому важному компоненту в питании бодибилдера и изучим все тонкие тонкости и нюансные нюансы.


Итак, не будем тянуть кота за затягивать, приступаем к рассмотрению теоретических основ: что такое белки, их строение, функции, роль и т.д.
Белки: что это такое и с чем их едят? Введение в теорию.
Начать хотелось бы с небольшого анонса – если Вы еще совсем зеленый в вопросах питания, тогда следующие статьи будут как нельзя кстати: [Пирамида питания. Руководство к применению], [Правильное и здоровое питание. Все, что надо знать].
Я уже ранее говорил, что пища в виде нутриентов (белков, жиров, углеводов, минералов и витаминов) поступает в наш организм. Однако намеренно не акцентировал свое внимание на том, сколько конкретно нужно употреблять этих компонентов, чтобы закрывать поставленные цели, будь то набор мышечной массы или сброс веса. Что ж, пришло время поговорить и об этом.
Итак, самое простое определение белка (с точки зрения его важности) было сформулировано еще Энгельсом, и звучало оно так, жизнь – способ существования белковых тел. Из него сразу понятно, что не будет белка – не будет жизни. Применительно к бодибилдингу можно сказать, что не будет белка – не будет мышц. Теперь окунемся в науку.


Белок (он же протеин) – это высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью. Аминокислотный состав белка полностью определяется 20 аминокислотами (9 — не заменимые/не синтезируются организмом и 11 – заменимые), входящими в его состав.
- Незаменимые: лейцин, изолейцин, валин, гистидин, лицин, метионин, треонин, триптофан, фенилаланин;
- Заменимые: аланин, аргенин, аспарагин, аспарагиновая кислота, глицин, глутамин, глутаминовая кислота, пролин, серин, тирозин, цистин.
Примечание:
Гемоглобин – самый известный белок, его химическая формула показывает, насколько это высокомолекулярные вещества – С3032H4816O872N780S8Fe4. Молекулярная масса белков колеблется от нескольких тысяч до нескольких миллионов. Например, Mr белка яйца = 36000, Mr белка мышц = 1500000 (для сравнения, Mr спирта =46).
Помимо этих 20 аминокислот есть еще и те, которые не входят в состав белка, однако выполняют важные функции в организме, например гамма-аминомасляная кислота и диоксифенилаланин участвуют в передаче нервных импульсов и являются важными компонентами нервной системы. Без них процесс тренировок был бы похож на бесконтрольные, амебной формы телодвижения (хотя, может у кого-то и с ними он так выглядит).
Самыми важными для организма (с точки зрения метаболизма) являются такие аминокислоты, как: лейцин, изолейцин и cвалин (см. таблицу).


Все три аминокислоты являются представителями так называемого ВСАА-класса (Branched Chain Amino Acids, разветвленная цепь). На долю этого класса из всех незаменимых кислот приходится 42%, что является весьма внушительной цифрой. ВСАА-аминокислоты играют важную роль в белковом обмене и энергетической составляющей работы мышц. Для оптимального протекания процессов синтеза белка все три аминокислоты должны входить в рацион питания (либо посредством натуральных продуктов, либо с пищевыми добавками).
С конкретными цифрами потребления этих трех аминокислот, а также с аминокислотным составом пищевых белков, Вы можете ознакомиться из следующей таблицы (см. таблицу).


Идем далее.
В состав белковых веществ входят такие химические элементы как: углерод, водород, кислород, сера, фосфор и, конечно же, основу составляет азот. В связи с этим, просто необходимо знать (помнить) о таком понятии, как азотистый баланс. Помимо того, что азот (в основном, из белка) поступает к нам с пищей, он также образуется (и выделяется из организма) в процессе обмена веществ из продуктов распада белков. Поэтому наш организм – это станция по переработке (с одной стороны) и выведению (с другой стороны) азота.
Разница между приходом и расходом азота позволяет нам говорить о положительном (потребляем больше, чем выделяем) или отрицательном (наоборот) азотистом балансе. Таким образом, необходимо помнить, что набрать силу и мышечную массу можно только при положительном азотистом балансе.
Примечание:
В зависимости от тренированности атлета для сохранения положительного азотистого баланса необходимо разное потребление белка на 1 кг веса тела атлета. В целом, цифры примерно следующие:
- атлет, бодибилдер со стажем (2-3 год и более) – 2 грамма/кг веса;
- новички (1 год и менее) – 2-3 грамма/кг веса.
Собственно, помимо того, что белок — это основной структурный элемент мышц, он также выполняет множество других функций. Давайте их более подробно рассмотрим.
Функции белков
Конечно, с точки зрения бодибилдинга наибольшее значение представляет строительная функция белков, однако они также выполняют еще много важных и нужных для организма (см. изображение).


Более наглядно с функциями и ролью белков можно ознакомиться из видео-ролика в конце статьи, так что дочитываем до конца!
Организм человека весьма умная, саморегулирующаяся система. Он заранее знает, что, хоть и белки могут выступать в качестве резервного источника энергии, но расходовать этот высококачественный материал на энергообеспечение нецелесообразно, поэтому использует углеводы. Когда же организм чувствует, что рацион питания спортсмена обеднен углеводами, ему ничего не остается делать, как брать ценный белок и использовать его в качестве источника энергии для подпитки организма. Так что не забывайте про углеводы тоже (о них мы также будем говорить в наших статьях, не пропустите).
Белки по-разному воздействуют на мышцы, это, в первую очередь, обуславливается их различным химическим составом и структурой молекул. Поэтому нужно знать источники высококачественных белков, которые в полном объеме будут строить Ваши мышцы. Здесь важное значение имеет такое понятие как биологическая ценность белка (BV) – это то его количество, которое запасается организмом при употреблении в пищу 100 гр данного белка. Кроме того, если BV=1, то это означает, что продукт содержит полный набор всех незаменимых аминокислот.
Примечание:
Например, куриное (перепелиное) яйцо обладает коэффициентом биологической полноценности (BV) – 1, а вот пшеница – содержит только половину незаменимых кислот (т.е. ее BV = 0,54). Получается, что при одинаковом содержании в продуктах количестве белка (12,7 грамм/100 гр. продукта), организм сможет наиболее полно и в большем объеме усвоить именно из яиц, ибо BV у них выше, чем у пшеницы.
После того, как мы употребили белки (в виде продуктов питания, пищевых добавок), они расщепляются в ЖКТ за счет ферментов до аминокислот, а затем и до конечных продуктов – воды, углекислого газа и аммиака, потом всасываются через стенки кишечника, распределяясь по всему организму, чтобы выполнить свои непосредственные функции.
Какие бывают белки?
Лучше преимущественно потреблять белковую пищу животного происхождения (мясо, рыба, морепродукты и т.п.), ибо она по своему аминокислотному профилю наиболее ценна с точки зрения получения питательных элементов из пищи. Однако не стоит забывать и про растительный белок. В целом, соотношение (только по белку) должно выглядеть примерно так: 70-80% – животного происхождения, 20-30% – растительного.
Белки, по степени усвояемости подразделяются на:
- Быстрые – скорость получения элементарных компонент из пищи высокая. Пример: рыба, яйца, куриная грудка, морепродукты;
- Медленные – наоборот. Пример: творог (“долгоиграющий” белок, на 70% состоит из казеина).
По аминокислотному составу белки бывают:
- Полноценные;
- Неполноценные;
- Простые – состоят только из аминок;
- Сложные – в составе аминокислота + неаминокислотный остаток (комплекс с липидами, углеводами).
По степени растворимости:
- Растворимые (образуют коллоидные растворы) в воде;
- Не растворимые в воде.
Когда говорят о бодибилдинге, под белками подразумевают протеины, высококонцентрированный белок. Наиболее распространенные протеины по способу их получения из продуктов следующие:
- Сывороточный – готовится из молочной сыворотки, обладает наибольшим BV и весьма быстро усваивается;
- Яичный – обладает высоким BV, время всасывания 4-6 часов;
- Казеиновый – самый долгий по усвоению, BV=80%;
- Соевый – снижает уровень холестерина в крови, BV=74%.
Если среди читателей есть вегетарианцы, тогда Вам стоит знать, что все растительные белки (соевый, грибной) – неполноценны по-своему аминокислотному составу. Мясо, молоко, яйца – вот те продукты, которые наиболее полно удовлетворяют требования полноценности содержания в их составе аминокислот. Они (белок молочной сыворотки — лактальбумин) и белок желтка вместе с альбумином (белок яйца) наиболее сбалансированы по своему аминокислотному профилю и лучше всего усваиваются организмом.
Таким образом, зная всю эту информацию, нужно правильно составлять свой рацион питания, чтобы он был сбалансирован по всем основным аминокислотам, и прежде всего — незаменимым. Следующий пункт на рассмотрении, это..
Строение белка
Мы уже знаем, что белок – это сложное высокомолекулярное органическое вещество, структурная организация которого может быть представлена 4 уровнями (структурами): первичной (1), вторичной (2), третичной (3) и четвертичной (4) (см. изображение).


Техническую сторону уровней организации белка (что и как устроено с точки зрения элементов/связей),Вам знать не обязательно, а вот практической мы сейчас займемся.
Итак, некоторые белковые продукты усваиваются на раз-два, а некоторые перевариваются в течении длительного времени. От чего это зависит, спросите Вы? Конечно же от их строения. Например, молочные и яичные белки усваиваются хорошо из-за того, что они находятся в растворе в виде отдельных молекул, свернутых в клубки. Допустим, если молоко скисло и получился творог (т.е. казеин выпал в осадок) или мы варим яйца, происходит денатурация (изменение пространственной структуры белка, связанное с потерей им своих уровней организации).
Часть связей (в особенности сульфидные мостики) в результате этого процесса рвется, белковые молекулы в продуктах распрямляются, спутываются и организму уже становится сложнее усвоить эту измененную структуру белка. Однако стоит заметить, что в процессе варки мяса, его белки наоборот становятся легкоусвояемыми, хотя и теряют некоторую пищевую ценность.
Приведенная информация вовсе не побуждает Вас есть сырые яйца или не кипятить молоко (хотя магазинное по большей части – пастеризованное). Просто помните, если у Вас есть свой домик в деревне (или Вы просто уверены в качестве приобретенных продуктов), то можете их употреблять в первозданном виде, без какой-либо обработки.
Примечание:
Куриные яйца можно легко заменить на перепелиные и есть их сырыми, ибо перепелка не болеет сальмонеллезом, т.к. ее температура тела составляет 42 градуса.
Насчет мяса следует сказать, что его белковые волокна не предназначены для поедания (во как, ну-ка перестали его есть), они предназначены для того, чтобы вырабатывать силу, как бодибилдер. Именно из-за этого его волокна жесткие, они пронизаны поперечными связями и его трудно переварить. Процесс денатурации (в частности, варка мяса) несколько облегчает задачу нашему ЖКТ, разрушая определенные поперечные связи, однако чтобы его полностью усвоить, организму порой требуется от 3 до 6 часов.
Бонусом за все старания в переваривании мяса является креатин – природный источник, повышающий работоспособность мускулатуры и интенсивность тренировок. Что у нас на растительном фронте?
По большей части, основной источник растительных белков – это различные семена (бобы, горох, чечевица и т.п.). В них белок “упакован” достаточно плотно, и чтобы привести его в чувства надлежащее (для быстрого переваривания) состояние, необходимо изрядно потрудиться. Грибной белок также тяжел из-за своей волокнистой структуры и присутствия в его составе углеводных остатков. Соя – вот та золотая середина (и по биологической ценности, и по хорошей усвояемости), которая является наиболее предпочтительным растительным белком, однако стоит помнить, что и ее белок неполноценен и нужно комбинировать его с продуктами животного происхождения.
Теперь давайте посмотрим на продукты с достаточно высоким содержанием белка, дабы иметь представление, что необходимо включить в свой рацион для наращивания мышечной массы (см. таблицу).


Собственно, исходя из приведенной таблицы, Вы уже можете составить свой рацион практически на весь день, главное помнить о принципах рационального питания и о том, какое количества белка Вам нужно употребить в течении суток. Давайте еще раз это закрепим на примере.
Для представителей мужского пола, которые только начали ходить в тренажерный зал, показатель суточного потребления белка на килограмм веса должен составлять от 1,5 до 2 гр, т.е. если Ваш вес 70 кг, то в день Вы должные съедать 105-140 гр чистого белка. Если Вы продвинутый атлет, тогда цифра потребления вырастет до 2,5 гр/кг, т.е. 170 гр (при том же весе) – это норма.
Потребляйте такое количество белка из разнообразных продуктов, т.е. не стоит “лупить” 7 раз в неделю одну куриную грудку или творог, варьируйте свою белковую продуктовую корзину, и тогда мышцы не заставят себя долго ждать!
Ну и напоследок разберем, какие существуют…
Критерии оценки качества белка
Мы уже упоминали про его биологическую ценность (BV). С точки зрения химии – это та доля азота (N), задерживающегося в организме от всего поступившего/всосавшегося азота. Измерение BV основано на том, что если в организме человека находится требуемое количество всех незаменимых аминокислот, то и задержка N – выше.
Помимо этого показателя существуют еще следующие:
- полный аминокислотный профиль
Белок должен быть сбалансирован по своему аминокислотному составу. Это значит, что белки пищи по соотношению незаменимых кислот, должны соответствовать белкам человека, чтобы не было процессов нарушения синтеза собственных белков и сдвига равновесия анаболизма-катаболизма мышц в сторону их распада;
- доступность аминокислот в белке
Чем больше в продуктах различных добавок, красителей и чем больше осуществляется тепловая обработка белков, тем ниже доступность отдельных аминокислот;
- перевариваемость – степень усвояемости белка
Отражает, насколько быстро или сколько времени прошло с момента, когда белок попал в желудок (и расщепился ферментами ЖКТ) и до последующего всасывания отдельных аминокислот через стенки кишечника;
- чистая утилизация белка
Показатель характеризует как степень задержки азота, так и количество перевариваемого белка;
- коэффициент эффективности белка
Специфический показатель, который определяется по воздействию конкретного белка на рост мускулатуры, т.е. прирост мышц пропорционален количеству потребленного белка;
- коэффициент усвоения белка по аминокислотному составу
Учитывает как химическую ценность (состав аминокислот), так и биологическую ценность (полноту переваривания) белков. Если коэффициент равен 1, значит продукт – самый полноценный источник протеина. Итак, теперь давайте ознакомимся с конкретными цифрами (да сколько можно :)) и оценим качество белков в конкретных продуктах питания (см. изображение).


Собственно на сим все, подведем некоторые итоги.
FAQ или ЧАВО надо усвоить?


Было бы просто непростительной ошибкой не подвести некоторый знаменатель всему тому, что тут было сказано (а сказано не мало). Поэтому запомните простые советы, которые позволят Вам лучше ориентироваться в вопросах включения в свой рацион такого ценного строителя мышц, фундаментального кирпичика как белок.
Всегда помните, что:
- Необходимо, чтобы в Вашем рационе преобладали белки преимущественного животного происхождения — до 80%, и только 20%, отдаем на откуп растительным;
- Сочетайте растительные и животные белки, например: картофель-соя, пшеница-яйца, рожь-молоко;
- Потребляйте необходимую Вам норму белка: 1,5-2 гр/кг веса тела – для новичков, для продвинутых бодибилдеров – до 2,5 гр;
- Заботьтесь о качестве потребляемого протеина, т.е. об источниках, откуда будете его получать;
- Не забывайте про незаменимые аминокислоты, которые организм не может самостоятельно синтезировать;
- Не обедняйте рацион за счет углеводов/жиров, не делайте перекосов по основным нутриентам (белкам, жирам, углеводам);
- Потребляйте витамины и их комплексы для полноценного усвоения белков (о них читайте в следующих статьях);
- Читайте проект “Азбука Бодибилдинга”!
Следуя этим простым советам (особенно последнему), Вы резко увеличите свои шансы на построение рельефных мышц.
Послесловие
Ну вот и подошла к концу наша очередная статья. Сегодня мы говорили про белок, его роль и место в рационе питания бодибилдера. Так же узнали все технические моменты, касающиеся его строения, состава и прочее. В следующий раз мы больше узнаем о практической стороне их применения, т.е. как максимально сохранить ценность белка, что такое протеин для качков и какие существуют мифы относительно протеинов в целом.
Так что далеко не уходим, подписываемся на статьи, читаем, анализируем и применяем информацию. Таки все, до связи!
PS. вторая часть заметки
ferrum-body.ru
Содержание
20
Введение………………………………………………………………….2
1. Химический состав и строение мышц.
Механизм мышечного сокращения…………………………………….3
1.1. Строение мышц…………………………………………………….3
1.2. Химический состав мышечной ткани…………………………….10
1.3. Мышечное сокращение……………………………………………12
1.4. Источники энергии для мышечной работы………………………15
Список используемой литературы……………………………………..20
Введение
Подвижность является характерным свойством всех форм жизни. Направленное движение имеет место при расхождении хромосом в процессе клеточного деления, активном транспорте молекул, перемещении рибосом в ходе белкового синтеза, сокращении и расслаблении мышц. Мышечное сокращение — наиболее совершенная форма биологической подвижности. В основе любого движения, в том числе и мышечного, лежат общие молекулярные механизмы.
У человека различают несколько видов мышечной ткани. Поперечнополосатая мышечная ткань составляет мышцы скелета (скелетные мышцы, которые мы можем сокращать произвольно). Гладкая мышечная ткань входит в состав мышц внутренних органов: желудочно-кишечного тракта, бронхов, мочевыводящих путей, кровеносных сосудов. Эти мышцы сокращаются непроизвольно, независимо от нашего сознания.
B данной главе мы рассмотрим строение и процессы сокращения и расслабления скелетных мышц, поскольку именно они представляют наибольший интерес для биохимии спорта.
1. Химический состав и строение мышц. Механизм мышечного сокращения.
1.1. Строение мышц
При изучении скелетных мышц с помощью светового микроскопа в них обнаружили поперечную исчерченность; отсюда их название поперечнополосатые.
B скелетной мышце выделяют сухожильную головку, которой мышца начинается на кости, мышечное брюшко, состоящее из волокон, и сухожильный хвост, которым мышца заканчивается на другой кости (рис. 1).
Мышечное волокно — структурная единица мышцы. Известны три типа мышечных волокон: белые быстро сокращающиеся (VT), промежуточные (FR) и медленно сокращающиеся (ST). Биохимически они различаются механизмами энергетического обеспечения мышечного сокращения. Их иннервируют разные мотонейроны, чем обусловлены неодновременность включения в работу и различная скорость сокращения волокон. Разные мышцы имеют разное сочетание типов волокон.

Рис. 1. Мышца
Каждая мышца состоит из нескольких тысяч мышечных волокон, объединяемых соединительными прослойками и такой же оболочкой. Мышца представляет собой многокомпонентный комплекс. Чтобы разобраться в строении мышцы следует изучить все уровни ее организации и структуры, входящие в ее состав (схема 1).

Схема 1. Уровни структурной организации мышцы
Строение мышечного волокна. Мышечные волокна построены из продольно расположенных миофибрилл диаметром около 1 мкм, в которых видны чередующиеся темные и светлые диски. Темные диски обладают двойным лучепреломлением и называются А-(анизотропными) дисками; светлые диски, необладающие двойным лучепреломлением, называются I-(изотропными) дисками (рис. 2). В середине диска I расположена плотная линия Z, которая пронизывает все волокно, как бы удерживая миофибриллы в пучке и одновременно упорядочивая расположение А- и I-дисков многих миофибрилл. Пучок миофибрилл от одной до другой Z-линии называется саркомером. Диски А имеют в середине более светлую полосу — зону Н, пересекаемую более темной М-зоной. В одной миофибрилле может содержаться до 1000-1200 саркомеров. Каждый саркомер включает: 1) сеть поперечных трубочек, ориентированных под углом 90° к продольной оси волокна и соединяющихся с наружной поверхностью клетки; 2) саркоплазматический ретикулум, составляющий 8-10% объема клетки; 3) несколько митохондрий.
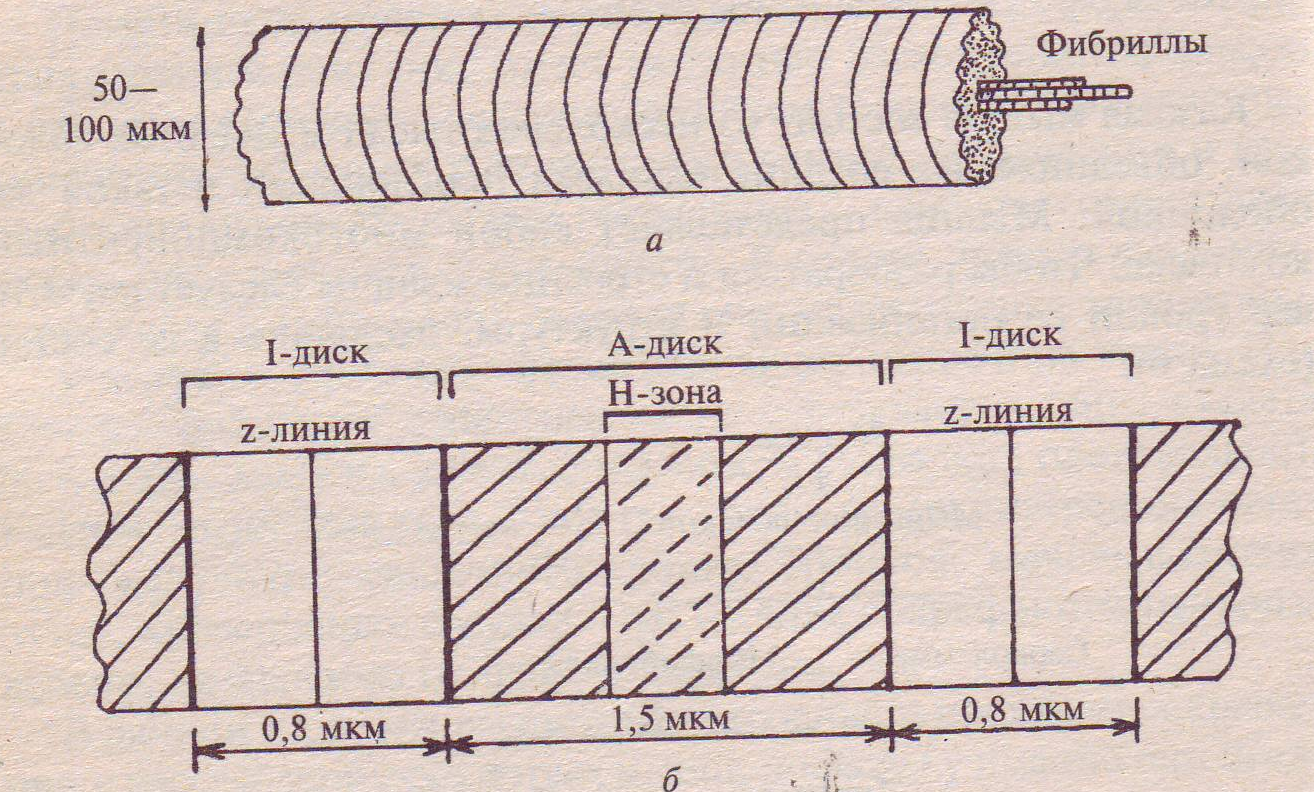
Рис. 2. Структура мышцы на разных уровнях организации: а – мышечное волокно; б – расположение миофибриллы в покоящейся мышце
Миофибриллярные структуры представляют собой агрегаты, состоящие из толстых филаментов диаметром около 14 нм и из расположенных между ними тонких филаментов диаметром 7-8 нм. Филаменты располагаются таким образом, что тонкие входят своими концами в промежутки между толстыми. Диски I состоят только из тонких филаментов, а диски А- из филаментов двух типов. Зона Н содержит только толстые филаменты, линия Z скрепляет тонкие филаменты между собой. Между толстыми и тонкими филаментами расположены поперечные мостики (спайки) толщиной около 3 нм, расстояние между этими мостиками 40 нм.
Толстые филаменты состоят из белка миозина. Общая структура миозина показана на рисунке 3. Палочковидная молекула миозина состоит из двух идентичных основных цепей (по 200 кДа) и четырех легких цепей (по 20 кДа), общая масса миозина около 500 кДа. Миозин состоит из глобулярной, образующей две головки, части, присоединенной к очень длинному стержню. Стержень представляет собой двухцепочечную а-спирализованную суперспираль.

Рис. 3. Схематичное изображение молекулы миозина
Молекулы миозина объединяются, образуя филаменты, состоящие примерно из 400 палочковидных молекул, связанных друг с другом таким образом, что пары головок миозиновых молекул ложатся на расстоянии 14,3 нм друг от друга; они располагаются по спирали (рис. 4). Миозиновые нити стыкуются «хвост к хвосту».
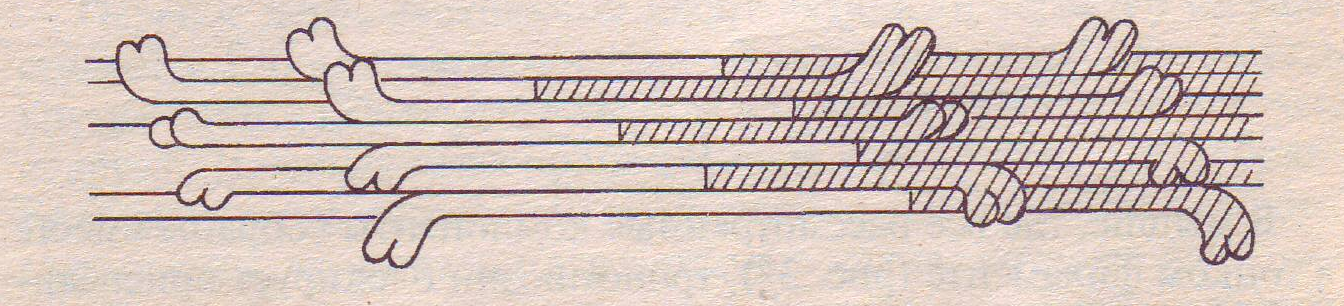
Рис. 4 . Упаковка миозиновых молекул при образовании толстого филамента
Миозин выполняет три биологически важные функции:
• При физиологических значениях ионной силы и рН молекулы миозина спонтанно образуют волокно.
• Миозин обладает каталитической активностью, т. e. является ферментом. В 1939 г. В.А. Энгельгардт и М.Н. Любимова обнаружили, что миозин способен катализировать гидролиз АТФ. Эта реакция является непосредственным источником свободной энергии, необходимой для мышечного сокращения.
• Миозин связывает полимеризованную форму актина — основного белкового компонента тонких миофибрилл. Именно это взаимодействие, как будет показано ниже, играет ключевую роль в мышечном сокращении.
Тонкие филаменты состоят из актина, тропомиозина и тропонина. Основным компонентом тонких филаментов является актин — водорастворимый глобулярный белок с молекулярной массой 42 кДа; эта форма актина обозначается как G-актин. В мышечном волокне актин находится в полимеризованной форме, которая обозначается как F-актин. Тонкие филаменты мышцы образованы двунитчатыми актиновыми структурами, связанными между собой нековалентными связями.
Тропомиозин представляет собой палочкообразную молекулу с молекулярной массой 70 кДа, состоящую из двух разных a-спиральных полипептидных цепей, закрученных относительно друг друга. Эта сравнительно жесткая молекула располагается в желобке спиральной цепочки F-актина; ее протяженность соответствует 7 G-актиновым мономерам.
Третий компонент тонких филаментов — тропонин (Тн), молекулярная масса которого около 76 кДа. Он представляет собой сферическую молекулу, состоящую из трех разных субъединиц, получивших название в соответствии с выполняемыми функциями: тропомиозинсвязывающей (Тн-Т), ингибирующей (Тн-I) и кальцийсвязывающей (Тн-С). Каждый компонент тонких филаментов соединяется с двумя другими нековалентными связями:

B мышце, где все рассмотренные компоненты собраны вместе в тонком филаменте (рис. 5), тропомиозин блокирует присоединение миозиновой головки к находящемуся рядом F-актиновому мономеру. Кальций, связываясь с Тн-С, значительно изменяет конформацию белка, увеличивая степень взаимодействия между субъединицами тропонина и одновременно ослабляя связь между Тн-I и F-актином. Это приводит к перемещению молекулы тропомиозина по желобку тонкого филамента. Результатом такого движения является открытие миозинсвязывающего центра на поверхности актина.
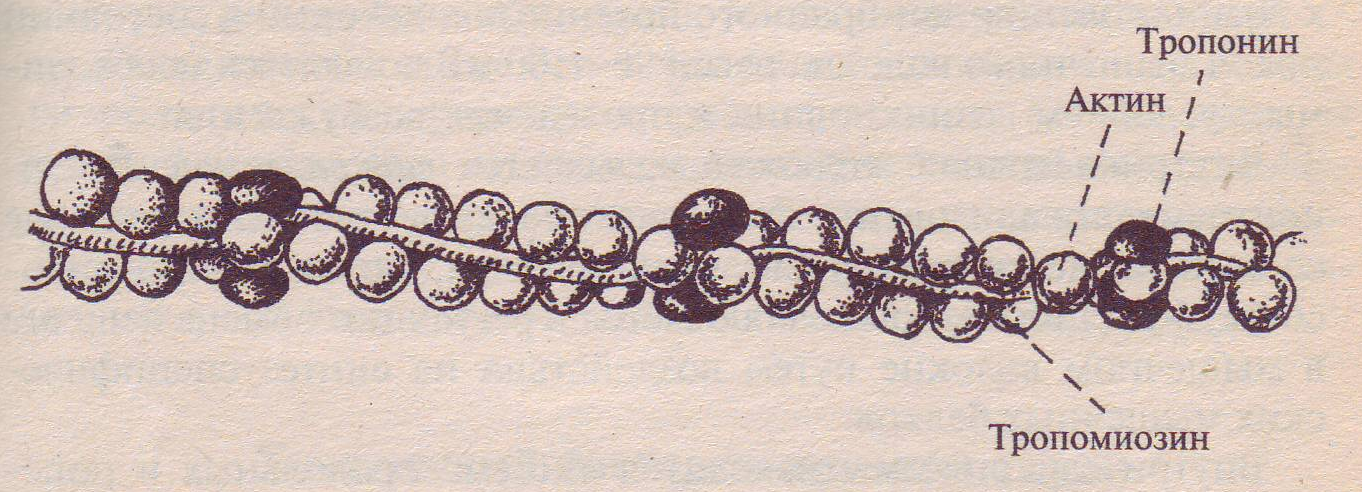
Рис. 5. Взаиморасположение тропомиозина, тропонина и актина в тонком филаменте мышцы
Актив-тропомиозин-тропонинмиозиновый
комплекс характеризуется как Са ,
Mg
,
Mg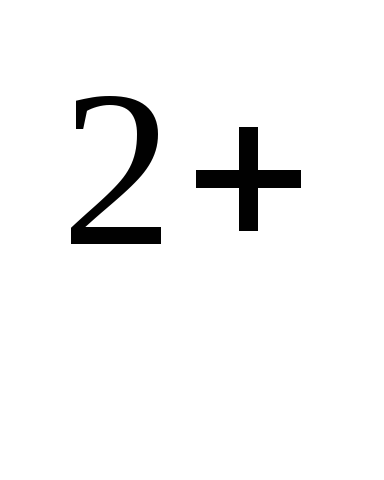 -АТФаза.
-АТФаза.
Рассмотрев сократительные элементы мышцы, перейдем к изучению других элементов, которые выполняют важные функции в мышечном сокращении.
Мышечное волокно состоит из клеток, окруженных электровозбудимой мембраной — сарколеммой, которая, как и любая другая мембрана, имеет липопротеиновую природу (толщина бимолекулярного слоя около 10 нм). Сарколемма отгораживает внутреннее содержимое мышечного волокна от межклеточной жидкости. Подобно другим мембранам, сарколемма имеет избирательную проницаемость для различных веществ. Через нее не проходят высокомолекулярные вещества (белки, полисахариды и др.), но проходят глюкоза, молочная и пировиноградная кислоты, кетоновые тела, аминокислоты и короткие пептиды.
Перенос через сарколемму носит активный характер (осуществляется с помощью посредников), что позволяет накапливать внутри клетки некоторые вещества в большей концентрации, чем снаружи. Избирательная проницаемость сарколеммы играет большую роль в возникновении возбуждения в мышечном волокне. Сарколемма проницаема для катионов калия, которые накапливаются внутри мышечного волокна. В то же время она содержит «ионный насос», выводящий из клетки катионы натрия. Концентрация катионов натрия в межклеточной жидкости выше, чем концентрация катионов калия внутри клетки; кроме того, во внутренних зонах волокна содержится значительное количество органических анионов. Все это приводит к возникновению на наружной поверхности сарколеммы избытка положительных, а на внутренней — отрицательных зарядов. Разность зарядов приводит к возникновению мембранного потенциала, который в состоянии покоя мышечного волокна равен 90-100 мВ и является необходимым условием возникновения и проведения возбуждения.
Внутриклеточная жидкость называется саркоплазмой. В саркоплазме локализованы органические вещества, минеральные соли, а также субклеточные частицы: ядра, митохондрии, рибосомы, функция которых заключается в регуляции обмена веществ в мышечном волокне путем воздействия на синтез специфических мышечных белков.
Внутри саркоплазмы находится система продольных и поперечных трубочек, мембран, пузырьков, носящая название саркоплазматический ретикулум (SR). Толщина мембран SR около 6 нм. Саркоплазматический ретикулум делит саркоплазму на отдельные отсеки, в которых протекают различные биохимические процессы. Пузырьки и трубочки оплетают каждую миофибриллу. Через трубочки, связанные с наружной клеточной мембраной, возможен прямой обмен веществами между клеточными органеллами и межклеточной жидкостью. Трубочки могут служить и для распространения волны возбуждения от наружной мембраны волокна к внутренним его зонам. Мембраны пузырьков, прилегающих к миофибриллам, содержат белки, связывающие катионы кальция.
Значение саркоплазматического ретикулума очень велико. Он связан непосредственно с сокращением и расслаблением мышцы, регулируя освобождение катионов кальция в мышечном волокне. Кроме того, к части саркоплазматического ретикулума прикреплены рибосомы, назначением которых является синтез белков. B той части ретикулума, где нет рибосом, синтезируется ряд необходимых мышечному волокну веществ: липидов, кликогена. Одним из важнейших структурных компонентов мышечного волокна являются митохондрии. Число митохондрий в мышечном волокне очень велико, и располагаются они цепочками вдоль миофибрилл, тесно прилегая к мембранам ретикулума.
Как и у всякой клетки (оговоримся, что применение этого термина к мышечному волокну не совсем корректно), у мышечного волокна есть ядра, которые располагаются под сарколеммой. Ядро отделено от саркоплазмы двумя мембранами, одну из которых (внутреннюю) можно назвать ядерной, а вторая (наружная) является оболочкой ядра, переходящей в мембрану ретикулума. Пространство между этими двумя мембранами сообщается с канальцами саркоплазматического ретикулума. Внутри ядра находится ядрышко и хроматин. B состав хроматина входит ДНК, белки и низкомолекулярные РНК. В ДНК закодирована информация о структуре всех белков, синтезируемых в мышечном волокне.
B мышечном волокне есть и лизосомы, в которых локализованы гидролитические ферменты, расщепляющие белки, липиды и полисахариды. При очень интенсивной мышечной работе происходит нарушение мембран лизосом (либо увеличение их проницаемости) и в саркоплазму выходят ферменты, расщепляющие локализовaнные в ней биополимеры. Но это явление — не дисфункция.
studfile.net
Биохимия мышечной ткани
Мышцы составляют более 40% массы тела. Вся деятельность организма связана в той или иной мере с работой мышц. Функция сосудов и сердца, дыхание, пищеварение, выполнение работы обусловлено деятельностью мышечной ткани. Биохимия мышц служит основой для понимания многообразных функций мышечной ткани и играет большую роль в развитии знаний по физиологии, гигиене, понимании патогенеза заболеваний, связанных с поражением мышечной ткани (инфаркт миокарда, миодистрофии, коллагеновые болезни). В биоэнергетике мышечной ткани большое значение играет метаболизм адениловых и гуаниловых нуклеотидов, содержимое которых изменяется при патологических состояниях.
Цель: изучить молекулярную организацию мышечного волокна, дать представление о метаболических процессах, обеспечивающие мышцы энергией.
Особенности строения мышечного волокна
Мышца состоит из отдельных волокон, которые представляют собой мышечные клетки, окруженные плазматической мембраной (сарколемой). В цитоплазме находятся многочисленные ядра (100-200), митохондрии и другие обычные для клеток органеллы.
В мышечной клетке имеются миофибриллы (пучки белков), располагающиеся вдоль клетки, которые построены из белковых нитей (филаментов) двух типов – толстых (миозин) и тонких (актин). Функциональной единицей миофибриллы является участок, ограниченный двумя Z-пластинками, к М-линии прикреплены миозиновые нити своей серединой, активные нити прикреплены к Z-пластинкам. Чередование толстых (А-диски) и тонких (I-диски) нитей создает поперечную полосатость мышц.

Структура мышечного волокна Химический состав поперечно-полосатых и гладких мышц
а) Сократительные белки: актин, миозин;
б) регуляторные белки: тропомиозин, тропонин.
Сокращение – один из характерных признаков живого. Сокращение
живой протоплазмы – основа многообразных движений. Функция мышц обусловлена рядом биохимических процессов, при которых в мышечных волокнах химическая энергия трансформируется в энергию, совершаемую мышцей при сокращении. Всю мускулатуру животного организма можно подразделить на две группы: поперечно-полосатые или скелетные мышцы, обеспечивающие все произвольные движения, выполнение физической работы, и гладкие – непроизвольные движения внутренних органов.
Структурная единица мышцы – мышечное волокно (его длина до 10-12 см., диаметр 0,1-0,02 мм).
Оболочка мышечного волокна построена из эластичных нитей – белков стромы, позволяющей клетке сокращаться и растягиваться. Сократительными элементами мышечной ткани являются миофибриллы, расположенные в форме пучков в цитоплазме мышечного волокна. Под микроскопом видна поперечная исчерченность из-за оптической неоднородности входящих в их состав белков.
Скелетные мышцы теплокровных животных содержат 74-78% Н2О и 26-22% сухого вещества. Основная масса сухого вещества приходится на долю белков 18-20%. Липиды составляют 1-3%, соли 1,5-2%, углеводы 0,5-3%. Содержание белковых мышц достигает 20,9%.
На основании растворимости белки можно разделить на фракции (содержание в % к общему белку мышц):
миогеновая фракция — 28%
группа глобулина Ŷ — 20%
группа миозина — 30-50%
группа актина — 10-12%
группа стромы — 9,5%
тропомизин — 2,5%
миоглобин — 0,2-0,6%
Миогеновая фракция: легко извлекается из мышц водой, представляет собой белки типа альбуминов. Ряд белков этой фракции обладает ферментативной активностью, катализируют процессы анаэробного и аэробного распада углеводов. Это – альдолаза, изомераза.
Глобулин Ŷ – также обладает ферментативной активностью.
Миозин представляет собой две полипептидные цепи, свернутые в двойную спираль. Конец (головка) молекулы миозина имеет глобулярное строение и связан нековалентно с четырьмя дополнительными короткими полипептидными цепями. При обработке трипсином миозин распадается на 2 фракции: легкий меромиозин и тяжелый меромиозин Н.
Миозин – высокомолекулярный белок (более 440 000). Имеет участки,
обладающие АТФ-азной активностью, проявляющейся в присутствии Са2+
.
studfile.net