Калий — это… Что такое Калий?
| Внешний вид простого вещества | |
|---|---|
| Серебристо-белый мягкий металл | |
| Свойства атома | |
| Имя, символ, номер | Калий / Kalium (K), 19 |
| Атомная масса (молярная масса) | 39,0983[1]а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 4s1 |
| Радиус атома | 235 пм |
| Химические свойства | |
| Ковалентный радиус | 203 пм |
| Радиус иона | 133 пм |
| Электроотрицательность | 0,82 (шкала Полинга) |
| Электродный потенциал | −2,92 В |
| Степени окисления | 1 |
| Энергия ионизации (первый электрон) | |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,856 г/см³ |
| Температура плавления | 63,51°С; 336,8 K |
| Температура кипения | 1047 K |
| Теплота плавления | 2,33 кДж/моль |
| Теплота испарения | 76,9 кДж/моль |
| Молярная теплоёмкость | 29,6[2] Дж/(K·моль) |
| Молярный объём | 45,3 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмно-центрированная |
| Параметры решётки | 5,332 Å |
| Температура Дебая | 100 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 79,0 Вт/(м·К) |
Ка́лий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета.
В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они всё же отличаются.
История и происхождение названия
Калий (точнее, его соединения) использовался с давних времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K
В 1807 году английский химик Дэви электролизом расплава едкого кали (KOH) выделил калий и назвал его «потассий» (лат. potassium; это название до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Нахождение в природе
В свободном состоянии не встречается. Породообразующий элемент, входит в состав слюд, полевых шпатов и т.д. Также калий входит в состав сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl
Месторождения
Крупнейшие месторождения калия находятся на территории Канады (производитель PotashCorp), России (ОАО «Уралкалий», г. Березники, ОАО «Сильвинит», г. Соликамск, Пермский край, Верхнекамское месторождение калийных руд
Получение
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расплавленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Важное промышленное значение имеют и методы термохимического восстановления:
и восстановление из расплава хлорида калия карбидом кальция, алюминием или кремнием.[6][7]
Физические свойства
Калий под слоем ТГФКалий — серебристое вещество с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки, калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет
Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,5247 нм, Z = 2.
Химические свойства
Элементарный калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. На воздухе свежий срез быстро тускнеет из-за образования плёнок соединений (оксиды и карбонат). При длительном контакте с атмосферой способен полностью разрушиться. С водой реагирует со взрывом. Хранить его необходимо под слоем бензина, керосина или силикона, дабы исключить контакт воздуха и воды с его поверхностью. С Na, Tl, Sn, Pb, Bi калий образует интерметаллиды.
Взаимодействие с простыми веществами
Калий при комнатной температуре реагирует с кислородом воздуха, галогенами; практически не реагирует с азотом (в отличие от лития и натрия). При умеренном нагревании реагирует с водородом с образованием гидрида (200—350 °C):
,
с халькогенами (100—200 °C, E = S, Se, Te):
При сгорании калия на воздухе образуется надпероксид калия KO2 (с примесью K2O2):
В реакции с фосфором в инертной атмосфере образуется фосфид зелёного цвета (200 °C):
Взаимодействие со сложными веществами
Калий при комнатной температуре активно реагирует с водой, кислотами, растворяется в жидком аммиаке (−50 °C) с образованием тёмно-синего раствора.
Калий глубоко восстанавливает разбавленные серную и азотную кислоты:
При сплавлении металлического калия со щелочами он восстанавливает водород гидроксогруппы:
При умеренном нагревании реагирует с газообразным аммиаком с образованием амида (65—105 °C):
Металлический калий реагирует со спиртами с образованием алкоголятов:
Алкоголяты щелочных металлов (в данном случае, этаноат калия) являются очень сильными основаниями и широко используются в органическом синтезе.
Соединения с кислородом
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия. Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O
В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
Также известен озонид калия KO3, оранжево-красного цвета. Получить его можно взаимодействием гидроксида калия с озоном при температуре не выше 20 °C:
Озонид калия является очень сильным окислителем, например, окисляет элементарную серу до сульфата и дисульфата уже при 50 °C:
Гидроксид
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого кали при 20 °C в 100 г воды составляет 112 г.
Применение
- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава: натрий 12 %, калий 47 %, цезий 41 % — обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений.
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединения
Кристаллы перманганата калияБиологическая роль
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в организме человека
 | В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 12 мая 2011. |
Калий содержится большей частью в клетках, до 40 раз больше чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса. Калий и натрий между собой функционально связаны и выполняют следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых от 1800 до 5000 миллиграммов. Потребность в калии зависит от общего веса тела, физической активности, физиологического состояния, и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются сушёные абрикосы, дыня, бобы, киви, картофель, батат, авокадо, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Практически все сорта рыбы содержат более 200 мг калия в 100 г. Количество калия в разных видах рыбы различается. Овощи, грибы и травы также содержат много калия, однако в консервированных продуктах его уровень может быть гораздо меньше. Много калия содержится в шоколаде.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин B6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При переизбытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
Изотопы
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным с периодом полураспада 1,251·109 лет. В каждом грамме природного калия в секунду распадается в среднем 32 ядра 40K, благодаря чему, например, в организме человека массой 70 кг ежесекундно происходит около 4000 радиоактивных распадов. Поэтому легкодоступные в быту соединения калия (поташ, хлорид калия, калийная селитра и т. д.) можно использовать как пробные радиоактивные источники для проверки бытовых дозиметров. 40K наряду с ураном и торием считается одним из основных источников геотермальной энергии, выделяемой в недрах Земли (полная скорость энерговыделения оценивается в 40—44 ТВт). В минералах, содержащих калий, постепенно накапливается калий-аргоновый метод является одним из основных методов ядерной геохронологии.
См. также
Примечания
- ↑ Atomic Weights and Isotopic Compositions for All Elements. NIST Physical Measurement Laboratory. Архивировано из первоисточника 22 августа 2011. Проверено 16 ноября 2010.
- ↑ Химическая энциклопедия: в 5 т / Редкол.: Кнунянц И. Л. (гл. ред.). — М.: Советская энциклопедия, 1990. — Т. 2. — С. 284. — 671 с. — 100 000 экз.
- ↑ J. P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- ↑ КАЛИЙНОЕ МЕСТОРОЖДЕНИЕ
- ↑ Химическое и агрохимическое сырье.
- ↑ А. Ф. Алабышев, К. Д Грачев, С. А. Зарецкий, М. Ф. Лантратов, Натрий и калий (получение, свойства, применение), Л: Гос. н-т. изд-во хим. лит., 1959, С. 321.
- ↑ Хим.энциклопедия, т.2, М.: Сов. энциклопедия, 1990, С.562.
- ↑ Элементы: проба на окрашивание пламени (рус.). Архивировано из первоисточника 22 августа 2011. Проверено 26 января 2010.
Литература
- Пилипенко А. Т. Натрий и калий // Справочник по элементарной химии. — 2-е изд. — Киев: Наукова думка, 1978. — С. 316—319.
- Дроздов А. Яростные металлы // Энциклопедия для детей. Химия. — М.: Аванта +, 2002. — С. 184—187. — ISBN 5-8483-0027-5
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Некрасов Б. В. Основы общей химии. — М.: Химия, 1974.
- Спицын В. И., Мартыненко Л. И. Неорганическая химия. — М.: МГУ, 1991, 1994.
- Лидин Р. А. и др. Элементы IA-группы. Калий // Химические свойства неорганических веществ: Уч. пособие для вузов. — 4-е изд. — М.: КолосС, 2003. — С. 29—40. — ISBN 5-9532-0095-1
Ссылки
 Электрохимический ряд активности металлов Электрохимический ряд активности металлов | |
|---|---|
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2, W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, Au |
| ||||||||||||
dic.academic.ru
Калия — это… Что такое Калия?
 Кришна танцует на головах змея Калия.
Кришна танцует на головах змея Калия.Калия (санскр. कालिया, Kāliyā IAST) в индуистской мифологии — огромный многоголовый демон-змей, живший в реке Ямуне в районе Вриндаваны и укрощённый Кришной. История Кришны и змея Калии описывается в Пуранах.
Согласно древнему обычаю, наги регулярно приносили Гаруде в дар пищу.[1] Однажды Калия возгордился и съел подношение, принесённое другими нагами для царя пернатых.[1] Гаруда пришёл в ярость и набросился на Калию, намереваясь убить его за проявленную дерзость.[1] Калия уставился на Гаруду множеством своих немигающих глаз, распахнул свои пасти и обнажив острые клыки, полные смертельного яда, всячески пытался укусить противника, бросаясь на него подобно молнии.[1] Гаруда каждый раз оказывался проворнее и уклонялся от укуса, а затем изловчился и тяжело ударил Калию своим мощным крылом.[1] Испуганный Калия пустился в бегство и, скрываясь от острых когтей Гаруды, скрылся в водах Ямуны, которых Гаруда не смел касаться из-за проклятия, полученного им ранее от святого мудреца.[1]
Однажды Гаруда поймал в Ямуне рыбу, и, намереваясь утолить голод, приготовился съесть её.[1] В этот момент к нему подошёл благочестивый риши и попросил его пощадить рыбе жизнь, отпустив её назад в реку.[1] Однако Гаруду терзал такой жестокий голод, что он не смог удержаться и съел пойманную им рыбу.[1] Мудрец сильно разгневался и проклял Гаруду, сказав, что если тот когда-либо ещё коснется вод Ямуны, то в тот же час и погибнет.[1] Калия знал об этом проклятии и потому укрылся от Гаруды в большом озере, находившимся под руслом Ямуны.[1] Водоём этот соединялся с Ямуной тесным проходом, через который смертельный яд змея попадал в воды реки и отравлял в ней всё живое.[1] Вся растительность на берегах Ямуны высохла. Птицы, пролетавшие над рекой, погибали от ядовитых испарений и падали в воду.[2] Когда ветер приносил ядовитые пары в лесные чащи, всё живое в лесах погибало.[2]
Однажды Кришна пригнал на водопой к Ямуне стадо телят.[1] На песчаном берегу реки он увидел мёртвые тела своих друзей, мальчиков-пастушков, а рядом с ними — павшее коровье стадо.[1] Пастухи и коровы погибли, напившись воды из Ямуны, отравленной Калией.[1] Тогда Кришна забрался на вершину дерева кадамба, нависшего над водою, и прыгнул в ядовитые воды реки.[2] Кришна начал как ни в чём не бывало плескаться, плавать и играть в воде, весело ударяя ладонями по ядовитым волнам.[2] Шум плеска воды и радостные клики Кришны разозлили Калию.[2] Многоглавый змей всплыл на поверхность и тугими кольцами обвил тело маленького Кришны.[2] В это время на берегу реки появились друзья Кришны. Увидев его в объятиях змея, они преисполнились ужаса и без чувств пали на землю, а телята протяжно замычали и заплакали горючими слезами.[2]
В это самое время во Вриндаване появились дурные предзнаменования, предвещавшие беду.[2] Жители Вриндавана пришли в великое беспокойство и отправились на поиски Кришны.[2] Его следы привели их к берегу Ямуны.[3] Узрев любимого Кришну недвижимым в смертельных объятиях змея, они горько заплакали и собрались было броситься в реку на помощь Кришне, но Баларама остановил их.[3] Вдруг тело Кришны стало расширяться и разомкнуло кольца Калии.[3] При виде оказавшегося на свободе Кришны, Калия пришёл в неистовую ярость.[3] Описывается, что его смрадное дыхание жгло как огонь, смертельный яд вытекал из его ртов и капал в воду, языки его алчно шевелились, и множество немигающих глаз с ненавистью уставились на Кришну, стремясь лишить его всякой силы.[3] Калия бросился на Кришну, который волчком стал вращаться в воде вокруг змея, приведя его ещё в большую ярость.[3] Когда силы Калии совсем иссякли и он уронил свои головы в воду, Кришна вскочил на него и стал плясать, перепрыгивая с одной головы на другую.[3] Изнемождённый Калия вновь и вновь тщетно пытался укусить Кришну, который не давал подняться его головам.[3] Калия, теряя последние силы, всё глубже и глубже погружался в воду.[3] Тогда жёны Калии, наблюдавшие за происходящим, стали возносить Кришне молитвы, прося пощадить их супруга.[3] Сжалившись над ними, Кришна перестал топтать змея и отпустил его на волю, повелев ему покинуть Ямуну и поселиться со всеми родичами в океане на острове Раманака (ассоциируется с островом Вити-Леву), где Гаруда не станет чинить им препятствий.[3] После ухода Калии Ямуна очистилась от яда, воды её прояснились, берега покрылись растительностью, а пастухи и коровы, умершие ранее от ядовитых испарений, снова вернулись к жизни.[4]
См. также
Примечания
Ссылки
dic.academic.ru
калий — это… Что такое калий?
КА́ЛИЙ -я; м. [араб. kali] Химический элемент (K), металл серебристо-белого цвета, добываемый из углекалиевой соли (поташа).
◁ Ка́лиевый, -ая, -ое. К-ые месторождения. К-ые соли. Кали́йный, -ая, -ое. К-ая промышленность. К-ые удобрения.
КА́ЛИЙ (лат. Kalium), K (читается «калий»), химический элемент с атомным номером 19, атомная масса 39,0983.Калий встречается в природе в виде двух стабильных нуклидов (см. НУКЛИД): 39К (93,10% по массе) и 41К (6,88%), а также одного радиоактивного 40К (0,02%). Период полураспада калия-40 Т1/2 примерно в 3 раза меньше, чем Т1/2 урана-238 и составляет 1,28 миллиарда лет. При b-распаде калия-40 образуется стабильный кальций-40, а при распаде по типу электронного захвата (см. ЭЛЕКТРОННЫЙ ЗАХВАТ) образуется инертный газ аргон-40.
Калий принадлежит к числу щелочных металлов (см. ЩЕЛОЧНЫЕ МЕТАЛЛЫ). В периодической системе Менделеева калий занимает место в четвертом периоде в подгруппе IА. Конфигурация внешнего электронного слоя 4s1, поэтому калий всегда проявляет степень окисления +1 (валентность I).
Атомный радиус калия 0,227 нм, радиус иона K+ 0,133 нм. Энергии последовательной ионизации атома калия 4,34 и 31,8 эВ. Электроотрицательность (см. ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ) калия по Полингу 0,82, что говорит о его ярко выраженных металлических свойствах.
В свободном виде — мягкий, легкий, серебристый металл.
История открытия
Соединения калия, как и его ближайшего химического аналога — натрия (см. НАТРИЙ), были известны с древности и находили применение в различных областях человеческой деятельности. Однако сами эти металлы были впервые выделены в свободном состоянии только в 1807 в ходе экспериментов английского ученого Г. Дэви (см. ДЭВИ Гемфри). Дэви, используя гальванические элементы как источник электрического тока, провел электролиз расплавов поташа (см. ПОТАШ) и каустической соды (см. КАУСТИЧЕСКАЯ СОДА) и таким образом выделил металлические калий и натрий, которые назвал «потассием» (отсюда сохранившееся в англоязычных странах и Франции название калия — potassium) и «содием». В 1809 английский химик Л. В. Гильберт предложил название «калий» (от арабского аль-кали — поташ).
Нахождение в природе
Содержание калия в земной коре 2,41% по массе, калий входит в первую десятку наиболее распространенных в земной коре элементов. Основные минералы, содержащие калий: сильвин (см. СИЛЬВИН) KСl (52,44% К), сильвинит (Na,K)Cl (этот минерал представляет собой плотно спрессованную механическую смесь кристалликов хлорида калия KCl и хлорида натрия NaCl), карналлит (см. КАРНАЛЛИТ) KCl·MgCl2·6H2O (35,8% К), различные алюмосиликаты (см. АЛЮМОСИЛИКАТЫ), содержащие калий, каинит (см. КАИНИТ) KCl·MgSO4·3H2O, полигалит (см. ПОЛИГАЛИТ) K2SO4·MgSO4·2CaSO4·2H2O, алунит (см. АЛУНИТ) KAl3(SO4)2(OH)6. В морской воде содержится около 0,04% калия.
Получение
В настоящее время калий получают при взаимодействии с жидким натрием расплавленных KOH (при 380—450°C) или KCl (при 760—890°C):
Na + KOH = NaOH + K
Калий также получают электролизом расплава KCl в смеси с K2CO3 при температурах, близких к 700°C:
2KCl = 2K + Cl2
От примесей калий очищают вакуумной дистилляцией.
Физические и химические свойства
Металлический калий мягок, он легко режется ножом и поддается прессованию и прокатке. Обладает кубической объемно центрированной кубической решеткой, параметр а = 0,5344 нм. Плотность калия меньше плотности воды и равна 0,8629 г/см3. Как и все щелочные металлы, калий легко плавится (температура плавления 63,51°C) и начинает испаряться уже при сравнительно невысоком нагревании (температура кипения калия 761°C).
Калий, как и другие щелочные металлы, химически очень активен. Легко взаимодействует с кислородом воздуха с образованием смеси, преимущественно состоящей из пероксида К2О2 и супероксида KO2 (К2О4):
2K + O2 = K2O2, K + O2 = KO2.
При нагревании на воздухе калий сгорает фиолетово-красным пламенем. С водой и разбавленными кислотами калий взаимодействует со взрывом (воспламеняется образующийся водород):
2K + 2H2O = 2KOH + H2
Кислородсодержащие кислоты при таком взаимодействии могут восстанавливаться. Например, атом серы серной кислоты восстанавливается до S, SO2 или S2–:
8К + 4Н2SO4 = K2S + 3K2SO4 + 4H2O.
При нагревании до 200—300 °C калий реагирует с водородом с образованием солеподобного гидрида КН:
2K + H2 = 2KH
С галогенами (см. ГАЛОГЕНЫ) калий взаимодействует со взрывом. Интересно отметить, что с азотом калий не взаимодействует.
Как и другие щелочные металлы, калий легко растворяется в жидком аммиаке с образованием голубых растворов. В таком состоянии калий используют для проведения некоторых реакций. При хранении калий медленно реагирует с аммиаком с образованием амида KNH2:
2K + 2NH3 жидк. = 2KNH2 + H2
Важнейшие соединения калия: оксид К2О, пероксид К2О2, супероксид К2О4, гидроксид КОН, иодид KI, карбонат K2CO3 и хлорид KCl.
Оксид калия К2О, как правило, получают косвенным путем за счет реакции пероксида и металлического калия:
2K + K2O2 = 2K2O
Этот оксид проявляет ярко выраженные основные свойства, легко реагирует с водой с образованием гидроксида калия КОН:
K2O + H2O = 2KOH
Гидроксид калия, или едкое кали, хорошо растворим в воде (до 49,10% массе при 20°C). Образующийся раствор — очень сильное основание, относящееся к щелочам (см. ЩЕЛОЧИ). КОН реагирует с кислотными и амфотерными оксидами:
SO2 + 2KOH = K2SO3 + H2O,
Al2O3 + 2KOH + 3H2O = 2K[Al(OH)4] (так реакция протекает в растворе) и
Al2O3 + 2KOH = 2KAlO2 + H2O (так реакция протекает при сплавлении реагентов).
В промышленности гидроксид калия KOH получают электролизом водных растворов KCl или K2CO3 c применением ионообменных мембран и диафрагм:
2KCl + 2H2O = 2KOH + Cl2+ H2,
или за счет обменных реакций растворов K2CO3 или K2SO4 с Ca(OH)2 или Ba(OH)2:
K2CO3 + Ba(OH)2 = 2KOH + BaCO3
Попадание твердого гидроксида калия или капель его растворов на кожу и в глаза вызывает тяжелые ожоги кожи и слизистых оболочек, поэтому работать с этими едкими веществами следует только в защитных очках и перчатках. Водные растворы гидроксида калия при хранении разрушают стекло, расплавы — фарфор.
Карбонат калия K2CO3 (обиходное название поташ) получают при нейтрализации раствора гидроксида калия углекислым газом:
2KOH + CO2 = K2CO3 + Н2О.
В значительных количествах поташ содержится в золе некоторых растений.
Применение
Металлический калий — материал для электродов в химических источниках тока. Сплав калия с другим щелочным металлом — натрием находит применение в качестве теплоносителя (см. ТЕПЛОНОСИТЕЛЬ) в ядерных реакторах.
В гораздо больших масштабах, чем металлический калий, находят применение его соединения. Калий — важный компонент минерального питания растений, он необходим им в значительных количествах для нормального развития, поэтому широкое применение находят калийные удобрения (см. КАЛИЙНЫЕ УДОБРЕНИЯ): хлорид калия КСl, нитрат калия, или калийная селитра, KNO3, поташ K2CO3 и другие соли калия. Поташ используют также при производстве специальных оптических стекол, как поглотитель сероводорода при очистке газов, как обезвоживающий агент и при дублении кож.
В качестве лекарственного средства находит применение иодид калия KI. Иодид калия используют также в фотографии и в качестве микроудобрения. Раствор перманганата калия КMnO4 («марганцовку») используют как антисептическое средство.
По содержанию в горных породах радиоактивного 40К определяют их возраст.
Калий в организме
Калий — один из важнейших биогенных элементов (см. БИОГЕННЫЕ ЭЛЕМЕНТЫ), постоянно присутствующий во всех клетках всех организмов. Ионы калия К+ участвуют в работе ионных каналов (см. ИОННЫЕ КАНАЛЫ) и регуляции проницаемости биологических мембран (см. БИОЛОГИЧЕСКИЕ МЕМБРАНЫ), в генерации и проведении нервного импульса, в регуляции деятельности сердца и других мышц, в различных процессах обмена веществ. Содержание калия в тканях животных и человека регулируется стероидными гормонами надпочечников. В среднем организм человека (масса тела 70 кг) содержит около 140 г калия. Поэтому для нормальной жизнедеятельности с пищей в организм должно поступать 2—3 г калия в сутки. Богаты калием такие продукты, как изюм, курага, горох и другие.
Особенности обращения с металлическим калием
Металлический калий может вызвать очень сильные ожоги кожи, при попадании мельчайших частичек калия в глаза возникают тяжелые поражения с потерей зрения, поэтому работать с металлическим калием можно только в защитных перчатках и очках. Загоревшийся калий заливают минеральным маслом или засыпают смесью талька и NaCl. Хранят калий в герметично закрытых железных контейнерах под слоем обезвоженного керосина или минерального масла.
dic.academic.ru
Калий — Медицинская энциклопедия
I
(Kalium, К)
химический элемент главной подгруппы I группы периодической системы элементов Д.И. Менделеева, один из основных внутриклеточных катионов, присутствует также во внеклеточной среде всех живых организмов, принимает участие в образовании и поддержании потенциала на клеточных мембранах.
Атомный номер калия 19, атомная масса 39,102. В природе существуют изотопы калия 39К, 40К, 41К. Изотоп 40К слабо радиоактивен, около 90% естественной радиоактивности организмов млекопитающих обеспечивается именно этим изотопом.
Калий — мягкий металл, его свежий срез имеет серебристо-белый цвет. Относительная плотность 0,862 г/см3 t°пл. 63,5°, t°кип. 760°. Химически активен, сильный восстановитель, бурно реагирует с водой. Валентность + 1. В свободном виде К. в природе не встречается ввиду его высокой химической реактивности. В основном в природе К. присутствует в виде солей. В организме человека и животных 98% всего К. находится внутри клеток, главным образом в ионизированной форме в виде катиона К+ Содержание К. в тканях животных составляет 6—10 мэкв/100 г сырой ткани. В организме человека содержится 160—250 г (4000—9000 мэкв) калия. Концентрация К. в разных тканях человека составляет (в мэкв/кг массы ткани): в костях — 15, зубах — 17, скелетных мышцах — 100, миокарде — 64, легких — 38, головном мозге — 84, печени — 55, почках — 45, эритроцитах — 115. Концентрация К. (в ммоль/л) в сыворотке крови составляет 4,5 (3,4—5,3), в цереброспинальной жидкости — 3,0, лимфе — 2,2.
Суточная потребность в К. для взрослых людей составляет 2—3 г (50—75 мэкв), для ребенка 16—30 мг/кг массы тела; необходимый минимум поступления К. в организм взрослого человека равен около 1 г/сут. Высоким содержанием К. отличаются абрикосы, персики, апельсины, бананы, ананасы, картофель, капуста, морковь, помидоры, салат, шпинат, редька и др. Недостаток калия в рационе ведет к дистрофии даже при нормальном потреблении белка.
Полученный с пищей К. всасывается в кишечнике, с кровью поступает в печень, а затем в периферический кровоток. Скорость обмена ионов К+ между клетками и внеклеточной жидкостью максимальна в почках, легких и кишечнике, несколько ниже она в печени, селезенке и мышцах, наиболее низкую величину такого обмена отмечаю; в эритроцитах, головном мозге, костях. около 80—90% поступившего с пищей К. выводится с мочой. В норме 1 л мочи содержит 42,8—85,6 мэкв калия, за сутки с мочой выводится 2—4 г калия. Значительно меньшее количество К. экскретируется с калом, немного К. выводится с потом.
В почках происходят фильтрация К. из плазмы крови, реабсорбция его в проксимальных отделах почечных канальцев и активная секреция калия клетками дистальных отделов почечных канальцев. Регуляция калийуреза осуществляется гипоталамическими нейрогормонами и гипофизарными гормонами, стероидными гормонами коры надпочечников, в первую очередь альдостероном, а также ц.н.с. (см. Водно-солевой обмен). Интенсивность выведения К. зависит от кислотно-щелочного состояния. Содержание К. в плазме крови находится в обратной зависимости от величины рН крови (см. Водородный показатель)
Концентрация ионов К+ существенно влияет на осмотическое давление в клетках. Одной из важнейших функций К является поддержание потенциала, образующегося на клеточной мембране. В возбудимых клетках содержание К. во много раз выше, а содержание натрия во много раз ниже, чем во внеклеточной жидкости. Мембранный потенциал покоя — разность потенциалов между клеточным содержимым и окружающей клетку средой — определяется градиентом концентрации ионов К+ снаружи и внутри мембраны (см. Мембраны биологические). Асимметричное распределение ионов К+ и Na+ обеспечивается и поддерживается работой Na+, К+-зависимой АТФ-азы (так называемого Na+, К+-ионного насоса) — фермента, локализованного в плазматической мембране и осуществляющего выведение из клетки трех ионов Na+ и аккумуляцию двух ионов К+. При возбуждении клетки происходит образование мембранного потенциала действия, проницаемость мембраны резко увеличивается сначала для ионов Na+, а затем и для ионов К+. После деполяризации мембраны ее исходный потенциал восстанавливается за счет активной работы Na+, К+-ионного насоса
Наличие конкурентных взаимоотношений между ионами К+ и Na+ и ионами К+ и Н+ обусловливает участие К. в регуляции кислотно-щелочного равновесия (Кислотно-щелочное равновесие) в организме. Нарушения гомеостаза ведут к патологическим нарушениям обмена К. Недостаток К. в пище вызывает его дефицит в организме, а затем и снижение концентрации в крови ниже 4 мэкв/л — гипокалиемию (Гипокалиемия). Гипокалиемию отмечают также в результате неправильного применения салуретиков, при поражении почечных канальцев при нефропатиях и Гиперальдостеронизме. Недостаточность К. ведет к нарушениям функции нервно-мышечной и сердечно-сосудистой систем и проявляется дискоординацией движений, сонливостью, спутанностью сознания, болью в мышцах, тремором конечностей, брадикардией, артериальной гипотензией. характерными изменениями на ЭКГ. При нарушении функции почек снижение общего содержания К. в организме может сопровождаться повышением его концентрации в крови — гиперкалиемией (концентрация ионов К+ в сыворотке крови превышает 6 мэкв/л), которую отмечают также при метаболическом ацидозе, печеночной недостаточности, передозировке некоторых лекарственных средств. Избыток К. встречается реже, чем его дефицит, клинически он проявляется (например, при интоксикациях соединениями калия) параличами конечностей, характерными для гиперкалиемии изменениями на ЭКГ (уменьшение вольтажа и уширение зубца Р при возможном сочетании с синоаурикулярной блокадой и признаками атриовентрикулярной блокады разной степени, а также замедление внутрижелудочковой проводимости — уширение интервала QRS— и ускорение конечной фазы реполяризации со значительным увеличением зубца Т, особенно в правых грудных отведениях; выраженность этих изменений в большой степени зависит от скорости развития гиперкалиемии) и др.
Различные соединения К. используются в качестве лекарственных средств. Это главным образом органические соли К. (калия оротат, калия аспарагинат, калия ацетат) и неорганические соли К. (калия хлорид), которые являются мочегонными средствами (Мочегонные средства) и противоаритмическими средствами (Противоаритмические средства).
Библиогр.: Крю Ж. Биохимия, Медицинские и биологические аспекты, пер. с франц., с. 46, М., 1979; Лабораторные методы исследования в клинике, под ред. В.В. Меньшикова, с.261, 263, М., 1987.
II
Калий (Kalium; К)
химический элемент I группы периодической системы Д.И. Менделеева; атомный номер 19, атомная масса 39,102; является необходимым компонентом внутренней среды всех живых организмов, участвуя в ряде жизненно важных процессов; некоторые соединения К. применяются в медицине как лекарственные средства.
Источник: Медицинская энциклопедия на Gufo.me
Значения в других словарях
- калий — -я, м. Химический элемент, металл серебристо-белого цвета, добываемый из углекалиевой соли (поташа). [араб. kali] Малый академический словарь
- калий — КАЛИЙ (Kalium) , хим. элемент I гр. периодич. системы элементов Менделеева. Металл. Химически очень активен. В свободном состоянии в природе не встречается. Содержание К. в литосфере 2,5% (по массе). Входит в состав полевого шпата, слюды, нефелина. Сельскохозяйственный словарь
- Калий — (нем. Kalium, франц. и англ. Potassium) — один из важнейших представителей группы щелочных металлов. «Едкое кали есть типичная щелочь, подобная едкому натру, как кислоты серная, азотная, соляная суть типичные кислоты… Энциклопедический словарь Брокгауза и Ефрона
- Калий — Калий авт. юморист. рассказов (Одесса, 1910—1912). {Венгеров} Большая биографическая энциклопедия
- калий — Калий, калии, калия, калиев, калию, калиям, калий, калии, калием, калиями, калии, калиях Грамматический словарь Зализняка
- калий — К’АЛИЙ, калия, мн. нет, ·муж., и кали, нескл., ср. (·араб. — поташ) (·хим. ). Химический элемент — щелочный металл серебристо-белого цвета, добываемый из углекалиевой соли. Толковый словарь Ушакова
- калий — сущ., кол-во синонимов: 4 металл 86 потассий 1 поташ 6 элемент 159 Словарь синонимов русского языка
- Калий — (Kalium) К, химический элемент 1 группы периодической системы Менделеева; атомный номер 19, атомная масса 39,098; серебряно-белый, очень лёгкий, мягкий и легкоплавкий металл. Большая советская энциклопедия
- калий — калий м. Химический элемент, серебристо-белый, мягкий, легкоплавкий металл, применяющийся (в соединениях) в сельском хозяйстве, промышленности, фармакологии и т.п. Толковый словарь Ефремовой
- калий — [ар.; см. кали] – хим. элемент из группы щелочных металлов, серебристо-белого цвета, символ К, порядковый помер 19, атомный вес 39,096; на воздухе легко окисляется; встречается в природе только в виде соединений (селитра, поташ, граниты, слюда и др. Большой словарь иностранных слов
- калий — КАЛИЙ, я, м. Химический элемент, мягкий металл серебристо-белого цвета. | прил. калиевый, ая, ое и калийный, ая, ое. Калиевые соли. Калийные удобрения. Толковый словарь Ожегова
- калий — КАЛИЙ -я; м. [араб. kali] Химический элемент (K), металл серебристо-белого цвета, добываемый из углекалиевой соли (поташа). ◁ Калиевый, -ая, -ое. К-ые месторождения. К-ые соли. Калийный, -ая, -ое. К-ая промышленность. К-ые удобрения. Толковый словарь Кузнецова
- КАЛИЙ — КАЛИЙ (символ К), распространенный химический элемент, относящийся к ЩЕЛОЧНЫМ МЕТАЛЛАМ. Впервые был выделен сэром Хэмфри Дэви в 1807 г. Его основными рудами являются сильвин (хлорид калия), карналлит и полигалит. Научно-технический словарь
- КАЛИЙ — КАЛИЙ (лат. Kalium) — К, химический элемент I группы периодической системы, атомный номер 19, атомная масса 39,0983, относится к щелочным металлам. Название от араб. аль-кали — поташ (давно известное соединение калия, добывающееся из древесной золы). Большой энциклопедический словарь
- калий — КАЛИЙ м. потасий, металл, составляющий основанье кали, весьма сходный с натрием (содием). Кали ср. несклон., растительная щелочь или щелочная соль; углекислый калий, чистый поташ. Калиевый, к калию относящ. Калистый, содержащий кали. Толковый словарь Даля
- калий — КАЛИЙ (от араб. аль-кали — поташ; лат. Kalium) K хим. элемент I гр. периодической системы; относится к щелочным металлам, ат. н. 19, ат. м. 39,0983. Химическая энциклопедия
- калий — орф. калий, -я Орфографический словарь Лопатина
- Калий — K (от араб, аль-кали — поташ * a. Potassium, potash; н. Kalium; ф. potassium; и. potasio), — хим. элемент I группы периодич. системы Mенделеева, ат.н. 19, ат. м. 39,102. Природный K. Горная энциклопедия
- калий — Ка́л/ий/. Морфемно-орфографический словарь

gufo.me
Калий — Википедия. Что такое Калий
| Внешний вид простого вещества | |
|---|---|
| Серебристо-белый мягкий металл | |
| Свойства атома | |
| Название, символ, номер | Калий / Kalium (K), 19 |
| Атомная масса (молярная масса) | 39,0983(1)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 4s1 |
| Радиус атома | 235 пм |
| Химические свойства | |
| Ковалентный радиус | 203 пм |
| Радиус иона | 133 пм |
| Электроотрицательность | 0,82 (шкала Полинга) |
| Электродный потенциал | −2,92 В |
| Степени окисления | 0; +1 |
| Энергия ионизации (первый электрон) | 418,5 (4,34) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,856 г/см³ |
| Температура плавления | 336,8К; 63,65 °C |
| Температура кипения | 1047К; 773,85 °C |
| Уд. теплота плавления | 2,33 кДж/моль |
| Уд. теплота испарения | 76,9 кДж/моль |
| Молярная теплоёмкость | 29,6[2] Дж/(K·моль) |
| Молярный объём | 45,3 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмно-центрированная |
| Параметры решётки | 5,332 Å |
| Температура Дебая | 100 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 79,0 Вт/(м·К) |
| Номер CAS | 7440-09-7 |
| Эмиссионный спектр | |
 | |
Ка́лий — элемент первой группы (по старой классификации — главной подгруппы первой группы), четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий — мягкий щелочной металл серебристо-белого цвета.
В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь.
Во многих свойствах калий очень близок натрию, но с точки зрения биологической функции и использования клетками живых организмов они антагонистичны.
История и происхождение названия
Соединения калия используются с древнейших времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил о выделении калия электролизом расплава едкого кали (KOH)[3](в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года[4]) и назвал его «потасий» (лат. potasium[3]:32; это название (правда, в некоторых языках с двумя буквами s) до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Нахождение в природе
В свободном состоянии не встречается. Породообразующий элемент, входит в состав слюд, полевых шпатов и т. д. Также калий входит в состав сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел Биологическая роль). Кларк калия в земной коре составляет 2,4 % (5-й по распространённости металл, 7-й по содержанию в коре элемент). Концентрация в морской воде — 380 мг/л[5].
Месторождения
Крупнейшие месторождения калия находятся на территории Канады (производитель PotashCorp), России (ПАО «Уралкалий», г. Березники, г. Соликамск, Пермский край, Верхнекамское месторождение калийных руд[6]), Белоруссии (ПО «Беларуськалий», г. Солигорск, Старобинское месторождение калийных руд[7]).
Получение
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расплавленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
- K++e−→K{\displaystyle {\mathsf {K^{+}+e^{-}\rightarrow K}}}
- 2Cl−→Cl2{\displaystyle {\mathsf {2Cl^{-}\rightarrow Cl_{2}}}}
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
- 4OH−→2h3O+O2{\displaystyle {\mathsf {4OH^{-}\rightarrow 2H_{2}O+O_{2}}}}
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Важное промышленное значение имеют и методы термохимического восстановления:
- Na+KOH→N2380−450oCNaOH+K{\displaystyle {\mathsf {Na+KOH{\xrightarrow[{N_{2}}]{380-450^{o}C}}NaOH+K}}}
и восстановление из расплава хлорида калия карбидом кальция, алюминием или кремнием.[8][9]
Физические свойства
Калий под слоем ТГФКалий — серебристый металл с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки, калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет[10].
Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH.Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,5247 нм, Z = 2.
Химические свойства
Элементарный калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. На воздухе свежий срез быстро тускнеет из-за образования плёнок соединений (оксиды и карбонат). При длительном контакте с атмосферой способен полностью разрушиться. С водой реагирует со взрывом. Хранить его необходимо под слоем бензина, керосина или силикона, дабы исключить контакт воздуха и воды с его поверхностью. С Na, Tl, Sn, Pb, Bi калий образует интерметаллиды.
Взаимодействие с простыми веществами
Калий при комнатной температуре реагирует с кислородом воздуха, галогенами; практически не реагирует с азотом (в отличие от лития и натрия). При умеренном нагревании реагирует с водородом с образованием гидрида (200—350 °C):
- 2K+h3⟶2KH{\displaystyle {\mathsf {2K+H_{2}\longrightarrow 2KH}}}
с халькогенами (100—200 °C, E = S, Se, Te):
- 2K+E⟶K2E{\displaystyle {\mathsf {2K+E\longrightarrow K_{2}E}}}
При сгорании калия на воздухе образуется надпероксид калия KO2 (с примесью K2O2):
- K+O2⟶KO2{\displaystyle {\mathsf {K+O_{2}\longrightarrow KO_{2}}}}
В реакции с фосфором в инертной атмосфере образуется фосфид зелёного цвета (200 °C):
- 3K+P⟶K3P{\displaystyle {\mathsf {3K+P\longrightarrow K_{3}P}}}
Взаимодействие со сложными веществами
Калий при комнатной температуре (20*С) активно реагирует с водой, кислотами, растворяется в жидком аммиаке (−50 °C) с образованием тёмно-синего раствора.
- 2K+2h3O⟶2KOH+h3↑{\displaystyle {\mathsf {2K+2H_{2}O\longrightarrow 2KOH+H_{2}\uparrow }}}
- 2K+2HCl⟶2KCl+h3↑{\displaystyle {\mathsf {2K+2HCl\longrightarrow 2KCl+H_{2}\uparrow }}}
- K+6Nh4⟶[K(Nh4)]6{\displaystyle {\mathsf {K+6NH_{3}\longrightarrow [K(NH_{3})]_{6}}}}
Калий глубоко восстанавливает разбавленные серную и азотную кислоты:
- 8K+6h3SO4⟶4K2SO4+SO2↑+S↓+6h3O{\displaystyle {\mathsf {8K+6H_{2}SO_{4}\longrightarrow 4K_{2}SO_{4}+SO_{2}\uparrow +S\downarrow +6H_{2}O}}}
- 21K+26HNO3⟶21KNO3+NO↑+N2O↑+N2↑+13h3O{\displaystyle {\mathsf {21K+26HNO_{3}\longrightarrow 21KNO_{3}+NO\uparrow +N_{2}O\uparrow +N_{2}\uparrow +13H_{2}O}}}
При сплавлении металлического калия со щелочами он восстанавливает водород гидроксогруппы:
- 2K+2KOH⟶2K2O+h3↑(450∘C){\displaystyle {\mathsf {2K+2KOH\longrightarrow 2K_{2}O+H_{2}\uparrow (450^{\circ }C)}}}
При умеренном нагревании реагирует с газообразным аммиаком с образованием амида (65—105 °C):
- 2K+2Nh4⟶2KNh3+h3{\displaystyle {\mathsf {2K+2NH_{3}\longrightarrow 2KNH_{2}+H_{2}}}}
Металлический калий реагирует со спиртами с образованием алкоголятов:
- 2K+2C2H5OH⟶2C2H5OK+h3↑{\displaystyle {\mathsf {2K+2C_{2}H_{5}OH\longrightarrow 2C_{2}H_{5}OK+H_{2}\uparrow }}}
Алкоголяты щелочных металлов (в данном случае − этанолат калия) являются очень сильными основаниями и широко используются в органическом синтезе.
Соединения с кислородом
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
- K+O2⟶KO2{\displaystyle {\mathsf {K+O_{2}\longrightarrow KO_{2}}}}
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
- KO2+3K⟶2K2O{\displaystyle {\mathsf {KO_{2}+3K\longrightarrow 2K_{2}O}}}
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
- K2O2+2h3O⟶2KOH+h3O2{\displaystyle {\mathsf {K_{2}O_{2}+2H_{2}O\longrightarrow 2KOH+H_{2}O_{2}}}}
- 4KO2+2h3O⟶4KOH+3O2↑{\displaystyle {\mathsf {4KO_{2}+2H_{2}O\longrightarrow 4KOH+3O_{2}\uparrow }}}
- 4KO2+2CO2⟶2K2CO3+3O2↑{\displaystyle {\mathsf {4KO_{2}+2CO_{2}\longrightarrow 2K_{2}CO_{3}+3O_{2}\uparrow }}}
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия. Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
Также известен озонид калия KO3, оранжево-красного цвета. Получить его можно взаимодействием гидроксида калия с озоном при температуре не выше 20 °C:
- 4KOH+4O3⟶4KO3+O2+2h3O{\displaystyle {\mathsf {4KOH+4O_{3}\longrightarrow 4KO_{3}+O_{2}+2H_{2}O}}}
Озонид калия является очень сильным окислителем, например, окисляет элементарную серу до сульфата и дисульфата уже при 50 °C:
- 6KO3+5S⟶K2SO4+2K2S2O7{\displaystyle {\mathsf {6KO_{3}+5S\longrightarrow K_{2}SO_{4}+2K_{2}S_{2}O_{7}}}}
Гидроксид
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого кали при 20 °C в 100 г воды составляет 112 г.
Применение
- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава: натрий 12 %, калий 47 %, цезий 41 % — обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений. Калий является одним из трех базовых элементов, которые необходимы для роста растений наряду с азотом и фосфором. В отличие от азота и фосфора, калий является основным клеточным катионом. При его недостатке у растения прежде всего нарушается структура мембран хлоропластов — клеточных органелл, в которых проходит фотосинтез. Внешне это проявляется в пожелтении и последующем отмирании листьев. При внесении калийных удобрений у растений увеличивается вегетативная масса, урожайность и устойчивость к вредителям.
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединения
- Бромид калия применяется в медицине и как успокаивающее средство для нервной системы.
- Гидроксид калия (едкое кали) применяется в щелочных аккумуляторах и при сушке газов.
- Карбонат калия (поташ) используется как удобрение, при варке стекла, как кормовая добавка для птицы.
- Хлорид калия (сильвин, «калийная соль») используется как удобрение.
- Нитрат калия (калийная селитра) — удобрение, компонент чёрного пороха.
- Перхлорат и хлорат калия (бертолетова соль) используются в производстве спичек, ракетных порохов, осветительных зарядов, взрывчатых веществ, в гальванотехнике.
- Дихромат калия (хромпик) — сильный окислитель, используется для приготовления «хромовой смеси» для мытья химической посуды и при обработке кожи (дубление). Также используется для очистки ацетилена на ацетиленовых заводах от аммиака, сероводорода и фосфина.
Биологическая роль
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в организме человека
Калий содержится большей частью в клетках, до 40 раз больше, чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса. Калий и натрий между собой функционально связаны и выполняют следующие функции:
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых — от 1800 до 5000 миллиграммов. Потребность в калии зависит от массы тела, физической активности, физиологического состояния, и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются бобы (в первую очередь белая фасоль), шпинат и капуста кормовая, финики, картофель, батат, сушёные абрикосы, дыня, киви, авокадо, помело, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Практически все сорта рыбы содержат более 200 мг калия в 100 г. Количество калия в разных видах рыбы различается. Овощи, грибы и травы также содержат много калия, однако в консервированных продуктах его уровень может быть гораздо меньше. Много калия содержится в шоколаде.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин B6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При избытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
Изотопы
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным с периодом полураспада 1,251·109 лет. В каждом грамме природного калия в секунду распадается в среднем 31,0±0,3 ядра 40K, благодаря чему, например, в организме человека массой 70 кг ежесекундно происходит около 4000 радиоактивных распадов. Поэтому легкодоступные в быту соединения калия (поташ, хлорид калия, калийная селитра и т. д.) можно использовать как пробные радиоактивные источники для проверки бытовых дозиметров. 40K наряду с ураном и торием считается одним из основных источников геотермальной энергии, выделяемой в недрах Земли (полная скорость энерговыделения оценивается в 40—44 ТВт). В минералах, содержащих калий, постепенно накапливается 40Ar, один из продуктов распада калия-40, что позволяет измерять возраст горных пород; калий-аргоновый метод является одним из основных методов ядерной геохронологии.
Один из искусственных изотопов — 37K, — с временем полураспада 1,23651 с, применяется в экспериментах по изучению Стандартной модели слабого взаимодействия[11].
См. также
Примечания
- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047-1078. — DOI:10.1351/PAC-REP-13-03-02.
- ↑ Химическая энциклопедия: в 5 т / Редкол.: Кнунянц И. Л. (гл. ред.). — М.: Советская энциклопедия, 1990. — Т. 2. — С. 284. — 671 с. — 100 000 экз.
- ↑ 1 2 Davy, H. (1808). «The Bakerian Lecture, on some new Phenomena of chemical Changes produced by Electricity particularly the Decomposition of the fixed Alkalies, and the Exhibition of the new substances which constitute their bases; and on the general Nature of alkaline Bodies». Philosophical Transactions 98: 1-44.
- ↑ Davy, John. The Collected Works of Sir Humphry Davy. — London : Smith, Elder, and Company, 1839. — Vol. I. — P. 109.
- ↑ J. P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- ↑ КАЛИЙНОЕ МЕСТОРОЖДЕНИЕ
- ↑ Химическое и агрохимическое сырье.
- ↑ А. Ф. Алабышев, К. Д Грачев, С. А. Зарецкий, М. Ф. Лантратов, Натрий и калий (получение, свойства, применение), Л: Гос. н-т. изд-во хим. лит., 1959, С. 321.
- ↑ Хим.энциклопедия, т.2, М.: Сов. энциклопедия, 1990, С.562.
- ↑ Элементы: проба на окрашивание пламени (рус.). Проверено 26 января 2010. Архивировано 22 августа 2011 года.
- ↑ P. D. Shidling et al. Precision half-life measurement of the β+ decay of 37K (англ.) // Physical Review C. — 2014. — Vol. 90. — P. 032501. — DOI:10.1103/PhysRevC.90.032501. — arXiv:1407.1742.
Литература
- Пилипенко А. Т. Натрий и калий // Справочник по элементарной химии. — 2-е изд. — Киев: Наукова думка, 1978. — С. 316—319.
- Дроздов А. Яростные металлы // Энциклопедия для детей. Химия. — М.: Аванта +, 2002. — С. 184—187. — ISBN 5-8483-0027-5.
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Некрасов Б. В. Основы общей химии. — М.: Химия, 1974.
- Спицын В. И., Мартыненко Л. И. Неорганическая химия. — М.: МГУ, 1991, 1994.
- Лидин Р. А. и др. Элементы IA-группы. Калий // Химические свойства неорганических веществ: Уч. пособие для вузов. — 4-е изд. — М.: КолосС, 2003. — С. 29—40. — ISBN 5-9532-0095-1.
Ссылки
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, | |
| |||||||
wiki.sc
Биологическая роль калия — это… Что такое Биологическая роль калия?
Калий (K) | |
|---|---|
| Атомный номер | 19 |
| Внешний вид простого вещества | Серебристо-белый мягкий металл |
| Свойства атома | |
| Атомная масса (молярная масса) | 39,0983 а. е. м. (г/моль) |
| Радиус атома | 235 пм |
| Энергия ионизации (первый электрон) | 418,5 (4,34) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 4s1 |
| Химические свойства | |
| Ковалентный радиус | 203 пм |
| Радиус иона | 133 пм |
| Электроотрицательность (по Полингу) | 0,82 |
| Электродный потенциал | -2,92В |
| Степени окисления | 1 |
| Термодинамические свойства простого вещества | |
| Плотность | 0,856 г/см³ |
| Удельная теплоёмкость | 0,753 Дж/(K·моль) |
| Теплопроводность | 79,0 Вт/(м·K) |
| Температура плавления | 336,8 K |
| Теплота плавления | 102,5 кДж/моль |
| Температура кипения | 1047 K |
| Теплота испарения | 2,33 кДж/моль |
| Молярный объём | 45,3 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Период решётки | 5,230 Å |
| Отношение c/a | n/a |
| Температура Дебая | 100,00 K |
| K | 19 |
| 39,0983 | |
| 4s1 | |
| Калий | |
Ка́лий — химический элемент с атомным номером 19 в периодической системе, обозначается символом K (лат. Kalium), мягкий щелочной металл серебристо-белого цвета. В природе калий встречается только в соединениях с другими элементами, например в морской воде, а также во многих минералах. Он очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щелочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они все же отличаются.
История и происхождение названия
Калий (точнее, его соединения) использовался с давних времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щелок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
В 1807 г. английский химик Дэви электролизом твёрдого едкого кали (KOH) выделил калий и назвал его «потассий» (лат. potassium; это название до сих пор употребительно в английском, французском, испанском, португальском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Присутствие в природе
В свободном состоянии не встречается. Калий входит в состав сильвинита KCl•NaCl, карналлита KCl•MgCl2•6H2O, каинита KCl•MgSO4•6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав почти всех растений.
Получение
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650°C), то чаще проводят электролиз расправленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
K+ + e— → K
2Cl— — 2e— → Cl2
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
4OH— — 4e— → 2H2O + O2
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов)
Физические свойства
Калий — серебристое вещество с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет.
Химические свойства
Калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, легко отдаёт электроны.
Является сильным восстановителем. Он настолько активно соединяется с кислородом, что образуется не оксид, а супероксид калия KO2 (или K2O4). При нагревании в атмосфере водорода образуется гидрид калия KH. Хорошо взаимодействует со всеми неметаллами, образуя галогениды, сульфиды, нитриды, фосфиды и т. д., а также со сложными веществами, такими, как вода (реакция проходит со взрывом), различные оксиды и соли. В этом случае они восстанавливают другие металлы до свободного состояния.
Калий хранят под слоем керосина.
Оксиды и пероксиды
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
- 2K + 2O2 → K2O4
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
- K2O4 + 6K → 4K2O
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
- 2K2O4 + 2CO2 → 2K2CO3 + 3O2
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия. Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
Гидроксиды
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого калия при 20 °C в 100 г. воды составляет 112 г.
Применение
- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава натрий 12 %, калий 47 %, цезий 41 % обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединения

Фиолетовый цвет пламени ионов калия в пламени горелки
- Бромид калия — применяется в медицине и как успокаивающее средство для нервной системы.
- Гидроксид калия (едкое кали) — применяется в щелочных аккумуляторах и при сушке газов.
- Карбонат калия (поташ) — используется как удобрение, при варке стекла.
- Хлорид калия (сильвин, «калийная соль») — используется как удобрение.
- Нитрат калия (калийная селитра) — удобрение, компонент чёрного пороха.
- Перхлорат и хлорат (бертолетова соль) используются в производстве спичек, ракетных порохов, осветительных зарядов, взрывчатых веществ, в гальванотехнике.
- Бихромат (хромпик) — сильный окислитель, используется для приготовления «хромовой смеси» для мытья химической посуды и при обработке кожи (дубление). Также используется для очистки ацетилена на ацетиленовых заводах от аммиака, сероводорода и фосфина.
- Перманганат калия — сильный окислитель, используется как антисептическое средство в медицине и для лабораторного получения кислорода.
- Тартрат натрия-калия (сегнетова соль) в качестве пьезоэлектрика.
- Дигидрофосфат и дидейтерофосфат в виде монокристаллов в лазерной технике.
- Пероксид калия и супероксид калия используются для регенерации воздуха на подводных лодках и в изолирующих противогазах (поглощает углекислый газ с выделением кислорода).
- Фтороборат калия — важный флюс для пайки сталей и цветных металлов.
- Цианид калия применяется в гальванотехнике (серебрение, золочение), при добыче золота и при нитроцементации стали.
- Калий совместно с перекисью калия применяется при термохимическом разложении воды на водород и кислород (калиевый цикл «Газ де Франс», Франция).
Биологическая роль
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в организме человека
Калий содержится большей частью в клетках, до 40 раз больше чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса. Калий и натрий между собой функционально связаны и выполняют следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений
- Поддержание осмотической концентрации крови
- Поддержание кислотно-щелочного баланса
- Нормализация водного баланса
- Обеспечение мембранного транспорта
- Активация многих энзимов
- Нормализация ритма сердца
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1800 до 5000 миллиграмм. Необходимость в калии зависит от общего веса тела, физической активности, физиологического состояния, и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются сушёные абрикосы, дыня, бобы, киви, картофель, авокадо, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин В6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При переизбытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
Изотопы
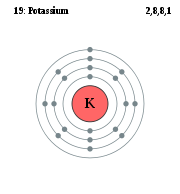
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным с периодом полураспада 1,251×109 лет. В каждом грамме природного калия в секунду распадается в среднем 32 ядра 40K, благодаря чему, например, в организме человека весом 70 кг ежесекундно происходит около 4000 радиоактивных распадов. 40K считается одним из основных источников геотермальной энергии, выделяемой в недрах Земли (мощность оценивается в 44 ТВт). В минералах, содержащих калий, постепенно накапливается 40Ar, один из продуктов распада калия-40, что позволяет измерять возраст горных пород; калий-аргоновый метод является одним из основных методов ядерной геохронологии.
См. также
Ссылки
Литература
- Пилипенко А.Т. Натрий и калий // Справочник по элементарной химии. — 2-е изд. — Киев: Наукова думка, 1978. — С. 316—319.
- Дроздов А. Яростные металлы // Энциклопедия для детей. Химия. — М.: Аванта +, 2002. — С. 184—187. — ISBN 5-8483-0027-5
| Электрохимический ряд активности металлов | |
|---|---|
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na | Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2, W, Sb, Bi, Ge, Re, Cu, Tс, Mn, Te, Rh, Po, Tl, Hg, Ag, Pb, Pd, Os, Ir, Pt, Au | |
| → активность металлов → |
Wikimedia Foundation. 2010.
dic.academic.ru
Калий химический элемент
Человечество знакомо с калием больше полутора веков. В лекции, прочитанной в Лондоне 20 ноября 1807 г. Хэмфри Дэви сообщил, что при электролизе едкого калия он получил «маленькие шарики с сильным металлическим блеском… Некоторые из них сейчас же после своего образования сгорали со взрывом». Это и был калий.
Калий — замечательный металл. Замечателен он не только потому, что режется ножом, плавает в воде, вспыхивает на ней со взрывом и горит, окрашивая пламя в фиолетовый цвет. И не только потому, что этот элемент — один из самых активных химически. Все это можно считать естественным, потому что соответствует положению щелочного металла калия в таблице Менделеева. Калий замечателен своей незаменимостью для всего живого и примечателен как всесторонне «нечетный» металл.
Обратите внимание: его атомный номер 19, атомная масса 39, во внешнем электронном слое — один электрон, валентность 1+. Как считают химики, именно этим объясняется исключительная подвижность калия в природе. Он входит в состав нескольких сотен минералов. Он находится в почве, в растениях, в организмах людей и животных. Он — как классический Фигаро: здесь — там — повсюду.
Калий и почва
Вряд ли можно объяснить случайностью или прихотью лингвистов тот факт, что в русском языке одним словом обозначаются и сама наша планета, и ее верхний слой — почва. «Земля-матушка», «земля-кормилица» — это, скорее, о почве, чем о планете в целом…
Но что такое почва? Самостоятельное и весьма своеобразное природное тело. Оно образуется из поверхностных слоев разнообразных горных пород под действием воздуха, воды, температурных перепадов, жизнедеятельности всевозможных обитателей Земли. Ниже, под почвой, скрыты так называемые материнские горные породы, сложенные из различных минералов. Они постепенно разрушаются и пополняют «запасы» почвы. А в почве, помимо чисто механического, постоянно происходит и другое разрушение. Его называют химическим выветриванием. Вода и углекислый газ (в меньшей мере другие вещества) постепенно разрушают минералы.
Почти 18% веса земной коры приходится на долю калийсодержащего минерала — ортоклаза. Это двойная соль кремневой кислоты K2Al2Si6O16 или K2O-Al2O3-BSiO2. Вот что происходит с ортоклазом в результате химического выветривания:
K2O*AI2O3*6SO2 + 2Н2О + CO2 → K2CO3+ Al2O3*2SO2*2H2O + + 4SiO2.
Ортоклаз превращается в каолин (разновидность глины), песок и поташ. Песок и глина идут на построение минерального костяка почвы, а K, перешедший из ортоклаза в поташ, «раскрепощается», становится доступным для растений. Но не весь сразу.
В почвенных водах молекулы K2CO3 диссоциируют: К2СO3 ↔ + К+ + КСO3— ↔ 2К+ + CO32-. Часть ионов калия остается в почвенном растворе, который для растений служит источником питания. Но большая часть ионов калия поглощается коллоидными частицами почвы, откуда корням растений извлечь их довольно трудно. Вот и получается, что, хотя калия в земле много, часто растениям его не хватает. Из-за того, что комочки почвы «запирают» большую часть калия, содержание этого элемента в морской воде почти в 50 раз меньше, чем натрия. Подсчитано, что из тысячи атомов калия, освобождающихся при химическом выветривании, только два достигают морских бассейнов, а 998 остаются в почве. «Почва поглощает калий, и в этом ее чудодейственная сила», — писал академик А. Е. Ферсман.
Калий и растения
Калий содержится во всех растениях. Отсутствие калия приводит растение к гибели. Почти весь калий находится в растениях в ионной форме — K+. Часть ионов находится в клеточном соке, другая часть поглощена структурными элементами клетки. Ионы калия участвуют во многих биохимических процессах, происходящих в растении. Установлено, что в клетках растений эти ионы находятся главным образом в протоплазме. В клеточном ядре они не обнаружены. Следовательно, в процессах размножения и в передаче наследственных признаков элемент № 19 не участвует. Но и без этого роль калия в жизни растения велика и многообразна.
Калий входит и в плоды, и в корни, и в стебли, и в листья, причем в вегетативных органах его, как правило, больше, чем в плодах. Еще одна характерная особенность: в молодых растениях больше калия, чем в старых. Замечено также, что по мере старения отдельных органов растений ионы калия перемещаются в точки наиболее интенсивного роста. При недостатке калия растения медленнее растут, их листья, особенно старые, желтеют и буреют по краям, стебель становится тонким и непрочным, а семена теряют всхожесть.
Установлено, что ионы калия активизируют синтез органических веществ в растительных клетках. Особенно сильно влияют они на процессы образования углеводов. Если калия не хватает, растение хуже усваивает углекислый газ, и для синтеза новых молекул углеводов ему недостает углеродного «сырья». Одновременно усиливаются процессы дыхания, и сахара, содержащиеся в клеточном соке, окисляются. Таким образом, запасы углеводов в растениях, оказавшихся на голодном пайке (по калию), не пополняются, а расходуются. Плоды такого растения — это особенно заметно на фруктах — будут менее сладкими, чем у растений, получивших нормальную дозу калия. Крахмал — тоже углевод, поэтому и на его содержание в плодах сильно влияет элемент № 19.
Но и это не все. Растения, получившие достаточно калия, легче переносят засуху и морозные зимы. Это объясняется тем, что элемент № 19 влияет на способность коллоидных веществ растительных клеток поглощать воду и набухать. Не хватает калия — клетки хуже усваивают и удерживают влагу, сжимаются, отмирают.
Ионы калия влияют и на азотный обмен веществ. При недостатке калия в клетках накапливается избыток аммиака. Это может привести к отравлению и гибели растения.
Уже упоминалось, что K влияет и на дыхание растений, а усиление дыхания сказывается не только на содержании углеводов. Чем интенсивнее дыхание, тем активнее идут все окислительные процессы, и многие органические вещества превращаются в органические кислоты. Избыток кислот может вызвать распад белков. Продукты этого распада — весьма благоприятная среда для грибков и бактерий. Вот почему при калийном голодании растения намного чаще поражаются болезнями и вредителями. Фрукты и овощи, содержащие продукты распада белков, плохо переносят транспортировку, их нельзя долго хранить.Одним словом, хочешь получать вкусные и хорошо сохраняющиеся плоды — корми растение калием вволю. А для зерновых калий важен еще по одной причине: он увеличивает прочность соломы и тем самым предупреждает полегание хлебов…
Интересное о калии
- ВСТРЕЧА С КАЛИЕМ? Если на складе или на товарной станции вы увидите стальные ящики с надписями: «Огнеопасно!», «От воды взрывается», то весьма вероятно, что вы встретились с калием.
Много предосторожностей предпринимают при перевозке этого металла. Поэтому, вскрыв стальной ящик, вы не увидите калия, а увидите тщательно запаянные стальные банки. В них — калий и инертный газ — единственная безопасная для калия среда. Большие партии калия перевозят в герметических контейнерах под давлением инертного газа, равным 1,5 атм.
- ЗАЧЕМ НУЖЕН МЕТАЛЛИЧЕСКИЙ КАЛИЙ? Металлический K используют как катализатор в производстве некоторых видов синтетического каучука, а также в лабораторной практике. В последнее время основным применением этого металла стало производство перекиси калия K2O2, используемой для регенерации кислорода. Сплав калия с натрием служит теплоносителем в атомных реакторах, а в производстве титана — восстановителем.
- ИЗ СОЛИ И ЩЕЛОЧИ. Получают элемент №19 чаще всего в обменной реакции расплавленных едкого калия и металлического натрия: KOH + Na → NaOH + K. Процесс идет в ректификационной колонне из никеля при температуре 380-440°С. Подобным образом получают элемент № 19 и из хлористого калия, только в этом случае температура процесса выше — 760-800°С. При такой температуре и натрий, и калий превращаются в пар, а хлористый калий (с добавками) плавится. Пары натрия пропускают через расплавленную соль и конденсируют полученные пары калия. Этим же способом получают и сплавы натрия с калием. Состав сплава в большой мере зависит от условий процесса.
- КАК БЫТЬ, ЕСЛИ вы впервые имеете дело с металлическим калием. Необходимо помнить о высочайшей реакционной способности этого металла, о том, что калий воспламеняется от малейших следов воды. Работать с калием обязательно в резиновых перчатках и защитных очках, а лучше — в маске» закрывающей все лицо. С большими количествами калия работают в специальных камерах, заполненных азотом или аргоном. (Разумеется, в специальных скафандрах.) А если K все-таки воспламенился, его тушат не водой, а содой или поваренной солью.
- КАК БЫТЬ С ОТХОДАМИ. Правила безопасности категорически запрещают накапливать в лабораториях больше двух граммов остатков или отходов какого-либо щелочного металла, калия в том числе. Отходы подлежат уничтожению на месте. Классический способ — образование под действием этилового спирта этилата калия C2H5OK: просто льют в отходы спирт. Но есть и другой — безспиртовой способ. Отходы заливают керосином или бензином. Калий с ними не реагирует и, будучи легче воды, но тяжелее этих органических жидкостей, оседает на дно. И тогда в наклоненный сосуд начинают по каплям добавлять воду. Когда вода доберется до металла, произойдет реакция и K превратится в едкое кали. Слои щелочного раствора и керосина или бензина довольно легко разделяются на делительной воронке.
- ЕСТЬ ЛИ В РАСТВОРЕ ИОНЫ КАЛИЯ? Выяснить это несложно. Проволочное колечко опустите в раствор, а затем внесите в пламя газовой горелки. Если калий есть, пламя окрасится в фиолетовый цвет, правда, не в такой яркий, как желтый цвет, придаваемый пламени соединениями натрия. Сложнее определить, сколько калия в растворе. Нерастворимых в воде соединений у этого металла немного. Обычно калий осаждают в виде перхлората — соли очень сильной хлорной кислоты HClO4. Кстати, перхлорат калия — очень сильный окислитель и в этом качестве применяется в производстве некоторых взрывчатых веществ и ракетных топлив.
- ДЛЯ ЧЕГО НУЖЕН ЦИАНИСТЫЙ КАЛИЙ? Для извлечения золота и серебра из руд. Для гальванического золочения и серебрения неблагородных металлов. Для получения многих органических веществ. Для азотирования стали — это придает ее поверхности большую прочность. К сожалению, это очень нужное вещество чрезвычайно ядовито. А выглядит KCN вполне безобидно: мелкие кристаллы белого цвета с коричневатым или серым оттенком.
- ЧТО ТАКОЕ ХРОМПИК? Точнее — хромпик калиевый. Это оранжевые кристаллы состава K2Cr2O7. Хромпик используют в производстве красителей, а его растворы — для «хромового» дубления кож, а также в качестве протравы при окраске и печатании тканей. Раствор хромпика в серной кислоте — хромовая смесь, которую во всех лабораториях применяют для мытья стеклянной посуды.
- ЗАЧЕМ НУЖНО ЕДКОЕ КАЛИ? В самом деле, зачем? Ведь свойства этой щелочи и более дешевого едкого натра практически одинаковы. Разницу между этими веществами химики обнаружили лишь в XVIII в. Самое заметное различие между NaOH и KOH в том, что едкое кали в воде растворяется еще лучше, чем едкий натр. KOH получают электролизом растворов хлористого калия. Чтобы примесь хлоридов была минимальной, используют ртутные катоды. А нужно это вещество прежде всего как исходный продукт для получения различных солей калия. Кроме того, без едкого кали не обойтись в производстве жидких мыл, некоторых красителей и органических соединений. Раствор едкого кали используется в качестве электролита в щелочных аккумуляторах.
- СЕЛИТРА ИЛИ СЕЛИТРЫ? Правильнее — селитры. Это общее название азотнокислых солей щелочных и щелочноземельных металлов. Если же говорят просто «селитра» (не «натриевая» или «кальциевая» или «аммиачная», а просто — «селитра»), то имеют в виду нитрат калия. Этим веществом человечество пользуется уже больше тысячи лет — для получения черного пороха. Кроме того, селитра — первое двойное удобрение: из трех важнейших для растений элементов в ней есть два — азот и калий. Вот как описал селитру Д. И. Менделеев в «Основах химии»:
«Селитра представляет бесцветную соль, имеющую особый прохладительный вкус. Она легко кристаллизуется длинными, по бокам бороздчатыми, ромбическими, шестигранными призмами, оканчивающимися такими же пирамидами. Ее кристаллы (уд. вес 1,93) не содержат воды. При слабом накаливании (339°) селитра плавится в совершенно бесцветную жидкость. При обыкновенной температуре в твердом виде KNO3 малодеятельна и неизменна, но при возвышенной температуре она действует как весьма сильное окисляющее средство, потому что может отдать смешанным с нею веществам значительное количество кислорода. Брошенная на раскаленный уголь селитра производит быстрое его горение, а механическая смесь ее с измельченным углем загорается от прикосновения с накаленным телом и продолжает сама собою гореть. При этом выделяется азот, а кислород селитры идет на окисление угля, вследствие чего и получаются углекалиевая соль и углекислый газ…
В химической практике и технике селитра употребляется во многих случаях как окислительное сродство, действующее при высокой температуре. На этом же основано применение ее для обыкновенного пороха, который есть механическая смесь мелко измельченных: серы, селитры и угля».
- ГДЕ И ДЛЯ ЧЕГО ПРИМЕНЯЮТСЯ ПРОЧИЕ СОЛИ КАЛИЯ? Бромистый калий KBr — в фотографии, чтобы предохранить негатив или отпечаток от вуали.
- Йодистый калий KI — в медицине и как химический реактив.
- Фтористый калий KF — в составе металлургических флюсов и для введения фтора в органические соединения.
- Углекислый калий (поташ) K2CO3 — в стекольном и мыловаренном производствах, а также как удобрение.
- Фосфаты калия, в частности K4P2O7 и K5P3O10, — как компоненты моющих средств.
- Хлорат калия (бертолетова соль) KClO3 — в спичечном производстве и пиротехнике.
- Кремнефтористый калий K2SiF6 — как добавка к шихте при извлечении редкоземельных элементов из минералов.
- Железистосинеродистый калий (желтая кровяная соль) K4Fe(CN)6-SH2O — как протрава при крашении тканей и в фотографии.
- ПОЧЕМУ КАЛИЙ НАЗВАЛИ КАЛИЕМ? Слово это арабского происхождения. По-арабски, «аль-кали» — зола растений. Впервые калий получен из едкого кали, а едкое кали — из поташа, выделенного из золы растений… Впрочем, в английском и других европейских языках сохранилось название potassium, данное калию его первооткрывателем X. Дэви. В русскую химическую номенклатуру название «калий» введено в 1831 г. Г. И. Гессом.
- ОТНЮДЬ HE ТОЛЬКО В КУРАГЕ. Сердечникам, в первую очередь людям, перенесшим инфаркт, для восполнения потерь калия в организме настоятельно рекомендуют есть курагу. Или в крайнем случае изюм. В 100 граммах кураги до 2 г калия. Столько же ее в урюке (но для точности при расчете надо вычесть вес косточек). Изюм содержит калия примерно вдвое меньше. Но не надо думать, будто сухофрукты — единственный источник калия. Его довольно много почти в любой растительной пище. Например, сорок граммов жареного картофеля эквивалентны 10 граммам отборной кураги. Богаты калием бобовые, чай, порошок какао. Одним словом, суточную дозу калия (2,5-5 г) при нормальном питании получить нетрудно.
natural-museum.ru

