Клинические проявления болезни Грейвса
Для БГ, в большинстве случаев, характерен относительно короткий анамнез: первые симптомы обычно появляются за 4-6 месяцев до обращения к врачу и постановки диагноза. Как правило, ключевые жалобы связаны с изменениями со стороны сердечно-сосудистой системы, так называемым катаболическим синдромом и эндокринной офтальмопатией.
Основным симптомом со стороны сердечно-сосудистой системы является тахикардия и достаточно выраженные ощущения сердцебиений. Тиреотоксикоз сопровождается дилатацией резистивных артериол и децентрализацией кровообращения. С одной стороны это приводит к тому, что пациенты могут ощущать сердцебиения не только в грудной клетке, но и голове, руках, животе. С другой стороны, гиперкинетическое состояние сердца (высокая ЧСС) в сочетании с децентрализацией кровообращения приводит к повышению пульсового давления (разница между систолическим и диастолическим АД). ЧСС в покое при синусовой тахикардии, обусловленной тиреотоксикозом, может достигать 120—130 ударов в минуту.
При длительно существующем тиреотоксикозе, особенно у пожилых пациентов, развиваются выраженные дистрофические изменения в миокарде, частым проявлением которых являются суправентрикулярные нарушения ритма, а именно фибрилляция (мерцание) предсердий. Это осложнение тиреотоксикоза достаточно редко развивается у пациентов моложе 50 лет. Дальнейшее прогрессирование миокардиодистрофии приводит к развитию изменений миокарда желудочков и застойной сердечной недостаточности.
Как правило, выражен катаболический синдром, проявляющийся прогрессирующим похудением (порой на 10-15 кг и более, особенно у лиц с исходным избытком веса) на фоне нарастающей слабости и повышенного аппетита. Кожа больных горячая, иногда имеется выраженный гипергидроз. Характерно чувство жара, пациенты не мерзнут при достаточно низкой температуре в помещении. У некоторых пациентов (особенно в пожилом возрасте) может быть выявлен вечерний субфебрилитет.
Изменения со стороны нервной системы характеризуются психической лабильностью: эпизоды агрессивности, возбуждения, хаотичной непродуктивной деятельности сменяются плаксивостью, астенией (раздражительная слабость). Многие пациенты некритичны к своему состоянию и пытаются сохранить активный образ жизни на фоне достаточно тяжелого соматического состояния. Длительно существующий тиреотоксикоз сопровождается стойкими изменениями психики и личности пациента. Частым, но неспецифичным симптомом тиреотоксикоза является мелкий тремор: мелкая дрожь пальцев вытянутых рук выявляется у большинства пациентов. При тяжелом тиретоксикозе тремор может определяться во всем теле и даже затруднять речь пациента.
Для тиреотоксикоза характерны мышечная слабость и уменьшение объема мускулатуры, особенно проксимальных мышц рук и ног. Иногда развивается достаточно выраженная миопатия. Весьма редким осложнением (возможно проявлением БГ) является тиреотоксический гипокалиемический периодический паралич, который проявляется периодически возникающими резкими приступами мышечной слабости. При лабораторном исследовании выявляется гипокалиемия, повышение уровня КФК. Чаще встречается у представителей азиатской расы.
Интенсификация костной резорбции приводит к развитию синдрома остеопении, а сам тиреотоксикоз рассматривается как один из наиболее важных факторов риска остеопороза. Частыми жалобами пациентов являются выпадение волос, ломкость ногтей.
Изменения со стороны желудочно-кишечного тракта развиваются достаточно редко. У пожилых пациентов в ряде случаев может быть диарея. При длительно существующем тяжелом тиреотоксикозе могут развиваться дистрофические изменения в печени (тиреотоксический гепатоз).
Нарушения менструального цикла встречаются достаточно редко. В отличие от гипотиреоза, тиреотоксикоз умеренной выраженности может не сопровождаться снижением
При тяжелом тиреотоксикозе у ряда пациентов выражены симптомы тиреогенной (относительной) надпочечниковой недостаточности, которую необходимо дифференцировать от истинной. К уже перечисленным симптомам добавляются гиперпигментация кожи, открытых частей тела (
В большинстве случаев при БГ происходит увеличение размеров ЩЖ, которое, как правило, имеет диффузный характер. Нередко железа увеличена значительно. В ряде случаев над ЩЖ можно выслушать систолический шум. Тем не менее зоб не является облигатным симптомом БГ, поскольку он отсутствует не менее чем у 25-30 % пациентов.
Ключевое значение в диагностике БГ имеют изменения со стороны глаз, которые являются своеобразной «визитной карточкой» БГ, т.е. их обнаружение у пациента с тиреотоксикозом практически однозначно свидетельствует именно о БГ, а не о другом заболевании. Очень часто благодаря наличию выраженной офтальмопатии в сочетании с симптомами тиреотоксикоза диагноз БГ очевиден уже при осмотре пациента (рис. 1).
Рис. 1. Внешний вид пациентов с болезнью Грейвса
Другим редким (менее 1 % случаев), ассоциированным с БГ, заболеванием является претибиальная микседема (рис. 2). Патогенез поражения клетчатки претибиальной области, вероятно, аналогичен таковому при ЭОП. Кожа передней поверхности голени становится отечной, уплотненной, пурпурно-красного цвета («апельсиновая корка»), часто сопровождается эритемой и зудом.
Рис. 2. Претибиальная микседема (а, б)
Клиническая картина тиреотоксикоза может иметь отклонения от классического варианта. Так, если у молодых БГ характеризуется развернутой клинической картиной, у пожилых пациентов ее течение зачастую олиго- или даже моносимптомное (нарушение ритма сердца, субфебрилитет). При так называемом «апатическом» варианте течения БГ, который встречается у пожилых пациентов, клинические проявления включают потерю аппетита, депрессию, гиподинамию.
Весьма редким осложнением БГ (крайне редко других заболеваний, протекающих с тиреотоксикозом) является тиреотоксический криз, патогенез которого не вполне понятен, т.к. криз может развиваться и без запредельного повышения уровня тиреоидных гормонов в крови. Причиной тиреотоксического криза могут оказаться сопутствующие БГ острые инфекционные заболевания, проведение оперативного вмешательства или терапии радиоактивным йодом на фоне выраженного тиреотоксикоза, отмена тиреостатической терапии, введение пациенту контрастного йодсодержащего препарата. Клинические проявления тиреотоксического криза включают резкое утяжеление симптомов тиреотоксикоза, гипертермию, спутанность сознания, тошноту, рвоту, иногда диарею. Регистрируется синусовая тахикардия свыше 120 уд/мин. Нередко отмечается мерцательная аритмия, высокое пульсовое давление с последующей выраженной гипотонией. В клинической картине может доминировать сердечная недостаточность, респираторный дистресс-синдром. Нередко выражены проявления относительной надпочечниковой недостаточности в виде гиперпигментации кожи. Кожные покровы могут быть желтушны вследствие развития токсического гепатоза. При лабораторном исследовании может выявляться лейкоцитоз (даже при отсутствии сопутствующей инфекции), умеренная гиперкальциемия, повышение уровня щелочной фосфатазы. Смертность при тиреотоксическом кризе достигает 30-50 %.
Дедов И.И., Мельниченко Г.А., Фадеев В.Ф.
Эндокринология
Опубликовал Константин Моканов
Способ лечения диэнцефально-катаболического синдрома
Изобретение относится к медицине, а именно к интенсивной терапии больных нейрохирургического профиля, и может быть использовано в терапии диэнцефально-катаболического синдрома (ДКС) у больных с поражением центральной нервной системы (ЦНС). Проводят непрерывную внутривенную инфузию клонидина в дозе 0,05-0,3 мкг/кг/ч до достижения вегетативной стабильности — температура тела не выше 38°С, частота сердечных сокращений не более 100 ударов в минуту, артериальное давление на «рабочем» уровне или не выше чем на 20% от этих показателей. Способ повышает эффективность лечения и снижает количество осложнений у пациентов с поражением ЦНС.
Изобретение относится к медицине, а именно к интенсивной терапии больных нейрохирургического профиля, и может быть использовано в терапии диэнцефально-катаболического синдрома (ДКС) у больных с поражением центральной нервной системы (ЦНС).
ДКС нередкое осложнение тяжелого повреждения головного мозга. Его развитие приводит к повышению катаболизма, снижению иммунитета, нарушению адаптивной реакции на стресс. При несвоевременном и неадекватном купировании этого синдрома возможны развитие тяжелого нейродистрофического синдрома, инфекционных осложнений, формирование патологической системы с устойчивой симпатоадреналовой активностью.
Наиболее близким к заявляемому является способ лечения ДКС с использованием нейролептиков, обладающих центральным стабилизирующим действием (аминазин, дроперидол, пипольфен) (Борщаговский М.Л. Применение нейроплегиков (аминазина и пипольфена) в остром периоде повреждения черепа и головного мозга: / М.Л.Борщаговский. Автореф. дис…. канд. мед наук. — Л., 1971, с.16), принятый за прототип. Известно, что препараты этого ряда обладают гемодинамическим, антипиррогенным, седативным эффектами. При развитии ДКС их назначают в плановом порядке парэнтерально (аминазин до 100 мг/сут, дроперидол до 20 мг/сут, пипольфен до 400 мг/сут), как правило, один или два из перечисленных. Параллельно проводят физическое охлаждение.
Однако прототип недостаточно эффективен, так как:
— доказан высокий риск развития злокачественного нейролептического синдрома у пациентов с поражением диэнцефальных структур на фоне применения нейролептиков;
— при использовании больших доз нейролептиков возможны выраженное угнетение гемодинамики и срыв ауторегуляции мозгового кровообращения.
Изобретение направлено на создание способа лечения диэнцефально-катаболического синдрома, повышающего эффективность лечения, снижение количества осложнений, улучшение качества жизни и снижение летальности пациентов с тяжелым повреждением головного мозга.
Указанный технический результат при осуществлении изобретения достигается тем, что в известном способе лечения ДКС путем применения препарата, обладающего центральным действием, особенность заключается в том, что проводят непрерывную внутривенную инфузию клонидина в дозе 0,05-0,3 мкг/кг/ч, до достижения вегетативной стабильности — температура тела не выше 38°С, частота сердечных сокращений не более 100 ударов в минуту, артериальное давление на «рабочем» уровне или не выше чем на 20% от этих показателей, максимальные сроки непрерывной внутривенной инфузии клонидина — 30 дней.
Клонидин является препаратом как центрального, так и периферического действия, оказывает гуморальное воздействие, изменяя продукцию регулирующих нейропептидов в структурах ЦНС, создавая стабильность гормонального фона (уровня катехоламинов, ренина, ангиотензина), гемодинамики, обладает анальгетическим эффектом, управляемым в использовании (Кондратьев А.Н. Сочетанное воздействие на опиоидную и адренергическую антиноцицептивные системы в анестезиологическом обеспечении нейрологических операций / А.Н.Кондратьев.: Дис…. докт. мед. наук. — СПб, 1992). Клонидин снимает избыточную адреностимуляцию и способствует стабилизации перфузионного давления мозга (Plaisange P, Qulntln L., Payen D. Clonidine decreases the sympathetic hyperactivity ogguring after head injury // Isthesiology. — 1988. — V.69. — N.3A (suppl.). — P.AI48). Регулирующее действие клонидина реализуется преимущественно, через нейрорегуляторные системы ствола головного мозга. Помимо нейрогенных влияний клонидин снижает уровень норадреналина на периферии, активируя α2-адренорецепторы.
Способ осуществляется следующим образом. Пациенту с клиникой ДКС: гипертермия выше 38°С, тахипноэ более 20 в минуту, тахикардия, артериальная гипертензия, гиперферментемия, признаки ирритации диэнцефальных структур по данным электроэнцефалографии назначают непрерывную внутривенную инфузию клонидина в дозе от 0,05 до 0,3 мкг/кг/ч. Дозу подбирают индивидуально по клиническому эффекту. Критериями адекватности проводимой терапии является достижение вегетативной стабильности — температура тела не выше 38°С, частота сердечных сокращений не более 100 ударов в минуту, артериальное давление на «рабочем» уровне или не выше чем на 20% от этих показателей. Длительность проведения инфузии клонидина индивидуальна до стабилизации вегетативных функций. Отмену препарата проводят постепенно, на 1/2, 1/3 дозы в сутки. При возобновлении признаков диэнцефально-катаболического синдрома терапию возобновляют. Максимальные сроки непрерывной внутривенной инфузии клонидина — 30 дней.
Способ разработан и прошел клинические испытания на базе реанимационного отделения ГУ РНХИ им. А.Л.Поленова при лечении 300 больных с различной патологией головного мозга. При этом были получены положительные результаты в виде снижения нейродистрофических, нейроинфекционных осложнений, а также снижения летальности.
Пример
Сведения из и/б №3099-2004 больного С., 18 лет.
Диагноз: Закрытая черепно-мозговая травма, ушиб головного мозга тяжелой степени, ушиб ствола головного мозга, диффузное аксональное повреждение, субарахноидальное кровоизлияние, дислокационный синдром от 12.12.2004.
Больной поступил в ФГУ РНХИ им. Проф. А.Л.Поленова 24.12.2004 по переводу из ГБ №16.
При поступлении состояние очень тяжелое, сознание на уровне комы 1, на боль — вялые сгибательные движения в конечностях. Мышечный тонус снижен. Лицо сальное. Периодически возникает гипергидроз. Артериальное давление 100-120/70 mm Hg, пульс 92-120 в минуту, лихорадит до 39,3°С, разница ректальной и подмышечной температур — 0,3°С. В клиническом анализе крови: гемоглобин 116 г/л, эритроцитов 3,9×1012/л, лейкоцитов 12,6×109/л, палочкоядерных — 4, сегментоядерных — 70, лимфоцитов — 16, моноцитов — 10, СОЭ — 46 мм/час. В биохимическом анализе крови: глюкоза — 7,18 ммоль/л, мочевина — 6 ммоль/л, общий белок — 68,6 г/л, креатинин — 64 мкмоль/л, креатинкиназа — 335,6, ЛДГ — 570 Ед/л, ACT — 50 Ед/л, АЛТ — 52 Ед/л, щелочная фосфотаза — 447 Ед/л, калий — 4,1 ммоль/л, натрий — 133 ммоль/л.
По данным ЭЭГ: выраженные диффузные изменения биоэлектрической активности головного мозга, свидетельствующие о нарушении подкорково-стволовых взаимоотношений, со значительным снижением нейродинамики коры, практически полным выпадением влияний диэнцефальных структур, дисфункция неспецефических стволовых структур.
Таким образом, клиническая картина была представлена тяжелым поражением головного мозга с поражением кортико-бульбарных и пирамидных путей, диэнцефальным синдромом.
Больной получал терапию, направленную на поддержание объема циркулирующей крови, антибактериальную, антигипоксанты, бензодиазепины с целью нейровегетативной стабилизации. На этом фоне отмечалась положительная динамика в виде снижения частоты сердечных сокращений до 80-90 в минуту, отсутствие гипергидроза, уменьшение лихорадки до субфебрильных цифр, однако, к концу третьей недели возобновились явления диэнцефально-катаболического сондрома — тахикардия до 120 ударов в минуту, лихорадка до 38°С, по данным ЭЭГ: нарастание дисфункции неспецифических структур ствола головного мозга. Согласно заявляемому способу была начата нейровегетативная стабилизация клонидином в начальной дозе 0,05 мкг/кг/ч с последующим увеличением до 0,07 мкг/кг/ч. Терапия проводилась в течение 30 дней, с постепенной отменой в течение последних 3-х дней (0,07-0,05-0,02 мкг/кг/ч). На фоне проводимой терапии отмечена положительная динамика: нормализация частоты сердечных сокращений до 80-90 в минуту, отсутствие гипергидроза, сальности кожи лица, нормализация температуры и лабораторных данных (глюкоза, креатинкиназа, ЛДГ, АЛТ, ACT). Положительная динамика по данным ЭЭГ в виде тенденции к восстановлению таламо-кортикальных связей, сохранности активизирующего влияния ретикулярной формации, отсутствие дисфункции неспецифических структур ствола головного мозга.
Больной выписан 28.03.2005 в компенсированном состоянии. В сознании, контактен, трахеостома удалена, глотает хорошо, артериальное давление 100-120/70 mm Hg, пульс 80-90 в минуту, не лихорадит.
Клонидин обладает меньшим количеством побочных эффектов: при предлагаемом способе использования не вызывает артериальной гипотензии и снижения перфузионного давления мозга, не вызывает злокачественной гипертермии, не оказывает выраженного седативного эффекта.
Использование предлагаемого способа лечений диэнцефально-катаболического синдрома:
— помогает повысить эффективность лечения пациентов с различной патологией головного мозга;
— позволяет снизить количество осложнений, связанных с развитием нейродистрофического синдрома;
— позволяет предотвратить формирование патологической симпато-адреналовой доминанты.
Способ лечения диэнцефально-катаболического синдрома путем введения препарата, обладающего центральным действием, отличающийся тем, что в качестве такого препарата используют клонидин, причем проводят непрерывную внутривенную инфузию клонидина в дозе 0,05-0,3 мкг/кг/ч до достижения вегетативной стабильности — температура тела не выше 38°С, частота сердечных сокращений не более 100 ударов в минуту, артериальное давление на «рабочем» уровне или не выше чем на 20% от этого показателя.
Болевые (алгогенные) мышечные синдромы — Неврология — LiveJournal

Группа болевых (или аллогенных) мышечных синдромов включает в себя следующие пять синдромов: [1] мышечно-[гипер]тонический, [2] мышечный гипертонически-гиперкинетический, [3] миофасциальный, [4] фибромиалгический и [5] мышечный синдром, который ассоциирован с ревматической патологией; [6] условно «патологической» является мышечная боль после физической нагрузки (см. далее «крепатура»).
 Общая характеристика миогенной боли: [1] уплотнение мышцы; [2] болезненность; [3] повышение сократительной активности; [4] нарушение нормальных координационных отношений между различными мышечными группами.
Общая характеристика миогенной боли: [1] уплотнение мышцы; [2] болезненность; [3] повышение сократительной активности; [4] нарушение нормальных координационных отношений между различными мышечными группами.Рассмотрим основные клинико-диагностические признаки болевых (аллогенных) мышечных синдромов:
 Мышечно-[гипер]тонический синдром характеризуется напряжением, уплотнением, укорочением мышцы, а также уменьшением объема движений, контрактурой в соответствующем двигательном сегменте или суставе. По распространенности повышенный мышечный тонус (далее – гипертонус) может быть локальным, когда он захватывает лишь участок мышцы, диффузным – с повышением тонуса во всей мышце, регионарным – с вовлечением группы мышц агонистов, генерализованным – со спазмом одновременно агонистов и антагонистов, сгибателей и разгибателей и вовлечением большой мышечной массы. По интенсивности гипертонус может быть легко, умеренно и резко выраженным. При легко выраженном гипертонусе больной ощущает дискомфорт, стягивание в мышце, которые проходят после ее поглаживания, растирания, а также прикладывания к ней грелки. При пальпации отмечается умеренное напряжение мышцы, боли нет. Умеренно выраженный гипертонус характеризуется болезненным спазмом мышцы, который не позволяет пальцу при пальпации свободно проникать в ее толщу, в мышце могут обнаруживаться локальные участки локального гипертонуса в виде болезненных тяжей, узелков. При резко выраженном гипертонусе мышца имеет каменистую плотность, болезненна при пальпации. Тепло, массаж не снимают напряжением, а наоборот, часто усиливают спазм и боль. По продолжительности мышечного спазма различают периодический и постоянный мышечно-гипертонический синдром (гипертонус). О периодическом (параксизмальном) гипертонусе говорят, если спазм возникает в виде приступа при неловком движении, вставании с постели, ходьбе или выполнении физической работы. Тоническое напряжение мышцы и судорога типа крампи могут продолжаться несколько секунд, минут или часов. Постоянный мышечный гипертонус продолжается днями, неделями и месяцами, не зависит от движений и позы. Также различают неосложненные и осложненные мышечно-гипертонические синдромы. При неосложненном гипертонусе во время приступа боль локализуется лишь в пораженной мышце. В покое при пальпации участок гипертонуса безболезненный, спазм может провоцироваться механическим раздражением активным сокращением мышцы. Осложненный гипертонус связан с раздражением болевых окончаний в спазмированной мышце за счет ишемии в зоне гипертонуса, с рефлекторным или компрессионным воздействием на сосудисто-нервные образования, с нарушением венозного и лимфатического оттока и микроциркуляции в тканях. В результате возникают интенсивные боли в мышце, усиливающиеся при пальпации, иррадиирующие в соседние в соседние и отдаленные области. Типичны чувство онемения, слабости, зябкости или жара в конечностях, парестезии. Могут обнаруживаться признаки сдавления нерва в фиброзно-мышечном туннеле соответствующей локализации.
Мышечно-[гипер]тонический синдром характеризуется напряжением, уплотнением, укорочением мышцы, а также уменьшением объема движений, контрактурой в соответствующем двигательном сегменте или суставе. По распространенности повышенный мышечный тонус (далее – гипертонус) может быть локальным, когда он захватывает лишь участок мышцы, диффузным – с повышением тонуса во всей мышце, регионарным – с вовлечением группы мышц агонистов, генерализованным – со спазмом одновременно агонистов и антагонистов, сгибателей и разгибателей и вовлечением большой мышечной массы. По интенсивности гипертонус может быть легко, умеренно и резко выраженным. При легко выраженном гипертонусе больной ощущает дискомфорт, стягивание в мышце, которые проходят после ее поглаживания, растирания, а также прикладывания к ней грелки. При пальпации отмечается умеренное напряжение мышцы, боли нет. Умеренно выраженный гипертонус характеризуется болезненным спазмом мышцы, который не позволяет пальцу при пальпации свободно проникать в ее толщу, в мышце могут обнаруживаться локальные участки локального гипертонуса в виде болезненных тяжей, узелков. При резко выраженном гипертонусе мышца имеет каменистую плотность, болезненна при пальпации. Тепло, массаж не снимают напряжением, а наоборот, часто усиливают спазм и боль. По продолжительности мышечного спазма различают периодический и постоянный мышечно-гипертонический синдром (гипертонус). О периодическом (параксизмальном) гипертонусе говорят, если спазм возникает в виде приступа при неловком движении, вставании с постели, ходьбе или выполнении физической работы. Тоническое напряжение мышцы и судорога типа крампи могут продолжаться несколько секунд, минут или часов. Постоянный мышечный гипертонус продолжается днями, неделями и месяцами, не зависит от движений и позы. Также различают неосложненные и осложненные мышечно-гипертонические синдромы. При неосложненном гипертонусе во время приступа боль локализуется лишь в пораженной мышце. В покое при пальпации участок гипертонуса безболезненный, спазм может провоцироваться механическим раздражением активным сокращением мышцы. Осложненный гипертонус связан с раздражением болевых окончаний в спазмированной мышце за счет ишемии в зоне гипертонуса, с рефлекторным или компрессионным воздействием на сосудисто-нервные образования, с нарушением венозного и лимфатического оттока и микроциркуляции в тканях. В результате возникают интенсивные боли в мышце, усиливающиеся при пальпации, иррадиирующие в соседние в соседние и отдаленные области. Типичны чувство онемения, слабости, зябкости или жара в конечностях, парестезии. Могут обнаруживаться признаки сдавления нерва в фиброзно-мышечном туннеле соответствующей локализации.
 Обратите внимание! Как правило, первично мышечно-[гипер]тонический синдром (МГТС) является физиологической реакцией, направленной на стабилизацию (иммобилизацию) [1] пораженного двигательного сегмента (сустав, в т.ч. позвоночный двигательный сегмент) или на иммобилизацию и/или пространственную изоляцию [2] пораженного внутреннего органа, дисфункция которых (1 или 2) обычно проявляется болью (миофиксация, как анталгический рефлекс). При сохранение указанной выше дисфункции (1 или 2) длительно сущесмтвующий МГТС приводит к появлению в заинтересованной мышце локально-продольных уплотнений (тяжи), а вдальнейшем и локально-шаровидных уплотнений (триггерные пункты или точки — ТТ [формируются сначала латентные, а затем и активные ТТ]). Данный процесс знаменует собой переход МГТС в мио-фасциальный молевой синдром (МФБС [см. далее пункт №3]).
Обратите внимание! Как правило, первично мышечно-[гипер]тонический синдром (МГТС) является физиологической реакцией, направленной на стабилизацию (иммобилизацию) [1] пораженного двигательного сегмента (сустав, в т.ч. позвоночный двигательный сегмент) или на иммобилизацию и/или пространственную изоляцию [2] пораженного внутреннего органа, дисфункция которых (1 или 2) обычно проявляется болью (миофиксация, как анталгический рефлекс). При сохранение указанной выше дисфункции (1 или 2) длительно сущесмтвующий МГТС приводит к появлению в заинтересованной мышце локально-продольных уплотнений (тяжи), а вдальнейшем и локально-шаровидных уплотнений (триггерные пункты или точки — ТТ [формируются сначала латентные, а затем и активные ТТ]). Данный процесс знаменует собой переход МГТС в мио-фасциальный молевой синдром (МФБС [см. далее пункт №3]).
 МГТС часто формируется при дегенеративных и/или воспалительных заболеваниях опорно-двигательного аппарата, и при неврологической патологии. В рамках последней представлен экстрапирамидный (ригидно-дистонический) мышечный синдром (например, при болезни паркинсона [БП]).
МГТС часто формируется при дегенеративных и/или воспалительных заболеваниях опорно-двигательного аппарата, и при неврологической патологии. В рамках последней представлен экстрапирамидный (ригидно-дистонический) мышечный синдром (например, при болезни паркинсона [БП]).
Болевой синдром является одним из частых немоторных проявлений БП, в т.ч. примерно у 10% пациентов боль бывает начальным симптомом заболевания (при этом она часто игнорируется врачами, ведущими пациента с БП). Анализ клинической феноменологии позволил условно выделить 3 частых типа связанного с БП болевого синдрома: [1] боль при моторных флюктуациях, [2] «центральная» боль, [3] боль вследствие локальных (регионарных) изменений [повышения] мышечного тонуса — ригидности или дистонии, — скелетно-мышечная ригидно-дистоническая боль (в дебюте БП особенно часто встречаются боль и болезненность мышц в плечелопаточной области, особенно двуглавой мышцы плеча). В контексте настоящего поста нас интересует последий вариант болевого синдрома при БП. Мышечная ригидность, лишая мышцу физиологического расслабления, приводит к морфологическим изменениям в миофибриллах, нарушению ионного обмена в клетке и, как результат, к явлениям асептического воспаления и отека, обусловливая микротравматизацию мышц, связочного аппарата и суставных капсул. В результате изменяется привычная биомеханика движения, изменяются взаимоотношения состояния мышц-агонистов и антагонистов, что, в свою очередь, может являться причиной возникновения мышечных болей, связанных с тоническими нарушениями в мышце.
 подробнее в статье (обзоре) «Особенности болевых синдромов при болезни Паркинсона» Бриль Е.В., Удалов Ю.Д., Аникина М.А., Зимнякова О.С.; ФГБУ «Государственный научный центр Российской Федерации — Федеральный медицинский биофизический центр им. А.И. Бурназяна» ФМБА России (Саратовский научно-медицинский журнал, №4, 2016) [читать]
подробнее в статье (обзоре) «Особенности болевых синдромов при болезни Паркинсона» Бриль Е.В., Удалов Ю.Д., Аникина М.А., Зимнякова О.С.; ФГБУ «Государственный научный центр Российской Федерации — Федеральный медицинский биофизический центр им. А.И. Бурназяна» ФМБА России (Саратовский научно-медицинский журнал, №4, 2016) [читать]

 Мышечные гипертонически-гиперкинетические синдромы: крампи, крампи-фасцикуляции и стеносолия.
Мышечные гипертонически-гиперкинетические синдромы: крампи, крампи-фасцикуляции и стеносолия.
Крампи представляют собой внезапные [кратковременные приступообразные] непроизвольные болезненные судорожные сокращения в одной или нескольких мышцах (как правило, в мышцах голеней и стоп), которые сохраняются в течение ограниченного времени и разрешающиеся спонтанно. При этом сокращение мышцы может быть изометрическим или сопровождаться движением конечности. Крампи сопровождается выраженными болями с неприятным эмоциональным оттенком. Одним кажется, будто в икроножные мышцы вонзили одновременно «тысячи иголок», что их «сдавливают прессом», «вводят в них скипидар, вывертывают, растягивают, ошпаривают кипятком». Другие отмечают прохождение «электрического тока» по мышце, раздирающую или сверлящую боль, а в последующем — такое ощущение, «будто в мышце работает бормашина и задевает за нервную веточку», что из-за невыносимой боли «даже останавливается сердце».
Болезненный спазм длится до десяти минут, после чего в течение нескольких часов может сохраняться резидуальная боль, что в совокупности существенно ухудшает качество сна. Прервать приступ можно с помощью усиленного растяжения мышцы. Мышца при крампи гипервозбудима: частота сокращения единичного волокна достигает 300 Гц по сравнению с 10 — 50 Гц при произвольном мышечном сокращении. Указанное явление может наблюдаться в самых различных мышцах: в челюстно-подъязычной (при зевании), подзатылочной, иногда в мышцах руки, в квадратной мышце поясницы, нежной, напрягающей широкую фасцию, флексорах пальцев ноги, в мышце, отводящей большой палец, но особенно — в трехглавой (икроножэной) мышце голени. В связи с некоторыми анатомическими и функциональными особенностями этой мышцы в ней наиболее часто наблюдается специфическое пароксизмально-судорожное явление — крампи. С возрастом частота встречаемости синдрома (крампи) повышается, он доминирует среди женщин.
Согласно Международной классификации расстройств сна (МКРС) третьего пересмотра (2014), выделяются следующие критерии диагностики крампи: [А] возникновение неприятных ощущений в ногах, которые сопровождаются уплотнением и напряжением мышцы; [В] мышечные сокращения чаще возникают в постели в состоянии бодрствования или во сне; [С] боль и мышечное сокращение облегчаются усиленным растяжением соответствующей мышцы.
Причина крампи в большинстве случаев остается неизвестной, и состояние расценивается как идиопатическое. Однако идентифицированы следующие провоцирующие факторы: дегидратация, электролитный и минеральный дисбаланс, мышечное утомление и снижение периферического кровотока. Икроножные крампи могут быть связаны со спинальным стенозом, периферической невропатией, длительным неподвижным положением ног, злоупотреблением алкоголем, циррозом печени, хроническим гемодиализом, венозной недостаточностью нижних конечностей, терапией онкозаболеваний и др. Спазмы мышц голеней также могут быть обусловлены внутривенным введением препаратов железа, конъюгированных эстрогенов, холестерин-снижающих препаратов, ралоксифена, напроксена и терипаратида. Крампи может быть сопутствующим симптомом таких заболеваний, как боковой амиотрофический склероз, болезнь Шарко — Мари — Тута, миодистрофия Беккера, хондро-дистрофическая миотония и т.д. Существенно реже крампи сопровождают прием других лекарств. В третьем триместре от крампи страдает около 30% беременных. Считается, что причина заключается в дефиците магния, необходимого для нормального развития плаценты, сдерживания роста артериального давления и профилактики судорог.
 читайте также пост: Крампи — болезненные мышечные спазмы (на laesus-de-liro.livejournal.com) [читать]
читайте также пост: Крампи — болезненные мышечные спазмы (на laesus-de-liro.livejournal.com) [читать]Синдром крампи-фасцикуляций. В популяции также встречается относительно редкий синдром крампи-фасцикуляций, который характеризуется болезненными спазмами мышц голеней, фасцикуляциями в них, скованностью и парестезиями. Этот синдром относится к группе синдромов периферической невральной гипервозбудимости и связан с нарушением функции вольтаж-зависимых калиевых каналов. Он может быть предвестником болезни мотонейрона и в ряде случаев генетически обусловлен. Этот синдром поддается терапии карбамазепином.
Стеносолия — синдром сжимающих болей в камбаловидной мышце (расположена под икроножной мышцей). Как и при стенокардии, приступы могут возникать на безболевом фоне, а в некоторых случаях — и на фоне постоянных нерезких болевых ощущений. Боли при синдроме стеносолии носят сжимающий, давящий характер, по интенсивности приближаются к крампи, но все же не столь мучительны, хотя и могут сопровождаться эмоционально неприятным, тягостным чувством. Они локализуются в глубине голени — преимущественно в камбаловидной мышце, особенно по наружному ее краю позади головки малоберцовой кости. Основными провоцирующими факторами являются те, которые вызывают перегрузку ягодичных мышц, особенно средней ягодичной, — стояние, ходьба, пребывание на больном боку, сидение. При пробе Ласега появляется боль как в ягодице, так и в голени. Нагрузки, направленные не на пояснично-ягодичные области, а непосредственно на голень, вызывают в ней продолжительную боль, медленно угасающую, но не типичный пароксизм. Положительные эмоции препятствуют развитию приступа. Его купированию способствует и непродолжительное пребывание на корточках. Лучшее средство его прекращения — горизонтальное положение на щите. Пальпаторно в камбаловидной мышце не по ходу выявляются миофасциальные триггерные пункты [см. далее пункт №3].
 Миофасциальный [болевой] синдром (МФБС или «синдром триггерного пункта») представляет собой хронический болевой синдром (локальный или сегментарный), возникающий от одного или нескольких триггерных пунктов одной или нескольких мышц. Триггерный (миофасциальный) пункт (точка) представляет собой гиперраздражимую область в уплотненном или тугом тяже скелетной мышцы и локализованную в мышечной ткани и/или в ее фасции; при этом миофасциальная боль может проявлять себя локальной болью или отраженной, то есть в удаленном от давления, но строго определенном месте (при надавливании на триггерную точку пациент непроизвольно пытается устранить вызвавший боль раздражитель, что известно под названием «симптом прыжка», который является характерным признаком МФБС). Пациенты, как правило, легко локализуют миофасциальные боли, четко определяют их интенсивность и характер. Со временем зона повышенной болевой чувствительности (в том числе количество триггерных точек) может расширяться (увеличиваться), а также выходить за пределы поврежденных тканей. При МФБС помимо триггерных пунктов могут формироваться участки повышенной болевой чувствительности к повреждающим стимулам, которые называют зонами гипералгезии, которые в свою очередь могут быть первичными и вторичными. Первичная гипералгезия охватывает поврежденные ткани, вторичная гипералгезия локализуется вне зоны повреждения, иногда на значительном удалении от места повреждения (в т.ч. и на противоположной стороне тела).
Миофасциальный [болевой] синдром (МФБС или «синдром триггерного пункта») представляет собой хронический болевой синдром (локальный или сегментарный), возникающий от одного или нескольких триггерных пунктов одной или нескольких мышц. Триггерный (миофасциальный) пункт (точка) представляет собой гиперраздражимую область в уплотненном или тугом тяже скелетной мышцы и локализованную в мышечной ткани и/или в ее фасции; при этом миофасциальная боль может проявлять себя локальной болью или отраженной, то есть в удаленном от давления, но строго определенном месте (при надавливании на триггерную точку пациент непроизвольно пытается устранить вызвавший боль раздражитель, что известно под названием «симптом прыжка», который является характерным признаком МФБС). Пациенты, как правило, легко локализуют миофасциальные боли, четко определяют их интенсивность и характер. Со временем зона повышенной болевой чувствительности (в том числе количество триггерных точек) может расширяться (увеличиваться), а также выходить за пределы поврежденных тканей. При МФБС помимо триггерных пунктов могут формироваться участки повышенной болевой чувствительности к повреждающим стимулам, которые называют зонами гипералгезии, которые в свою очередь могут быть первичными и вторичными. Первичная гипералгезия охватывает поврежденные ткани, вторичная гипералгезия локализуется вне зоны повреждения, иногда на значительном удалении от места повреждения (в т.ч. и на противоположной стороне тела).

Диагностика МФБС основывается на выявлении типичных признаков и клинических проявлений согласно диагностическим критериям J. Travell и D. Simons (одобрены Международной ассоциацией по изучению боли): [1] «Большие» критерии (необходимо наличие всех 5): [1.1] жалобы на местную (локальную) или региональную боль; [1.2] пальпируемый в пораженной мышце тугой тяж; [1.3] участок повышенной чувствительности (триггерная точка [ТТ]) в пределах тугого тяжа; [1.4.] характерная для данной пораженной мышцы зона отраженной боли (рисунок отраженной боли) или или обнаружение зон расстройств чувствительности; [1.5] ограничение объема движений ограничение функциональной активности мышцы, имеющей ТТ. [2] «Малые» критерии (необходимо наличие 1 из 3): [2.1] воспроизводимость боли или чувствительных нарушений при стимуляции ТТ; [2.2] вздрагивание (локальный судорожный ответ) пораженной мышцы при пальпации ТТ или при проколе ее инъекционной иглой; [2.3] уменьшение боли при растяжении пораженной мышцы, поверхностном охлаждении (хлорэтил) или введении в ТТ анестетика.
 По данным клинического обследования чаще всего болезненным изменениям подвергаются мышцы, относящиеся к категории преимущественно тонических, регулирующих статокинетическую функцию организма: мышца, поднимающая лопатку, трапециевидная мышца, квадратная мышца поясницы, грушевидная мышца.
По данным клинического обследования чаще всего болезненным изменениям подвергаются мышцы, относящиеся к категории преимущественно тонических, регулирующих статокинетическую функцию организма: мышца, поднимающая лопатку, трапециевидная мышца, квадратная мышца поясницы, грушевидная мышца.
 читайте также статью «Состояние скелетных мышц при хронической неспецифической боли в нижней части спины и подходы к терапии» Д.О. Рожков, О.Е. Зиновьева, А.Н. Баринов, И.М. Вихлянцев, А.Д. Уланова; Первый Московский государственный медицинский университет им. И.М. Сеченова; Межрегиональная ассоциация специалистов паллиативной и интервенционной медицины; Институт теоретической и экспериментальной биофизики РАН (журнал «Эффективная фармакотерапия» №11, 2018) [читать]
читайте также статью «Состояние скелетных мышц при хронической неспецифической боли в нижней части спины и подходы к терапии» Д.О. Рожков, О.Е. Зиновьева, А.Н. Баринов, И.М. Вихлянцев, А.Д. Уланова; Первый Московский государственный медицинский университет им. И.М. Сеченова; Межрегиональная ассоциация специалистов паллиативной и интервенционной медицины; Институт теоретической и экспериментальной биофизики РАН (журнал «Эффективная фармакотерапия» №11, 2018) [читать]
 Фибромиалгический синдром (ФМС) характеризуется диффузными болями, утомляемостью скелетной мускулатуры и снижением уровня болевого порога при пальпации в характерных местах, обозначаемых как «болезненные точки». ФМС является облигатным проявлением такого заболевания, как фибромиалгия (ФМ). Основной симптом ФМ — хроническая диффузная боль, не обусловленная какой-либо патологией скелетно-мышечного аппарата, которая беспокоит пациента не менее трех месяцев. Боль носит диффузный характер, распространяется по всему телу выше и ниже талии. Обычно пациенты описывают свое состояние как «я чувствую, что у меня болит везде» или «я себя ощущаю постоянно простуженным». Пациенты обычно описывают боль, которая распространяется по всем мышцам, но иногда также отмечают боль и припухлость в суставах. Кроме того, больные часто жалуются на парестезии, онемение, покалывание,жжение, ощущение ползания мурашек по коже, особенно в области ног и рук. У пациентов с ФМ при физикальном обследовании обнаруживается повышенная чувствительность или болезненность в определенных точках тела (с двух сторон, симметрично). Следует подчеркнуть, что фибромиалгия — это не только болевой синдром. Это состояние включает в себя целый комплекс беспокоящих больного других неболевых нарушений.
Фибромиалгический синдром (ФМС) характеризуется диффузными болями, утомляемостью скелетной мускулатуры и снижением уровня болевого порога при пальпации в характерных местах, обозначаемых как «болезненные точки». ФМС является облигатным проявлением такого заболевания, как фибромиалгия (ФМ). Основной симптом ФМ — хроническая диффузная боль, не обусловленная какой-либо патологией скелетно-мышечного аппарата, которая беспокоит пациента не менее трех месяцев. Боль носит диффузный характер, распространяется по всему телу выше и ниже талии. Обычно пациенты описывают свое состояние как «я чувствую, что у меня болит везде» или «я себя ощущаю постоянно простуженным». Пациенты обычно описывают боль, которая распространяется по всем мышцам, но иногда также отмечают боль и припухлость в суставах. Кроме того, больные часто жалуются на парестезии, онемение, покалывание,жжение, ощущение ползания мурашек по коже, особенно в области ног и рук. У пациентов с ФМ при физикальном обследовании обнаруживается повышенная чувствительность или болезненность в определенных точках тела (с двух сторон, симметрично). Следует подчеркнуть, что фибромиалгия — это не только болевой синдром. Это состояние включает в себя целый комплекс беспокоящих больного других неболевых нарушений.
 читайте также пост: Фибромиалгия (на laesus-de-liro.livejournal.com) [читать]
читайте также пост: Фибромиалгия (на laesus-de-liro.livejournal.com) [читать]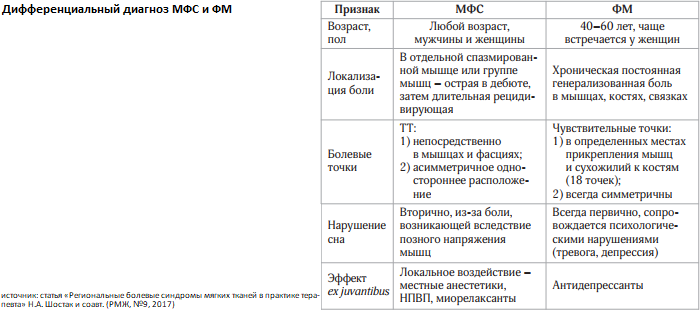
 читайте также статью «Региональные болевые синдромы мягких тканей в практике терапевта» Н.А. Шостак, Н.Г. Правдюк, дВ.Т. Тимофеев, Д.В. Абельдяев; ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» МЗ РФ, Москва (РМЖ, №9, 2017) [читать]
читайте также статью «Региональные болевые синдромы мягких тканей в практике терапевта» Н.А. Шостак, Н.Г. Правдюк, дВ.Т. Тимофеев, Д.В. Абельдяев; ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» МЗ РФ, Москва (РМЖ, №9, 2017) [читать] читайте также материалы из книги «Миофасциальные боли и дисфункции. Руководство по триггерным точкам в 2 томах» Трэвелл и Симонс (на healthy-back.livejournal.com ) [читать]
читайте также материалы из книги «Миофасциальные боли и дисфункции. Руководство по триггерным точкам в 2 томах» Трэвелл и Симонс (на healthy-back.livejournal.com ) [читать] Мышечный синдром ассоциированный с ревматической патологией. Наиболее яркими представителями этого синдрома являются: ревматическая полимиалгия и полимиозит.
Мышечный синдром ассоциированный с ревматической патологией. Наиболее яркими представителями этого синдрома являются: ревматическая полимиалгия и полимиозит.Для ревматической полимиалгии характерна боль и скованность в проксимальных отделах конечностей, как правило симметрично с двух сторон (но в самом начале заболевания возможна односторонность поражения). Боли могут возникать и в других областях опорно-двигательного аппарата, например, в голенях, спине и даже в предплечьях, но не столь закономерно. Боли обычно постоянные режущего, тянущего, рвущего характера резко усиливаются при движении. Интенсивность болей четко связана с активностью болезни. Характерна утренняя скованность. Кроме того, ощущение скованности появляется после любого периода неподвижности. Важно пронаблюдать, как больной поднимается с постели: сначала медленно, морщась от боли, поворачивается на бок, подтягивает ноги к животу, спускает их с постели, опираясь руками, с трудом садится и лишь затем, также с помощью рук, встает. Из-за болей ограничиваются движения: больным трудно встать, сесть, поднять руки, завести их за спину, невозможно без помощи войти в транспорт и т. д. В покое боли обычно стихают, хотя в 25 — 30% случаев сохраняются. Часто беспокоят ночные боли, которые усиливаются под влиянием тяжести тела, давления. Сон из-за этого становится прерывистым, отдых нарушается. При пальпации мышц болезненность небольшая или отсутствует вообще. Нет ни атрофий, ни инфильтраций в мышцах плечевого и тазового пояса, мышечная сила сохранена (нет истинных парезов, но возможно некоторое снижение силы из-за анталгической реакции).
 читайте также пост: Ревматическая полимиалгия (на laesus-de-liro.livejournal.com) [читать]
читайте также пост: Ревматическая полимиалгия (на laesus-de-liro.livejournal.com) [читать]Классическая клиническая картина полимиозита (ПМ) включает [в комплексе с другими симптомами ПМ] мышечную симметричную слабость проксимальных отделов мышц: слабость плечевого и тазового пояса, проксимальных отделов конечностей, мышц шеи (передняя группа мышц — сгибатели), реже — длинных мышц спины; а также миалгии (при пальпации мышц или спонтанные [существует миалгическая форма полимиазита]) и отеки мышц. У таких пациентов наблюдаются затруднения при вставании, подъеме по лестнице, например при входе в автобус, при одевании и причесывании. По мере прогрессирования болезни возможны внезапные падения при ходьбе по ровной поверхности, трудность при переворачивании в постели. Постепенно слабость нарастает, и зачастую (в т.ч. при отсутствии терапии) пациент становится практически обездвижен. Поражение поперечнополосатых мышц голосовых связок приводит к дисфонии (т.е. к «гнусавости» голоса), а вовлечение мышц глотки — к дисфагии («поперхиванию» твердой пищей и выливанию жидкой пищи через нос), повышая риск развития аспирационной пневмонии.
 читайте также пост: Полимиозит и другие воспалительные миопатии (на laesus-de-liro.livejournal.com) [читать]
читайте также пост: Полимиозит и другие воспалительные миопатии (на laesus-de-liro.livejournal.com) [читать] Крепатура или мышечная боль после физической нагрузки (в специальной спортивной литературе и именуется общепризнанной аббревиатурой «DOMS» — Delayed onset Muscle Soreness — отсроченное начало боли в мышцах). Практически все теоретики силовой подготовки и тренеры едины в том, что главным виновником DOMS являются эксцентрические упражнения, связанные с удлинением мышцы под воздействие внешней нагрузки — выполняемая в уступающем режиме работа с отягощениями, бег вниз по склону или ступенькам, альпинистский спуск и т.д. Клинические проявления DOMS включают: [1] мышечную болезненность, начинающуюся после 12 — 24 часов с момента окончания тренировки с манифестацией симптомов ко вторым суткам; [2] болезненность при пальпации вдоль вовлеченного брюшка мышцы или мышечно-сухожильного сочленения; [3] повышенную болезненность при пассивном растягивании или активном сокращении вовлечённой мышцы; [4] локальный отек и гиперемия; [5] мышечную напряженность, проявляющуюся спонтанным мышечным сокращением до возникновения боли; [6] снижение мышечной силы с момента возникновения мышечной болезненности, которая сохраняется еще до одной-двух недель после стихания болевых ощущений.
Крепатура или мышечная боль после физической нагрузки (в специальной спортивной литературе и именуется общепризнанной аббревиатурой «DOMS» — Delayed onset Muscle Soreness — отсроченное начало боли в мышцах). Практически все теоретики силовой подготовки и тренеры едины в том, что главным виновником DOMS являются эксцентрические упражнения, связанные с удлинением мышцы под воздействие внешней нагрузки — выполняемая в уступающем режиме работа с отягощениями, бег вниз по склону или ступенькам, альпинистский спуск и т.д. Клинические проявления DOMS включают: [1] мышечную болезненность, начинающуюся после 12 — 24 часов с момента окончания тренировки с манифестацией симптомов ко вторым суткам; [2] болезненность при пальпации вдоль вовлеченного брюшка мышцы или мышечно-сухожильного сочленения; [3] повышенную болезненность при пассивном растягивании или активном сокращении вовлечённой мышцы; [4] локальный отек и гиперемия; [5] мышечную напряженность, проявляющуюся спонтанным мышечным сокращением до возникновения боли; [6] снижение мышечной силы с момента возникновения мышечной болезненности, которая сохраняется еще до одной-двух недель после стихания болевых ощущений. читайте также пост: Мышечная боль после физической нагрузки (на laesus-de-liro.livejournal.com) [читать]
читайте также пост: Мышечная боль после физической нагрузки (на laesus-de-liro.livejournal.com) [читать] читайте также статью (лекцию) «Миалгии: подходы к дифференциальной диагностике, лечение» Н.А. Шостак, ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва (журнал «Современная ревматология» №3, 2013) [читать]
читайте также статью (лекцию) «Миалгии: подходы к дифференциальной диагностике, лечение» Н.А. Шостак, ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва (журнал «Современная ревматология» №3, 2013) [читать]Синдром гиперкортицизма — Википедия
Синдро́м гиперкортици́зма (синдром Ице́нко — Ку́шинга, кушинго́ид, синдром Ку́шинга, англ. Cushing’s syndrome) — предклиническое состояние, при котором происходит длительное хроническое воздействие на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение количества этих гормонов в крови.
Синдромом Кушинга называют предклиническое состоянием с повышенным уровнем эндогенного кортизона. При дальнейшем повышении уровня секреции кортизона диагностируется болезнь Кушинга[1].
Синдром гиперкортицизма сопровождается следующими типичными проявлениями:
- нарушается обмен белков, жиров и углеводов;
- активируется распад белков, образуется избыточное количество свободных жиров в крови, повышается количество глюкозы в крови пациента, что может привести к развитию стероидного сахарного диабета.
Проявления и синдрома, и болезни Кушинга обусловлены избыточной секрецией гормонов коры надпочечников, прежде всего глюкокортикоидов.
Один из видов синдрома, циклический синдром Кушинга или синдром периодического гиперкортицизма, характеризуется периодическим повышением уровня выработки кортизона и встречается чрезвычайно редко. Он диагностируется при обнаружении не менее трёх пиков секреции кортизона с промежуточными спадами. Это состояние сопровождается повышенным уровнем секреции адренокортикотропный гормона гипофизом[2].
Избыточная секреция кортизона нередко приводит к ожирению[2].
История[править | править код]
В 1912 году этот синдром описан американским врачом Харви Кушингом, который назвал его англ. polyglandular syndrome[3], и независимо от него в 1924-м одесским неврологом Николаем Михайловичем Иценко. Просуммировав свои наблюдения в 1932 году, Кушинг опубликовал работу «Базофильные аденомы гипофиза и их клинические проявления»[4].
Причиной синдрома Кушинга могут быть различные состояния. Чаще всего синдром гиперкортицизма (избыточное образование гормонов коры надпочечников) бывает обусловлен повышенной выработкой адренокортикотропного гормона гипофиза (болезнь Иценко — Кушинга). Этот гормон может вырабатываться микроаденомой гипофиза или эктопированной (расположенной не на обычном месте) кортикотропиномой. Эктопированная злокачественная кортикотропинома может располагаться в бронхах, яичках, яичниках.
Реже синдром Кушинга возникает при первичном поражении коры надпочечников (доброкачественные или злокачественные опухоли коры надпочечников, гиперплазия коры надпочечников). Гормонально-активная опухоль коры надпочечника называется кортикостерома. Она продуцирует в кровь избыточное количество глюкокортикоидов. При этом из-за избыточного количества глюкокортикоидов в крови снижается количество адренокортикотропного гормона гипофиза и оставшаяся ткань надпочечников подвергается атрофическим изменениям.
Синдром гиперкортицизма может возникнуть при поступлении глюкокортикоидов в организм извне, например, при длительном лечении различных заболеваний при помощи глюкокортикоидов, а также инъекциях глюкокортикоидных препаратов в область суставов и нервов, использовании некоторых кремов для кожи (включая отбеливающие), растительных препаратов, “тоников”, применении мегестрола ацетата (синтетического производного прогестерона с глюкокортикоидной активностью)[1][5]. Также причиной гиперкортицизма может быть приём глюкокортикоидов втайне от врачей с целью имитации заболевания[6]. Достаточно часто гиперсекреция кортизола наблюдается при ожирении, хронической алкогольной интоксикации, беременности и некоторых психических и неврологических заболеваниях — такое состояние называется «Псевдо-Кушинга синдром» или «функциональный гиперкортицизм», который не вызван опухолями, но клиническая картина наблюдается как и при истинном синдроме Иценко — Кушинга.
В основе патогенеза патологических изменений, которые развиваются при синдроме Кушинга со стороны большинства органов и систем, лежит в первую очередь гиперпродукция кортизола. Кортизол в нефизиологических концентрациях оказывает действие на белковые структуры и матрицы большинства тканей и структур (кости, мышцы, в том числе гладкие и миокард, кожа, внутренние органы и т. п.), в которых постепенно развиваются выраженные дистрофические и атрофические изменения. Нарушения углеводного обмена заключаются в стойкой стимуляции глюконеогенеза и гликогенолиза в мышцах и печени, что приводит к гипергликемии (стероидный диабет). Сложным образом меняется жировой обмен: на одних участках тела происходит избыточное отложение, а на других — атрофия жировой клетчатки, что объясняется разной чувствительностью отдельных жировых отделов к глюкокортикоидам. Важным компонентом патогенеза синдрома Кушинга являются электролитные расстройства (гипокалиемия, гипернатриемия), которые обусловлены влиянием избытка кортизола на почки. Прямым следствием этих электролитных сдвигов является артериальная гипертензия и усугубление миопатии, в первую очередь кардиомиопатии, которая приводит к развитию сердечной недостаточности и аритмиям. Иммуносупрессивное действие глюкокортикоидов обусловливает склонность к инфекциям.
Наиболее частым вариантом синдрома Кушинга, с которым сталкиваются врачи большинства специальностей, является экзогенный синдром Кушинга, который развивается на фоне терапии глюкокортикоидами.[7] Болеют в основном лица в возрасте 20—40 лет.
Наиболее ранним признаком болезни является ожирение, с типичным отложением жировой клетчатки в области лица, шеи, груди, живота. Лицо при этом выглядит округлым, лунообразным. На щеках появляется пурпурный румянец.
Глюкокортикоиды вызывают повышение аппетита и изменяют обмен веществ, увеличивая уровень глюкозы в крови и усиленное отложение жира. Конечности наоборот становятся тонкими из-за уменьшения массы мышечной ткани.
На коже в области живота, плечевого пояса, ягодиц и бедер появляются багрово-синюшные полосы растяжения — стрии. Это результат растяжения кожи при избыточном отложении жиров и нарушения обмена белка, из-за чего кожа истончается и легко растягивается. На коже появляются угревые высыпания. Раны и порезы заживают медленно.
В местах трения в области воротника на шее, в области живота, локтей возникает усиленная окраска кожных покровов. В этих местах откладывается меланин, количество которого увеличивается вместе с количеством адренокортикотропного гормона.
У женщин возникает гирсутизм (избыточное оволосение). Появляются волосы на верхней губе, подбородке, груди. Избыточный рост волос у женщин обусловлен усилением продукции мужских половых гормонов андрогенов корой надпочечников, что у женщин вызывает также нарушения менструального цикла. У мужчин возникает импотенция.
Вначале появляется периодическое, затем постоянное повышение артериального давления. Постепенно развивается разрежение костной ткани — остеопороз, который проявляется сначала болями в костях и суставах, затем могут возникнуть спонтанные переломы ребер, конечностей. Избыток глюкокортикоидов как вызывает нарушение образования белковой основы костей, так и усиливает выход кальция из костной ткани.
Пациенты жалуются на слабость, головные боли, увеличение массы тела. Иногда у больных болезнью с гиперкортицизмом возникают нарушения психики. Появляются депрессия, различные нарушения сна, психозы.
Цель лечения — нормализация уровня гормонов коры надпочечников в крови. Применяются препараты, снижающие продукцию гормонов в коре надпочечников — кетоконазол, мамомит — в течение длительного времени.
В некоторых случаях применяется дексаметазон с целью угнетения функции коры надпочечников[2].
Проводится симптоматическое лечение, направленное на коррекцию нарушений белкового и углеводного обмена, нормализацию уровня артериального давления, лечение сердечной недостаточности. При наличии у пациента кортикостеромы, производится одностороннее удаление надпочечника (односторонняя адреналэктомия).
- ↑ 1 2 The diagnosis of Cushing’s syndrome : an Endocrine Society Clinical Practice Guideline // The Journal of Clinical Endocrinology and Metabolism. |volume=93 |issue=5 |pages=1526—1540 |pmid=18334580 |pmc=2386281 |doi=10.1210/jc.2008-0125 |язык=en |автор=Nieman |автор имя=L. K. |автор2=Biller |автор2 имя=B. M. |автор3=Findling |автор3 имя=J. W. |автор4=Newell-Price |автор4 имя=J. |автор5= M. O. Savage, P. M. Stewart, V. M. Montori |месяц=5 |год=2008}}
- ↑ 1 2 3 M. Alberich, Ruano. Cyclic Cushing’s syndrome due to occult ectoric ACTH secretion : [англ.] / Ruano M. Alberich, M. Boronat Cortés, C. Rodriguez Perez … [] // Endocrine Abstracts. — 2012. — Vol. 29. — P. 359. — ISSN 1479-6848.
- ↑ The Pituitary Body and its Disorders. Clinical States produced by Disorders of the Hypophysis Cerebri. Philadelphia, J. B. Lippincott, 1912.
- ↑ Papers Relating to the Pituitary Body, Hypothalamus and Parasympathetic Nervous System. Springfield Illinois, C. C. Thomas, 1932
- ↑ Cushing Syndrome (англ.). NORD. National Organization for Rare Disorders (2017). Дата обращения 10 ноября 2019.
- ↑ Kinns, H. Munchausen syndrome and factitious disorder : the role of the laboratory in its detection and diagnosis : [англ.] / H. Kinns, D, Housley, D. B. Freedman // Annals of Clinical Biochemistry (англ.)русск.. — 2013. — Vol. 50, no. Pt. 3 (May). — P. 194—203. — DOI:10.1177/0004563212473280. — PMID 23592802.
- ↑ Синдром Кушинга | Эндокринология — aorta.ru | заболевания, медицина, здоровье, болезни, секс
| Нозологии |
| ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Гормоны и медиаторы | Белковые гормоны: Пептидные гормоны: АКТГ, СТГ, Меланоцитостимулирующий гормон, Пролактин, Паратгормон, Кальцитонин, Инсулин, Глюкагон;
| ||||||||||||||||||
Мышечно-тонический синдром: причины, симптомы, лечение

Мышечно-тонический синдром — сложный симптомокомплекс, обусловленный перенапряжением мышечных волокон, появлением в их толще болезненных и плотных тяжей. Это компенсаторное повышение тонуса мышц, возникающее в зоне иннервации пораженного сегмента позвоночника. Спазм мышц происходит спонтанно при сдавливании и раздражении определенного нервного волокна. Причиной развития недуга чаще всего являются дегенеративные и дистрофические явления в позвоночнике, протекающие в форме остеохондроза или спондилеза.
Заболевание чаще всего развивается при поражении шейных структур. Его основным проявлением является боль — цервикалгия. Болевой синдром имеет резкий характер. Он усиливается при движении головой и сопровождается цефалгией, головокружением, снижением остроты зрения. Шейный отдел позвоночника поражается намного чаще грудного и поясничного сегментов. Его позвонки высоко подвижны и окружены обилием мышц. Они способны совершать движения в различных направлениях. Сосудисто-нервные стволы шеи отличаются особым расположением, что также играет роль в развитии данной патологии. Депрессии и стрессы провоцируют психовегетативный синдром, который проявляется дистонией мышц шеи, лица и головы, приводящей к появлению боли в голове и прочих симптомов синдрома.

Заболевания органов, расположенных в грудной полости, сопровождаются изменением тонуса и чрезмерным натяжением соответствующих мышц. Патология почек, органов мочевыведения и репродуктивной системы проявляются расстройствами сексуальной сферы, болевым синдромом, перенапряжением мышц крестцово-поясничной области.
Виды патологии:
- Умеренный синдром — боль возникает только при прикосновении, в мышце пальпируются болезненные уплотнения;
- Выраженный синдром — боль становится нестерпимой при каждом прикосновении, ее интенсивность усиливается при растирании пораженной части, мышечные волокна напоминают фиброзные тяжи.

формирование уплотнений в мышцах при прогрессировании мышечно-тонического синдрома
Типы синдрома:
- Локальный — поражение одной мышцы или ее одного участка;
- Диффузный — поражение целой группы мышц.
Этиология и патогенез
Патология имеет вертеброгенное происхождение и является следствием остеохондроза. При раздражении болевых рецепторов возникает дискомфорт, который постепенно перерастает в мучительную и нестерпимую боль. В ответ на ее появление пораженные мышцы спазмируются. Длительный спазм — причина боли. Так замыкается порочный круг, лежащий в основе данного недуга.
Заболевания, проявляющиеся признаками патологии:
- Воспаление позвоночника с ограничением его подвижности,
- Межпозвоночные грыжи,
- Артроз суставов,
- Анкилозирующий спондилит,
- Сколиоз, кифоз, лордоз,
- Миофасциальный синдром,
- Травматическое повреждение позвоночника,
- Воспаление оболочек мозга,
- Геморрагический инсульт,
- Заглоточный или эпидуральный абсцесс,
- Аутоиммунные заболевания соединительной ткани.

Факторы, способствующие развитию патологии:
- продолжительное нахождение в неправильном положении,
- нарушение осанки,
- гиподинамия,
- физическое перенапряжение,
- сквозняки,
- всплески эмоций,
- гиповитаминоз,
- табакокурение,
- деформация нижних конечностей,
- лишний вес,
- несбалансированное питание.
Шейный мышечно-тонический синдром часто развивается у лиц, работающих за компьютером, у офисных работников и всех, кто ведет малоподвижный образ жизни, трудится в одной и той же позе с фиксированным положением головы. Тяжелая верхняя одежда, узкий ворот рубашки и туго затянутый галстук оказывают давление на структуры шеи, что также способствует развитию патологии.
Развитию синдрома поясничного отдела способствует чрезмерно активное перекапывание земли, подъем тяжестей, долгие пешие прогулки. Провоцирует его появление также неудобная постель, атипичная постановка стопы, не по размеру подобранная обувь.
Патогенетические звенья патологии:
- Дегенеративно-дистрофические изменения в позвоночнике,
- Раздражение рецепторов боли, расположенных около межпозвоночного диска и вдоль связочного аппарата позвоночного столба,
- Спазматическое сокращение мышц,
- Чрезмерное мышечное перенапряжение,
- Нарушение оттока крови,
- Отечность тканей,
- Нарастание боли,
- Долгое мышечное спазмирование,
- Сдавливание сосудисто-нервных пучков уплотненными мышцами,
- Кислородное голодание,
- Дистрофия,
- Дисфункция пораженных мышц,
- Отмирание мышечных волокон,
- Замена мышц соединительной тканью,
- Рубцевание — образование жестких тяжей,
- Ограничение подвижности позвоночника,
- Усиление проявлений синдрома.

Мышечный спазм сигнализирует о наличии заболевания спины, которое рано или поздно проявит себя. Остеохондроз без лечения неуклонно прогрессирует.
Клиническая картина
Проявления патологии, возникающие при поражении шейного отдела позвоночника:
- Тяжесть и дискомфорт в шее,
- Цервикалгия,
- Трудности при поворотах и наклонах головы,
- Резкая или давящая, тупая головная боль, не поддающаяся действию анестетиков и распространяющаяся от затылочной области к височной,
- Образование уплотнений в мышечной ткани,
- При пальпации мышцы напоминают резиновый шланг,
- Отечность шеи,
- Скачки кровяного давления,
- Хруст в шее, возникающий при движении головой,
- Снижение остроты зрения,
- Расстройство слуха,
- Парестезии рук и лица.

Боль является основным симптомом патологии. Она имеет ноющий, тупой, мучительный характер и большую распространенность. Пациенты могут указать конкретное место локализации боли. При нажатии на болевую точку неприятные ощущения усиливаются. Болезненные чувства переносятся крайне тяжело. У пациентов возникает бессонница из-за постоянного поиска выгодной позы. Они устают, изматываются, впадают в отчаяние, погружаются в депрессию. В тех местах, где боль максимально выражена, образуются очаги уплотнения, обусловленные отложением солей кальция.
Цервикалгия при мышечно-тоническом синдроме имеет различную степень выраженности. Иногда состояние пациента ухудшается настолько, что у него мутнеет в глазах, возникает общая слабость и чувство тяжести в затылочной области, которое больной сравнивает с ощущением шлема на голове. Резкая боль в шее отдает в левую или правую часть головы. Пальпаторно по задней поверхности шеи обнаруживаются плотные и болезненные тяжи. Это довольно плотные и грубые образования, напоминающие на ощупь веретена. По мере прогрессирования патологии больные начинают жаловаться на появление дискомфортных ощущений в плече. Они отмечают локальную боль, ограничение подвижности сустава, повышенную чувствительность кожи плечевой области. Боль в течение дня постоянная, ее пик приходится на утреннее или ночное время. При надавливании пальцем на межпозвоночные связки боль обостряется. Спазмированные мышечные волокна непроизвольно подергиваются. При активном выполнении различных действий плечом появляется характерный хруст. Такой же хруст возникает при ощупывании тяжа на шее. Шея у больных симметричная, но опухшая. В дальнейшем они отмечают онемение, дискомфорт и боль в запястье и пальцах.
При развитии патологии на уровне груди основным симптомом также является боль. Она возникает внезапно и затрудняет полноценный вдох и выдох. Болевой синдром напоминает кардиалгию при заболеваниях сердечно-сосудистой системы. В результате в крови накапливается углекислота, и возникает гипоксия. Симптомы подобных процессов: головокружение, слабость мышц, судороги, апатия.
Гипертонус мышц поясничного отдела позвоночника проявляется мучительной болью, ограничивающей выполнение повседневных действий, а также парестезиями и слабостью в ногах. Больным очень сложно сгибаться и разгибаться, вставать с кровати. При пальпации позвонков боль усиливается.
Диагностические мероприятия
Диагностика патологии заключается в выслушивании жалоб больного и тщательном сборе анамнеза. Специалисты пытаются понять, как долго длится болевой синдром, насколько он интенсивен, какой характер имеет и как взаимосвязаны спазмы и движения?

Определение неврологического статуса пациента — следующий этап в постановке диагноза. Обычно у больных с мышечно-тоническим синдромом отсутствуют общемозговые и очаговые симптомы, менингеальные знаки. Определяется болезненная пальпация краниовертебрального перехода и паравертебральных точек на всех уровнях. Простукивание мышц перкуссионным молоточком позволяет обнаружить дефект.
Инструментальная и лабораторная диагностика:
- Рентгенологическое исследование позвоночника выявляет дегенеративные изменения в костной ткани.
- С помощью томографического исследования можно обнаружить патологические изменения в мышцах и связках.
- Электромиография позволяет выявить имеющееся нарушение нервно-мышечной проводимости.
- Анализ крови на параклинические и биохимические показатели — обязательные стандартные методики.
- Биопсия и гистологическое исследование пораженных мышечных волокон проводится по строгим врачебным показаниям.
Лечение
Диагностикой и лечением патологии занимаются специалисты в области неврологии. Врач после обследования больного ставит окончательный диагноз и назначает лечение по современным медицинским методикам.
Мышечно-тонический синдром неизлечим. Общетерапевтические мероприятия должны быть направлены на основное заболевание, ставшее первопричиной мышечных спазмов. Больным показана симптоматическая терапия, позволяющая вернуть их к нормальной жизни.

Специалисты назначают пациентам следующие группы препаратов:
- НПВС – «Кетопрофен», «Ибупрофен», «Мелоксикам», «Мовалис»;
- Новокаиновые блокады — введение «Новокаина» в пораженную область;
- Кортикостероиды назначают в виде местных инъекций для снятия боли и прочих признаков воспаления – «Кеналог», «Дипроспан»;
- Миорелаксанты для расслабления пораженных мышц – «Мидокалм», «Сирдалуд»;
- Хондропротекторы – «Алфлутоп», «Терафлекс»;
- Витамины группы В нормализуют обменные процессы в нервной ткани;
- Местно — мази и гели с НПВС: «Вольтарен», «Нурофен», «Долгит»;
- Средства, улучшающие кровоснабжение – «Актовегин», «Трентал»;
- Спазмолитики – «Папаверин», «Дротаверин»;
- Антидепрессанты и антиконвульсанты по индивидуальному врачебному назначению.
Эти лекарства лишь устраняют симптомы. Они не способны полностью восстановить хрящи и оказать благоприятное воздействие на структуры позвоночника. После стихания боли и нормализации мышечного тонуса больные возвращаются к полноценной жизни.
Помимо медикаментозного воздействия широко применяют физиотерапевтические процедуры.
- Массаж устраняет боль, восстанавливает нервно-мышечную проходимость в зоне поражения.
- Специальные корсеты снимают компрессию и разгружают пораженный отдел позвоночника. Они позволяют добиться ортопедического эффекта.
- Всем больным, особенно страдающим цервикалгией, показан сон на ортопедических подушках. С помощью них позвоночник расслабляется и максимально распрямляется.
- Занятия ЛФК и кинезитерапия помогут избежать повторного возникновения синдрома.
- Иглорефлексотерапия нормализует функции нервных волокон и устраняет боль.
- Магнитотерапия, УВЧ-терапия, диадинамические токи и электрофорез усиливают эффект медикаментозного воздействия, уменьшают боль, улучшают кровообращение, нормализуют мышечный тонус.
Если подобное комплексное лечение не дает ожидаемого эффекта, пациенту требуется помощь мануального терапевта или хирурга.
Только устранив источник болезни, можно избавиться от мышечно-тонического синдрома. Почувствовав временное облегчение от приема анестетиков, многие пациенты прерывают курс лечения, а болезнь продолжает прогрессировать. Избавиться от таких патологий, как остеохондроз и другие дегенеративные процессы, очень сложно, а порой и просто невозможно. Именно поэтому следует приложить максимум усилий, чтобы сохранить свое здоровье на оптимальном уровне.
Профилактические мероприятия при данной патологии — занятия посильными видами спорта, ходьба на большие дистанции, правильное питание. Общая физическая подготовка – фундамент здорового тела. Укрепление мышц спины, регулярные физические нагрузки, удобство рабочего и спального места помогают избежать развития синдрома.
Видео: о мышечно-тоническом синдроме при остеохондрозе
Мышечная гипотония — Википедия
Материал из Википедии — свободной энциклопедии
Мышечная гипотония (мышечный гипотонус) — состояние пониженного мышечного тонуса (степени напряжения мышцы или её сопротивления движению), часто в сочетании со снижением мышечной силы (парезом). Гипотония — неспецифическое мышечное расстройство, которое может являться проявлением множества различных заболеваний, поражающих мотонейроны, контролируемые центральной нервной системой. Распознать гипотонию, даже в раннем младенчестве, обычно несложно; более сложно, зачастую невозможно, выявить причину данного состояния. Долгосрочные эффекты гипотонии в развитии ребёнка и дальнейшей жизни зависят в первую очередь от тяжести мышечной слабости и от природы заболевания. Некоторые расстройства подлежат специфической терапии, однако ведущим методом лечения большинства гипотоний идиопатической и неврологической природы является физиотерапия и/или трудотерапия.
Считается, что гипотония ассоциирована с нарушением афферентной импульсации от рецепторов растяжения и/или потерей растормаживающего эфферентного влияния мозжечка на фузимоторную систему (систему, иннервирующую интрафазульные мышечные волокна и контролирующую таким образом мышечную чувствительность на растяжение).[1] При осмотре выявляется снижение мышечного сопротивления пассивным движениям; пальпаторно можно отметить необычную мягкость мышц.[1] Также могут выявляться сниженные сухожильные рефлексы.
В числе причин гипотонии:
Врождённые заболевания[править | править код]
Врождённые заболевания, в том числе проявляющиеся в течение 6 месяцев от рождения:
Приобретённые заболевания[править | править код]
Заболевания, дебютирующие в течение жизни:
- Метаболические
- Неврологические
Мышечная гипотония может возникать при поражении периферического нерва, периферического мотонейрона в области передних рогов спинного мозга, а также мозжечка. Поражение червя мозжечка ведёт обычно к диффузной гипотонии мышц, тогда как при поражении полушария мозжечка снижение мышечного тонуса отмечается на стороне патологического очага[4].
Существуют разнообразные объективные симптомы гипотонии. Часто выявляется задержка формирования двигательных навыков, в сочетании с гипермобильностью и повышенной гибкостью суставов, слюнотечение и проблемы с речью, бедные рефлексы, снижение мышечной силы, снижение устойчивости к активности, рассеянность внимания и т. д. Выраженность объективных симптомов зависит от возраста пациента, тяжести гипотонии, локализации поражённых мышц, иногда — причины гипотонии. Например, некоторые пациенты с гипотонией могут жаловаться на запор, а у других проблемы с толстым кишечником отсутствуют.
При гипотонии зачастую ставится диагноз мышечной дистрофии или ДЦП, в зависимости от симптомов и врача. Если предполагается, что причина гипотонии лежит в ЦНС, ставится диагноз ДЦП. Если больше похоже, что поражены мышцы, это может расцениваться как мышечная дистрофия, даже несмотря на том, что большинство форм гипотонии не сопровождаются серьёзной дистрофией. Если предполагается поражение нервов, суждение о диагнозе может склониться в любую, или ни в какую, сторону. В любом случае, гипотония редко является проявлением мышечной дистрофии или церебрального паралича, и в связи с этим часто вообще никак не классифицируется[5].
Оригинальный текст (англ.)
A diagnosis of hypotonia is sometimes considered a form of muscular dystrophy or cerebral palsy, depending on the symptoms and the doctor. If the cause of the hypotonia is thought to lie in the brain, then it might be classified as a cerebral palsy. If the cause seems to be in the muscles, it might be classified as a muscular dystrophy, even though most forms of hypotonia are not seriously dystrophic. If the cause is thought to be in the nerves, it could be classified as either or neither. In any case, hypotonia is rarely an actual muscular dystrophy or cerebral palsy, and is often not classified as either one, or anything at all for that matter.
Диагностика включает сбор семейного анамнеза, физикальное обследование, могут потребоваться дополнительные исследования, включая компьютерную и магнитно-резонансную томографию, электроэнцефалографию, анализы крови, генетическое тестирование (хросомосное кариотипирование и т. д.), исследование ликвора, электромиографию, биопсию мышцы или нерва.
Боковой амиотрофический склероз — Википедия
Боково́й (латера́льный) амиотрофи́ческий склеро́з (БАС; также известен как боле́знь мото́рных нейро́нов, мотонейро́нная боле́знь, боле́знь Шарко́, в англоязычных странах — болезнь Лу Ге́рига [англ. Lou Gehrig’s disease]) — прогрессирующее, неизлечимое дегенеративное заболевание центральной нервной системы, при котором происходит поражение как верхних (моторная кора головного мозга), так и нижних (передние рога спинного мозга и ядра черепных нервов) двигательных нейронов, что приводит к параличам и последующей атрофии мышц.
Характеризуется прогрессирующим поражением двигательных нейронов, сопровождаемым параличом (парезом) конечностей и атрофией мышц. Смерть наступает от инфекций дыхательных путей или отказа дыхательной мускулатуры. Боковой амиотрофический склероз следует отличать от синдрома БАС, который может сопровождать такие заболевания, как клещевой энцефалит.
Болезнь впервые описана в 1869 году Жан-Мартеном Шарко.
На международном уровне показатели заболеваемости боковым амиотрофическим склерозом (amyotrophic lateral sclerosis, ALS) или заболеванием двигательных нейронов (motor neurone disease, MND) по всему миру оцениваются в диапазоне от 0,86 до 2,5 на 100 тысяч человек в год[3], то есть БАС является редким заболеванием.
Точная этиология БАС неизвестна. Примерно в 5% случаев встречаются семейные (наследственные) формы заболевания. 20% семейных случаев БАС связаны с мутациями гена супероксиддисмутазы-1, расположенного в 21-й хромосоме[4][5]. Как полагают, этот дефект наследуется аутосомно-доминантно.
В патогенезе заболевания ключевую роль играет повышенная активность глутаматергической системы, при этом избыток глутаминовой кислоты вызывает перевозбуждение и гибель нейронов (т. н. эксайтотоксичность). Сохранившиеся мотонейроны могут спонтанно деполяризироваться, что клинически выявляется фасцикуляциями.
Учёные из Университета Джонса Хопкинса в Балтиморе установили молекулярно-генетический механизм, лежащий в основе возникновения данного заболевания. Он связан с появлением в клетках большого количества четырёхспиральной ДНК и РНК в гене C9orf72, что приводит к нарушению процесса транскрипции, а, следовательно, и синтеза белка. Однако, вопрос о том, как именно эти изменения ведут к деградации мотонейронов, остаётся открытым[6].
Также важное значение в патофизиологии имеет TDP-43, который был определен как основной компонент убиквитинированных цитоплазматических белковых агрегатов у всех пациентов со спорадическим БАС, но расположенный вне ядра (в нормальных нейронах он находится в ядре). Несмотря на то, что вопрос того, являются ли данные агрегаты причиной нейродеградации при БАС, остается открытым, мутации в TARDBP были обнаружены всего лишь в 3 % случаях наследственной формы склероза и у 1,5 % пациентов со спорадическим БАС, позволяя предположить, что агрегаты TDP-43 играют ключевую роль в инициации БАС. Помимо мутаций в гене TARDBP ионы цинка также могут вызывать агрегацию TDP-43[7][8].
Обнаружение мутаций гена FUS (Fusion in Sarcoma — ген «слияния в саркоме») в 16-й хромосоме, которые связаны с наследственными формами БАС, поддерживает данную теорию. Агрегаты FUS не были явно определены у пациентов с патологическими изменениями в TDP-43 или SOD1, что указывает на новый путь возникновения болезни.
На БАС приходится примерно 3% всех органических поражений нервной системы. Болезнь обычно развивается начиная с возраста 30—50 лет[9][10].
Суммарный риск получить БАС в течение жизни составляет 1:400 для женщин и 1:350 для мужчин.
5—10 % заболевших — носители наследственной формы БАС; на тихоокеанском острове Гуам выявлена особая, эндемичная форма заболевания. Абсолютное большинство случаев (90—95 %) не связаны с наследственностью и не могут быть положительно объяснены какими-либо внешними факторами (перенесёнными заболеваниями, травмами, экологической ситуацией и т. п.)[11].
Несколько научных исследований[12][13][14][15] нашли статистические корреляции между БАС и некоторыми сельскохозяйственными пестицидами.
Ранние симптомы болезни: подёргивания, судороги, онемение мышц, слабость в конечностях, затруднение речи — также свойственны многим более распространённым заболеваниям, поэтому диагностика БАС затруднена — до тех пор, пока болезнь не развивается до стадии мышечной атрофии.
В редких случаях возможно наличие продромальной фазы, до 1 года, во время которой будут наблюдаться изолированные фасцикуляции и/или судороги.
В зависимости от того, какие части тела поражены в первую очередь, различают
- БАС конечностей (до трёх четвертей больных) начинается, как правило, с поражения одной или обеих ног. Больные чувствуют неловкость при ходьбе, негибкость в голеностопе, спотыкаются. Реже встречаются поражения верхних конечностей, при этом затруднено выполнение обычных действий, требующих гибкости пальцев или усилия кисти.
- Бульбарный БАС проявляется в затруднении речи (больной говорит «в нос», гнусавит, плохо управляет громкостью речи, в дальнейшем испытывает трудности с глотанием).
Во всех случаях мышечная слабость постепенно охватывает всё больше частей тела (больные бульбарной формой БАС могут не доживать до полного пареза конечностей). Симптомы БАС включают признаки поражения как нижних, так и верхних двигательных нервов:
- поражение верхних двигательных нейронов: гипертонус мышц, гиперрефлексия, аномальный рефлекс Бабинского.
- поражение нижних двигательных нейронов: слабость и атрофию мышц, судороги, непроизвольные фасцикуляции (подёргивания) мышц.
Рано или поздно больной теряет способность самостоятельно передвигаться. Болезнь не влияет на умственные способности, но приводит к тяжёлому состоянию в ожидании неминуемой смерти. На поздних этапах болезни поражается дыхательная мускулатура, больные испытывают перебои в дыхании, в конечном итоге их жизнь может поддерживаться только искусственной вентиляцией лёгких и искусственным питанием. Обычно от выявления первых признаков БАС до смерти проходит от трёх до пяти лет. Однако широко известный физик-теоретик Стивен Хокинг (1942-2018) и гитарист Джейсон Беккер (род. 1969) — единственные известные больные с однозначно диагностированным БАС, у которых состояние со временем стабилизировалось.
- слабость;
- мышечные спазмы;
- нарушения речи и глотания;
- нарушение равновесия;
- спастика;
- повышение глубоких рефлексов или расширение рефлексогенной зоны[16];
- патологические рефлексы;
- атрофия;
- зависание стопы;
- респираторные расстройства;
- приступы непроизвольного смеха или плача;
- депрессия.
Существует множество заболеваний, вызывающих те же симптомы, что и ранние стадии БАС. Диагностика заболевания возможна только методом исключения более распространённых заболеваний. Оба ключевых признака БАС (поражения и верхних, и нижних двигательных нейронов) проявляются на достаточно развитых стадиях болезни.
Международной федерацией неврологии (англ. World Federation of Neurology) разработаны Эль-Эскориальские критерии для постановки диагноза БАС[17]. Для этого необходимо наличие:
- признаков поражения центрального мотонейрона по клиническим данным
- признаков поражения периферического мотонейрона по клиническим, электрофизиологическим и патоморфологическим данным
- прогрессирующего распространения симптомов в пределах одной или нескольких областей иннервации, что выявляют при наблюдении за больным
При этом должны быть исключены другие причины данных симптомов.
Для электрофизиологического обследования используется электромиография, которая полезна в исследовании проводимости нервов и определении наличия признаков поражения периферического мотонейрона (потенциалы фибрилляций, потенциалы фасцикуляций, положительные острые волны и др).
Также важно дифференцировать фасцикуляции при БАС от фасцикуляций при синдроме доброкачественных фасцикуляций (англ. BFS), который зачастую диагностируется при наличии фасцикуляций и одновременном отсутствии объективной слабости и изменений на ЭМГ, и имеет чаще всего психологическую причину.
Второстепенными методами диагностики являются:
- МРТ головного и спинного мозга
- биохимический анализ крови (КФК, креатинин, общий белок, АЛС, АСТ, ЛДГ)
- клинический анализ крови
- исследование ликвора (белок, клеточный состав)
- серологические анализы (антитела к боррелиям, к ВИЧ)
- транскраниальная магнитная стимуляция (ТМС)
- биопсия мышцы или нерва
Возможные изменения при обследовании второстепенными методами диагностики:
- повышение КФК в 2-3 раза (у 50 % больных)
- незначительное повышение АЛТ, АСТ, ЛДГ
- выявление отмирания пирамидных путей на МРТ
- признаки атрофии и денервации при гистологическом исследовании
Больным БАС требуется поддерживающая терапия для облегчения симптомов[18].
Постепенно у больных начинает ослабляться дыхательная мускулатура, развивается дыхательная недостаточность и становится необходимым применение оборудования для облегчения дыхания во время сна (IPPV или BIPAP). Затем, после полного отказа дыхательной мускулатуры, требуется круглосуточное использование аппарата искусственной вентиляции лёгких.[18]
Ведутся исследования по методу лечения, использующего блокировку генов, вызывающих это заболевание[19].
Замедление прогрессирования[править | править код]
Рилузол (рилутек) — единственный препарат, достоверно замедляющий прогрессирование БАС[20][21]. Доступен с 1995 года. Он ингибирует высвобождение глутамата, тем самым уменьшая повреждение двигательных нейронов. Продлевает жизнь больных в среднем на месяц, немного отдаляет момент, когда больному потребуется искусственная вентиляция легких[22].
HAL-терапия, новый метод роботизированного лечения, официально допущен к применению в реабилитации БАС в Европе и Японии[23].
Также проводятся клинические исследования по применению препаратов Radicava[24] и Masitinib.
В России[править | править код]
В Москве действуют:
В то же время в России многим больным БАС не оказывается надлежащая медицинская помощь[25]. Например, до 2011 года БАС даже не был включен в список редких заболеваний, а единственный препарат, замедляющий течение болезни, Рилузол, не зарегистрирован[26].
Летом 2014 года проходила популярная вирусная акция по повышению осведомлённости о заболевании и сбор средств, получившая название Ice Bucket Challenge или ALS Ice Bucket Challenge. Летом 2018 года акция прошла повторно для сбора средств на построение клиники по борьбе с заболеванием в Южной Корее.
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Epidemiology of Sporadic ALS. (англ.) (недоступная ссылка). Stanford Medicine » School of Medicine. Дата обращения 24 октября 2015. Архивировано 8 октября 2015 года.
- ↑ Conwit, Robin A. Preventing familial ALS: A clinical trial may be feasible but is an efficacy trial warranted? (англ.) // Journal of the Neurological Sciences (англ.)русск. : journal. — 2006. — December (vol. 251, no. 1—2). — P. 1—2. — ISSN 0022-510X. — DOI:10.1016/j.jns.2006.07.009. — PMID 17070848.
- ↑ Al-Chalabi, Ammar; P. Nigel Leigh. Recent advances in amyotrophic lateral sclerosis (англ.) // Current Opinion in Neurology (англ.)русск.. — Lippincott Williams & Wilkins (англ.)русск., 2000. — August (vol. 13, no. 4). — P. 397—405. — ISSN 1473-6551. — DOI:10.1097/00019052-200008000-00006. — PMID 10970056.
- ↑ «Болезнь Хокинга» объяснили появлением четырехспиральной ДНК // Лента.ру, 2014-03-07
- ↑ Cyrille Garnier, François Devred, Deborah Byrne, Rémy Puppo, Andrei Yu. Roman. Zinc binding to RNA recognition motif of TDP-43 induces the formation of amyloid-like aggregates (En) // Scientific Reports. — 2017-07-28. — Т. 7, вып. 1. — ISSN 2045-2322. — DOI:10.1038/s41598-017-07215-7.
- ↑ Aphrodite Caragounis, Katherine Ann Price, Cynthia P.W. Soon, Gulay Filiz, Colin L. Masters. Zinc induces depletion and aggregation of endogenous TDP-43 // Free Radical Biology and Medicine. — Т. 48, вып. 9. — С. 1152—1161. — DOI:10.1016/j.freeradbiomed.2010.01.035.
- ↑ Хондкариан О. А., Боковой амиотрофический склероз, в кн.: Многотомное руководство по неврологии, под ред. С. Н. Давиденкова, т. 3, кн. 1, М., 1962
- ↑ Амиотрофический боковой склероз — статья из Большой советской энциклопедии.
- ↑ http://www.ninds.nih.gov/disorders/amyotrophiclateralsclerosis/detail_ALS.htm Архивная копия от 4 января 2015 на Wayback Machine «In 90 to 95 percent of all ALS cases, the disease occurs apparently at random with no clearly associated risk factors. … About 5 to 10 percent of all ALS cases are inherited. The familial form of ALS usually results from a pattern of inheritance that requires only one parent to carry the gene responsible for the disease. Mutations in more than a dozen genes have been found to cause familial ALS.»
- ↑ Exposure to pesticides and risk of amyotrophic lateral sclerosis: a population-based case-control study.By Bonvicini F, Marcello N, Mandrioli J, Pietrini V, Vinceti M. In Ann Ist Super Sanita. 2010; 46(3):284-7.PMID 20847462
- ↑ Pesticide exposure as a risk factor for amyotrophic lateral sclerosis: A meta-analysis of epidemiological studies: Pesticide exposure as a risk factor for ALS. By Malek AM, Barchowsky A, Bowser R, Youk A, Talbott EO. In Environ Res. 2012 Aug; 117:112-9. PMID 22819005
- ↑ Are environmental exposures to selenium, heavy metals, and pesticides risk factors for amyotrophic lateral sclerosis?. By Vinceti M, Bottecchi I, Fan A, Finkelstein Y, Mandrioli J. In Rev Environ Health. 2012; 27(1):19-41. PMID 22755265
- ↑ Pesticide exposure and amyotrophic lateral sclerosis. By Kamel F, Umbach DM, Bedlack RS, Richards M, Watson M, Alavanja MC, Blair A, Hoppin JA, Schmidt S, Sandler DP. In Neurotoxicology. 2012 Jun; 33(3):457-62. PMID 22521219
- ↑ Рефлексогенные зоны — статья из Большой советской энциклопедии.
- ↑ Brooks B.R., Miller R.G., Swash M., Munsat T.L. El Escorial revisited: revised criteria for the diagnosis of amyotrophic lateral sclerosis (англ.) // Amyotroph. Lateral Scler. Other Motor Neuron Disord. : journal. — 2000. — December (vol. 1, no. 5). — P. 293—299. — PMID 11464847.
- ↑ 1 2 http://www.ninds.nih.gov/disorders/amyotrophiclateralsclerosis/detail_ALS.htm Архивная копия от 4 января 2015 на Wayback Machine How is ALS treated?
- ↑ Эрон Гитлер, Леонард Петручелли. Разгадка тайны БАС // В мире науки. — 2017. — № 8/9. — С. 50—56.
- ↑ Неврология. Национальное руководство. — ГЭОТАР-Медиа, 2010. — 2116 с. — 2000 экз. — ISBN 978-5-9704-0665-6.
- ↑ Riluzole // PATIENT & CAREGIVER EDUCATION (рус.)
- ↑ http://www.ninds.nih.gov/disorders/amyotrophiclateralsclerosis/detail_ALS.htm Архивная копия от 4 января 2015 на Wayback Machine However, the Food and Drug Administration (FDA) approved the first drug treatment for the disease—riluzole (Rilutek)—in 1995. Riluzole is believed to reduce damage to motor neurons by decreasing the release of glutamate. Clinical trials with ALS patients showed that riluzole prolongs survival by several months
- ↑ Nagata, Kazuaki. Japan recognizes Cyberdyne’s robotic suit as medical device, widespread use anticipated (англ.), The Japan Times Online (26 ноября 2015). Дата обращения 10 февраля 2016.
- ↑ FDA Approves ALS Drug Radicava (edaravone) (неопр.). mailchi.mp. Дата обращения 9 августа 2017.
- ↑ Епископ РОСХВЕ просит главу Минздрава РФ изменить ситуацию с отношением к больным «непризнанным» недугом, NewsRu, 21 августа 2013
- ↑ Где взять право на надежду? // «Честное слово» № 3 (832), 23.01.2013
