Что такое натриевая соль — Здоровье феникса
Кто-нибудь задумывался о пользе и вреде соли, да и в целом, какие виды соли существуют, и функции которые они выполняют? В этой статье мы предлагаем подробно рассмотреть наиболее значимые разновидности соли и влияние каждого из них на наш организм.
Кроме как усилитель вкуса, в пищевой промышленности она также применяется для консервации и хранения рыбы и мяса.
В науке пищевых продуктов и питания — соленый — считается одним из пяти основных вкусов, распознаваемых рецепторами во рту. Остальные четыре: сладкий, горький, кислый и «безвкусный» (послевкусие глутаминовой кислоты).
Содержание статьи:
Натриевая соль (NaCl)
Натриевая соль (NaCl) — это обычная пищевая соль, которую мы используем в повседневной жизни. Хотя, в настоящее время, в приправу включают смесь различных видов.
Польза: обогащает организм натрием, участвует в регулировании количества жидкости.
Вред: чрезмерное употребление хлорида натрия приводит к повышенной жажде и, как следствие, удержанию воды в клетках. А это чревато отеками и увеличением артериального давления.
Доказано, что при интенсивных занятиях физическими упражнениями из тела через пот выводится на 50% больше соли. Новейшие исследования указывают на прямую связь соли с метаболическими реакциями.
Рекомендуемая дозировка:
- До 5 граммов в день. Токсичной для взрослых считается доза более 11 г в сутки.
Калиевая соль (KCl)
Встречающуюся в овощах, калиевую соль используют в сочетании с натриевой. Это делается для того, чтобы сбалансировать водный баланс.
Польза: Выполняет функцию обогащения калием, который, в свою очередь, балансирует количество натрия и кальция.
Смешение калиевой и натриевой солей в пище исключает возникновение приступов жажды, контролируя количество жидкости. Обладает мочегонным эффектом, т. е. приводит к потере воды и кальция с мочой.
Вред: передозировка кальцием, чтоможет привести к таким последствиям, как обезвоживание, мышечные спазмы и, даже, к инфаркту.
Рекомендуемая дозировка:
- Средняя в день: 0,2 г
- Максимум: 1 г
Йодированная соль (KI/NaI)
Йодированная соль полезна для профилактики йододефицитных заболеваний. Дефицит йода приводит к проблемам щитовидной железы и нарушению метаболизма.
Польза: восполняет недостаток в йоде, калие и натрие.
Дозировка:
- Дети: 15-35 мг
- Взрослые: 130 мг
Фторированная соль (KF/NaF)
Этот тип используется в Европе, где не фторируют питьевую воду. Часто фтор используется в составе зубной пасты. Таким образом, в большинстве стран с нефторированной питьевой водой, добавление фторида калия или фторида натрия в соль является частой практикой.
Пока не существует единой точки зрения по поводу пользы фторированной соли.
Более того, есть исследования, доказывающие ее однозначный вред.
В связи с этим, мы воздержимся от публикации точных данных.
Source: 3diet.ru
Читайте также
БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — это… Что такое БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ?
- БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ
- Бензилпенициллина натриевая соль
Действующее вещество
›› Бензилпенициллин* (Benzylpenicillin*)
* * *
БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ ( Веnzylpenicillinum-natrium ). Синоним: Веnzylpenicillinum Natricum. Белый мелкокристаллический порошок горького вкуса, слегка гигроскопичен. Легко разрушается при действии кислот, щелочей и окислителей, при нагревании в водных растворах, а также при действии пенициллиназы. Медленно разрушается при хранении в растворах при комнатной температуре. Очень легко растворим в воде, растворим в спирте. Теоретически активность натриевой соли бензилпенициллина равна 1670 ЕД в 1 мг, практически препарат выпускается активностью не менее 1600 ЕД в 1 мг. Бензилпенициллин активен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, возбудителя дифтерии, анаэробных спорообразующих палочек, палочки сибирской язвы), грамотрицательных кокков (гонококков, менингококков), а также в отношении спирохет, некоторых актиномицетов и других микроорганизмов. Препарат неэффективен в отношении большинства грамотрицательных бактерий, риккетсий, вирусов, простейших, грибов. К действию бензилпенициллина устойчивы штаммы стафилококков, образующие фермент пенициллиназу, разрушающий бензилпенициллин. Низкая активность бензилпенициллина в отношении бактерий кишечной группы, синегнойной палочки и других микроорганизмов также связана в определенной маре с выработкой ими пенициллиназы. Бензилпенициллин при внутримышечном введении быстро всасывается в кровь и обнаруживается в жидкостях и тканях организма; в спинномозговую жидкость проникает в незначительных количествах. Максимальная концентрация в крови наблюдается после внутримышечного введения через 30 — 60 мин. При подкожном введении скорость всасывания менее постоянна, обычно максимальная концентрация в крови отмечается через 6О мин. Через 3 — 4 ч после однократной внутримышечной или подкожной инъекции в крови обнаруживаются лишь следы антибиотика. Чтбы поддержать концентрацию на достаточно высоком для необходимого терапевтического эффекта уровне, надо производить инъекции через каждые 3 — 4 ч. При внутривенном введении, концентрация пенициллина в крови быстро снижается. При приеме внутрь препарат плохо всасывается и разрушаетая желудочным соком и пенициллиназой, продуцируемой микрофлорой кишечника. Выделяется в основном почками. Концентрация и продолжительность циркуляции бензилпенициллина в крови зависят от величины вводимой дозы. Антибиотик хорошо проникает в ткани и жидкости организма. В спинномозговой жидкости он обнаруживается в норме в незначительном количестве, однако при воспалении мозговых оболочек его концентрация повышается. Применяют бензилпенициллин при болезнях, вызванных чувствительными к нему микроорганизмами: крупозной и очаговой пневмониях, остром и подостром септическом эндокардитах, раневых инфекциях, гнойных инфекциях кожи, мягких тканей и слизистых оболочек, гнойном плеврите, перитоните, цистите, септицемии и пиемии, остром и хроническом остеомиелите, разных формах ангин, дифтерии, рожистом воспалении, гнойно-воспалительных заболеваниях в акушерско-гинекологической и оториноларингологической практике; при воспалительных заболеваниях глаза, менингите (При воспалении мозговых оболочек препарат проникает через гематоэнцефалический барьер, однако для получения терапевтического эффекта при внутримышечном применении его необходимо вводить в больших дозах. В особо тяжелых случаях внутримышечное введение комбинируют с эндолюмбальным.), скарлатине, гонорее, бленнорее, сифилисе, сибирской язве, актиномикозе и других инфекционных заболеваниях. При инфекциях, вызванных чувствительными к пенициллину микроорганизмами, бензилпенициллин является эффективным лекарственным средством. Бензилпенициллин и другие препараты этой группы эффективно действуют на все формы сифилиса. Они являются основными средствами лечения этого заболевания. Активные формы сифилиса лучше поддаются лечению пенициллинами. При инфекциях, вызванных микроорганизмами, не чувствительными к пенициллину (в том числе при гриппе без осложнений бактериальной инфекцией), применение бензилпенициллина нерационально и не вполне безопасно в связи с возможными побочными явлениями, вызываемыми антибиотиком. Бензилпенициллина натриевую соль вводят в виде растворов внутримышечно или подкожно, а при необходимости — в вену и в полости (брюшную, плевральную и др.). При заболеваниях легких применяют также в виде аэрозоля, при заболеваниях глаз — в виде глазных капель и субконъюнктивально. Из всех препаратов бензилпенициллина, только натриевую соль вводят эндолюмбально. Другие препараты пенициллина для этой цели не применяют. Наиболее распространен внутримышечный способ введения бензилпенициллина. Для внутримышечного введения препарат готовят ех tempore, добавляя к содержимому флакона 1 — 3 мл стерильной воды для иньекций, изотонического раствора натрия хлорида или 0,5 % раствора новокаина. Раствор в новокаине обеспечивает несколько более длительное пребывание препарата в организме (см. Бензилпенициллина новокаиновая соль). Готовят растворы, соблюдая правила асептики. Растворитель вводят стерильным шприцем непосредственно во флакон, прокалывая для этого резиновую пробку флакона, предварительно протертую спиртом. Растворы бензилпенициллина в растворе новокаина иногда становятся мутными вследствие образования новокаиновой соли бензилпенициллина. Это не является препятствием для внутримышечного введения. Вводят бензилпенициллин внутримышечно обычно глубоко в мышцы. Внутривенно (струйно или капельно) вводят бензилпенициллина натриевую соль при тяжелых заболеваниях (сепсис, менингит и др.). При внутримышечном и внутривенном введении бензилпенициллина натриевой соли разовые дозы при среднетяжелом течении инфекции (заболевания мочеи желчевыводящих путей, инфекция мягких тканей и др.) составляют обычно 250 000 — 500 000 ЕД; суточные 1 000 000 — 2 000 000 ЕД. При тяжелых инфекциях (сепсис, септический эндокардит, менингит и др.) вводят до 10 000 000 — 20 000 000 ЕД в сутки; при газовой гангрене — до 40 000 000 — 60 000 000 ЕД. Для внутривенного струйного введения разовую дозу бензилпенициллина натриевой соли (1 000 000 — 2 000 000 ЕД) растворяют в 5 — 10 мл стерильной воды для инъекций или изотонического раствора натрия хлорида и вводят медленно, в течение 3 — 5 мин. Для внутривенного капельного введения, разводят 2 000 000 — 5 000 000 ЕД в 100 — 200 мл изотонического раствора натрия хлорида или 5 — 10 % раствора глюкозы и вводят со скоростью 60 — 80 капель в минуту. При капельном ведении детям в качестве растворителя пользуются 5 — 10 % раствором глюкозы (30 — 100 мл в зависимости от дозы и возраста). Растворы используют сразу после приготовления, не допуская добавления к ним других лекарств. Детям бензилпенициллин назначают в разных суточных дозах: в возрасте до 1 года — по 50 000 — 100 000 ЕД на 1 кг массы тела, старше 1 года — по 50 000 ЕД/кг. При тяжелых инфекциях (менингит, сепсис, тяжелые формы острой пневмонии), суточную дозу можно увеличить до 200 000 — 300 000 ЕД/кг, а в исключительных случаях (по жизненным показаниям) — до 500 000 ЕД/кг. Суточную дозу распределяют на 4 — 6 введений. Внутривенно бензилпенициллина натриевую соль вводят 1 — 2 раза в сутки в сочетании с внутримышечными инъекциями. Лечение бензилпенициллином (и другими препаратами этой группы) больных сифилисом, а также гонореей производят по специально разработанным схемам. Эндолюмбально бензилпенициллина натриевую соль вводят при гнойных заболеваниях головного и спинного мозга и мозговых оболочек. В зависимости от характера болезни назначают взрослым 5000 — 10 000 ЕД, детям — от 2000 до 5000 ЕД. Разводят препарат в стерильной воде для инъекций или в изотоническом растворе натрия хлорида из расчета 1000 ЕД на 1 мл. Перед инъекцией (в зависимости от уровня внутричерепного давления) удаляют из спинномозгового канала 5 — 10 мл спинномозговой жидкости и добавляют ее к раствору антибиотика в равном соотношении. Вводят медленно (1 мл в минуту), обычно раз в сутки в течение 2 — 3 дней, затем переходят к внутримышечным инъекциям. Подкожно применяют бензилпенициллина натриевую соль для обкалывания инфильтратов (100 000 — 200 000 ЕД в 1 мл 0,25 — 0,5 % раствора новокаина). В полости (брюшную, плевральную и др.) вводят раствор бензилпенициллина натриевой соли в концентрации 10 000 — 20 000 ЕД в 1 мл для взрослых и 2000 — 5000 ЕД в 1 мл для детей. Растворяют в стерильной воде для инъекций или изотоническом растворе натрия хлорида. Продолжительность введения 5 — 7 дней, затем переходят на внутримышечное введение. При заболеваниях легких (хронические бронхиты, пневмонии, гангрена легких и др.) часто применяют аэрозоль пенициллина: разовая доза для взрослых 100 000 — 300 000 ЕД. Разводят в 3 — 5 мл дистиллированной воды; применяют 1 — 2 раза в сутки; продолжительность ингаляции 10 — 30 мин. При нагноительных процессах в легких вводят также раствор препарата интратрахеально (после тщательной анестезии зева, гортани и трахеи). Применяют обычно 100 000 ЕД в 10 мл изотонического раствора натрия хлорида. При заболеваниях глаз (острый конъюнктивит, язва роговицы, гонобленнорея и др.) иногда назначают глазные капли, содержащие 20 000 — 100 000 ЕД натриевой соли бензилпенициллина в 1 мл изотонического раствора натрия хлорида или дистиллированной воды. Вводят по 1 — 2 капли 6 — 8 раз в день. Для ушных капель или капель в нос применяют растворы, содержащие 10 000 — 100 000 ЕД в 1 мл. Лечение бензилпенициллином в зависимости от формы и тяжести болезни может продолжаться от 7 — 10 дней до 2 мес и больше (при сепсисе, септическом эндокардите и т. п.). Если через 3 — 5 дней после начала лечения эффекта не отмечается, следует перейти к применению других антибиотиков либо вводить бензилпенициллин вместе с другими антибиотиками или синтетическими химиотерапевтическими препаратами. Комбинированная терапия может усиливать эффективность препаратов и предупреждать развитие устойчивых форм бактерий; следует, однако, учитывать возможность усиления побочных эффектов. Применять бензилпенициллин и содержащие его препараты необходимо только по назначению и под наблюдением врача. Пенициллин назначают лишь в тех случаях, если заболевание вызвано чувствительными к этому антибиотику микроорганизмами. Следует иметь в виду возможность развития резистентности ряда возбудителей (особенно пенициллиназообразующих стафилококков) к бензилпенициллину. Необходимо учитывать, что применение недостаточных доз бензилпенициллина (как и других антибиотиков) или слишком раннее прекращение лечения часто приводит к появлению резистентных штаммов возбудителей. При обнаружении резистентности возбудителей к бензилпенициллину следует заменить его другим антибиотиком. Бензилпенициллина натриевая соль и другие препараты пенициллина могут вызывать различные побочные явления. У некоторых больных, особенно с повышенной чувствительностью, наблюдаются головная боль, повышение температуры тела, крапивница, сыпь на коже и слизистых оболочках, боли в суставах, эозинофилия, ангионевротический отек и другие аллергические реакции; описаны случаи анафилактического шока со смертельным исходом. При ингаляциях пенициллина могут развиться фарингиты и ларингиты аллергического характера, приступы бронхиальной астмы. В случае выраженных аллергических реакций назначают адреналин, глюкокортикоиды, противогистаминные препараты (димедрол или другие), кальция хлорид. Применяют также ферментный препарат пенициллиназу (см.). При тяжелых аллергических реакциях назначают преднизолон или другие глюкокортикостероиды. При первых признаках анафилактического шока должны быть приняты меры для выведения больного из этого состояния (введение адреналина, димедрола, кальция хлорида, применение сердечных средств, вдыхание кислорода, согревание и др.; сразу после выведения больного из состояния асфиксии и шока вводят 1 000 000 ЕД пенициллиназы). Применение очень больших доз бензилпенициллина и особенно при эндолюмбальном введении може
Словарь медицинских препаратов. 2005.
- Benzylpenicillinum-kalium
- Benzylpenicillinum-natrium
Смотреть что такое «БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ» в других словарях:
Соль — получить на Академике актуальный промокод на скидку GRACY или выгодно соль купить с дисконтом на распродаже в GRACY
Бензилпенициллина натриевая соль кристаллическая — Действующее вещество ›› Бензилпенициллин* (Benzylpenicillin*) Латинское название Benzylpenicillinum Natrium crystallisatum АТХ: ›› J01CE01 Бензилпенициллин Фармакологическая группа: Пенициллины Состав и форма выпуска 1 флакон с порошком для… … Словарь медицинских препаратов
БЕНЗИЛПЕНИЦИЛЛИНА НОВОКАИНОВАЯ СОЛЬ — Действующее вещество ›› Бензилпенициллин* (Benzylpenicillin*) Латинское название Benzylpenicillinum Novocainum АТХ: ›› J01CE09 Пенициллин прокаин Фармакологическая группа: Пенициллины Состав и форма выпуска Бензилпенициллина натриевая соль… … Словарь медицинских препаратов
БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ — (КАЛИЕВАЯ) СОЛЬ. Benzylpenicillinum natrium (kalium). Синонимы: амфоциллин, буциллин, делациллин, топоциллин. Относятся к группе пенициллинов, получаемых при биосинтезе Penicillinum chrysogenum. Свойства. Белые кристаллические порошки, хорошо… … Отечественные ветеринарные препараты
ОКСАЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Действующее вещество ›› Оксациллин* (Oxacillin*) Латинское название Oxacillinum natrium АТХ: ›› J01CF04 Оксациллин Фармакологическая группа: Пенициллины Нозологическая классификация (МКБ 10) ›› A41 Другая септицемия ›› J18 Пневмония без уточнения … Словарь медицинских препаратов
МЕТИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Methicillinum natrium. Синонимы: лукопенин, сантициллин. Метициллин является представителем полусинтетических пенициллинов. Свойства. Белый кристаллический порошок, хорошо растворимый в воде. Под действием кислот, щелочей и окислителей разрушает … Отечественные ветеринарные препараты
Пенициллин G натриевая соль — Действующее вещество ›› Бензилпенициллин* (Benzylpenicillin*) Латинское название Penicillin G sodium АТХ: ›› J01CE01 Бензилпенициллин Фармакологическая группа: Пенициллины Нозологическая классификация (МКБ 10) ›› A22 Сибирская язва ›› A36… … Словарь медицинских препаратов
ПЕНВЕТИНА НАТРИЕВАЯ — (КАЛИЕВАЯ) СОЛЬ. Penvetinum natrium (kalium). Свойства. Белый или слегка желтоватый мелкокристаллический порошок горького вкуса. Гигроскопичен. Легко разрушается при действии кислот, щелочей, окислителей и при нагревании в водных растворах. Форма … Отечественные ветеринарные препараты
Benzylpenicillinum-natrium — БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ ( Веnzylpenicillinum natrium ). Синоним: Веnzylpenicillinum Natricum. Белый мелкокристаллический порошок горького вкуса, слегка гигроскопичен. Легко разрушается при действии кислот, щелочей и окислителей, при… … Словарь медицинских препаратов
ЛИСТЕРИОЗ — мед. Листериоз полиморфное инфекционное заболевание, протекающее с поражением нервных тканей или в виде ангинозно септической формы. Наиболее часто встречается во внутриутробном периоде (диссеминированный инфантильный листериоз), у новорождённых… … Справочник по болезням
ИНФЕКЦИЯ ГОНОКОККОВАЯ — мед. Гонорея инфекционное заболевание, вызываемое гонококками рода нейссерий и передаваемое половым путём. Частота. Заболеваемость в России составила в 1996 г. 139,0 на 100 000 населения. Преобладающий возраст 15 35 лет. Этиология Возбудители… … Справочник по болезням
Хлорид натрия — это… Что такое Хлорид натрия?
| Хлорид натрия | |
 | |
 | |
| Общие | |
|---|---|
| Традиционные названия | обычная соль, поваренная соль, столовая соль, пищевая соль, каменная соль, галит[1] |
| Химическая формула | NaCl |
| Физические свойства | |
| Молярная масса | 58,44277 г/моль |
| Плотность | 2,165 г/см³ |
| Термические свойства | |
| Температура плавления | 800,8 °C |
| Температура кипения | 1465 °C |
| Молярная теплоёмкость (ст. усл.) | 50,8 Дж/(моль·К) |
| Удельная теплота испарения | 170,85 кДж/моль Дж/кг |
| Удельная теплота плавления | 28,68 кДж/моль Дж/кг |
| Химические свойства | |
| pKa | 6,7–7,3 |
| Растворимость в воде | 35,6 (0 °C) 35,9 (25 °C) 39,1 (100 °C) г/100 мл |
| Растворимость в метаноле | 14,9 г/100 мл |
| Растворимость в аммиаке | 21,5 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,5442 (589 нм) |
| Структура | |
| Координационная геометрия | Октаэдральная (Na +) Октаэдральная (Cl -) |
| Кристаллическая структура | гранецентрированная кубическая, cF8 |
| Классификация | |
| Рег. номер CAS | [7647-14-5] |
| Рег. номер PubChem | 5234 |
| Рег. номер EINECS | 231-598-3 |
| SMILES | [Na+].[Cl-] |
| RTECS | VZ4725000 |
| Безопасность | |
| ЛД50 | 3000–8000 мг/кг |
| NFPA 704 |  |
Хлори́д на́трия — химическое соединение NaCl, натриевая соль соляной кислоты, хлористый натрий.
Хлорид натрия известен в быту под названием поваренной соли, основным компонентом которой он является. Хлорид натрия в значительном количестве содержится в морской воде, создавая её солёный вкус. Встречается в природе в виде минерала галита (каменная соль).
Чистый хлорид натрия имеет вид бесцветных кристаллов, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита, который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов, соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 10 15 тонн NaCl, то есть из каждой тысячи тонн морской воды можно получить в среднем 1,3 тонны хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, состоят из NaCl. Также он найден в кристаллах снега[2].
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах теплых морей или на соляных озёрах, где на мелководье соленая вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора, «соль была рождена благородными родителями: солнцем и морем»[3].
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решетку и содержит 39,34 % Na, 60,66 % Cl. Другими химическими элементами, входящими в состав примесей, являются: Br, N, H, Mn, Cu, Ga, As, I, Ag, Ba, Tl, Pb, K, Ca, S, O. Плотность 2,1—2, 2 г / см ³, а твёрдость по шкале Мооса — 2. Бесцветный, прозрачный минерал, со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и т. п.[4]
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (желтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, йодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и т. д.[4]
По условиям формирования месторождений каменную соль подразделяют на следующие виды[4]:
- рассолы современных соляных бассейнов
- соляные подземные воды
- залежи минеральных солей современных соляных бассейнов
- ископаемые залежи (важнейшие для промышленности).
Морская соль
Морская соль является смесью солей (хлориды, карбонаты, сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:
| Соединение | Масс. доля, % |
|---|---|
| NaCl | 77,8 |
| MgCl2 | 10,9 |
| MgSO4 | 4,7 |
| KCl | 2,5 |
| K2SO4 | 2,5 |
| CaCO3 | 0,3 |
| Ca(HCO3)2 | 0,3 |
| другие соли | 0,2 |
 Очищенная кристаллическая морская соль
Очищенная кристаллическая морская сольПри испарении морской воды при температуре 20 — 35 ° C в осадке сначала кристаллизуются наименее растворимые соли — карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них — сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу — горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз. Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль с Мёртвого моря. В очищенном виде этот вид соли также предлагается в продуктовой торговой сети — как натуральная и богатая йодом пищевая[5].
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских, девонских, пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах[4]. Среди озёрных месторождений России крупнейшие — Эльтонское, Баскунчак в Прикаспии, Кучукское озеро, о. Кулундинское, Эбейты и др. озера в Зап. Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими — 60—90 м. Извлечённую соль выливали в особый резервуар — творило, откуда она через отверстия стекала в нижний резервуар, и системой желобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка. В 1137 новгородский князь Святослав определил налог на соляные варницы[6]:
 | …на мори от чрена и от салгы по пузу… |  |
[7]
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли. Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.
Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн)[8].
-

Добыча соли в южной части Мертвого моря, Израиль
-

Кристаллы каменной соли
-

Плантация морской соли в Дакаре
-

Соляные кучи на солончаке Уюни, Боливия
Применение
В пищевой промышленности и кулинарии
Соль повареннаяВ пищевой промышленности и кулинарии используют хлорид натрия, чистота которого должна быть не менее 97 %. Его применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия имеет товарное название поваренная соль, порой также употребляются названия пищевая, столовая, а также уточнение названия в зависимости от её происхождения — каменная, морская, и по составу добавок — йодированная, фторированная и т. д. Такая соль является кристаллическим сыпучим продуктом с солёным вкусом без привкуса, без запаха (за исключением йодированной соли), в котором не допускаются посторонние примеси, не связанные с методом добывании соли. Кроме хлорида натрия, поваренная соль содержит небольшое количество солей кальция, магния, калия, которые придают ей гигроскопичности и жёсткости. Чем меньше этих примесей в соли, тем выше её качество.
Выделяют сорта: экстра, высший, первый и второй. Массовая доля хлористого натрия в сортах,%:
- экстра — не менее 99,5;
- высший — 98,2;
- первый — 97,5;
- второй — 97,0.
Массовая доля влаги в выварочной соли сорта «экстра» 0,1 %, в высшем сорте — 0,7 %. Допускают добавки йодида калия (йодистого калия), йодата калия, фторидов калия и натрия. Массовая доля йода должна составлять (40,0 ± 15,0) × 10 −4 %, фтора (25,0 ± 5,0) × 10 −3 %. Цвет экстра и высшего сортов — белый, однако для первого и второго допускается серый, желтоватый, розовый и голубоватый оттенки в зависимости от происхождения соли. Пищевую поваренную соль производят молотой и сеяной. По размеру зёрен молотую соль подразделяют на номера: 0, 1, 2, 3. Чем больше номер, тем больше зерна соли.
В кулинарии хлорид натрия потребляют как важнейшую приправу. Соль имеет характерный вкус, без которого пища кажется человеку пресной. Такая особенность соли обусловлена физиологией человека. Однако зачастую люди потребляют соли больше, чем нужно для физиологических процессов.
Хлорид натрия имеет слабые антисептические свойства — 10-15 % содержание соли предотвращает размножение гнилостных бактерий. Этот факт обусловливает её широкое применение как консерванта.
В медицине
Изотонический раствор хлорида натрия в воде (0,9 %) применяется как дезинтоксикационное средство, для коррекции состояния систем организма в случае обезвоживания, как растворитель других лекарственных препаратов. Гипертонические растворы (10 % р-р) используют как вспомогательный осмотический диуретик при лёгочных, желудочных и кишечных кровотечениях для обеспечения форсированного диуреза, в состояниях, характеризующихся дефицитом ионов натрия и хлора, при отравлении нитратом серебра, для обработки гнойных ран (местно). В офтальмологии как местное средство раствор хлорида натрия обладает противоотёчным действием[9].
В коммунальном хозяйстве. Техническая соль
Зимой хлорид натрия, смешанный с другими солями, песком или глиной — так называемая техническая соль — применяется как антифриз против гололеда. Ею посыпают тротуары, хотя это отрицательно влияет на кожаную обувь и техническое состояние автотранспорта в виду коррозийных процессов.
Регенерация Nа-катионитовых фильтров
Nа-катионитовые фильтры широко применяются в котельных установках всех мощностей для смягчения воды при водоподготовке. Катионитовым материалом на современных водоподготовительных установках служат в основном глауконит, сульфанованные угли и синтетические смолы. Наиболее распространены сульфоугли.
Регенерацию Nа-катионитовых фильтров осуществляют 6—8%-м раствором поваренной соли, в результате действие сульфоуголя восстанавливается. Реакции идут по уравнениям:
- CaR2 + 2NаСl = 2NаR + CaСl2.
- МgR2 + 2NаСl = 2NаR + МgСl2.
Химическая промышленность
Соль, наряду с каменным углем, известняками и серой, образует «большую четвёрку» продуктов минерального сырья, которые являются важнейшими для химической промышленности[10]. Из неё получают соду, хлор, соляную кислоту, гидроксид натрия, сульфат натрия и металлический натрий. Кроме этого соль используется также для промышленного получения легкорастворимого в воде хлората натрия, который является средством для уничтожения сорняков[11]. Суммарное уравнение реакции электролиза горячего раствора хлорида натрия[12]:
- NaCl + 3 H2O → NaClO3 + 3 H2↑
Получение хлора и гидроксида натрия
В промышленности путём электролиза раствора хлорида натрия получают хлор. Процессы, происходящие на электродах[13][14]:
- на катоде как побочный продукт выделяется водород вследствие восстановления ионов H +, образованных в результате электролитической диссоциации воды:
- H2O ⇆ H+ + OH−
- 2 H+ + 2 e− → H2↑
- поскольку (вследствие практически полной электролитической диссоциации NaCl), хлор в растворе находится в виде хлорид-ионов, они окисляются на аноде до свободного хлора в виде газа:
- NaCl → Na+ + Cl−
- 2 Cl− − 2 e− → Cl2↑
- суммарная реакция:
- 2 NaCl + 2 H2O → 2 NaOH + Cl2↑ + H2↑
Как видно из уравнения суммарной реакции, ещё одним продуктом является гидроксид натрия. Расход электроэнергии на 1 т хлора составляет примерно 2700 кВт × час. Полученный хлор сжижается на жёлтую жидкость уже при обычной температуре[15].
Если между анодом и катодом нет диафрагмы, то растворенный в воде хлор начинает реагировать с гидроксидом натрия, образуя хлорид и гипохлорит натрия NaClO[14]:
- 2 NaOH + Cl2 → NaCl + NaClO + H2O
Поэтому для получения гидроксида натрия применяют диафрагму и соответствующий метод получения NaOH называют диафрагменным. В качестве диафрагмы применяют асбестовый картон. В процессе электролиза раствор хлорида натрия постоянно подается в анодное пространство, а из катодного пространства непрерывно вытекает раствор хлорида и гидроксида натрия. Во время выпаривания последнего хлорид кристаллизуется, поскольку его растворимость в 50 % растворе NaOH ничтожно мала (0,9 %). Полученный раствор NaOH выпаривают в железных чанах, затем сухой остаток переплавляют.
Для получения чистого гидроксида натрия (без добавок хлорида натрия) применяют ртутный метод, где используют графитовый анод и ртутный катод. Вследствие того, что перенапряжение выделения водорода на ртути очень большое, на ней вновь появляются ионы натрия и образуется амальгама натрия[14][16]:
- Na+ + e− → Na(Hg)
Амальгаму позже разлагают горячей водой с образованием гидроксида натрия и водорода, а ртуть перекачивают насосом обратно в электролизер:
- 2 Na(Hg) + 2 H2O → 2 NaOH + H2↑
Суммарная реакция процесса такая же, как и в случае диафрагменного метода.
Получение металлического натрия
Металлический натрий получают электролизом расплава хлорида натрия. Происходят следующие процессы:
- на катоде выделяется натрий:
- 2 Na+ + 2 e− → 2 Na
- на аноде выделяется хлор (как побочный продукт):
- 2 Cl− − 2 e− → Cl2
- суммарная реакция:
- 2 Na+ + 2 Cl− → 2 Na + Cl2
Ванна электролизера состоит из стального кожуха с футеровкой, графитового анода и кольцевого железного катода. Между катодом и анодом располагается сетчатая диафрагма. Для снижения температуры плавления NaCl (800 ° C), электролитом является не чистый хлорид натрия, а его смесь с хлоридом кальция CaCl 2 (40:60) с температурой плавления 580 ° C. Металлический натрий, который собирается в верхней части катодного пространства, содержит до 5 % примесь кальция, но последний со временем почти полностью отделяется, поскольку его растворимость в жидком натрии при температуре его плавления (371 ° C) составляет всего 0,01 %. С расходованием NaCl его постоянно добавляют в ванну. Затраты электроэнергии составляют примерно 15 кВт × ч на 1 кг натрия[17].
Получение соляной кислоты и сульфата натрия
Среди многих промышленных методов получения соляной кислоты, то есть водного раствора хлороводорода (HCl), применяется реакция обмена между хлоридом натрия и серной кислотой:
- NaCl + H2SO4 → NaHSO4 + HCl↑
- NaCl + NaHSO4 → Na2SO4 + HCl↑
Первая реакция происходит в значительной степени уже при обычных условиях, а при слабом нагреве идет почти до конца. Вторая происходит лишь при высоких температурах. Процесс осуществляется в специальных механизированных печах большой мощности. Хлороводород, который выделяется, обеспыливают, охлаждают и поглощают водой с образованием соляной кислоты. Как побочный продукт образуется сульфат натрия Na2SO4[18][19].
Этот метод применяется также для получения хлороводорода в лабораторных условиях.
Физические и физико-химические свойства
Температура плавления 800,8 С, кипения 1465 С.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в г на 100 г воды) равен 35,9 при 21 °C и 38,1 при 80 °C. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена. В чистом виде хлорид натрия не гигроскопичен. Однако соль часто бывает загрязнена примесями (преимущественно ионами Ca 2 +, Mg 2 + и SO2−4), и такая соль на воздухе сыреет[20]. Кристаллогидрат NaCl · 2H 2 O можно выделить при температуре ниже +0,15 ° C[21].
Смесь измельченного льда с мелким порошком хлорида натрия является эффективным охладителем. Так, смесь состава 30 г NaCl на 100 г льда охлаждается до температуры −20 ° C. Это происходит потому, что водный раствор соли замерзает при температуре ниже 0 ° C. Лед, имеющий температуру около 0 ° C, плавится в таком растворе, поглощая тепло окружающей среды.
| Термодинамические характеристики | |
|---|---|
| ΔfH0g | −181,42 кДж/моль |
| ΔfH0l | −385,92 кДж/моль |
| ΔfH0s | −411,12 кДж/моль |
| ΔfH0aq | −407 кДж/моль |
| S0g, 1 bar | 229,79 Дж/(моль·K) |
| S0l, 1 bar | 95,06 Дж/(моль·K) |
| S0s | 72,11 Дж/(моль·K) |
Диэлектрическая проницаемость NaCl — 6,3
Плотность и концентрация водных растворов NaCl
| Концентрация, % | Концентрация, г/л | Плотность, г/мл |
|---|---|---|
| 1 | 10,05 | 1,005 |
| 2 | 20,25 | 1,012 |
| 4 | 41,07 | 1,027 |
| 6 | 62,47 | 1,041 |
| 8 | 84,47 | 1,056 |
| 10 | 107,1 | 1,071 |
| 12 | 130,2 | 1,086 |
| 14 | 154,1 | 1,101 |
| 16 | 178,5 | 1,116 |
| 18 | 203,7 | 1,132 |
| 20 | 229,5 | 1,148 |
| 22 | 256 | 1,164 |
| 24 | 283,2 | 1,18 |
| 26 | 311,2 | 1,197 |
Лабораторное получение и химические свойства
При действии серной кислоты выделяет хлороводород. С раствором нитрата серебра образует белый осадок хлорида серебра.
Учитывая огромные природные запасы хлорида натрия, необходимости в его промышленном или лабораторном синтезе нет. Однако, его можно получить различными химическими методами как основной или побочный продукт.
- получение из простых веществ натрия и хлора является экзотермической реакцией[22]:
- Na(тв) + 1/2Cl2(г) → NaCl(тв) + 410 кДж
- нейтрализация щелочи гидроксида натрия соляной кислотой[23]:
- NaОН + НCl → NaCl + Н2О
Поскольку хлорид натрия в водном растворе почти полностью диссоциирован на ионы: NaCl → Na+ + Cl−, его химические свойства в водном растворе определяются соответствующими химическими свойствами катионов натрия и хлорид-анионов.
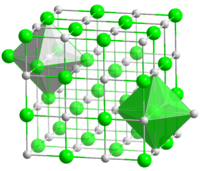
Структура
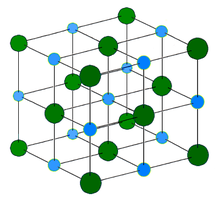 Кристаллическая решётка хлорида натрия.
Кристаллическая решётка хлорида натрия.Голубой цвет = Na+
Зелёный цвет = Cl−
Хлорид натрия образует бесцветные кристаллы кубической сингонии, пространственная группа F m3m, a = 0,563874 нм, d = 2,17 г/см³. Каждый из ионов Cl− окружен шестью ионами Na+ в октаедральний конфигурации, и наоборот. Если мысленно отбросить, например, ионы Na+, то останется плотно упакованная кубическая структура с ионов Cl−, называемая гранецентрированной кубической решеткой. Ионы Na+ тоже образуют плотно упакованную кубическую решетку. Таким образом, кристалл состоит из двух подрешеток, сдвинутых друг относительно друга на полупериод. Такая же решетка характерна для многих других минералов.
В кристаллической решетке между атомами преобладает ионная химическая связь, что является следствием действия электростатического взаимодействия противоположных по заряду ионов
См. также
Примечания
- ↑ Натрия хлорид на сайте Национального института стандартов и технологии (англ. National Institute of Standards and Technology) (англ.)
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 218
- ↑ Пифагор. Золотой канон. Фигуры эзотерики. — М.: Изд-во Эксмо, 2003. — 448 с. (Антология мудрости).
- ↑ 1 2 3 4 Малая горная энциклопедия. В 3-х т. / Под ред. В. С. Белецкого . — Донецк: «Донбасс», 2004. — ISBN 966-7804-14-3
- ↑ УНИАН: Морская соль для красоты и здоровья кожи
- ↑ Российское законодательство Х-ХХ веков. Законодательство Древней Руси. т. 1. М, 1984. С. 224—225. (рус.)
- ↑ В переводе с поморской «говори» слово чрен (црен) означает четырёхугольный ящик, кованный из листового железа, а салга — котёл, в котором варили соль. Пузом в беломорских солеварнях называли мешок соли в два четверика, то есть, объёмом около 52 литров.
- ↑ Соль (PDF), Геологический обзор США на сайте Программы минеральных ресурсов (англ.)
- ↑ Энциклопедия здоровья
- ↑ Онлайн Энциклопедия кругосвет. Натрий
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 261
- ↑ Синтез хлората натрия (англ.)
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 249
- ↑ 1 2 3 М. Л. Глинка Общая химия (Учебник), изд. 2-е изд., Перераб. и доп .. — С. 608, Киев: «Высшая школа», 1982.
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 254
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 231
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 219
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 250
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 257—258
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 215—216
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 234
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 255
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 191
Ссылки
Шаблон:АТХ код A07
Плазмозамещающие и перфузионные растворы — АТХ код: B05
| B05A |
| ||
|---|---|---|---|
| B05B |
| ||
| B05C |
| ||
| B05D |
| ||
| B05X |
| ||
| B05Z |
Натриевая соль — это… Что такое Натриевая соль?
- Натриевая соль
- adj
chem. Natriumsalz
Универсальный русско-немецкий словарь. Академик.ру. 2011.
- Наталь
- Натуропатия
Смотреть что такое «Натриевая соль» в других словарях:
Соль — получить на Академике рабочий купон на скидку Галерея Косметики или выгодно соль купить с бесплатной доставкой на распродаже в Галерея Косметики
Натриевая соль пропилового эфира пара-оксибензойной кислоты — Химичес … Википедия
натриевая соль гуминовых кислот — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN CC 16Ligcon … Справочник технического переводчика
НАТРИЕВАЯ СОЛЬ ЗООКУМАРИНА — Свойства. Тонкоизмельченный порошок желтого цвета. Растворима в воде. Хранят под замком, в хорошо закупоренных банках, в сухом, прохладном месте. Действие и применение. Действует, подобно зоокумарину, но более ядовит для мышевидных грызунов. Отн … Отечественные ветеринарные препараты
натриевая соль хлорамида n-толуолсульфокислоты — хлорамин T … Cловарь химических синонимов I
БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Действующее вещество ›› Бензилпенициллин* (Benzylpenicillin*) * * * БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ ( Веnzylpenicillinum natrium ). Синоним: Веnzylpenicillinum Natricum. Белый мелкокристаллический порошок горького вкуса, слегка гигроскопичен.… … Словарь медицинских препаратов
ДИКЛОКСАЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Dicloxacillinum natrium. Синонимы: бриспен, клоцил, констафил, диклекс, дикллоцил, диклоксапен, динапен, ноксабен, патоцил, стампен, верациллин и др. Свойства. По внешним признакам это белый кристаллический порошок горького вкуса со специфически … Отечественные ветеринарные препараты
АМПИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Действующее вещество ›› Ампициллин* (Ampicillin*) Латинское название Ampicillinum natrium АТХ: ›› J01CA01 Ампициллин Фармакологическая группа: Пенициллины Нозологическая классификация (МКБ 10) ›› A09 Диарея и гастроэнтерит предположительно… … Словарь медицинских препаратов
ОКСАЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Действующее вещество ›› Оксациллин* (Oxacillin*) Латинское название Oxacillinum natrium АТХ: ›› J01CF04 Оксациллин Фармакологическая группа: Пенициллины Нозологическая классификация (МКБ 10) ›› A41 Другая септицемия ›› J18 Пневмония без уточнения … Словарь медицинских препаратов
ЦЕФАЛОТИНА НАТРИЕВАЯ СОЛЬ — ( Сеphalotinum nаtrium ). 7 (2 Тиенилацетамидо)цефалоспориновой кислоты натриевая соль. Белый или почти белый кристаллический порошок. Легко растворим в воде. Синонимы: Кефлин, Аveran, Сеfalotin, Celorex, Сероracin, Кеflin, Losроven, Rimigal,… … Словарь медицинских препаратов
Мефенамина натриевая соль — Кислота мефенамовая (Acidum mephenamicum) N (2,3 Диметилфенил) антраниловая кислота. Применяется в медицине, как лекарственное средство нестероидный противовоспалительный препарат (НПВС). Аналогично используется и её натриевая соль. Содержание 1… … Википедия
АМПИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ — Ampicillinum natrium. Свойства. Ампициллина натриевая соль полусинтетический антибиотик группы пенициллинов. Порошок или пористая масса белого цвета с кремовым оттенком, хорошо растворяется в воде. Форма выпуска. Для перорального применения выпу … Отечественные ветеринарные препараты
Предложения со словосочетанием НАТРИЕВАЯ СОЛЬ
Солонцеватые почвы характеризуются избыточным содержанием натриевых солей. Натриевая соль борной кислоты, или бура. Кемпферол оказывает тонизирующее, капилляроукрепляющее, мочегонное, противовоспалительное действие, выводит натриевые соли. Компонент кемпферол, входящий в состав золотого уса, обладает тонизирующим, диуретическим, противовоспалительными свойствами, укрепляет капилляры и выводит натриевые соли. Таким способом можно нейтрализовать натриевые соли.
 Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: превосходительство — это что-то нейтральное, положительное или отрицательное?
Положительное
Отрицательное
Натриевая соль — это анестезирующее и противовоспалительное средство, способствующее заживлению повреждённой слизистой оболочки, к тому же оно обладает противотрихомонадной активностью. Они вносятся в двенадцатиперстную кишку вместе с желчью в виде натриевых солей. Применяют для лечения артритов, бронхиальной астмы, при воспалительных заболеваниях желудочно-кишечного тракта, очищения организма от натриевых солей по 15 капель, разбавленных 0, 5 стакана воды. Натриевая соль борной кислоты, естественный минерал, легко растворимый в воде. Вместо гипса допустимо использовать известь, глиногипс, хлористый кальций, но эти вещества менее эффективны в борьбе с натриевыми солями. Кемпферол обладает тонизирующим, капилляроукрепляющим, диуретическим, противовоспалительным действиями, выводит натриевые соли. Однако, из-за переизбытка натриевых солей в составе система неустойчива, что приводит к расслоению антифриза при хранении и перепадах температур. Одним из эффективных средств для удаления кутикулы является пилинг, содержащий глицерин, масло сладкого миндаля, аллантоин, натриевую соль гиалуроновой кислоты, кварц, фруктовые кислоты. Вещества группы флавонолов отличаются ещё и тем, что стимулируют работу выделительной системы, а также способствуют очищению организма от натриевых солей. Твёрдые мыла представляют собой преимущественно натриевые соли жирных кислот, расщеплённых подсолнечного, соевого, конопляного и других растительных масел. Натриевые соли легко растворимы в воде. У кемпферола есть замечательное свойство — он выводит натриевые соли. В конце концов, глутамат натрия — мононатриевая соль глутаминовой кислоты — состоит из натриевой соли, обладающей солёным вкусом, и глутамата, который является носителем чистого вкуса умами. Кемпферол обладает тонизирующим, капилляроукрепляющим, диуретическим, противовоспалительным действием, выводит натриевые соли. Синонимы. Ампициллина натриевая соль, Ампициллина тригидрат, Кампициллин, Пенбритин, Пентрексил, Росциллин. Яблочная кислота, например, входит в состав некоторых слабительных средств, различные соли винной кислоты (тартраты) используют для создания эффективных алкалоидных препаратов; натриевая соль лимонной кислоты широко используется при консервировании крови. Самый распространённый рассол состоит из стабилизаторов Е450 и Е451 (фосфаты, не опасные для организма), желирующих агентов Е407 (каррагинан, вытяжка из водорослей), декстрозы, усилителей вкуса и аромата Е621 (глутамат натрия), антиокислителей Е301 (натриевая соль аскорбиновой кислоты), загустителя Е415 (природный полисахарид). Один из заменителей сахара, кристаллогидрат натриевой соли. Обычная натриевая соль известна в быту в качестве поваренной соли. Известно, что при испарении влаги из сложного солевого раствора первоначально в кристаллическое состояние переходят натриевая соль (NaCl) как труднорастворимая, затем соль калийная (KCI) и в последнюю очередь легкорастворимый хлорид магния (MgCl). Помимо натриевой соли (в виде минерала галита) они содержат калийную соль (в виде минерала сильвина), а также большинство жизненно необходимых микроэлементов в виде микропримесей. На самом деле глутамат натрия — натриевая соль глутаминовой кислоты, одной из важнейших аминокислот, входящей в состав практически любого белка (а белки есть в любых клетках). Смертельные отравления этими препаратами чаще наблюдаются у детей первых лет жизни, а наиболее токсичной считается натриевая соль железа. Компенсированный ацидоз отличается изменением абсолютных количеств составляющих карбонатного буфера, отношение же натриевой соли угольной кислоты к угольной кислоте остаётся в пределах нормы, и pH крови существенно не меняется. Кемпферол обладает капилляроукрепляющим, диуретическим, тонизирующим действием, он также способствует выводу из организма натриевых солей. При приёме бензилпенициллина (пенициллин G натриевая соль, прокаин-бензилпенициллин) возможны появление сыпи на слизистых оболочках, повышение рефлекторной возбудимости, симптомы менингизма, судороги, кома. Если снижено содержание калия при повышенном количестве натриевых солей, провоцирующих отёчность, в рацион включают продукты, содержащие калий в большом количестве. Для местного применения по широким показаниям промышленность традиционно выпускает большое число растворимых натриевых солей разных сульфаниламидов (больше, чем приведено в классификации): стрептоцида, норсульфазола, этазола, сульфапиридазина и др. Нужно выявить связь усиления болей с периодом приёма натриевой соли или калиевых продуктов. Тогда цикл чередования будет следующим: 4 — 5 дней приём натриевой соли, а затем 1 — 3 дня калийсодержащая пища и жидкости. Таблетки активированного угля «KM» (Tablettae Carbonis activati «KM») содержат 0, 2 г активированного угля, 0, 0455 г белой глины и 0, 0045 г натриевой соли карбоксиметилцеллю-лозы, выпускаются в упаковке по 10 шт. Они обладают большей адсорбирующей активностью, чем карболен, поскольку натриевая соль карбоксиметилцеллюлозы увеличивает поглощающую способность угля в 2 раза, а белая глина способствует лучшей распадаемости таблеток при поступлении их в желудок. Состоят из кристаллов мочевой кислоты и её натриевой соли; имеют гладкую поверхность, твёрдую консистенцию, зернистую структуру. Бактокумарин — препарат, содержащий бактерии тифа грызунов и натриевую соль зоокумарина, внешне напоминает влажное зерно. При более тяжёлых состояниях или у детей младшего возраста используют бензилпенициллина натриевую соль для внутримышечного введения. Натриевая соль фузидовой кислоты применяется в лечении эритразмы, карбункулов, фурункулов, гидраденита, фолликулита. Выпускается в виде натриевой соли для медицинского применения.Неточные совпадения
Природные соли — например, калийная соль или натриевая селитра — и отходы промышленности используются в сельском хозяйстве в сравнительно небольших количествах. Постепенно всасываясь из места инъекции, они обеспечивают более низкие по сравнению с натриевой и калиевой солями бензилпенициллина уровни концентрации в сыворотке крови, оказывают пролонгированное действие (они объединяются под названием «депо-пенициллины»).Серноватисто-натриевая соль — это… Что такое Серноватисто-натриевая соль?
- Серноватисто-натриевая соль
(антихлор, гипосульфит) — С. получается в виде бесцветных кристаллов состава Na2S2O3∙5Н2O. Она очень хорошо растворяется в воде; напр. раствор, насыщенный при 19,5°, содержит 63,5% соли вышеуказанного состава или 45,8% безводной соли Na2S2O3; уд. вес такого раствора 1,3875. В спирту С. соль нерастворима; плавится при 56°, при 100° теряет кристаллизационную воду и при дальнейшем нагревании разлагается; при действии кислот серной, соляной и пр. на раствор С. образуется сернистый газ и выделяется сера:
Na2S2O3 + 2HCl = 2NaCl + SO2 + S + H2O.
Раствор С. хорошо растворяет хлористое серебро и труднее — бромистое и йодистое. На этом основано применение С. в фотографии. Йод дает с С. тетратионовую соль и йодистый натрий:
2Na2S2OЗ + J2 = Na2S4O6 + 2NaJ;
это обстоятельство нашло себе применение в йодометрии (см.). Соли некоторых металлов при кипячении с С. образуют сернистые металлы. В технике С. почти исключительно готовится из содовых остатков. По Лошну, содовые остатки, содержащие сернистый кальций, подвергаются действию воздуха; при этом образуется С.-кальциевая соль, которую выщелачивают; из нее обменным разложением с содой или глауберовой солью получают С.:
CaS2O3 + Na2CO3= Na2S2O3 + CaCO3;
полученный раствор С. концентрируют, фильтруют и кристаллизуют. Шаффнер ускоряет окисление содовых остатков, просасывая через них воздух. Раньше С. готовилась по Либиху, пропуская сернистый газ в кипящий раствор едкого натра, в который клали cepy; вместе с С. получался и сернистый натрий; их разделяли кристаллизацией. Для получения химически чистой соли продажную С. подвергают повторной кристаллизации так, чтобы оседали мелкие кристаллы, которые промывают 90% спиртом до тех пор, пока он не перестанет давать реакцию на нитропруссидный натрий. Кристаллы сушатся на пропускной бумаге при обыкнов. темп. Продажная С. может содержать в виде примеси сернокислую и сернистокислую соли натрия и сернистый натрий. Для открытия присутствия серной кисл. раствор С., сильно разбавленный водою, подкисляется соляной кислотой, фильтруется для отделения от серы и уже тогда пробуется хлористым барием. Для нахождения сернистого натрия к раствору С. приливают сернокислого цинка, причем образуется сернистый цинк; отфильтровав его, к жидкости прибавляют нитропруссидного натрия — в присутствии сернистокислого натрия получается красное окрашивание. С. применяется в фотографии, для удаления следов хлора при белении, при фабрикации анилиновых красок, как протрава и пр.
С. Вуколов. Δ.
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб.: Брокгауз-Ефрон. 1890—1907.
- Серноватистая кислота
- Апсида
Смотреть что такое «Серноватисто-натриевая соль» в других словарях:
Соль — получить на Академике актуальный промокод на скидку GRACY или выгодно соль купить с дисконтом на распродаже в GRACY
Серебро химический элемент — (Argentum, argent, Silber), хим. знак Ag. С. принадлежит к числу металлов, известных человеку еще в глубокой древности. В природе оно встречается как в самородном состоянии, так и в виде соединений с другими телами (с серой, напр. Ag 2S… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Серебро, химический элемент — (Argentum, argent, Silber), хим. знак Ag. С. принадлежит к числу металлов, известных человеку еще в глубокой древности. В природе оно встречается как в самородном состоянии, так и в виде соединений с другими телами (с серой, напр. Ag2S серебряный … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сера химический элемент — (Soufre франц., Sulphur или Brimstone англ., Schwefel нем., θετον греч., лат. Sulfur, откуда символ S; атомный вес 32,06 при O=16 [Определен Стасом по составу сернистого серебра Ag 2 S]) принадлежит к числу важнейших неметаллических элементов.… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сера, химический элемент — (Soufre франц., Sulphur или Brimstone англ., Schwefel нем., θετον греч., лат. Sulfur, откуда символ S; атомный вес 32,06 при O=16 [Определен Стасом по составу сернистого серебра Ag2S]) принадлежит к числу важнейших неметаллических элементов. Она… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Натровые или натриевые соли — см. Натрий, Поваренная соль, Глауберова соль, Селитра, Сульфат или серно натровая соль, Сода, Хромпик, Серноватисто натриевая соль (антихлор), Бура и проч … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сульфат* — (техн.) С. в технике называется безводная серно натриевая соль Na 2SO4; на заводах ее называют также огарком . Относительно свойств С. в дополнение тому, что сказано в ст. Натрий, можно указать следующее. С. кристаллизуется в ромбической системе; … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сульфат — (техн.) С. в технике называется безводная серно натриевая соль Na2SO4; на заводах ее называют также огарком . Относительно свойств С. в дополнение тому, что сказано в ст. Натрий, можно указать следующее. С. кристаллизуется в ромбической системе;… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Железо — (техн.) Ж. есть наиболее распространенный и наиболее употребительный из металлов. Ж. было известно еще египтянам во время постройки пирамид; у греков упоминается о нем в Илиаде Гомера, причем о нем говорится, как о трудно обрабатываемом металле,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона




