13 Натрийсодержащие природные соли. Добыча и переработка натриевых солей
Лекция №13
Натрийсодержащие природные соли. Добыча и переработка натриевых солей.
Высокая потребность экономики Казахстана в натриевых солях и необходимость в современных экономических условиях использования собственных сырьевых залежей обуславливают особую актуальность разработки надежной технологии получения хлоридов, сульфатов, фосфатов, кальцинированной и каустической соды и других продуктов из местных природных хлоридных солей.
В республике имеются крупные запасы природных солей, содержащих хлорид натрия с примесями: в Гурьевской области – Индерское месторождение, в Жамбылской области – Ашы-Кольское, в Южно-Казахстанской области – месторождение Сузакского района и др. До сих пор такое сырье в Казахстане не перерабатывается на технические продукты ввиду отсутствия приемлемой технологии.
Многочисленные области применения хлорида натрия в народном хозяйстве, особенно в химической промышленности, требуют все возрастающих объемов производства этого важного товарного продукта.
Значительно возрастет и потребность в поваренной соли для нужд химической промышленности, так как многие ее подотрасли— хлорная, содовая и др. в качестве исходного сырья используют поваренную соль в виде кристаллического продукта или галитового рассола.
Значительно возрастет потребность в поваренной соли также в энергетике, в нефтегазодобывающей и легкой промышленности, в животноводстве и многих других отраслях народного хозяйства. При этом предъявляются более высокие требования к качеству и ассортименту поваренной соли, что требует решения новых задач в области технологии производства поваренной соли.
Поваренная соль широко используется в различных отраслях народного хозяйства, особенно в химической промышленности для получения натрия и хлора, а также многих важных соединений этих элементов. Кроме того, поваренная соль используется для консервирования продуктов, в быту для приготовления пищи. Товарный продукт представляет собой кристаллическое вещество определенного помола, состоящее преимущественно из хлорида натрия.
Главным потребителем хлорида натрия является химическая промышленность. Хлорид натрия является сырьем для производства кальцинированной соды аммиачным способом, хлора и каустической соды методом электролиза, а также используется для производства многих химических препаратов, средств защиты растений, моющих средств, различных красителей и т. д. [1].
Хлористый натрий, характеристика месторождения, запасы
Хлорид натрия относится к одной из наиболее широко распространенных природных солей. Используется в основном для производства кальцинированной соды. Наибольшее его количество содержится в океанской воде в виде раствора порядка 3,9 . 1016 хлорида натрия.
Основные запасы хлорида натрия находятся в земной коре в виде каменной соли, пластовых отложений и на поверхности земли в виде «сухих» или рассолами соляных озер. Наиболее крупные месторождения хлорида натрия – галита расположены, с основном, в Прикаспийском, Аральском и Северо-Восточном регионах Республики Казахстан. К ним относятся Индерское месторождение, озеро Жаксы-Кылыш, озеро Б.Калкаман, озера Светлица и Маралды.
По характеру солевого питания озеро Жаксы-Кылыш относится к озерам морского происхождения, озеро Б.Таболжан – озеро со смешанным питанием.
Состав самоосадочной и садочной поваренной соли озер Республики Казахстан представлен в таблице 4.
Таблица 4 — Состав самоосадочной-1 и садочной-2 поваренной соли
Месторождение | Цвет поваренной соли | Состав, % масс в пересчете на сухое вещество | |||||
NaCl | Ca2+ | Mg2+ | SO42- | Na2SO4 | H.O. | ||
1.Жаксы-Кылыш | 1-серый 2-желтый | 94,2 96,1 | 0,35 0,25 | 0,04 0,25 | 2,55 1,90 | 1,34 1,21 | 0,78 0,10 |
2. Большой Калкаман | 1-темно-серый 2-серый | 89,1 97,8 | 0,84 0,31 | 0,84 0,60 | 4,16 2,74 | — — | 5,50 0,82 |
3. Светлица | 1-серый 2-сероватый | 92,2 98,4 | 0,38 0,21 | 0,40 0,12 | 0,69 0,52 | — — | 4,65 0,23 |
4. Большой Таболжан | 1-желтый 2-светло-желтый | 79,9 92,6 | 1,21 0,62 | 0,15 0,04 | 2,24 1,48 | — — | 14,00 4,01 |
5. Индерское | светло-желтый | 98,5 | 0,15 | 0,017 | 0,10 | — | 0,3 |
6. Аральское | желтый | 97,67 | 0,13 | 0,07 | 0,61 | — | 0,19 |
Значительные количества садочной соли находятся в Кзыл-Ординской области, озера Жаксы-Кылыш, Арыскумское. Озеро Жаксы-Кылыш по характеру солевого питания относится к озерам морского происхождения и самое большое соленое озеро Прикаспийской низменности, расположено в Аральском регионе. Соляная толща представлена мелко- и крупнокристаллической гранаткой серовато-белого и белого цветов и солями насадки. Мощность соляной залежи озера составляет около 2 м, и из двух частей площадью 18 и 58 км2.
В составе залежи содержат:
— хлорид натрия 91,5-99,3%
— сульфат кальция (ангидрид) 0,3-4,3%
— сульфат магния 0,07-3,26%
— хлорид магния 1,1%
— сульфат натрия 1,6%
— Н.О., глинистые шламы 1,4%
В отдельных местах залежей имеются астраханит и эпсомит. В настоящее время в озере перерабатывают более 8% добываемой самосадочной соли, и оно является сырьевой базой АО «Аралсульфат».
Утвержденные запасы поваренной соли – галита по Кызыл-Ординской области составляют:
— Жаксы-Кылыш осадочная 41,5 млн.т
соль 175 млн.т.
— Арыскумское осадочная 3,3 млн.т
соль —
Разрабатывается в регионе дополнительно остаток поваренной соли около 13 млн.т.
Значительные запасы поваренной и кормовой соли находятся в Жамбылской и Шымкентской областях.
По данным поисково-оценочных работ было найдено 9 соленых озер, из которых положительную оценку получили следующие озера в Жамбылской области – Майдегенколь, Каракыр, Буранкол-тузы и Юнкиколь. Эти озера находятся на территории Сарысуйского района в низовьях реки Шу.
В составе соляной залежи содержится: NaCl – 95,5%, Ca – 0,5%, Mg – 0,05%, SO4 – 2,1%, Н.О. – 2,1%. На некоторых участках этого месторождения под галитовым слоем залегает слой мирабалита с содержанием Na2SO4 – 34% /81/.
Озеро Юнкиколь расположено в 22 км к западу от поселка Большие Камкалы. Общая площадь 2 м2. Мощность полезной толщи в среднем 0,8 м. Содержание поваренной соли в залежах около 90%. Запасы по категории С1 – 918,7 тыс.т.
Кроме того, в Жамбылской области находиться озеро Буранкол-тузы. Месторождение расположено в 20 км к северу от поселка Жайлаукол. Мощность полезной толщи до 1,5 м. Состав залежи: NaCl – 86%, Ca – 1,7%, Mg – 0,14%, SO4 – 4,5%, Н.О. – 5,3%.
В Сарысуйском районе, в 22 км к западу от поселка Калкалы и непосредственно от дороги Улабек-Жусалы, находится участок поваренной соли – озеро № 1. Мощность полезной толщи пласта до 1,7 м. В составе соли содержится: NaCl – 90,6%, Ca – 1,03%, Mg – 0,18%, SO4 – 2,5%, Н.О. – 3,5%.
В Сузакском районе Южно-Казахстанской области в 33 км к юго-востоку от поселка Аксумбе и на расстоянии 4 км от колодца Бугай-жайлы расположено галитовое месторождение. Мощность полезной толщи от 1 до 1,8 м. Вскрышные работы практически отсутствуют. Средний состав залежей: NaCl – 90,9%, Ca – 0,69%, Mg – 0,19%, SO4 – 2,7%, Н.О. – 3,0%.
В этом же районе находятся скважины. Пробы, взятые из них, показали присутствие в ней природной соды с содержанием Na2CO3 – 61%.
Огромные запасы поваренной соли находятся в других регионах Республики Казахстан. Например, в Атырауской области – месторождение Индер, запасы поваренной соли составляют более 1 млрд.т. Запасы поваренной соли по областям представлены в таблице 5.
Таблица 5- Запасы поваренной соли по данным ГПО «Казгеология»
№ | Название областей Казахстана | Запасы поваренной соли, тыс.т |
1. | Актюбинская | 8267 |
2. | Атырауская | 1069000 |
3. | Кустанайская | 2012 |
4. | Кокчетавская | 42509 |
5. | Павлодарская | 163447 |
6. | Семипалатинская | 29728 |
7. | Кызыл-Ординская | 27383 |
8. | Южно-Казахстанская | 3887 |
9. | Талды-Курганская | 627 |
10. | Жамбылская | 10040 |
Один из путей – заполнение водоемов водой, другой – изыскивать запасы солей для потребности промышленности и переработки жизненно важных продуктов.
Состав хлорида натрия Индерского месторождения Атырауской области и Аральского месторождения представлен в таблицах 6 и 7.
Таблица 6 — Состав хлорида натрия Индерского месторождений
Наименование | Масс.% |
NaCl | 98,5 |
Ca | 0,015 |
Mg | 0,017 |
Fe | 5.104 |
SiO2 | 0,3 |
K | 0,03 |
H.O. | 0,015 |
Таблица 7- Состав хлорида натрия Аральского месторождения
Наименование | Масс.% |
NaCl | 97,67 |
SO4 | 0,89 |
MgO | 0,07 |
CaO | 0,139 |
H.O. | 0,19 |
Контрольные вопросы:
- Натрийсодержащие природные соли.
- Хлористый натрий, характеристика месторождения, запасы
- Добыча и переработка натриевых солей.
Натриевые соли жирных кислот — Справочник химика 21
Натриевая соль жирной кислоты (натрия олеат и др.) 16,0 [c.397]Обычные широко распространенные, а ранее единственные моющие вещества — жировые мыла (натриевые соли жирных кислот) — имеют весьма существенные недостатки. В жесткой воде они образуют кальциевые и магниевые соли жирных кислот, не растворимые в воде. Эти соли, оседая на ткани нри стирке, ускоряют окисление тканей кислородом воздуха, являясь катализаторами окисления, делают ткань хрупкой и ломкой в результате значительно ускоряется износ тканей, ухудшается их внешний вид, краски на них блекнут. [c.394]
Другое предложение сводится к получению сухих натриевых солей жирных кислот, содержащихся в конденсате, путем нейтрализации конденсата и последующей выпарки и сушки. Смесь натриевых солей низших жирных кислот предложено использовать при приготовлении консистентных смазок. [c.472]
Эмульгирующая сиособность ПАВ характеризуется гидрофиль-но-липофильным балансом (ГЛБ), гидрофильно-олеофильным соотношением (ГОС). Если ПАВ лучше растворяется в воде, чем в масле, образуется прямая эмульсия м/в, если растворимость его лучше в масле, то получается обратная эмульсия в/м (правило Банкрофта). Прямую эмульсию дают эмульгаторы с числом ГЛБ, равным 8- 13, а при числе ГЛБ 3 6 получаются обратные эмульсии. Эффективность эмульгатора тем выше, чем лучше полярные и неполярные части его молекул отвечают природе обеих фаз эмульсии. Например, наиболее эффективными эмульгаторами для получения прямых эмульсий углеводородов являются натриевые соли жирных кислот (мыла) с числом углеродных атомов 8—10, а также алкилсульфаты, алкилсульфонаты и др.
Жесткая вода не дает пены с мылом, так как содержащиеся в мыле растворимые натриевые соли жирных кислот — пальмитиновой и стеариновой — переходят в нерастворимые кальциевые соли тех же кислот [c.675]
В куб колонны через барботер непрерывно подается острый пар. Обогрев куба производится глухим паром, благодаря чему температура в кубе поддерживается на уровне 102—104° С. Смесь паров воды и спиртов поднимается в колонне, конденсируется в дефлегматоре и конденсат стекает во флорентийский сосуд. Во флорентийском сосуде вода отделяется от спиртов. Часть водного слоя возвращается на орошение колонны (в количестве, необходимом для образования 5%-ного раствора натриевых солей жирных кислот), а остальное количество водного слоя поступает в емкость бутанольных вод. Верхний спиртовой слой из флорентийского сосуда поступает через промежуточный сборник в колонну для осушки спиртов.
Мыла и моющие вещества. Обычное мыло получается омылением жиров, т. е. глицеридов высших ( e— ,j) жирных кнслот. Говяжье сало нагревается с раствором едкого натра. Когда процесс гидролиза, т. е. образование свободного глицерина и натриевых солей жирных кислот, заканчивается, к смеси прибавляют поваренную соль, которая высаливает эти соли, при этом образуется два слоя. Для приготовления ядрового мыла слой натриевых солей отделяют от водного подмыльного щелока (из которого вырабатывают глицерин), охлаждают, превращают в стружки и подсушивают. После добавления красителей и отдушек (ароматических веществ) стружки мыла спрессовывают и штампуют в виде кусков хозяйственного и туалетного мыла.
Как известно, с повышением температуры поверхностное натяжение чистых жидкостей понижается, что связано с уменьшением сил когезии — молекулярного сцепления в жидкости вследствие увеличения среднего расстояния между молекулами. Ослабление взаимодействия между молекулами растворителя должно приводить к уменьшению работы адсорбции и, следовательно, поверхностной активности в соответствии с уравнением (43). Действительно, показано, например, что поверхностная активность натриевых солей жирных кислот (мыл) снижается с повышением температуры [5]. Вместе с тем известно, что в гомологических рядах ПАВ величина р при повышении температуры уменьшается (Р 1), т. е. при этом сглаживается различие в поверхностной активности соседних гомологов.
Не во всех случаях можно прямо связывать солюбилизирующую способность растворов со структурой мицеллярных образований ПАВ. Зависимость между ними даже для строго неполярных соединений сложна . катионоактивные вещества превосходят анионоактивные по солюбилизирующей опособности, кроме того, натриевые соли жирных кислот солюбилизируют красители лучше, чем калиевые. Для алкиларилсульфонатов солюбилизирующая способность меняется симбатно мицеллярным массам.
Стерины относятся к самым устойчивым компонентам экстрактивных веществ, тогда как жиры подвергаются превращениям уже при хранении древесины. При сульфатной варке в результате взаимодействия смоляных и жирных кислот, жиров и восков с гидроксидом натрия образуется сульфатное мыло. Жиры и воски в щелочной среде омыляются с образованием натриевых солей жирных кислот. Поверхностно-активные свойства мыла способствуют эмульгированию части неомыляемых липофильных компонентов экстрактивных веществ. В результате отбираемое после отстаивания упаренного отработанного варочного раствора (черного щелока) сульфатное мыло будет содержать натриевые соли смоляных и жирных кислот и неомыляемые соединения (фитостерины и др.). При обработке сульфатного мыла раствором серной кислоты получают талловое масло. Оно представляет собой смесь смоляных и жирных кислот и нейтральных веществ (фитостерин, высшие алифатические спирты, углеводороды). Вакуум-ректификацией таллового масла получают талловые продукты (дистиллированное талловое масло, талловую канифоль, талловые жирные кислоты и талловый пек).
В процессе стирки тканей карбонат натрия переводит жировые загрязнения в раствор в виде натриевых солей жирных кислот), повышая тем самым моющее действие СМС. Кроме того, кальцинированная сода способна умягчать жесткую воду, связывая ионы кальция и магния и переводя их соли в водорастворимые соединения. Карбонат натрия применяется в безводной форме без примесей тяжелых металлов (они ухудшают цвет моющего средства). Выпускаемая кальцинированная сода первого сорта содержит [в % (масс.)] карбоната натрия — не менее 99,4,
Хлорид натрия — это… Что такое Хлорид натрия?
| Хлорид натрия | |
 | |
 | |
| Общие | |
|---|---|
| Традиционные названия | обычная соль, поваренная соль, столовая соль, пищевая соль, каменная соль, галит[1] |
| Химическая формула | NaCl |
| Физические свойства | |
| Молярная масса | 58,44277 г/моль |
| Плотность | 2,165 г/см³ |
| Температура плавления | 800,8 °C |
| Температура кипения | 1465 °C |
| Молярная теплоёмкость (ст. усл.) | 50,8 Дж/(моль·К) |
| Удельная теплота испарения | 170,85 кДж/моль Дж/кг |
| Удельная теплота плавления | 28,68 кДж/моль Дж/кг |
| Химические свойства | |
| pKa | 6,7–7,3 |
| Растворимость в воде | 35,6 (0 °C) 35,9 (25 °C) 39,1 (100 °C) г/100 мл |
| 14,9 г/100 мл | |
| Растворимость в аммиаке | 21,5 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,5442 (589 нм) |
| Структура | |
| Координационная геометрия | Октаэдральная (Na +) Октаэдральная (Cl -) |
| Кристаллическая структура | гранецентрированная кубическая, cF8 |
| Классификация | |
| Рег. номер CAS | [7647-14-5] |
| 5234 | |
| Рег. номер EINECS | 231-598-3 |
| SMILES | [Na+].[Cl-] |
| RTECS | VZ4725000 |
| Безопасность | |
| ЛД50 | 3000–8000 мг/кг |
| NFPA 704 |  |
Хлори́д на́трия — химическое соединение NaCl, натриевая соль соляной кислоты, хлористый натрий.
Хлорид натрия известен в быту под названием поваренной соли, основным компонентом которой он является. Хлорид натрия в значительном количестве содержится в морской воде, создавая её солёный вкус. Встречается в природе в виде минерала галита (каменная соль).
Чистый хлорид натрия имеет вид бесцветных кристаллов, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита, который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов, соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 10 15 тонн NaCl, то есть из каждой тысячи тонн морской воды можно получить в среднем 1,3 тонны хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, состоят из NaCl. Также он найден в кристаллах снега[2].
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах теплых морей или на соляных озёрах, где на мелководье соленая вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора, «соль была рождена благородными родителями: солнцем и морем»[3].
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решетку и содержит 39,34 % Na, 60,66 % Cl. Другими химическими элементами, входящими в состав примесей, являются: Br, N, H, Mn, Cu, Ga, As, I, Ag, Ba, Tl, Pb, K, Ca, S, O. Плотность 2,1—2, 2 г / см ³, а твёрдость по шкале Мооса — 2. Бесцветный, прозрачный минерал, со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и т. п.[4]
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (желтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, йодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и т. д.[4]
По условиям формирования месторождений каменную соль подразделяют на следующие виды[4]:
- рассолы современных соляных бассейнов
- соляные подземные воды
- залежи минеральных солей современных соляных бассейнов
- ископаемые залежи (важнейшие для промышленности).
Морская соль
Морская соль является смесью солей (хлориды, карбонаты, сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:
| Соединение | Масс. доля, % |
|---|---|
| NaCl | 77,8 |
| MgCl2 | 10,9 |
| MgSO4 | 4,7 |
| KCl | 2,5 |
| K2SO4 | 2,5 |
| CaCO3 | 0,3 |
| Ca(HCO3)2 | 0,3 |
| другие соли | 0,2 |
 Очищенная кристаллическая морская соль
Очищенная кристаллическая морская сольПри испарении морской воды при температуре 20 — 35 ° C в осадке сначала кристаллизуются наименее растворимые соли — карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них — сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу — горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз. Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль с Мёртвого моря. В очищенном виде этот вид соли также предлагается в продуктовой торговой сети — как натуральная и богатая йодом пищевая[5].
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских, девонских, пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах[4]. Среди озёрных месторождений России крупнейшие — Эльтонское, Баскунчак в Прикаспии, Кучукское озеро, о. Кулундинское, Эбейты и др. озера в Зап. Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими — 60—90 м. Извлечённую соль выливали в особый резервуар — творило, откуда она через отверстия стекала в нижний резервуар, и системой желобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка. В 1137 новгородский князь Святослав определил налог на соляные варницы[6]:
 | …на мори от чрена и от салгы по пузу… |  |
[7]
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли. Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.
Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн)[8].
-

Добыча соли в южной части Мертвого моря, Израиль
-

Кристаллы каменной соли
-

Плантация морской соли в Дакаре
-

Соляные кучи на солончаке Уюни, Боливия
Применение
В пищевой промышленности и кулинарии
Соль повареннаяВ пищевой промышленности и кулинарии используют хлорид натрия, чистота которого должна быть не менее 97 %. Его применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия имеет товарное название поваренная соль, порой также употребляются названия пищевая, столовая, а также уточнение названия в зависимости от её происхождения — каменная, морская, и по составу добавок — йодированная, фторированная и т. д. Такая соль является кристаллическим сыпучим продуктом с солёным вкусом без привкуса, без запаха (за исключением йодированной соли), в котором не допускаются посторонние примеси, не связанные с методом добывании соли. Кроме хлорида натрия, поваренная соль содержит небольшое количество солей кальция, магния, калия, которые придают ей гигроскопичности и жёсткости. Чем меньше этих примесей в соли, тем выше её качество.
Выделяют сорта: экстра, высший, первый и второй. Массовая доля хлористого натрия в сортах,%:
- экстра — не менее 99,5;
- высший — 98,2;
- первый — 97,5;
- второй — 97,0.
Массовая доля влаги в выварочной соли сорта «экстра» 0,1 %, в высшем сорте — 0,7 %. Допускают добавки йодида калия (йодистого калия), йодата калия, фторидов калия и натрия. Массовая доля йода должна составлять (40,0 ± 15,0) × 10 −4 %, фтора (25,0 ± 5,0) × 10 −3 %. Цвет экстра и высшего сортов — белый, однако для первого и второго допускается серый, желтоватый, розовый и голубоватый оттенки в зависимости от происхождения соли. Пищевую поваренную соль производят молотой и сеяной. По размеру зёрен молотую соль подразделяют на номера: 0, 1, 2, 3. Чем больше номер, тем больше зерна соли.
В кулинарии хлорид натрия потребляют как важнейшую приправу. Соль имеет характерный вкус, без которого пища кажется человеку пресной. Такая особенность соли обусловлена физиологией человека. Однако зачастую люди потребляют соли больше, чем нужно для физиологических процессов.
Хлорид натрия имеет слабые антисептические свойства — 10-15 % содержание соли предотвращает размножение гнилостных бактерий. Этот факт обусловливает её широкое применение как консерванта.
В медицине
Изотонический раствор хлорида натрия в воде (0,9 %) применяется как дезинтоксикационное средство, для коррекции состояния систем организма в случае обезвоживания, как растворитель других лекарственных препаратов. Гипертонические растворы (10 % р-р) используют как вспомогательный осмотический диуретик при лёгочных, желудочных и кишечных кровотечениях для обеспечения форсированного диуреза, в состояниях, характеризующихся дефицитом ионов натрия и хлора, при отравлении нитратом серебра, для обработки гнойных ран (местно). В офтальмологии как местное средство раствор хлорида натрия обладает противоотёчным действием[9].
В коммунальном хозяйстве. Техническая соль
Зимой хлорид натрия, смешанный с другими солями, песком или глиной — так называемая техническая соль — применяется как антифриз против гололеда. Ею посыпают тротуары, хотя это отрицательно влияет на кожаную обувь и техническое состояние автотранспорта в виду коррозийных процессов.
Регенерация Nа-катионитовых фильтров
Nа-катионитовые фильтры широко применяются в котельных установках всех мощностей для смягчения воды при водоподготовке. Катионитовым материалом на современных водоподготовительных установках служат в основном глауконит, сульфанованные угли и синтетические смолы. Наиболее распространены сульфоугли.
Регенерацию Nа-катионитовых фильтров осуществляют 6—8%-м раствором поваренной соли, в результате действие сульфоуголя восстанавливается. Реакции идут по уравнениям:
- CaR2 + 2NаСl = 2NаR + CaСl2.
- МgR2 + 2NаСl = 2NаR + МgСl2.
Химическая промышленность
Соль, наряду с каменным углем, известняками и серой, образует «большую четвёрку» продуктов минерального сырья, которые являются важнейшими для химической промышленности[10]. Из неё получают соду, хлор, соляную кислоту, гидроксид натрия, сульфат натрия и металлический натрий. Кроме этого соль используется также для промышленного получения легкорастворимого в воде хлората натрия, который является средством для уничтожения сорняков[11]. Суммарное уравнение реакции электролиза горячего раствора хлорида натрия[12]:
- NaCl + 3 H2O → NaClO3 + 3 H2↑
Получение хлора и гидроксида натрия
В промышленности путём электролиза раствора хлорида натрия получают хлор. Процессы, происходящие на электродах[13][14]:
- на катоде как побочный продукт выделяется водород вследствие восстановления ионов H +, образованных в результате электролитической диссоциации воды:
- H2O ⇆ H+ + OH−
- 2 H+ + 2 e− → H2↑
- поскольку (вследствие практически полной электролитической диссоциации NaCl), хлор в растворе находится в виде хлорид-ионов, они окисляются на аноде до свободного хлора в виде газа:
- NaCl → Na+ + Cl−
- 2 Cl− − 2 e− → Cl2↑
- суммарная реакция:
- 2 NaCl + 2 H2O → 2 NaOH + Cl2↑ + H2↑
Как видно из уравнения суммарной реакции, ещё одним продуктом является гидроксид натрия. Расход электроэнергии на 1 т хлора составляет примерно 2700 кВт × час. Полученный хлор сжижается на жёлтую жидкость уже при обычной температуре[15].
Если между анодом и катодом нет диафрагмы, то растворенный в воде хлор начинает реагировать с гидроксидом натрия, образуя хлорид и гипохлорит натрия NaClO[14]:
- 2 NaOH + Cl2 → NaCl + NaClO + H2O
Поэтому для получения гидроксида натрия применяют диафрагму и соответствующий метод получения NaOH называют диафрагменным. В качестве диафрагмы применяют асбестовый картон. В процессе электролиза раствор хлорида натрия постоянно подается в анодное пространство, а из катодного пространства непрерывно вытекает раствор хлорида и гидроксида натрия. Во время выпаривания последнего хлорид кристаллизуется, поскольку его растворимость в 50 % растворе NaOH ничтожно мала (0,9 %). Полученный раствор NaOH выпаривают в железных чанах, затем сухой остаток переплавляют.
Для получения чистого гидроксида натрия (без добавок хлорида натрия) применяют ртутный метод, где используют графитовый анод и ртутный катод. Вследствие того, что перенапряжение выделения водорода на ртути очень большое, на ней вновь появляются ионы натрия и образуется амальгама натрия[14][16]:
- Na+ + e− → Na(Hg)
Амальгаму позже разлагают горячей водой с образованием гидроксида натрия и водорода, а ртуть перекачивают насосом обратно в электролизер:
- 2 Na(Hg) + 2 H2O → 2 NaOH + H2↑
Суммарная реакция процесса такая же, как и в случае диафрагменного метода.
Получение металлического натрия
Металлический натрий получают электролизом расплава хлорида натрия. Происходят следующие процессы:
- на катоде выделяется натрий:
- 2 Na+ + 2 e− → 2 Na
- на аноде выделяется хлор (как побочный продукт):
- 2 Cl− − 2 e− → Cl2
- суммарная реакция:
- 2 Na+ + 2 Cl− → 2 Na + Cl2
Ванна электролизера состоит из стального кожуха с футеровкой, графитового анода и кольцевого железного катода. Между катодом и анодом располагается сетчатая диафрагма. Для снижения температуры плавления NaCl (800 ° C), электролитом является не чистый хлорид натрия, а его смесь с хлоридом кальция CaCl 2 (40:60) с температурой плавления 580 ° C. Металлический натрий, который собирается в верхней части катодного пространства, содержит до 5 % примесь кальция, но последний со временем почти полностью отделяется, поскольку его растворимость в жидком натрии при температуре его плавления (371 ° C) составляет всего 0,01 %. С расходованием NaCl его постоянно добавляют в ванну. Затраты электроэнергии составляют примерно 15 кВт × ч на 1 кг натрия[17].
Получение соляной кислоты и сульфата натрия
Среди многих промышленных методов получения соляной кислоты, то есть водного раствора хлороводорода (HCl), применяется реакция обмена между хлоридом натрия и серной кислотой:
- NaCl + H2SO4 → NaHSO4 + HCl↑
- NaCl + NaHSO4 → Na2SO4 + HCl↑
Первая реакция происходит в значительной степени уже при обычных условиях, а при слабом нагреве идет почти до конца. Вторая происходит лишь при высоких температурах. Процесс осуществляется в специальных механизированных печах большой мощности. Хлороводород, который выделяется, обеспыливают, охлаждают и поглощают водой с образованием соляной кислоты. Как побочный продукт образуется сульфат натрия Na2SO4[18][19].
Этот метод применяется также для получения хлороводорода в лабораторных условиях.
Физические и физико-химические свойства
Температура плавления 800,8 С, кипения 1465 С.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в г на 100 г воды) равен 35,9 при 21 °C и 38,1 при 80 °C. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена. В чистом виде хлорид натрия не гигроскопичен. Однако соль часто бывает загрязнена примесями (преимущественно ионами Ca 2 +, Mg 2 + и SO2−4), и такая соль на воздухе сыреет[20]. Кристаллогидрат NaCl · 2H 2 O можно выделить при температуре ниже +0,15 ° C[21].
Смесь измельченного льда с мелким порошком хлорида натрия является эффективным охладителем. Так, смесь состава 30 г NaCl на 100 г льда охлаждается до температуры −20 ° C. Это происходит потому, что водный раствор соли замерзает при температуре ниже 0 ° C. Лед, имеющий температуру около 0 ° C, плавится в таком растворе, поглощая тепло окружающей среды.
| Термодинамические характеристики | |
|---|---|
| ΔfH0g | −181,42 кДж/моль |
| ΔfH0l | −385,92 кДж/моль |
| ΔfH0s | −411,12 кДж/моль |
| ΔfH0aq | −407 кДж/моль |
| S0g, 1 bar | 229,79 Дж/(моль·K) |
| S0l, 1 bar | 95,06 Дж/(моль·K) |
| S0s | 72,11 Дж/(моль·K) |
Диэлектрическая проницаемость NaCl — 6,3
Плотность и концентрация водных растворов NaCl
| Концентрация, % | Концентрация, г/л | Плотность, г/мл |
|---|---|---|
| 1 | 10,05 | 1,005 |
| 2 | 20,25 | 1,012 |
| 4 | 41,07 | 1,027 |
| 6 | 62,47 | 1,041 |
| 8 | 84,47 | 1,056 |
| 10 | 107,1 | 1,071 |
| 12 | 130,2 | 1,086 |
| 14 | 154,1 | 1,101 |
| 16 | 178,5 | 1,116 |
| 18 | 203,7 | 1,132 |
| 20 | 229,5 | 1,148 |
| 22 | 256 | 1,164 |
| 24 | 283,2 | 1,18 |
| 26 | 311,2 | 1,197 |
Лабораторное получение и химические свойства
При действии серной кислоты выделяет хлороводород. С раствором нитрата серебра образует белый осадок хлорида серебра.
Учитывая огромные природные запасы хлорида натрия, необходимости в его промышленном или лабораторном синтезе нет. Однако, его можно получить различными химическими методами как основной или побочный продукт.
- получение из простых веществ натрия и хлора является экзотермической реакцией[22]:
- Na(тв) + 1/2Cl2(г) → NaCl(тв) + 410 кДж
- нейтрализация щелочи гидроксида натрия соляной кислотой[23]:
- NaОН + НCl → NaCl + Н2О
Поскольку хлорид натрия в водном растворе почти полностью диссоциирован на ионы: NaCl → Na+ + Cl−, его химические свойства в водном растворе определяются соответствующими химическими свойствами катионов натрия и хлорид-анионов.
Структура
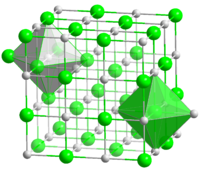
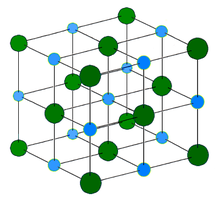 Кристаллическая решётка хлорида натрия.
Кристаллическая решётка хлорида натрия.Голубой цвет = Na+
Зелёный цвет = Cl−
Хлорид натрия образует бесцветные кристаллы кубической сингонии, пространственная группа F m3m, a = 0,563874 нм, d = 2,17 г/см³. Каждый из ионов Cl− окружен шестью ионами Na+ в октаедральний конфигурации, и наоборот. Если мысленно отбросить, например, ионы Na+, то останется плотно упакованная кубическая структура с ионов Cl−, называемая гранецентрированной кубической решеткой. Ионы Na+ тоже образуют плотно упакованную кубическую решетку. Таким образом, кристалл состоит из двух подрешеток, сдвинутых друг относительно друга на полупериод. Такая же решетка характерна для многих других минералов.
В кристаллической решетке между атомами преобладает ионная химическая связь, что является следствием действия электростатического взаимодействия противоположных по заряду ионов
См. также
Примечания
- ↑ Натрия хлорид на сайте Национального института стандартов и технологии (англ. National Institute of Standards and Technology) (англ.)
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 218
- ↑ Пифагор. Золотой канон. Фигуры эзотерики. — М.: Изд-во Эксмо, 2003. — 448 с. (Антология мудрости).
- ↑ 1 2 3 4 Малая горная энциклопедия. В 3-х т. / Под ред. В. С. Белецкого . — Донецк: «Донбасс», 2004. — ISBN 966-7804-14-3
- ↑ УНИАН: Морская соль для красоты и здоровья кожи
- ↑ Российское законодательство Х-ХХ веков. Законодательство Древней Руси. т. 1. М, 1984. С. 224—225. (рус.)
- ↑ В переводе с поморской «говори» слово чрен (црен) означает четырёхугольный ящик, кованный из листового железа, а салга — котёл, в котором варили соль. Пузом в беломорских солеварнях называли мешок соли в два четверика, то есть, объёмом около 52 литров.
- ↑ Соль (PDF), Геологический обзор США на сайте Программы минеральных ресурсов (англ.)
- ↑ Энциклопедия здоровья
- ↑ Онлайн Энциклопедия кругосвет. Натрий
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 261
- ↑ Синтез хлората натрия (англ.)
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 249
- ↑ 1 2 3 М. Л. Глинка Общая химия (Учебник), изд. 2-е изд., Перераб. и доп .. — С. 608, Киев: «Высшая школа», 1982.
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 254
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 231
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 219
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 250
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 257—258
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 215—216
- ↑ Б. В. Некрасов. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 234
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 255
- ↑ Б. В. Некрасов. Основы общей химии. Т. 1. Изд. 3-е, испр. и доп. Москва, издательство «Химия», 1973 г. 656 с.; 160 табл.; 391 рис. С. 191
Ссылки
Шаблон:АТХ код A07
Плазмозамещающие и перфузионные растворы — АТХ код: B05
| B05A |
| ||
|---|---|---|---|
| B05B |
| ||
| B05C |
| ||
| B05D |
| ||
| B05X |
| ||
| B05Z |
Ацетат натрия — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 3 мая 2019; проверки требуют 2 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 3 мая 2019; проверки требуют 2 правки.Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
Также ацетат натрия является источником углерода для бактерий, выращиваемых на питательной среде.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
Ацетат натрия также используется в быту как составная химических грелок (англ. heating pad) или химических обогревателей (англ. Hand warmer), применяется как составная часть смеси «горячего льда» (англ. «hot ice»), при кристаллизации ацетата натрия выделяется тепло — это экзотермический процесс. При нагреве тригидрата ацетата натрия (имеющего точку плавления в 58 °C) до 100 °C (обычно ёмкость с ним кладут в кипящую воду) он расплавляется (вернее, растворяется в собственной кристаллизационной воде) и переходит в водный раствор ацетата натрия. При охлаждении этого раствора образуется перенасыщенный раствор ацетата натрия в воде. Этот раствор прекрасно переохлаждается до комнатной температуры без образования твёрдой фазы, затем нажатием на металлический диск в ёмкости образуется центр кристаллизации, который, вырастая, заставляет перенасыщенный раствор переходить в твёрдую фазу тригидрата ацетата натрия. Этот процесс сопровождается значительным выделением тепла (экзотермическая реакция)[2][3][4], теплота фазового перехода составляет 264-289 кДж/кг[5].
На этом свойстве основан довольно красивый химический опыт — «горячий лёд».
- Ch4COOH+NaHCO3⟶Ch4COONa+h3O+CO2↑{\displaystyle {\mathsf {CH_{3}COOH+NaHCO_{3}\longrightarrow CH_{3}COONa+H_{2}O+CO_{2}\uparrow }}}
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 г гидрокарбоната натрия реагируют с 750 г 8%-го винного уксуса (или же с 86 г 70%-й уксусной эссенции) с образованием 82 г ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия. Для получения тригидрата ацетата натрия без выпаривания необходимо смешать 84 г гидрокарбоната натрия (пищевой соды) с 86 г 70%-ной уксусной кислоты и 10 г воды.
- Также ацетат натрия может быть получен и в ходе экзотермической реакции растворения металлического натрия в уксусной кислоте:
- 2Ch4COOH+2Na⟶2Ch4COONa+h3↑+Q{\displaystyle {\mathsf {2CH_{3}COOH+2Na\longrightarrow 2CH_{3}COONa+H_{2}\uparrow +Q}}}
Ацетат натрия может быть использован для образования сложного эфира по реакции с алкилгалогенидами, такими как, например, бромэтан:
- Ch4COONa+Ch4Ch3Br→Ch4COOC2H5+NaBr{\displaystyle {\mathsf {CH_{3}COONa+CH_{3}CH_{2}Br\rightarrow CH_{3}COOC_{2}H_{5}+NaBr}}}
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
- 2Ch4COONa→Na2CO3+(Ch4)2CO{\displaystyle {\mathsf {2CH_{3}COONa\rightarrow Na_{2}CO_{3}+(CH_{3})_{2}CO}}}
Ацетат натрия может всасываться в организм при проглатывании. Является ирритантом. LD50 25956 мг/кг. По другим данным из того же источника: LD50(крысы, орально): 3500 мг/кг, LD50(мыши, орально): 4960 мг/кг. [6]
-

Химический обогреватель c перенасыщенным раствором ацетата натрия
Ацетат натрия
Гидроксид натрия — Википедия
Гидрокси́д на́трия (лат. Nátrii hydroxídum; другие названия — каустическая сода, едкий натр) — неорганическое химическое вещество, самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется около 57 миллионов тонн едкого натра.
Интересна история тривиальных названий как гидроксида натрия, так и других щелочей. Название «едкая щёлочь» обусловлено свойством разъедать кожу (вызывая сильные ожоги), бумагу и другие органические вещества. До XVII века щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 году французский учёный Анри Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой, а карбонат калия — поташом. В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.
Гидроксид натрия — белое твёрдое вещество. Сильно гигроскопичен, на воздухе «расплывается», активно поглощая пары воды из воздуха. Хорошо растворяется в воде, при этом выделяется большое количество теплоты. Раствор едкого натра мылок на ощупь.
Термодинамика растворов
ΔH0 растворения для бесконечно разбавленного водного раствора −44,45 кДж/моль.
Из водных растворов при +12,3…+61,8 °C кристаллизуется моногидрат (ромбическая сингония), температура плавления +65,1 °C; плотность 1,829 г/см³; ΔH0обр −425,6 кДж/моль), в интервале от −28 до −24 °C — гептагидрат, от −24 до −17,7 °C — пентагидрат, от −17,7 до −5,4 °C — тетрагидрат (α-модификация). Растворимость в метаноле 23,6 г/л (t = +28 °C), в этаноле 14,7 г/л (t = +28 °C). NaOH·3,5Н2О (температура плавления +15,5 °C).
Гидроксид натрия (едкая щёлочь) — сильное химическое основание (к сильным основаниям относят гидроксиды, молекулы которых полностью диссоциируют в воде), к ним относят гидроксиды щелочных и щёлочноземельных металлов подгрупп Iа и IIа периодической системы Д. И. Менделеева, KOH (едкое кали), Ba(OH)2 (едкий барит), LiOH, RbOH, CsOH, а также гидроксид одновалентного таллия TlOH. Щёлочность (основность) определяется валентностью металла, радиусом внешней электронной оболочки и электрохимической активностью: чем больше радиус электронной оболочки (увеличивается с порядковым номером), тем легче металл отдаёт электроны, и тем выше его электрохимическая активность и тем левее располагается элемент в электрохимическом ряду активности металлов, в котором за ноль принята активность водорода.

Водные растворы NaOH имеют сильную щелочную реакцию (pH 1%-раствора = 13,4). Основными методами определения щелочей в растворах являются реакции на гидроксид-ион (OH−), (c фенолфталеином — малиновое окрашивание и метиловым оранжевым (метилоранжем) — жёлтое окрашивание). Чем больше гидроксид-ионов находится в растворе, тем сильнее щёлочь и тем интенсивнее окраска индикатора.
Гидроксид натрия вступает в следующие реакции:
- с кислотами, амфотерными оксидами и гидроксидами
- NaOH+HCl→NaCl+h3O{\displaystyle {\mathsf {NaOH+HCl\rightarrow NaCl+H_{2}O}}}
- NaOH+h3S→NaHS+h3O{\displaystyle {\mathsf {NaOH+H_{2}S\rightarrow NaHS+H_{2}O}}} (кислая соль, при отношении 1:1)
- 2NaOH+h3S→Na2S+2h3O{\displaystyle {\mathsf {2NaOH+H_{2}S\rightarrow Na_{2}S+2H_{2}O}}} (в избытке NaOH)
Общая реакция в ионном виде:
- OH−+H+→h3O{\displaystyle {\mathsf {OH^{-}+H^{+}\rightarrow H_{2}O}}}
- с амфотерными оксидами которые обладают как основными, так и кислотными свойствами, и способностью реагировать с щелочами, как с твёрдыми при сплавлении:
- 2NaOH+ZnO →500−600oC Na2ZnO2+h3O{\displaystyle {\mathsf {2NaOH+ZnO\ {\xrightarrow[{}]{500-600^{o}C}}\ Na_{2}ZnO_{2}+H_{2}O}}}
- 2NaOH+ZnO+h3O→Na2[Zn(OH)4]{\displaystyle {\mathsf {2NaOH+ZnO+H_{2}O\rightarrow Na_{2}[Zn(OH)_{4}]}}} — в растворе
- с амфотерными гидроксидами
- NaOH+Al(OH)3 →1000oC NaAlO2+2h3O{\displaystyle {\mathsf {NaOH+Al(OH)_{3}\ {\xrightarrow {1000^{o}C}}\ NaAlO_{2}+2H_{2}O}}} — при сплавлении
- 3NaOH+Al(OH)3→Na3[Al(OH)6]{\displaystyle {\mathsf {3NaOH+Al(OH)_{3}\rightarrow Na_{3}[Al(OH)_{6}]}}} — в растворе
- с солями в растворе:
- 2NaOH+CuSO4→Cu(OH)2↓+Na2SO4{\displaystyle {\mathsf {2NaOH+CuSO_{4}\rightarrow Cu(OH)_{2}\!\downarrow +Na_{2}SO_{4}}}}
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия, действуя гидроксидом натрия на сульфат алюминия в водном растворе, при этом избегая избытка щёлочи и растворения осадка. Его и используют, в частности, для очистки воды от мелких взвесей.
- c неметаллами:
например, с фосфором — с образованием гипофосфита натрия:
- 4P+3NaOH+3h3O→Ph4↑+3Nah3PO2{\displaystyle {\mathsf {4P+3NaOH+3H_{2}O\rightarrow PH_{3}\!\uparrow +3NaH_{2}PO_{2}}}}
с серой:
- 3S+6NaOH→2Na2S+Na2SO3+3h3O{\displaystyle {\mathsf {3S+6NaOH\rightarrow 2Na_{2}S+Na_{2}SO_{3}+3H_{2}O}}}
- с галогенами
- 2NaOH+Cl2→NaClO+NaCl+h3O{\displaystyle {\mathsf {2NaOH+Cl_{2}\rightarrow NaClO+NaCl+H_{2}O}}} (дисмутация хлора в разбавленном растворе при комнатной температуре)
- 6NaOH+3Cl2→NaClO3+5NaCl+3h3O{\displaystyle {\mathsf {6NaOH+3Cl_{2}\rightarrow NaClO_{3}+5NaCl+3H_{2}O}}} (дисмутация хлора при нагревании в концентрированном растворе)
- с металлами
Гидроксид натрия вступает в реакцию с алюминием, цинком, титаном. Он не реагирует с железом и медью (металлами, которые имеют низкий электрохимический потенциал). Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксоалюмината натрия и водорода:
- 2Al+2NaOH+6h3O→2Na[Al(OH)4]+3h3↑{\displaystyle {\mathsf {2Al+2NaOH+6H_{2}O\rightarrow 2Na[Al(OH)_{4}]+3H_{2}\!\uparrow }}}
Эта реакция использовалась в первой половине XX века в воздухоплавании: для заполнения водородом аэростатов и дирижаблей в полевых (в том числе боевых) условиях, так как данная реакция не требует источников электроэнергии, а исходные реагенты для неё могут легко транспортироваться.
- с эфирами, амидами и алкилгалогенидами (гидролиз):
с жирами (омыление) такая реакция необратима, так как получающаяся кислота со щёлочью образует мыло и глицерин. Глицерин впоследствии извлекается из подмыльных щёлоков путём вакуум-выпарки и дополнительной дистилляционной очистки полученных продуктов. Этот способ получения мыла был известен на Ближнем Востоке с VII века.
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла в зависимости от состава жира.
- с многоатомными спиртами — с образованием алкоголятов:
- HOCh3Ch3OH+2NaOH→NaOCh3Ch3ONa+2h3O{\displaystyle {\mathsf {HOCH_{2}CH_{2}OH+2NaOH\rightarrow NaOCH_{2}CH_{2}ONa+2H_{2}O}}}
Качественное определение ионов натрия[править | править код]
 Атомы натрия придают пламени жёлтое свечение.
Атомы натрия придают пламени жёлтое свечение.- По цвету пламени горелки — атомы натрия придают пламени жёлтую окраску
- С использованием специфических реакций на ионы натрия
| Реагент | Фторид аммония | Нитрит цезия-калия-висмута | Ацетат магния | Ацетат цинка | Пикро- лоновая кислота | Диокси- винная кислота | Бромбензол- сульфокислота | Ацетат уранила-цинка |
|---|---|---|---|---|---|---|---|---|
| Цвет осадка | белый | бледно-жёлтый | жёлто-зелёный | жёлто-зелёный | белый | белый | бледно-жёлтый | зеленовато-жёлтый |
Гидроксид натрия может получаться в промышленности химическими и электрохимическими методами.
Химические методы получения гидроксида натрия[править | править код]
К химическим методам получения гидроксида натрия относятся пиролитический, известковый и ферритный.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество энергоносителей, получаемый едкий натр сильно загрязнён примесями.
В настоящее время эти методы почти полностью вытеснены электрохимическими методами производства.
Пиролитический метод[править | править код]
Пиролитический метод получения гидроксида натрия является наиболее древним и начинается с получения оксида натрия Na2О путём прокаливания карбоната натрия (например, в муфельной печи). В качестве сырья может быть использован и гидрокарбонат натрия, разлагающийся при нагревании на карбонат натрия, углекислый газ и воду:
- 2NaHCO3 →250oC Na2CO3+CO2↑+ h3O{\displaystyle {\mathsf {2NaHCO_{3}\ {\xrightarrow {250^{o}C}}\ Na_{2}CO_{3}+CO_{2}\!\uparrow +\ H_{2}O}}}
- Na2CO3 →1000oC Na2O+CO2↑{\displaystyle {\mathsf {Na_{2}CO_{3}\ {\xrightarrow {1000^{o}C}}\ Na_{2}O+CO_{2}\!\uparrow }}}
Полученный оксид натрия охлаждают и очень осторожно (реакция происходит с выделением большого количества тепла) добавляют в воду:
- Na2O+h3O→2NaOH{\displaystyle {\mathsf {Na_{2}O+H_{2}O\rightarrow 2NaOH}}}
Известковый метод[править | править код]
Известковый метод получения гидроксида натрия заключается во взаимодействии раствора соды с гашеной известью при температуре около 80 °С. Этот процесс называется каустификацией и проходит по реакции:
- Na2CO3+Ca(OH)2→2NaOH+CaCO3↓{\displaystyle {\mathsf {Na_{2}CO_{3}+Ca(OH)_{2}\rightarrow 2NaOH+CaCO_{3}\!\downarrow }}}
В результате реакции получается раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора фильтрацией, затем раствор упаривается до получения расплавленного продукта, содержащего около 92 % масс. NaOH. Затем NaOH плавят и разливают в железные барабаны, где он кристаллизуется.
Ферритный метод[править | править код]
Ферритный метод получения гидроксида натрия состоит из двух этапов:
- Na2CO3+Fe2O3→850oC2NaFeO2+CO2↑{\displaystyle {\mathsf {Na_{2}CO_{3}+Fe_{2}O_{3}{\xrightarrow {850^{o}C}}2NaFeO_{2}+CO_{2}\!\uparrow }}}
- 2NaFeO2+2h3O →H+ 2NaOH+Fe2O3⋅h3O↓{\displaystyle {\mathsf {2NaFeO_{2}+2H_{2}O\ {\xrightarrow {H^{+}}}\ 2NaOH+Fe_{2}O_{3}\cdot H_{2}O\!\downarrow }}}
Первая реакция представляет собой процесс спекания кальцинированной соды с окисью железа при температуре 800 – 900°С. При этом образуется спек — феррит натрия и выделяется двуокись углерода. Далее спёк обрабатывают (выщелачивают) водой по второй реакции; получается раствор гидроксида натрия и осадок Fe2O3⋅{\displaystyle \cdot }nH2О, который после отделения его от раствора возвращается в процесс. Получаемый раствор щёлочи содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92 % масс. NaOH, а затем получают твёрдый продукт в виде гранул или хлопьев.
Электрохимические методы получения гидроксида натрия[править | править код]
Способ основан на электролизе растворов галита (минерала, состоящего в основном из поваренной соли NaCl) с одновременным получением водорода и хлора. Этот процесс можно представить суммарной формулой:
- 2NaCl+2h3O→h3↑+Cl2↑+2NaOH{\displaystyle {\mathsf {2NaCl+2H_{2}O\rightarrow H_{2}\!\uparrow +Cl_{2}\!\uparrow +2NaOH}}}
Едкая щёлочь и хлор вырабатываются тремя электрохимическими методами. Два из них — электролиз с твёрдым катодом (диафрагменный и мембранный методы), третий — электролиз с жидким ртутным катодом (ртутный метод).
В мировой производственной практике используются все три метода получения хлора и каустика с явной тенденцией к увеличению доли мембранного электролиза.
| Показатель на 1 тонну NaOH | Ртутный метод | Диафрагменный метод | Мембранный метод |
|---|---|---|---|
| Выход хлора, % | 99 | 96 | 98,5 |
| Электроэнергия, кВт·ч | 3150 | 3260 | 2520 |
| Концентрация NaOH, % | 50 | 12 | 35 |
| Чистота хлора, % | 99,2 | 98 | 99,3 |
| Чистота водорода, % | 99,9 | 99,9 | 99,9 |
| Массовая доля O2 в хлоре, % | 0,1 | 1—2 | 0,3 |
| Массовая доля Cl− в NaOH, % | 0,003 | 1—1,2 | 0,005 |
В России приблизительно 35 % от всего выпускаемого каустика вырабатывается электролизом с ртутным катодом и 65 % — электролизом с твёрдым катодом.
Диафрагменный метод[править | править код]
 Схема старинного диафрагменного электролизера для получения хлора и щёлоков: А — анод, В — изоляторы, С — катод, D — пространство заполненное газами (над анодом — хлор, над катодом — водород), М — диафрагма
Схема старинного диафрагменного электролизера для получения хлора и щёлоков: А — анод, В — изоляторы, С — катод, D — пространство заполненное газами (над анодом — хлор, над катодом — водород), М — диафрагмаНаиболее простым из электрохимических методов в плане организации процесса и конструкционных материалов для электролизера является диафрагменный метод получения гидроксида натрия.
Раствор соли в диафрагменном электролизере непрерывно подаётся в анодное пространство и протекает через, как правило, нанесённую на стальную катодную сетку асбестовую диафрагму, в которую иногда добавляют небольшое количество полимерных волокон.
Во многих конструкциях электролизеров катод полностью погружен под слой анолита (электролита из анодного пространства), а выделяющийся на катодной сетке водород отводится из под катода при помощи газоотводных труб, не проникая через диафрагму в анодное пространство благодаря противотоку.
Противоток — очень важная особенность устройства диафрагменного электролизера. Именно благодаря противоточному потоку, направленному из анодного пространства в катодное через пористую диафрагму, становится возможным раздельное получение щёлоков и хлора. Противоточный поток рассчитывается так, чтобы противодействовать диффузии и миграции OH— ионов в анодное пространство. Если величина противотока недостаточна, тогда в анодном пространстве в больших количествах начинает образовываться гипохлорит-ион (ClO—), который затем может окисляться на аноде до хлорат-иона ClO3—. Образование хлорат-иона серьёзно снижает выход по току хлора и является основным побочным процессом в этом методе получения гидроксида натрия. Также вредит и выделение кислорода, которое, к тому же, ведёт к разрушению анодов и, если они из углеродных материалов, попаданию в хлор примесей фосгена.
- Анод:
- 2Cl−→Cl2+2e−{\displaystyle {\mathsf {2Cl^{-}\!\rightarrow Cl_{2}\!+2e^{-}}}} — основной процесс
- 2h3O→O2+4H++4e−{\displaystyle {\mathsf {2H_{2}O\rightarrow O_{2}+4H^{+}\!+4e^{-}}}}
- 6ClO3−+3h3O→2ClO3−+4Cl−+1.5O2↑+ 6H++6e−{\displaystyle {\mathsf {6ClO_{3}^{-}\!+3H_{2}O\rightarrow 2ClO_{3}^{-}+4Cl^{-}\!+1.5O_{2}\!\uparrow \!+\ 6H^{+}\!+6e^{-}}}}
- Катод:
- 2h3O+2e−→h3↑+2OH−{\displaystyle {\mathsf {2H_{2}O+2e^{-}\!\rightarrow H_{2}\!\uparrow +2OH^{-}}}} — основной процесс
- ClO−+h3O+2e−→Cl−+2OH−{\displaystyle {\mathsf {ClO^{-}+H_{2}O+2e^{-}\!\rightarrow Cl^{-}+2OH^{-}}}}
- ClO3−+3h3O+6e−→Cl−+6OH−{\displaystyle {\mathsf {ClO_{3}^{-}+3H_{2}O+6e^{-}\!\rightarrow Cl^{-}+6OH^{-}}}}
В качестве анода в диафрагменных электролизерах может использоваться графитовый или угольный электроды. На сегодня их, в основном, заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые.
На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до товарной концентрации 42—50 % масс. в соответствии со стандартом.
Поваренная соль, сульфат натрия и другие примеси при повышении их концентрации в растворе выше их предела растворимости выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или продолжают стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией.
Обратную, то есть кристаллизовавшуюся в осадок, поваренную соль возвращают назад в процесс, приготавливая из неё так называемый обратный рассол. От неё, во избежание накапливания примесей в растворах, перед приготовлением обратного рассола отделяют примеси.
Убыль анолита восполняют добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов, минеральных рассолов типа бишофита, предварительно очищенного от примесей или растворением галита. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния.
Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Благодаря относительной простоте и дешевизне диафрагменный метод получения гидроксида натрия до сих пор широко используется в промышленности.
Мембранный метод[править | править код]
Мембранный метод производства гидроксида натрия наиболее энергоэффективен, однако сложен в организации и эксплуатации.
С точки зрения электрохимических процессов мембранный метод подобен диафрагменному, но анодное и катодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Благодаря этому свойству становится возможным получение более чистых, чем в случае с диафрагменного метода, щелоков. Поэтому в мембранном электролизере, в отличие от диафрагменного, не один поток, а два.
В анодное пространство поступает, как и в диафрагменном методе, поток раствора соли. А в катодное — деионизированная вода. Из анодного пространства вытекает поток обеднённого анолита, содержащего также примеси гипохлорит- и хлорат-ионов и хлор, а из катодного — щёлока и водород, практически не содержащие примесей и близкие к товарной концентрации, что уменьшает затраты энергии на их упаривание и очистку.
Щёлочь, получаемая с помощью мембранного электролиза, практически не уступает по качеству получаемой при помощи метода с использованием ртутного катода и постепенно заменяет щёлочь, получаемую ртутным методом.
Однако, питающий раствор соли (как свежий, так и оборотный) и вода предварительно максимально очищается от любых примесей. Такая тщательная очистка объясняется высокой стоимостью полимерных катионообменных мембран и их уязвимостью к примесям в питающем растворе.
Кроме того, ограниченная геометрическая форма а также низкая механическая прочность и термическая стойкость ионообменных мембран во многом определяют сравнительно сложные конструкции установок мембранного электролиза. По той же причине мембранные установки требуют наиболее сложных систем автоматического контроля и управления.
- Схема мембранного электролизера.
Ртутный метод с жидким катодом[править | править код]
Натриевая соль пропилового эфира пара-оксибензойной кислоты — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 июня 2016; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 июня 2016; проверки требует 1 правка.Натриевая соль пропилового эфира пара-оксибензойной кислоты (англ. Sodium propyl para-oxybenzoate) — пищевая добавка, запрещенная к применению в пищевой промышленности в России[1]. На текущий момент используется в косметических средствах на водной основе (кремы, лосьоны, шампуни и т. д.)
В Е-кодах данная добавка обозначается как E217[2].
Внешне данная добавка выглядит как белый порошок с лёгким анестезирующим действием на язык.[3]
Данная добавка относится к категории консервантов[4]. Консерванты — вещества, угнетающие рост микроорганизмов в продукте. При этом, как правило, предупреждают продукт от появления неприятного вкуса и запаха, плесневения и образования токсинов микробного происхождения. Они бывают как натуральными так и синтетическими.
До некоторого времени данная добавка использовалась в производстве мясных продуктов, в том числе бульонов, паштетов, а также желе и конфет с начинкой.[5]. C 22 февраля 2005 года постановлением Роспотребнадзора от 18.01.2005 г. ввоз продуктов с использованием в их производстве данной добавки запрещён, а с 1 марта 2005 года её использование запрещено в пищевой промышленности России.[6]
Добавка Е217 может вызывать головные боли, расстройство кишечника, раковые опухоли, гиперактивность у детей и др. Консервант Е217 противопоказан астматикам, гипотоникам и аллергикам. Кроме того, добавка Е217 отрицательно влияет на нервно-сосудистую систему.[7]
Ю. А. Александров. Описание // Основы производства безопасной и экологически чистой животноводческой продукции. Учебное пособие. — Аграрно-технологический институт, 2008. — Т. 1. — С. 224. — 303 с. — ISBN 978-5-94808-388-9.
Перхлорат натрия — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 июня 2018; проверки требуют 3 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 июня 2018; проверки требуют 3 правки.| Перхлорат натрия | |||
|---|---|---|---|
| |||
| Систематическое наименование | Перхлорат натрия, натрий хлорнокислый | ||
| Сокращения | ПХН | ||
| Хим. формула | NaClO4 | ||
| Молярная масса | 122,45 г/моль | ||
| Плотность | безводная соль: 2,4994 г/см3 моногидрат: 2,02 г/см³ | ||
| Температура | |||
| • плавления | моногидрат: 130 °C | ||
| • разложения | безводная соль: 468 °C | ||
| Растворимость | |||
| • в воде | 21125; 330100 г/100 мл | ||
| Показатель преломления | 1,4617 (nD) | ||
| Рег. номер CAS | 7601-89-0 | ||
| PubChem | 522606 | ||
| Рег. номер EINECS | 231-511-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | SC9800000 | ||
| ChEBI | 132103 | ||
| Номер ООН | 1502 | ||
| ChemSpider | 22668 | ||
| NFPA 704 |  | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |||
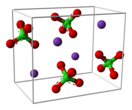
Перхлора́т на́трия (также, ПХН) — химическое соединение NaClO4, натриевая соль хлорной кислоты. Сильный окислитель. При кристаллизации из водных растворов при температурах выше 51 градуса Цельсия выпадает безводная соль, ниже 51 градуса Цельсия моногидрат NaClO4·H2O, ниже −13 градусов — дигидрат. Как безводная соль, так и кристаллогидраты очень гигроскопичны, поэтому перхлорат натрия в основном используется как сырьё для получения других перхлоратов обменными реакциями.
Бесцветное кристаллическое вещество с орторомбической структурой. Молекулярная масса 122,45 а. е. м.. Очень хорошо растворим в воде — более 209,6 г на 100 г воды при 25 градусах Цельсия[1]. Хорошо растворим также в этиловом спирте.
При нагревании до 482 °С разлагается.
Перхлорат натрия как окислитель может взаимодействовать с широким кругом горючих веществ, например, с глюкозой:
- 3NaClO4+C6h22O6→6CO2+6h3O+3NaCl{\displaystyle {\mathsf {3NaClO_{4}+C_{6}H_{12}O_{6}\rightarrow 6CO_{2}+6H_{2}O+3NaCl}}}
Перхлорат натрия может быть получен несколькими различными способами, в том числе:
- 4NaClO3→400−500oC3NaClO4+NaCl{\displaystyle {\mathsf {4NaClO_{3}{\xrightarrow[{}]{400-500^{o}C}}3NaClO_{4}+NaCl}}}
- Электролитическое окисление хлората натрия на платиновом аноде.
- Реакцией между хлорной кислотой и гидроксидом или карбонатом натрия.
В промышленности сейчас используется почти исключительно второй метод.
Ранее перхлорат натрия использовался, как гербицид. Даже небольшая его примесь в чилийской селитре вызывала гибель пшеницы и некоторых других культурных растений. Сейчас перхлорат натрия самостоятельного применения практически не находит, но его отличная растворимость в воде позволяет из него получать перхлораты любых металлов, аммония:
- NaClO4+Nh5Cl→Nh5ClO4+NaCl{\displaystyle {\mathsf {NaClO_{4}+NH_{4}Cl\rightarrow NH_{4}ClO_{4}+NaCl}}}
Кроме того, воздействуя на перхлорат натрия серной кислотой, можно получить свободную хлорную кислоту.
- NaClO4+h3SO4→NaHSO4+HClO4{\displaystyle {\mathsf {NaClO_{4}+H_{2}SO_{4}\rightarrow NaHSO_{4}+HClO_{4}}}}
Сведения о токсичности перхлората натрия для животных противоречивы. В то же время, очевидно, что в силу большей стабильности тетраэдрического аниона перхлораты менее токсичны, чем хлораты, хлориты и гипохлориты. Однако при попадании внутрь организма перхлорат натрия сильно нарушает натрий-калиевый баланс, так как перхлорат калия почти нерастворим в воде (и в биологических жидкостях) при обычных температурах.
У грызунов (крыс, мышей, морских свинок) перхлорат натрия вызывает увеличение рефлекторной возбудимости, судороги и столбняк, часто с опистотонусом. Эти симптомы наблюдались в течение 10 минут после подкожного введения крысам 0,1 г перхлората натрия, а после введения 0,22 г крысы погибали через 10 часов.






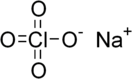
 (
(