как их классифицируют по свойствам, строение
Общее понятие об углеводах
Углеводы — класс органических соединений, к которому относятся глюкоза, фруктоза, сахароза, а также полисахариды (крахмал, целлюлоза, пектины). С точки зрения биологии и биохимии — это биологически активные вещества, содержащиеся в 80% живых клеток растений и необходимые человеку для функционирования. С точки зрения химии — соединения, состоящие из нескольких карбонильных и гидроксильных групп.
Фруктоза была впервые выделена из «медовой воды» в 1792 году, глюкозу открыли чуть позже, в 1802 году. Химия полисахаридов получила развитие после того, как в 1811 году впервые был осуществлен гидролиз крахмала.
Химическое строение
Все углеводы отвечают единой химической характеристике: они состоят только из углерода, кислорода и водорода, при этом соотношение атомов водорода и кислорода в них такое же, как в молекулах воды.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Простые углеводы, моносахариды — органические соединения, содержащие в своей структуре гидроксильные и карбонильные группы: альдегидоспирты, кетоспирты.
Сложные углеводы — это дисахариды с двумя моносахаридными фрагментами и полисахариды, в молекулах которых таких фрагментов больше двух. Поскольку многие из них на вкус сладкие, этот класс веществ называют еще и сахарами. Кроме классификации по количеству структурных единиц, существует классификация по числу атомов углерода в молекуле.
Молекулы моносахаридов состоят из нескольких гидроксильных групп и одной карбонильной. Самый известный моносахарид — глюкоза. Название происходит от греческого слова «гликис», «сладкий». Глюкоза принадлежит к классу альдегидоспиртов. Особенность строения глюкозы в том, что она существует в виде двух оптических изомеров, молекулы которых зеркально отображают друг друга: D- и L-форма.
Подобно глюкозе, изомерная ей фруктоза легко образует циклические полуацетали, только состоят они преимущественно из пятичленных циклов. Крахмал, образующийся из глюкозы — энергетический резерв растений, быстро перерабатывающийся в легко усваиваемый моносахарид. В состав крахмала входят амилоза и амилопектин.
Крахмал, образующийся из глюкозы — энергетический резерв растений, быстро перерабатывающийся в легко усваиваемый моносахарид. В состав крахмала входят амилоза и амилопектин.
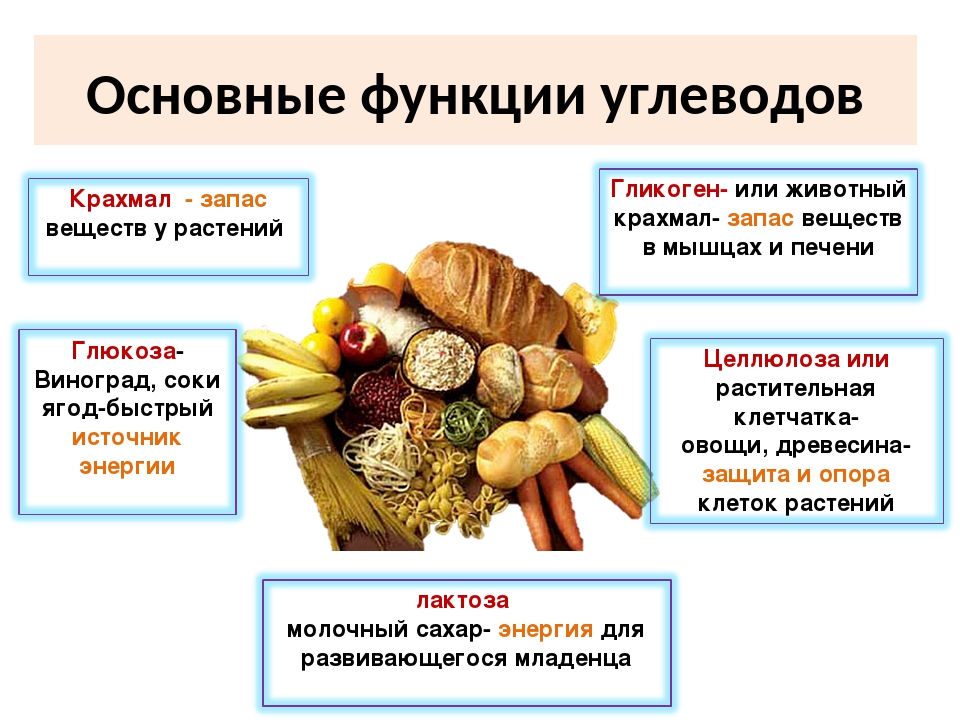
Функции углеводов в организме человека
Попадая в организм, дисахариды(например, сахароза и лактоза) и полисахариды (крахмал и проч.) под действием специальных ферментов гидролизуются с образованием глюкозы и фруктозы. Организм перерабатывает глюкозу и фруктозу, превращая их в углекислоту и воду, и таким образом получает энергию для всех идущих в нем процессов.
Классификация по свойствам
Строительная функция углеводов
Мукополисахариды, соединения углеводов с белками, являются важной составляющей суставной смазки у животных и человека. Рибоза и дезоксирибоза входят в состав РНК и ДНК.
Энергетическая функция углеводов
В организме любого животного должно постоянно содержаться определенное количество глюкозы: например, в крови человека — около 15 граммов.
Структурная функция углеводов
Часть углеводов является структурными элементами клеток и входит в состав многих сложных молекул: гормонов, ферментов, иммунных веществ. Например, гликопротеины на поверхности клеток способствуют избирательности межклеточного взаимодействия и обеспечивают иммунный ответ. Гепарин служит ингибитором свертывания крови и предотвращает возникновение тромбов.
Регуляторная функция углеводов
Клетчатка, содержащаяся в овощах и фруктах, перерабатывается только полезной микрофлорой кишечника и в процессе стимулирует его стенки, улучшая перистальтику. Кроме того, углеводы регулируют осмотическое давление крови, которое зависит от количества содержащейся в ней глюкозы.
Запасающая функция
Когда организм получает углеводы вдоволь, их избыток может откладываться. Хранить глюкозу в чистом виде живым организмам довольно обременительно: ее не слишком большие молекулы легко покидают клетки. Поэтому живые организмы составляют новые соединения из молекул глюкозы: растения запасают углеводы в виде крахмала, а животные и грибы — в виде более легко растворимого гликогена. Запасы гликогена в человеческом организме, как правило, невелики — 150–200 граммов. Основное место складирования — печень. Если углеводов в пище недостаточно или они плохо усваиваются, начинается расщепление гликогена. Так временно восполняется дефицит. Когда запасы гликогена истощаются, материалом для синтеза глюкозы становятся жиры и белки.
4. Состав, свойства и функции углеводов
Углеводы — это природные органические соединения, содержащиеся во всех клетках живых организмов и выполняющие важные функции.
Состав и классификация углеводов
Молекулы углеводов состоят из атомов трёх элементов — углерода, водорода и кислорода. Состав большинства углеводов можно выразить формулой: Cn(h3O)m. В состав производных углеводов могут входить и другие элементы. Так, в хитине содержатся ещё и атомы азота.
Состав большинства углеводов можно выразить формулой: Cn(h3O)m. В состав производных углеводов могут входить и другие элементы. Так, в хитине содержатся ещё и атомы азота.
Углеводы делят на три класса.
Рис. \(1\). Классификация углеводов
Самое простое строение имеют моносахариды. Наиболее распространённый моносахарид — это глюкоза.
Рис. \(2\). Модель молекулы глюкозы
Глюкоза является главным источником энергии в клетках всех живых организмов.
Фруктоза содержится в мёде, ягодах и фруктах.
Рибоза входит в состав важных химических соединений — РНК, АТФ, некоторых ферментов.
Дезоксирибоза — компонент молекул ДНК.
Все моносахариды — это сладкие на вкус кристаллические вещества, хорошо растворимые в воде.
Олигосахариды
Олигосахариды содержат в молекулах от двух до десяти остатков моносахаридов. Молекулы дисахаридов образуются в результате соединения двух молекул моносахаридов. По свойствам они похожи на моносахариды: хорошо растворяются в воде, сладкие на вкус.
Сахароза состоит из остатков глюкозы и фруктозы. В растениях это вещество является растворимым запасным углеводом, а также продуктом фотосинтеза, который транспортируется от листьев к другим органам. Знакома всем как сахар (свекловичный или тростниковый).
Лактоза (молочный сахар) образована молекулами глюкозы и галактозы. Содержится в молоке.
Мальтоза (солодовый сахар) состоит из глюкозы. Образуется из крахмала при прорастании семян, является источником энергии для процесса прорастания.
Полисахариды
Молекулы полисахаридов состоят из большого числа остатков моносахаридов. Эти вещества не имеют вкуса и не растворяются в воде.
Эти вещества не имеют вкуса и не растворяются в воде.
Крахмал — запасной углевод растений. Его молекулы образованы остатками глюкозы, соединёнными в линейные или разветвлённые цепи.
Целлюлоза входит в состав клеточных стенок грибов и растений и придаёт им прочность. Молекулы целлюлозы тоже образованы остатками глюкозы, но они намного длиннее молекул крахмала. Целлюлоза не растворяется в воде и других растворителях.
Гликоген похож по строению на крахмал. Это запасной углевод у животных.
Хитин похож по строению на целлюлозу, но отличается наличием в его молекулах атомов азота.
Функции углеводов
1. Энергетическая функция углеводов заключается в том, что под влиянием ферментов происходит их расщепление и окисление с выделением энергии. Важно, что углеводы могут расщепляться как в присутствии кислорода, так и без него. Продуктами полного окисления этих веществ являются углекислый газ и вода.
Продуктами полного окисления этих веществ являются углекислый газ и вода.
2. Запасающая функция проявляется в накоплении излишков углеводов в клетках: у растений — крахмала, у животных и грибов — гликогена. При необходимости запасные углеводы расщепляются до глюкозы и используются клеткой для получения энергии.
3. Строительная функция заключается в том, что углеводы служат строительным материалом: целлюлоза входит в состав клеточных стенок растений, а хитин образует клеточные стенки грибов и кутикулу членистоногих. Эти же углеводы выполняют защитную функцию.
4. Сигнальная (рецепторная) функция состоит в том, что гликопротеины (комплексные соединения углеводов и белков), расположенные на поверхности клетки, воспринимают и передают в клетку сигналы из внешней среды.
Источники:
Рис. 1. Классификация углеводов. © ЯКласс.
Рис. 2. Модель молекулы глюкозы. https://image. shutterstock.com/image-illustration/molecule-glucose-isolated-on-white-600w-570551413
shutterstock.com/image-illustration/molecule-glucose-isolated-on-white-600w-570551413
Функции углеводов
Углеводы
Функции углеводов
- Являются источником углерода
- Обеспечивают до 70% потребности организма в энергии
- Резервная функция
- Структурная
- Защитная
- Спецефическая функция углеводов – участие в образовании гибридных (комплексных) молекул, а именно гликопротеинов и гликолипидов
- По числу углеродных атомов, входящих в состав молекулы (триозы, тетрозы, пентозы и т.д.
- По характеру карбонильной группы (кетозы и альдозы)
- По наличию других (кроме карбонильной и гидроксильной) функциональных групп:
— Нейтральные сахара
— аминосахара
— кислые сахара
Классификация углеводов
- Моносахариды, или простые сахара, содержат только одну структурную единицу;
- Олигосахариды – углеводы, состоящие из нескольких остатков (2-10) моносахаридов;
- Полисахариды – высокомолекулярные вещества, состоящие из остатков моносахаридов со степенью полимеризации выше 10.

Классификация моносахаридов
D-ряд альдомоносахаридов
All altruists gladly make gum in gallon tanks
D-Allose
D-Altrose
D-Glucose
D-Mannose
D-Gulose
D-Idose
D-Galactose
D-Talose
Циклические формы углеводов
H
OH
Мутаротация
Циклические формы углеводов
Проекционные формулы Хеуорса
Конформационные формулы гексоз
Производные моносахаридов
- Альдиты (сахарные спирты)
- Кислые сахара
- Гликозиды
- Простые и сложные эфиры моносахаридов
Химические свойства моносахаридов
Реакция полуацетального гидроксила
Синтез гликозидов по Фишеру
Синтез гликозидов через гликозилгалогениды
Расщепление гликозидов
Аномеризация гликозидов
Синтез N-гликозидов
- Восстановление альдоз и кетоз
Реакции карбонильной группы
Окисление (получение альдоновых кислот)
Окисление (получение альдаровых кислот)
Окисление (восстановление реактивов Фелинга и Толленса)
Реакция с фенилгидразинами
Наращивание углеводородной цепи моносахаридов
(метод Килиани-Фишера)
Укорачивание цепи углеводов
(деградация по Руффу)
Укорачивание цепи углеводов
(метод Воля)
Реакции с участием гидроксильных групп
Взаимодействие с ионами Сu++
Дегидратация пентоз
Реакции с участием полуацетального звена
1.
2. Исчерпывающее алкилирование
3. Ацилирование
Расщепление действием HIO4
2.3.2. Органические вещества клетки. Углеводы, липиды.
2.3.2. Органические вещества клетки. Углеводы, липиды.
Углеводы.Общая формула Сn (h3O)n: углеводы содержат в своем составе только три химических элемента.
Таблица. Сравнение классов углеводов.
Растворимые в воде углеводы.
Моносахариды:
глюкоза – основной источник энергии для клеточного дыхания;
фруктоза – составная часть нектара цветов и фруктовых соков;
рибоза и дезоксирибоза – структурные элементы нуклеотидов, являющихся мономерами РНК и ДНК.
Дисахариды:
сахароза (глюкоза + фруктоза) – основной продукт фотосинтеза, транспортируемый в растениях;
лактоза (глюкоза + галактоза) – входит в состав молока млекопитающих;
мальтоза (глюкоза + глюкоза) – источник энергии в прорастающих семенах.
Функции растворимых углеводов:
- транспортная,
- защитная,
- сигнальная,
- энергетическая.
полимерные:
крахмал,
гликоген,
целлюлоза,
хитин.
Функции полимерных углеводов:
- структурная,
- запасающая,
- энергетическая,
- защитная.
Крахмал состоит из разветвленных спирализованных молекул, образующих запасные вещества в тканях растений.
Целлюлоза – полимер, образованный остатками глюкозы, состоящими из нескольких прямых параллельных цепей, соединенных водородными связями. Такая структура препятствует проникновению воды и обеспечивает устойчивость целлюлозных оболочек растительных клеток.
Хитин состоит из аминопроизводных глюкозы. Основной структурный элемент покровов членистоногих и клеточных стенок грибов.
Гликоген – запасное вещество животной клетки.
Таблица. Наиболее распространенные углеводы.
Таблиица.Основные функции углеводов.
Липиды.
Липиды – сложные эфиры жирных кислот и глицерина. Нерастворимы в воде, но растворимы в неполярных растворителях. Присутствуют во всех клетках. Липиды состоят из атомов водорода, кислорода и углерода.
Функции липидов:Запасающая – жиры, откладываются в запас в тканях позвоночных животных.
Энергетическая – половина энергии, потребляемой клетками позвоночных животных в состоянии покоя, образуется в результате окисления жиров. Жиры используются и как источник воды. Энергетический эффект от расщепления 1 г жира – 39 кДж, что в два раза больше энергетического эффекта от расщепления 1 г глюкозы или белка.
Защитная – подкожный жировой слой защищает организм от механических повреждений.
Структурная – фосфолипиды входят в состав клеточных мембран.
Теплоизоляционная – подкожный жир помогает сохранить тепло.
Электроизоляционная – миелин, выделяемый клетками Шванна (образуют оболочки нервных волокон), изолирует некоторые нейроны, что во много раз ускоряет передачу нервных импульсов.
Питательная – некоторые липидоподобные вещества способствуют наращиванию мышечной массы, поддержанию тонуса организма.
Смазывающая – воски покрывают кожу, шерсть, перья и предохраняют их от воды. Восковым налетом покрыты листья многих растений, воск используется в строительстве пчелиных сот.
Гормональная – гормон надпочечников – кортизон и половые гормоны имеют липидную природу.
Таблица. Основные функции липидов.
ТЕМАТИЧЕСКИЕ ЗАДАНИЯ
Часть А
А1. Мономером полисахаридов может быть:
1) аминокислота
2) глюкоза
3) нуклеотид
4) целлюлоза
А2. В клетках животных запасным углеводом является:
1) целлюлоза
2) крахмал
3) хитин
4) гликоген
А3. Больше всего энергии выделится при расщеплении:
1) 10 г белка
2) 10 г глюкозы
3) 10 г жира
4) 10 г аминокислоты
А4. Какую из функций липиды не выполняют?
1) энергетическую
2)каталитическую
3) изоляционную
4) запасающую
А5. Липиды можно растворить в:
Липиды можно растворить в:
1) воде
2) растворе поваренной соли
3) соляной кислоте
4) ацетоне
Часть В
В1. Выберите особенности строения углеводов
1) состоят из остатков аминокислот
2) состоят из остатков глюкозы
3) состоят из атомов водорода, углерода и кислорода
4) некоторые молекулы имеют разветвленную структуру
5) состоят из остатков жирных кислот и глицерина
6) состоят из нуклеотидов
В2. Выберите функции, которые углеводы выполняют в организме
1) каталитическая
2) транспортная
3) сигнальная
4)строительная
5) защитная
6) энергетическая
ВЗ. Выберите функции, которые липиды выполняют в клетке
1) структурная
2) энергетическая
3) запасающая
4) ферментативная
5) сигнальная
6) транспортная
В4. Соотнесите группу химических соединений с их ролью в клетке:
|
РОЛЬ СОЕДИНЕНИЯ В КЛЕТКЕ |
СОЕДИНЕНИЕ |
|
|
|
Часть С
С1. Почему в организме не накапливается глюкоза, а накапливается крахмал и гликоген?
Почему в организме не накапливается глюкоза, а накапливается крахмал и гликоген?
Биоорганические соединения – углеводы — Документ
Оглавление.
Введение. 1
Биоорганические соединения – углеводы, белки и липиды. 2
Углеводы. 2
Функции углеводов. 3
Строение моносахаридов. 6
Химические свойства моносахаридов. 8
Дисахариды. 9
Полисахариды. 10
Белки. 12
Функции белков и пептидов. 13
Аминокислоты. 15
Аминокислоты, входящие в состав белков. 16
Получение аминокислот. 17
Химические свойства. 17
Липиды. 19
Функции липидов. 22
Физические свойства жиров. 24
Химические свойства жиров. 24
Описание задач практикума. 26
Тема углеводы. 26
1.
Восстанавливающие свойства моно- и
дисахаридов.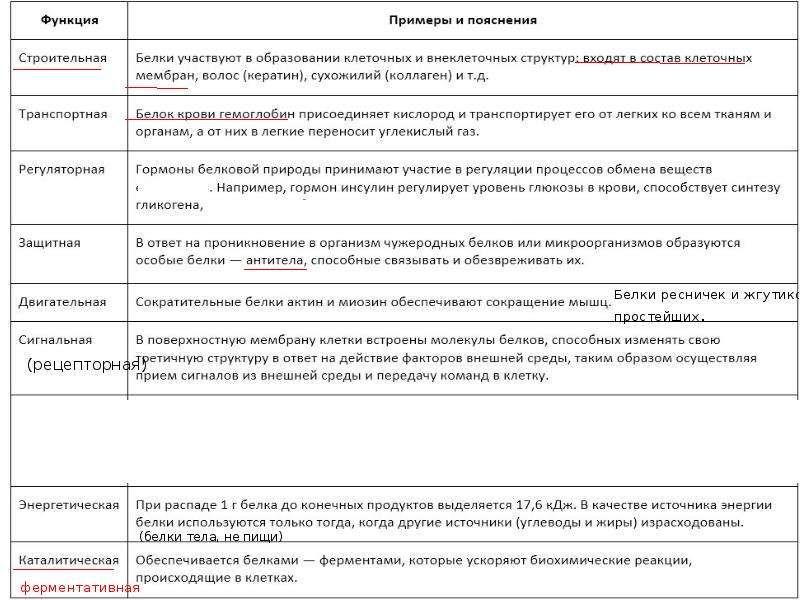 26
26
2. Ферментативный гидролиз крахмала. 26
3. Действие аммиачного раствора оксида серебра на глюкозу. 27
Данный опыт покажет вам одну из самых красивых реакций — реакцию серебряного зеркала. (так же качественная реакция). 27
5. Действие гидроксида меди(II) на глюкозу. 27
Данный эксперимент продемонстрирует реакцию медного зеркала. 27
Тема белки. 27
Цветные и качественные реакции на аминокислоты и белки. 27
Тема липиды. 27
Растворимость жиров. 27
Заключение. 28
28
Список литературы: 28
Введение.
Естественные науки, такие как
биохимия, невозможно изучать без
экспериментов. Поэтому в наше время
очень актуально представлять учащимся
не только теоретический материал, но и
практический. Без сомнений, теоретический
материал в учебных пособиях по биохимии
представлен очень хорошо, однако
практикум представлен очень скудно. Те
эксперименты, которые включены в него,
зачастую не получаются. Возможно, это
связано с неточностями в описании
экспериментов. Поэтому нужно составить
такой практикум, где эксперименты давали
бы положительные результаты.
Те
эксперименты, которые включены в него,
зачастую не получаются. Возможно, это
связано с неточностями в описании
экспериментов. Поэтому нужно составить
такой практикум, где эксперименты давали
бы положительные результаты.
Таким образом, Ццелью моей работы является составление практикума по биохимии.
В качестве практикума для анализа мной был выбран практикум по биологии
для 10 – 11 класса профильного уровня: Практикум для учащихся 10 – 11 классов по биологии «Профильный уровень» Г.М.Дымшиц, О.В. Саблина.
В процессе работы мной были поставлены следующие задачи:
1.Отобрать теоретический материал по определенным критериям.
Освоить программу по написанию химических формул ChemWindow
2. Написать текст, адаптированный для учащихся 10 класса теоретический материал.

Подобрать эксперименты.
3. Проделать опытыэксперименты и заснять их на камеру. – сделать видео, которое наглядно будет показывать учащимся порядок проведения опытов.
Сделать видео с помощью программы Windows Move Maker, которое наглядно будет показывать учащимся порядок проведения опытов.
Зачем делать видео к практикуму?
Для того, чтобы наглядно показать учащимся свойства определенного вещества,
Может служить пособием по проведению опыта.
В качестве контроля усвоения материала.
Отбор экспериментов проходил по следующим критериям: свойства органических веществ, качественные реакции, доступность реактивов и воспроизводимости экспериментов.
Биоорганические соединения – углеводы, белки и липиды.
Углеводы.
1Углеводы – органические вещества с общей формулой Сn(H2O)n, где n больше или равно 3, — служат источником энергии для животных и растительных клеток; во многих растениях они образуют также составные части клеток, клеточные оболочки и служат опорными элементами для всей клетки или растения. Растения обладают способностью синтезировать самые разнообразные углеводы из двуокиси углерода и воды в присутствии света. Углеводы являются основой для синтеза остальных органических веществ. В животных тканях число различных углеводов значительно меньше; к наиболее важным из этих относятся глюкоза, галактоза, гликоген и их полимеры.
свет
реакция фотосинтеза.
Функции углеводов.
2ФУНКЦИЯ | УРОВЕНЬ ОРГАНИЗАЦИИ | ПРИМЕРЫ |
Составная часть жизненно важных веществ клетки. | молекулярный | 1.Входит в состав носителей генетической информации – нуклеиновых кислот: рибоза – в состав РНК, дезоксирибоза – в состав ДНК. 2. Рибоза входит в состав основного носителя энергии клетки – АТФ. 3. Рибоза входит в состав акцепторов водорода – ФАД, НАД и НАДФ. |
Участие в фиксации углерода. | Клеточный | Пентоза рибулозодифосфат является непосредственным акцептором углекислого газа в темновой фазе фотосинтеза. |
Энергетическая. | Клеточный | Глюкоза является одним из наиболее распространенных дыхательных субстратов, т.е. источников получения энергии. |
Резервная | Организменный | 1. Крахмал является наиболее распространенным запасным веществом у растений. 2. Водорастворимые углеводы (сахароза, глюкоза, фруктоза) запасаются в клеточном соке растений. 3. У животных, прокариот и грибов. Резервным полисахаридом является гликоген. 4. Редуценты и симбиотическая микрофлора кишечника используют целлюлозу, так как они имеют специфические ферменты, гидролизирующие ее до глюкозы. |
Структурная. | Клеточный | 1. Целлюлоза составляет основную массу клеточных стенок бактерий и растительных клеток. 2. Хитин образует клеточные стенки грибов. |
Тканевый | 1. Углеводные компоненты гликокаликса обеспечивают узнавание клетками друг друга. Благодаря этому происходит ряд процессов: сперматозоиды опознают яйцеклетку своего биологического вида; клетки одного типа удерживаются вместе, образуя ткани; оттаргаются несовместимые органы при трансплантации. 2. Углеводные компоненты придают специфичность групповым веществам крови. 3. Гликокаликс микроворсинок кишечного эпителия является носителем ферментов пристеночного пищеварения. 4. Гепарин (производное полисахаридов препядствует свертыванию крови). | |
Организменный | 1. Хитин образует покровы тела членистоногих. 2. Муреин образует опору клеточной стенки бактерий – клеточный мешок. | |
Защитная | Тканевый | 1. Углеводные компоненты гликокаликса являются рецепторами тканевой совместимости, а также выполняют рецепторную функцию при фагоцитозе. 2. Вязкие растворы полисахаридов выстилают полости дыхательного и пищеварительного трактов и защищают от механических повреждений ткани и органы. |
Организменный | 1. Камеди (производные моносахаридов), выделяющиеся в местах повреждения стволов и ветвей, защищают деревья и кустарники от проникновения инфекции через раны. 2. Слизи (полисахариды) разбухают во влажной среде и тем самым защищают от пересыхания зародыши прорастающих семян. 3. Твердые клеточные стенки одноклеточных организмов или хитиновый покров членистоногих защищают от неблагоприятных воздействий внешней среды. |
Строение и свойства углеводов.
Можно схему!Углеводы, имеющие биологическое значение, делятся на три класса: моносахариды, дисахариды и полисахариды. Моно- и дисахариды, обычно называемые сахарами, легко растворимы в воде, могут кристаллизироваться и легко проходят через мембраны. В отличие от них полисахариды не кристаллизируются и не проходят через мембраны.
Моносахариды – такие углеводы, которые не могут гидролизоваться с образованием более простых углеводов
Моносахариды представляют собой простые сахара с формулой Сn(H2O)m. В зависимости от числа углеродных атомов в их молекуле различают триозы, пентозы, гексозы, гептозы. В природе наиболее распространены пентозы (рибоза и дезоксирибоза) и гексозы (глюкоза, фруктоза).
Все моносахариды разделяют на альдозы и кетозы в зависимости от того, имеются ли в молекуле моносахарида альдегидная или кетонная группа. Простейший моносахарид – глицериновый альдегид (С3H6O3):
глицериновый альдегид.
Остальные моносахариды делят на группы по числу атомов кислорода (обычно это число равно числу атомов углерода): тетрозы (С4H8O4), пентозы (С5H10O5) и гексозы (С6H12O6).
Строение моносахаридов.Глюкоза и фруктоза являются изомерами – их строение различно, но молекулярные формулы совпадают – С6H12O6.
Глюкоза Фруктоза
Рибоза Дезоксирибоза
Сахара могут также существовать и в виде циклов. Сахара с шестичленными циклами называю пиранозными, а сахара с пятичленным циклом называют фуранозными.
Фуранозный цикл Пиранозный цикл.
β – Глюкоза. α – Глюкоза.
Рибоза. Дезоксирибоза.
Названия моносахаридов содержат греческие названия числа атомов кислорода (углерода) и окончание –оза (тетроза, пентоза, гексоза).
Наличие альдегидной группы обозначают прибавлением приставки альдо- (глюкоза – альдогексоза), наличие кетонной группы выражается наличием приставки кето – (фруктоза – кетогексоза).
Изомерия моносахаридов обусловлена наличием:
Альдегидной или кетонной группы (структурная изомерия)
Асимметричностью атома углерода(одного или нескольких), следовательно, оптическая изомерия.
Пространственная изомерия.
Количество изомеров у сахаров очень велико.
Моносахариды выделяют из природных объектов. Глюкозу чаще всего получают гидролизом крахмала в присутствии серной кислоты.
nC6H12O6 → (C6H10O5)n + nH2O
Кроме того многие моносахарид встречаются в природе в свободном виде, например мед – смесь фруктозы и глюкозы.
Химические свойства моносахаридов.
Химические свойства моносахаридов определяются наличием в их молекулах гидроксильных групп и карбонильной группы.
Реакции альдегидной группы:
Восстановление альдегидной группы приводит к образованию шестиатомного спирта (сорбита):
Окисление мягкими окислителями (хлорная или бромная вода) приводит к образованию одноосновной кислоты (окисляется только альдегидная группа). Сильные окислители превращают в СOOH группу не только альдегидную, но и первичную спиртовую группу с образованием двухосновной кислоты.
Как и все альдегиды, глюкоза вступает в реакцию серебряного зеркала.
НОСН2(СНОН)4СHO + 2 [Ag(NH3)2]OH => НОСН2(CHОН)4СООH + 2 Ag + 3NH3 + H2O
Реакции гидроксильных групп.1). Глюкоза может образовывать сложные эфиры – ациклирование глюкозы.
2). Качественные реакции с гидроксидом меди (II).
Реакции брожения.
Брожением называют процесс, при котором происходит расщипление моносахаридов некоторыми микроорганизмами. В зависимости от основных продуктов, получающихся при брожении, различают следующие виды брожения:
Спиртовое:
Молочнокислое:
Маслянокислое:
Дисахариды.
Олигосахариды – продукты конденсации нескольких (от 2 до 8, чаще всего – двух) молекул моносахаридов.
Дисахариды – это олигосахариды, молекулы которых состоят из двух циклических моносахаридных остатков (одинаковых или разных).
В зависимости от того, участвуют ли в создании связи между остатками моносахаридов два гликозидных гидроксила обоих моносахаридов, или один гидроксильный гликозил, различают две группы дисахаридов, отношение к окислителям которых различно: невосстанавливающиеся и восстанавливающиеся.
Примером сахарида первого типа является сахароза. Она не дает качественных реакций на альдегидную группу и способна вступать только в реакции характерные для гидроксильных групп.
сахароза
Пример сахарида второго типа – лактоза. В растворе молекулы этого типа могут переходить из циклической в альдегидную форму; отсюда и их восстановительные свойства: они дают реакцию «серебряного зеркала» и способны окисляться до монокарбоновых кислот.
Все дисахариды способны превращаться при гидролизе в моносахариды.
Сахароза глюкоза фруктоза
Дисахариды получают из природных источников, таких как сахарная свекла или сахарный тростник (получают сахарозу). Лактоза (молочный сахар) содержится в молоке.
Мальтоза.
Лактоза.
Полисахариды.
Полисахариды образуются путем соединения многих моносахаридов и имеют формулу (С6Н10О5)n. При гидролизе они дают молекулы простых сахаров. Набольшее биологическое значение имеют полисахариды крахмал и гликоген, являющиеся резервными веществами в клетках растений и животных соответственно, и целлюлоза –важнейший структурный элемент растительной клетки. Целлюлоза состоит из нескольких сотен молекул глюкозы. С увеличением числа мономеров растворимость сахаридов падает.
Крахмал – это природный полисахарид образованный остатками глюкозы. Крахмал образуется в растениях при фотосинтезе. Наиважнейшим из свойств крахмала является его гидролиз, конечным продуктом которого является глюкоза.
Крахмал не является индивидуальным веществом – это смесь полисахаридов амилопектина и амилозы, которые состоят из остатков глюкозы, соединенных гликозидными связями.
Крахмал.
Крахмал является основным источником углеводов в пище человека: в больших количествах крахмал содержится в хлебе, крупах и овощах.
Наиболее важным химическим свойством крахмала является его гидролиз, конечным продуктом которого является глюкоза.
Целлюлоза (клетчатка) – наиболее распространенный в растительном мире полисахарид. Из целлюлозы состоят клетки стенок растений. Молекулы целлюлозы в отличие от крахмала имеют только линейное строение, причем цепи расположены параллельно друг другу и соединены между собой множеством водородных связей – отсюда неспособность целлюлозы растворяться в воде.
n
Целлюлоза
Молекула целлюлозы состоит из остатков βb – глюкозы, связанных через первый и четвертичный атом углерода.
Целлюлоза способна образовывать сложные эфиры.
Гидролиз целлюлозы приводит к образованию глюкозы.
Сбраживание глюкозы приводит к образованию этилового спирта, который в этом случае называют гидролизным.
Хитин. По своей структуре и функции хитин очень близок к целлюлозе, это тоже структурный полисахарид. Хитин встречается у некоторых грибов, где он играет в клеточных стенках опорную роль благодаря своей волокнистой структуре, а также у некоторых групп животных (членистоногих) в качестве важного компонента их наружного скелета.
Гликоген – резервный полисахарид, основной запасной углевод у животных и человека. Он постоянно синтезируется организмом и накапливается во всех его тканях. Структура гликогена очень близка к структуре амилопектина – компонента крахмала. Оба из остатков состоят из остатков β a – глюкозы, соединенных между собой гликозидными связями двух типов: С(1) – О – (С)4 и (С)1 – O – (C)6. Гликоген отличается от амилопектина прежде всего своей молекулярной массой. Молекула гликогена отличается более плотной, компактной и глобулярной структурой.
Белки.
3Белки – обязательная составная часть всех клеток. В жизни органических соединений белки имеют первостепенное значение. В состав белка входят углерод, азот, водород, некоторые белки содержат еще и серу. Роль мономеров в белках играют аминокислоты. У каждой аминокислоты имеется карбоксильная группа (-COOH) и аминогруппа (-NH2). Наличие в одной молекуле кислотной и основной группы обуславливает их высокую реактивность. Между соединившимися кислотами возникает связь….., называемая пептидной, а образовавшееся соединение из нескольких аминокислот называется пептидом. Соединение из большого числа аминокислот называется полипептидом. В белках встречаетсяНаиболее распространены 20 аминокислот, отличающихся своим строением. Разные белки образуются в результате соединения аминокислот в разной последовательности. Огромное разнообразие живых существ в значительной степени определяется различиями в составе имеющихся у них белков.
В строении молекул белков различают 4 уровня организации.
Первичная структура – полипептидная цепь из аминокислот, связанных в определенной последовательности ковалентными пептидными связями.
Например, молекула инсулина состоит из 2- полимерных цепочек; одна цепочка состоит из 21 остатка, а вторая 30
Вторичная структура – полипептидная цепь, закрученная в виде спирали. В ней между соседними витками возникают мало прочные водородные связи. В комплексе они обеспечивают довольно прочную структуру.
Третичная структура представляет собой причудливую, но для каждого белка специфическую конфигурацию – глобулу. Она удерживается мало прочными гидрофобными связями или силами сцепления между полярными радикалами, которые встречаются у многих аминокислот. Благодаря их многочисленности они обеспечивают достаточную устойчивость белковой макромолекулы и ее подвижность. Третичная структура белков поддерживается также ковалентными S-S связями, возникающими между удаленными друг от друга радикалами серосодержащей аминокислоты – цистеина.
Благодаря соединению нескольких молекул белков между собой образуется четвертичная структура. Если пептидные цепи уложены виде клубка, то такие белки называются глобулярными. Если пептидные цепи уложены в пучки нитей, они носят название фибриллярных белков.
Нарушение природной структуры белка называют денатурацией. Она может возникать под действием температуры, химических веществ, радиации и т.д. Денатурация может быть как обратимой, так и необратимой.
Функции белков и пептидов.
4Функции. | Уровень организации. | Примеры. |
Структурная. | Доклеточный. | Составляет капсиды вирусов. |
Клеточный. | Обязательный компонент всех мембран клетки | |
Тканевый и органный. | Коллаген – компонент соединительной ткани и кожи. Кератин – компонент перьев, шерсти, волос, рогов, копыт, ногтей, когтей | |
Организменный. | Склеротин входит в состав покровов тела насекомых. | |
Транспортная. | Клеточный. | Участие в активном транспорте веществ через клеточные мембраны против градиента концентраций. Диффузия через клеточный мембраны. |
Организменный. | Гемоглобин переносит кислород и углекислый газ в крови позвоночных. Сывороточный альбумин переносит жирные кислоты. Различные глобулины переносят ионы металлов и гормонов. | |
Двигательная. | Клеточный. | Тубулины микротрубочек обеспечивают работу веретена деления клеток. Флагеллин обеспечивает движение жгутиков прокариот. |
Организменный. | Актин и миозин обеспечивают сокращение волокон поперечнополосатой мускулатуры, за счет чего совершается передвижение тела животных и человека | |
Рецепторная. | Тканевый. | Гликопротеины являются компонентами гликокаликса. Гликопротеины – антигены тканевой совместимости – ответственны за распознавание тканей. |
Организменный. | Опсин – составная часть светочувствительных пигментов родопсина и йодопсина, находящихся в клетке сетчатки глаза. | |
Защитная. | Клеточный. | Антитела связывают инородные белки, образуя с ними комплексы. Интерфероны – универсальные противовирусные белки |
Тканевый. | Тромбопластин, протромбин, тромбин и фибриноген предохраняют организм от кровопотери, образуя тромб. Антиоксидантные ферменты (каталаза), препятствует развитию свободно радикальных процессов, очень важных для организма | |
Организменный. | Кожа, в формировании которой принимают участие различные белки, защищает тело позвоночных. | |
Ферментативная. | Клеточный. | Большинство ферментов является белками. |
Пищевая. | Организменный. | Белки – основной источник аминокислот. Казеин молока- источник белка для детенышей млекопитающих и человека. |
Запасающая. | Органный. | Ферритин – запасает железо в печени, селезенке, яичном желтке. |
Организменный. | Альбумин – запасает воду в яичном желтке. Белки семян растений семейства бобовых – источник питания для зародыша. | |
Регуляторная. | Организменный. | Гормоны. Нейропептиды – пептиды, присутствующие в мозге и влияющие на функции ЦНС. |
Антибиотики. | Организменный. | Многие антибиотики являются белками. |
Белки резервные — Справочник химика 21
Однако следует подчеркнуть, что не имеется резервных белков в том смысле, как это понимается для резервных углеводов (гликоген) или резервных жиров (жиры, отложенные в жировых депо). Резервные белки — это не особые отложения белков, а обычные специфические для данной ткани белки, которые используются при недостатке белка в питании для покрытия потребностей в белке всего организма. На это указывает, например, тот факт, что усиленное белковое питание может привести к увеличению содержания белка в ткани на 50%, но это увеличение распространяется на все белковые фракции, а не на какую-либо резервную фракцию. [c.311]Под термином резервные белки понимают не особые отложения белков, а легкомобилизуемые при необходимости тканевые белки, которые после гидролиза под действием специфических протеиназ служат поставщиками аминокислот, необходимых для синтеза ферментов, гормонов и др. Опыты на животных показали, что при голодании наблюдается неравномерное изменение массы отдельных органов и тканей в значительно большей [c.416]
Высокая скорость обновления белков, доказанная при помощи меченых атомов, сввдетельствует о том, что в организме происходит постоянное смешивание эндогенных белковых молекул и продуктов их гвдролиза — аминокислот с молекулами белков и их производных, синтезированных из аминокислот белков пищи. Эта смесь эндогенного и экзогенного материала, которая может в принципе служить источником анаболических и катаболических реакций азотистого обмена, существует в качестве резервного материала, называемого метаболическим пулом. С помощью изотопных методов установлено, что примерно /з общего пула аминокислот приходится на эндогенные источники и только /з имеет своим источником белки пищи. Эти данные указывают прежде всего на исключительную важность эндогенного источника аминокислот и, кроме того, сввдетельствуют о высокой скорости обновления белков тела. [c.411]
Прн проращивании в зерне происходят процессы распада и синтеза. В эндосперме гидролизуются резервные вещества — крахмал, белки, а также пектиновые вещества, гемицеллюлозы, целлюлоза образующиеся растворимые продукты поступают через щиток в зародыш. В результате синтетических процессов из зародыша вырастают стебелек и корешки. [c.129]
По общим биологическим функциям можно подразделить белки на ферменты, структурные, транспортные, резервные и рецепторные белки. [c.344]
Транспортные и резервные белки [c.412]
Однако по мере изучения природы белков и биологической роли каждого из них классификация сильно изменялась и стала основываться на свойствах, которые связаны с их большим функциональным разнообразием и распространенностью. Белки организма в целом представлены широким спектром веществ на долю белков, входящих в состав клеток, обычно приходится более половины сухой массы. Можно выделить некоторые отдельные группы ферменты, которые обеспечивают катализ биохимических реакций в клетке резервные белки структурные белки транспортные белки мышечные белки антитела токсины гормоны и регуляторные белки. Возможно также несколько более широкое понимание биологических функций белков для того, чтобы их классифицировать на три основные категории (табл. 23.1.2)—резервные белки, структурные, или механические белки и белки, проявляющие свои различные биологические свойства при комбинации или связывании с ионами или другими молекулами. [c.221]
Нормальное функционирование клетки, т. е. обмен веществ, рост и размножение может происходить только тогда, когда в ней имеется достаточное количество воды и если клетки погружены в водную среду с растворенными в ней питательными веществами. При отделении клеток от питательной среды, например путем центрифугирования или фильтрования, обмен веществ продолжается до тех пор, пока в межклеточном пространстве имеется вода и в ней растворены питательные вещества. После их использования обмен веществ в клетках продолжается за счет клеточных резервов (углеводы, липиды) в том случае, есл 1 сохраняются оптимальные температура и реакция среды. Когда использованы и резервные вещества, начинается автолиз клеток— саморазрушение, в результате которого белки распадаются на аминокислоты и углерод аминокислот идет для энергетических нужд. [c.24]
Углеводы — большая группа органических веществ, широко распространенных в живой природе. Представителями углеводов являются виноградный сахар (глюкоза), свекловичный, или тростниковый, сахар (сахароза), крахмал, целлюлоза. В результате процесса фотосинтеза (с. 217) растениями на нашей планете ежегодно создается огромное количество углеводов, которое оценивается содержанием углерода 4 -10 ° т. Поэтому можно считать, что углеводы являются наиболее распространенными органическими соединениями. Около 80% сухого вещества растений приходится на углеводы, из которых состоят опорные ткани растений в зерне, картофеле, овощах, плодах углеводы служат резервными питательными веществами. Невозможно переоценить значение углеводов как одного из основных средств питания человека и сельскохозяйственных животных. Углеводы являются обязательной составной частью животных организмов в микроорганизмах они составляют 20—30%. Наряду с белками, нуклеиновыми кислотами и липидами углеводы являются необходимой составной частью живой клетки и выполняют важные биологические функции. Вещества, регулирующие процессы жизнедеятельности, — некоторые протеиды, нуклеиновые кислоты (с. 604) и др. — содержат остатки молекул углеводов. [c.207]
Количество простых белков (протеинов) в клетке невелико. Обычно они играют пассивную роль резервных веществ. [c.45]
Питательная (резервная) функция. Эту функцию выполняют так называемые резервные белки, являющиеся источниками питания для плода, например белки яйца (овальбумины). Основной белок молока (казеин) также выполняет главным образом питательную функцию. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессы метаболизма. [c.21]
Ряд белков используется клетками в качестве резервного, питательного материала. К ним относятся, в частности, проламины и глютелины — белки растений, преимущественно зерновых. Из животных белков можно отметить овальбумин — питательный белок птичьих яиц. [c.46]
По мере исчерпания резервных углеводов дрожжи начинают расщеплять собственные белки, что влечет за собой изменение многих жизненно важных структур и в конце концов приводит к гибели клетки. Присутствие кислотообразующйх бактерии не снижает стойкости дрожжей, так как эти бактерии содержат эндопротеазу гнилостные же, наоборот, содержат очень активную экзопротеазу и значительно ускоряют порчу дрожжей. Стойкость последних находится в обратной зависимости от интенсивности протеолиза. [c.364]
Основным направлением биохимических изменений стационарных клеток является переключение метаболизма на эндотрофный обмен, синтезы резервных веществ, вторичных метаболитов и компонентов, повышающих устойчивость клеток к наступившим неблагоприятным для роста условиям (рис. 4.7). В этих условиях в клетке включается так называемый строгий ответ — сложный комплекс реакций, приводящих к резкому снижению синтезов РНК, нуклеотидов, углеводов, липидов, полиаминов, пептидогликана клеточной стенки, повышению деградации белка, ограничению мембранного транспорта. При этом повышается контроль трансляции белков и включаются синтезы сериновых протеиназ, участвующих в белковом процессинге превращения проферментов в их активные формы в результате отщепления некодирующей аминокислотной последовательности. [c.91]
Жиры являются необходимой и весьма ценной составной частью пищи. С жирами организм получает значительно большее количество энергии, чем с таким же количеством белков и углеводов (по весу и объему). При усвоении 1 г жира выделяется 9,3 ккал. После приема в пищу жиров долго сохраняется ощущение сытости, что позволяет принимать пищу через более продолжительные промежутки времени. В природных жирах в качестве примесей содер-жется и другие полезные вещества, в том числе витамины А, Д, Е. Средний суточный рацион для человека 60—70 г жира. Жиры в организме вследствие их энергетической ценности служат резервным питательным веществом. В кишечнике под влиянием ферментов (липазы) жиры подвергаются гидролизу на глицерин и органические кислоты. Продукты гидролиза всасываются стенками кишечника и в организме синтезируются новые жиры. [c.188]
Весьма важным является вопрос о том, имеются ли в животном организме резервные отложения белка наподобие тех, какие известны для жиров и углеводов. [c.310]
Особенно демонстративной формой этого эндогенного питания является состояние голодания, при котором жизненно наиболее важные органы, например мозг и сердце, питаются за счет потребления белков других видов тканей, например мышечной ткани. Белки мышц становятся источником белкового питания для мозга и сердца. Интересным примером эндогенного питания является также увеличение массы половых продуктов у осетровых рыб в период нереста за счет использования белков иных тканей, в первую очередь мышц. Все это приводит к предположению о возможном существовании лабильных резервов белка. По-видимому, б е л к и, дл а з м ы крови, а отчасти также печени и мышц, можно с известным правом рассматривать как резервные белки. Концентрация белков в плазме может уменьшаться в случае недостатка белка в пище и вновь восстанавливаться при благоприятном белковом питании. [c.328]
Примером водной эмульсии жира, стабилизованной белком, является молоко. Эмульгирование необходимо для быстрого переваривания жиров пищи пищеварительными органами. Во время пищеварения жиры под действием фермента липазы (находится в слюне, печени, желудочном и кишечном соках) гидролизуются до свободных кислот и глицерина, которые проходят через стенки кишечника и затем снова связываются в различных комбинациях, отлагаясь в виде резервного жира. [c.269]
Превращения веществ в клетке (обмен веществ, или метаболизм), в результате которых из сравнительно простых предшественников, например глюкозы, жирных кислот с длинной цепью или ароматических соединений, образуется новое клеточное вещество, можно ради простоты подразделить на три основные группы. Сначала питательные вещества расщепляются на небольшие фрагменты (распад, или катаболизм), а затем в ходе реакций промежуточного обмена, или амфиболизма, они превращаются в ряд органических кислот и фосфорных эфиров. Эти два пути переходят незаметно один в другой. Многообразные низкомолекулярные соединения-это тот субстрат, из которого синтезируются основные строительные блоки клетки. Строительными блоками мы называем аминокислоты, пуриновые и пиримидиновые основания, фос-форилированные сахара, органические кислоты и другие метаболиты — конечные продукты цепей биосинтеза, иногда длинных. Из них строятся полимерные макромолекулы (нуклеиновые кислоты, белки, резервные вещества, компоненты клеточной стенки и т.п.), из которых состоит клетка. Эти два этапа биосинтеза клеточных веществ-синтез строительных блоков и синтез полимеров-составляют синтетическую ветвь метаболизма, или анаболизм (рис. 7.1). [c.214]
Большое значение имеет клиническое исследование на кислотность желудочного сока активную (обусловлена содержанием сильной соляной кислоты, слабой молочной кислбты, кислых фосфатов, муцина и других белков), резервную (представляет собой разность общей и активной кислотности). [c.107]
В тканях человека и других животных, а также в зеленых растениях и грибах значительная часть железа находится в форме ферритина, красновато-коричневого водорастворимого белка . Ферритин представляет собой резервную форму Fe(lII) в растворимом и нетоксичном состоянии, легко пригодном для использования. Ферритин — несколько необычный белок. Содержание железа в ферритине составляет 17—23%, причем оно находится в виде расположенной в центре плотной массы гидратированной гидроокиси железа (III), заполняющей пространство диаметром 7 нм. Эта масса окружена белковой оболочкой из 24 субъединиц, распол( женных в соответствии с кубической симметрией, во многом аналогично тому, как это показано на рис. 8-17. Внешний диаметр частицы составляет 12 нм. Молекулярный вес апоферритина равен 445 ООО, а каждая субъединица имеет молекулярный вес 18 500. Полностью заполненная (до 23% Ре) молекула ферритина содержит свыше 2000 атомов железа, упакованных почти как в кристаллической решетке. Сердцевина молекулы легко различима в электронном микроскопе, н в микроскопии ферритин часто используют как своеобразный маркер. Другая резервная форма железа, гемосидерин, по-видимому, состоит из молекул ферритина вместе с добавоч- [c.126]
Количество экстрактивных веществ и их состав в образцах коры зависят не только от древесной породы, но и от условий произрастания дерева, его возраста, места взятия образца коры (корни, ветви, ствол, по высоте ствола) и срока его хранения. Содержание некоторых компонентов экстрактивных веществ подвергается сезонным изменениям. Состав и количество экстрактивных веществ различны для внутреннехо и внешнего слоев коры. Флоэма содержит больше резервных питательных веществ и промежуточных продуктов биосинтеза, способных транспортироваться клеточным со- ом, т.е. жиров, углеводов, гликозидов, белков и т.п., тогда как в корке концентрируются воски и фенольные соединения. [c.528]
Биологические функции. Белки могут выполнять в живых организмах самые различные функции катализировать (ферменты) и регулировать (гормоны) биохимич. реакции входить в состав соединительной ткани (напр., коллаген) или мышц (актин, миозин) служить резервными питательными веществами (гранулы белка в цитоплазме) и др. Функции дезоксирибонуклеиновой к-ты — передача генетич. информации из поколения в поколение при клеточном делении. Этот Б. служит исходной матрицей при передаче информации внутри клетки. Рибонуклеиновая к-та также участвует в этом процессе, приводящем к синтезу специфич. белков клетки. Полисахариды могут служить резервными питательными веществами (напр., крахмал, гликоген), выполнять структурные функции (напр., целлюлоза полисахариды соединительной ткани), обеспечивать специфические свойства поверхности клеток (напр.1, антигенные полисахариды микроорганизмов) или защиг ту организма в целом (напрнмер, камеди и слизи растений). [c.128]
Все эти соединения вьшолняют самые разнообразные функции в живых организмах. Так, изображенная на рис. 3-12 В-глюкоза не только служит строительным блоком резервного углевода крахмала и структурного углевода целлюлозы, но и играет роль предшественника в синтезе других сахаров, таких, как В-фруктоза, О-манноза и сахароза (тростниковый сахар). Жирные кислоты-это компоненты не только сложных липидов клеточных мембран, но и жиров-богатых энергией соединений, обеспечивающих накопление запасного топлива в организме. Кроме того, жирные кислоты входят в состав защитного воскового налета на листьях и плодах растений, а также служат предшественниками других специализированных соединений, инокислоты — это не только строителШые блоки белков некоторые из них могут быть нейроме- [c.69]
Глобулины служат в растениях главным образом питательным резервным веществом и скапливаются в белках семян (например, эдестин из коно пляного семени, легумин из гороха и Др.). К глобулинам животного происхождения относятся некоторые белки мышечных волокон (миозин), энзимы (пепсин), глобулин крови, глобулин яйца, глобулин молока и т. д. [c.710]
Следует ожидать, что в силу своей биологической функции формы запасания железа должны характеризоваться высоким его содгржанием, и, следовательно, в них должно иметь место взаимодействие между ионами Ре(П1), образующими многоядерные структуры. Молекулярный вес внутреннего ядра ферритина — резервного белка, в виде которого запасается железо (разд. 21.3), может достигать величины, сопоставимой с молекулярным весом полипептидной цепи белка [1001. Этот резервный белок выглядит как дискретная компактная сфера, образованная полимерным Ре(1И), [c.352]
Липиды находятся в организме либо в виде протоплазматиче-ского жира (входят в состав протоплазмы клеток), либо в виде запасного, резервного жира (входят в состав жировой ткани). Про-топлазматический жир как составная часть клетки находится в организме в виде сложных соединений с белком и количество его не меняется при истощении организма от голода или при ожирении. При таких обстоятельствах меняется количество резервного жира. [c.267]
Резервные питательные вещества в нормированном кормлении
Липиды — обширная группа жиров и жироподобных веществ, которые содержатся во всех живых клетках.
По химической природе они представляют собой сложные эфиры жирных кислот и спирта. Липиды нерастворимы в воде, но хорошо растворяются в неполярных органических растворителях (эфир, бензин, хлороформ и др.). Отличаются большим химическим разнообразием. Важнейшими группами липидов являются: нейтральные жиры (масла, рыбий жир и др.), стероиды (желчные кислоты, холестерин, половые гормоны, витамин D), терпены (ростовые вещества растений, витамин К), воски, фосфо- и гликолипиды (компоненты клеточных мембранах), липопротеины.
Важнейшей функцией липидов является энергетическая. При полном расщеплении и окислении 1 г жира выделяется 38,9 кДж энергии, а при окислении 1 г углеводов только 17.2 кДж. Основная функция жира корма сводится к тому, что жир является главным аккумулятором энергии в организме, служит важным источником тепла. Роль жира не исчерпывается только его энергетической ценностью. Он входит в качестве структурного материала в состав протоплазмы клеток в растениях и у животных. У последних он играет роль основной резервной (запасной) ткани. Жир необходим для нормальной работы некоторых пищеварительных желез, и как несущий в себе растворенные жизненно важные вещества — витамины. При недостатке жира в кормах животные обычно испытывают недостаток жирорастворимых витаминов A, D, Е, К. Кроме того, жир играет пока еще не вполне выясненную роль в ряде физиологических функций и в образовании жира молока. Наряду со структурной функцией жиры выполняют так же защитную (теплоизоляция организма) и регуляторную функции.
При зоотехническом анализе кормов определяют сырой жир. В сырой жир входят, кроме собственно жира, воск, хлорофилл, смолы, красящие вещества, органические кислоты, фосфатиды, стерины и другие соединения.
Животные могут потреблять сырой жир в виде жира и масла. Они имеют одинаковое строение и химический состав, но различный набор жирных кислот и, следовательно, они обладают различными свойствами. Так, отдельные жирные кислоты (линолевая, арахидиновая, льняная и линоленовая) жизненно необходимы для нормальных процессов обмена веществ, роста и развития животных и потому обязательно должны доставляться с кормом.
Фосфолипиды, относятся к группе сложных липидов. Они встречаются в составе клеток всех живых организмов, где включаются в образование белково-липидных комплексов мембран. А так же вместе с другими липидами фосфолипиды образуют периферический слой клетки и ее липидную оболочку. Одними из лучших источников фосфолипидов являются зерна сои, семена подсолнечника (содержания жира 30—40%). Общеизвестно, что в зернах и семенах растений жира больше, чем в стеблях и листьях, а тем более в корнях и клубнях. Так, в зернах кукурузы и овса содержится жира 5—6%, ржи и пшеницы— 1—2%, в корнях и клубнях —0,1 %.
Углеводы.
Углеводы являются неотъемлемым компонентом клеток и тканей всех живых организмов, составляя (по массе) основную часть органического вещества на Земле. Соединения этого класса составляют около 80% сухой массы растений и 2—3% массы животных. Все углеводы состоят из отдельных «единиц», которыми являются сахариды. В зависимости от количества сахаридов выделяют моносахариды, олигосахариды и полисахариды. Организмы животных не способны синтезировать углеводы из неорганических веществ. Они получают их от растений с пищей и используют в качестве главного источника энергии, получаемой в процессе окисления. Энергетические углеводы в организме окисляются до СО, Н, О с выделением энергии, которая необходима для поддержания нормальной температуры тела, работы мышц и внутренних органов. При окислении 1 грамма углеводов в организме животных выделяется 17.0 кДж энергии. Избыточное количество углеводов в организме животных откладывается в виде жира. Таким образом, гликоген (главный резервный полисахарид) и жир являются резервными веществами в теле животных. Отложения жира, например у свиней, является генетическим признаком, а при откорме овец и крупного рогатого скота, необходимо, чтобы в корме содержалось избыточное количество углеводов. Углеводы необходимы так же для работы мышц и тканевого дыхания клеток с окислением до углекислоты и воды. При мышечной работе содержание уровня глюкозы в крови и гликогена в мышцах снижается. Снижение уровня глюкозы в крови вызывает расщепление гликогена в печени. Только гликоген, запасённый в клетках печени может быть переработан в глюкозу для питания всего организма.
Углеводы, содержащиеся в кормах, необходимы животным как источник энергии, они определяют в организме уровень энергетического питания, а так же оказывают влияние на интенсивность обмена жиров и белков. Содержание углеводов в различных растениях колеблется в очень широких пределах. Это обязательно нужно учитывать при составлении рационов. Даже в одних и тех же растениях содержание углеводов изменяется в зависимости от фазы вегетации, условий хранения корма и т.д. Много сахаров в полусахарной и сахарной свекле (80-120г/кг), а крахмала в них всего 4-6г/кг. В моркови, несмотря на сладкий вкус, сахара значительно меньше — всего 35 г/кг. Крахмала много в картофеле (около 140г/кг). Содержание углеводов в зеленых кормах зависит от их вида: в 1 кг травы клевера их содержится 10-12 г, тимофеевки — 25 г, кукурузы молочно-восковой спелости — 40 г. В силосованных кормах сахара очень мало или нет вообще, так как при силосовании он превращается в органические кислоты. Поэтому при скармливании коровам силоса в рацион необходимо включать сахаросодержащие корма. На основании изучения потребности животных в углеводах рекомендованы оптимальные нормы содержания в рационе клетчатки. Например, считается, что в сухом веществе рациона молочных коров должно содержаться 20-25% клетчатки. В то же время ее количество в пастбищном корме в зависимости от вида и фазы вегетации трав может колебаться от 15 до 40%.
Витамины.
- Витамин А(ретинол) необходим для нормального роста и воспроизводства, а так же для повышения устойчивости организма к возбудителям различных заболеваний. Основная биологическая роль витамина А в организме животных заключается в том, что он принимает участие в синтезе зрительного пигмента (родопсина), являясь соединением белка с витамином А, он поддерживает в нормальном состоянии слизистые оболочки, стимулирует рост молодых животных.
При недостатке в организме животных витамина А у молодняка замедляется рост, появляются заболевания глаз. Недостаток витамина А ведет так же к дегенеративным изменениям в нервной ткани, а так же к нарушению функций репродуктивных органов, так как витамин А учавствует в синтезе гонадотропинов, следовательно, при недостатке ретинола у животных наблюдается стерильность, плохая оплодотворяемость, рождение слабого нежизнеспособного потомства. В растительных кормах содержится провитамин А – каротиноиды из которых в организме животных образуется витамин А. Местом превращения каротина в витамин являются стенки тонкого кишечника. С практической точки зрения важно отметить, что животные могут откладывать в теле витамин А и каротин. Но запасы эти очень небольшие: например, у коров, получавших продолжительное время корм, богатый каротином, в теле его оказалось лишь 3,6 г, из которых 70-90% находилось в печени, а остальные — в жировом депо; в печени преобладал витамин А, в жире — каротин. При витаминном голодании животные очень экономно расходуют эти резервы.
Животные разных видов и пород различаются по способности превращать каротиноиды в витамин А, что нужно учитывать при контроле А-витаминной обеспеченности кормовых рационов. Например, из 1 кг бета-каротина образуется витамина А: у крупного рогатого скота — 120 мкг (400 МЕ), у свиней — 160 мкг (533 МЕ), у овец — 174 мкг (580 МЕ), у лошадей — 167 мкг (555 МЕ), у птицы — 500 мкг (1667 МЕ). Нормирование А-витаминного питания крупного рогатого скота, овец и кроликов производится только по каротину; свиней и лошадей — по каротину и витамину; птицы — по витамину.
Содержание каротина в различных кормах неодинаково. Особенно много каротина в молодой зеленой траве, моркови, травяной муке, травяной резке, сене хорошего качества, желтых сортах кукурузы и тыквы, свекольной ботве и листьях кормовой капусты. Практически нет каротина в зерне, картофеле, свекле, брюкве, турнепсе, соломе, жоме.
- Витамин D (кальциферол) — антирахитический витамин совместно с гормоном паращитовидной железы принимает участие в регуляции фосфорно-кальциевого обмена в организме животных, а также росте и минерализации костной ткани. При недостатке витамина D в кормах у животных неправильно развивается костяк, у молодняка появляется рахит, у взрослых животных — остеомаляция, остеопороз, тетания. При недостатке витамина D в рационах птиц возникает рахит, грудная кость искривляется, суставы конечностей утолщаются; яйца от такой птицы имеют тонкую скорлупу,а цыплята, полученные из таких яиц, ослаблены и подвержены различным заболеваниям. В натуральных кормах и пищевых продуктах витамин D практически отсутствует. Зеленые растения очень бедны витамином D или совсем его не содержат.
Антирахитические вещества образуются в коже животных при освещении их солнцем или искусственными источниками ультрафиолетового света из неактивных стеринов в результате фотохимических реакций, эти вещества поступают в кровь и проявляют действие, аналогичное витамину D из пищи. Поэтому летом на пастбище животные не страдают от недостатка витамина D в корме, зимой антирахитическое действие света значительно слабее и потребность в витамине D у животных проявляется острее. В летний период при нахождении животных на солнце у них могут создаваться небольшие резервы витамина D в печени. При содержании животных и птицы в помещениях без выгула на открытом воздухе они должны в течение всего года получать витамин D с кормами или периодически подвергаться ультрафиолетовому облучению. Потребность сельскохозяйственных животных в витамине обеспечивается, главным образом, путем добавок в рационы облученных дрожжей, в 1 г которых содержится до 4 тыс. МЕ витамина D, кормового рыбьего жира, витаминных препаратов: раствора витамина D2 и D3 в масле, видеина (D3), тривитамина и др. В птицеводстве применяют препараты витамина D3 в виде казеинового концентрата. Применение препаратов витамина D требует строгого нормирования. Для животных вреден как недостаток, так и избыток витамина D. При избытке витамина D происходит усиленная мобилизация кальция из пищи, кальций откладывается в почках, на стенках кровеносных сосудов и в других органах. Гипервитаминозы D обычно сопровождаются расстройством пищеварения.
Эволюция и функция биосинтеза углеводных резервов у паразитических протистов
https://doi.org/10.1016/j.pt.2021.06.005Получить права и контентОсновные моменты
Многие важные с медицинской точки зрения протисты унаследовали способность синтезировать гликоген или амилопектин от свободноживущих предков.
Удержание биосинтеза гликогена / амилопектина связано с паразитарным образом жизни, который включает стадии инцистирования и / или медленнорастущие стадии жизненного цикла, которые вызывают длительные стойкие инфекции.
Полная потеря биосинтеза углеводного резерва у некоторых протистов ( Plasmodium , Babesia , Theileria и Trypanosoma ), вероятно, отражает множество факторов, включая зависимость от гликолитического метаболизма на некоторых этапах жизненного цикла.
Совершенно новый путь биосинтеза углеводов развился в Leishmania и родственных протистах, которые, возможно, позволили этим паразитам установить длительные хронические инфекции у позвоночных-хозяев.
Почти все эукариотические клетки синтезируют запасы углеводов, таких как гликоген, крахмал или низкомолекулярные олигосахариды. Однако некоторые паразитические протисты утратили эту способность, в то время как другие потеряли и впоследствии развили совершенно новые пути. Недавние исследования показывают, что сохранение, потеря или приобретение этих путей у разных протистов тесно связано с их образом жизни. В частности, паразиты с запасами углеводов часто вызывают долгоживущие хронические инфекции и / или продуцируют цисты окружающей среды, тогда как потеря этих путей связана с паразитами, которые имеют очень пролиферативные и метаболически активные стадии жизненного цикла.Эволюция биосинтеза манногена у Leishmania и родственных паразитов указывает на то, что эти пути сыграли роль в определении круга хозяев и ниш, занимаемых некоторыми простейшими.
Ключевые слова
метаболизм паразитов
эволюция
углевод
патогенез
Рекомендуемые статьиЦитирующие статьи (0)
Полный текст© 2021 Elsevier Ltd. Все права защищены.
Рекомендуемые статьи
Цитирующие статьи
| |||
Экологические функции углеводов, хранящихся в клубнелуковицах Tipularia обесцвеченных (Orchidaceae) в JSTOR
Абстрактный1.Орхидеи Tipularia обесцветить имеет от двух до пяти подземных клубнелуковиц, содержащих высокую концентрацию общего количества неструктурных углеводов (TNC). Мы исследовали роль клубнелуковицы в инициировании нового роста после сезонной спячки, в размножении, и в ответ растений на искусственной дефолиации. 2. Увольнение старых клубнелуковиц (что составляет с. 30% от общей биомассы клубнелуковицы) под влиянием новых побегов инициации, но мало или вообще не влияет на растения в процессе производства фруктового или в их реакцию на дефолиацию.3. Затенение растений во время начала роста не оказало заметного влияния на рост побегов или их использование при хранении. Инициирование роста вызывало уменьшение массы клубнелуковиц, но не изменение процента TNC в клубнелуковицах. Размножение было связано с уменьшением как массы клубнелуковицы, так и процента TNC. 4. Искусственная дефолиация мало повлияла на использование существующих запасов углеводов. 5. Сделан вывод, что хранение углеводов в клубнелуковицах было относительно неважным для восстановления растений от травоядных по сравнению с их ролью в инициации роста и воспроизводства.
Информация о журналеFunctional Ecology публикует оригинальные статьи по экологии организмов, включая физиологическую экологию, поведенческую экологию и эволюционную экологию, и их значение для моделей и процессов сообществ и экосистем. Статьи может описывать экспериментальные, сравнительные или теоретические исследования любого типа организм. Работа, которая носит чисто описательный характер или посвящена динамике численности населения (без исследования основных факторов, влияющих на динамику населения) не будет принят, если он не проливает свет на упомянутые конкретные области выше.Функциональная экология издает стандартные статьи, обзоры, форумы. и перспективные статьи, в дополнение к специальным функциям, которые являются коллекциями статей по одной теме. Журнал издается шесть раз в год. Дальше подробности доступны на сайте www.functionalecology.org. JSTOR предоставляет цифровой архив печатной версии Functional Экология. Электронная версия функциональной экологии доступно по адресу http://www3.interscience.wiley.com/journal/117987963/home. Авторизованные пользователи могут иметь доступ к полному тексту статей на этом сайте.
Информация об издателеБританское экологическое общество — это гостеприимный и инклюзивный дом для всех, кто интересуется экологией. Общество было основано в 1913 году и насчитывает более 6000 членов по всему миру, объединяя людей в региональном, национальном и глобальном масштабах для продвижения экологической науки. Многие виды деятельности BES включают публикацию ряда научной литературы, в том числе семи всемирно известных журналов, организацию и спонсорство широкого спектра встреч, финансирование многочисленных схем грантов, образовательную работу и политическую работу.
Углеводы и диабет (для подростков)
Углеводы и сахар в крови
Следить за уровнем сахара в крови означает следить за тем, что вы едите, а также принимать лекарства, например, инсулин, если это необходимо. Ваш врач мог также упомянуть, что вам следует отслеживать, сколько углеводов вы едите. Но что такое углеводы и как они влияют на уровень сахара в крови?
Пища, которую мы едим, содержит питательные вещества, обеспечивающие энергию, и другие вещи, в которых нуждается организм, и одна из них — углеводы.Двумя основными формами углеводов являются:
- сахара , такие как фруктоза, глюкоза и лактоза
- крахмалы , которые содержатся в таких пищевых продуктах, как крахмалистые овощи (например, картофель или кукуруза), зерно, рис, хлеб и крупы
Организм расщепляет или превращает большинство углеводов в сахар глюкозу. Глюкоза всасывается в кровоток и с помощью гормона, называемого инсулином, перемещается в клетки тела, где может использоваться для получения энергии.
Люди с диабетом имеют проблемы с инсулином, которые могут вызывать повышение уровня сахара в крови. У людей с диабетом 1 типа поджелудочная железа теряет способность вырабатывать инсулин. У людей с диабетом 2 типа организм не может нормально реагировать на вырабатываемый инсулин.
Углеводы могут быть частью здорового питания
Поскольку организм превращает углеводы в глюкозу, употребление углеводов повышает уровень сахара в крови. Но это не значит, что вам следует избегать углеводов, если у вас диабет.Углеводы — здоровая и важная часть полноценного питания.
Однако одни углеводы более полезны для здоровья, чем другие. Например, цельнозерновые продукты и фрукты являются более здоровым выбором, чем конфеты и газировка, поскольку они содержат клетчатку, витамины и другие питательные вещества.
Клетчатка важна, потому что она помогает вам чувствовать сытость и поддерживает правильную работу пищеварительной системы. На самом деле, употребление большого количества клетчатки может даже помочь замедлить усвоение сахара организмом, если его есть вместе с сахаром в одной пище.Клетчатка нужна каждому, а большинству людей ее не хватает. Некоторые эксперты считают, что люди с диабетом должны есть больше клетчатки, чем люди без диабета, чтобы контролировать уровень сахара в крови.
Сладкие продукты, такие как газированные напитки и конфеты, обычно не содержат клетчатки и обычно содержат «пустые калории». Это означает, что в них содержится мало калорий, но при их употреблении слишком много калорий может остаться мало места для здоровой пищи. Употребление слишком большого количества низкокалорийной пищи также может повысить вероятность ожирения или избыточного веса.Эти продукты также могут вызвать кариес.
Стр. 1
Баланс углеводов
После приема пищи, содержащей углеводы, уровень сахара в крови повышается. Что касается контроля над диабетом, ваша цель — сбалансировать инсулин в организме и упражнения, которые вы выполняете, с углеводами, которые вы едите. Баланс инсулина, физической активности и потребления углеводов поддерживает нормальный уровень сахара в крови.
Следование плану питания помогает отслеживать потребление углеводов.Вы и ваша медицинская бригада, работающая с диабетом, составите план питания, который будет включать общие рекомендации по потреблению углеводов. Ваш план питания будет учитывать ваш возраст, размер, желаемый вес, уровень упражнений, лекарства и другие медицинские проблемы. В план питания также будут входить продукты, которые вы любите есть, поэтому сообщите об этом своему лечащему врачу.
Если вы не знаете, сколько углеводов содержится в пище, проверьте этикетку или спросите своего врача или диетолога. Кроме того, проверяйте этикетки диетических продуктов перед тем, как съесть их, потому что эти продукты могут быть с низким содержанием жира, но могут содержать дополнительный сахар.Выполняя баланс между углеводами, физическими упражнениями и инсулином, вы можете поддерживать нормальный уровень сахара в крови и при этом наслаждаться хорошей едой.
Углеводов, роль, которую они играют и зачем они вам нужны
Понимание роли углеводов в обеспечении здоровья кишечника
МАР. 02, 2021 3 МИН. ЧИТАТЬ
Правильное питание помогает питать ваше тело, и, как и многие другие вещи в жизни, все дело в балансе.Вначале нам советуют есть самые разные продукты из всех пищевых групп — фрукты, овощи, злаки, молочные продукты и белки, — и этот совет имеет веские причины. Чтобы функционировать и развиваться, вам нужны различные продукты, чтобы получать все необходимые организму питательные вещества, такие как углеводы, белки, жиры, витамины и минералы.
В последние десятилетия — и с появлением таких диет, как кетогенная, палеоидная и диета Аткинса — растет недоразумение относительно роли и важности одного питательного вещества, в частности, углеводов.Тем не менее, этот макроэлемент остается важной частью общей сбалансированной диеты и необходим для хорошего здоровья. Понимание роли углеводов и продуктов, в которых они содержатся, может помочь вам придерживаться полноценной и сбалансированной диеты.
Роль углеводов: от энергии к здоровью кишечника
Углеводы, также известные как углеводы, жизненно важны на всех этапах жизни. Они являются основным источником энергии тела и предпочтительным источником энергии для мозга. Углеводы расщепляются организмом на глюкозу — разновидность сахара.Глюкоза используется в качестве топлива клетками, тканями и органами вашего тела. Когда ваше тело не получает достаточного количества углеводов, оно ищет другой источник энергии, расщепляя белок в ваших мышцах и жировой ткани, чтобы использовать его в качестве энергии. Глюкоза важна для мозга, который не может легко использовать другие источники топлива, такие как жир или белок, для получения энергии.
Хотя углеводы больше всего известны своей энергией, некоторые из них также могут способствовать здоровью пищеварительной системы. Микробиом — это огромное собрание микробных организмов, которые живут в вашем теле и в нем, большинство из них находится в желудочно-кишечном тракте или кишечнике.Многие микробы в кишечнике — это здоровые бактерии, которые помогают поддерживать иммунитет и здоровье пищеварительной системы. Определенные углеводы, такие как клетчатка, служат пищей для полезных бактерий в кишечнике и способствуют их росту. Употребление в пищу продуктов с высоким содержанием клетчатки, таких как фрукты, овощи и цельнозерновые, также может помочь с регулярным испражнением, минимизировать проблемы, связанные с запорами, и может помочь снизить уровень холестерина и сахара в крови.
«Каждый ингредиент, который входит в наши продукты, служит важной цели.Для некоторых людей наши продукты питания обеспечивают их полное питание, поэтому продукты должны быть сбалансированы важными питательными веществами, в том числе углеводами, чтобы люди могли получать питание, необходимое для роста, исцеления или процветания ».
Хаким Бузамондо, MD, MSC, MBA, вице-президент подразделения глобальных исследований и разработок, Abbott
Функция углеводов в готовых пищевых продуктах
Хотя углеводы естественным образом содержатся во многих продуктах, таких как макароны, фрукты, овощи, молоко и хлеб, их часто добавляют в готовые продукты, чтобы сбалансировать питательные вещества и улучшить вкус и текстуру.И они играют существенную роль.
Принимать добавки питания, например. Некоторые пищевые добавки, как питания напитки, являются питательными веществами и предназначены для обеспечения важных макро-питательных веществ, витаминов и минералов. Углеводы являются одним из основных источников энергии и играют важную роль во вкусе и консистенции тоже. Сахар может добавить толщины, а также помогают предотвратить слипание белка в смеси порошков, которые могут повлиять на структуру и консистенцию. Сахар также обеспечивает сладость питательных продукты и помогает улучшить положительные ароматы или маскировать негативные, так что продукты легко пить.
«Когда мы создаем пищевые продукты, мы добавляем определенные ингредиенты для создания сбалансированных, богатых питательными веществами продуктов», — говорит Хаким Бузамондо, доктор медицинских наук, магистр наук, магистр делового администрирования, вице-президент отдела глобальных исследований и разработок Abbott. «Каждый ингредиент, который входит в наши продукты, служит важной цели. Для некоторых людей наши продукты питания обеспечивают их полное питание, поэтому продукты должны быть сбалансированы важными питательными веществами, в том числе углеводами, чтобы люди могли получать питание, необходимое для роста, выздоровления или процветания.”
Если у вас есть вопросы о диете, обязательно спросите своего лечащего врача. А понимание различных видов углеводов, где их можно найти в продуктах и как сделать их приоритетными в своем рационе, поможет вам наслаждаться разнообразными продуктами, обеспечивая организм необходимыми питательными веществами.
Уровень питательности фосфора, запасы углеводов и качество цветов в оливках
Abstract
Оливковое дерево обычно характеризуется относительно низким окончательным завязыванием плодов, что является следствием значительного количества неразвитых пестиков, выкидыша пестика и опадения цветков и плодов.Признано, что этими процессами управляет конкуренция за ресурсы между развивающимися вегетативными и репродуктивными органами. Чтобы изучить роль уровня фосфора (P) в питании в репродуктивном развитии, деревья выращивали при четырех уровнях фосфора в течение трех лет в больших контейнерах. Уровень питания фосфором положительно зависел от скорости распада репродуктивных почек, массы соцветий, количества цветков гермафродитов, веса пестика, устойчивости плодов, завязывания плодов и, следовательно, общего количества плодов.Положительное влияние питания P на показатели продуктивности не было связано ни с запасами углеводов, ни с транспортом углеводов к развивающемуся соцветию. Деревья с дефицитом фосфора продемонстрировали значительное нарушение скорости ассимиляции, и тем не менее, углеводы накапливались в соцветиях на уровнях, сравнимых или более высоких, чем у деревьев, получавших высокий P. В отличие от женских репродуктивных органов, жизнеспособность пыльцы была постоянно выше у деревьев с дефицитом фосфора, возможно, из-за повышенная доступность углеводов.В целом, было обнаружено, что положительный эффект P на репродуктивное развитие женщин не зависит от общей доступности углеводов. Следовательно, предполагается, что P оказывает прямое влияние на репродуктивные процессы.
Образец цитирования: Эрел Р., Ермияху У., Ясуор Х., Коэн Чамус Д., Шварц А., Бен-Гал А. и др. (2016) Уровень содержания фосфора, запасы углеводов и качество цветов в оливках. PLoS ONE 11 (12): e0167591. https://doi.org/10.1371/journal.pone.0167591
Редактор: Цзинь-Сун Чжан, Институт генетики и биологии развития Китайской академии наук, КИТАЙ
Поступила: 9 августа 2016 г .; Одобрена: 16 ноября 2016 г .; Опубликовано: 1 декабря 2016 г.
Авторские права: © 2016 Erel et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Авторы не получали специального финансирования на эту работу.
Конкурирующие интересы: Авторы заявили, что конкурирующих интересов не существует.
Введение
Оливковые деревья ( Olea europaea L.) дают большое количество цветов, только небольшая часть из которых в конечном итоге дает плоды [1].В результате конкуренции между развивающимися плодоносами либо питательными веществами, либо ассимилятами, вскоре после оплодотворения происходит массовое опадение плодов. Таким образом, окончательное завязывание плодов определяется примерно через 5–6 недель после цветения [2, 3]. Завязка плодов во многом зависит от условий окружающей среды, истории рождения [4–6] и генетических особенностей [7]. Для достижения экономически достаточного урожая, помимо удовлетворительного количества цветков, необходимо качество цветков. Качество цветков определяется множеством характеристик, которые повышают вероятность успешного оплодотворения и сохранения плодов [8, 9].Признано, что характеристики цветов оливок играют важную роль в завязывании плодов и развитии плодов, в том числе: частота выкидыша пестика, развитие зародышевого мешка, восприимчивость стигмы, продолжительность жизни семяпочек, размер завязи, содержание углеводов, жизнеспособность пыльцы и содержание азота (N). [4, 10].
Оливки — андромоносный вид, имеющий смесь идеальных (гермафродитных) и мужских (тычинок) цветков с абортированными (недоразвитыми) пестиками. Пестиковый аборт — это механизм управления ресурсами в зависимости от спроса, наличия и условий окружающей среды [11].Усиление конкуренции или истощение ресурсов увеличивает масштабы прерывания беременности на пестиках, тем самым одновременно снижая потенциал плодоношения и сохраняя вложения углерода в цветы [12]. В идеальных цветках больший размер завязи считается положительным признаком, тесно связанным с силой поглощения [13]. Большие яичники обычно связаны с большей вероятностью завязывания плодов [12]. Во время цветения из пыльников в воздух выделяется огромное количество пыльцы [14], что является типичным признаком ветроопыляемого таксона.Из огромного количества выпущенного зерна только часть является жизнеспособной, может прорасти на рыльце и оплодотворить одну из четырех семяпочек. Жизнеспособность пыльцы в значительной степени является генетическим признаком [15, 16], который, как было показано, сходен для тычиночных и совершенных цветов [12]. Оливки являются частично самонесовместимыми видами, для которых перекрестное опыление приводит к более высокому уровню удобрения [1, 17]. Несмотря на то, что требуется большое количество жизнеспособной пыльцы, переносимой по воздуху [16, 18, 19], перекрестное опыление редко является ограничивающим фактором для завязывания плодов в традиционных регионах выращивания [20].
В целом, запасы углеводов в цветках поддерживают рост пыльцевых трубок и раннее развитие эмбрионов [21] и, следовательно, считаются значительными усилителями продуктивности [22–24]. У оливок индукция цветения, по-видимому, не зависит от запасов углеводов, как показали Штутте и Мартин [25], используя управление светом и CO 2 , а также Cherbiy-Hoffmann et al. (2015), используя манипуляции с интенсивностью света. В полевых испытаниях Bustan et al. [26] не обнаружили значительного влияния фруктовой нагрузки на общие запасы углеводов и, таким образом, пришли к выводу, что роль резервов в основном связана с выживанием деревьев.Что касается развития цветков оливы, Reale et al. [27] сообщили о тесной корреляции между содержанием крахмала и образованием цветов гермафродитов. Кроме того, косвенные доказательства центральной роли доступности углеводов для продуктивности были обнаружены в испытаниях с опоясывающими мышцами. Было показано, что опоясывающий лишай, который увеличивает доступность углеводов в побегах, увеличивает процент идеальных цветков, завязываемость плодов и урожайность [28, 29].
Как указано выше, на качественные характеристики цветов влияют генетические факторы и факторы окружающей среды.Информация о взаимодействии качества цветов, урожайности и минерального питания ограничена только N [30, 31]. Последние данные указывают на положительный вклад фосфора (P) в продуктивность оливок [32]. Фосфор является важным макроэлементом для многих функций растений, включая метаболизм углеводов [33] и транспорт [34]. Несмотря на относительное обилие, дефицит фосфора часто ограничивает производство растений на многих пахотных почвах [35]. Это в основном связано с ограниченной подвижностью и доступностью фосфора в почве, особенно при низкой влажности почвы [36].Сообщалось, что ирригация улучшает поглощение фосфора оливками [37].
Оливковые деревья способны плодоносить на бедных почвах и суровых условиях окружающей среды, следовательно, культура традиционно выращивалась в условиях экстенсивной неорошаемой культуры, связанной с низкой урожайностью [38]. Из-за этого, а также, вероятно, в результате обширной корневой системы дерева и симбиоза с микоризными грибами [39], дефицит фосфора в оливках считается редким, а удобрение фосфатом обычно не рекомендуется [40]. За последние три десятилетия интенсивные, плотные, орошаемые сады стали обычным явлением.Считается, что орошение, являющееся частью современных производственных систем, значительно повысило урожайность оливок [41–44]. Ожидается, что благодаря высоким темпам роста и урожайности, а также уникальным методам внесения удобрений, применяемым на современных плантациях, оливковое дерево будет реагировать на потребности в питательных веществах и удобрениях. Однако роль удобрений в продуктивности оливок в целом и роль фосфора в продуктивности интенсивных садов в частности, тщательно не исследованы.
В предыдущем исследовании мы обнаружили постоянное увеличение завязываемости плодов в ответ на увеличение нормы внесения фосфора на молодых оливковых деревьях [45]. Дальнейшие исследования подтвердили это наблюдение и выявили тесную связь между статусом питания P, показателем идеальных цветков и завязыванием плодов [32]. Хотя положительное влияние фосфора на производство оливок хорошо известно, механизмы, в которых питание фосфора способствует повышению урожайности оливок, еще не изучены. Фосфор признан необходимым для ассимиляции загрузки и транспортировки и, таким образом, может сдерживать конкуренцию с поглотителями [34].Успешное завязывание плодов часто зависит от эффективной транспортировки ассимилятов к оплодотворенным цветкам, а не от накопления больших запасов крахмала. Мы предположили, что при интенсивном выращивании улучшенное питание P увеличивает доступность углеводов. Следовательно, более высокая продуктивность в ответ на увеличение фосфора может быть результатом уменьшения конкуренции за ассимиляты и питательные вещества во время цветения и развития плодов. Целью настоящего исследования было изучить влияние питания P на динамику углеводов в развивающихся цветках, на качество цветов и на продуктивность орошаемых оливок.
Материалы и методы
Двухлетние оливковые деревья «Barnea» были посажены в марте 2011 года в Исследовательском центре Гилат, Израиль (31 ° 20_N широты, 34 ° 39_E). Деревья выращивали в 150-литровых контейнерах, заполненных гранулированным перлитом типа 2 (0–2 мм) (Agrekal, Habonim Industries Ltd, Израиль). Эксперимент был организован по рандомизированной блочной схеме с 10 повторностями. Изначально деревья обильно поливали и удобряли жидкими товарными удобрениями 7-3-7 + микроэлементы (Fertilizers and Chemicals ltd, Израиль).Оросительный раствор содержал 4,51, 0,84 и 3,74 мМ азота, фосфора и калия (К) соответственно. Дифференциальная обработка удобрений была начата 16 мая 2011 года. Концентрация минералов P и номенклатура обработки приведены в Таблице 1. Остальные питательные вещества были внесены на все деревья в одинаковых количествах. Целевая концентрация питательных веществ была достигнута путем пропорционального растворения солей: KH 2 PO 4 , KNO 3 , NaNO 3 , MgSO 4 и NH 4 NO 3 .Питательные микроэлементы поставлялись в виде раствора хелата EDTA (Fertilizers and Chemicals Ltd, Израиль) с конечными концентрациями раствора: 4,71 мМ NO 3 ; 0,49 мМ NH 4 ; 2,85 мМ K; 0,84 мМ Ca; 0,56 мМ Mg; 13,8 мкМ Fe, 5,5 мкМ Mn, 3,9 мкМ Zn и 0,4 мкМ Cu. PH и ЕС оросительного раствора составляли 7,1 ± 0,5 и 1,0 ± 0,1 dS m -1 , соответственно. Деревья поливались ежедневно в избытке с помощью автоматической системы капельного орошения. Растворы для орошения для каждой обработки подавали от 1.5 м 3 резервуаров для воды, содержащих. Для обеспечения точности обработки дважды в месяц контролировали pH воды для орошения, EC, концентрацию минералов и дренажный объем. После первого сбора урожая деревья были обрезаны, чтобы обеспечить достаточное проникновение света.
Таблица 1. Средние значения ± стандартное отклонение: концентрации фосфора (P) в ирригационном растворе и соответствующей концентрации P в листьях, измеренной в период цветения, процентной доли бутонов, развившихся в соцветия, от цветков до плодов и общего количества плодов на дереве, все за каждый из двух лет обучения.
Различными буквами обозначены значения со значительными различиями при p <0,05 (6 повторений).
https://doi.org/10.1371/journal.pone.0167591.t001
Измерения
Биомасса.
В мае 2012 года, после завязывания плодов, четыре дерева для каждой обработки были срезаны на рассвете и разделены на четыре фракции: листья, ветви, конечности и ствол, каждая из которых была взвешена, и репрезентативный образец был мульчирован, взвешен и высушен в печи для определения содержания воды.Та же процедура была применена к оставшимся деревьям в конце испытания (июль 2013 г.).
Минеральный анализ.
В мае 2012 и 2013 гг., Вскоре после цветения, были взяты образцы молодых полностью распустившихся листьев в соответствии с процедурой, описанной Beutel et al. [46]. Концентрацию общего фосфора в листьях определяли после переваривания серной кислотой и перекисью. Концентрацию P определяли с помощью автоанализатора (Lachat Instrument, Милуоки, Висконсин, США).
Параметры цветения.
В 2012 году деревья были разделены на две группы: по четыре дерева на каждый уровень Р использовались для частого отбора образцов деструктивных соцветий, а оставшиеся шесть деревьев использовались для определения дополнительных параметров. В 2013 г. данные были собраны с оставшихся шести деревьев (частый отбор образцов соцветий не проводился). Подробное описание методов сбора данных было дано в предыдущем исследовании (Erel et al. [32]. Вкратце, скорость распускания репродуктивной почек определялась путем подсчета количества соцветий на 10 обозначенных ветвях на дереве (n = 6), деленного на количество листьев.Количество цветков и количество идеальных цветков подсчитывали на 10 отобранных соцветиях на дереве, имеющем смесь открытых и закрытых цветков. Для определения процента завязывания плодов в марте каждого года подсчитывали цветы на шести отмеченных ветвях на каждом дереве. Ветви, используемые для определения завязывания плодов, отбирали по периметру каждого дерева на высоте 1,5–2,0 метра. В июне подсчитывали количество плодов на отмеченных ветвях и определяли завязку плодов как соотношение плодов к цветкам на ветке.Каждый год в июле все плоды удаляли и подсчитывали вручную. Во время цветения для каждого дерева визуально определяли дату полного цветения. Полное цветение (FB) определяли в соответствии с Рапопортом и Ралло [2], как день, когда более 50% цветков распускались на более чем 50% ветвей.
Соцветие вес.
После появления соцветий еженедельно отбирали образцы по 20 соцветий с дерева (n = 4), пока не выпали лепестки. Чтобы не повлиять на параметры продуктивности, для частого отбора проб соцветий использовали только четыре повтора, эти деревья не использовали для определения завязки и плодоношения.Отобранные соцветия позже использовали для анализа углеводов. Ряд точек отбора проб P1 отсутствует из-за низкой интенсивности цветения, из-за которой количество соцветий было недостаточным для частого деструктивного анализа.
Газообмен.
Чистая скорость ассимиляции CO 2 ( A n ) и устьичная проводимость паров H 2 O ( г с ) были измерены одновременно портативной системой измерения газообмена ( LI-6400-40 LI-COR, Inc., Линкольн, штат Нью-Йорк). Молодые, развитые и полностью освещенные листья измеряли по периметру каждого дерева. Условия камеры были установлены для окружающей среды CO 2 , концентрация 400 мкмоль CO 2 моль -1 , плотность потока фотосинтетических фотонов 1000 мкмоль моль м -2 с -1 , влажность 15 ммоль H 2 O моль -1 и температура блока 25 ° C. Измерения проводились в ясные дни 7 -го , 10 -го и 14 -го мая 2012 года.Использовали четыре измерения на дерево и четыре дерева на обработку (n = 16).
Вес пестика.
В FB недавно открывшиеся соцветия были удалены с четырех деревьев за одну обработку и немедленно доставлены в лабораторию. Лепестки отбрасывали, а пестики осторожно удаляли с чашелистиков, нажимая на их основание с помощью пинцета. Пестики определялись как верхушечные или базальные в зависимости от их положения на соцветии. Для каждого дерева взвешивали не менее 100 пестиков.
Динамика опадения пестика.
Используя метод, заимствованный у Рапопорта и Ралло [2], в FB отмечали четыре ветви на каждое дерево от шести деревьев за обработку и подсчитывали цветы. В течение мая эти ветки ежедневно складывали в мешки. Обнаруженные в мешочках отсеченные пестики были разделены на идеальные и несовершенные классы и подсчитаны. Данные представлены в виде относительной скорости опадания.
Жизнеспособность пыльцы.
Для оценки жизнеспособности пыльцы использовались два метода. В 2012 году реактив Александера [47] использовался для окрашивания пыльцы на ФБ восьми соцветий за обработку.Было исследовано около 200 зерен в соцветии. Потенциально жизнеспособными считались только зерна, окрашенные в пурпурный цвет. В 2013 году применялись методы окрашивания как реагентом Александера, так и флуоресцеина диацетатом (FDA). Окрашивание FDA проводили, как описано Пинни и Полито [48].
Крахмал и растворимые углеводы (SCH).
Концентрацию крахмала в соцветиях определяли с использованием тех же образцов, которые использовались для оценки веса соцветий, как описано выше. Листья и цветы замораживали в жидком азоте, лиофилизировали, измельчали и хранили при -20 ° C до анализа.Растворимые углеводы (SCH) трижды экстрагировали 80% этанолом при 80 ° C. Крахмал определяли в остатке путем переваривания нерастворимого в этаноле остатка амилоглюкозидазой, как описано в Vishnevetsky et al. [49]. Глюкозу в растворе определяли колориметрической реакцией с динитросалициловой кислотой по Миллеру [50]. SCH в развитых соцветиях определяли с использованием этанольных экстрактов, описанных выше. Экстракты упаривали досуха и повторно растворяли в 4 мл бидистиллированной воды, из которой лиофилизировали аликвоты по 500 мкл.Высушенный материал дериватизировали в течение 90 минут при 37 ° C (в 40 мкл 20 мг -1 гидрохлорида метоксиамина в пиридине) с последующей 30-минутной обработкой 70 мкл N-метил-N (триметилсилил) трифторацетамида при температуре 37 ° C и центрифугирование. После дериватизации SCH анализировали с помощью Agilent 6850 GC / 5795C MS (Agilent Technology, Пало-Альто, Калифорния). Один мкл вводили в режиме без разделения при 230 ° C. Газ-носитель гелий использовали при расходе 1 мл мин. -1 . Хроматографию проводили на капиллярной колонке HP-5MS (30 м × 0.250 мм × 0,25 мкм). Масс-спектры получали при сканировании 2,4 сек. -1 с сканированием m / z 50-550. Температуру МС устанавливали равной 230 ° C. Как ионные хроматограммы, так и масс-спектры оценивали с использованием программного обеспечения MSD ChemStation E.02.00.493. Углеводы были идентифицированы путем сравнения времени удерживания и масс-спектров с соответствующими стандартами (Sigma-Aldrich, Израиль), и каждый SCH был количественно определен с использованием калибровочной кривой.
Статистический анализ
Данные были проанализированы с помощью JMP 10.0 (Институт САС). Четыре уровня P можно проверить с помощью регрессии как непрерывную независимую переменную, однако трех-четырех уровней P вряд ли достаточно для регрессионного анализа. Мы решили обозначить уровень P как дискретную переменную (т.е. очень высокий, высокий, низкий и недостаточный) и использовать ANOVA (качественный). Эффект обработок анализировали с использованием однофакторного дисперсионного анализа (критерий множественного сравнения Тьюки-Крамера).
Результаты
Три экспериментальных года позволили провести два последовательных сезона плодоношения: 2012 и 2013 гг.После первого года плодоношения (два года после начала обработки) обработка с низким содержанием P (P1, 0,1 мг / л -1 P) выявила симптомы серьезного дефицита, включая практически нулевой рост или урожайность деревьев (данные не показаны). Таким образом, P1 был исключен и не анализировался во втором сезоне.
Биомасса
Биомасса деревьев была ограничена P только тогда, когда P листьев упал ниже 0,1% (т.е. обработки P1 и P2), в то время как при высоких уровнях P накопление биомассы не пострадало.Во время цветения (май 2012 г.) средняя сухая масса побегов составляла 0,7, 4,0, 10,0 и 10,3 кг дерева –1 для P1 – P4 соответственно. Средняя биомасса побегов к концу эксперимента (июль 2013 г.) составила 11,3, 22,6 и 23,6 кг дерева –1 для P2 – P4 соответственно. Как правило, вес листьев, ветвей, ветвей и ствола был тесно связан с общей биомассой и поэтому не представлен.
Концентрация питательных веществ в листьях, репродуктивных почках, завязке плодов и номер плода
В таблице 1 представлены уровни P в оросительном растворе и полученный P листа, количество репродуктивных почек, количество цветков на соцветие, идеальное соотношение цветков, завязка плодов и количество плодов на дереве.Через год после начала обработки концентрация фосфора в листве существенно зависела от уровня внесения. Самая высокая обработка P, P4, имела концентрацию P в листьях 0,16%, что в четыре раза больше, чем самая низкая обработка (P1, 0,04%). Сопоставимые уровни фосфора в листьях были обнаружены во втором сезоне, в мае 2013 года. Два последовательных года плодоношения в исследовании сильно различались по скорости распускания почек зимой-весной и, следовательно, по потенциалу плодоношения. Такой сезонный эффект является обычным для оливковых деревьев и может быть связан с подавляющим эффектом плодоношения 2012 года, истощением ресурсов или несходными зимними температурами.В 2012 году процент распускания репродуктивной почки зависел от наличия фосфора, увеличившись с 1,5% в P1 до 32–34% на двух самых высоких уровнях P, P3 и P4. В следующем сезоне распускание почек было заметно ниже (10–15%), и не было обнаружено значительных различий между тремя оставшимися уровнями фосфора. Количество цветков в соцветии увеличивалось с увеличением уровня P, но два самых высоких уровня P не различались статистически. Соотношение идеальных цветков постоянно увеличивалось с увеличением уровня P и было самым высоким при самом высоком уровне P в оба сезона.Для любого уровня P соотношение идеальных цветов было выше в 2013 году, в сезон с меньшей интенсивностью цветения. Завязываемость плодов в 2012 году была относительно высокой, и оба года было обнаружено значительное влияние уровня Р. В 2012 году завязка плодов составляла от 2,6 до 8,2% для P1 и P4, соответственно, а в 2013 году — от 1,6 до 4,3% для P2 и P3, соответственно. Комбинированный эффект уровня цветения и завязывания плодов привел к сильному эффекту обработки P на количество плодов на дереве; от 2 до 4889 для P1 и P4 соответственно в 2012 году и от 695 до 2718 для P2 и P4 соответственно в 2013 году.Деревья, получившие два самых высоких уровня P, P3 и P4, имели одинаковое количество плодов.
Развитие соцветия
Фосфор влияет на массу соцветий с ранней стадии развития, в начале марта, на протяжении всего периода развития соцветий. Более высокая масса соцветий была очевидна при увеличении P до P3 (рис. 1). Замедленное развитие лечения низким уровнем P отразилось на небольшой задержке во времени FB. В течение обоих сезонов, независимо от уровня Р, свежая масса соцветий начинала незначительно снижаться до ПС.В 2012 году для любого заданного уровня P максимальный вес соцветия был значительно выше, а FB откладывалась по сравнению с 2013 годом.
Рис. 1. Средняя свежая масса соцветий во время развития цветков оливковых деревьев, получавших обработку P (0,1, 1, 10 и 26 мг л -1 P при орошении для P1 – P4 соответственно, n = 4).
2012 (а) и 2013 (б). Планки погрешностей представляют собой стандартное отклонение. Вертикальные линии обозначают дату полного цветения (FB) при визуальной оценке.
https: // doi.org / 10.1371 / journal.pone.0167591.g001
CO
2 ассимиляция и устьичная проводимостьЧистый коэффициент ассимиляции ( A n ) был значительно ниже только на самом низком уровне P. P1 имел среднее значение A n 13,4 мкмоль м -2 s -1 , в то время как P2 – P4 все имели на 25% выше A n значения в диапазоне 17,8–18,0 мкмоль м -2 с -1 (рис.2).Устьичная проводимость ( г, с ) также оказалась самой низкой на уровне P1, но разница была менее выраженной и была значительно ниже только по сравнению с лечением P2. По сравнению с P2 – P4, среднее сокращение g s деревьев P1 составило 16%.
Рис. 2. Скорость ассимиляции (a, A n ) и устьичная проводимость (b, g s ) оливковых деревьев в ответ на четыре уровня фосфора (P) (0.1, 1, 10 и 26 мг л ( -1 P при орошении для P1 – P4 соответственно).
Измерения проводились между 10: 00–12: 00 в течение трех дней в начале мая 2012 г. Каждый день измеряли четыре дерева на обработку (n = 16). Разные буквы указывают на значимые различия при p <0,05.
https://doi.org/10.1371/journal.pone.0167591.g002
Содержание крахмала и растворимых углеводов в развивающихся соцветиях
Содержание крахмала (в пересчете на сухой вес) в соцветиях на самой ранней стадии развития было самым высоким, примерно 7.7% и постепенно уменьшалась по мере развития соцветий до ~ 6,0% вскоре после FB (рис. 3a). Обработки P2 – P4 были сопоставимы, в то время как P1 всегда имел более высокую концентрацию крахмала, за исключением первого и последнего дат отбора проб. Содержание крахмала в соцветии (умножение концентрации на биомассу) накапливалось с относительно низкой скоростью с момента зарождения до конца марта, а затем накапливалось с более высокой скоростью до FB (рис. 3b). Концентрацию крахмала в листьях определяли примерно через три недели после FB.Как и в соцветии, P1 имел самую высокую концентрацию крахмала, 16,8%, что значительно выше, чем у обработок P2 – P4, у которых концентрации в листьях составляли 13,1–11,7% (рис. 3c). В отличие от крахмала, уровень P не влиял на SCH, поэтому среднее значение четырех обработок представлено вместе (рис. 4). В целом, наиболее распространенным SCH в соцветии была глюкоза, за ней следовали маннит, сахароза и фруктоза, последние три SCH имели сопоставимые концентрации в FB. Мио-инозитол был идентифицирован в очень низких концентрациях при всех обработках (данные не показаны).Общая концентрация SCH имеет тенденцию к снижению с начала марта до начала апреля, а затем резко возрастает параллельно с резким увеличением скорости роста соцветий (рис. 1). В течение апреля SCH был высоким, а после цветения SCH снова снизился. Различные SCH обычно следовали описанной схеме с небольшими колебаниями. Несколько исключительной была концентрация фруктозы, которая постоянно увеличивалась по мере развития соцветий.
Рис. 3. Концентрация крахмала (а) и содержание крахмала (б) в развивающихся соцветиях и концентрация крахмала в листьях (в) в зависимости от четырех уровней фосфора (0.1, 1, 10 и 26 мг л ( -1 P при орошении для P1 – P4 соответственно).
Для соцветий каждая точка представляет в среднем четыре дерева на обработку и два повтора на дерево (n = 8). Планки погрешностей указывают на стандартное отклонение. Образцы листьев были отобраны 18 мая -го 2012. Каждая точка представляет собой среднее значение трех деревьев на обработку и восьми повторов на дерево (n = 24), разные буквы указывают на значимые различия при p <0,05.
https: // doi.org / 10.1371 / journal.pone.0167591.g003
Рис. 4. Средние концентрации общих растворимых углеводов (SCH) и глюкозы (а) и маннита, сахарозы и фруктозы (b) в развивающихся соцветиях от появления до полного цветения (март). -Апрель 2012 г.).
Поскольку уровень фосфора не влиял на SCH, все измерения оценивались вместе (n = 16). Планки погрешностей указывают на стандартное отклонение.
https://doi.org/10.1371/journal.pone.0167591.g004
Масса пестика
Как правило, пестики в апикальном положении имели большую массу, чем в базальном (Рис. 5).Разница в весе между базальным и апикальным положениями была очень выражена при низком P, при этом на 34% больше массы в апикальном положении соцветий P1 по сравнению с просто на 11% больше в P4. Постепенное увеличение веса пестика с увеличением доступности фосфора наблюдалось в обоих положениях пестика; от 0,77 г в P1 до 1,25 мг в P4 для апикального положения и от 0,51 г в P1 до 1,12 г в P4 для базального положения. В 2013 году наблюдалась сопоставимая тенденция, абсолютные значения которой стабильно ниже, чем в 2012 году.
Рис. 5. Сырой вес пестика в зависимости от уровня Р.
Измерения проводились непосредственно перед полным цветением, 30 -е апреля 2012 г. (a) и 7 -е мая 2013 г. (b) в зависимости от уровня P (0,1, 1, 10 и 26 мг л -1 P in орошение для P1 – P4 соответственно). Разные буквы указывают на значительные различия между обработками при p <0,05.
https://doi.org/10.1371/journal.pone.0167591.g005
Динамика опущения мужских и идеальных цветков
Динамика опадания определена только в 2012 г.Данные были нормализованы по дате FB каждого отдельного дерева. Независимо от уровня P, опадение мужских цветков начиналось через четыре дня после FB, и почти все мужские цветки опадали через 20 дней после FB. Идеальные цветки сохранялись намного дольше, и опадение началось примерно через 10 дней и продолжалось до 30 дней после FB. Мужские цветки двух обработок с низким P имели тенденцию опадать раньше, чем цветки P3 и P4. Например; 50% опадения мужских цветков произошло на пять дней раньше в P1 по сравнению с обработкой с высоким содержанием P (Рис. 6).Идеальные цветы дольше оставались на соцветии, а влияние уровня Р было менее выраженным. Несмотря на это, P1 демонстрировал немного ускоренное опадание между 17 и 24 днями после FB.
Рис. 6. Относительная динамика опадания мужских (a) и гермафродитных (b) пестиков в зависимости от уровня фосфора (0,1, 1, 10 и 26 мг л -1 P при орошении для P1 – P4 соответственно).
Каждая точка представляет собой среднее значение четырех деревьев на обработку и пяти цветущих ветвей на дерево (n = 20).
https://doi.org/10.1371/journal.pone.0167591.g006
Жизнеспособность пыльцы
На жизнеспособность пыльцы отрицательно влияло наличие фосфора. Жизнеспособность пыльцы, измеренная с помощью реактива Александра, варьировалась от 66% в P1 до 35% в P4 в 2012 году и от 70% в P2 до 58% в P4 в 2013 году. Метод FDA показал аналогичную тенденцию с более низкими значениями, 30%. до 9,5% для P1 и P4 соответственно в 2013 г. (рис. 7).
Рис. 7. Жизнеспособность пыльцы в зависимости от уровня фосфора (0.1, 1, 10 и 26 мг л ( -1 P при орошении для P1 – P4 соответственно).
В 2012 г. (а) измерено реактивом Александера и в 2013 г. (б) как реактивом Александера, так и методом флуоресцеиндиацетата (FDA) (200–300 цветков на обработку). Разные буквы указывают на достоверные различия при p <0,05.
https://doi.org/10.1371/journal.pone.0167591.g007
Обсуждение
У оливкового дерева есть несколько средств для балансировки и контроля плодовой нагрузки с учетом доступности ресурсов, что отражается в состоянии питания дерева [4, 6, 13].Хотя индукция цветения, по-видимому, не контролируется общей доступностью углеводов [25], пол и параметры качества цветка тесно связаны с доступностью ресурсов (азота и углеводов) [29, 31], и завязка плодов определяется соответственно [5, 28] . В текущем исследовании было показано, что повышенный уровень питания P в целом улучшает качество цветков и окончательное завязывание плодов у самок. Ранее мы предполагали, что положительное влияние питания P на идеальное формирование цветов и завязывание плодов связано с доступностью углеводов и динамикой транспорта [32].Однако текущее исследование показывает, что положительный эффект P не зависит от общей доступности углеводов для репродуктивных органов (за исключением пыльцы).
Считается, что низкая цветочная нагрузка связана с более высоким качеством цветков [4, 51] и, следовательно, более высокой скоростью завязывания плодов [5, 6, 52]. Напротив, низкая доступность фосфора снижает интенсивность цветков и завязываемость плодов, как показано в этом (Таблица 1) и в предыдущем исследовании [32]. Уменьшение интенсивности цветков и завязывания плодов при низком статусе P указывает на центральное значение P для репродуктивного успеха.Параметры качества цветка, включая долю идеальных цветков, соцветие и биомассу пестика, и, в определенной степени, устойчивость пестика и завязку плодов, наряду с производством цветов, все были положительно связаны с питательным статусом P. Напротив, концентрации крахмала и SCH не были увеличены P. В предыдущем исследовании было продемонстрировано, что положительное влияние уровня питания P на соотношение идеальных цветов было более выраженным в высокоиндуктивных условиях [32], вероятно, в результате более сильной конкуренции. за ресурсы.Таким образом, мы пришли к выводу, что положительное влияние фосфора на качество цветов могло быть более выраженным, если бы интенсивность цветения была выше.
Биомасса пестиков считается важным признаком, положительно связанным с силой погружения [13], и, следовательно, большие пестики имеют повышенную вероятность успешного завязывания плодов. В два исследованных сезона увеличение доступности фосфора сопровождалось постоянным увеличением биомассы пестиков как в апикальном, так и в базальном положениях (рис. 5). Эффект от повышения P был более выражен на базальных, менее обработанных позициях.В исследовании Куэваса и Полито [12] мужские цветки имели тенденцию развиваться на второстепенных, менее конкурентных позициях. Здесь мы показываем, что также в популяции идеальных цветов биомасса завязи связана с ее положением в соцветии, и более крупные пестики, вероятно, будут располагаться на верхушке. Этот образец распределения внутри соцветия указывает на второй уровень распределения ресурсов по позициям с лучшими шансами на оплодотворение. Высокий уровень питательных веществ фосфора препятствует конкуренции между идеальными цветами в соцветии.Например, в 2012 г. пестики в базальных положениях имели на 34, 24, 15 и 11% более низкую биомассу по сравнению с пестиками на вершине для P1 – P4, соответственно.
Существенное опадение цветков и плодов происходит сразу после FB [17]. Позднее опадение обычно связано с конкуренцией между оплодотворенными яичниками [3]. В текущем исследовании динамика поглощения была очень похожа на модель, описанную для «Мансанильо» [2]. При низких уровнях P было обнаружено снижение устойчивости пестиков, в то время как высокие уровни P были связаны с большей выносливостью, особенно мужских цветов (Рис. 6).Скорее всего, это не окажет значительного влияния на урожайность, поскольку эффективный период опыления оливок, вероятно, составляет не более трех дней [53]. Различная динамика опадания может скорее указывать на большую силу опускания и лучшее качество цветков у деревьев с высоким Р.
Для успешного оплодотворения требуется жизнеспособная пыльца мужских репродуктивных органов, способная прорастать, расти и оплодотворять одну из семяпочек. Этот процесс принципиально лучше в случае перекрестного опыления [18, 20], следовательно, количество пыльцы и ее жизнеспособность важны для продуктивности соседних сортов.В отличие от качества женских цветов, жизнеспособность пыльцы значительно и постоянно снижалась по мере увеличения уровня фосфора (рис. 7). Исследование, проведенное на Lilium , выявило тесную связь между уровнем крахмала и развитием пыльцы [54]. Предположительно, для деревьев с дефицитом фосфора комбинация более высоких запасов крахмала, обнаруженных в соцветиях, с меньшим количеством пыльников для конкуренции за углеводы, могла способствовать повышенной жизнеспособности пыльцы этих цветов. Если это так, дефицит фосфора ухудшает женские органы, косвенно улучшая мужскую функцию.Между двумя методами оценки уровня жизнеспособности пыльцы и изменчивости между сезонами для данного метода наблюдалась относительно большая разница (рис. 7). В целом оба метода показали схожие тенденции, то есть снижение жизнеспособности с повышением уровня Р. Реагент Александера имеет тенденцию переоценивать жизнеспособность [55], в то время как метод FDA, как было показано, тесно связан с прямым тестом на прорастание и, таким образом, считается более надежным для пыльцы оливок [56]. Значения FDA (30–9,5%) хорошо согласуются с диапазоном, определенным для шести хорватских сортов за шесть лет (32–2%) по результатам прямых тестов на всхожесть [7].
Известно, что дефицит фосфора отрицательно влияет на процессы фотосинтеза [57], вероятно, из-за его центральной роли в транспорте триосфосфата из стромы [34, 58]. Следовательно, при дефиците фосфора ожидается, что крахмал и SCH будут накапливаться в исходном органе (листьях) и уменьшаться в приемных органах (цветках и плодах) [59]. Результаты настоящего исследования согласуются с сообщаемым ингибирующим эффектом дефицита фосфора на A n и повышенным накоплением крахмала в листьях (рис. 2 и 3), но не было обнаружено значительного влияния фосфора на измеренный SCH. .Ожидается, что комбинированные процессы приведут к существенному снижению доступности ассимилятов для поглощения репродуктивных органов. Такой эффект может быть наиболее выражен в период цветения и завязывания плодов, когда потребность в углеводах наиболее высока. Ранее было продемонстрировано, что запасы крахмала коррелируют с жизнеспособностью цветков некоторых фруктовых деревьев, включая абрикос [21], авокадо [23, 24] и цитрусовые [60]. В оливках Reale et al. [27] показали, что уровни крахмала в яичниках и семязачатках тесно связаны с идеальным развитием цветка.Rapoport et al. [61] сообщили о снижении содержания крахмальных зерен в завязи и семяпочки после стресса, вызванного засухой, что впоследствии привело к снижению завязываемости плодов. Вышеупомянутая информация в сочетании с положительной ассоциацией между более высоким соотношением листьев / цветов и опоясанием к завязыванию плодов [28, 31] указывает на то, что повышенный уровень углеводов положительно влияет на качество цветов и завязываемость плодов.
В текущем исследовании ингибирование ассимиляции P-дефицитных деревьев было очевидным в период завязывания плодов.Уменьшение A n сопровождалось незначительным уменьшением на g s . Чуть меньшее значение g s может лишь частично объяснить нарушение ассимиляции A n относительно нечувствительно к изменениям g s при высоких значениях из-за асимптотической природы его кривая отклика [62]. Следовательно, ингибирование A n на самом низком уровне P, вероятно, в основном связано с более медленным экспортом триосфосфата и, следовательно, ингибированием по обратной связи.Крахмал накапливался в листьях и соцветиях P-дефицитных деревьев (рис. 3), в то время как концентрация SCH не изменялась P. Эти результаты позволяют сделать вывод, что, несмотря на нарушение A n , доступность углеводов не изменилась. не ограничивают репродуктивные процессы P-дефицитных деревьев. Хотя это противоречит нашей исходной гипотезе, сопоставимые аналоги этого вывода можно найти в литературе для других видов. Например, у растений риса с дефицитом фосфора одновременно уменьшались A n и рост корней.Манипулируя интенсивностью света Wissuwa et al. [63] продемонстрировали, что ингибирование роста корней не является причиной ограничения ассимилятов (ограничение источника), а напрямую связано с дефицитом фосфора (ограничение поглотителя). Точно так же мы предполагаем, что в оливках с дефицитом фосфора поступление углеводов не ограничивает продуктивность, а скорее, что развитие репродуктивных органов ограничивается доступностью фосфора. Снижение жизнеспособности цветков с пониженной доступностью фосфора дополнительно выявляется по динамике опадания цветков (рис. 6).Цветы с деревьев с низким значением P опадают раньше. Быстрое опадание цветков и плодов указывает на более низкую силу поглощения цветков с низким содержанием фосфора, а не на ограниченное количество углеводов, как ранее было продемонстрировано для цитрусовых [60]. В текущем исследовании общий доступный крахмал и SCH, по-видимому, не играют важной роли в репродуктивных процессах оливок. Несмотря на это, фосфор и углеводы могут участвовать посредством передачи сигналов и чередования определенных сахаров или фосфорилированных сахаров. Было показано, что определенные углеводные формы, такие как фосфорилированные гексозы, опосредуют метаболические, ферментативные или генетические свойства [64].Например, было предложено, чтобы сахароза и малат служили сигналами, контролирующими движение устьиц [65, 66]. Хотя это указывает на потенциальное участие определенных углеводов, на которые влияет уровень фосфора, было определено только незначительное фосфорилирование SCH и SCH.
В нескольких исследованиях изучалась сезонная динамика SCH различных тканей оливкового дерева (т.е.) [26, 67, 68]. Эти исследования, поддержанные Штюттом и Мартином [25], показали отсутствие связи между уровнем углеводного резерва и образованием цветов.Де ла Роса и др. [69] продемонстрировали накопление крахмала в почках в начале дифференцировки оливок. Образование гранул крахмала, вероятно, жизненно важно для правильного формирования и функционирования пестика [27]. В текущем исследовании уровень крахмала был самым высоким ближе к зарождению и уменьшался во время развития соцветия, в то время как содержание крахмала в соцветии увеличивалось (рис. 3). Первоначально высокая концентрация обусловлена накоплением крахмала зимой [69]. Концентрация SCH показала динамическое поведение; на первой фазе развития SCH имеет тенденцию к снижению со временем, что, вероятно, указывает на зависимость молодого соцветия от SCH и запасов крахмала.Впоследствии, во время фазы быстрого развития соцветий, SCH увеличился до максимальных значений. Высокое содержание углеводов может помочь развивающимся цветкам в правильном развитии пыльцы [54] и поддержать будущее оплодотворение и сохранение плодов [23, 24]. Выраженное снижение биомассы, крахмала и SCH во время и после FB, вероятно, связано с высвобождением пыльцевых зерен и усилением метаболических процессов. Об уменьшении сухой массы соцветий за несколько дней до цветения также сообщили Kitsaki et al.[70].
В заключение, уровень питательности фосфора оказался положительно связан с параметрами качества цветков, в основном из-за более низкой частоты выкидышей пестиков и увеличения «идеальных» пестиков и биомассы соцветий. Эти черты, вероятно, увеличивают силу опускания цветов, что положительно связано с устойчивостью пестиков и плодов и окончательным завязыванием плодов. Положительное влияние питания P не было связано ни с общими запасами углеводов, ни с транспортом углеводов к развивающемуся соцветию.Несмотря на низкое качество A n , деревья с низким содержанием фосфора накапливают углеводы в соцветии до уровней, которые сравнимы или выше, чем у деревьев, подверженных высоким уровням фосфора. Низкое завязывание плодов и высокие запасы углеводов означают, что нехватка фосфора напрямую ограничивает репродуктивные процессы, от зарождения цветков до завязывания плодов. Более высокие запасы углеводов, обнаруженные в соцветиях с низким содержанием фосфора, могли способствовать значительному увеличению жизнеспособности пыльцы.
Благодарности
Мы благодарим сотрудников Исследовательского центра Гилат, Инну Фейнгольд, Юлию Соботину, Людмилу Юсупову и Исаака Ципори за лабораторную и полевую поддержку. Особая благодарность доктору Хаве Рапопорту за полезные советы и рекомендации.
Вклад авторов
- Концептуализация: RE UY AS AD.
- Получение финансирования: UY.
- Методология: HY DCC RE.
- Написание — черновик: AD AB RE.
- Написание — просмотр и редактирование: AB AD UY.
Ссылки
- 1. Лави С. Олив. В: Монселиса С.П., редактор. CRC Справочник по завязыванию и развитию плодов. Флорида: CRC Press; 1986. стр. 261–76.
- 2. Рапопорт Х., Ралло Л. Опадение цветка и плода постантезиса у оливы «мансанильо». J Am Soc Hortic Sci. 1991. 116 (4): 720–3.
- 3. Куэвас Дж., Рапопорт Х., Ралло Л. Взаимосвязи репродуктивных процессов и опадения плодов у «оливы Arbequina».Достижения в области садоводства. 1995. 9 (2): 92–6.
- 4. Куэвас Дж., Ралло Л., Рапопорт Х.Ф. Влияние культурной нагрузки на качество цветов оливок. Scientia Horticulturae. 1994. 59 (2): 123–30.
- 5. Лаве С., Ралло Л., Рапопорт Х. Ф., Тронкосо А. Цветочная биология оливок: влияние количества, типа и распределения цветков на завязь. Scientia Horticulturae. 1996. 66 (3–4): 149–58.
- 6. Lavee S, Rallo L, Rapoport HF, Troncoso A. Цветочная биология оливок — II.Влияние загрузки соцветий и распределения по побегам на завязку и загрузку плодов. Scientia Horticulturae. 1999. 82 (3–4): 181–92.
- 7. Вулетин Селак Г., Перика С., Горета Бан С., Букан Л., Поляк М. Стерильность цветков и всхожесть пыльцы как генетические признаки семи сортов оливы (Olea europaea L.), выращиваемых в Хорватии. Журнал садоводства и биотехнологии. 2012. 87 (3): 237–42.
- 8. Martins PC, Cordeiro AM, Rapoport HF. Качество цветов в садах оливковых, Olea europaea L., резюме. Мориска. Достижения в области садоводства. 2006; 20: 262–6.
- 9. Рапопорт Х.Ф., Мартинс ПК, редакторы. Качество цветов в оливковом масле: расширение концепции. Proc 2-го международного семинара «Последние достижения оливковой индустрии»; 2006.
- 10. Морено-Алиас I, де ла Роса Р., Рапопорт Х.Ф. Компоненты цветочного качества нового сорта оливок и его родителей. Sci Hortic-Amsterdam. 2013; 154 (0): 17–9.
- 11. Бертен Р. Эволюция и поддержание андромоэзии.Эволюционная теория. 1982; 6: 25–32.
- 12. Куэвас Дж., Полито В.С. Роль тычиночных цветков в системе размножения olea europaea (Oleaceae): андромоноидного таксона, опыляемого ветром. Летопись ботаники. 2004. 93 (5): 547–53. pmid: 15037451
- 13. Rosati A, Zipancic M, Caporali S, Paoletti A. Завязка плодов обратно пропорциональна массе цветов и плодов оливок (Olea europaea L.). Scientia Horticulturae. 2010. 126 (2): 200–4.
- 14. Рохо Дж., Салидо П., Перес-Бадиа Р.Производство цветов и пыльцы оливкового сорта «Cornicabra» (Olea europaea L.) и влияние факторов окружающей среды. Деревья. 2015: 1–11.
- 15. Перика С., Бан С.Г., Букан Л., Поляк М. Стерильность цветков и всхожесть пыльцы как генетические признаки семи оливок (Olea.2012; 87: 237–42.
- 16. Вулетин Селак Дж., Куэвас Дж., Горета Бан С., Перика С. Показатели пыльцевых трубок при оценке совместимости с оливковыми сортами (Olea europaea L.). Scientia Horticulturae.2014; 165 (0): 36–43. http://dx.doi.org/10.1016/j.scienta.2013.10.041.
- 17. Лави С. Биология и физиология оливы. В: МОК, редактор. Всемирная энциклопедия оливок. Мадрид, Испания: Международный совет по оливковому маслу; 1996. с. 59–106.
- 18. Лави С., Тарьян Дж., Левин Дж., Хаскал А. Значение перекрестного опыления для различных сортов оливок в условиях интенсивного орошения. Olivae. 2002; 91: 25–36.
- 19. Вулетин Селак Г., Перика С., Бан С.Г., Радунич М., Поляк М.Репродуктивный успех после самоопыления и перекрестного опыления оливковых сортов в Хорватии. HortScience. 2011; 46 (2): 186–91.
- 20. Пинильос В., Куэвас Дж. Открытое опыление обеспечивает достаточный уровень перекрестного опыления в испанских моновариальных оливковых садах. Hortscience. 2009. 44 (2): 499–502.
- 21. Родриго Дж., Хормаза Дж. И., Эрреро М. Запасы крахмала в яичниках и развитие цветов абрикоса (Prunus armeniaca). Physiol Plantarum. 2000. 108 (1): 35–41.
- 22.Жан Д., Лапоинт Л. Ограниченная доступность углеводов как потенциальная причина выкидыша у Rubus chamaemorus. Physiol Plantarum. 2001. 112 (3): 379–87.
- 23. Alcaraz ML, Hormaza JI, Rodrigo J. Запасы крахмала в яичниках и развитие пестиков авокадо (Persea americana). Physiol Plantarum. 2010. 140 (4): 395–404.
- 24. Алькарас М.Л., Хормаза Дж. И., Родриго Дж. Запасы пестичного крахмала при антезисе коррелируют с конечной судьбой цветка в авокадо ( Persea americana ).PLoS ONE. 2013; 8 (10): e78467. pmid: 24167627
- 25. Штутте Г., Мартин Г. Влияние интенсивности света и запасов углеводов на цветение оливок. Журнал Американского общества садоводческих наук. 1986. 111 (1): 27–31.
- 26. Бустан А., Авни А., Лави С., Зипори И., Есельсон Ю., Шаффер А.А. и др. Роль углеводных запасов в урожайности интенсивно выращиваемых масличных оливковых деревьев (Olea europaea L.). Физиология деревьев. 2011.
- 27. Реале Л., Сгромо С., Эдерли Л., Паскуалини С., Орланди Ф., Форнасиари М. и др.Морфологическое и цитологическое развитие и накопление крахмала у гермафродитных и тычиночных цветков оливы (Olea europaea L.). Половое размножение растений. 2009. 22 (3): 109–19. pmid: 20033432
- 28. Левин А.Г., Лави С. Влияние опоясания на тип цветка, количество, плотность соцветий, завязку плодов и урожайность у трех различных сортов оливок (Barnea, Picual и Souri). Австралийский журнал сельскохозяйственных исследований. 2005. 56 (8): 827–31.
- 29. Хартманн Х., редактор Влияние опоясания на тип цветка, завязку плодов и урожайность оливок.Слушания Американского общества садоводческих наук; 1950.
- 30. Фернандес-Эскобар Р., Ортис-Уркиса А, Прадо М., Рапопорт Х. Ф. Влияние азотного статуса на качество цветков оливкового дерева и продолжительность жизни семяпочек. Environ Exp Bot. 2008. 64 (2): 113–9.
- 31. Уриу К., редактор «Периоды прерывания пестика в развитии цветков оливы». Proc Amer Soc Hort Sci; 1959.
- 32. Эрель Р., Ермияху Ю., Ван Опсталь Дж., Бен-Гал А., Шварц А., Даг А. Важность оливкового масла (Olea europaea L.Питательный статус дерева от его продуктивности. Scientia Horticulturae. 2013; 159: 8–18. http://dx.doi.org/10.1016/j.scienta.2013.04.036.
- 33. Вэнс С.П., Удэ-Стоун С., Аллан Д.Л. Приобретение и использование фосфора: критические адаптации растений для обеспечения невозобновляемых ресурсов. Новый фитолог. 2003. 157 (3): 423–47.
- 34. Замски Э., Шаффер АА. Распределение фотоассимилятов в растениях и сельскохозяйственных культурах: взаимосвязь источник-поглотитель: Marcel Dekker Inc .; 1996.
- 35.Линч Дж. П., Браун К. М.. Корневые стратегии для получения фосфора. Экофизиология взаимодействия растений и фосфора: Springer; 2008. с. 83–116.
- 36. Маршнер П. Минеральное питание высших растений Маршнера. Издание третье изд. Лондон, Великобритания: Academic Press; 2012.
- 37. Зипори И., Ермияху Ю., Эрел Р., Преснов Е., Файнгольд И., Бен-Гал А. и др. Влияние уровня орошения на пищевой статус оливкового дерева. Irrig Sci. 2015: 1–11.
- 38.Фоссен П. Оливковое масло: история, производство и характеристики классических масел в мире. Hortscience. 2007. 42 (5): 1093–100.
- 39. Даг А., Ермияху Ю., Бен-Гал А., Зипори И., Капульник Ю. Реакция оливковых деревьев на арбускулярные микоризные грибы в засушливых регионах в питомниках и после трансплантации. Crop Pasture Sci. 2009. 60 (5): 427–33.
- 40. Фернандес-Эскобар Р. Оплодотворение. 2010. В: Оливковое выращивание [Интернет]. Австралия: RIRDC. 5-е издание. [267–97].
- 41. Лави С., Нашеф М., Воднер М., Харшемеш Х. Эффект дополнительного орошения старых оливковых деревьев (Olea europaea L.) cv. Сури от характеристик плодов, урожайности и масличности. Adv Hort Sci. 1990; 4: 135–8.
- 42. Мориана А., Оргаз Ф., пастор М., Феререс Э. Реакция зрелого оливкового сада на нехватку воды. J Am Soc Hortic Sci. 2003. 128 (3): 425–31.
- 43. Граттан С. Р., Беренгер М. Дж., Коннелл Дж. Х., Полито В. С., Фоссен П. М..Производство оливкового масла зависит от количества используемой воды. Agr Water Manage. 2006. 85 (1–2): 133–40. http://dx.doi.org/10.1016/j.agwat.2006.04.001.
- 44. Бен-Гал А., Ермияху У., Зипори И., Преснов Э., Ханох Э., Даг а. Влияние циклов подшипников на реакцию производства оливкового масла на орошение. Ирригационная наука. 2011. 29 (3): 253–63.
- 45. Эрель Р., Даг А., Бен-Гал А., Шварц А., Ермияху У. Цветение и завязывание плодов оливковых деревьев в ответ на азот, фосфор и калий.J Am Soc Hortic Sci. 2008. 133 (5): 639–47.
- 46. Бейтель Дж., Уриу К., Лиллеланд О. Анализ листьев лиственных плодов в Калифорнии. В: Райзенауэр Х.М., редактор. Тестирование почвы и тканей растений в Калифорнии. Bul. 1879 г. Беркли, Калифорния: Калифорнийский университет; 1983. с. 15–7.
- 47. Александр МП. Дифференциальное окрашивание абортированной и неизмененной пыльцы. Биотехника и гистохимия. 1969; 44 (3): 117–22.
- 48. Пинни К., Полито В., редакторы.Хранение оливковой пыльцы и проращивание in vitro. Международный симпозиум по выращиванию оливок 286; 1989.
- 49. Вишневецкий Ю., Замский Е., Зив М. Углеводный обмен в луковицах Nerine sarniensis, развивающихся в жидкой культуре. Physiol Plantarum. 2000. 108 (4): 361–9.
- 50. Миллер ГЛ. Использование реактива динитросалициловой кислоты для определения редуцирующего сахара. Anal Chem. 1959. 31 (3): 426–8.
- 51. Реале Л., Сгромо С., Бонофиглио Т., Орланди Ф., Форнасиари М., Ферранти Ф. и др.Репродуктивная биология оливковых сортов (Olea europaea L.) DOP Umbria. Половое растение Reprod. 2006. 19 (4): 151–61.
- 52. Ралло Л., Фернандес-Эскобар Р. Влияние прореживания сорта и цветка в соцветии на конкуренцию между оливковыми плодами. Журнал Американского общества садоводческих наук. 1985. 110 (2): 303–8.
- 53. Вулетин Селак Г., Куэвас Дж., Пинильос В., Горета Бан С., Поляк М., Перика С. Оценка эффективного периода опыления оливок (Olea europaea) с помощью флуоресцентной микроскопии и реакции растений на последовательные опыления: ограничения и недостатки существующих методик.Деревья. 2014; 28 (5): 1497–505.
- 54. Клеман С., Шавант Л., Буррус М., Одран Дж. Вариации крахмала пыльника у Lilium в процессе развития пыльцы. Половое растение Reprod. 1994. 7 (6): 347–56.
- 55. Stone JL, Thomson JD, Dent-Acosta SJ. Оценка жизнеспособности пыльцы в экспериментах по ручному опылению: обзор. Американский журнал ботаники. 1995. 82 (9): 1186–97.
- 56. Феррара Дж., Кампосео С., Палашано М., Години А., редакторы. Сравнение двух методов оценки качества пыльцы и всхожести оливок (Olea europaea L.). VI Международный симпозиум по выращиванию оливок 2012: Acta Hort.
- 57. Родригес Д., Кельтьенс В.Г., Гудриан Дж. Расширение площади листьев и производство ассимилятов у пшеницы (Triticum aestivum L.), растущей в условиях низкого содержания фосфора. Растение и почва. 1998. 200 (2): 227–40.
- 58. Ститт М., Квик РП. Фотосинтетическое разделение углерода: его регулирование и возможности манипуляции. Physiologia Plantarum. 1989. 77 (4): 633–41.
- 59. Херманс К., Хаммонд Дж. П., Уайт П. Дж., Вербрюгген Н.Как растения реагируют на нехватку питательных веществ выделением биомассы? Тенденции в растениеводстве. 2006. 11 (12): 610–7. http://dx.doi.org/10.1016/j.tplants.2006.10.007.
- 60. Руис Р., Гарсиа-Луис А., Монерри С., Гвардиола Ю.Л. Доступность углеводов по отношению к опаданию плодов в цитрусовых. Летопись ботаники. 2001. 87 (6): 805–12.
- 61. Rapoport HF, Hammami SBM, Martins P, Pérez-Priego O, Orgaz F. Влияние дефицита воды в разное время во время соцветия оливкового дерева и цветения.Экологическая и экспериментальная ботаника. 2012; 77 (0): 227–33. http://dx.doi.org/10.1016/j.envexpbot.2011.11.021.
- 62. Эрл Р., Бен-Гал А., Даг А., Шварц А., Ермияху У. Натриевая замена калия в физиологических процессах оливковых деревьев (вар. Barnea), пострадавших от засухи. Физиология деревьев. 2014; 34 (10): 1102–17. pmid: 25281842
- 63. Wissuwa M, Gamat G, Ismail AM. Влияют ли на рост корней при дефиците фосфора ограничения по источнику или поглотителю? Журнал экспериментальной ботаники.2005; 56 (417): 1943–50. pmid: 15911558
- 64. Грано Д., Дэвид-Шварц Р., Келли Г. Гексозокиназы и их роль в обнаружении сахара и развитии растений. Границы растениеводства. 2013; 4 (44).
- 65. Лоусон Т., Симкин А.Дж., Келли Г., Грано Д. Фотосинтез мезофилла и метаболизм замыкающих клеток влияет на поведение устьиц. Новый фитолог. 2014. 203 (4): 1064–81. pmid: 25077787
- 66. Келли Дж., Мошелион М., Дэвид-Шварц Р., Гальперин О., Уоллах Р., Аттиа З. и др.Гексокиназа опосредует закрытие устьиц. Заводской журнал. 2013; 75 (6): 977–88. pmid: 23738737
- 67. Ulger S, Sonmez S, Karkacier M, Ertoy N, Akdesir O, Aksu M. Определение уровней эндогенных гормонов, сахаров и минерального питания во время стадии индукции, инициации и дифференциации и их влияние на формирование цветков оливок. Регулирование роста растений. 2004. 42 (1): 89–95.
- 68. Дроссопулос Дж. Б., Ниавис, Калифорния. Сезонные изменения метаболитов в тканях листьев, коры и ксилемы оливкового дерева (Olea europaea.L) II. Углеводы. Летопись ботаники. 1988. 62 (3): 321–7.
- 69. Де ла Роса Р., Ралло Л., Рапопорт Х. Ф. Рост цветочных бутонов оливы и содержание крахмала во время зимнего покоя и весеннего распускания почек. HortScience. 2000. 35 (7): 1223–7.
- 70. Китсаки С.К., Веммос С.Н., Цуцуку К.Г. Изменения частоты дыхания, выделения этилена и содержания абсцизовой кислоты в развивающихся соцветиях и молодых плодах оливы (Olea europaea L. cv. Konservolia). J Регулятор роста растений. 1999; 18 (1): 1–7.pmid: 10467012
Структура запасов и растворимых углеводов в холодное время года в сахарном клене и поврежденных льдом деревьях двух возрастных классов после засухи
Структура запасов и растворимых углеводов в холодное время года в сахарном клене и поврежденных льдом деревьях двух возрастных классов после засухи | Treesearch Перейти к основному содержанию .gov означает, что он официальный.
веб-сайтов федерального правительства часто заканчиваются на.gov или .mil. Прежде чем делиться конфиденциальной информацией, убедитесь, что вы находитесь на сайте федерального правительства.
Сайт безопасен.
https: // гарантирует, что вы подключаетесь к официальному веб-сайту и что любая предоставляемая вами информация шифруется и безопасно передается.
Тип публикации:
Научный журнал (JRNL)
Первичные станции:
Северная научная станция
Источник:
Ботаника.87: 293-305.
Описание
В этом исследовании изучается влияние летней засухи на состав и профиль холодного сезона и растворимых углеводов у деревьев сахарного клена ( Acer saccharum Marsh.) (Возрастом 50-100 или ~ 200 лет), у которых кроны не были повреждены и не повреждены ледяной бурей 1998 года. Общие профили запаса углеводов в холодный сезон в ткани ветвей деревьев, подвергшихся стрессу от засухи (DS) и деревьев, не подвергавшихся стрессу от засухи (NDS), были в целом аналогичными, хотя наблюдались различия в количестве резервных углеводов у деревьев DS и NDS.Уровень содержания крахмала в древесных тканях деревьев DS в начале осени в холодное время года составлял примерно от одной трети до одной пятой, чем у деревьев NDS. Содержание сахара в деревьях DS в холодное время года было значительно выше, чем можно объяснить только разложением хранимого крахмала. Уровень сахарозы в деревьях DS оставался высоким на протяжении всей зимы до выхода из состояния покоя и отвердения. Концентрации зимней глюкозы и фруктозы в деревьях DS достигли пикового уровня во время выхода из состояния покоя и снизились во время обезвоживания.Профили глюкозы и фруктозы в DS и поврежденных DS деревьях в целом отличались от профилей сахарозы на протяжении безлистной фазы. Напротив, профили глюкозы и фруктозы в деревьях NDS очень похожи на профили сахарозы. Повышенные уровни сахарозы, глюкозы и фруктозы в сахарных кленах DS в холодное время года могут действовать как осморегуляторы для защиты от замерзания. Низкий уровень сахара или отсутствие повышения уровня сахара после обезвоживания деревьев DS может указывать на ограниченное изменение клеточных компонентов при адаптации к низким температурам.
Цитата
Wong, B.L .; Baggett, K. L .; Рай, А.Х. 2009. Структура запасов и растворимых углеводов в холодное время года в сахарном клене и поврежденных льдом деревьях двух возрастных классов после засухи. Ботаника 87: 293-305.
Процитировано
Примечания к публикации
- Мы рекомендуем вам также распечатать эту страницу и прикрепить ее к распечатке статьи, чтобы сохранить полную информацию о цитировании.