Применение солей — урок. Химия, 8–9 класс.
Соли находят применение в самых различных отраслях народного хозяйства, в науке и в быту. Назовём только некоторые и наиболее характерные примеры.
Применение солей в промышленности
В промышленности соли используют в качестве сырья для получения различных веществ.Хлорид натрия \(NaCl\) — для получения гидроксида натрия \(NaOH\), хлора \(Cl_2\), пищевой соды \(NaHCO_3\).
Фосфат кальция \(Ca_3(PO_4)_2\) — для получения фосфора \(P\), фосфорной кислоты \(H_3PO_4\), фосфорных удобрений.
Сульфиды служат сырьём для получения металлов (свинца \(Pb\), цинка \(Zn\), олова \(Sn\)) и серной кислоты \(H_2SO_4\).
Карбонаты натрия (сода) \(Na_2CO_3\) и калия (поташ) \(K_2CO_3\) являются сырьём в производстве стекла и моющих веществ.
Карбонат кальция \(CaCO_3\) служит сырьём в производстве негашёной извести \(CaO\), a также в металлургии при выплавке чугуна и стали для выведения примесей в шлак.
Применение солей в сельском хозяйстве
В сельском хозяйстве соли используют для улучшения качества почвы и для повышения урожайности сельскохозяйственных культур.Карбонат кальция \(CaCO_3\) вносят в почву для регулирования её кислотности.
В качестве азотных удобрений используют нитрат аммония \(NH_4NO_3\), нитрат калия \(KNO_3\), нитрат натрия \(NaNO_3\), нитрат кальция \(Ca(NO_3)_2\).
В качестве фосфорных удобрений используют гидрофосфат \(CaHPO_4\) и дигидрофосфат кальция \(Ca(H_2PO_4)_2\), гидрофосфат \((NH_4)_2HPO_4\) и дигидрофосфат аммония \(NH_4H_2PO_4\).
В качестве калийных удобрений используют хлорид калия \(KCl\), сульфат калия \(K_2SO_4\), нитрат калия \(KNO_3\). На приусадебных участках в качестве калийного удобрения часто используют золу, которая содержит до \(10\) % карбоната калия (поташа) \(K_2CO_3\).
Соли меди, цинка, марганца, железа, кобальта используют для подкормки растений в качестве микроудобрений.
Пентагидрат сульфата меди (медный купорос) \(CuSO_4\cdot5H_2O\) используется как средство борьбы с болезнями растений.
Применение солей в строительстве
Из известняка \(CaCO_3\), доломита \(CaCO_3\cdot MgCO_3\) изготавливают щебёнку, которую используют в строительстве и при ремонте дорог.Мрамор \(CaCO_3\), доломит \(CaCO_3\cdot MgCO_3\) используют при отделочных работах.
Гемигидрат сульфата кальция (жжёный гипс) \(CaSO_4\cdot0,5H_2O\) используют в качестве материала при строительных и ремонтных работах.
Силикат натрия \(Na_2SiO_3\) и калия \(K_2SiO_3\) (жидкое стекло) применяют для гидроизоляции, а также для укрепления грунтов.
Применение солей в медицине
Со времён ятрохимии (\(XVI\)–\(XVII\) в.) соли широко используются для лечения различного рода заболеваний, а также как вспомогательные средства.
Жжёный гипс \(CaSO_4\cdot0,5H_2O\) применяют для изготовления фиксирующих повязок при переломах.
Хлорид натрия \(NaCl\) используют для приготовления физиологического раствора.
Раствор перманганата калия \(KMnO_4\) используется для дезинфекции.
Нитрат серебра \(AgNO_3\) используется как дезинфицирующее и прижигающее средство.
Соли магния применяют в качестве слабительного.
Применение солей в средствах гигиены
Соли входят в состав различных средств личной гигиены.Мыла содержат натриевые соли органических кислот, например, стеарат натрия C17h45COONa.
Карбонат кальция \(CaCO_3\) используется в зубных пастах в качестве абразивной (соскабливающей) составной части.
В регионах, где ощущается дефицит фтора, для укрепления зубной эмали рекомендуется использовать зубные пасты (или растворы для полоскания), содержащие фторид натрия \(NaF\).
Соли алюминия, например, гидроксохлорид \(AlOHCl_2\), используются в дезодорантах.
Соли в средствах повышения безопасности
В зимний период для борьбы с обледенением дорог и тротуаров используют хлорид натрия \(NaCl\), хлорид кальция \(CaCl_2\), ацетат кальция \((CH_3COO)_2Ca\).В порошковых огнетушителях основу смеси, используемой для борьбы с огнём, составляют такие соли, как гидрофосфат \((NH_4)_2HPO_4\) и дигидрофосфат аммония \(NH_4H_2PO_4\), карбонат \(Na_2CO_3\) и гидрокарбонат натрия \(NaHCO_3\).
Применение солей в ювелирном деле
Декагидрат тетрабората натрия (буру) \(Na_2B_4O_7\cdot10H_2O\) используют при плавке и пайке металлов.Нитрат серебра (ляпис) \(AgNO_3\) используют для гальванического серебрения изделий.
Тетрацианоаурат(\(III\)) натрия \(Na[Au(CN)_4]\) используют для гальванического золочения изделий.
Солями являются многие драгоценные и поделочные камни. Например, жемчуг, основная составная часть которого — карбонат кальция \(CaCO_3\), изумруд \(3BeSiO_3\cdot Al_2(SiO_3)_3\), малахит\((CuOH)_2CO_3\).
www.yaklass.ru
Соль с низким содержанием натрия
Всем привет!
Чувствую себя совсем-совсем отставшей от жизни. Оказывается, уже давно продается «соль с пониженным содержанием натрия», а я только недавно узнала об этом. Точнее сказать, слышала об этом когда-то, но искренне считала шуткой, выдумкой, очередным интернет-маразмом типа водородной воды или мало осмысленным модным трендом типа угольного латте. Но оказалось, что все не совсем так. Вот и решила разобраться, что такое соль с низким содержанием натрия, какой у нее состав и чем она отличается от обычной пищевой соли.
Часть 1. Терминология
Начну с того, что термин «соль с пониженным содержанием натрия» (low sodium salt) с точки зрения химии – полная ерунда. Что такое пищевая поваренная соль – это химическое вещество хлорид натрия (также говорят «хлористый натрий). Его химическая формула – один атом натрия и один атом хлора, соединенные между собой так называемой ионной связью, то есть положительно заряженный ион натрия соединен с отрицательно заряженным ионом хлора.

Что будет, если «понизить» содержание натрия в этом веществе, убрать его? Сам по себе оставшийся ион хлора существовать не сможет, значит, к нему обязательно вместо натрия нужно присоединить что-то другое. Но если мы присоединим что-то другое, ну, например, кальций, то изменится состав. Будет уже не хлорид натрия, а хлорид кальция. Совершенно другое вещество с совершенно другими свойствами. То есть это уже будет не поваренная соль.
О какой тогда пищевой соли с пониженным содержанием натрия можно говорить? Чушь. С точки зрения терминологии и химии это бред.
Откуда же он взялся? Мое предположение — от малограмотных, но ушлых маркетологов, которые просто чётко и вовремя сыграли на стремлении людей к здоровому образу жизни.
Следим за логической цепочкой.
Большое количество людей страдает от повышенного давления и осложнений, связанным с ним. Одним из факторов, способствующим повышению давления, является избыток ионов натрия в организме. Откуда он берется? В основном, из пищи в виде хлорида натрия, то есть соли. Запрещаем (да, есть такие врачи) или сильно ограничиваем количество потребляемой соли – получаем меньше случаев повышения давления.
Тут в дело вступает маркетинг и говорит: «А хотите купить соль с низким содержанием натрия? И вам даже не придется напрягаться и контролировать, сколько соли вы насыпали в суп! Вот вам волшебный порошок».

И очень мало кому придет в голову, что такая соль – это… как бы помягче сказать… С точки зрения химии – разводилово. Не бывает пищевой соли со сниженным содержанием натрия, это нонсенс. Бывает соль с пониженным содержанием хлорида натрия, но об этом – ниже. Так что, здесь дело в химически неграмотной терминологии.
Часть 2. Что продается под видом соли с пониженным содержанием натрия
Теперь разберемся с тем, а что же бывает, что нам продают под этой заманчивой биркой а-ля здоровая соль. Разбираться, как обычно, начинаем с терминологии.
Здесь все просто. Как я уже сказала, пищевая соль – это хлорид натрия. Чтобы уменьшить поступление натрия в организм, надо его чем-то заменить, причем не один атом натрия, а всю молекулу, в которой он содержится. Вот и заменяют. Уменьшают весовое (процентное) количество хлорида натрия в пачке и добавляют другие вещества. Чаще всего это хлорид калия (в скобках скажу, что калий в разумных количествах необходим для работы сердечно-сосудистой системы, но подробно об этом не рассказываю, так как цель сегодняшней статьи не в этом).

Сколько хлорида натрия содержится в обычной пищевой соли? Обратимся к ГОСТ Р 51574-2000 «Соль поваренная пищевая. Техническая условия». Читаем:
Настоящий стандарт распространяется на пищевую поваренную соль, представляющую собой хлористый натрий и изготовленную для внутреннего рынка и экспорта.
Для сорта «Экстра»:
- Массовая доля хлористого натрия не менее 99,7%
- Массовая доля кальций-иона не более 0,02%
- Массовая доля магний-иона не более 0,01%
- Массовая доля калий-иона не более 0,02%
Посмотрите, насколько маленькое содержание примесей. В основном, вся соль – это хлористый натрий.
Также можно посмотреть более новый ГОСТ Р 58008-2017 «Соль пищевая. Термины и определения». Здесь интересны термины:
- Пищевая соль: Кристаллический продукт, содержащий не менее 97,0% хлорида натрия, используемый в качестве ингредиента в пище, представляющий собой кристаллы, гранулы, чешуйки или хлопья, зерна или куски.
- Обогащенная соль: Пищевая соль, содержащая помимо хлорида натрия регулируемое количество минералов и микроэлементов. В качестве микроэлементов обогащенная соль может содержать фтор или йод.
- Лечебно-профилактическая соль: Пищевая соль с пониженным содержанием хлорида натрия, обогащенная калием и магнием.
Обратите внимание — пониженное содержание не натрия, но хлорида натрия! О чем я и говорила выше.
Что касается ГОСТа или хотя бы технического регламента на так называемую соль с пониженным содержанием натрия, то мне не удалось его найти. Может, кто-то из вас найдет, поделитесь со мной, если не трудно. В принципе, на упаковке должен быть указан нормативный документ, но, к сожалению, я не могу посмотреть, так как у нас в городе такая соль не продается.
Нашла только вот такой документ — «Рекомендуемые (регламентируемые) уровни содержания витаминов в витаминизированных пищевых продуктах» СанПиН 42-123-4717-88, разработанный Институтом питания и утвержденный Министерством здравоохранения. Здесь говорится, что пищевая соль относится к продуктам массового потребления и ее рекомендуется обогащать йодом, фтором, калием и магнием. Подчеркиваю – это всего лишь рекомендация, а не ГОСТ и не техрегламент для производства нужного продукта.
Итак, какие добавки используются, чтобы снизить количество хлорида натрия (а, следовательно, и натрия) в поваренной соли?
Чаще всего это хлорид калия. Также могут добавляться хлориды кальция и магния.
Общемировая тенденция – поиск солезаменителей в качестве пищевых добавок, например, при производстве мясных изделий. Но с хлоридом калия, который для этого используется, есть проблема – он способствует появлению у продуктов горьковатого привкуса, который приходится маскировать дополнительными приправами и специями. Его пробуют заменять на хлориды кальция и магния, на сульфаты и фосфаты калия и магния, на хлорид аммония, лимонную кислоту и мальтодекстрин.
Ну как, дорогие боящиеся «химии»? Вы довольны? Зато без натрия, ага. Без «натурального», «природного» натрия…
Еще одна проблема, о которой не совсем внятно говорят производители «здоровой» соли – это то, что такая соль менее соленая за счет того, что собственно пищевой соли в ней меньше, а добавок больше. Следовательно, есть риск, что вы положите ее в большем количестве в пищу, чтобы добиться привычного соленого вкуса. Соответственно, а есть ли тогда смысл ее покупать, если вы получите практически то же количество натрия просто за счет большего употребления такой соли?
Недавно мне на глаза попалось исследование, где как раз пытались решить проблему вкуса. Более-менее приемлемыми оказались два варианта.
- Первый, когда получали смесь, состоящую из 96,4% хлорида натрия, 1,6% хлорида калия и 2% хлорида кальция.
- Второй — 78% хлорида натрия и 22% хлорида кальция.
Так что, глядишь, может быть когда-нибудь и такая соль появится на прилавках наших магазинов. Другое дело, что снижать поступления натрия в организм нужно не за счет увеличения поступления других веществ (добавок), а за счет уменьшения общего использования соли – меньше солить готовую пищу, меньше употреблять уже готовую сильно соленую еду – консервы, чипсы, фастфуд и т.д.
P.S. Кому интересно – вот рекомендации Всемирной организации здравоохранения на тему соли. А здесь – отличная статья на эту тему.
До встречи в следующей статье!
Наталья Брянцева
KidsChemistry теперь есть и в социальных сетях. Присоединяйтесь прямо сейчас! Одноклассники, В контакте, Facebook, Twitter.
kidschemistry.ru
Соль без натрия – что это, зачем она нужна? – свежие статьи и интересная информация
В магазинах можно увидеть новинку для здорового питания – соль без содержания натрия. Что такое заменитель соли без натрия, что входит в его состав? Чем соль без натрия лучше обыкновенной соли?
Формула обыкновенной поваренной соли знакома каждому еще со школы – это хлорид натрия. Злоупотребление продуктов с содержанием натрия приводит к его накоплению в организме и развитию заболеваний. При избыточном количестве натрия всегда наблюдается дефицит калия, так как эти элементы плохо сочетаются друг с другом. Калий невозможно получить из обработанных продуктов, так как он разрушается при очистке, приготовлении и хранении. Недостаток калия является причиной развития гипертонии и другим заболеваниям сердца и сосудов.
Когда люди садятся на солевую диету, они преследуют цель снизить количество натрия в рационе и организме, при этом им приходится мириться с непривычным пресным вкусом еды. Заменители соли без натрия изготавливаются на основе калия хлорида, внешне заменитель выглядит точно так же, как и соль, обладает похожим вкусом. Употребление соли без натрия способствует улучшению вкусовых качеств блюд, а также восполнению недостатка калия в организме, как следствие – нормализации артериального давления.
Что означает «без натрия»?
Производитель имеет право поставить на свою продукцию маркировку «без натрия», если количество натрия на порцию не превышает 5 мг. Нормой по употреблению натрия для взрослого человека является 500 мг в день, максимальное количество, которое можно употребить за день без риска для здоровья – 2400 мг, столько натрия содержится в половине столовой ложки поваренной соли. Учитывая то, что соль попадает в организм не только из солонки, определенное количество соли уже присутствует в продуктах, дневная норма постоянно превышается, в среднем люди употребляют от 2300 до 6900 мг ежедневно.
Соль с маркировкой «без натрия» помогает снизить количество натрия в рационе до нормального показателя и компенсировать недостаток калия.
Из чего состоит заменитель соли?
Основу заменителей соли без натрия составляет калия хлорид, суточная норма по употреблению калия для взрослого человека составляет 2000 мг в день. В отличие от натрия, который представлен в продуктах в избытке, калий поступает в организм в количествах намного меньше нормы. Для людей с заболеваниями почек и другими специфическими диагнозами потребность в калии увеличивается до 3500 мг в день. Роль калия хлорида заключается в поддержании водного баланса и регуляции сокращений сердца, дефицит калия проявляется в слабости и раздражительности.
Помимо калия хлорида производители добавляют в заменители соли другие полезные вещества – аминокислоты и микроэлементы. К примеру, л-лизин моно гидрохлорид необходим для здоровья костной системы, а также для преобразования жиров из продуктов питания в энергию, синтеза коллагена и других важных процессов. А глютаминовая кислота, которая тоже используется для производства заменителя соли, необходима для иммунной и нервной системы, она обеспечивает движение нейронов в головном мозге.
fiteria.ru
Химические свойства солей — урок. Химия, 8–9 класс.
1. Соли являются электролитами.
В водных растворах соли диссоциируют на положительно заряженные ионы (катионы) металлов и отрицательно заряженные ионы (анионы) кислотных остатков.
Например, при растворении кристаллов хлорида натрия в воде положительно заряженные ионы натрия и отрицательно заряженные ионы хлора, из которых образована кристаллическая решётка этого вещества, переходят в раствор:
NaCl→Na++Cl−.При электролитической диссоциации сульфата алюминия образуются положительно заряженные ионы алюминия и отрицательно заряженные сульфат-ионы:
Al2SO43→2Al3++3SO42−.2. Соли могут взаимодействовать с металлами.
В ходе реакции замещения, протекающей в водном растворе, химически более активный металл вытесняет менее активный.
Например, если кусочек железа поместить в раствор сульфата меди, он покрывается красно-бурым осадком меди. Раствор постепенно меняет цвет с синего на бледно-зелёный, поскольку образуется соль железа(\(II\)):
Fe+CuSO4→FeSO4+Cu↓.
Видеофрагмент:
взаимодействие сульфата меди(\(II\)) с железом |
При взаимодействии хлорида меди(\(II\)) с алюминием образуются хлорид алюминия и медь:
2Al+3CuCl2→2AlCl3+3Cu↓.
3. Соли могут взаимодействовать с кислотами.
Протекает реакция обмена, в ходе которой химически более активная кислота вытесняет менее активную.
Например, при взаимодействии раствора хлорида бария с серной кислотой образуется осадок сульфата бария, а в растворе остаётся соляная кислота:
BaCl2+h3SO4→BaSO4↓+2HCl.
При взаимодействии карбоната кальция с соляной кислотой образуются хлорид кальция и угольная кислота, которая тут же разлагается на углекислый газ и воду:
CaCO3+2HCl→CaCl2+h3O+CO2↑⏟h3CO3.
Видеофрагмент:
Взаимодействие кислот с солями |
4. Растворимые в воде соли могут взаимодействовать со щелочами.
Реакция обмена возможна в том случае, если в результате хотя бы один из продуктов является практически нерастворимым (выпадает в осадок).
Например, при взаимодействии нитрата никеля(\(II\)) с гидроксидом натрия образуются нитрат натрия и практически нерастворимый гидроксид никеля(\(II\)):
NiNO32+2NaOH→NiOh3↓+2NaNO3.
Видеофрагмент:
Взаимодействие нитрата никеля(\(II\)) с гидроксидом натрия |
При взаимодействии карбоната натрия (соды) с гидроксидом кальция (гашёной известью) образуются гидроксид натрия и практически нерастворимый карбонат кальция:
Na2CO3+CaOh3→2NaOH+CaCO3↓.
5. Растворимые в воде соли могут вступать в реакцию обмена с другими растворимыми в воде солями, если в результате образуется хотя бы одно практически нерастворимое вещество.
Например, при взаимодействии сульфида натрия с нитратом серебра образуются нитрат натрия и практически нерастворимый сульфид серебра:
Na2S+2AgNO3→NaNO3+Ag2S↓.
Видеофрагмент:
Взаимодействие сульфида натрия с нитратом серебра |
При взаимодействии нитрата бария с сульфатом калия образуются нитрат калия и практически нерастворимый сульфат бария:
BaNO32+K2SO4→2KNO3+BaSO4↓.
6. Некоторые соли при нагревании разлагаются.
Причём химические реакции, которые протекают при этом, можно условно разделить на две группы:
- реакции, в ходе которых элементы не изменяют степень окисления,
- окислительно-восстановительные реакции.
A. Реакции разложения солей, протекающие без изменения степени окисления элементов.
В качестве примеров таких химических реакций рассмотрим, как протекает разложение карбонатов.
При сильном нагревании карбонат кальция (мел, известняк, мрамор) разлагается, образуя оксид кальция (жжёную известь) и углекислый газ:
CaCO3⇄t°CaO+CO2↑.
Видеофрагмент:
| Разложение мела при нагревании |
Гидрокарбонат натрия (пищевая сода) при небольшом нагревании разлагается на карбонат натрия (соду), воду и углекислый газ:
2NaHCO3⇄t°Na2CO3+h3O+CO2↑.
Видеофрагмент:
| Разложение гидрокарбоната натрия |
Кристаллогидраты солей при нагревании теряют воду. Например, пентагидрат сульфата меди(\(II\)) (медный купорос), постепенно теряя воду, превращается в безводный сульфат меди(\(II\)):
CuSO4⋅5h3O→t°CuSO4+5h3O.
При обычных условиях образовавшийся безводный сульфат меди можно превратить в кристаллогидрат:
CuSO4+5h3O→CuSO4⋅5h3O
Видеофрагмент:
| Разрушение и образование медного купороса |
Аналогичная химическая реакция протекает, когда к гемигидрату сульфата кальция (жжёному гипсу) при помешивании добавляют воду. Получившаяся кашица быстро застывает в результате образования дигидрата сульфата кальция (гипса):
CaSO4⋅0,5h3O+1,5h3O→CaSO4⋅2h3O
Видеофрагмент:
| Застывание гипса |
Б. Окислительно-восстановительные реакции разложения солей.
Окислительно-восстановительные процессы протекают при разложении нитратов.
Например, при термическом разложении нитрата калия образуются нитрит этого металла и кислород:
2KN+5O−23⟶t°2KN+3O2+O2↑0
Видеофрагмент:
Разложение нитрата калия |
Разложение перманганата калия в лабораторных условиях можно использовать для получения кислорода. При разложении этой соли, кроме кислорода, образуются манганат калия и оксид марганца(\(IV\)):
2KMn+7O−24⟶t°K2Mn+6O4+Mn+4O2+O2↑0
www.yaklass.ru
хлористый натрий — Sodium chloride
«NaCl» перенаправляется сюда. Для использования в других целях, см NaCl (значения) .  Хлорид натрия в качестве минерального галита | |
 Кристаллическая структура с натрием в фиолетовый и хлорида в зеленый | |
| имена | |
|---|---|
| название IUPAC хлористый натрий | |
Другие имена
| |
| Идентификаторы | |
| 3D модель ( JSmol ) | |
| 3534976 | |
| ChEMBL | |
| ChemSpider | |
| ИКГВ InfoCard | 100.028.726 |
| Номер EC | 231-598-3 |
| 13673 | |
| KEGG | |
| MeSH | Хлорид натрия + |
| номер RTECS | VZ4725000 |
| UNII | |
| |
| свойства | |
| NaCl | |
| Молярная масса | 58,443 г / моль |
| Внешность | Бесцветные кубические кристаллы |
| запах | непахнущий |
| плотность | 2,17 г / см 3 |
| Температура плавления | 800,7 ° С (1,473.3 ° F, 1,073.8 К) |
| Точка кипения | |
| 360 г / л | |
| Растворимость в аммиаке | 21,5 г / л |
| Растворимость в метаноле | 14,9 г / л |
| -30,2 · 10 -6 см 3 / моль | |
| 1,5441 (при 589 нм) | |
| Состав | |
| Гранецентрированные ( см текст ), CF8 | |
| Fm 3 м, № 225 | |
= 564,02 м | |
| Восьмигранная (Na + ) октаэдрической (Cl — ) | |
| термохимия | |
| 50,5 Дж / (К · моль) | |
| 72,1 Дж / (К · моль) | |
| -411,12 кДж / моль | |
| Фармакология | |
| A12CA01 ( ВОЗ ) B05CB01 ( ВОЗ ), B05XA03 ( ВОЗ ), S01XA03 ( ВОЗ ) | |
| опасности | |
| Паспорт безопасности | См: страница данных |
| NFPA 704 |  |
| Смертельная доза или концентрация ( LD , LC ): | |
| 3 г / кг (перорально, крысы) | |
| Родственные соединения | |
| Фторид натрия Натрий бромид натрия йодида astatide натрия | |
| Хлорид лития калия хлорид рубидия хлорид цезий хлорида хлорид Франций | |
| Дополнительная страница данных | |
| Показатель преломления ( п ), Диэлектрическая постоянная (ε г ) и т.д. | |
Термодинамические | Фазовое поведение твердое тело-жидкость-газ |
| УФ , ИК , ЯМР , МС | |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
 N проверить ( что ?) N проверить ( что ?)  Y Y N N | |
| ссылки Infobox | |
Хлорид натрия , широко известный как соль (хотя морская соль содержит также другие химические соли ), представляет собой ионное соединение с химической формулой
Пользы
В дополнении к знакомому внутреннему использованию соли, более доминирующие применения приблизительно 250 мегатонн в год производство (данные 2008) включают в себя химические вещества и антиобледенительный.
производство химических веществ
Соль используется, прямо или косвенно, в производстве многих химических веществ, которые потребляют большую часть мирового производства.
Хлорная промышленность
Это является отправной точкой для процесса хлорщелочного , который обеспечивает мир хлор и гидроксид натрия в соответствии с химическим уравнением
- 2 NaCl + 2 H 2 O → Cl 2 + H 2 + 2 NaOH
Этот электролиз проводится в любом ртутной клетки, клетки диафрагмы или мембраны клетки. Каждый из них использовать другой метод , чтобы отделить хлор из гидроксида натрия. Другие технологии находятся в стадии разработки в связи с высоким уровнем потребления энергии при электролизе, в результате чего небольшое повышение эффективности может иметь большие экономические окупаемости. Некоторые применения хлора включают ПВХ , дезинфицирующие средства, а также растворители. Гидроксид натрия позволяет отрасль , которые производят бумагу, мыло, и алюминий.
Сода зольность промышленность
Хлорид натрия используется в процессе Сольве для получения карбоната натрия и хлорида кальция . Карбонат натрия, в свою очередь, используется для производства стекла , бикарбонат натрия , и красителей , а также множество других химических веществ. В процессе Mannheim и в процессе Hargreaves , хлорид натрия используется для производства сульфата натрия и соляной кислоты .
стандарт
Хлорид натрия имеет международный стандарт, созданный по ASTM International . Стандарт называется ASTM E534-13 и стандартные методы испытаний для химического анализа хлорида натрия. Эти методы , перечисленные процедуры обеспечения для анализа хлорида натрия , чтобы определить , является ли она подходит для предполагаемого использования и применения.
Разные виды промышленного использования
Хлорид натрия широко используется, так что даже относительно небольшие приложения могут потреблять в огромных количествах. В разведке нефти и газа, соль является важным компонентом буровых растворов в бурении скважин. Он используется для флокуляции и увеличить плотность бурового раствора , чтобы преодолеть давление высокого downwell газа. Всякий раз , когда сверло попадает в образование соли, соль добавляют в буровой раствор для насыщения раствора , с тем чтобы свести к минимуму растворение внутри солевого слоя. Соль также используется для увеличения твердения бетона в сцементированных оболочках.
В текстильной промышленности и крашения, соль используется в качестве солевого раствора для полоскания, чтобы отделить органические загрязнители, чтобы содействовать «высаливание» красящего вещества выпадает в осадок, и смешать с концентрированными красителями, чтобы стандартизировать их. Одна из его главных ролей, чтобы обеспечить положительный заряд ионов, чтобы способствовать поглощению отрицательно заряженных ионов красителей.
Он также используется в обработке алюминия , бериллий , медь , сталь и ванадий . В целлюлозно-бумажной промышленности , соль используется для отбеливания древесной массы. Он также используется , чтобы сделать хлорат натрия , который добавляется вместе с серной кислотой и водой в производстве двуокиси хлора , отличный кислород на основе отбеливающего химического вещества. Процесс диоксида хлора, который возник в Германии после Первой мировой войны, становится все более популярным из — за нагрузки на окружающую среду , чтобы уменьшить или устранить хлорсодержащие отбеливающие соединения. В дубления и кожи лечения, соль добавляют в животных кож для ингибирования активности микроорганизмов на нижней стороне шкуры и привлечь влагу обратно в шкуры.
В производстве резины, соль используются для изготовления Буны , неопрена и белого резинового типа. Соль сол ного раствор и серная кислота используют коагулировать эмульгированный латекс , изготовленный из хлорированного бутадиена .
Соль также добавляют, чтобы обеспечить почву и обеспечить стойкость к фундаменту, на котором построены шоссейные дороги. Соль действует, чтобы минимизировать эффекты сдвига вызваны в геологической среде путем изменения влажности и нагрузки трафика.
Хлорид натрия иногда используются в качестве дешевого и безопасного осушителя из — за его гигроскопичность свойств, что делает посол эффективного метода сохранения пищи исторически; соль притягивает воду из бактерий через осмотическое давление , удерживая его от воспроизведения, основным источником порчи продуктов. Несмотря на то, более эффективные осушители доступны, некоторые из них безопасны для людей , чтобы глотать.
смягчение воды
Жесткая вода содержит ионы кальция и магния , которые мешают действие мыла и способствуют накоплению масштаба или пленок щелочных минеральных отложений в бытовой и промышленном оборудовании и трубах. Коммерческое и жилое водный смягчающее устройство использует ионообменные смолы для удаления ионов нарушителей , которые вызывают твердость. Эти смолы генерируются и регенерированный с использованием хлорида натрия.
Дорожная соль
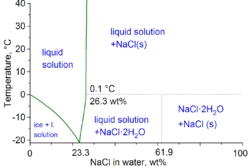 Фазовая диаграмма воды NaCl-смеси
Фазовая диаграмма воды NaCl-смесиВторое основное применение соли для борьбы с обледенением и защиты от обледенения дорог, как в зернистости бункерах и распространяются зимой обслуживания автомобилей . В ожидании снегопада, дороги оптимальны «анти-замороженный» солевой раствор (концентрированный раствор соли в воде), который предотвращает связывание между снежным льдом и поверхностью дороги. Эта процедура устраняет тяжелое использование соли после снегопада. Для борьбы с обледенением, используют смеси рассола и соли, иногда с дополнительными агентами , такими как хлорид кальция и / или хлорид магния . Использование соли или рассола становится неэффективным ниже -10 ° C (14 ° F).
 Курганы дорожной соли для использования в зимний период
Курганы дорожной соли для использования в зимний периодСоль для антиобледенительной в Соединенном Королевстве в основном происходит из одной шахты в Winsford в графстве Чешир . Перед распределением его смешивают с <100 частей на миллион ферроцианида натрия в качестве предотвращающего слипание агента, что позволяет каменной соли свободно вытекать из Скрипнув транспортных средств , несмотря на то , складированы перед использованием. В последние годы эта добавка была также использована в поваренной соли. Другие добавки были использованы в дорожной соли , чтобы уменьшить общую стоимость. Так , например, в США, побочный продукт углеводов решения от переработки сахарной свеклы смешивает с каменной солью и привязано к дорожной поверхности около 40% лучше , чем только рыхлой каменной соли. Потому что он остался на дороге больше, лечение не должно быть повторено несколько раз, экономя время и деньги.
В техническом плане физической химии, минимальная температура замерзания водно-солевой смеси -21.12 ° C (-6,02 ° F) в течение 23,31 мас% соли. Замораживание вблизи этой концентрации, однако , настолько медленно , что эвтектическая точка из -22.4 ° C (-8,3 ° F) может быть достигнута приблизительно 25% мас соли.
Воздействие на окружающую среду
Дорожная соль заканчивается в пресноводных водоемах и может нанести вред водных растений и животных, нарушая их осморегуляция способности. Вездесущность соли представляет собой проблему в любом приложении прибрежного покрытия, так как запертые соли вызывают большие проблемы в адгезии. Морские власти и кораблестроители контроля концентрации соли на поверхности во время строительства. Максимальные концентрации солей на поверхности зависят от власти и применения. ИМО регулирование в основном используется и устанавливает уровни соли до максимума 50 мг / м 2 растворимых солей , измеренных как хлорид натрия. Эти измерения проводятся с помощью теста Бресла . Засоление (увеличение соленость, известное пресноводное засоление синдром ) и последующее выщелачивание металлов увеличились является постоянной проблемой в Северной Америке и европейских свежие водных путях.
В шоссе обледенения, соль была связана с коррозией мостовых настилов, моторными транспортными средств, арматурный стержень и проволока, а также незащищенные стальные конструкции , используемые в дорожном строительстве. Поверхностный сток, автомобиль напыление, и раздутые действия также влияют на почву, растительность придорожной и местные поверхностные и подземные воды поставок. Хотя свидетельство экологической нагрузки соли было обнаружено во время пиковой нагрузки, весенних дождей и оттаивает обычно разбавленные концентрации натрия в области , где была применена соль. Исследование 2009 установлено , что примерно 70% от дорожной соли применяется в Миннеаполис-Сент — Пол районе метро сохраняется в локальном водоразделе.
подмена
Некоторые агентства подставляя пиво, патока и свекольный сок вместо дорожной соли. Авиалинии используют больше гликоль и сахар , а не соль на основе решения для борьбы с обледенением .
Пищевая промышленность и сельское хозяйство
Многие микроорганизмы не могут жить в слишком соленой среде: вода вытесняется из своих клеток путем осмоса . По этой причине , соль используется , чтобы сохранить некоторые продукты, такие как копченый бекон, рыбы или капусту.
Соль добавляется в пищу, либо производителем пищи или потребителем, в качестве усилителя вкуса, консерванта, связующего вещества, ферментации -контроль добавки, текстуры управления агентом и цветного проявителя. Потребление соли в пищевой промышленности подразделяется, в порядке убывания потребления, в другой пищевой промышленности, мясо упаковщиков, консервной, хлебопекарной, молочной и мукомольной продукции. Соль добавляется в целях содействия развития цвета в беконе, ветчине и других мясных продуктах. В качестве консерванта, соль ингибирует рост бактерий. Соль действует в качестве связующего вещества в колбасах , чтобы сформировать связывающий гель, состоящие из мяса, жира и влаги. Соль также действует как усилитель вкуса и как Тендеризер .
Во многих молочной промышленности, соль добавляется в сыром виде цвето-, fermentation- и текстуры управления агентом. Молочная подотрасль включает в себя компании , которые производят маслозавод масло, сгущенное и сгущенное молоко, замороженные десерты, мороженое, натуральный и плавленый сыр, и специальные молочные продукты. В консервировании, соль, прежде всего , добавляют в качестве усилителя вкуса и консерванта . Он также используется в качестве носителя для других ингредиентов, дегидратирующего агента, ингибитора фермента и Тендеризер. В выпечки, соль добавляют для управления скоростью ферментации в тесто для хлеба. Он также используется для укрепления клейковины (эластичная сложный белок-вода в некоторых пастах) и как усилитель вкуса, такие как долив на хлебобулочных изделиях. Категория пищевой содержит также хлебные продукты. Эти продукты состоят из размола муки и рис и производство зерновых завтраков пищи и смешанных или подготовленных мук. Соль также используется приправа агент, например , в картофельные чипсы, крендели , кошки и корм для собак.
Хлорид натрия используется в ветеринарной медицине в качестве рвоты -causing агента. Это дается как теплым насыщенным раствором. Рвота может быть также вызвана глоточным размещением небольшого количества простых солей или кристаллов соли.
Лекарственное средство
 Назальный спрей обычно делается с физиологическим раствором в качестве активного ингредиента.
Назальный спрей обычно делается с физиологическим раствором в качестве активного ингредиента.Хлорид натрия используется вместе с водой в качестве одного из основных растворов для внутривенной терапии . Назальный спрей часто содержит физиологический раствор.
Пожаротушение
 Класс-D Огнетушитель для различных металлов
Класс-D Огнетушитель для различных металловХлорид натрия является основным огнетушащим веществом в огнетушителях (Меты-LX, Супер D) , используемых на металлические горючих пожарах , такие как магний, калий, натрий и сплавы NAK (Класс D). Термопластичный порошок добавляют к смеси, а также гидроизоляции (стеараты металлов) и предотвращающего слипание материалов (трикальцийфосфат) с образованием огнетушащего вещества. Когда он применяются к огню, соль действует как поглотитель тепла, отвод тепла от огня, а также образует корочку кислорода за исключением заглушить огнь. Пластиковые добавки плавятся и помогает коре сохранять свою целостность до тех пор , пока горение металла остывает ниже его температуры воспламенения. Этот тип гасителя был изобретен в конце 1940 — х годов в качестве патрона управлением блока, хотя сохраненные версии давления сейчас популярны. Общие размеры 30 фунтов (14 кг) портативные и 350 фунтов (160 кг) колесные.
очищающее средство
Так , по крайней мере средневековые времена, люди использовали соль в качестве очищающего средства натирали бытовых поверхностей. Она также используется во многих марок шампуня , зубной пасты и популярно оледенением проездов и участки льда.
Оптическое использование
Бездефектного NaCl кристаллы имеют оптическую прозрачность примерно 90% для инфракрасного света, в частности в диапазоне от 200 нм до 20 мкм . Таким образом , они были использованы в оптических компонентах (окна и призмы) , работающих в этой области спектра, где существуют несколько не-поглощающих альтернатив и где требование к отсутствию микронеоднородностей являются менее жестким , чем в видимом диапазоне. В то время как недорогие, кристаллы NaCl мягкие и гигроскопичен — при воздействии окружающего воздуха, они постепенно покрывают «инеем». Это ограничивает применение NaCl в сухой среде, вакуумной запечатана сборка области или для кратковременного использования , такого , как прототипирования. В настоящее время материалы , такие как селенида цинка (ZnSe), которые являются сильными механически и менее чувствительны к воздействию влаги, используют вместо NaCl для инфракрасной области спектра.
Химия
Твердый хлорид натрия
В твердом хлорида натрия, каждый ион окружен шестью ионами противоположного заряда , как и ожидалось от электростатических основаниях. Окружающие ионы расположены в вершинах правильного октаэдра . На языке плотной упаковки , тем больше хлоридные ионы расположены в виде кубической решетки , тогда как меньшие натриевые ионы заполняют все зазоры кубических (октаэдрические пустоты) между ними. Та же самая базовая структура встречается во многих других соединениях , и обычно известна как галит или каменной соли кристаллической структуры. Он может быть представлен в виде гранецентрированной кубической (ГЦК) решетки с двумя атомами в основе или как две взаимопроникающие гранецентрированной кубической решеткой. Первый атом находится в каждой точке решетки, а второй атом расположен на полпути между точками решетки вдоль края элементарной ячейки ГЦКА.
Твердый хлорид натрия имеет температуру плавления 801 ° С. Теплопроводность хлорида натрия в зависимости от температуры имеет максимум 2,03 Вт / (К) см при 8 К (-265.15 ° C; -445,27 ° F) и уменьшается до 0,069 при 314 К (41 ° С; 106 ° F ). Кроме того , уменьшается с легированием .
Водные растворы
Притяжение между Na + и Cl — ионы в твердом настолько сильны , что только сильно полярные растворители , такие как вода растворения NaCl хорошо.
При растворении в воде, структура хлорида натрия распадается как Na + и Cl — ионы становятся в окружении полярных молекул воды. Эти растворы состоят из аквакомплексов с формулой [Na (H 2 O) 8 ] + , с Na-O расстоянием 250 часов . Ионы хлорида также сильно сольватирован, каждый из которых окружен в среднем на 6 молекул воды. Растворы хлорида натрия имеют очень разные свойства от чистой воды. Точка замерзания составляет -21.12 ° C (-6,02 ° F) в течение 23,31 % масс соли, а температура кипения насыщенного солевого раствора находится вблизи 108,7 ° C (227,7 ° F). Из холодных растворов, соль кристаллизуется в качестве дигидрата NaCl · 2H 2 O.
Вид одной плиты из NaCl (Н 2 О) 2 (красный = О, белый = Н, зеленый = Cl, фиолетовый = Na).рН растворов хлорида натрия
РН раствора хлорида натрия остается ≈7 вследствие чрезвычайно слабой основность Cl — ион, который является сопряженным основанием сильной кислоты HCl. Другими словами, NaCl , не оказывает никакого влияния на рН системы в разбавленных растворах , где эффекты ионных коэффициентов силы и активности пренебрежимо малы.
Неожиданные стабильные стехиометрические варианты
Поваренная соль имеет 1: 1 молярное соотношение натрия и хлора. В 2013 годе , соединение натрия и хлорид различной стехиометрии было обнаружено; пять новых соединений были предсказаны (например, Na 3 Cl, Na 2 Cl, Na 3 Cl 2 , NaCl , 3 и NaCl , 7 ). Существование некоторых из них было подтверждено экспериментально при высоких давлениях: кубической и орторомбической NaCl , 3 и двумерной металлической тетрагональной Na 3 Cl. Это указывает на то, что соединения , нарушающие химическую интуицию возможны, в простых системах при nonambient условиях.
Вхождение
Небольшие частицы морской соли являются доминирующими ядра конденсации облаков далеко в море, которые позволяют образование облаков в противном случае , не загрязненного воздуха .
производство
Соль в настоящее время массового производства путем выпаривания из морской воды или рассола из рассола скважин и соленых озер . Добыча каменной соли также является основным источником. Китай является основным поставщиком в мире соли. В 2017 году мировое производство оценивается в 280 млн тонн , в первую пятерку производителей (в миллионах тонн) являются Китай (68,0), США (43,0), Индия (26,0), Германия (13,0) и Канада (13,0). Соль также является побочным продуктом калия добычи.
Смотрите также
Рекомендации
![]() Эта статья включает в себя материалы для общественности области из Геологической службы США документа: «Соль» (PDF) .
Эта статья включает в себя материалы для общественности области из Геологической службы США документа: «Соль» (PDF) .
Статьи, ссылающиеся источники
внешняя ссылка
 | Викискладе есть медиафайлы по теме NaCl . |
ru.qwertyu.wiki
Способы получения кислых, основных и комплексных солей — урок. Химия, 8–9 класс.
Способы получения кислых солей
1. Кислые соли образуются при взаимодействии средних солей с кислотами.
Например, если к раствору сульфата натрия добавить раствор серной кислоты, из полученного раствора можно выкристаллизовать гидросульфат натрия:
Na2SO4+h3SO4→2NaHSO4.
Нерастворимые в воде природные карбонаты (известняк и другие) в присутствии воды и углекислого газа (угольной кислоты) превращаются в растворимые гидрокарбонаты.
Например, карбонат кальция превращается в гидрокарбонат:
CaCO3+h3O+CO2⏟h3CO3→CaHCO32.
В результате этой химической реакции возрастает жёсткость природной воды, обусловленная присутствием растворимых солей кальция и магния, образуются карстовые пещеры, а также происходит разрушение коралловых рифов.
Видеофрагмент:
Взаимопревращение карбонатов и гидрокарбонатов |
2. Кислые соли образуются при неполной нейтрализации многоосновных кислот.
Например, при взаимодействии гидроксида натрия с серной кислотой в соотношении количества вещества \(1 : 1\) образуется гидросульфат натрия:
NaOH+h3SO4→NaHSO4+h3O.
Если гидроксид кальция взаимодействует с фосфорной (ортофосфорной) кислотой в
соотношении количества вещества \(1 : 2\), образуется дигидрофосфат кальция:
CaOh3+2h4PO4→Cah3PO42+2h3O.
3. Кислые соли образуются при действии избытка кислотного оксида на основание.
Например, если гидроксид натрия реагирует с оксидом углерода(\(IV\)) в соотношении количества вещества \(1 : 1\), образуется гидрокарбонат натрия:
NaOH+CO2→NaHCO3.
Способы получения основных солей
1. Основные соли образуются при взаимодействии щелочей с растворимыми в воде солями.Например, если смешать растворы хлорида кальция и гидроксида кальция, из полученного раствора можно выкристаллизовать гидроксохлорид кальция:
CaOh3+CaCl2→2CaOHCl.
2. Основные соли образуются при взаимодействии избытка основания с кислотой.
CaOh3+HCl→CaOHCl+h3O.
3. Гидроксокарбонат меди(\(II\)), свинца(\(II\)), цинка и некоторых других металлов образуется при взаимодействии растворов солей этих металлов с растворами карбонатов.
Например, при взаимодействии раствора сульфата меди(\(II\)) (медного купороса) с раствором карбоната натрия (соды) образуется осадок гидроксокарбоната меди:
2CuSO4+2Na2CO3+h3O→CuOh3CO3↓+CO2↑+2Na2SO4.
Видеофрагмент:
Получение основного карбоната меди |
Получение комплексных солей
1. Комплексные соли образуются при действии растворов щелочей на амфотерные гидроксиды.Например, при действии раствора гидроксида калия на гидроксид цинка образуется тетрагидроксоцинкат калия:
2KOH+ZnOh3→K2ZnOh5.
При действии разбавленного раствора гидроксида натрия на гидроксид алюминия образуется тетрагидроксоалюминат натрия:
NaOH+AlOh4→NaAlOh5.
2. Ещё один способ получения комплексных солей — действие растворов щелочей на амфотерные оксиды.
Например, при действии раствора гидроксида натрия на оксид цинка образуется тетрагидроксоцинкат натрия:
2NaOH+ZnO+h3O→Na2ZnOh5.
Комплексные соли образуются также при растворении в щёлочи цинка или алюминия.
Одним из продуктов реакции в этом случае является водород:
2NaOH+Zn+2h3O→Na2ZnOh5+h3↑,
2NaOH+2Al+6h3O→2NaAlOh5+3h3↑.
www.yaklass.ru
хлорид натрия это щёлочь или соль
Хлори́д на́трия — химическое соединение NaCl, натриевая соль соляной кислоты, хлористый натрий. Хлорид натрия известен в быту под названием поваренной соли, основным компонентом которой он является. Хлорид натрия в значительном количестве содержится в морской воде, создавая её солёный вкус. Встречается в природе в виде минерала галита (каменная соль) . Чистый хлорид натрия имеет вид бесцветных кристаллов, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Поваренная соль
Соль конечно:)
помойму это даже ребенку ясно что соль
touch.otvet.mail.ru
