ХиМиК.ru — ГОРМОНЫ — Химическая энциклопедия
ГОРМОНЫ животных (от греч. hormao-привожу в движение, побуждаю), в-ва, вырабатываемые специализиров. клетками и железами внутр. секреции и регулирующие обмен в-в отдельных органов и всего организма в целом. Для всех гормонов характерна большая специфичность действия и высокая биол. активность.Химическое строение. Известно более 40 гормонов человека и животных (см. табл.). По хим. строению их делят на три группы: производные аминокислот, стероидные и пептидные.
Гормоны первой группы (напр., адреналин, тироксин)по структуре близки
к тирозину и триптофану (см. Аминокислоты). Стероидные гормоны, содержащие
в своей основе структуру циклопентанпергидрофенантренового кольца, по числу
углеродных атомов делят на три семейства: гормоны коры надпочечников и прогестерон
(С21-стероиды) — производные прегнана (ф-ла I), мужские половые
гормоны (С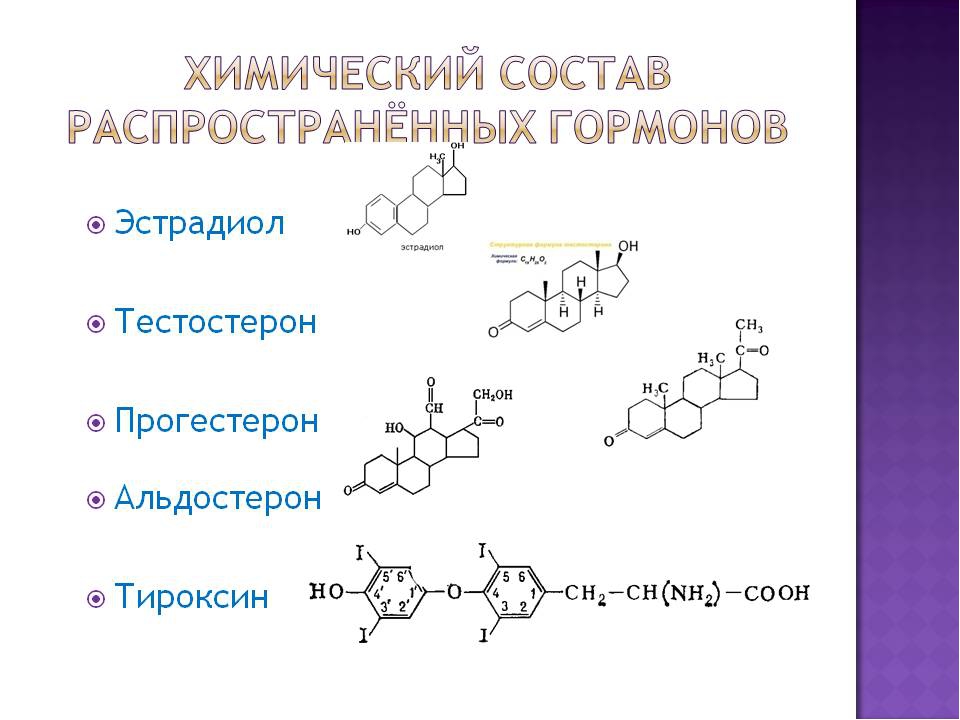
Пептидные гормоны условно делят на четыре подгруппы: пептиды (вазопрессин, окситоцин и др.), полипептиды (адренокортикотропин, глюкагон, инсулин, кальцитопин и др.), простые белки (напр., плацентарный лактоген, пролактин, соматотропин)и гликопротеины (лютеинизирующий гормон, фолликулостимулирующий гормон и др.). Последние состоят из двух субъединиц, причемсубъединицы во всех гликопротеинных гормонах имеют очень сходное строение, тогда как строениесубъединиц характерно для каждого гормона этой подгруппы и определяет специфику его действия.
Изучается взаимосвязь между структурой и ф-цией пеп-тидных гормонов. Для этого при помощи фрагментации молекулы выявляют аминокислотные звенья, к-рые определяют биол. активность гормонов, путем хим. модификаций молекул гормонов устанавливают роль разл. функц. групп.
Механизм действия. Стероидные гормоны, проникнув в клетку, связываются с
цитоплазматич.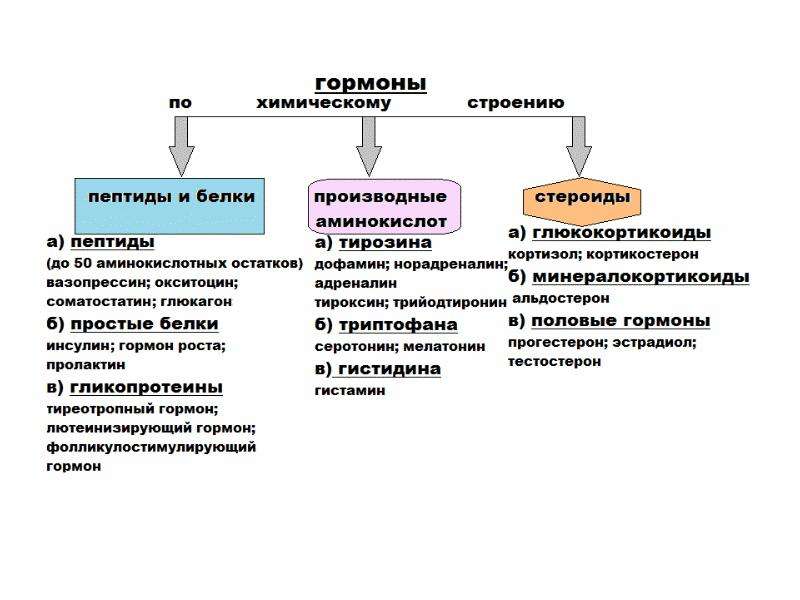 рецепторами, образовавшийся комплекс транспортируется в
ядро, где он связывается с белками хроматина и регулирует транскрипцию
определенных генов. Гормоны щитовидной железы также действуют непосредственно
на ядро, но, в отличие от стероидных, после проникания в клетку сразу связываются
с ядерными рецепторами. Все остальные гормоны взаимод. с рецепторами, находящимися
на клеточной пов-сти. Действие подавляющего большинства этих гормонов опосредовано
изменением в клетке концентрации циклич. 3′,5′-аденозинмонофосфата (ц-АМФ).
Связывание гормонов с-рецептором, находящимся на клеточной пов-сти, вызывает
активацию фермента аденилатциклазы, катализирующего превращение АТФ в ц-АМФ;
последний взаимод. с регуляторной субъединицей фермента протеинкиназы и
вызывает ее отщепление от каталитич. субъединицы. Освободившаяся субъединица
протеинкиназы катализирует фосфорилирование ряда белков, в результате чего
изменяются конформация нёк-рых структурных белков и активность мн.
рецепторами, образовавшийся комплекс транспортируется в
ядро, где он связывается с белками хроматина и регулирует транскрипцию
определенных генов. Гормоны щитовидной железы также действуют непосредственно
на ядро, но, в отличие от стероидных, после проникания в клетку сразу связываются
с ядерными рецепторами. Все остальные гормоны взаимод. с рецепторами, находящимися
на клеточной пов-сти. Действие подавляющего большинства этих гормонов опосредовано
изменением в клетке концентрации циклич. 3′,5′-аденозинмонофосфата (ц-АМФ).
Связывание гормонов с-рецептором, находящимся на клеточной пов-сти, вызывает
активацию фермента аденилатциклазы, катализирующего превращение АТФ в ц-АМФ;
последний взаимод. с регуляторной субъединицей фермента протеинкиназы и
вызывает ее отщепление от каталитич. субъединицы. Освободившаяся субъединица
протеинкиназы катализирует фосфорилирование ряда белков, в результате чего
изменяются конформация нёк-рых структурных белков и активность мн.
Получение. Небелковые гормоны, пептидные гормоны небольшой мол. массы и активные фрагменты нек-рых полипептидных гормонов синтезируют. Полипептидные и белковые гормоны получают гл. обр. экстрагированием из желез убойного скота и послед. очисткой. Разработаны способы получения нек-рых пептидных гормонов (напр., инсулина и соматотропина) с использованием генной инженерии. Метод основан на выделении гена соответствующего гормона и включении его в геном бактериальных клеток, приобретающих т. обр. способность к синтезу данного гормона. В результате размножения образуются большие массы бактерий, активно синтезирующих гормоны.
Применение. Наиб. широко гормоны используют при эндокринных заболеваниях,
связанных с недостатком или отсутствием в организме эндогенного гормона (напр.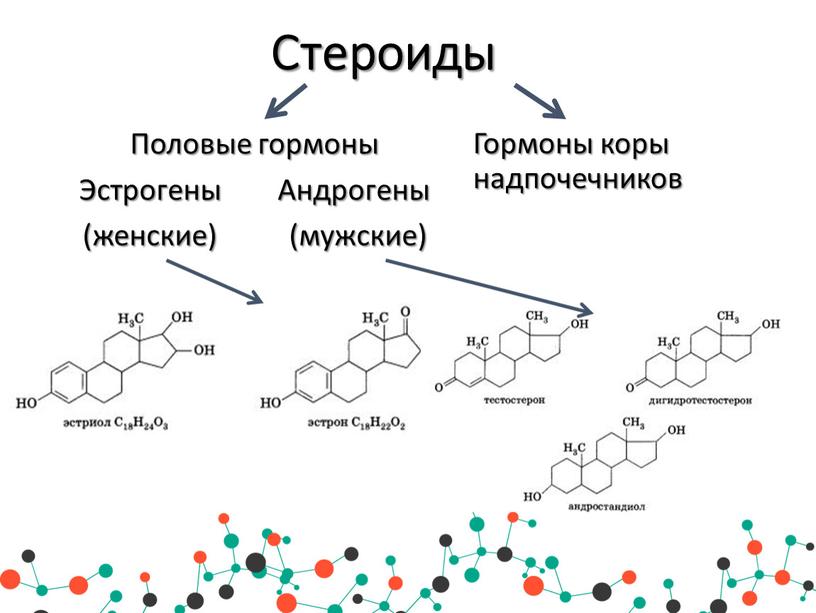

ХИМИЧЕСКАЯ КЛАССИФИКАЦИЯ ГОРМОНОВ ПОЗВОНОЧНЫХ
Методы количеств. определения. Концентрация гормонов в крови и тканях очень
мала (10-6-10-10 М), поэтому для их определения требуются
высокочувствит. методы. Широко используются радиолигандные методы, основанные
на конкурентном связывании меченого и немеченого гормонов с разл. белками: антителами,
транспортными белками (напр., связывание кортизола, прогестерона и половых
гормонов с соответствующими транспортными белками крови) или рецепторами (напр.,
связывание адренокортикотропина с мембранами надпочечников и лютеинизирующего
гормона с мембранами семенников крыс). Для анализа небелковых гормонов применяют хим.
методы; напр., стероидные гормоны и адреналин определяют флуорометрич. и колориметрич.
Лит. Биохимия гормонов и гормональной регуляции, М., 1976; Взаимодействие
гормонов с рецепторами, пер. с англ., М., 1979; Кли мов П. К., в кн.: Физиология
эндокринной системы. Л., 1979, с. 414-48; Савченко О. Н., Гормоны половых
желез, там же, с. 352-71; Hormones and cell regulation, Amst., 1981 (Proc.
of the 5
===
Исп. литература для статьи «ГОРМОНЫ»: нет данных
Страница «ГОРМОНЫ» подготовлена по материалам химической энциклопедии.
§ 17. Гормоны
Глава VI. БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
§ 17. ГОРМОНЫ
Общие представления о гормонах
Слово гормон происходит от греч. гормао — возбуждать.
Гормоны – это органические вещества, выделяемые железами внутренней секреции в небольших количествах, транспортируемые кровью к клеткам-мишеням других органов, где они проявляют специфическую биохимическую или физиологическую реакцию. Некоторые гормоны синтезируются не только в эндокринных железах, но и клетками других тканей.
Для гормонов характерны следующие свойства:
a) гормоны секретируются живыми клетками;
b) секреция гормонов осуществляется без нарушения целостности клетки, они поступают непосредственно в кровяное русло;
c) образуются в очень малых количествах, их концентрация в крови составляет 10-6 – 10-12 моль/л, при стимуляции секреции кокого-либо гормона его концентрация может возрасти на несколько порядков;
d) гормоны обладают высокой биологической активностью;
e) каждый гормон действует на определенные клетки-мишени;
f) гормоны связываются со специфическими рецепторами, образуя гормон-рецепторный комплекс, который определяет биологический ответ;
g) гормоны имеют небольшой период полужизни, обычно несколько минут и не более одного часа.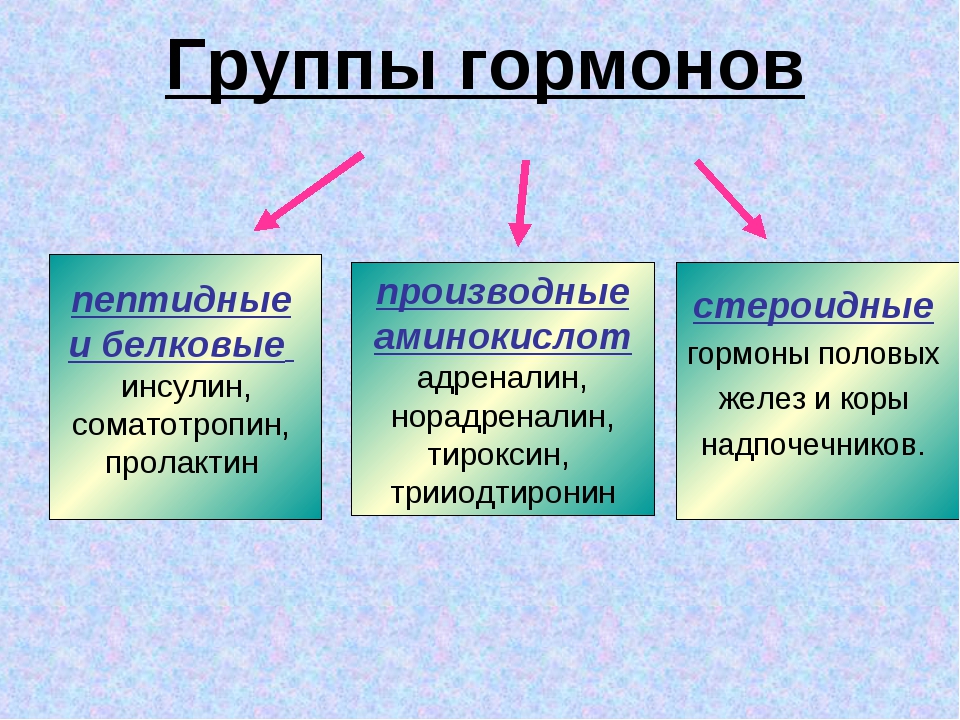
Гормоны по химическому строению делятся на три группы: белковые и пептидные гормоны, стероидные гормоны и гормоны, являющиеся производными аминокислот.
Пептидные гормоны представлены пептидами с небольшим числом аминокислотных остатков. Белки-гормоны содержат до 200 аминокислотных остатков. К их числу относятся гормоны поджелудочной железы инсулин и глюкагон, гормон роста и др. Большинство белковых гормонов синтезируются в виде предшественников – прогормонов, не обладающих биологической активностью. В частности, инсулин синтезируется в виде неактивного предшественника препроинсулина, который в результате отщепления 23 аминокислотных остатков со стороны N-конца превращается в проинсулин и при удалении еще 34 аминокислотных остатков – в инсулин (рис. 58).
Рис. 58. Образование инсулина из предшественника.
К производным аминокислот относятся гормоны адреналин, норадреналин, тироксин, трииодтиронин. К стероидным принадлежат гормоны коры надпочечников и половые гормоны (рис.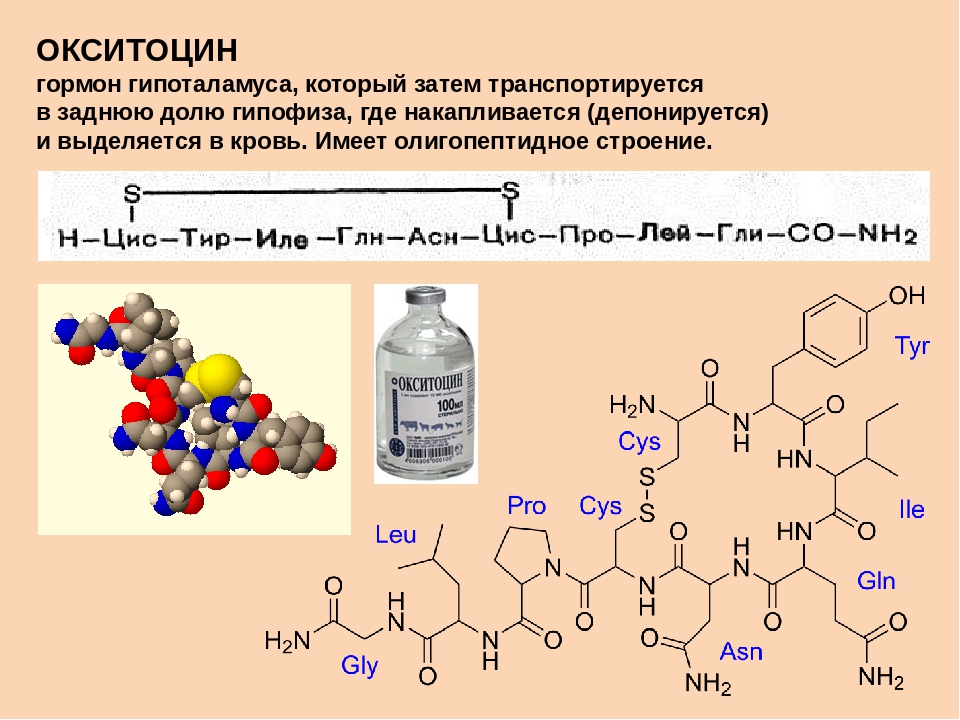 3).
3).
Регуляция секреции гормонов
Верхнюю ступень в регуляции секреции гормонов занимает гипоталамус – специализированная область мозга (рис. 59). Этот орган получает сигналы из центральной нервной системы. В ответ на эти сигналы гипоталамус выделяет ряд регуляторных гипоталамических гормонов. Их называют рилизинг-факторы. Это пептидные гормоны, состоящие из 3 – 15 аминокислотных остатков. Рилизинг-факторы поступают в переднюю долю гипофиза – аденогипофиз, расположенный непосредственно под гипоталамусом. Каждый гипоталамический гормон регулирует секрецию какого-либо одного гормона аденогипофиза. Одни рилизинг-факторы стимулируют секрецию гормонов, их называют либеринами, другие, наоборот, тормозят, это – статины. В случае стимуляции гипофизом в кровь выделяются так называемые тропные гормоны, стимулирующие деятельность других желез внутренней секреции. Те в свою очередь начинают выделять собственные специфические гормоны, которые воздействуют на соответствующие клетки-мишени. Последние в соответствии с полученным сигналом вносят коррективы в свою деятельность. Надо отметить, что циркулирующие в крови гормоны в свою очередь тормозят деятельность гипоталамуса, аденогипофиза и желез, в которых они образовались. Такой способ регуляции носит название регуляции по принципу обратной связи.
Последние в соответствии с полученным сигналом вносят коррективы в свою деятельность. Надо отметить, что циркулирующие в крови гормоны в свою очередь тормозят деятельность гипоталамуса, аденогипофиза и желез, в которых они образовались. Такой способ регуляции носит название регуляции по принципу обратной связи.
Рис. 59. Регуляция секреции гормонов
Интересно знать! Гипоталамические гормоны, по сравнению с другими гормонами, выделяются в наименьших количествах. Например, для получения 1 мг тиролиберина (стимулирующего деятельность щитовидной железы) потребовалось 4 т ткани гипоталамуса.
Механизм действия гормонов
Гормоны отличаются по своему быстродействию. Одни гормоны вызывают быстрый биохимический или физиологический ответ. Например, печень начинает выделять глюкозу в кровь после появления адреналина в кровяном русле уже через несколько секунд. Ответ же на действие стероидных гормонов своего максимума достигает через несколько часов и даже дней.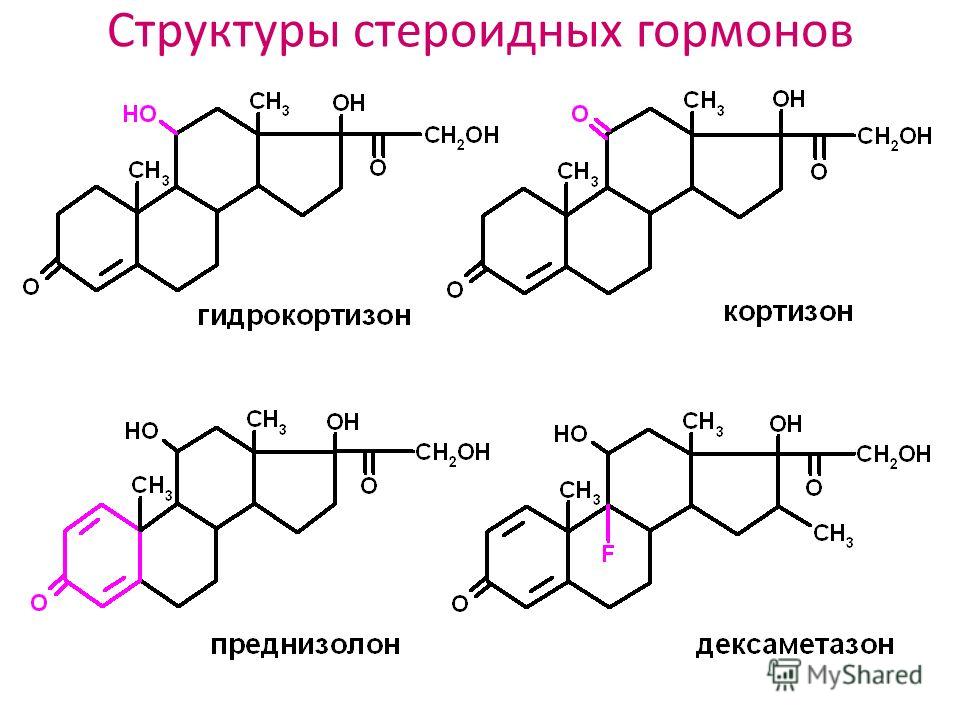 Столь значительные различия в скорости ответа на введение гормона связаны с различным механизмом их действия. Действие стероидных гормонов направлено на регуляцию транскрипции. Стероидные гормоны легко проникают через клеточную мембрану в цитоплазму клетки. Там они связываются со специфическим рецептором, образуя гормон-рецепторный комплекс. Последний, попадая в ядро, взаимодействует с ДНК и активирует синтез иРНК, которая далее транспортируется в цитоплазму и инициирует синтез белка (рис. 60.). Синтезированный белок определяет биологический ответ. Аналогичным механизмом действия обладает и гормон щитовидной железы тироксин.
Столь значительные различия в скорости ответа на введение гормона связаны с различным механизмом их действия. Действие стероидных гормонов направлено на регуляцию транскрипции. Стероидные гормоны легко проникают через клеточную мембрану в цитоплазму клетки. Там они связываются со специфическим рецептором, образуя гормон-рецепторный комплекс. Последний, попадая в ядро, взаимодействует с ДНК и активирует синтез иРНК, которая далее транспортируется в цитоплазму и инициирует синтез белка (рис. 60.). Синтезированный белок определяет биологический ответ. Аналогичным механизмом действия обладает и гормон щитовидной железы тироксин.
Действие пептидных, белковых гормонов и адреналина направлено не на активацию синтеза белка, а на регуляцию активности ферментов или других белков. Эти гормоны взаимодействуют с рецепторами, находящимися на поверхности клеточной мембраны. Образовавшийся гормон-рецепторный комплекс запускает серию химических реакций. В результате происходит фосфорилирование некорых ферментов и белков, вследствие которого изменяется их активность. В итоге наблюдается биологический ответ (рис. 61).
В итоге наблюдается биологический ответ (рис. 61).
Рис. 60. Механизм действия стероидных гормонов
Рис. 61. Механизм действия пептидных гормонов
Гормоны – производные аминокислот
Как отмечалось выше, к гормонам, являющимся производными аминокислот, относятся гормоны мозгового слоя надпочечников (адреналин и норадреналин) и гормоны щитовидной железы (тироксин и трииодтиронин) (рис. 62). Все эти гормоны являются производными тирозина.
Рис. 62. Гормоны – производные аминокислот
Органами–мишенями адреналина являются печень, скелетные мышцы, сердце и сердечно-сосудистая система. Близок по структуре к адреналину и другой гормон мозгового слоя надпочечников – норадреналин. Адреналин ускоряет ритм сердца, повышает кровяное давление, стимулирует расщепление гликогена печени и увеличивает содержание глюкозы в крови, обеспечивая, таким образом, мышцы топливом. Действие адреналина направлено на то, чтобы подготовить организм к экстремальным условиям. В состоянии тревоги концентрация адреналина в крови может увеличиться почти в 1000 раз.
Действие адреналина направлено на то, чтобы подготовить организм к экстремальным условиям. В состоянии тревоги концентрация адреналина в крови может увеличиться почти в 1000 раз.
Щитовидная железа, как отмечали выше, секретирует два гормона – тироксин и трииодтиронин, их соответственно обозначают Т4 и Т3. Главным результатом действия этих гормонов является увеличение скорости основного обмена.
При повышенной секреции Т4 и Т3 развивается так называемая Базедова болезнь. В таком состоянии скорость обмена веществ увеличена, пища сгорает быстро. Больные выделяют больше тепла, им свойственна повышенная возбудимость, у них наблюдаются тахикардия, потеря массы тела. Дефицит гормонов щитовидной железы у детей приводит к задержке роста и умственного развития – кретинизму. Недостаточность иода в пище, а иод входит в состав этих гормонов (рис. 62), вызывает увеличение щитовидной железы, развитие эндемического зоба.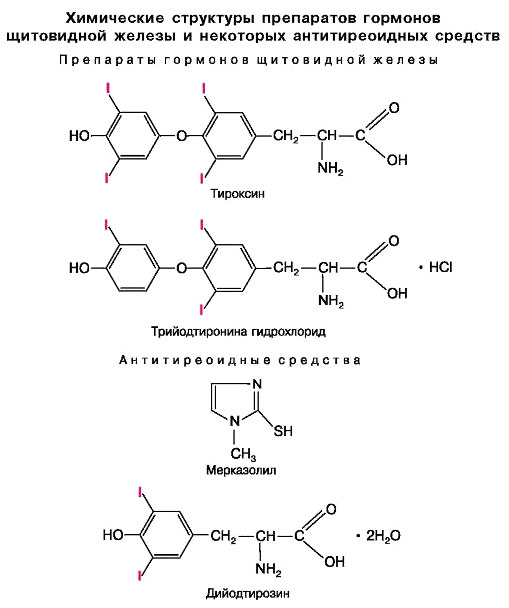 Добавление иода в пищу приводит к уменьшению зоба. С этой целью в Беларуси в состав пищевой соли вводят иодид калия.
Добавление иода в пищу приводит к уменьшению зоба. С этой целью в Беларуси в состав пищевой соли вводят иодид калия.
Интересно знать! Если поместить головастиков в воду, не содержащую иод, то их метаморфоз задерживается, они достигают гигантских размеров. Добавление иода в воду приводит к метаморфозу, начинается редукция хвоста, появляются конечности, они превращаются в нормальную взрослую особь.
Пептидные и белковые гормоны
Это наиболее разнообразная группа гормонов. К ним относятся рилизинг-факторы гипоталамуса, тропные гормоны аденогипофиза, гормоны эндокринной ткани поджелудочной железы инсулин и глюкагон, гормон роста и многие другие.
Главной функцией инсулина является поддержание определенного уровня глюкозы в крови. Инсулин способствует поступлению глюкозы в клетки печени и мышц, где она в основном превращается в гликоген. При недостатке выработки инсулина или полном его отсутствии развивается заболевание сахарный диабет. При этом заболевании ткани больного не могут поглощать глюкозу в достаточных количествах, несмотря на ее повышенное содержание в крови. У больных происходит выведение глюкозы с мочой. Это явление получило название «голод среди изобилия».
При этом заболевании ткани больного не могут поглощать глюкозу в достаточных количествах, несмотря на ее повышенное содержание в крови. У больных происходит выведение глюкозы с мочой. Это явление получило название «голод среди изобилия».
Глюкагон оказывает противоположное инсулину действие, он повышает содержание глюкозы в крови, способствует распаду гликогена в печени с образованием глюкозы, поступающей затем в кровь. В этом его действие сходно с действием адреналина.
Секретируемый аденогипофизом гормон роста, или соматотропин, ответствен за рост скелета и увеличение массы тела человека и животных. Недостаточность этого гормона приводит к карликовости, избыточная же его секреция выражается в гигантизме, или акромегалии, при которой происходит усиленный рост кистей рук, ступней ног, лицевых костей.
Стероидные гормоны
Как отмечено выше, к стероидным гормонам принадлежат гормоны коры надпочечников и половые гормоны (рис. 3).
3).
В коре надпочечников синтезируются свыше 30 гормонов, их называют также кортикоидами. Кортикоиды делят на три группы. Первая группа – это глюкокортикоиды, они регулируют углеводный обмен, оказывают противовоспалительное и антиаллергическое действие. Вторую группу составляют минералокортикоиды, они поддерживают, главным образом, водно-солевой баланс в организме. К третьей группе относятся кортикоиды, занимающие промежуточное положение между глюкокортикоидами и минералокортикоидами.
Среди половых гормонов различают андрогены (мужские половые гормоны) и эстрогены (женские половые гормоны). Андрогены стимулируют рост и созревание, поддерживают функционирование репродуктивной системы и формирование вторичных половых признаков. Эстрогены регулируют активность женской репродуктивной системы.
Гормоны щитовидной железы
- Т3 общий
- Т4 общий
- Т3 свободный
- Т4 свободный
- ТТГ (тиреотропный)
- Антитела к тиреоглобулину(АТ-ТГ)
- Антитела к тиреопероксидазе (АТ-ТПО)
Щитовидная железа и ее гормоны совместно с нервной и иммунной системами принимает участие в регуляции работы всех органов человека (сердца, головного мозга, почек и т. д.). В отличии от большинства гормонов, которые действуют только на определенные клетки отдельных органов (например, для эстрадиола это половые органы), гормоны щитовидной железы необходимы для нормальной работы всем тканям и всем органам без исключения. Приникая внутрь клетки, гормон направляется в ядро, где связываясь с определенными участками на хромосомах, активирует комплекс реакций, отвечающих за процессы окисления и восстановления. Гормоны щитовидной железы являются основными регуляторами расхода энергии в организме, и поддержание их концентрации на необходимом уровне крайне важно для нормальной деятельности всех органов и систем. Для синтеза гормонов щитовидной железы необходимы два обязательных компонента — йод и аминокислота тирозин. Без йода синтез гормонов полностью прекращается, поэтому крайне важно обеспечить получение достаточного количества йода с пищей. Тирозин также поступает в организм с пищей, он – основа не только гормонов щитовидной железы, но и адреналина, меланина, дофамина.
д.). В отличии от большинства гормонов, которые действуют только на определенные клетки отдельных органов (например, для эстрадиола это половые органы), гормоны щитовидной железы необходимы для нормальной работы всем тканям и всем органам без исключения. Приникая внутрь клетки, гормон направляется в ядро, где связываясь с определенными участками на хромосомах, активирует комплекс реакций, отвечающих за процессы окисления и восстановления. Гормоны щитовидной железы являются основными регуляторами расхода энергии в организме, и поддержание их концентрации на необходимом уровне крайне важно для нормальной деятельности всех органов и систем. Для синтеза гормонов щитовидной железы необходимы два обязательных компонента — йод и аминокислота тирозин. Без йода синтез гормонов полностью прекращается, поэтому крайне важно обеспечить получение достаточного количества йода с пищей. Тирозин также поступает в организм с пищей, он – основа не только гормонов щитовидной железы, но и адреналина, меланина, дофамина.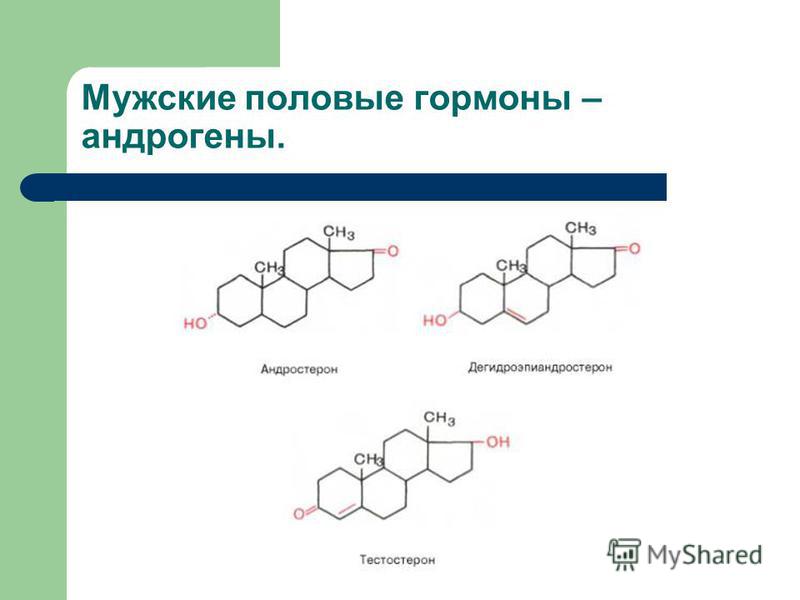
Т3 и Т4. Основные два гормона, которые вырабатывает щитовидная железа – трийодтиронин и тетрайодтиронин (тироксин). В состав трийодтиронина входят 3 молекулы йода, а в состав тироксина — 4 молекулы. Сокращённо эти гормоны называют, соответственно, Т3 и Т4. В клетках и тканях нашего организма Т4 постепенно превращается в Т3, который является главным биологически активным гормоном, непосредственно влияющим на обмен веществ. Тем не менее, тироксин (Т4) составляет около 90 % от общего количества гормонов, выделяемых щитовидной железой.
Свободный Т3 и Т4. Гормоны щитовидной железы перед попаданием в кровь должны быть связаны с транспортными белками-глобулинами (для того чтоб не «вымываться» почками), но для попадания внутрь клетки и в ткани они должны освободиться от этого «транспорта». Т.о. в крови Т3 и Т4 встречаются либо в свободном, либо в связанном виде. Уровень свободных гормонов составляет менее 0,1% от общего их количества, но именно свободная фракция гормонов является наиболее биологически активной, и именно они обеспечивают все эффекты гормонов щитовидной железы.
Анализ уровня основных гормонов Т3, Т4 и их свободных вариантов — первый и самый главный шаг в определении качества работы щитовидной железы при любых подозрениях на её заболевание.
Тиреотропный гормон (ТТГ) – основной регулятор функции щитовидной железы. Вырабатывается гипофизом – небольшой железой, расположенной на нижней поверхности головного мозга. ТТГ управляет выработкой гормонов щитовидной железы (тироксина и трийодтиронина), которые, в свою очередь, регулируют процессы образования энергии в организме. Механизм обратной связи, позволяет поддерживать стабильный уровень этих гормонов — когда их содержание в крови понижается, гипоталамус определяет этот факт и даёт сигнал гипофизу на синтез ТТГ. Повышение концентрации ТТГ, в свою очередь, стимулирует выработку тиреоидных гормонов щитовидной железой. Обратный процесс происходит аналогично.Дисфункция гипофиза может вызывать неуправляемое повышение или понижение уровня тиреотропного гормона, провоцируя тем самым, щитовидную железу на выработку тироксина и трийодтиронина в аномальных количествах.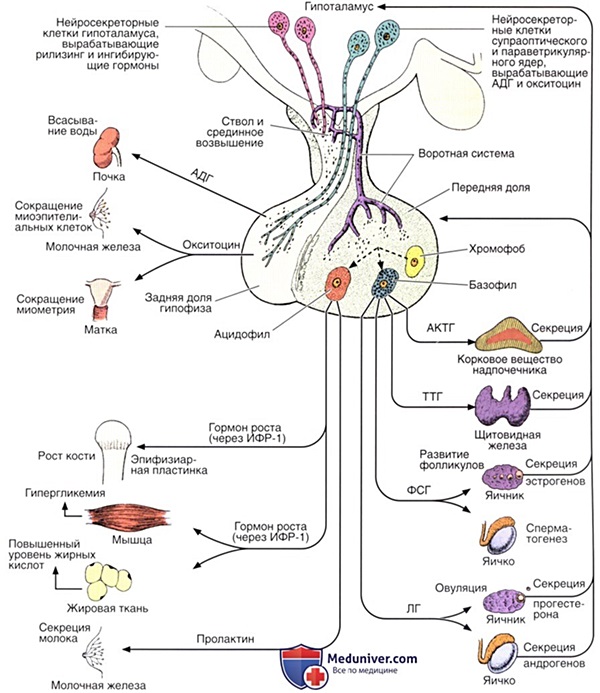 Повышение их концентрации становится причиной гипертиреоза, а снижение, соответственно, гипотиреоза. Заболевания гипоталамуса — регулятора секреции ТТГ гипофизом, также могут стать причиной сбоев в этой системе. Кроме того, заболевания щитовидной железы, сопровождающиеся нарушением выработкии тиреоидных гормонов, могут опосредованно (по механизму обратной связи) влиять на синтез тиреотропного гормона, вызывая понижение или повышение его концентрации.
Повышение их концентрации становится причиной гипертиреоза, а снижение, соответственно, гипотиреоза. Заболевания гипоталамуса — регулятора секреции ТТГ гипофизом, также могут стать причиной сбоев в этой системе. Кроме того, заболевания щитовидной железы, сопровождающиеся нарушением выработкии тиреоидных гормонов, могут опосредованно (по механизму обратной связи) влиять на синтез тиреотропного гормона, вызывая понижение или повышение его концентрации.
Антитела к тиреоглобулину (АТ-ТГ) и к тиреопероксидазе (АТ-ТПО) Вообще, антитела — это белки, синтезируемые клетками иммунной системы. Их основная функция — выявление и уничтожение чужеродных объектов (бактерий, вирусов, и т.п). Однако случается, что в результате сбоя, организм начинает вырабатывать антитела против собственных здоровых тканей. В щитовидной железе, чаще всего, объектами для выработки антител становятся фермент тиреопероксидаза (ТПО) и основа для синтеза гормонов — тиреоглобулин (ТГ).
Тиреоглобулин — это заготовка для гормонов щитовидной железы, из него клетки щитовидной железы «делают» гормоны Т3 и Т4. Вначале клетки вырабатывают тиреоглобулин (создавая т.о. запасы йода), который «складируется на будущее» в специальных емкостях — фолликулах. Потом, по мере необходимости, из тиреоглобулина синтезируются Т3 и Т4.
Тиреоидная пероксидаза – фермент щитовидной железы участвующий в образовании активной формы йода и, таким образом, играющий ключевую роль в выработке гормонов щитовидной железы.
Повреждающее действие антител может приводить к нарушению нормальной продукции гормонов щитовидной железы и негативно влиять на регуляцию её функции, что в итоге вызывает хронические патологии, связанные с гипо- или гипертиреозом. Тем не менее, важно подчеркнуть, что антитела к ТПО и ТГ не являются ключевым звеном в патогенезе аутоиммунных заболеваний щитовидной железы и начинают вырабатываться уже в ответ на её повреждение. Поэтому попытки снижения уровня антител лишены какого-либо практического смысла.
Тесты АТ-ТГ и АТ-ТПО используются для подтверждения или исключения аутоиммунной природы того или иного заболевания щитовидной железы (увеличения щитовидной железы без нарушения её функции, первичного гипо- или гипертиреоза, офтальмопатии и др.), так как это позволяет назначить наиболее эффективную терапию. Тесты также назначаются детям, рождённым от матерей с патологией эндокринных органов, для определения групп риска по развитию заболеваний щитовидной железы. Количественный анализ сыворотки крови на АТ-ТПО – наиболее чувствительный метод диагностики аутоиммунных заболеваний щитовидной железы. Анализ АТ-ТГ ценен при дифференциальной диагностике.
Цены на исследования можно узнать в разделе «Прейскурант» клинической лаборатории. Кровь на исследования принимается ежедневно (кроме воскресенья) с 7 до 11 часов. Строго натощак.
Прочтите так же о Гормонах надпочечников и Половых гормонах
Блог врача
Что содержат противозачаточные таблетки?
Одним из самых распространенных и надёжных способов контрацепции являются противозачаточные таблетки, не представляющие угрозы женскому организму и решающие многие женские проблемы. Вред противозачаточных таблеток не так уж и велик, как думают многие женщины.
Вред противозачаточных таблеток не так уж и велик, как думают многие женщины.
В состав современных противозачаточных таблеток входит маленькое количество гормонов при почти 100 процентной гарантии защиты от беременности. Эстроген и прогестаген – вот два основных компонента противозачаточных таблеток. Их дозировка и комбинации в различных химических контрацептивах разные. Поэтому, необходимо правильно подбирать дозу, а также время и частоту приема, чтобы вред противозачаточных таблеток был минимален.
Как действуют противозачаточные таблетки?
Комбинированные противозачаточные таблетки, во-первых, предотвращают овуляцию, во-вторых, затрудняют попадание сперматозоидов в матку, а также препятствуют оплодотвореннной яйцеклетке прикрепиться к стенкам матки.
Существуют монофазные и трехфазные противозачаточные таблетки. Монофазные препараты имеют одинаковый состав вне зависимости от дня цикла, а трехфазные имеют разное содержание гормонов.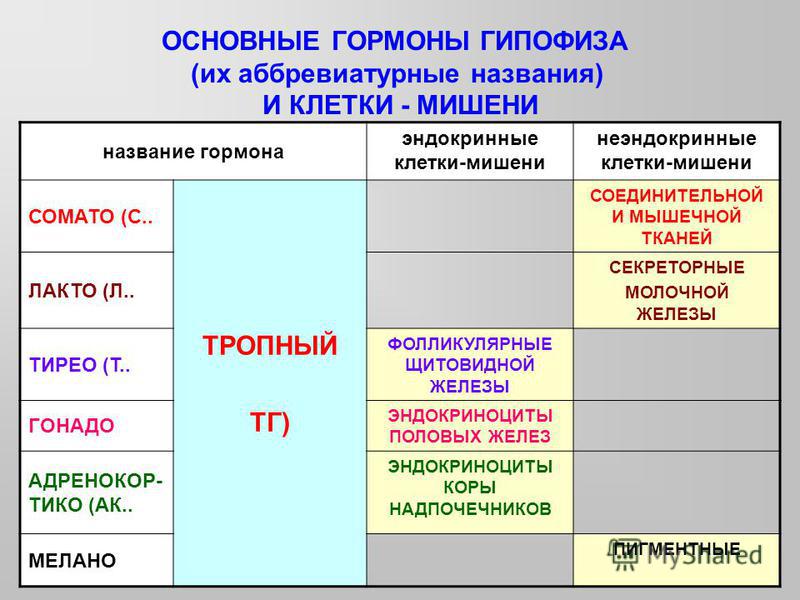 Разумеется, и вред противозачаточных таблеток этих двух классов различен. Особый вид противозачаточных таблеток – мини-пили. Они не содержат эстроген.
Разумеется, и вред противозачаточных таблеток этих двух классов различен. Особый вид противозачаточных таблеток – мини-пили. Они не содержат эстроген.
Какой вред противозачаточных таблеток может быть причинен?
Несмотря на свой положительный эффект, многие женщины опасаются принимать химические контрацептивы вследствие устоявшихся мифов о том, какой вред противозачаточных таблеток может быть причинен.
Существует несколько распространенных мифов о противозачаточных таблетках, которые не имеют под собой четких оснований.
«Противозачаточные таблетки приводят к быстрому увеличению веса»
Этот миф самый популярный. Эстроген, содержащийся в противозачаточных таблетках, приводит к накоплению жидкостей в тканях, что увеличивает вес тела на 1-2 кг. Однако, это не жировые отложения, а просто жидкость в тканях. В результате может появиться целлюлит. Это единственный возможный вред противозачаточных таблеток в этой ситуации.
«Применение противозачаточных таблеток приводит к появлению рака».
На самом деле многие противозачаточные таблетки предотвращают овуляцию, что наоборот уменьшает риск возникновения воспалительных процессов.
«Противозачаточные таблетки приведут к появлению угревой сыпи»
Привыкание к химическим контрацептивам может привести к излишней жирности на лице. Это и есть небольшой вред в данном случае. Если это не проходит, то нужно проконсультироваться со своим врачом и сменить препарат. Кроме того, в состав химических контрацептивов вход дроспиренон, который устраняет проблемы с кожей. Обычно противозачаточные таблетки оказывают положительное воздействие на кожу, прыщи и угревая сыпь проходят.
«Долгое применение противозачаточных таблеток может привести к бесплодию».
Противозачаточные средства не влияют на возможность женщины иметь детей. Просто после окончания приема препарата организм женщины проходит адаптацию в течение нескольких месяцев.
«При постоянном приеме противозачаточных таблеток необходимы паузы».
Паузы делать не нужно. Перерыв, напротив, может привести к нежелательной беременности, при этом устоявшийся цикл собьется. Противозачаточные таблетки можно принимать несколько лет даже десятилетний без всяких перерывов.
-
При приеме химических контрацептивов нужно обязательно обратить внимание на следующее:
-
Первые три месяца приема противозачаточных таблеток возможны выделения между менструациями.
-
Если вдруг забыли принять препарат, то, как только вспомните – принимайте. Пусть даже получится, что вы приняли в день 2 противозачаточные таблетки. Если пропуск составил более одного дня, то есть риск забеременеть. Упаковку нужно допить все равно до конца, пусть даже месячные уже начались.
-
При применении антибиотиков может снизиться эффективность противозачаточных таблеток.

-
Если в течение нескольких часов после принятия препарата началась диарея, то нужно принять еще одну противозачаточную таблетку.
-
Противозачаточные таблетки не влияют на здоровье и развитие ребенка.
Женщинам старше 35 лет, и при этом курящим, не рекомендуется принимать химические контрацептивы. Возникает риск появления тромбов и в этом случае вред противозачаточных средств может проявиться в полной мере.
Препараты половых гормонов (андрогены, эстрогены)
Заказать препараты половых гормонов
Ищете препараты половых гормонов? В каталоге представлены средства из разных стран производителей, которые пользуются доверием и популярностью у потребителей.
При заказе в онлайн режиме заказчик имеет следующие преимущества:
- широкий ассортимент лекарственных средств;
- неограниченное время для изучения свойств, состава, противопоказаний и прочих особенностей препарата;
- обязательно можно подобрать аналоги;
- цена доступная из-за отсутствия посредников и работы напрямую с производителем;
- лицензирование и сертификация всех товаров;
- гибкая система скидок, бонусов и акций;
- доставка в максимально короткий срок.

Заказать препарат означает его быструю доставку в ближайшее отделение аптеки 36,6. Доставка лекарств на дом запрещена действующим законодательством Российской Федерации. Оплата производится по факту получения.
Показания
Половые гормоны в таблетках назначаются мужчинам и женщинам при наличии следующей симптоматики и заболеваний:
- нарушения менструации;
- недостаточность выработки гормонов;
- дисфункции яичников;
- климактерические расстройства;
- остеопороз;
- бесплодие;
- слабая родовая деятельность;
- гипертонические заболевания.
При начале курса лечения обязательно проконсультируйтесь с врачом и только потом начинайте прием женских половых гормонов в таблетках. Самолечение может вызывать ухудшение состояния здоровья и переход заболеваний в хроническую форму [1].
Противопоказания
Большинство препаратов имеют побочные действия и противопоказания, которые зависят от состава средств, производителя и прочих нюансов. Перед началом лечения обязательно изучите инструкцию к применению и следуйте ей строго.
Перед началом лечения обязательно изучите инструкцию к применению и следуйте ей строго.
В предоставленных препаратах отмечены следующие противопоказания:
- возрастные ограничения;
- период беременности и кормления грудью;
- нельзя применять при раковых опухолях;
- тромбоэмболических заболеваниях;
- хронические, тяжелые заболевания печени и почек;
- индивидуальная непереносимость составляющих препарата;
- болезни дыхательной системы (астма и прочее).
Формы выпуска
Чаще всего половые гормоны производятся в таблетках, но встречаются и иные формы производства, например, порошок, свечи, концентраты и прочее. Средства, представленные у нас изготовлены в виде:
- таблеток;
- геля, который наносится на чистый, сухой участок кожи в нижней части живота, на пояснице, плечах, предплечьях и ягодицах. Каждый раз область нанесения меняется.
Страны изготовители
На страницах нашего сайта представлены препараты не только российского производства. Мы подобрали препараты лучших мировых брендов производства
Финляндии, России, Венгрии, Германии, Нидерландов и Франции.
Мы подобрали препараты лучших мировых брендов производства
Финляндии, России, Венгрии, Германии, Нидерландов и Франции.
ПЕРЕД ПРИМЕНЕНИЕМ ПРЕПАРАТОВ НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО ПРИМЕНЕНИЮ ИЛИ ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ.
Список литературы:
- [i] Половые гормоны — Краткая медицинская энциклопедия — Библиотека Природы
Гормон мужественности: что такое тестостерон и как его повысить
https://rsport.ria.ru/20191107/1560649434.html
Гормон мужественности: что такое тестостерон и как его повысить
Гормон мужественности: что такое тестостерон и как его повысить — РИА Новости Спорт, 17.12.2019
Гормон мужественности: что такое тестостерон и как его повысить
Тестостерон — основной половой гормон у мужчин, который отвечает за мужественность и сильно влияет на сексуальную жизнь. Снижение его уровня в организме может… РИА Новости Спорт, 17.12.2019
2019-11-07T08:00
2019-11-07T08:00
2019-12-17T12:41
зож
спорт
гормоны
вокруг спорта
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21. img.ria.ru/images/19389/57/193895757_0:194:3005:1884_1920x0_80_0_0_777e1e7405adb944545a2cd2794b6c48.jpg
img.ria.ru/images/19389/57/193895757_0:194:3005:1884_1920x0_80_0_0_777e1e7405adb944545a2cd2794b6c48.jpg
Тестостерон — основной половой гормон у мужчин, который отвечает за мужественность и сильно влияет на сексуальную жизнь. Снижение его уровня в организме может привести к ослаблению мышечного тонуса, повышенной утомляемости, облысению и депрессии. О главном гормоне мужественности — в нашем обзоре.Тестостерон: мифы и реальностьМужской организм вырабатывает порядка семи миллиграммов тестостерона в сутки. Этот гормон нужен для развития первичных и вторичных половых признаков, стимулирует наращивание мышечной массы и отвечает за метаболизм жиров и половое влечение. Тестостерон также вырабатывается и женским организмом (особенно у спортсменок), но в меньших количествах.У здорового мужчины концентрация тестостерона в организме равняется 280-1100 нг/дл, у женщины — 15-70 нг/дл. В женском организме тестостерон отвечает за укрепление и рост костей, формирование мышц, развитие нервной системы и мозга. И самое важное: благодаря тестостерону в женском организме вырабатывается эстроген — главный женский гормон. Спортивным федерациям даже приходится разрабатывать специальные нормативы по уровню содержания тестостерона в крови для спортсменок с повышенным уровнем мужского гормона и спортсменок-трансгендеров.Долгое время было принято считать, что именно с высоким уровнем тестостерона связана агрессивность мужчин, их успешность в сравнении с женщинами и вечное желание заниматься сексом. На самом деле большинство этих тезисов уже было опровергнуто.Если о связи тестостерона с агрессивностью ученые до сих пор спорят, то теория превосходства мужчин над прекрасным полом во многих сферах благодаря этому гормону была опровергнута: женщины могут действовать решительно, быстро усваивать информацию, умеют рисковать не хуже мужчин.Тестостерон отвечает за либидо, но даже высокий уровень гормона в крови не означает, что мужчина круглосуточно хочет и готов заниматься сексом. У него могут быть другие сильные раздражители (работа, спорт, одержимость идеей), которые будут отвлекать от сексуального влечения.Также было опровергнуто утверждение о том, что чем больше тестостерона в организме, тем лучше для него и тем мужественнее мужчина. Уровень гормона сильно выше нормы может вызвать раздражительность, сильные перепады настроения, нарушения сна.Избыток гормона влияет на выпадение волос, появление прыщей на коже, а также может спровоцировать различные заболевания, в том числе инфаркт и инсульт.Что приводит к падению тестостеронаК снижению уровня тестостерона в крови приводит ряд факторов: стресс, употребление алкоголя и плохой сон. И если не восстановить норму гормона в организме, можно попасть в замкнутый круг: из-за стресса и недосыпа падает тестостерон, что приводит к повышению утомляемости и депрессии, которые не позволяют бороться со стрессом.Тревожным звонком снижения уровня тестостерона в организме может стать нежелание что-то делать и постоянная утомленность. Тестостерон всегда связан с активностью: физической и умственной. Еще один признак — набор веса. Но если исключить негативные факторы, уровень тестостерона может восстановиться достаточно быстро: понадобится от двух недель до пары месяцев.Как повысить уровень тестостеронаУровень тестостерона может повыситься за счет эмоционального всплеска: радостное событие, победа команды, за которую ты болеешь, успех на работе. Но для того чтобы действительно восстановить уровень тестостерона или повысить его, придется потрудиться.Повысить уровень тестостерона помогут правильное питание, сон, отдых и физические нагрузки.ПитаниеПитание играет ключевую роль в жизни и здоровье человека вне зависимости от уровня тестостерона. Но для выработки гормона организму необходимы определенные элементы. В рацион необходимо включить продукты богатые цинком и магнием (шпинат и зеленые салаты), а также белком и холестерином (мясо, яйца, авокадо, орехи).Не стоит бояться продуктов, которые содержат жиры и холестерин. Согласно исследованиям, именно они помогают увеличивать уровень тестостерона, а вот диеты с низким содержанием жиров, напротив, могут привести к снижению уровня мужского гормона в крови.Хорошим подспорьем может стать добавление к питанию витамина D. А вот алкоголь и особенно пиво не рекомендуются — они приводят к снижению тестостерона.ТренировкиФизическая нагрузка даже сама по себе может привести к повышению уровня тестостерона. Но чтобы действительно помочь организму вырабатывать этот гормон, нужны планомерные тренировки. Самыми полезными считаются базовые упражнения: жим лежа, приседания, становая тяга, так как они работают на крупные мышцы. Кардиотренировки могут быть эффективны для сжигания жира, но не для роста уровня тестостерона. Перебарщивать с тренировками тоже не стоит: это вызовет усталость и переутомление, а следовательно, и стресс, что приведет к снижению уровня мужского гормона в организме.Отдых и сонСамая высокая концентрация тестостерона у мужчин — сразу после пробуждения, так как выработка гормона происходит во сне. Если же начать пренебрегать сном, то у организма просто не будет времени на выработку тестостерона. Также во сне снижается уровень кортизола — гормона, блокирующего тестостерон. В малых дозах кортизол, который также вырабатывается во время стресса, не опасен. Но если вы находитесь в состоянии постоянного дискомфорта и депрессии, то кортизола вырабатывается больше и он блокирует тестостерон.
И самое важное: благодаря тестостерону в женском организме вырабатывается эстроген — главный женский гормон. Спортивным федерациям даже приходится разрабатывать специальные нормативы по уровню содержания тестостерона в крови для спортсменок с повышенным уровнем мужского гормона и спортсменок-трансгендеров.Долгое время было принято считать, что именно с высоким уровнем тестостерона связана агрессивность мужчин, их успешность в сравнении с женщинами и вечное желание заниматься сексом. На самом деле большинство этих тезисов уже было опровергнуто.Если о связи тестостерона с агрессивностью ученые до сих пор спорят, то теория превосходства мужчин над прекрасным полом во многих сферах благодаря этому гормону была опровергнута: женщины могут действовать решительно, быстро усваивать информацию, умеют рисковать не хуже мужчин.Тестостерон отвечает за либидо, но даже высокий уровень гормона в крови не означает, что мужчина круглосуточно хочет и готов заниматься сексом. У него могут быть другие сильные раздражители (работа, спорт, одержимость идеей), которые будут отвлекать от сексуального влечения.Также было опровергнуто утверждение о том, что чем больше тестостерона в организме, тем лучше для него и тем мужественнее мужчина. Уровень гормона сильно выше нормы может вызвать раздражительность, сильные перепады настроения, нарушения сна.Избыток гормона влияет на выпадение волос, появление прыщей на коже, а также может спровоцировать различные заболевания, в том числе инфаркт и инсульт.Что приводит к падению тестостеронаК снижению уровня тестостерона в крови приводит ряд факторов: стресс, употребление алкоголя и плохой сон. И если не восстановить норму гормона в организме, можно попасть в замкнутый круг: из-за стресса и недосыпа падает тестостерон, что приводит к повышению утомляемости и депрессии, которые не позволяют бороться со стрессом.Тревожным звонком снижения уровня тестостерона в организме может стать нежелание что-то делать и постоянная утомленность. Тестостерон всегда связан с активностью: физической и умственной. Еще один признак — набор веса. Но если исключить негативные факторы, уровень тестостерона может восстановиться достаточно быстро: понадобится от двух недель до пары месяцев.Как повысить уровень тестостеронаУровень тестостерона может повыситься за счет эмоционального всплеска: радостное событие, победа команды, за которую ты болеешь, успех на работе. Но для того чтобы действительно восстановить уровень тестостерона или повысить его, придется потрудиться.Повысить уровень тестостерона помогут правильное питание, сон, отдых и физические нагрузки.ПитаниеПитание играет ключевую роль в жизни и здоровье человека вне зависимости от уровня тестостерона. Но для выработки гормона организму необходимы определенные элементы. В рацион необходимо включить продукты богатые цинком и магнием (шпинат и зеленые салаты), а также белком и холестерином (мясо, яйца, авокадо, орехи).Не стоит бояться продуктов, которые содержат жиры и холестерин. Согласно исследованиям, именно они помогают увеличивать уровень тестостерона, а вот диеты с низким содержанием жиров, напротив, могут привести к снижению уровня мужского гормона в крови.Хорошим подспорьем может стать добавление к питанию витамина D. А вот алкоголь и особенно пиво не рекомендуются — они приводят к снижению тестостерона.ТренировкиФизическая нагрузка даже сама по себе может привести к повышению уровня тестостерона. Но чтобы действительно помочь организму вырабатывать этот гормон, нужны планомерные тренировки. Самыми полезными считаются базовые упражнения: жим лежа, приседания, становая тяга, так как они работают на крупные мышцы. Кардиотренировки могут быть эффективны для сжигания жира, но не для роста уровня тестостерона. Перебарщивать с тренировками тоже не стоит: это вызовет усталость и переутомление, а следовательно, и стресс, что приведет к снижению уровня мужского гормона в организме.Отдых и сонСамая высокая концентрация тестостерона у мужчин — сразу после пробуждения, так как выработка гормона происходит во сне. Если же начать пренебрегать сном, то у организма просто не будет времени на выработку тестостерона. Также во сне снижается уровень кортизола — гормона, блокирующего тестостерон. В малых дозах кортизол, который также вырабатывается во время стресса, не опасен. Но если вы находитесь в состоянии постоянного дискомфорта и депрессии, то кортизола вырабатывается больше и он блокирует тестостерон.
https://ria.ru/20191105/1560507188.html
https://rsport.ria.ru/20191102/1560496973.html
РИА Новости Спорт
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости Спорт
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://rsport.ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости Спорт
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/19389/57/193895757_338:0:3005:2000_1920x0_80_0_0_851e60ff4e681c22bec284ecfbc92cd4.jpgРИА Новости Спорт
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости Спорт
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
спорт, гормоны, вокруг спорта
Тестостерон — основной половой гормон у мужчин, который отвечает за мужественность и сильно влияет на сексуальную жизнь. Снижение его уровня в организме может привести к ослаблению мышечного тонуса, повышенной утомляемости, облысению и депрессии. О главном гормоне мужественности — в нашем обзоре.
Тестостерон: мифы и реальность
Мужской организм вырабатывает порядка семи миллиграммов тестостерона в сутки. Этот гормон нужен для развития первичных и вторичных половых признаков, стимулирует наращивание мышечной массы и отвечает за метаболизм жиров и половое влечение. Тестостерон также вырабатывается и женским организмом (особенно у спортсменок), но в меньших количествах.У здорового мужчины концентрация тестостерона в организме равняется 280-1100 нг/дл, у женщины — 15-70 нг/дл. В женском организме тестостерон отвечает за укрепление и рост костей, формирование мышц, развитие нервной системы и мозга. И самое важное: благодаря тестостерону в женском организме вырабатывается эстроген — главный женский гормон. Спортивным федерациям даже приходится разрабатывать специальные нормативы по уровню содержания тестостерона в крови для спортсменок с повышенным уровнем мужского гормона и спортсменок-трансгендеров.Долгое время было принято считать, что именно с высоким уровнем тестостерона связана агрессивность мужчин, их успешность в сравнении с женщинами и вечное желание заниматься сексом. На самом деле большинство этих тезисов уже было опровергнуто.
Если о связи тестостерона с агрессивностью ученые до сих пор спорят, то теория превосходства мужчин над прекрасным полом во многих сферах благодаря этому гормону была опровергнута: женщины могут действовать решительно, быстро усваивать информацию, умеют рисковать не хуже мужчин.Тестостерон отвечает за либидо, но даже высокий уровень гормона в крови не означает, что мужчина круглосуточно хочет и готов заниматься сексом. У него могут быть другие сильные раздражители (работа, спорт, одержимость идеей), которые будут отвлекать от сексуального влечения.
Также было опровергнуто утверждение о том, что чем больше тестостерона в организме, тем лучше для него и тем мужественнее мужчина. Уровень гормона сильно выше нормы может вызвать раздражительность, сильные перепады настроения, нарушения сна.
Избыток гормона влияет на выпадение волос, появление прыщей на коже, а также может спровоцировать различные заболевания, в том числе инфаркт и инсульт.
5 ноября 2019, 08:00НаукаТестостероновая бомба. Почему мужчины умирают чаще женщинЧто приводит к падению тестостерона
К снижению уровня тестостерона в крови приводит ряд факторов: стресс, употребление алкоголя и плохой сон. И если не восстановить норму гормона в организме, можно попасть в замкнутый круг: из-за стресса и недосыпа падает тестостерон, что приводит к повышению утомляемости и депрессии, которые не позволяют бороться со стрессом.
Тревожным звонком снижения уровня тестостерона в организме может стать нежелание что-то делать и постоянная утомленность. Тестостерон всегда связан с активностью: физической и умственной. Еще один признак — набор веса. Но если исключить негативные факторы, уровень тестостерона может восстановиться достаточно быстро: понадобится от двух недель до пары месяцев.
Как повысить уровень тестостерона
Уровень тестостерона может повыситься за счет эмоционального всплеска: радостное событие, победа команды, за которую ты болеешь, успех на работе. Но для того чтобы действительно восстановить уровень тестостерона или повысить его, придется потрудиться.
Повысить уровень тестостерона помогут правильное питание, сон, отдых и физические нагрузки.
Питание
Питание играет ключевую роль в жизни и здоровье человека вне зависимости от уровня тестостерона. Но для выработки гормона организму необходимы определенные элементы. В рацион необходимо включить продукты богатые цинком и магнием (шпинат и зеленые салаты), а также белком и холестерином (мясо, яйца, авокадо, орехи).
Не стоит бояться продуктов, которые содержат жиры и холестерин. Согласно исследованиям, именно они помогают увеличивать уровень тестостерона, а вот диеты с низким содержанием жиров, напротив, могут привести к снижению уровня мужского гормона в крови.Хорошим подспорьем может стать добавление к питанию витамина D. А вот алкоголь и особенно пиво не рекомендуются — они приводят к снижению тестостерона.2 ноября 2019, 08:00ЗОЖКрепкий орешек: как тренируется и питается Джейсон СтэтхэмТренировки
Физическая нагрузка даже сама по себе может привести к повышению уровня тестостерона. Но чтобы действительно помочь организму вырабатывать этот гормон, нужны планомерные тренировки. Самыми полезными считаются базовые упражнения: жим лежа, приседания, становая тяга, так как они работают на крупные мышцы. Кардиотренировки могут быть эффективны для сжигания жира, но не для роста уровня тестостерона.
Перебарщивать с тренировками тоже не стоит: это вызовет усталость и переутомление, а следовательно, и стресс, что приведет к снижению уровня мужского гормона в организме.
Отдых и сон
Самая высокая концентрация тестостерона у мужчин — сразу после пробуждения, так как выработка гормона происходит во сне. Если же начать пренебрегать сном, то у организма просто не будет времени на выработку тестостерона. Также во сне снижается уровень кортизола — гормона, блокирующего тестостерон. В малых дозах кортизол, который также вырабатывается во время стресса, не опасен. Но если вы находитесь в состоянии постоянного дискомфорта и депрессии, то кортизола вырабатывается больше и он блокирует тестостерон.
Состав грудного молока | Из чего состоит грудное молоко?
1 Ballard O, Morrow AL. Human milk composition: nutrients and bioactive factors. Pediatr Clin North Am. 2013;60(1):49-74. Баллард О., Морроу А.Л., «Состав грудного молока: нутриенты и биологически активные факторы». Педиатр Клин Норт Ам. 2013;60(1):49-74.
2 Hassiotou F et al. Cells in human milk: state of the science. J Human Lact. 2013;29(2):171-182. — Хассиоту Ф. и соавторы, «Клетки грудного молока: что знает наука». Ж Хьюман Лакт (Журнал Международной ассоциации консультантов по лактации). 2013;29(2):171-182.
3 Beck KL, et al. Comparative proteomics of human and macaque milk reveals species-specific nutrition during postnatal development. J Proteome Res. 2015;14(5):2143-2157. — Бек К.Л. и соавторы, «Сравнительная протеомика человеческого молока и молока макаки демонстрирует видоспецифичность питания в период постнатального развития». Ж Протеом Рес. 2015;14(5):2143-2157.
4 Zhang Z et al. Amino acid profiles in term and preterm human milk through lactation: a systematic review. Nutrients. 2013;5(12):4800-4821. — Аминокислотный профиль молока после своевременных и преждевременных родов: систематический обзор. Нутриентс. 2013;5(12):4800-4821.
5 Sánchez CL et al. The possible role of human milk nucleotides as sleep inducers. Nutr Neurosci. 2009;12(1):2-8. — Санчес С.Л. и соавторы, «Нуклеотиды в грудном молоке могут способствовать засыпанию ребенка». Нутр Нейросай. 2009;12(1):2-8.
6 Moukarzel S, Bode L. Human milk oligosaccharides and the preterm infant: a journey in sickness and in health. Clin perinatol. 2017;44(1):193-207. — Мукарцел С., Боуд Л., «Олигосахариды грудного молока и доношенный ребенок: путь к болезни и здравию». Клин Перинатол (Клиническая перинатология). 2017;44(1):193-207.
7 Hamosh M. Bioactive factors in human milk. Pediatric Clinics. 2001;48(1):69-86. — Хэмош М., «Биологические активные факторы грудного молока. Педиатрик Клиникс. 2001;48(1):69-86.
8 Brandtzaeg P. The mucosal immune system and its integration with the mammary glands. The J Pediatr. 2010;156(2):S8-15. — Брандтцег П., «Мукозная иммунная система и ее интеграция с молочными железами». Ж Педиатр (Журнал Педиатрии). 2010;156(2):S8-15.
9 Uauy R et al. Essential fatty acids in early life: structural and functional role. Proc Nutr Soc. 2000;59(1):3-15. — Уай Р. и соавторы, «Важнейшие жирные кислоты первых дней жизни: структурная и функциональная роль». Нутр Соц. 2000;59(1):3-15.
10 Alsaweed M et al. Human milk cells and lipids conserve numerous known and novel miRNAs, some of which are differentially expressed during lactation. PLoS One. 2016;11(4):e0152610. — Алсавид М. и соавторы, «Клетки грудного молока и липиды сохраняют множество известных и неизвестных видов микроРНК, многие из которых демонстрируют дифференцированную экспрессию в период лактации». ПЛоС Уан. 2016;11(4):e0152610.
11 Neville MC et al. Studies in human lactation: milk volumes in lactating women during the onset of lactation and full lactation. Am J Clin Nutr. 1988;48(6):1375-1386. — Невилл М.С. и соавторы, «Исследование женской лактации: количество молока у лактирующих женщин в начале и на пике периода лактации». Ам Ж Клин Нутр. 1988;48(6):1375-1386.
12 Marchbank T et al. Pancreatic secretory trypsin inhibitor is a major motogenic and protective factor in human breast milk. Am J Physiol Gastrointest Liver Physiol. 2009;296(4):G697-703. Марчбэнк Т. и соавторы, «Ингибитор трипсина в секрете поджелудочной железы как важнейший мотогенный и защитный фактор грудного молока». Ам Ж Физиол Гастроинтест Лайвер Физиол. 2009;296(4):G697-703.
13 Herrmann K, Carroll K. An exclusively human milk diet reduces necrotizing enterocolitis. Breast Med. 2014;9(4):184-190. — Херрманн К., Кэрролл К., «Питание исключительно грудным молоком снижает риск развития некротизирующего энтероколита». Брест Мед (Медицина грудного вскармливания). 2014;9(4):184-190.
14 Lawrence RA, Lawrence RM. Breastfeeding: A guide for the medical profession. 7th ed. Maryland Heights MO, USA: Elsevier Mosby; 2010. 1128 p — Лоуренс Р.А., Лоуренс Р.М., «Грудное вскармливание: руководство для медиков». Седьмое издание. Издательство Maryland Heights, Миссури, США: Элсевьер Мосби; 2010. Стр. 1128.
15 Martin CR et al. Review of infant feeding: key features of breast milk and infant formula. Nutrients. 2016;8(5):279. — Мартин С.Р. и соавторы, «Обзор проблем младенческого вскармливания: основные особенности грудного молока и детских смесей». Нутриентс. 2016;8(5):279.
16 Montagne P et al. Changes in lactoferrin and lysozyme levels in human milk during the first twelve weeks of lactation. InBioactive components of human milk 2001 (pp. 241-247). Springer, Boston, MA.- Монтань П. и соавторы. «Изменение уровня лактоферрина и лизоцима в грудном молоке в первые двенадцать недель лактации». В сборнике «Биологически активные компоненты грудного молока» 2001 г. (стр. 241-247). Спрингер, Бостон, Массачусетс.
17 Kent JC, et al. Volume and frequency of breastfeedings and fat content of breast milk throughout the day. Pediatrics. 2006;117(3):e387-395. — Кент Дж.С. и соавторы, «Объем и частота кормлений и содержание жира в молоке в течение дня». Педиатрикс (Педиатрия). 2006;117(3):e387-395.
18 Kuo AA et al. Introduction of solid food to young infants. Matern child health J. 2011;15(8):1185-1194.- Куо А.А. и соавторы. «Введение прикорма». Матерн чайлд хелс(Здоровье матери и ребенка). 2011;15(8):1185-1194.
19 Dewey KG et al. Breast milk volume and composition during late lactation (7-20 months). J Pediatr Gastroenterol Nutr. 1984;3(5):713-720. — Дьюи К.Г. и соавторы, «Количество и состав грудного молока в поздний период лактации (7-20 месяцев)». Ж Педиатр Гастроэнтерол Нутр. 1984;3(5):713-720.
видов гормонов | Безграничная биология
Гормональные функции
Эндокринная система играет роль в росте, метаболизме и других процессах, высвобождая гормоны в кровь.
Цели обучения
Оценить гормоны и их назначение в организме
Основные выводы
Ключевые моменты
- Гормоны служат в организме как химические посредники и помогают поддерживать гомеостаз.
- Гормоны попадают в жидкости организма, например кровь, и переносят их к клеткам-мишеням.
- Клетки-мишени реагируют на гормон, когда они экспрессируют специфический рецептор этого гормона.
- Гормоны также играют роль в регуляции гибели клеток, иммунной системы, репродуктивного развития, перепадов настроения и тяги к голоду.
- В надпочечниках адреналин и норадреналин регулируют реакцию на стресс; в щитовидной железе гормоны щитовидной железы регулируют скорость метаболизма.
Ключевые термины
- клетка-мишень : любая клетка, имеющая специфический рецептор гормона
- гормон : любое вещество, вырабатываемое одной тканью и переносимое кровотоком в другую для воздействия на физиологическую активность
- эндокринная система : система управления железами без протоков, которые выделяют гормоны, которые циркулируют через кровоток для воздействия на клетки в определенных органах
Эндокринная система: гормоны
Эндокринная система животного контролирует процессы в организме посредством выработки, секреции и регулирования гормонов.Гормоны служат химическими «посланниками», которые участвуют в деятельности клеток и органов, поддерживая гомеостаз тела. Поддержание гомеостаза в организме требует координации множества различных систем и органов. Связь между соседними клетками, а также между клетками и тканями в отдаленных частях тела происходит посредством высвобождения гормонов в жидкости организма (обычно в кровь), которые переносят их к своим клеткам-мишеням. Клетки-мишени, имеющие рецептор сигнала, реагируют на гормон, когда они экспрессируют специфический рецептор этого гормона.Клеточные реципиенты определенного гормонального сигнала могут быть одним из нескольких типов клеток, которые находятся в разных тканях, как в случае с инсулином, который вызывает широкий спектр системных физиологических эффектов. Различные типы тканей также могут по-разному реагировать на один и тот же гормональный сигнал.
Высвобождая гормоны, эндокринная система играет роль в росте, метаболизме и половом развитии. Гормоны также играют роль в индукции или подавлении гибели клеток, активации или подавлении иммунной системы, перепадах настроения и жажде голода.У людей общие заболевания эндокринной системы включают заболевание щитовидной железы и сахарный диабет.
Примеры эндокринных желез: надпочечники, вырабатывающие гормоны, такие как адреналин и норадреналин, регулирующие реакцию на стресс, и щитовидную железу, вырабатывающую гормоны щитовидной железы, регулирующие скорость метаболизма. У организмов, претерпевающих метаморфоз, процесс контролируется эндокринной системой. Например, превращение головастика в лягушку является сложным и тонким, чтобы адаптироваться к конкретным условиям окружающей среды и экологическим обстоятельствам.
Гормоны в метаморфозе : Процесс метаморфоза земноводных, как видно на показанных здесь стадиях превращения головастика в лягушку, осуществляется гормонами.
Липидные, аминокислотные и пептидные гормоны
Все гормоны в организме человека можно разделить на гормоны липидного, аминокислотного и пептидного происхождения.
Цели обучения
Распознавать характеристики, связанные с липидными, аминокислотными и пептидными гормонами
Основные выводы
Ключевые моменты
- Большинство липидных гормонов представляют собой стероидные гормоны, которые обычно представляют собой кетоны или спирты и нерастворимы в воде.
- Стероидные гормоны (оканчивающиеся на «-ол» или «-он») включают эстрадиол, тестостерон, альдостерон и кортизол.
- Гормоны, производные от аминокислот (оканчивающиеся на «-ine»), являются производными тирозина и триптофана и включают адреналин и норадреналин (продуцируемые мозговым веществом надпочечников).
- Гормоны, производные от аминокислот, также включают тироксин (вырабатываемый щитовидной железой) и мелатонин (вырабатываемый шишковидной железой).
- Пептидные гормоны состоят из полипептидной цепи; они включают такие молекулы, как окситоцин (короткая полипептидная цепь) или гормоны роста (белки).
- Гормоны, производные от аминокислот, и белковые гормоны растворимы в воде и не растворяются в липидах.
Ключевые термины
- окситоцин : гормон, стимулирующий схватки во время родов, а затем выработку молока
- адреналин : (адреналин) гормон аминокислотного происхождения, секретируемый надпочечниками в ответ на стресс
- эстроген : любой из группы стероидов (липидных гормонов), которые секретируются яичниками и действуют как женские половые гормоны
Типы гормонов
Хотя в организме человека существует множество различных гормонов, их можно разделить на три класса в зависимости от их химической структуры: гормоны липидного происхождения, производные аминокислот и пептидные гормоны (включая пептиды и белки).Одной из ключевых отличительных особенностей гормонов липидного происхождения является то, что они могут диффундировать через плазматические мембраны, тогда как гормоны, производные от аминокислот и пептиды, не могут.
Гормоны липидного происхождения (или липидорастворимые гормоны)
Большинство липидных гормонов получают из холестерина, поэтому структурно схожи с ним. Основным классом липидных гормонов человека являются стероидные гормоны. Химически эти гормоны обычно представляют собой кетоны или спирты; их химические названия заканчиваются на «-ол» для спиртов или на «-он» для кетонов.Примеры стероидных гормонов включают эстрадиол, который представляет собой эстроген, или женский половой гормон, и тестостерон, который представляет собой андроген, или мужской половой гормон. Эти два гормона выделяются женскими и мужскими репродуктивными органами соответственно. Другие стероидные гормоны включают альдостерон и кортизол, которые выделяются надпочечниками вместе с некоторыми другими типами андрогенов. Стероидные гормоны не растворяются в воде; они переносятся транспортными белками крови. В результате они остаются в кровотоке дольше, чем пептидные гормоны.Например, кортизол имеет период полураспада от 60 до 90 минут, тогда как адреналин, гормон, производный от аминокислоты, имеет период полураспада примерно в одну минуту.
Липидные гормоны : Показанные здесь структуры представляют (а) холестерин плюс стероидные гормоны (б) тестостерон и (в) эстрадиол.
Гормоны, производные аминокислот
Гормоны, производные от аминокислот, представляют собой относительно небольшие молекулы, производные от аминокислот тирозина и триптофана. Если гормон является производным от аминокислоты, его химическое название заканчивается на «-ine».Примеры гормонов, производных от аминокислот, включают адреналин и норэпинефрин, которые синтезируются в мозговом веществе надпочечников, и тироксин, который вырабатывается щитовидной железой. Шишковидная железа в головном мозге вырабатывает и секретирует мелатонин, который регулирует циклы сна.
Гормоны, производные от аминокислот : (a) Гормон адреналин, который вызывает реакцию «бей или беги», происходит из аминокислоты тирозина. (б) Гормон мелатонин, регулирующий циркадные ритмы, происходит из аминокислоты триптофана.
Пептидные гормоны
Структура пептидных гормонов представляет собой структуру полипептидной цепи (цепи аминокислот). Пептидные гормоны включают молекулы, которые представляют собой короткие полипептидные цепи, такие как антидиуретический гормон и окситоцин, вырабатываемые в головном мозге и высвобождаемые в кровь в задней доле гипофиза. Этот класс также включает небольшие белки, такие как гормоны роста, вырабатываемые гипофизом, и большие гликопротеины, такие как фолликулостимулирующий гормон, вырабатываемый гипофизом.
Пептидные гормоны : Показаны структуры пептидных гормонов (а) окситоцина, (б) гормона роста и (в) фолликулостимулирующего гормона. Эти пептидные гормоны намного больше, чем те, которые получены из холестерина или аминокислот.
Секретируемые пептиды, такие как инсулин, хранятся в пузырьках в клетках, которые их синтезируют. Затем они высвобождаются в ответ на раздражители (например, в виде высокого уровня глюкозы в крови в случае инсулина). Аминокислотные и полипептидные гормоны растворимы в воде и не растворяются в липидах.Эти гормоны не могут проходить через плазматические мембраны клеток; следовательно, их рецепторы находятся на поверхности клеток-мишеней.
гормонов — обзор | Темы ScienceDirect
Гормоны и иммунный ответ
Хотя гормоны, особенно эстрогены, считаются важными участниками аберраций иммунного ответа и проявления болезни, их точная молекулярная роль и механизмы действия все еще плохо изучены. Исследования показали влияние гормонов на выработку цитокинов различными иммунными клетками, регуляцию генов в Т-клетках, выработку иммуноглобулина В-лимфоцитами и функцию гранулоцитов и NK-клеток. 5,6 Некоторые из первых прямых молекулярных доказательств роли эстрогена в аутоиммунности были получены в исследованиях, проведенных на неаутоиммунных мышах, трансгенных по тяжелой цепи патогенного антитела против дцДНК. Эстроген усиливает экспрессию антиапоптотической молекулы Bcl-2 и способствует выживанию аутореактивных В-клеток, позволяя им избежать индукции толерантности. 7 Важным аспектом активации B-клеток является созревание аффинности антитела, которое включает соматическую гипермутацию и рекомбинацию с переключением классов, оба из которых требуют индуцированного активацией фермента дезаминазы (AID). 8 Было показано, что эстроген напрямую активирует транскрипцию AID через связывающие элементы в промоторе AID. 9 Кроме того, эстроген обеспечивает выживание и сохранение аутореактивных Т-клеток за счет подавления FasL и подавления вызванной активацией гибели Т-клеток СКВ человека. 10
Исследования, проведенные на Т-клетках периферической крови человека, показали, что эстроген увеличивает экспрессию мРНК кальциневрина и активность кодируемой протеинфосфатазы (PP) 2B ER-зависимым образом.PP2B вызывает дефосфорилирование ядерного фактора активированного фактора транскрипции Т-клеток и последующую ядерную транслокацию и связывание с генами-мишенями, такими как CD40L. Эстроген может способствовать усилению родственной помощи Т-клеткам аутореактивным В-клеткам, поскольку было показано, что введение эстрадиола усиливает экспрессию CD40L в Т-клетках пациентов с волчанкой, но не здоровых людей. 11 Воздействие эстрадиола на нормальные Т-клетки периферической крови человека привело к повышенной экспрессии репрессора транскрипции, модулятора элемента ответа циклического АМФ (CREM) альфа и подавлению продукции цитокинов интерлейкина (ИЛ-2). 12,13
Нарушения цитокинов являются важным компонентом аберрантного иммунного ответа у пациентов с СКВ. Иммунный ответ при СКВ характеризуется Th3-типом цитокинового окружения, так что цитокины IL-4, IL-6 и IL-10 повышаются в сыворотке крови пациентов. Кроме того, у пациентов с СКВ наблюдаются повышенные сывороточные уровни провоспалительного цитокина IL-17 и увеличенная доля дифференцированных клеток Th27, которые, как считается, вносят вклад в патогенез аутоиммунных заболеваний. 14 Известно, что эстроген регулирует иммунную систему, регулируя выработку цитокинов. Известно, что высокие дозы эстрогена способствуют выработке цитокинов Th3 (IL-4, IL-10, TGFβ). Высокие уровни эстрогена в сыворотке коррелировали с низкими уровнями IL-2 у склонных к волчанке мышей NZB / NZW. Кроме того, лечение эстрогеном увеличивало уровни фактора некроза опухоли (TNF) и IL-6 после заражения липополисахаридом (LPS) как у нормальных, так и у склонных к волчанке мышей MRL / lpr; эти эффекты были обращены селективным модулятором ER тамоксифеном.Исследования на животных показали, что мыши, получавшие синтетический эстроген, были восприимчивы к бактериальной инфекции Listeria monocytogenes и их спленоциты вырабатывали меньше IL-2, в то время как повышенная продукция IL-17 наблюдалась в спленоцитах мышей, получавших эстроген. 15,16 Известно также, что эстроген регулирует провоспалительный цитокин IFNγ и, как было показано, усиливает ответы CD4 и клетки, продуцирующие IFNγ из лимфатических узлов, 17 и фактор транскрипции дифференцировки Th2 T-bet был повышен эстрогеном в мышиных спленоцитах. 18
Дендритные клетки (ДК) являются инициаторами врожденных, а также адаптивных иммунных ответов и обильно экспрессируют Toll-подобные рецепторы (TLR) распознавания образов. TLR7- и TLR9-дефицитные мыши, склонные к волчанке, демонстрируют снижение заболеваемости, что указывает на важность TLR в патогенезе волчанки. DC дефектны при СКВ как у людей, так и у мышей, проявляющих чрезмерно стимулированный фенотип и функцию с повышенной экспрессией основных комплексов гистосовместимости (MHCs), а также костимулирующих молекул CD80 / 86. 19 Эстроген может модулировать дифференцировку и функцию DC несколькими способами: изменять экспрессию белков MHC, костимулирующих молекул или TLR; регулируют продукцию цитокинов DC прямо или косвенно через другие типы клеток; и модулировать миграционную функцию посредством изменения продукции цитокинов или хемокинов. Кроме того, эстроген необходим для активации и дифференцировки DC, особенно тех, которые обладают свойствами клеток Лангергана, таких как DC. 20
Помимо прямой роли эстрогена в иммунной системе, существует еще одно представление о том, что регуляторные механизмы, которые обычно контролируют вызванное эстрогеном возбуждение иммунного ответа, могут быть ненормальными у пациентов с СКВ.С этой целью анализ ДНК-микрочипов генов, экспрессируемых в мононуклеарных клетках периферической крови во время менструального цикла здоровых женщин, сравнивался с таковыми у женщин с СКВ и показал интересные различия. В частности, член суперсемейства рецепторов фактора некроза опухолей 14 (TNFRSF14; синоним: медиатор проникновения вируса герпеса, HVEM) был увеличен в корреляции с повышением уровней эстрогена в сыворотке у здоровых женщин, но не у пациентов с СКВ. TNFRSF14 является лигандом для аттенюатора В- и Т-лимфоцитов, ингибирующего рецептора, который подавляет активацию лимфоцитов и играет важную роль в поддержании иммунного гомеостаза.Эти результаты предполагают, что механизмы, регулирующие иммунные активирующие эффекты эстрогена, могут быть дефектными у пациентов с СКВ. 21
Общая химическая структура и функция эндокринной системы животных — эндокринная система
Стероидные гормоны являются производными холестерина и включают продукты коры надпочечников, яичников и семенников, а также соответствующую молекулу, витамин D. белковые / полипептидные гормоны, зрелые стероидные гормоны не хранятся в больших количествах.При необходимости они быстро синтезируются из холестерина в результате ряда ферментативных реакций. Большая часть холестерина, необходимого для быстрого синтеза стероидных гормонов, хранится внутриклеточно в исходной ткани. В ответ на соответствующие сигналы предшественник перемещается к органеллам (митохондриям и гладкой эндоплазматической сети), где ряд ферментов (например, изомеразы, дегидрогеназы) быстро превращает молекулу в соответствующий стероидный гормон. Таким образом, идентичность конечного стероидного продукта определяется набором ферментов, экспрессируемых в этой ткани.
Стероидные гормоны гидрофобны и легко проходят через клеточные мембраны. В крови они в значительной степени связаны с белками-носителями. Альбумин довольно слабо связывает многие стероиды; кроме того, глобулины специфического связывания существуют для многих стероидных гормонов. Большая часть циркулирующего стероидного гормона связана с белками-носителями, а небольшая часть циркулирует в свободном или несвязанном виде. Считается, что эта последняя фракция доступна для входа в клетки-мишени, т.е. является биологически активной частью.Во внеклеточной жидкости существует быстрое равновесие между связанными с белками и несвязанными стероидами. Возможные роли белков, связывающих стероидные гормоны, включают помощь в доставке стероидов в ткани путем обеспечения равномерного распределения по всем клеткам в ткани-мишени, буферизации против больших колебаний свободного гормона и продления периода полужизни стероидов в крови. По сравнению с белковыми / полипептидными гормонами стероиды обычно имеют более длительный период полураспада, часто в диапазоне от многих минут до часов.
Стероидные гормоны действуют на клетки-мишени через рецепторы, расположенные внутри клетки.Эти рецепторы обычно находятся в ядре, хотя некоторые из них, по-видимому, находятся, когда не заняты, в цитоплазме. Существует несколько классов стероидных рецепторов — для глюкокортикоидов, минералокортикоидов, прогестинов и т. Д. Стероидные рецепторы включают семейство родственных белков, которые также проявляют гомологию с рецепторами гормонов щитовидной железы и витамина D. задачи: одна для распознавания и связывания стероида, другая для связывания с определенной областью хромосомной ДНК и третья для помощи в регулировании транскрипционного комплекса.
Стероидные гормоны проникают в мишени, диффундируя через клеточную мембрану и затем связываясь с рецептором, вызывая конформационные изменения в новом комплексе. Это, в свою очередь, приводит к высвобождению связанных белков (например, белков теплового шока) и перемещению в ядро (при необходимости) с последующим связыванием комплекса с участками ДНК, расположенными рядом со специфическими регулируемыми стероидами генами. В результате изменяется скорость транскрипции определенных генов, увеличивая или уменьшая их экспрессию.Таким образом, стероидные гормоны в первую очередь действуют, влияя на скорость производства специфической информационной РНК и белков в мишенях.
Действие стероидов проявляется относительно медленно (часы), но может быть длительным из-за продолжительности продукции и периодов полураспада информационной РНК и белков, индуцированных в клетках-мишенях. Становится все более очевидным, что некоторые стероиды действуют через негеномные механизмы. Например, считается, что многие из противовоспалительных эффектов глюкокортикоидов обусловлены связыванием комплекса глюкокортикоид-рецептор с провоспалительными факторами транскрипции внутри клеток и ингибированием их действия.Кроме того, быстрые эффекты стероидов, вероятно, опосредованы, по крайней мере частично, их связыванием с неклассическими рецепторами, расположенными на мембранах клеток-мишеней.
Стероиды из крови выводятся метаболизмом в печени. Производятся восстановленные формы, которые впоследствии конъюгируются с глюкуроновой кислотой и сульфатом. Эти метаболиты легко растворяются в крови и выводятся из организма через почечную экскрецию и через желудочно-кишечный тракт. Небольшие количества свободного стероидного гормона также напрямую выводятся почками.
Физиология, эндокринные гормоны — StatPearls
Проблемы, вызывающие озабоченность
Гипоталамус
Гормоны заднего гипофиза (нейрогипофиза)
Задний гипофиз является продолжением проекций аксонов супраоптических и паравентрикулярных ядер нервной ткани гипоталамуса, где окситоцин и антидиуретический гормон хранятся на концах аксонов или тельцах сельди [1]. ] Секреция окситоцина вызывает положительную обратную связь во время родов, что приводит к усилению сокращений.Окситоцин также влияет на лактацию. Окситоцин подробно обсуждается в этой статье. [2]
Антидиуретический гормон (ADH) или вазопрессин важен для регулирования объема крови и уровня электролитов, особенно натрия. Его основная функция — регулировать осмолярность сыворотки. Когда осмоляльность у нормального человека ниже 280 мОсм / кг, уровни АДГ будут ниже. Это приводит к выведению воды. И наоборот, когда осмоляльность плазмы превышает 280 мОсм / кг, уровни АДГ повышаются, что приводит к реабсорбции воды.Помимо стимуляции осморецепторов, рецепторы, чувствительные к объему, также могут запускать высвобождение АДГ. [3] Чувствительные к объему рецепторы увеличивают АДГ только при внезапном и значительном падении давления. Небольшого постепенного снижения будет недостаточно для активации АДГ — ренин и норадреналин вместо этого справятся с этими меньшими изменениями. [4] [5] АДГ увеличивает задержку воды и повышает кровяное давление через два разных рецептора. В дистальном отделе нефрона рецепторы V2 помогают увеличить реабсорбцию воды за счет увеличения количества каналов аквапорина в основных клетках собирательного канала.Повышенный уровень АДГ также стимулирует рецепторы V1, которые увеличивают сопротивление сосудов во всем теле. [6] [7] Подробно это обсуждается в этой статье. [8]
Гормоны, влияющие на переднюю часть гипофиза
Ось гипоталамо-гипофиз-надпочечники (HPA) — это портальная система крови, соединяющая гипоталамус и передний гипофиз, что позволяет контролировать несколько гормонов. Гипоталамус анатомически связан с гипофизом через воронку. Внутри воронки находятся капилляры, которые впадают в воротные вены и текут непосредственно в переднюю долю гипофиза.Эта система гарантирует, что гормоны, выделяемые гипоталамусом, циркулируют непосредственно в передней доле гипофиза, никогда не попадая в общий кровоток. Гормоны, выделяемые гипоталамусом, включают кортикотропин-высвобождающий гормон, тиреотропин-высвобождающий гормон, гонадотропин-высвобождающий гормон, высвобождающий гормон роста, соматостатин, пролактин-высвобождающий гормон и дофамин. [1]
Гонадотропин-рилизинг-гормон (GnRH) — это гормон, выделяемый гипоталамусом и действующий на гипофиз для контроля репродуктивных функций.Есть два важных фактора для правильной функции ГнРГ, включая правильную миграцию нейронов во время развития и пульсирующую секрецию. [9] Небольшое количество нейронов гипоталамуса высвобождает гонадолиберин, клетки плода мигрируют в обонятельную луковицу и обонятельный тракт, откуда они переходят в медиобазальный гипоталамус в преоптической области, а также в дугообразное ядро. Клетки плода в обонятельной области обладают способностью обнаруживать пахучие стимулы и высвобождать гонадолиберин. Важность миграции нейронов ГнРГ получила подтверждение в случае абортированного плода с диагнозом синдрома Каллмана.[10] У плода был старший брат с такой же делецией Х-хромосомы; однако дальнейшее невропатологическое обследование показало, что нейроны ГнРГ были задержаны на решетчатой пластине. Плод был достаточно взрослым, чтобы эти нейроны уже должны были переместиться в гипоталамус. [10] Кроме того, считается, что аносмия присутствует у пациентов с дефицитом ГнРГ из-за тесной ассоциации нейронов ГнРГ с обонятельной луковицей и трактом. Пульсирующее свойство нейронов ГнРГ было продемонстрировано, когда иммортализованная ткань in vitro продолжала высвобождать ГнРГ пульсирующим образом — не только предполагая возможный внутренний генератор импульсов гипоталамуса, но и подчеркивая важность самого импульса.[9] Генератор импульсов выделяет GnRH очень дискретными, случайными, но все же регулярными всплесками. В настоящее время точно установлено, что пульсация гонадолиберина приводит к соответствующему физиологическому уровню гонадотропина. Однако, когда ГнРГ вводится непрерывно, уровень гонадотропинов в сыворотке сначала повышается, но быстро снижается из-за десенсибилизации. [11] [12] [13] Это имеет важное клиническое значение при различных формах рака и гинекологической патологии. При прекращении непрерывного приема гонадолиберина спонтанные импульсы гонадолиберина вернутся, восстанавливая гонадотропиновый ответ.
ГнРГ имеет очень короткий период полураспада, всего от 2 до 4 минут, и стимулирует высвобождение лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) — эти два гормона обычно называют гонадотропинами. [14] Гонадотропины и половые стероиды имеют как отрицательную, так и положительную обратную связь по пульсации гонадолиберина. Как работают эти петли, до конца не изучено. Однако не только половые гормоны влияют на гонадолиберин, но и многие другие молекулы влияют на гонадолиберин. Некоторые из этих молекул включают опиаты, гонадные стероиды, кисспептин, нейрокинин B, катехоламины, нейропептид Y, кортикотропин-рилизинг-гормон, галанин, динорфин и пролактин.ГнРГ, ЛГ и ФСГ регулируют различные функции, важные для полового развития человека, производства секса и фертильности. [15] [16] Для получения дополнительной информации см. Разделы о ЛГ и ФСГ. Это подробно обсуждается в этой статье. [17]
Кортикотропин-рилизинг-гормон (CRH) — еще один гормон, участвующий в системе гипоталамус-гипофиз-надпочечники (HPA). CRH вырабатывается в паравентрикулярном ядре гипоталамуса (PVH), которое высвобождается и стимулирует выделение адренокортикотропного гормона (ACTH) передней долей гипофиза.[18]
Гормон, высвобождающий гормон роста, (GHRH) — это гипоталамический гормон, который связывается с рецепторами гипофиза для стимуляции высвобождения гормона роста (GH). Связывание с его рецептором приводит к активации связанного G-белка, который стимулирует выработку цАМФ. Эта внутриклеточная передача сигналов приводит к фактическому высвобождению GH и пролиферации соматотрофов. Есть подозрение, что GHRH выделяется пульсирующим образом, поскольку GH является пульсирующим. Однако это еще не полностью понято. [19]
Соматостатин — имеет две биологически активные формы — соматостатин-14 (S14) и соматостатин-28 (S28) — это 14 и 28 аминокислот соответственно.Он синтезируется дельта-клетками островков Лангерганса в поджелудочной железе и паракринными клетками, разбросанными по желудочно-кишечному тракту. Соматостатин присутствует во всем организме, но его особенно много в нервной ткани спинного мозга, ствола мозга, гипоталамуса и коры головного мозга. [20] При высвобождении соматостатин имеет очень короткий период полувыведения. После внутривенного введения 50% будет выведено из обращения менее чем за три минуты. В результате концентрация соматостатина в крови довольно низкая, обычно в субпикомолярных количествах.Рецепторы соматостатина — это рецепторы, связанные с G-белком, которые при активации снижают уровни цАМФ. Существует пять подтипов рецепторов, подтипы 1-5. Все пять присутствуют в мозгу; однако каждый рецептор обладает тканевой специфичностью. Подтип 1 присутствует в головном мозге, легких, поджелудочной железе, печени и желудочно-кишечном тракте. Подтип 2 обнаруживается в головном мозге и почках. Подтип 3 находится в головном мозге и поджелудочной железе. Подтип 4 присутствует в головном мозге и легких. Подтип 5 встречается в головном мозге, скелетных мышцах, желудочно-кишечном тракте, сердце, надпочечниках и гипофизе.[21]
Как только соматостатин связывается со своим рецептором, он ингибирует высвобождение GH из гипофиза. [22] Помимо ингибирования GH, соматостатин обладает дополнительными физиологическими свойствами во многих органах. Внутри мозга он обладает антиноцицепционными свойствами. В печени / желчном пузыре соматостатин снижает кровоток, подавляет сокращение желчного пузыря и подавляет секрецию желчных протоков. Поджелудочная железа будет иметь как эндокринные, так и экзокринные секреции, которые подробно обсуждаются в этой статье.Наконец, соматостатин ингибирует амилазу слюны, желудочную кислоту и секрецию желудочно-кишечных гормонов в желудочно-кишечной системе. Он также задерживает опорожнение желудка, замедляет моторику, подавляет абсорбцию и уменьшает внутренний кровоток. [23] [24] Подробно это обсуждается в этой статье. [25]
Допамин — важная молекула в организме человека; он играет роль во многих различных органах. Это наиболее часто обсуждается в психиатрических и неврологических учреждениях из-за его роли в качестве нейротрансмиттера.Однако дофамин также является эндокринным гормоном, секретируемым гипоталамусом в гипофиз. Основная роль в физиологии эндокринных гормонов заключается в подавлении секреции пролактина. Было хорошо установлено и изучено, что патология или побочные эффекты лекарств от снижения дофамина приводят к гиперпролактинемии и патофизиологии, связанной с этим состоянием. [26] Это подробно обсуждается в этой статье. [27]
Тиротропин-рилизинг-гормон (TRH) состоит из трех пептидов, пироглутамил-гистидил-пролинеамида.TRH начинается как про-TRH и в процессе пептизации и циклизации глутамина образует пироглутамильный остаток. [10] Метаболизм TRH происходит быстро, с периодом полувыведения из плазмы примерно три минуты. TRH — еще один гормон, участвующий в оси HPA, помогающий определять регуляцию секреции ТТГ. В частности, TRH обнаруживается в самых высоких концентрациях в PVH и среднем возвышении гипоталамуса. Однако он также присутствует в центральной нервной системе, желудочно-кишечном тракте, островках поджелудочной железы, гипофизе и репродуктивных трактах — функция TRH на этих участках неизвестна.Наконец, высокие уровни или экзогенное введение TRH будут стимулировать дополнительные гормоны помимо ТТГ, особенно пролактин. [28] [29] [30] [31]
Передний гипофиз
Фолликулостимулирующий гормон (ФСГ) и Лютеинизирующий гормон (ЛГ) — см. Раздел эндокринных половых гормонов ниже.
Пролактин — это гормон, вырабатываемый лактотрофами передней доли гипофиза. Регулирование пролактина осуществляется гипоталамусом ингибирующим образом, то есть дофамин высвобождается из гипоталамуса, чтобы уменьшить секрецию пролактина.Все остальные гормоны зависят от сигнала стимуляции от гипоталамуса, который будет синтезироваться и высвобождаться. Это объясняет, почему с отключением оси HPA уровни пролактина увеличиваются, тогда как уровни других гормонов уменьшаются. [32]
Когда пролактин секретируется, он стимулирует выработку молока в молочных железах. Во время беременности повышенный уровень эстрогена воздействует на переднюю долю гипофиза, дополнительно увеличивая секрецию пролактина, подготавливая молочные железы к грудному вскармливанию. Однако также повышается уровень прогестерона, который действует на грудь, подавляя пролактин.Вот почему секреция молока начинается только после рождения, потому что послеродовая физиология приводит к резкому снижению уровня прогестерона, что приводит к потере ингибирования пролактина. [33] Это подробно обсуждается здесь. [34]
При первичном гипотиреозе уровень ТТГ будет повышаться при попытках повысить уровень ТТГ. TRH может воздействовать на переднюю долю гипофиза, повышая уровень пролактина. Антипсихотические средства являются антагонистами дофамина, что означает потерю обычного ингибирующего гормона, что приводит к повышению пролактина.В любом из вышеперечисленных сценариев, помимо нескольких других (например, пролактиномы), будет присутствовать гиперпролактинемия. Повышенный уровень пролактина приводит к ингибированию GnRH, снижение пульсации приводит к снижению уровней FSH и LH. Обычно проявляющиеся симптомы включают аменорею и бесплодие как у мужчин, так и у женщин. [35] [36] [37] [38]
Тиреотропный гормон (тиреотропин) (ТТГ) — ТТГ синтезируется и высвобождается из клеток передней доли гипофиза, известных как тиреотрофы.Этот гормон состоит из двух субъединиц: 1 альфа и 1 бета. ТТГ — один из четырех гормонов, которые имеют одну и ту же альфа-единицу. Бета-единица — это то, что делает ТТГ уникальным и определяет его специфичность в организме человека. Благодаря физиологическим эффектам тироксина (Т4) и трийодтиронина (Т3) эти два гормона помогают жестко контролировать уровень ТТГ, выделяемого в организм. [39] Незначительное повышение Т3 и Т4 в сыворотке приведет к ингибированию ТТГ. И наоборот, небольшое снижение Т3 и Т4 в сыворотке приводит к увеличению ТТГ.Уровни T3 и T4 также будут работать для увеличения / уменьшения TRH через отрицательную обратную связь, еще один механизм для модуляции уровней TSH. [40]
Уровни ТТГ будут медленно меняться в зависимости от нескольких факторов, таких как начальный уровень ТТГ, введенный гормон (Т3 или Т4) и доза данного гормона. Для снижения более высокого уровня ТТГ потребуется больше времени, и он будет постепенно снижаться в течение нескольких дней. Уровни ТТГ быстрее реагируют на Т3, чем на Т4. Кроме того, при более высокой дозе ТТГ будет реагировать быстрее.Если вводить высокие дозы Т3, уровень ТТГ начнет снижаться в течение нескольких часов у пациентов с гипотиреозом. Другие ингибиторы ТТГ включают соматостатин, дофамин и глюкокортикоиды. Дофамин может вызвать быстрое снижение уровня ТТГ, и, соответственно, антагонисты дофамина могут резко повысить уровень ТТГ. У пациентов в отделении интенсивной терапии (ОИТ) часто изменяются уровни ТТГ при приеме дофамина или антагонистов дофамина. ТТГ — один из четырех эндокринных гормонов (ХГЧ, ТТГ, ЛГ, ФСГ), которые имеют одну и ту же альфа-единицу.Существуют патологические состояния, такие как хориокарцинома, при которых резкое повышение уровня ХГЧ приводит к симптомам гипертиреоза, поскольку рецепторы ТТГ связывают ХГЧ за счет общей альфа-единицы. [41] [42] Это подробно обсуждается здесь. [43]
ТТГ является важным гормоном щитовидной железы. Он стимулирует каждый этап синтеза гормонов в щитовидной железе, влияет на экспрессию нескольких генов и может вызвать гиперплазию или гипертрофию щитовидной железы. Действие начинается, когда ТТГ связывается с рецептором плазматической мембраны, активируя аденилатциклазу, которая увеличивает циклический аденозинмонофосфат (цАМФ), что приводит к активации нескольких протеинкиназ.Через тот же рецептор ТТГ стимулирует фосфолипазу С, увеличивая оборот фосфоинозитидов, активность протеинкиназы С и концентрацию внутриклеточного кальция. Как указанные выше шаги конкретно связаны с синтезом, высвобождением Т3 и Т4 и другими метаболическими процессами в щитовидной железе, до конца не изучено. [44] [42]
Гормон роста (GH) — гормон, синтезируемый соматотрофными клетками гипофиза. Он имеет пять различных генов, которые влияют на окончательный гормон мРНК сплайсинга. [45] Преобладающая форма — 22 кДа GH; другая форма — 20 кДа GH (только 10%).Многие факторы влияют на производство и высвобождение GH, двумя основными факторами являются GHRH и соматостатин — стимулирующий и ингибирующий, соответственно. Однако пол, возраст, питание и инсулиноподобный фактор роста-1 (IGF-1) — все это влияет на уровень GH. [46] Его производство начинается у плода. Материнские уровни GH фактически снизятся из-за увеличения плацентарного GH, который заменяет материнские уровни. Пик уровня GH в период полового созревания, во время экстенсивного роста, составляет около 150 мкг / кг. По мере того как старение продолжается, уровень гормона роста снижается параллельно снижению индекса массы тела.Каждые семь лет уровень GH снижается примерно на 50%. К 55 годам уровень гормона роста будет примерно 25 мкг / кг. [47]
Высвобождение GH является пульсирующим — предполагается, что это связано с пониженным тоническим ингибированием соматостатина и, возможно, всплесками GHRH. Каждый день происходит десять пульсаций продолжительностью 90 минут, каждая из которых разделена 128 минутами. Как упоминалось ранее, пол влияет на уровень гормона роста. У мужчин пульсация гормона роста более заметна, тогда как у женщин секреция гормона роста более непрерывна. Пик секреции гормона роста происходит в течение одного часа после начала глубокого сна.Средний уровень гормона роста в сыворотке крови в ночное время составляет 1,0 ± 0,2 нг / мл. Напротив, средний дневной уровень гормона роста составляет всего 0,6 +/- 0,1 нг / мл. IGF-1, лептин, возраст, ожирение и гипергликемия — все это факторы, ингибирующие высвобождение GH. И наоборот, грелин, инсулино-индуцированная гипогликемия, эстроген, дофамин, альфа-адренергические агонисты и бета-адренергические антагонисты — все стимулируют GH. Хотя многие различные факторы модулируют уровни GH, важно помнить, что GHRH и соматостатин в первую очередь определяют уровни GH.[48] [49] [50] Более подробно это обсуждается здесь. [51]
После связывания GH его рецептора, в первую очередь обнаруженного в печени, активируется каскад фосфорилирования с участием пути JAK / STAT. Преобладающее действие — стимулировать печень к синтезу и секреции IGF-1. IGF-1 является чрезвычайно важным белком, индуцируемым GH, и считается, что он отвечает за большинство свойств роста GH. Некоторые из специфических эффектов GH включают: стимуляцию линейного роста у детей, усиление липолиза, усиление синтеза белка, удержание фосфатов, натрия и воды и антагонизм инсулина.Опять же, большинство этих действий, как полагают, происходит от GH в тандеме с IGF-1. [45] [52] [53]
Адренокортикотропный гормон (АКТГ) — гормон, секретируемый передней долей гипофиза в ответ на CRH. АКТГ проходит через системный кровоток, воздействуя на надпочечники, в частности на фасцикулярную и сетчатую зоны коры надпочечников. АКТГ в первую очередь действует непосредственно в фасцикулярной зоне, высвобождая кортизол. АКТГ стимулирует фермент холестерин-десмолазу, который является первым ферментом, участвующим в преобразовании холестерина в несколько стероидных гормонов.АКТГ также стимулирует выработку андрогенов в ретикулярной зоне, побочного продукта синтеза кортизола (дополнительную информацию см. В разделе «Андрогены надпочечников» ниже). [54] [55]
Шишковидная железа
Мелатонин — гормон, синтезируемый в шишковидной железе из аминокислоты триптофана. [56] Триптофан гидроксилируется, а затем декарбоксилируется с образованием 5-гидрокситриптамина или серотонина. Когда есть солнечный свет, серотонин накапливается в пинеалоцитах, что делает его недоступным для моноаминоксидазы, фермента, который превращает серотонин в мелатонин.В отсутствие света симпатический ввод увеличивается, вызывая выброс адреналина. Это вызывает высвобождение серотонина в пинеалоцитах. Одновременно норэпинефрин активирует моноаминоксидазу, серотонин-N-ацетилтрансферазу и гидроксииндол-O-метилтрансферазу. [57] [56] [58] Результатом является быстрое повышение уровня мелатонина с 2 до 10 пг / мл до 100-200 пг / мл. [56] Мелатонин хорошо растворяется в липидах, что позволяет ему свободно диффундировать через клеточные мембраны и гематоэнцефалический барьер. [59] Его выпуск посылает сообщения по всему телу, в первую очередь в мозг, влияя на синтез вторичных мессенджеров.У мелатонина есть три рецептора: M1, M2 и M3. Все три экспрессируются в супрахиазматическом ядре (SCN) гипоталамуса. Эти три рецептора выражены по-разному в зависимости от ткани. Однако внутри SCN M1 будет подавлять активацию нейронов SCN в ночное время.
Кроме того, M2 в SCN подавляет циркадный ритм SCN. Эти эффекты могут способствовать улучшению сна мелатонином. M1 и M2 легко десенсибилизируются, поэтому при хроническом приеме экзогенного мелатонина могут потребоваться более высокие дозы для достижения того же эффекта.[60] [61] Каскад мелатонина в первую очередь влияет на сон и циркадные ритмы. Предполагается, что мелатонин является одним из основных факторов стимуляции и поддержания сна из-за его заметного увеличения по вечерам. Как упоминалось ранее, циркадный ритм характеризуется низким уровнем мелатонина в дневное время и заметно повышенным уровнем в ночное время — пик между 23:00 и 3:00 — быстро снижающийся снова перед восходом солнца. [56] Свет из окружающей среды имеет тесную связь с циркадным ритмом; однако этот ритм сохраняется, когда люди остаются в темной комнате в течение нескольких дней.[62]
Кроме того, если человек перемещается через часовые пояса в новое место, где солнце восходит и заходит в разные часы, циркадный ритм не изменится немедленно. [63] Мелатонин не вырабатывается в значительных количествах в других частях тела — у людей после пинеалэктомии практически не будет мелатонина и полного отсутствия циркадного ритма. [64] Эти данные указывают на важность мелатонина в циркадных ритмах, а также в индукции и поддержании сна.
Щитовидная железа
Общие действия T3 / 4 — гормоны щитовидной железы имеют решающее значение на протяжении всей жизни человека.В детском возрасте гормоны щитовидной железы помогают развивать несколько систем организма, особенно мозг. В зрелом возрасте гормоны щитовидной железы помогают управлять метаболической активностью и функциями почти всех органов. Поскольку это необходимо для очень многих различных систем, требуется постоянное поступление гормонов щитовидной железы, но при этом общие уровни в сыворотке всегда строго контролируются; в противном случае возникнет патология. Два механизма контролируют производство гормонов щитовидной железы. Первый — через гормональные пути и петли отрицательной обратной связи.Уровни TRH, TSH, T4 и T3 будут сигнализировать щитовидной железе, повышать или понижать уровни гормонов щитовидной железы. Второй — через потребление гормонов экстратироидными тканями в зависимости от пищевых, гормональных и связанных с заболеванием факторов — эффект варьируется в зависимости от ткани.
Первый механизм помогает защитить щитовидную железу от гипер / гипосекретирования, а второй механизм помогает реагировать на быстрые изменения в тканях. Как упоминалось ранее в разделе ТТГ, существует два гормона щитовидной железы, Т3 и Т4.Однако, прежде чем любой из гормонов сможет начать синтез, йодид должен подвергнуться окислению до йода и включиться в остатки тирозина в коллоиде. Йодид является важным ионом в физиологии щитовидной железы и будет снова обсужден в патофизиологии. Остальные этапы синтеза гормона включают объединение двух молекул дииодтирозина (DIT) для образования T4 или объединение одного монойодтирозина и одного DIT для создания T3. Тироглобин — это гликопротеин, который включается в экзоцитотические везикулы, которые сливаются с апикальной клеточной мембраной — только после того, как эти этапы выполнены, может происходить йодирование и связывание Т4 и Т3.Чтобы высвободить эти гормоны во внеклеточную жидкость и, в конечном итоге, в циркуляцию, тиреоглобулин должен резорбироваться в фолликулярных клетках щитовидной железы с образованием коллоидных капель. Эти коллоидные капли сливаются с лизосомами, образуя фаголизосомы, позволяя гидролизовать тиреоглобулин, обеспечивая секрецию гормона. [65] [40] [42]
Т4 (99,95%) и Т3 (99,5%) в основном связаны с кровотоком, что препятствует его метаболической активности. Белки, связывающие Т4 и Т3, перечисленные в списке от наиболее распространенных до наименее распространенных, следующие: тироксин-связывающий глобулин (ГТГ), транстиретин (TTR), альбумин и липопротеины.Оставшиеся 0,02 процента свободного Т4 оставляет в организме только 2 нг / дл. Точно так же 0,05 процента Т3 оставляет только 0,4 нг / дл. Поскольку большая часть Т4 и Т3 связывается в сыворотке, изменения сывороточных концентраций связывающих белков приводят к резким эффектам на общий уровень Т4 и Т3 в сыворотке. Однако изменения в связывающих белках не влияют на концентрацию свободных гормонов или скорость T4, и T3 метаболизируется. [66]
Тироксин (T4) — T4 менее метаболически активен и вырабатывается исключительно в щитовидной железе.Суточная выработка составляет от 80 до 100 мкг и деградирует примерно на 10% в день. Примерно 80% деиодировано — из них 40% преобразуется в T3, остальные 40% преобразуются в обратный T3 (rT3). Конечные 20% конъюгаты с тетрайодтироуксусной кислотой. Превращение на периферии Т4 в Т3 опосредуется ферментом 5’-дейодиназой. Т3 — это основной метаболит Т4, обладающий физиологической активностью; другие метаболиты Т4 неактивны. Этот процесс преобразования регулируется в экстратироидной ткани. Таким образом, продукция Т3 может изменяться независимо от состояния гипофиза и щитовидной железы.[67]
Трийодтиронин (T3) — T3 — это основной метаболический гормон щитовидной железы, который является движущей силой метаболических и внутренних процессов. Около 80% продукции Т3 происходит в экстратироидной ткани за счет дейодирования Т4. Остальные 20% синтезируются в щитовидной железе. Суточная выработка составляет от 30 до 40 мкг, но экстратироидный резерв Т3 составляет примерно 50 мкг. Доля Т3, продуцируемая по всему телу из Т4, значительно варьируется от ткани к ткани. Некоторые ткани, такие как передняя доля гипофиза и печень, содержат высокие уровни ядерных рецепторов Т3, что делает их более чувствительными к Т3 в сыворотке.[67] [68]
T3 действует путем модификации транскрипции генов. Благодаря широкому действию Т3, он влияет почти на все ткани на способность синтезировать белок и субстрат обмена. Ядерное действие T3 будет зависеть от четырех факторов: доступности гормона, ядерных рецепторов (TR) тироидных гормонов, доступности рецепторных кофакторов и регуляторных элементов ДНК. В большинстве тканей Т3 попадает путем простой диффузии. Однако в головном мозге и щитовидной железе Т3 активно транспортируется в клетки. В зависимости от ткани Т3 будет иметь разное действие, которое определяется местным продуцированием Т3, а также количеством и распределением изоформ TR.Изоформы состоят из TR-альфа-1 и 2 и TR-бета-1,2 и 3. Изоформ TR недостаточно изучены, но из-за регионального или клеточно-специфического распределения TR это наводит на мысль о различных функционирует даже в пределах одной и той же ткани. Например, TR-альфа является доминирующей изоформой в головном мозге, но TR-бета-2 присутствует в очень высоких количествах в гипоталамусе и гипофизе.
Данные, которые существуют для изоформ TR, получены в основном от мышей с нокаутом с точечными мутациями гена TR.Мыши с делецией TR-альфа демонстрируют плохое питание и рост, замедленную частоту сердечных сокращений, низкую базальную температуру тела и пониженную минерализацию костей. Мыши с инактивацией гена TR-бета показали признаки несоответствующего нормального уровня ТТГ в сыворотке, высоких концентраций Т4 в сыворотке и гиперплазии щитовидной железы. Наконец, нокаутные мыши без генов TR-альфа и бета показали гиперплазию щитовидной железы и заметно высокие сывороточные концентрации Т4, Т3 и ТТГ, которые были в 11 раз, 30 раз и 160 раз выше нормы, соответственно.[69] [70] [42] [39]
Как упоминалось ранее, T3 связывается с TR в ядре, что приводит к модуляции экспрессии гена. Все затронутые гены имеют специфические последовательности ДНК, которые связывают TR с высокой аффинностью. В конечном итоге проект генома человека предоставил данные, позволяющие идентифицировать конкретные последовательности ДНК. Без этих специфических последовательностей ДНК Т3-зависимая активация гена будет минимальной или полностью отсутствовать.
В различных тканях на периферии имеется одна из 3 дейодиназ, которые превращают прогормон Т4 в активный Т3.Три из трех ферментов будут экспрессироваться в зависимости от конкретной модели развития и типа ткани. [68] [71]
5’-дейодиназа типа 1 (Dio1) обнаруживается в основном в печени, почках и мышцах. Было обнаружено, что Dio1 имеет пониженную активность у пациентов с гипотиреозом.
5’-дейодиназа типа 2 (Dio2) была изучена на грызунах и показала более высокую распространенность в коре головного мозга, буром жире и гипофизе. У людей Dio2 также экспрессируется в скелетных мышцах, сердце и щитовидной железе.У людей Dio2 производит большую часть циркулирующего Т3. Было обнаружено, что Dio2 увеличивается у субъектов с гипотиреозом и йодной недостаточностью.
5’-дейодиназа типа 3 (Dio3) фактически инактивирует Т4 и обнаруживается в основном в плаценте, коже, скелетных мышцах и развивающемся мозге. Это важно для сенсорного развития, особенно во внутреннем ухе. Во время человеческого развития Dio3 выражается первым; по мере увеличения Dio1 и Dio2 экспрессия Dio3 будет уменьшаться.
Хорошо известно, что Т4 и Т3 имеют далеко идущие эффекты и могут влиять почти на все системы органов в организме; В частности, три основных области включают кости, сердце и регуляцию метаболизма.
- Кости. У пациентов младенческого возраста, родившихся с врожденным гипотиреозом и не получающих заместительную гормональную терапию, будет задержка развития эпифиза и замедленный рост. Такой же результат наблюдался у пациентов с резистентностью к гормонам щитовидной железы [18, стр. 6]. Все изоформы TR экспрессируются в костях. Однако мыши с нокаутом TR-альфа и альфа / бета показали аномальное развитие костей. [72] [73]
- Сердце — Пациенты с резистентностью к Т3 демонстрируют повышенный уровень Т3, что приводит к тахикардии.Это, вероятно, демонстрирует, что пациенты, устойчивые к T3, не будут иметь сопротивления сердца. Пациенты с мутациями TR-бета будут фенотипически представлены таким образом, концепция поддерживается мышами с нокаутом T3-beta, которые также не имеют сердечной резистентности к T3. [74]
- Регуляция метаболизма — Т3 регулирует скорость метаболизма и может влиять на умеренные изменения массы тела. Люди с мутациями TR-бета и резистентностью к Т3 демонстрируют повышенную активность Т3-альфа — эта стимуляция приводит к усиленному питанию и усиленному окислению жирных кислот.Т3 также влияет на метаболизм глюкозы, увеличивая ее усвоение. Когда Dio2 не функционирует должным образом, очевидна связь с непереносимостью глюкозы. Это еще недостаточно изучено, но у пациентов с нарушенным митохондриальным окислительным метаболизмом (наблюдаемым при метаболическом синдроме и диабетиках 2 типа) может быть снижено действие гормона Т3. Осложнения неправильного метаболизма будут обсуждаться в разделе «Патология гормонов щитовидной железы». [75] [76] [42]
Паращитовидная железа
Паратироидный гормон (ПТГ) — ПТГ является основным регулятором гомеостаза кальция и фосфата в организме человека.ПТГ синтезируется как пре-про-ПТГ, который состоит из 115 аминокислот. В клетках паращитовидной железы он расщепляется до про-ПТГ, 90 аминокислот, и, наконец, до ПТГ, 84 аминокислоты. Версия ПТГ из 84 аминокислот является основной запасенной, секретируемой и активной формой гормона. Кратковременный контроль уровня кальция в сыворотке опосредуется исключительно ПТГ. В долгосрочной перспективе ПТГ отвечает за преобразование кальцидиола в кальцитриол, которое происходит в клетках почечных канальцев. [77] [78] [79]
ПТГ быстро выводится из кровотока почками и печенью.Период полураспада интактного ПТГ составляет 2-4 минуты. Он расщепляется на активные амино-фрагменты (PTH 1-34) и неактивные карбоксильные фрагменты. Поскольку ПТГ в первую очередь контролирует уровни кальция, кальций будет регулировать количество выделяемого, синтезируемого и разлагаемого ПТГ. В гипокальциемическом состоянии деградация ПТГ снижается, и наоборот, во время гиперкальциемии. [80] Изменения концентрации ионизированного кальция в сыворотке до 0,1 мг / дл приведут к увеличению / снижению ПТГ в зависимости от направления сдвига кальция.Эти мелкие изменения улавливаются чрезвычайно чувствительными рецепторами, чувствительными к кальцию (CaSR), которые возникают на поверхности клеток паращитовидной железы. [81] На исходном уровне CaSR активируются посредством белков, связывающих гуанин-нуклеотид, которые используют различные вторичные мессенджеры (внутриклеточный кальций, цАМФ или инозитолфосфаты) для ингибирования ПТГ.
Когда CaSR деактивируется во время гипокальциемии, клетки паращитовидной железы стимулируются к высвобождению ПТГ. CaSR опосредует следующие действия ПТГ: экзоцитоз ПТГ в кровоток (от секунд до минут), уменьшает внутриклеточный распад ПТГ (от минут до часа), увеличивает экспрессию гена ПТГ (от часов до суток), пролиферирует клетки паращитовидной железы (от нескольких дней до недель). ).[77] Хотя кальций является основным двигателем ПТГ, другие молекулы также влияют на высвобождение ПТГ; они включают внеклеточный фосфат, кальцитриол и фактор роста фибробластов 23 (FGF23). [82] [83] [84]
Первичный рецептор PTH, известный как PTh2R, будет связываться и отвечать на PTH, PTH-родственный белок (PTHrP) и PTh2-34. Рецептор сильно экспрессируется в костях и почках, но также может присутствовать в груди, сердце, коже, поджелудочной железе и сосудистой ткани. Когда PTh2R активируется, множественные внутриклеточные пути передачи сигналов (цАМФ, путь фосфолипазы C, протеинкиназа C и внутриклеточный кальций) помогают опосредовать эффекты PTH.Биологическое действие ПТГ включает: усиление резорбции костей (в течение нескольких минут), увеличение абсорбции кальция в ЖКТ, опосредованное кальцитриолом (24 часа или более [ПТГ стимулирует гидроксилирование кальцидиола в кальцитриол]) и снижение экскреции кальция с мочой (в течение нескольких минут. ).
Если углубиться в действие ПТГ на кости, то две основные фазы опосредуют увеличение кальция. Во-первых, ПТГ почти сразу мобилизует кальций из запасов скелета. Во-вторых, как упоминалось ранее, ПТГ увеличивает резорбцию костей, что приводит к высвобождению кальция и фосфата (эти действия не сразу).Наконец, почки реабсорбируют кальций по разным механизмам в зависимости от области нефрона, в которой происходит реабсорбция. Например, в проксимальном канальце кальций пассивно реабсорбируется посредством благоприятных электрических градиентов по сравнению с дистальным нефроном, где кальций активно реабсорбируется. Чистым эффектом этих одновременных путей является повышение уровня кальция, что помогает вернуть организм к гомеостатическому уровню. [79] [85] [86]
Поджелудочная железа
Инсулин — инсулин прямо или косвенно влияет на несколько тканей; однако в этой статье основное внимание уделяется жировой ткани, мышцам и печени.Инсулин — это пептид из 51 аминокислоты, который синтезируется и секретируется бета-клетками поджелудочной железы. Его действие начинается, когда он связывает гетеротетрамерный рецептор клеточной мембраны. Рецептор имеет две альфа-субъединицы, которые связывают инсулин, две бета-субъединицы, которые передают сигнал. Благодаря каскаду клеточных сигналов инсулин является мощным регулятором метаболических процессов. Когда происходит нарушение клеточной передачи сигналов, резистентность или снижение инсулина, может возникнуть множество различных патологий — см. Раздел патологии для получения дополнительной информации.Несколько факторов могут дополнительно стимулировать высвобождение инсулина или ингибировать его. Глюкоза, манноза, лейцин и стимуляция блуждающего нерва увеличивают секрецию инсулина. Альфа-адренергические эффекты, соматостатин и некоторые препараты могут подавлять секрецию инсулина.
Одна из основных функций инсулина — контролировать уровень глюкозы. Глюкозу можно получить из трех источников: глюконеогенеза, перорального приема и гликогенолиза. Когда глюкоза оказывается внутри клеток, происходит одно из двух: она может храниться в виде гликогена или подвергаться гликолизу и превращаться в пируват.Инсулин модулирует то, что происходит с глюкозой, несколькими различными способами, например: стимулирует синтез гликогена, увеличивает транспорт глюкозы в мышцы и жировую ткань, ингибирует гликогенолиз и глюконеогенез и увеличивает гликолиз в мышцах и жировой ткани. В то время как большинство тканей могут производить глюкозу в своих клетках, только почки и печень обладают глюкозо-6-фосфатазой, которая необходима для выброса глюкозы в кровь. Печень производит от 80 до 90% глюкозы у пациентов без патологии, связанной с глюкозой, что делает печень основной мишенью для инсулина.Инсулин прямо и косвенно воздействует на печень несколькими различными путями. Инсулин непосредственно ингибирует гликогенфосфорилазу, гликогенолитический фермент, тем самым подавляя выработку глюкозы. Косвенно инсулин снижает поток предшественников глюкозы, а также снижает секрецию глюкагона. Исследование инфузии инсулина собакам продемонстрировало основные эффекты инсулина на глюкозу в печени из-за прямого пути инсулина. Однако при вливании значительных количеств инсулина косвенный эффект стал преобладать.
Утилизация глюкозы возможна за счет клеточного поглощения, что стало возможным благодаря переносчикам глюкозы, GLUT-1,2,3,4 и 5. GLUT-4 является основным переносчиком в мышцах и жировой ткани; он находится в цитоплазме до тех пор, пока сигнал инсулина не переместится к клеточной мембране. Когда организм находится в эугликемическом состоянии, большая часть поглощения глюкозы, которая опосредуется инсулином, будет происходить в мышцах. Менее 10% глюкозы поглощается жировой тканью, в основном из-за ингибирования липолиза инсулином.Мышцы будут получать большую часть глюкозы, потому что, когда свободные жирные кислоты недоступны, требуется повышенное потребление глюкозы для снабжения мышечной ткани. Инсулин оптимизирует гликолиз в мышцах, катализируя гликолитический путь за счет увеличения активности гексокиназы и 6-фосфофруктокиназы.
Как упоминалось ранее, при эугликемических состояниях инсулин подавляет липолиз. После еды инсулин способствует накоплению триглицеридов в жировых клетках. Это опосредуется тремя основными механизмами. Во-первых, инсулин увеличивает клиренс хиломикронов, богатых триглицеридами, за счет увеличения липопротеинлипазы.Однако инсулин только стимулирует экспрессию липопротеинлипазы в жировой ткани; в мышцах инсулин фактически ингибирует липопротеинлипазу, что приводит к накоплению триглицеридов. Второй механизм заключается в стимулируемой инсулином переэтерификации жирных кислот в триглицериды в жировых клетках. Наконец, третий механизм связан с ингибированием липолиза инсулином. Общий эффект метаболизма жиров под действием инсулина заключается в сильном снижении глюконеогенеза в печени и высвобождения глюкозы в печени за счет блокирования поступления жирных кислот в печень.
Динамика кетонов и инсулина — При физиологических состояниях, которые приводят к недостаточному уровню инсулина, например, при длительном голодании или неконтролируемом сахарном диабете, жир мобилизуется для удовлетворения метаболических потребностей. Печень не может справиться со всеми жирными кислотами, которые перемещаются по ней, что приводит к выработке кетоновых тел. Это результат неполного бета-окисления длинноцепочечных жирных кислот, которые поступают в печень в избытке. Кетокислоты можно использовать в качестве топлива во внепеченочных тканях, таких как скелетные мышцы и сердце.Однако при очень продолжительном голодании мозг также будет использовать кетокислоты для получения энергии. Инсулин поддерживает низкий уровень кетоновых тел; он сильно снижает циркулирующие уровни с помощью трех механизмов. Во-первых, инсулин подавляет липолиз, поэтому жирные кислоты, необходимые для производства кетоновых тел, недоступны. Во-вторых, инсулин будет действовать в печени, напрямую подавляя кетогенез. В-третьих, инсулин помогает увеличить периферический клиренс кетоновых тел.
Белковый метаболизм и паракринные эффекты. Как упоминалось ранее, инсулин подавляет глюконеогенез, благодаря чему аминокислоты остаются доступными для синтеза белка.Инсулин ускоряет транспортировку аминокислот в печень и скелетные мышцы. Кроме того, инсулин увеличивает количество и эффективность рибосом. Наконец, инсулин подавляет распад белка; примерно 40% протеолиза зависит от инсулина. Конечный результат — усиление синтеза протеина.
Инсулин оказывает большое влияние на другие гормоны в организме. Клетки островков поджелудочной железы содержат альфа-, бета- и дельта-клетки. Альфа секретирует глюкагон, бета секретирует инсулин, а дельта секретирует соматостатин.Когда эти гормоны секретируются, они оказывают паракринное действие на окружающие клетки. Инсулин сначала достигает альфа-клеток и подавляет высвобождение глюкагона, что вызывает усиление его метаболических действий. В гипергликемических состояниях соматостатин также будет секретироваться, препятствуя высвобождению глюкагоном альфа-клетками и снижением уровня глюкозы. [87] [88] [89] [90] [91]
Инсулин выполняет другие функции, помимо энергетического метаболизма, которые важны для клинических условий, поскольку аномальные реакции на инсулин могут привести к нескольким различным патологиям.Инсулин влияет на стероидогенез, фибринолиз, функцию сосудов и рост. [92] [93] [94] [95] [96]
Глюкагон — пептид из 29 аминокислот, секретируемый альфа-клетками островков Лангерганса. Он противостоит действию инсулина, повышая уровень глюкозы в организме. Прием белка, гипогликемия и физические упражнения приводят к секреции глюкагона, что приводит к повышению уровня глюкозы. Глюкагон может повышать уровень глюкозы в организме за счет увеличения гликогенолиза, конечным продуктом которого является глюкоза.Он также способствует глюконеогенезу, то есть производству глюкозы с использованием молекул-предшественников, таких как аминокислоты и глицерин, в печени. [97] [98]
Надпочечники
Надпочечник расположен чуть выше почки и вырабатывает несколько гормонов, таких как альдостерон, кортизол, ДГЭА, норадреналин и адреналин. Эти гормоны вырабатываются разными участками надпочечников. Кора головного мозга состоит из трех слоев: клубочковой зоны, фасцикульной зоны и ретикулярной зоны, которые секретируют соответственно альдостерон, кортизол и ДГЭА.Мозговое вещество надпочечника состоит из хромаффинных клеток и отвечает за синтез и высвобождение норадреналина и адреналина.
Кортизол — это глюкокортикоидный гормон, синтезируемый в фасцикулярной зоне надпочечников, и АКТГ стимулирует его выработку. Кортизол в первую очередь увеличивает уровень глюкозы в организме, что происходит за счет усиления глюконеогенеза, липолиза и протеолиза. Чтобы поддерживать высокий уровень глюкозы, кортизол также увеличивает инсулинорезистентность, поэтому высокий уровень кортизола может привести к сахарному диабету.Поскольку кортизол является глюкокортикоидом, он обладает дополнительными свойствами, поэтому его можно использовать в качестве лекарства для госпитализированных пациентов. Он может повысить аппетит, повысить кровяное давление, уменьшить образование костей и, что наиболее важно, уменьшить воспалительные и иммунные реакции. У кортизола есть петля отрицательной обратной связи, которая действует на гипоталамус, переднюю долю гипофиза и надпочечники, подавляя высвобождение КРГ, АКТГ и кортизола соответственно. [99] [100]
Альдостерон — Альдостерон является важным минералокортикоидным гормоном в ренин-ангиотензиновой системе (РАС), который важен для регуляции физиологии сердца, почек и сосудов.Путь RAS начинается с расщепления ренина ангиотензиногена на неактивный ангиотензин I, который затем преобразуется через действие ангиотензинпревращающего фермента (АПФ) ангиотензин II (прежде всего в легких). Ангиотензин II опосредует высвобождение альдостерона из клубочковой зоны надпочечников через рецепторы ангиотензина II типа 1 (AT1R). [101]
Путь RAS является основным стимулом альдостерона; однако надпочечники будут вырабатывать небольшие уровни ангиотензина II, АКТГ из передней доли гипофиза, а калий будет стимулировать высвобождение альдостерона.[102] Основное действие альдостерона происходит в почках, где он увеличивает экспрессию натриевых каналов в эпителии в дистальных канальцах. Это, в свою очередь, увеличивает реабсорбцию натрия и, как следствие, воду, выделяя калий. В результате увеличивается объем внеклеточной жидкости, снижается уровень калия в сыворотке и повышается артериальное давление. Ранее считалось, что первичный альдостеронизм является редкой причиной гипертонии. Однако исследования за последние 15 лет показали, что распространенность намного выше.[103] [104] Первоначальное обследование при первичном альдостеронизме включает измерение соотношения ренин: альдостерон, что помогает определить, какие дальнейшие обследования необходимы пациентам с подозрением на это заболевание. [103]
Андрогены надпочечников — это в первую очередь дегидроэпиандростерон (ДГЭА) и сульфат ДГЭА. Производство этих андрогенов в надпочечниках является побочным продуктом синтеза кортизола. В результате основным стимулятором ДГЭА и сульфата ДГЭА является АКТГ. Эти два гормона обладают минимальными андрогенными свойствами, если таковые имеются.Однако хорошо известно, что избыточная секреция DHEA и сульфата DHEA является признаком врожденной гиперплазии надпочечников (CAH). Небольшой процент будет преобразован в андростендион, а затем в тестостерон (и, возможно, эстроген) как в надпочечниках, так и в периферических тканях. Как только это преобразование произойдет, проявятся физиологические эффекты андрогенов (дополнительную информацию см. В разделе «Эндокринные половые гормоны»). Следовательно, вирилизацию у молодых женщин вызывают не ДГЭА и сульфат ДГЭА; скорее, повышенные уровни преобразуются в более сильные андрогены, которые вызывают классический фенотип, наблюдаемый при ХАГ.
Обычно у представителей обоих полов уровни DHEA и сульфата DHEA повышаются в течение периода полового созревания и в течение нескольких лет после полового созревания. Пик уровней приходится на третье десятилетие, а затем постепенно снижается; к 80 годам андрогены надпочечников составляют около 25% по сравнению с возрастом 25 лет. Значение этого открытия (также известного как адренопауза) неизвестно. У мужчин тестостерон из надпочечников составляет менее 5%. Однако у женщин общее количество сывороточного тестостерона, полученного из DHEA и сульфата DHEA, значительно выше.В менструальном цикле, особенно в фолликулярной фазе, 65% выработки тестостерона прямо или косвенно происходит за счет андрогенов надпочечников. [105] [106] [107]
Эпинефрин (адреналин) и n орепинефрин (норадреналин) — эти два гормона будут обсуждаться вместе, поскольку оба они вырабатываются мозговым веществом надпочечников и имеют много общего. Это обсуждение объяснит различные эффекты стимуляции рецепторов альфа-1, бета-1 и бета-2.Понимание того, что происходит при активации определенных рецепторов, облегчит понимание эффектов адреналина и норадреналина. В клинических условиях адреналин и норадреналин имеют несколько различных применений в зависимости от дозы и показаний пациента. [108] [109]
Альфа-1 — стимуляция приводит к использованию каскада IP3-DAG, что приводит к увеличению внутриклеточного кальция. Активация периферических артерий приводит к сужению сосудов, что приводит к увеличению сопротивления и повышению среднего артериального давления (САД).Альфа-1 сужает не только артерии, но и вены. Веноконстрикция приводит к увеличению венозного возврата к сердцу. Некоторые дополнительные случайные эффекты альфа-1 включают мидриаз (расширение зрачка) и задержку мочи за счет сокращения сфинктера уретры и гладких мышц простаты.
Бета-1 — эти рецепторы в основном присутствуют в сердце и при стимуляции вызывают повышенную инотропию и хронотропию, не влияя на сосуды. Бета-1 может также увеличивать высвобождение ренина, что приводит к повышению артериального давления.
Бета-2 — стимуляция этих рецепторов в кровеносных сосудах приведет к расширению сосудов, снижению системного сосудистого сопротивления (SVR), что приведет к снижению диастолического артериального давления. В легких бета-2 вызывает расширение бронхов, в печени — способствует глюконеогенезу, а в глазах — увеличивает образование водянистой влаги.
Адреналин связывает и стимулирует все три рецептора. Преобладание пораженного рецептора зависит от введенной дозы.При более низких дозах преобладает действие бета-рецепторов, что приводит к увеличению сердечного выброса (СО) из-за инотропных и хронотропных эффектов бета-1. Стимуляция альфа-1, которая обычно вызывает сужение сосудов, компенсируется расширением сосудов бета-2. Результатом стимуляции всех трех рецепторов является повышение СО, снижение УВО и различное влияние на САД. Адреналин в высоких дозах вызывает преобладающую стимуляцию альфа-1. Это приводит к увеличению УВО и CO. Адреналин попадает в кровоток во время сильного стресса, такого как сценарии «драки или бегства», или просто жизненный стресс (школа, спорт и т. Д.)). Сильные эмоции, включая гнев или страх, также могут стимулировать секрецию. Его удачно назвали адреналином, потому что, когда вам нужен прилив энергии (чему способствуют вышеупомянутые физиологические эффекты), высвобождается адреналин. [110] [111] [112]
Норэпинефрин действует на рецепторы как альфа-1, так и бета-1, причем преобладающее действие происходит от стимуляции альфа-1. В результате происходит сильное сужение сосудов и незначительное увеличение сердечного выброса. Отмечается умеренный хронотропный эффект, но из-за рефлекторной брадикардии от повышенного САД эффект отменяется.Норэпинефрин часто секретируется вместе с адреналином, потому что стрессоры, которые индуцируют адреналин, также вызывают высвобождение норадреналина. Однако бывают случаи, когда эти два гормона будут секретироваться независимо друг от друга. Норэпинефрин и адреналин имеют другие функции; однако они выходят за рамки эндокринных гормонов и не будут здесь обсуждаться. [113]
Эндокринные половые гормоны
Эндокринные половые гормоны из-за их сложных и совпадающих свойств для обоих полов будут объяснены и обсуждены с гендерной точки зрения, а не с разбивкой по органам.Каждый из половых гормонов выражен и активен как у мужчин, так и у женщин; именно уровни и концентрации помогают развивать и определять внешние и внутренние функции человеческого тела. Исследования и случаи пациентов показали, что мутации классических мужских гормонов или классических женских гормонов по-прежнему могут приводить к патологии, если они отсутствуют у любого пола.
Женское половое развитие, экспрессия и активность гормонов
Физиолог Альфред Йост сформулировал простую модель нормального полового развития.Хромосомный пол (XX или XY) определяет пол гонад, который, в свою очередь, определяет фенотипический пол (мужской или женский). [114] На основе этого модуля должны быть выполнены три взаимозависимых, но последовательных шага. Во-первых, определение хромосомного пола в течение первых шести недель беременности, мужское и женское развитие идентично. Через шесть недель гонады разовьются в соответствующую ткань: яички у мужчин или яичники у женщин. Яички начнут выделять гормоны примерно на шестой неделе; яичник гормонально молчит.[115] Наконец, на 12 неделе мужской фенотип будет завершен; женское завершение происходит немного позже мужского. Анатомические структуры включают как внутренние мочеполовые пути — Мюллеровы или Вольфовы протоки — так и наружные гениталии. Женские мюллеровы протоки становятся верхним отделом влагалища, маточными трубами и маткой.
Наружные гениталии имеют три общие структуры: генитальные складки, припухлости половых органов и генитальные бугорки. В зависимости от гормонов, выделяемых гонадами, будет определяться структура.У мужчин половые складки удлиняются и сливаются, образуя стержень полового члена и уретру; половой бугорок становится головкой полового члена, а припухлости половых органов — мошонкой. И наоборот, у женщин складки половых органов становятся малыми половыми губами, припухлости половых органов — большими половыми губами, а генитальный бугорок — клитором. [116] [117] При аномальном развитии, когда гонады отсутствуют, фенотипическое развитие будет женским. Это говорит о том, что развитие плода по умолчанию будет женским, если на него не влияют андрогены.Неизвестно, зависит ли женское развитие от гормонов, поскольку беременность происходит в женском организме. На сегодняшний день не существует метода выделения гормонов внутри плода, чтобы определить, является ли их роль решающей для женского развития.
Менструальный цикл делится на две фазы, фолликулярную и лютеиновую, в зависимости от эндокринных гормонов, которые управляют циклом.
- Фолликулярная фаза — Фолликулярная фаза начинается с началом менструации и заканчивается за день до выброса лютеинизирующего гормона (ЛГ).В начале фазы яичник имеет низкую гормональную активность, что приводит к низким уровням эстрадиола и прогестерона. Однако пульсация ЛГ увеличивается с одного раза в несколько часов в конце лютеиновой фазы до одного раза каждые 90 минут. В средней фолликулярной фазе повышается уровень фолликулостимулирующего гормона (ФСГ), стимулируя фолликулогенез, и повышается уровень эстрадиола. ФСГ продолжает повышать уровень эстрадиола, стимулируя ароматазу для продолжения развития фолликулов. Повышение уровня эстрадиола в конечном итоге приводит к отрицательной обратной связи как для ЛГ, так и для ФСГ.На поздних этапах фолликулярной фазы уровни ФСГ и ЛГ остаются на низком уровне, но ФСГ действует на рецепторы ЛГ в яичниках, что приводит к секреции внутриутробных факторов роста. [118] [119]
- Лютеиновая фаза — Из фолликулярной в лютеиновую фазу эстрадиол продолжает расти, достигая пика за день до овуляции. В это время происходит уникальный эндокринный феномен — переключение с отрицательной обратной связи на положительную, что приводит к всплеску в середине цикла. Наблюдается 10-кратное повышение уровня ЛГ и меньший выброс ФСГ.Всплеск ЛГ не может быть смоделирован у женщин путем введения высоких уровней эстрогена и прогестерона, что указывает на участие других факторов. Примерно через 36 часов после выброса ЛГ фолликул высвобождает ооцит, и он проходит через маточную трубу в полость матки. Прогестерон начинает повышаться из-за секреции желтого тела. Прогестерон повышает температуру тела, расслабляет гладкие мышцы матки и предотвращает гиперплазию эндометрия. Проще говоря, эстроген стимулирует разрастание эндометрия при подготовке к имплантации, а прогестерон поддерживает эндометрий как подходящую среду для оплодотворения и имплантации.В конце лютеиновой фазы, если ооцит не подвергается оплодотворению, уровень ЛГ будет снижаться, а уровень прогестерона и эстрогена снизится, что приведет к отслаиванию внешнего слоя эндометрия, что приведет к менструации. Если ооцит оплодотворяется, он имплантируется в эндометрий. Эмбрион начнет секретировать хорионический гонадотропин человека (ХГЧ), который поддерживает уровень желтого тела и прогестерона. [120] [121] [122]
У женщин ограниченное количество циклов овуляции, прежде чем наступит менопауза, что вызвано уменьшением количества фолликулов яичников.Менопауза определяется как аменорея в течение 12 месяцев и обычно происходит в возрасте около 50 лет. Отсутствие фолликулов яичников приводит к снижению эстрогена — это состояние отмечается чрезвычайно высоким уровнем ФСГ. Это происходит из-за потери петли отрицательной обратной связи, потому что эстроген больше не присутствует, чтобы ингибировать ФСГ. [123] Эстроген важен для развития вторичных половых признаков, а также репродуктивного цикла. Действие эстрогена облегчается рецепторами эстрогена (ER).Есть две молекулы ER, ER-альфа и ER-бета. [124]
Когда эстроген проникает в клетку и попадает в ядро, он связывает ER и в конечном итоге модулирует скорость транскрипции генов, реагирующих на эстроген. У женщин, если эстроген отсутствует и способен должным образом связывать ER, будет отсутствие полового развития, задержка закрытия эпифиза, низкая плотность костной ткани и бесплодие. [125] [126]
Другие проблемы со здоровьем имеют последствия с низкой функцией эстрогена, такие как сердечно-сосудистая реакция, инсулинорезистентность и ожирение; однако необходимы дополнительные исследования.У женщин вторичные половые признаки развиваются через стимуляцию ER, которые вызывают активацию генов, что приводит к изменению габитуса тела. Например, связывание ER-альфа в молочной железе стимулирует образование почек. И прогестерон, и эстроген необходимы для нормального образования протоков молочной железы посредством стимуляции ER и рецепторов прогестерона (PR). Скорость пролиферации клеток в дольчатых структурах груди прямо пропорциональна уровню PR и ER в ткани.
Что касается фертильности, то и самки, и самцы для правильного воспроизводства полагаются на эстроген и его эффекты. Подобно самцам, мыши с дефицитом ER-альфа или ER-альфа и ER-бета будут бесплодны, в то время как мыши с дефицитом ER-бета будут субфертильными. Кроме того, мыши, у которых отсутствует ароматаза, являются ановуляторными и, следовательно, бесплодными. Тестостерон также играет важную роль в развитии женщин, особенно в мышцах, общем росте, репродуктивной ткани и психологическом поведении. Известно, что надфизиологические или субфизиологические уровни приводят к отклонению от типичных женских черт; однако степень влияния тестостерона на женщин до конца не изучена.[127] [128]
Половое развитие мужчин, экспрессия и активность гормонов
Как упоминалось ранее в разделе о женских особях, с эмбриологической точки зрения развитие по умолчанию будет женским. Самцы генетически относятся к XY — область на Y-хромосоме, критическая для развития яичек, — это ген SRY (определяющий пол участок Y-хромосомы). Это ген, заставляющий нейтральные гонады развиваться в семенники. Яички плода выделяют три гормона: антимюллеров гормон (АМГ), тестостерон и 5-альфа-дигидротестостерон (ДГТ).АМГ в первую очередь вызывает регрессию мюллерова протоков — тестостерон и ДГТ (андрогены) — это гормоны, на которых мы в первую очередь сосредоточимся. [129] [130]
- Возбудитель внутреннего урогенитального тракта первоначально создается хорионическим гонадотропином человека (ХГЧ), а позже развивается лютеинизирующим гормоном (ЛГ), секретируемым передней долей гипофиза плода. В зависимости от стадии развития ХГЧ или ЛГ вызывают секрецию тестостерона семенниками плода — это способствует дифференцировке вольфовых протоков в придатки яичка, семявыносящие протоки, семенные пузырьки и семявыбрасывающие протоки.[129]
- Наружный мочеполовой тракт управляется преобразованием тестостерона в ДГТ с помощью фермента 5-альфа-редуктазы. ДГТ регулирует внутриутробное развитие простаты и наружных половых органов, которые полностью формируются к двенадцатой неделе беременности. Изучая животных и людей с дефицитом 5-альфа-редуктазы, можно сделать вывод, что тестостерон отвечает за внутреннее половое развитие, в то время как ДГТ необходим для внешнего развития. Пациенты с 5-альфа-редуктазой будут иметь нормальную внутреннюю мужскую анатомию, но будут иметь неоднозначные внешние гениталии и не будут иметь вторичных мужских половых признаков.Это связано с нормальной функцией тестостерона, но с низким уровнем ДГТ. Андрогены, помимо полового развития, влияют на состав тела — была прямая корреляция веса при рождении со степенью андрогенизации, а не хромосомного пола. [129] [131]
Как обсуждалось ранее, ГнРГ вызывает регуляцию лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). Пульсирующая секреция ГнРГ из гипоталамуса вызывает аналогичное пульсирующее появление ЛГ и ФСГ — период полувыведения ЛГ значительно короче, чем ФСГ.Секреция гонадолиберина действует на гонадотропные клетки передней доли гипофиза, что приводит к высвобождению ФСГ и ЛГ. [132]
- ЛГ действует в первую очередь на клетки Лейдига, связываясь с рецепторами на клеточной мембране. Это приводит к стимуляции и высвобождению цАМФ, который активирует протеинкиназу А, в результате чего клетки Лейдига вырабатывают свой основной гормональный продукт — тестостерон. Выработка тестостерона в среднем составляет от 5 до 7 мг каждый день. [133]
- ФСГ связывается с клеточной мембраной клеток Сертоли, вызывая стимуляцию и высвобождение цАМФ, активируя протеинкиназу А.В результате внутриклеточной передачи сигналов увеличивается экспрессия генов и уровни белка для поддержки сперматогенеза. [134]
Это основные роли FSH и LH. В общем, это можно резюмировать: ЛГ действует на клетки Лейдига, секретируя тестостерон, а ФСГ действует на клетки Сертоли, способствуя сперматогенезу. Тестостерон, как и все стероидные гормоны, происходит из холестерина. Как только тестостерон продуцируется, он может далее метаболизироваться путем ароматизации в эстрадиол или восстанавливаться с помощью 5-альфа-редуктазы до ДГТ.Клетки с рецепторами андрогенов (AR) могут связываться и активироваться тестостероном или DHT, последний имеет гораздо более высокое сродство связывания. Независимо от того, какая молекула стимулирует AR, индуцируется конформационное изменение, позволяющее перемещаться в ядро. Внутри ядра гомодимер образуется в результате объединения со второй молекулой гормона-AR. Это создает активную молекулу, которая может связываться с элементами андрогенного ответа, вызывая повышающую / понижающую регуляцию генов транскрипции и, в конечном итоге, синтез белка.[135] Физиологическое действие тестостерона опосредуется самим гормоном и его активными метаболитами — ДГТ и эстрадиолом, что приводит к следующим основным функциям у мужчин [136] [137]:
Развитие мужского фенотипа в эмбриональном развитии (как обсуждалось выше)
Обратная связь по гонадотропной гипоталамо-гипофизарной оси
Провокация половой зрелости в период полового созревания и поддержание на протяжении всей взрослой жизни
Сексуальная функция (либидо, сексуальное удовлетворение и эректильная функция)
Мышечная и костная масса в период полового созревания и во взрослом возрасте
Поддержание более низкой жировой массы, инициирование и поддержание сперматогенеза
Поддержание уровней эритропоэза и гематокрита
Петля отрицательной обратной связи секреции ЛГ работает через два механизма.Эстрадиол подавляет GnRH путем подавления на уровне гипоталамуса, в то время как тестостерон и DHT подавляют непосредственно гипофиз. [138] Петля отрицательной обратной связи ФСГ опосредуется двумя молекулами: ингибином B (тестикулярный пептид) и эстрадиол-ингибином B, который является более важной регуляторной молекулой. [139] [140] [141]
Эстрадиол обычно вырабатывается у мужчин, когда тестостерон подвергается ароматизации, примерно 20% синтеза эстрадиола находится в яичках. Остальные 80% вырабатываются в жировой, кожной, мозговой и костной тканях, причем жировая ткань является наиболее заметным местом производства эстрадиола у мужчин.При дефиците эстрадиола у мужчин могут возникнуть следующие проблемы: увеличение жировых отложений, задержка закрытия эпифизов и снижение плотности костей. Крысы и мыши с дефицитом ER-альфа были изучены, и было показано, что они бесплодны. Семенники этих грызунов, у которых отсутствует ER-альфа, имеют расширенные семенные канальцы, не содержащие сперматозоидов. ER-alpha не нужен для функции сперматозоидов, но он необходим для созревания сперматозоидов. Было показано, что ER-альфа, ER-альфа и ER-бета или мыши с дефицитом ароматазы имеют ненормальное поведение при спаривании.Мыши с дефицитом только ER-beta будут нормально спариваться. Хотя это до конца не изучено, предполагается, что ER-альфа и эстрадиол необходимы для нормального спаривания и агрессивного поведения, наблюдаемого в мужском генотипе. [136] [137] [142]
Постановление об аппетите
Грелин — Классически считается «гормоном голода» из-за его стимуляции аппетита. Это пептид из 28 аминокислот, синтезируемый преимущественно в желудке, в частности, на дне желудка, где обнаруживаются клетки P / D1 кислородной железы.[143] Эти клетки бывают двух типов. Открытый тип имеет выход в просвет желудка и секретируется непосредственно в желудок для смешивания с желудочным содержимым. Закрытый тип находится рядом с собственной пластинкой и секретируется непосредственно в сосудистую сеть. [144] Грелин также присутствует в поджелудочной железе, плаценте, почках и гипофизе, но в гораздо меньших количествах. [145] Рецепторы грелина (рецептор, усиливающий секрецию гормона роста [GHS-R]) имеют две формы: GHS-R1a и GHS-R1b. GHS-R1a обнаруживается как в центральной нервной системе, так и в периферических тканях и обеспечивает прием пищи и насыщение.GHS-R1b имеет более широкое распространение, но его функция неизвестна, поскольку он не связан с тем же комплексом G-белка, что и GHS-R1a. [146] [147] Уровень грелина повышается во время голодания, голодания и анорексии — всплески отмечаются и перед едой. Питательные вещества подавляют грелин, углеводы, обладающие наибольшим ингибирующим действием, за ними следуют белок и липиды. Снижение уровня грелина происходит через невагинальные сигналы желудка и кишечника. [148]
Грелин стимулирует в первую очередь секрецию GH и, возможно, сам GHRH, дополнительно стимулируя секрецию GH.Результатом является повышение аппетита и положительный энергетический баланс в дополнение к эффектам GH (см. Раздел GH для получения дополнительной информации). Грелин действует локально в желудке, усиливая сокращение желудка и усиливая его опорожнение. Известно, что GH влияет на формирование и массу костей, но интересно, что остеобласты экспрессируют GHS-R1a, что указывает на возможный прямой эффект. Дефекты GHS-R связаны с низким ростом, что еще больше влияет на формирование костей. [149] [150]
Было продемонстрировано, что грелин увеличивает частоту приема пищи, но не увеличивает ее размер.Грелин также играет регулирующую роль в долгосрочной массе тела. В нормальных диапазонах ИМТ уровни грелина находятся в пределах от 550 до 650 пг / мл. В то время как у людей с ожирением диапазон от 200 до 350 пг / мл указывает на то, что грелин имеет обратную связь с ИМТ. [151] [152] [153] Уровни грелина наиболее высоки при голодании, анорексии и кахектике, где в среднем уровни превышают 1000 пг / мл. [154] Как видно на примере пациентов с ожирением, снижение уровня грелина коррелирует с гастритом (независимо от наличия Helicobacter pylori ).[155]
Лептин — И наоборот, лептин классически считается «гормоном сытости» из-за его подавления аппетита. Это белок из 167 аминокислот, продуцируемый геном ob и экспрессирующийся в основном в адипоцитах. [156] Он опосредует свои действия путем связывания рецепторов лептина (LEPR), из которых существуют шесть изоформ LEPR-a, с LEPR-f. Самая длинная форма — LEPR-b, обнаруживается во многих органах, но, что важно, она обнаруживается в головном мозге, особенно в ядрах гипоталамуса и ствола мозга.Мутации в этой изоформе приводят к тяжелому ожирению. [157] [158]
Было показано, что люди с нормальным ИМТ снижают потребление пищи при повышении уровня лептина. У пациентов с ожирением лептиновый ответ притупляется даже при введении экзогенного лептина на супрафизиологическом уровне. [159] [160] [161] Процент жира в организме напрямую связан с производством лептина и его кровообращением. [158] Переедание увеличивает уровень лептина примерно на 40% всего за 12 часов. Для сравнения, голодание приводит к снижению уровня лептина на 60-70% за 48 часов и может достигать 80% за 72 часа.[162] [163] При регулярном приеме пищи лептин взаимодействует с жировой тканью, и, исходя из процентного содержания жировой ткани в организме, адипоциты соответственно будут секретировать лептин. На лептин влияет пол, поскольку гормоны влияют на скорость его секреции. У женщин эстроген увеличивает уровень лептина, и что интересно, плацента и грудное молоко являются источниками лептина. У мужчин андрогены снижают уровень лептина в сыворотке [164] [165]. Также существует связь между питанием и иммунной функцией, опосредованная лептином.У субъектов с низким уровнем лептина (что наблюдается при длительном голодании или кахексии) имеется дисбаланс Th2 / Th3, низкое количество CD4 и сниженная продукция Т-клеток. [156] [166] Наконец, лептин оказывает как прямое, так и косвенное воздействие на кости. Однако исследования показали как положительную, так и отрицательную корреляцию между концентрацией лептина и плотностью костей. В настоящее время неясно, какое влияние лептин оказывает на кости, и это область продолжающихся исследований. [167] [168]
Характеристики гормонов | SEER Training
Химическая природа гормонов
По химическому составу гормоны можно разделить на белки и стероиды.Все гормоны в организме человека, кроме половых гормонов и гормонов коры надпочечников, являются белками или производными белков.
Механизм гормона
Действие Гормоны разносятся кровью по всему телу, но влияют только на определенные клетки. Конкретные клетки, которые реагируют на данный гормон, имеют рецепторные участки для этого гормона. Это своего рода замковый механизм. Если ключ подходит к замку, то дверь откроется. Если гормон подходит к участку рецептора, то будет эффект.Если гормон и рецепторный участок не совпадают, то реакции нет. Все клетки, у которых есть рецепторы для данного гормона, составляют ткань-мишень для этого гормона. В некоторых случаях ткань-мишень локализуется в отдельной железе или органе. В других случаях ткань-мишень является диффузной и разбросанной по всему телу, так что поражаются многие области. Гормоны оказывают свое характерное воздействие на клетки-мишени, изменяя клеточную активность.Белковые гормоны реагируют с рецепторами на поверхности клетки, и последовательность событий, приводящих к действию гормонов, относительно быстра.Стероидные гормоны обычно реагируют с рецепторными участками внутри клетки. Поскольку этот метод действия на самом деле включает синтез белков, он относительно медленный.
Контроль за действием гормонов
Гормоны — очень сильнодействующие вещества, а это означает, что очень небольшое количество гормона может оказывать сильное влияние на метаболические процессы. Из-за их активности секреция гормонов должна регулироваться в очень узких пределах, чтобы поддерживать гомеостаз в организме.
Многие гормоны контролируются той или иной формой механизма отрицательной обратной связи.В системе этого типа железа чувствительна к концентрации вещества, которое она регулирует. Система отрицательной обратной связи вызывает обратное увеличение и уменьшение состояния организма, чтобы поддерживать состояние стабильности или гомеостаза. Некоторые эндокринные железы выделяют гормоны в ответ на другие гормоны. Гормоны, вызывающие секрецию других гормонов, называются тропическими гормонами. Гормон из железы A заставляет железу B выделять свой гормон. Третий метод регулирования секреции гормонов — прямая нервная стимуляция.Нервный раздражитель заставляет железу А выделять свой гормон.
химических классов гормонов
Гормоны — это химические посредники, выделяемые эндокринными железами без протоков непосредственно в кровоток. Гормоны имеют различные структуры, которые иногда могут быть воспроизведены синтетически, чтобы обеспечить заместительную гормональную терапию у людей с определенными типами дефицита гормонов. К основным классам гормонов относятся:
Моноамины
Моноамины — это гормоны, полученные из ароматических аминокислот, таких как фенилалин, тирозин и триптофан, и участвующие в нейротрансмиссии.Примеры включают катехоламины, такие как адреналин, норадреналин и дофамин, и триптамины серотонин и мелатонин.
Пептидные гормоны
Пептидные гормоны — это белки, состоящие из аминокислотных цепей. Одним из примеров небольшого пептида является рилизинг-гормон тиреотропина (TRH), секретируемый гипоталамусом для стимуляции высвобождения тиреотропного гормона (TSH) передней долей гипофиза. В свою очередь, ТТГ стимулирует выработку тироксина и пролактина щитовидной железой.
Другой пример — вазопрессин, секретируемый задней долей гипофиза. Это регулирует солевой и водный баланс и, следовательно, уровень удержания воды в организме, среди других функций. Более длинные пептидные цепи включают инсулин и гормон роста.
Инсулин секретируется бета-клетками поджелудочной железы и регулирует метаболизм глюкозы. Гормон роста регулирует рост и развитие.
Пептидные гормоны, которые имеют ковалентно присоединенный углеводный фрагмент, называются гликопротеинами.Примеры гликопротеинов включают лютеинизирующий гормон (ЛГ) и фолликулостимулирующий гормон (ФСГ). ЛГ и ФСГ играют важную роль в регуляции репродуктивной системы как у мужчин, так и у женщин.
Липидные и фосфолипидные гормоны
Это гормоны, полученные из жиров или липидов, таких как линолевая кислота, арахидоновая кислота и фосфолипиды. Основным классом гормонов липидного происхождения являются стероиды, полученные из холестерина и эйкозаноидов. Стероидные гормоны включают тестостерон, эстроген и кортизол.Тестостерон и эстроген — важные регуляторы репродуктивной функции, секретируемые как яичками, так и яичниками.
Кортизол — это гормон, вырабатываемый надпочечниками в ответ на стресс или снижение уровня глюкокортикоидов в крови, и участвует в стимуляции синтеза глюкозы, а также в антистрессовых и противовоспалительных процессах.
Дополнительная литература
гормонов | ProSpec
О гормонах:
Слово «гормон приходит» означает «подстегивать», что отражает то, как гормоны действуют как катализаторы других химических изменений на клеточном уровне, необходимых для роста, развития и энергии.
Гормоны — это химические посредники, которые переносят и передают сигналы в кровотоке от одной клетки или железы к другим тканям и органам для поддержания химических уровней в кровотоке, которые обеспечивают гомеостаз. Все клеточные организмы производят гормоны.
Гормоны также регулируют функцию своих клеток-мишеней, которые экспрессируют рецептор гормона. Действие гормонов определяется многочисленными факторами, такими как характер их секреции и реакция принимающей ткани (реакция передачи сигнала).
Хотя небольшое количество гормонов циркулирует в кровотоке в растворенном виде, большинство из них переносятся кровью в связке с белками плазмы. Например, стероидные гормоны, которые являются высокогидрофобными, транспортируются связанными с белками плазмы.
Примером антагонистических пар гормонов является инсулин, который вызывает снижение уровня глюкозы при его повышении, а глюкагон вызывает повышение уровня сахара в крови при его падении.
Есть два основных класса гормонов 1. Белки, пептиды и модифицированные аминокислоты 2.Стероиды. В общем, стероиды — это половые гормоны, связанные с половым созреванием и фертильностью. Стероиды производятся из холестерина через плаценту, наши надпочечники или гонады (яички или яичники). Пептиды регулируют такие функции, как сон и концентрацию сахара. Они состоят из длинных цепочек аминокислот, поэтому иногда их называют «белковыми» гормонами. Например, гормон роста помогает нам сжигать жир и наращивать мышцы. Другой пептидный гормон, инсулин, запускает процесс преобразования сахара в клеточную энергию.
Гормоны прекрасно и эффективно управляют гомеостазом благодаря циклам отрицательной обратной связи. Наша цель — поддерживать концентрацию определенного химического вещества, такого как тестостерон, на постоянном уровне в течение определенного периода времени, как работает термостат. При использовании отрицательной обратной связи изменение условий вызывает ответ, который возвращает условия в их исходное состояние. Когда температура в комнате падает, термостат срабатывает, включая нагрев. В комнате возвращается идеальная температура, и обогреватель выключается, поддерживая относительно постоянные условия.
Эндокринные гормоны секретируются в кровь и переносятся кровью и тканевыми жидкостями к клеткам, на которые они действуют, в то время как экзокринные гормоны выделяются в проток, а затем в кровоток. Экзокринные гормоны передаются от клетки к клетке путем диффузии (паракринная передача сигналов).
Гормоны действуют медленно, с течением времени и влияют на множество различных процессов в организме, таких как рост и развитие, метаболизм, сексуальная функция, репродуктивное настроение,
Эндокринные железы и т. Д. Основными эндокринными железами являются гипофиз, шишковидная железа, вилочковая железа, щитовидная железа, надпочечники и поджелудочная железа.Кроме того, у мужчин вырабатываются гормоны в яичках, а у женщин — в яичниках.
Гормоны оказывают сильное воздействие, и требуется несколько пикограмм, чтобы вызвать большие изменения в клетках или даже во всем теле. Вот почему слишком много или слишком мало определенного гормона может вызвать серьезные проблемы и осложнения. В лабораторных экспериментах можно измерить уровень гормонов в крови, моче или слюне.
Уровни гормонов, циркулирующих в кровотоке, контролируются гомеостатическим механизмом, например, 1 гормон стимулирует выработку 2 nd , 2 nd подавляет выработку 1 st .
Например, ФСГ стимулирует высвобождение эстрогенов из фолликула яичника, но при высоких уровнях эстрогена он подавляет дальнейшее производство ФСГ.
1 основной класс гормонов — это белки, пептиды и модифицированные аминокислоты, которые представляют собой гидрофильные (и в основном большие) молекулы гормонов, которые связываются с рецепторами на поверхности «клеток-мишеней», клетки способны реагировать на присутствие гормона. Эти рецепторы представляют собой трансмембранные белки. Связывание гормона с его рецептором инициирует последовательность внутриклеточных сигналов, которая изменяет поведение клетки (открытие или закрытие мембранных каналов) или стимулирует (или подавляет) экспрессию генов в ядре путем включения (или выключения) промоторов и энхансеры генов.
Гормон связывается с участком внеклеточной части рецептора, который действует как трансмембранный белок, проходящий через плазматическую мембрану x7, при этом N-конец открыт снаружи клетки, а С-конец выступает в цитоплазму.
Как только гормон связывается с рецептором, он активирует G-белок, связанный с С-концом цитоплазмы, который инициирует выработку второго мессенджера, такого как циклический АМФ (цАМФ), который продуцируется аденилатциклазой из АТФ и инозитолом 1,4, 5-трифосфат (IP3)
Посланник 2 и инициирует серию внутриклеточных событий, таких как фосфорилирование и активация ферментов, высвобождение Са2 + в цитозоль из запасов внутри эндоплазматического ретикулума.
цАМФ активирует фактор транскрипции CREB (белок, связывающий элемент ответа цАМФ), который включает транскрипцию гена. Клетка начинает продуцировать соответствующие генные продукты в ответ на гормональный сигнал, полученный с ее поверхности.
Стероидные гормоны представляют собой гидрофобные белки / пептиды и свободно диффундируют в клетки. Однако их «клетки-мишени» содержат цитоплазматические и / или ядерные белки, которые служат рецепторами гормона. Гормон связывается с рецептором, а комплекс связывается с элементами ответа на гормон — участками ДНК в промоторах генов, реагирующих на гормон.Комплекс гормон / рецептор действует как фактор транскрипции, «включающий» (или «выключающий») гены-мишени. Гормоны свободно циркулируют в кровотоке, ожидая, пока их распознает клетка-мишень, по назначению. У клетки-мишени есть рецептор, который может быть активирован только гормоном определенного типа. После активации клетка знает, что в ее стенках запускается определенная функция. Могут активироваться гены или возобновиться производство энергии. Как особые категории, аутокринные гормоны действуют на клетки секреторной железы, в то время как паракринные гормоны действуют на соседние, но не связанные клетки.
Секреция гормона увеличивается (или уменьшается) тем же веществом, уровень которого снижается (или повышается) гормоном. Повышающийся уровень Ca2 + в кровотоке подавляет выработку ПТГ, но низкий уровень Ca2 + стимулирует его.
.

