— этапы катаболизма — Биохимия
Метаболизм представляет собой высоко координированную и целенаправленную клеточную активность, обеспеченную участием многих взаимосвязанных ферментативных систем, и включает два неразрывных процесса анаболизм и катаболизм.
Он выполняет три специализированные функции:
- Энергетическая – снабжение клетки химической энергией,
- Пластическая – синтез макромолекул как строительных блоков,
- Специфическая – синтез и распад биомолекул, необходимых для выполнения специфических клеточных функций.
Анаболизм
Анаболизм – это биосинтез белков, полисахаридов, липидов, нуклеиновых кислот и других макромолекул из малых молекул-предшественников. Поскольку он сопровождается усложнением структуры, то требует затрат энергии. Источником такой энергии является энергия АТФ.
Цикл НАДФ-НАДФН
Также для биосинтеза некоторых веществ (жирные кислоты, холестерол) требуются богатые энергией атомы водорода – их источником является
Катаболизм
Катаболизм – расщепление и окисление сложных органических молекул до более простых конечных продуктов. Оно сопровождается высвобождением энергии, заключенной в сложной структуре веществ. Большая часть высвобожденной энергии рассеивается в виде тепла. Меньшая часть этой энергии «перехватывается» коферментами окислительных реакций НАД и ФАД, некоторая часть сразу используется для синтеза АТФ.
Атомы водорода, высвобождаемые в реакциях окисления веществ, в основном используются клеткой по двум направлениям:
- на анаболические реакции в составе НАДФН (например, синтез жирных кислот и холестерина),
- на образование АТФ в митохондриях при окислении НАДН и ФАДН2.
Первый этап
Происходит в кишечнике (переваривание пищи) или в лизосомах (самообновление клеток) при расщеплении уже ненужных или лишних молекул. При этом освобождается около 1% энергии, заключенной в молекуле. Она рассеивается в виде тепла.
Второй этап
Вещества, образованные при внутриклеточном гидролизе или проникающие в клетку из крови, на втором этапе обычно превращаются
Локализация второго этапа –
Схема общих и специфичных путей катаболизма
(более подробная схема представлена здесь)
Под специфичными путями катаболизма понимают реакции, осуществляемые специфичными ферментами в специфичных, для разных классов веществ, реакциях 1 и 2 этапов. После того, как эти процессы закончатся, образуются пируват и ацетил-SКоА (в основном) и начинаются общие пути превращений. Подразумевается, что независимо от источника происхождения пирувата и ацетил-SKoA (из аминокислот, жирных кислот или моносахаридов) они попадают в общий путь катаболизма – 3 этап биологического окисления.
Третий этап
Все реакции этого этапа идут в митохондриях. Ацетил-SКоА (и кетокислоты) включается в реакции цикла трикарбоновых кислот, где углероды веществ окисляются до углекислого газа. Выделенные атомы водорода соединяются с НАД и ФАД, восстанавливают их и после этого НАДН и ФАДН2 переносят водород в цепь ферментов дыхательной цепи, расположенную на внутренней мембране митохондрий. Сюда же отдают свои атомы водорода молекулы НАДН и ФАДН2, образованные на втором этапе (гликолиз, окисление жирных кислот и аминокислот). В третьем этапе выделяется до 70% всей энергии вещества. Из этого количества усваивается почти две трети (66%), что составляет около 46% от общей. Таким образом, из 100% энергии окисляемой молекулы клетка запасает больше половины – 59%.
Соотношение выделенной и запасенной энергии
при биологическом окислении
На внутренней мембране митохондрий в результате процесса под названием «окислительное фосфорилирование» образуется вода и главный продукт биологического окисления – АТФ.
Роль АТФ
Энергия, высвобождаемая в реакциях катаболизма, запасается в виде связей, называемых макроэргическими. Основной и универсальной молекулой, которая запасает энергию и при необходимости отдает ее, является АТФ.
Все молекулы АТФ в клетке непрерывно участвуют в каких-либо реакциях, постоянно расщепляются до АДФ и вновь регенерируют.
Существует три основных способа использования АТФ:
- биосинтез веществ,
- транспорт веществ через мембраны,
- изменение формы клетки и ее движение.
Эти процессы вкупе с процессом образования АТФ получили название АТФ-цикл:
Кругооборот АТФ в жизни клетки
biokhimija.ru
Болезни и изменения клеточного метаболизма
Нейродегенеративные и онкологические болезни — самые распространенные возрастные патологии после болезней сердца и сосудов. Как показывают исследования, эти патологии тесным образом связаны с энергетическим обменом и митохондриальной дисфункцией. Детальное и масштабное изучение изменений клеточного метаболизма при развитии этих патологий способствует разработке более совершенных диагностических инструментов, позволяющих обнаруживать заболевание на самой ранней его стадии.


Спецпроект о клеточном энергетическом метаболизме, работе митохондрий и АТФ, а также о заболеваниях, связанных с нарушениями функций клеточных «батареек».
Спонсор спецпроекта — «БиоХимМак» — поставщик научного и медицинского оборудования в лаборатории России и стран СНГ.
Наверное, у каждого, кто начинает знакомиться с удивительной организацией наших клеток, возникает чувство восхищения невероятной сложностью внутриклеточного мира. Каждую секунду в миллиардах наших клеток протекают сложные и строго скоординированные процессы. И одним из таких очень важных процессов является производство в митохондриях главной энергетической молекулы — аденозинтрифосфата, или АТФ. Сегодня уже хорошо известно, что работа митохондрий очень тесно связана со здоровьем и продолжительностью жизни [1]. Митохондрии производят энергию для поддержания жизни, но при этом они же служат основными источниками активных форм кислорода, избыток которых для клеток губителен.
Энергетический обмен
Любой живой организм находится в постоянной связи с окружающей средой, непрерывно обмениваясь с ней веществом. В этом процессе можно выделить три этапа:
- поступление веществ;
- метаболизм;
- выделение конечных продуктов.
Внутриклеточный метаболизм, в свою очередь, включает в себя два типа реакций: катаболизм и анаболизм.
Катаболизм — это процесс расщепления и окисления органических молекул, приводящий к образованию тепла и энергетических молекул, АТФ. Именно за счет постоянного производства—расщепления последних съеденные нами калории направляются «по адресу»: гидролиз двух высокоэнергетических (макроэргических) связей в молекулах АТФ обеспечивает энергией всевозможные синтетические и транспортные процессы в клетках.
На первом этапе катаболизма под воздействием пищеварительных ферментов сложные органические соединения (белки, полисахариды, жиры) распадаются на более простые — аминокислоты, моносахариды, жирные кислоты и глицерин, — которые клетка использует для реакций анаболизма (пластического обмена) и получения энергии. Аминокислоты идут на синтез белков. Жирные кислоты выполняют энергетическую функцию, входят в состав клеточных мембран и служат субстратом для синтеза эйкозаноидов
На втором этапе происходит гликолиз — расщепление молекул глюкозы (рис. 1) до пировиноградной кислоты (ПВК). Дальнейший ход реакций зависит от присутствия или отсутствия кислорода в клетке. Если кислорода нет (
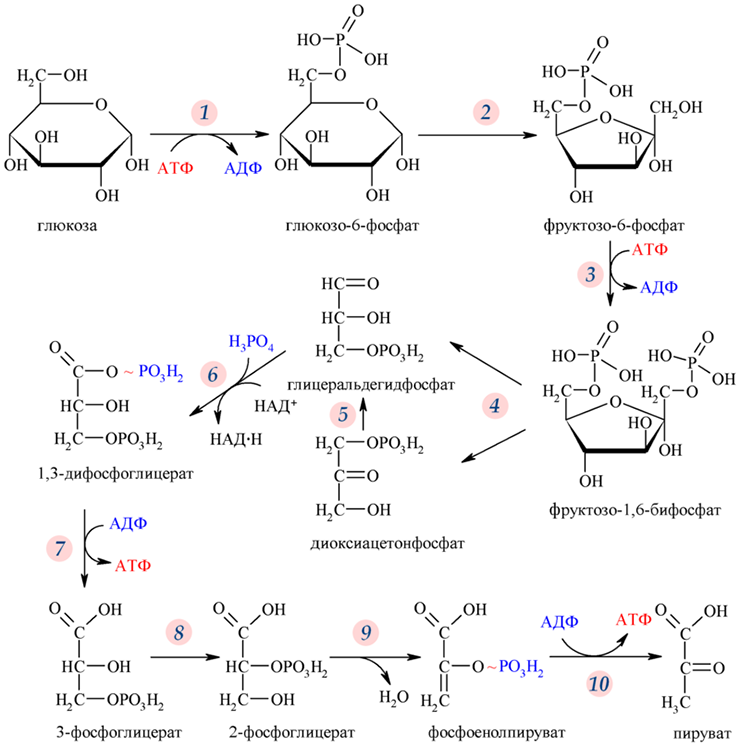
Рисунок 1. Реакции гликолиза. На 10 этапах гликолиза (пяти подготовительных и пяти этапах синтеза АТФ) из шестиуглеродной молекулы глюкозы образуются две трехуглеродные молекулы пировиноградной кислоты. Полученная от расщепления глюкозы энергия запасается в «энергетической валюте» клетки — двух молекулах АТФ и двух молекулах НАДФ.
Если же кислород в клетке есть, ПВК будет расщепляться на углекислый газ и воду и тоже высвобождать заключенную в углеводной молекуле энергию. Этот процесс называется аэробным клеточным дыханием и проходит в специальных органеллах — митохондриях. Окисление в митохондриях дает гораздо больше энергии, чем гликолиз.
Митохондрии и производство АТФ
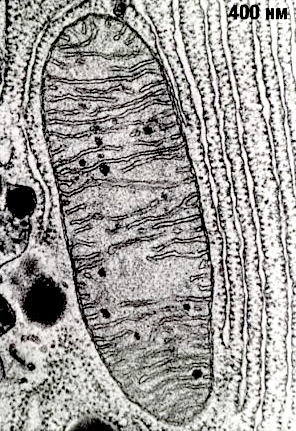
Рисунок 2. Митохондрия под электронным микроскопом.
Митохондрии — настоящее биологическое чудо, сотворенное эволюцией. Несмотря на очень маленький размер (в одной клетке может быть более 1000 митохондрий), эти органеллы поражают чрезвычайно сложной организацией (рис. 2). Они представляют собой вытянутые «пузырьки», окруженные двумя мембранами. Считается, что митохондрии сформировались в результате поглощения археями-фагоцитами пурпурных фотосинтезирующих бактерий, которые, приспосабливаясь к избытку кислорода, освоили аэробное дыхание [3], [4]. Мембраны митохондрий состоят из липидов и гидрофобных, нерастворимых в воде белков. (Здесь мы так подробно описываем строение митохондрий не случайно, а для того чтобы потом было понятно, как их нормальная работа и дисфункция влияют на здоровье.)
Строение мембран очень важно для процесса дыхания. Внешняя мембрана митохондрий — гладкая, а внутренняя — многократно складчатая. Эти складки (или кристы) позволяют увеличить рабочую площадь мембраны, что необходимо для размещения там всего комплекса белков, осуществляющих дыхание. Вначале окисляются углеродные атомы углеводов, жирных кислот и аминокислот до СО2 (гликолиз, цикл Кребса и β-окисление жирных кислот), а полученные таким образом электроны используются для образования НАДФ. Далее НАДФ окисляется молекулярным кислородом с образованием воды. НАДФ-оксидазная реакция сопровождается выделением очень большого количества свободной энергии (около 1,1 эВ при переносе одного электрона с НАДФ на кислород), которая может запасаться дыхательной цепью в виде трансмембранной разности электрохимических потенциалов ионов H+ (протонов).
Работа же дыхательных белков-ферментов похожа на работу насосов: передавая электроны друг другу, они перекачивают протоны в межмембранное пространство (см. видео 1). В результате внутренняя мембрана митохондрии заряжается подобно конденсатору. Создаются потенциалы: электрический (положительные заряды — снаружи митохондриальной мембраны, отрицательные — внутри органеллы) и химический (возникает разница концентраций протонов: внутри митохондрии их меньше, снаружи — больше). Известно, что электрический потенциал на мембране митохондрий, которая служит хорошим диэлектриком, достигает 200 мВ при толщине мембраны всего 10 нм [5]. Для сравнения: потенциал действия на мембранах нервных клеток при передаче сигнала достигает всего 30 мВ.
Видео 1. Как работает митохондрия
Накопившись в межмембранном пространстве, протоны, подобно электрическому току, устремляются назад, в митохондрию — туда, где их концентрация ниже. Однако они могут проходить только по специальным каналам АТФ-синтазы, встроенной во внутреннюю мембрану: протонный канал (ротор) этого фермента закреплен в мембране, а каталитический комплекс торчит внутрь митохондрии, в матрикс (рис. 3). Поток протонов раскручивает ротор, как река водяную мельницу. В результате ротор вращается с невероятной скоростью — 300 оборотов в секунду (см. видео 2)! И именно это вращение приводит к образованию высокоэнергетической молекулы — АТФ [6]. Подсчитано, что в сутки в организме взрослого человека синтезируется и расходуется около 40 кг АТФ, при этом жизнь каждой молекулы очень коротка.
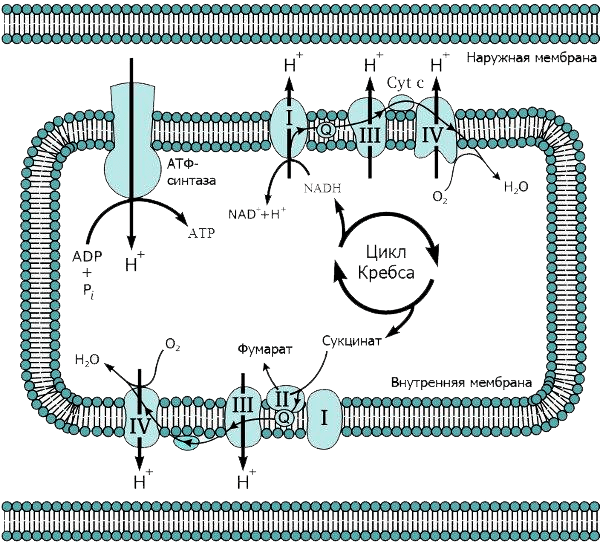
Рисунок 3. Схема дыхательной цепи митохондрий.
Видео 2. Работа АТФ-синтазы в мембране митохондрии
Всё вышесказанное имеет самое непосредственное отношение к старению. Дело в том, что в процессе дыхания ферменты работают не совсем «чисто», и в результате образуются побочные продукты — активные формы кислорода (АФК). Пока человек молод и здоров, образующиеся в митохондриях АФК не представляют для него ощутимой угрозы, так как легко нейтрализуются организмом. Но когда человек стареет, ведет нездоровый образ жизни или имеет генетическую предрасположенность к определенным болезням, его защитные системы дают сбой, рушась одна за другой.
Жирные кислоты и дисфункция митохондрий
То, что старение и возрастные патологии сопровождаются дисфункцией митохондрий, которые начинают производить меньше АТФ и хуже обновляться, уже ни у кого не вызывает сомнения. Выяснилось также, что дисфункция митохондрий и старение тесным образом связаны с повышением уровня свободных жирных кислот в крови [7], чему сильно способствуют малоподвижность и нерациональное питание. Жирные кислоты, попадая в клетку, способны напрямую снижать синтез АТФ, разобщая окисление и фосфорилирование. Этот связанный с терморегуляцией организма феномен был открыт еще шесть десятилетий назад академиком Скулачевым и его коллегами [8]. Снижение синтеза АТФ, в свою очередь, запускает сразу несколько негативных цепных реакций, связанных с возрастными болезнями и старением в целом.
И вот что происходит. Повышение уровня свободных жирных кислот в организме приводит к резистентности к инсулину: инсулинзависимые клетки перестанут реагировать на этот гормон. В результате нарушается усвоение глюкозы и жирных кислот, ухудшается окисление последних. Дело в том, что характерный для состояния инсулинорезистентности высокий уровень инсулина активирует целый каскад реакций, который блокирует работу фермента карнитинпальмитоилтрансферазы I (СРT1), участвующего в переносе жирных кислот внутрь митохондрий [9]. Из-за этого ухудшается синтез АТФ, а жирные кислоты накапливаются в цитоплазме клеток, вызывая эффект липотоксичности. Кроме резистентности к инсулину, избыток жирных кислот в организме вызывает резистентность к еще одному «пищевому» гормону — лептину. А из-за этого страдает функция одного из главных участников биогенеза (обновления) митохондрий — коактиватора рецептора гамма, активируемого пролифераторами пероксисом (PGC-1α). В итоге митохондрии производят меньше АТФ, стареют, погибают и провоцируют гибель клеток путем апоптоза [10].
Ну и наконец, избыток жирных кислот вызывает стресс эндоплазматического ретикулума (ЭПР) — внутриклеточного органоида, участвующего в синтезе белков и множестве других процессов. При стрессе ЭПР в цитоплазму высвобождаются ионы кальция, способные вызывать дисфункцию и гибель митохондрий [11]. Ионы кальция могут накапливаться в клетке и по другой причине — из-за ухудшения работы ионных насосов, откачивающих кальций из клетки. А причиной этому служит нарушение работы митохондрий, сопровождающееся снижением синтеза АТФ, без которого отказываются работать ионные насосы. В итоге формируется порочный круг: снижение выработки АТФ приводит к дисфункции митохондрий, что еще больше снижает выработку АТФ, и т.д.
Жирные кислоты, церамиды и повреждения нейронов
Как выяснилось, избыток жирных кислот и дисфункция митохондрий напрямую связаны с возникновением возрастных нейродегенеративных патологий. Надо сказать, что клетки нервной системы — самые уязвимые для возрастного окислительного стресса и снижения синтеза АТФ. Такая исключительная чувствительность нейронов к дефициту энергии и повышению генерации АФК объясняется несколькими причинами.
Во-первых, нервная ткань в силу своей физиологии нуждается в наибольшем потреблении кислорода. Вследствие этого в митохондриях нейронов происходит интенсивный окислительный метаболизм, который и становится основной причиной повышенной генерации АФК.
Во-вторых, из-за того, что мембраны нейронов содержат много ненасыщенных жирных кислот, они легко подвергаются перекисному окислению липидов. Так как активность антиоксидантных систем в ткани головного мозга ниже, чем в других органах, а с возрастом сокращается и количество некоторых ферментов-антиоксидантов, становится понятным, почему клетки нервной системы наиболее чувствительны к окислительным повреждениям [12].
В настоящее время известно несколько факторов, повреждающих нейроны. Среди них — белки, образующие внутри- и внеклеточные агрегаты (β-амилоидный белок и другие), а также церамиды и липофусцин. На их количество влияет прежде всего избыток жирных кислот в организме. Отягчающим обстоятельством в этом случае выступает чрезмерное содержание насыщенных кислот (пальмитиновой и стеариновой) в пищевом рационе. Всё это вместе служит мощным стимулом развития разнообразных нейродегенеративных заболеваний, таких как болезнь Альцгеймера [13], [14].
Но каким же образом пальмитиновая кислота может способствовать нейродегенерации? Установлено, что из-за избытка этой кислоты накапливаются церамиды, которые участвуют в регуляции терминальной дифференцировки, пролиферации и апоптоза нейронов. Посредством нескольких химических реакций они воздействуют на регуляторы клеточного цикла, повышая концентрацию ингибиторов киназ p21/SDI1 и p27/KIP1. Таким образом церамиды останавливают клеточный цикл, что, в свою очередь, активирует главного «стража генома» — белок р53 — и «насылает» на клетку апоптоз [15]. Кроме этого, при деградации церамида образуется вещество сфингозин, обладающее цитотоксическим действием и способное вызывать как апоптоз, так и некроз клеток. Но и это еще не всё. Обнаружено, что накопление насыщенных жирных кислот (пальмитиновой и стеариновой) стимулирует специальные клетки головного мозга (астроглию) на эндогенный (внутренний) синтез церамидов. Эти произведенные церамиды запускают цепную реакцию следующего вида: церамиды → повышение секреции провоспалительных цитокинов и оксида азота → увеличение производства АФК и окислительный стресс → активация стресс-регулируемых киназ (CDK5 и GSK-3) в нейронах → образование β-амилоидного белка и гиперфосфорилирование τ-белка [16].
Нейродегенеративные патологии и дисфункция митохондрий
Сегодня важнейшими и самыми распространенными нейродегенеративными патологиями считают болезни Альцгеймера, Паркинсона, Хантингтона, а также боковой амиотрофический склероз. Их возникновение связывают со структурными изменениями различных белков, приводящими к образованию внутриклеточных агрегатов. К таким белкам относятся:
Болезнь Альцгеймера (БА) — тяжелое нейродегенеративное заболевание, для которого характерны синаптическая дисфункция и гибель нейронов, что сопровождается снижением когнитивных способностей: ухудшением памяти и мышления, постепенной потерей социальных и моторных навыков [17]. В зоне риска развития болезни находятся в основном пожилые люди. Лишь 1–2% людей в возрасте до 65 лет страдают БА. Согласно одной из гипотез развития БА — амилоидной, — болезнь возникает из-за накопления в головном мозге агрегатов β-амилоида. Этот пептид состоит из 39–43 аминокислотных остатков и является фрагментом крупного трансмембранного белка под названием предшественник бета-амилоида (amyloid precursor protein, APP). Находясь в избытке, молекулы β-амилоида начинают «склеиваться» и образовывать нерастворимые бляшки (рис. 4). Именно в таком состоянии белок нарушает работу нервных клеток и вызывает симптомы БА. У страдающих БА в пораженных участках мозга находят большое количество амилоидных бляшек и нейрофибриллярных клубков [18].
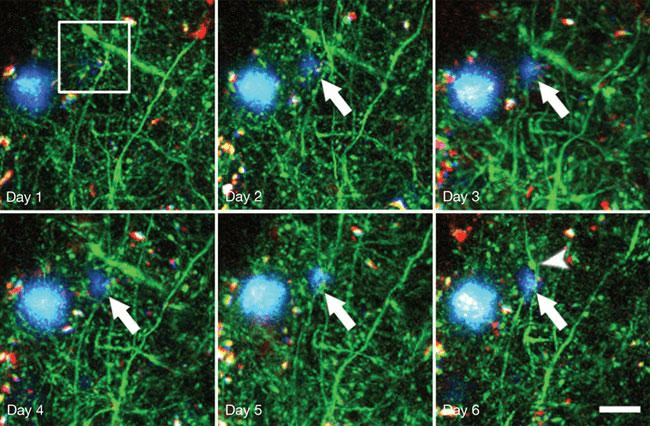
Рисунок 4. Образование амилоидной бляшки у генно-инженерных мышей (показано длинной стрелкой). На 6-й день уже видна дистрофия нейрона (короткая стрелка). Синим цветом обозначены отложения амилоида, зеленым — нейроны. Длина масштабной линейки — 20 мкм; снимки сделаны с помощью мультифотонного микроскопа.
Однако амилоидная гипотеза — не единственная, объясняющая возникновение БА. В 1993 году Аллен Роузес, профессор Университета Дьюка, предложил еще одну гипотезу возникновения БА — генетическую, связанную с геном APOE, кодирующим аполипопротеин Е (ApoE). Выяснилось, что наследование одного из вариантов гена APOE — APOE4 — в несколько раз повышает шансы заболеть БА. Всё больше исследователей склоняются к мысли, что β-амилоид излишне «демонизирован» и не является первопричиной развития БА. Неудавшаяся терапия, направленная на очистку клеток от β-амилоида, подтверждает, что с этой болезнью не всё до конца ясно [19].
Болезнь Паркинсона (БП) — еще одно тяжелое и довольно распространенное возрастное нейродегенеративное заболевание. У больных БП в нейронах черной субстанции накапливается α-синуклеин, который образует особые гранулы — тельца Леви. Надо сказать, что существует так называемая деменция с тельцами Леви, для которой характерно скопление многочисленных телец Леви в кортикальных и субкортикальных нейронах и развитие прогрессирующего когнитивного расстройства уже в первый год заболевания. Но пока не совсем ясно, считать ли эту деменцию формой БП или же правильнее ее рассматривать как отдельное заболевание. В случае БП скопления телец Леви приводят к дисфункции нейронов и их гибели, при этом характерно поражение областей мозга из состава так называемого нигростриарного дофаминового пути. Этот путь регулирует двигательную активность, снижая напряжение в мышцах. Вот почему, когда гибнут дофаминовые нейроны, у больных возникают соответствующие симптомы: нарастающее повышение мышечного тонуса и дрожание рук. Кроме нарушения моторных функций для БП характерны и другие симптомы, связанные с нарушением сна, депрессией, тревогой, ухудшением зрения и замедлением мышления [20].
Болезнь Хантингтона (БХ) — тоже не слишком редкое нейродегенеративное заболевание [21]. Как и в случае болезни Альцгеймера, для патогенеза БХ характерно образование токсичных белковых агрегатов с участием мутантных форм белков, которые синтезируются в нервной ткани. Но если к основному «виновнику» БА, β-амилоиду, у ученых есть вопросы, в случае с БХ сомнений гораздо меньше. Установлено, что именно генетические особенности — полиморфизмы определенных участков ДНК — приводят к появлению патологических форм белка хантингтина. Такой хантингтин способен к ассоциации с другими белками нервной ткани, в результате чего образуются нерастворимые токсичные агрегаты, повреждающие кору и полосатое тело головного мозга. Для БХ типичны всплески непроизвольной двигательной активности, эмоциональные расстройства и потеря памяти. В то же время нормальная физиологическая функция белка хантингтина в организме остается под вопросом. Предполагают, что он играет какую-то роль в эмбриогенезе [22].
Все три упомянутые патологии самым тесным образом связаны с дисфункцией митохондрий. Прежде всего, надо отметить, что ее развитие под действием дефектных белков, специфичных для нейропатологий, было установлено несколькими способами: in vitro (на клеточных линиях и внеклеточных системах) и in vivo (на трансгенных животных). Обнаружили и обратную связь: оказалось, что дисфункция митохондрий может стимулировать появление дефектных белков. Так, нарушение активности дыхательного комплекса I ведет к накоплению в нервных клетках гиперфосфорилированного τ-белка и α-синуклеина [23].
Со скоплением дефектных белков связали и уже упоминавшийся стресс эндоплазматического ретикулума. Один из таких белков, α-синуклеин, может снижать активность протеасом, что заканчивается стрессом ЭПР, увеличением производства АФК и инициацией апоптозных процессов. Это происходит потому, что из митохондрий высвобождается апоптозный фактор, цитохром С, который активирует «клеточных убийц» — каспазу-9 и каспазу-3 [24]. Как полагают, на начальных этапах нейродегенерации при БА накопление β-амилоида и гиперфосфорилирование τ-белка могут быть физиологическими механизмами защиты клетки от окислительного стресса, вызванного прогрессирующей митохондриальной дисфункцией. Однако при избыточном накоплении этих белков в клетке происходит сбой в работе митохондрий. Так, у пациентов с БА обнаружили, что β-амилоид накапливается в митохондриях и нарушает реакции гликолиза и цикла Кребса, активизирует продукцию АФК. Более того, β-амилоид способен напрямую подавлять синтез АТФ. Это возможно из-за структурного сходства белка с естественным ингибитором F(1)-субъединицы АТФ-синтазы митохондрий. Также β-амилоид может взаимодействовать с митохондриальной мембраной, формируя стабильные комплексы с двумя транслоказами, TOM40 и TIM23. Такие комплексы подавляют импорт в митохондрии белков, кодируемых ядерным геномом, — субъединиц IV и Vb цитохромоксидазы. На что органелла откликается увеличением производства агрессивного пероксида водорода.
Но и это еще не всё: белок — предшественник β-амилоида может формировать поры в мембранах митохондрий и других органелл, что нарушает ионный баланс в клетке и запускает ее апоптоз [25]. Также этот белок повышает активность фосфолипазы D, в результате изменяя фосфолипидный состав митохондриальных мембран, увеличивая концентрацию фосфатидилхолина, фосфатидилэтаноламина и фосфатидной кислоты и нарушая работу мембран. Известно, что β-амилоид может связывать гем, а это ведет к дефициту гема в клетке, из-за чего нарушается работа гем-содержащего IV комплекса электронтранспортной цепи митохондрий [26].
Но не только β-амилоид способен негативно влиять на митохондрии. В экспериментах с трансгенными грызунами, экспрессирующими ген хантингтина человека, обнаружили агрегацию этого белка в митохондриях с последующим развитием их дисфункции. Другой «зловредный» белок, α-синуклеин, накапливаясь во внутренней митохондриальной мембране, способен снижать активность дыхательного комплекса I. Как следствие, митохондрии увеличивают продукцию АФК [27]. Также обнаружено, что α-синуклеин, взаимодействуя с митохондриями, может стимулировать высвобождение из них цитохрома С, а значит, инициировать апоптоз.
В целом, можно сказать, что запуск апоптоза — характерный эффект белков, вызывающих нейродегенерацию. Они могут прямо или косвенно воздействовать на регуляторные белки, связанные с апоптозом: p53, Akt, Bad, Bax, Bcl-x(L) и кальцинейрин [28].
Также описано, что сверхсинтез белка — предшественника β-амилоида приводит к повреждению системы слияния—деления митохондрий. Негативно влияют на эту же систему и на утилизацию дефектных митохондрий аутофагосомами мутации гена паркина (PARK2), обнаруженные у больных БП. Дефектные формы τ-белка и хантингтина тоже мешают нормальной работе митохондрий, ухудшая тем самым энергообеспечение отростков нервных клеток и синаптическую передачу, вызывая дегенерацию синапсов [29].
Таким образом, белки, участвующие в развитии нейродегенеративных патологий, могут способствовать митохондриальной дисфункции посредством целого ряда механизмов. В свою очередь, уже возникшая дисфункция может усугублять патологические процессы, стимулируя появление дефектных белков и замыкая тем самым порочный круг развития болезни.
Эффект Варбурга
И напоследок стόит коснуться еще одного момента, связанного с патологиями и изменением клеточного метаболизма. В 1926 году немецкий биохимик Отто Варбург сравнил скорости образования молочной кислоты (лактата) в нормальных и опухолевых клетках. Оказалось, что опухолевые клетки потребляют очень много глюкозы, образуя при этом лактат. И делают это они гораздо быстрее, чем нормальные клетки: злокачественная ткань в эксперименте производила молочную кислоту в восемь раз активнее, чем это происходит в мышце, выполняющей физическую работу. Варбург установил, что раковые клетки используют гликолиз для получения энергии вне зависимости от доступности кислорода (рис. 5) [30]. В честь первооткрывателя этот феномен назвали эффектом Варбурга [2].
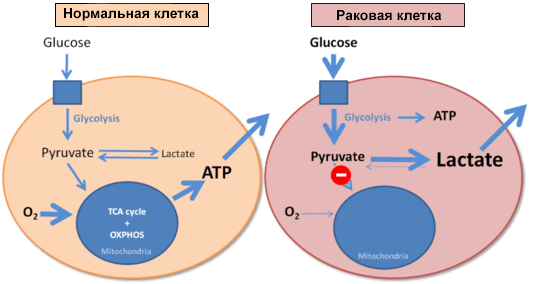
Рисунок 5. Энергообеспечение нормальной и раковой клеток. Синим квадратом обозначена поступающая в клетку глюкоза.
Обнаружив этот эффект, Варбург логично предположил, что его можно объяснить дисфункцией митохондрий в опухолевых клетках и нарушением окислительного фосфорилирования. Сегодня эта точка зрения ставится под сомнение, так как и в перерожденной ткани обнаруживают большое количество нормально работающих митохондрий. Около половины всей энергии опухолевые клетки получают из молекул АТФ, произведенных в митохондриях [31]. Эффект Варбурга проявляется в клетках уже в самом начале их трансформации в опухолевые. И это дает возможность проводить раннюю диагностику неопластических процессов: как только клетка начала расходовать глюкозу в повышенных масштабах, пора бить тревогу. Обнаружить эти процессы можно с помощью позитронно-эмиссионной томографии с использованием фторированного аналога глюкозы, 2-(18F)-2-дезокси-D-глюкозы.
Но зачем раковые клетки переходят на анаэробный гликолиз? Сейчас считается, что так они получают преимущество, заранее подготавливаясь к «тяжелым временам» — развитию гипоксии. А кроме этого, такой способ энергообеспечения дает клеткам возможность использовать промежуточные продукты гликолиза для анаболических реакций, усиления своей антиоксидантной защиты и отражения иммунной атаки организма [32].
Таким образом, изменения в метаболизме глюкозы и появление дефектных белков и внутриклеточных агрегатов могут говорить о начале развития патологии. Своевременное выявление подобных внутриклеточных процессов может сыграть решающую роль в предупреждении и терапии самых распространенных нейродегенеративных и онкологических заболеваний. А для того чтобы это было возможным, необходимо изучать фундаментальные аспекты патологий, связанные с работой митохондрий и энергетическим обменом. Сегодня уже разработаны системы, позволяющие заглянуть «вглубь» этих заболеваний и даже провести диагностику на самой ранней стадии их развития. Подробнее об этих системах, принципах их действия и исследованиях с их использованием расскажут следующие статьи спецпроекта.

Компания более 25 лет успешно занимается поставками научного и медицинского оборудования российских и зарубежных производителей: Beckman Coulter, Bio-Rad, Molecular Devices, Thermo Fisher Scientific, UVP, Seahorse Bioscience (part of Agilent), Immucor, MRC Holland и др. «БиоХимМак» обслуживает более 5000 научных и медико-диагностических лабораторий в России и странах СНГ.
Отдел молекулярной диагностики (Life Science MDx)
Молекулярная онкология, преимплантационный скрининг, цитогенетика, пренатальные и постнатальные исследования, диагностика инфекций, наследственных, мультифакторных заболеваний, детекция генномодифицированных источников и бактериального загрязнения в продуктах питания, криминалистические приложения — это лишь неполный перечень областей, которые входят в сферу интересов отдела.
Основные направления деятельности отдела:
- комплексная поставка ПЦР- и иного оборудования для всех этапов анализа — пробоподготовки, амплификации, различных вариантов детектирования и архивирования результатов;
- запуск оборудования и обучение персонала;
- поставка расходных материалов и реагентов для диагностики и научных исследований;
- поиск и поставка тест-систем для решения уникальных задач или использующих передовые технологии, не имеющие пока широкого распространения в диагностической практике.
Отдел работает как с инновационной продукцией (MLPA, PGS и NGS исследования, клеточная биоэнергетика Agilent Seahorse Bioscience), так и с зарекомендовавшими себя мировыми брендами — Beckman Coulter, Bio-Rad, Molecular Devices, UVP, Thermo Fisher Scientific.
Материал предоставлен партнёром — компанией «БиоХимМак»
- Вода студеная, вареная и кипящее молоко, или Еще раз об омоложении;
- Страшней клешней на свете нет…;
- Как появились митохондрии (рассказ, похожий на сказку);
- От сложного к простому: трудности симбиогенеза;
- Ржешевский А.В. (2016). Нанороботы внутри нас: как работают клетки. Популярная механика. 1, 31–34;
- Романовский Ю.М. и Тихонов А.Н. (2010). Молекулярные преобразователи энергии живой клетки. Протонная АТФ-синтаза — вращающийся молекулярный мотор. Успехи физических наук. 9, 931–956;
- Терёшина Е.В. (2007). Роль жирных кислот в развитии возрастного окислительного стресса. Успехи геронтологии. 20, 59–65;
- Скулачев В.П. (1998). Альтернативные функции клеточного дыхания. Соросовский образовательный журнал. 8, 2–7;
- Ржешевский А.В. (2014). Снижение синтеза АТР и дисфункция биологических мембран. Биохимия. 10, 1300–1315;
- Roger H. Unger. (2003). Minireview: Weapons of Lean Body Mass Destruction: The Role of Ectopic Lipids in the Metabolic Syndrome. Endocrinology. 144, 5159-5165;
- C. Xu. (2005). Endoplasmic reticulum stress: cell life and death decisions. Journal of Clinical Investigation. 115, 2656-2664;
- Иллариошкин С.Н. (2012). Нарушения клеточной энергетики при заболеваниях нервной системы. Нервные болезни. 1, 34–38;
- R. A Whitmer. (2005). Obesity in middle age and future risk of dementia: a 27 year longitudinal population based study. BMJ. 330, 1360-0;
- β-амилоид: невидимый враг или тайный защитник? Запутанная тропка болезни Альцгеймера;
- L. M. Obeid. (2003). Ceramide, Stress, and a «LAG» in Aging. Science of Aging Knowledge Environment. 2003, 27pe-27;
- Бабенко Н.А., Семенова Я.А., Харченко В.С. (2009). Влияние обогащенной жирами диеты на содержание сфинголипидов и когнитивные функции у старых крыс. Нейрофизиология. 41, 309–315;
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Смерть после жизни, болезнь Альцгеймера и почему мы хотим перемен;
- Болезнь Альцгеймера: ген, от которого я без ума;
- C. A. Davie. (2008). A review of Parkinson’s disease. British Medical Bulletin. 86, 109-127;
- Как спасти Тринадцатую? (Перспективы лечения болезни Хантингтона);
- Francis O Walker. (2007). Huntington’s disease. The Lancet. 369, 218-228;
- Gunter U. Hoglinger, Annie Lannuzel, Myriam Escobar Khondiker, Patrick P. Michel, Charles Duyckaerts, et. al.. (2005). The mitochondrial complex I inhibitor rotenone triggers a cerebral tauopathy. J Neurochem. 95, 930-939;
- W. W. Smith. (2005). Endoplasmic reticulum stress and mitochondrial cell death pathways mediate A53T mutant alpha-synuclein-induced toxicity. Human Molecular Genetics. 14, 3801-3811;
- Судаков Н.П., Бывальцев В.А., Никифоров С.Б., Сороковиков В.А., Клименков И.В., Константинов Ю.М. (2010). Дисфункция митохондрий при нейродегенеративных заболеваниях. Журнал неврологии и психиатрии. 9, 87–91;
- H. Atamna, K. Boyle. (2006). Amyloid-beta peptide binds with heme to form a peroxidase: Relationship to the cytopathologies of Alzheimer’s disease. Proceedings of the National Academy of Sciences. 103, 3381-3386;
- L. Devi, V. Raghavendran, B. M. Prabhu, N. G. Avadhani, H. K. Anandatheerthavarada. (2008). Mitochondrial Import and Accumulation of -Synuclein Impair Complex I in Human Dopaminergic Neuronal Cultures and Parkinson Disease Brain. Journal of Biological Chemistry. 283, 9089-9100;
- Sandra M. Cardoso, Catarina R. Oliveira. (2005). The role of calcineurin in amyloid-β-peptides-mediated cell death. Brain Research. 1050, 1-7;
- Francis C. Chee, Amritpal Mudher, Matthew F. Cuttle, Tracey A. Newman, Daniel MacKay, et. al.. (2005). Over-expression of tau results in defective synaptic transmission in Drosophila neuromuscular junctions. Neurobiology of Disease. 20, 918-928;
- Robert A. Gatenby, Robert J. Gillies. (2004). Why do cancers have high aerobic glycolysis?. Nat Rev Cancer. 4, 891-899;
- Peter L. Pedersen. (2007). Warburg, me and Hexokinase 2: Multiple discoveries of key molecular events underlying one of cancers’ most common phenotypes, the “Warburg Effect”, i.e., elevated glycolysis in the presence of oxygen. J Bioenerg Biomembr. 39, 211-222;
- Куликов В.А. и Беляева Л.Е. (2013). Метаболическое перепрограммирование раковых клеток. Вестник Витебского государственного медицинского университета. 2, 6–18;
- Melanie Meyer-Luehmann, Tara L. Spires-Jones, Claudia Prada, Monica Garcia-Alloza, Alix de Calignon, et. al.. (2008). Rapid appearance and local toxicity of amyloid-β plaques in a mouse model of Alzheimer’s disease. Nature. 451, 720-724.
biomolecula.ru
Метаболизм | справочник Пестициды.ru
Cхема метаболических процессовCхема метаболических процессов
Процессы метаболизма
Метаболизм включает две группы жизненно важных процессов – катаболизм (энергетический обмен) и анаболизм (биосинтез, или пластический обмен).[3]
- Катаболизм – это совокупность процессов расщепления питательных веществ, которые происходят в основном за счет реакций окисления. В результате выделяется энергия. Основными формами катаболизма у микроорганизмов являются брожение и дыхание. При брожении происходит неполный распад сложных органических веществ с выделением небольшого количества энергии и накоплении богатых энергией конечных продуктов. При дыхании (аэробном) обычно осуществляется полное окисление соединений с выходом большого количества энергии.[3]
- Анаболизм объединяет процессы синтеза молекул из более простых веществ, которые присутствуют в окружающей среде. Реакции анаболизма связаны с потреблением свободной энергии, которая вырабатывается в процессах дыхания, брожения. Для протекания пластического обмена необходимо поступление в организм питательных веществ, на основе которых при участии выделенной в ходе катаболизма энергии обновляются структурные компоненты клеток, происходит рост и развитие.[3]
Катаболизм и анаболизм протекают параллельно, многие их реакции и промежуточные продукты являются общими. Тем не менее, на протяжении разных периодов существования интенсивность пластического и энергетического обмена неодинакова. Так, у насекомых в период размножения, линьки, во время ранних фаз развития (яйцо, личинка) синтетические процессы преобладают над процессами распада. В тоже время, определенные дегенеративные изменения в организме (старение, заболевания) способны приводить к преобладанию интенсивности катаболизма над анаболизмом, что порой угрожает гибелью живому объекту.[3](фото)
Превращение сульфооксида в сульфонПревращение сульфооксида в сульфон
Использовано изображение:[2]
Метаболизм пестицидов
Метаболизм пестицидов – превращения пестицидов под влиянием продуктов жизнедеятельности различных живых организмов – бактерий, грибов, высших растений и животных.[4]
В результате биотрансформации токсичных веществ в большинстве случаев образуются менее токсичные продукты (метаболиты), более растворимые и легко выводимые из организма. В некоторых случаях токсичность метаболитов оказывается выше, чем попавших в организм веществ. Обмен промышленных ядов возможен за счет реакций окисления, восстановления, гидролитического расщепления, метилирования, ацилирования и др.[1]
В метаболизме пестицидов большое значение имеют реакции окисления атома серы в молекулах некоторых веществ, что характерно, например, для инсектицидов из группы производных карбаминовой и фосфорной кислот. Окисление серы у этих соединений происходит независимо от структуры остальной части молекулы, при этом вначале образуется соответствующий сульфооксид, а затем сульфон: (фото) Продукты окисления не отличаются по токсичности от исходного вещества, но они значительно более стойки к гидролизу.
Окисление тионофосфатовОкисление тионофосфатов
А — тионофосфат, В – фосфат, 1 и 2- свободные радикалы, 3 — кислотный остаток
Использовано изображение:[2]
Реакции метаболизма, происходящие в растениях, обусловливают длительное инсектицидное действие для ряда эфиров фосфорных кислот с тиоэфирным радикалом. Окисление тионофосфатов в различных организмах рассматривается как активирующая ступень в процессах метаболизма этих веществ.[2](фото)
Токсичность продукта реакции для млекопитающих и насекомых увеличивается в десятки и сотни раз по сравнению с исходным веществом. Однако эти токсичные метаболиты легко гидролизуются и поэтому сохраняются в биологических средах непродолжительное время.[2]
Близкие статьи
Ссылки:
Все статьи о токсикологии в разделе: Основы токсикологии
Статья составлена с использованием следующих материалов:
Литературные источники:
1.Голдовская Л.Ф. Химия окружающей среды. М.: Мир; БИНОМ. Лаборатория знаний, 2007. – 295 с
2.Груздев Г.С. Химическая защита растений. Под редакцией Г.С. Груздева — 3-е изд., перераб. и доп. — М.: Агропромиздат, 1987. — 415 с.: ил.
3.Липунов И.Н., Первова И.Г. Основы микробиологии и биотехнологии: курс лекций. – Екатеринбург: Урал. гос. лесотехн. Университет, 2008. – 231 с
4.Мельников Н.Н., Новожилов К.В., Белан С.Р., Пылова Т.Н. Справочник по пестицидам — М.: Химия, 1985. — 352 с.
Свернуть Список всех источниковwww.pesticidy.ru
Биология для студентов — 09. Основные особенности метаболических процессов: обмен веществ и его пути. Характеристика функций метаболизма
В живых клетках протекает множество ферментативных реакций. Всю совокупность этих реакций объединяют общим понятием метаболизм (обмен веществ). Он выполняет четыре специфические функции:
- снабжение химической энергией, которая добывается путем расщепления богатых энергией пищевых веществ, поступающих из среды, или путем преобразования улавливаемой энергии солнечного света;
- превращение молекул пищевых веществ в строительные блоки, которые в дальнейшем используются клеткой для построения макромолекул;
- сборка белков, нуклеиновых кислот, липидов, полисахаридов и прочих клеточных компонентов из этих строительных блоков;
- синтез и разрушение тех биомолекул, которые необходимы для выполнения каких-либо специфических функций.
Выделяют внешний и промежуточный обмен веществ. Внешний обмен веществ — внеклеточное переваривание веществ на путях их поступления и выделения из организма.

Промежуточный обмен веществ — превращение веществ внутри клеток с момента их поступления до образования конечных продуктов. Попав внутрь клетки, питательное вещество метаболизируется, т.е. претерпевает ряд химических изменений, катализируемых ферментами. Определённая последовательность таких химических изменений называется метаболическим путём, а образующиеся промежуточные продукты — метаболитами. Большей частью метаболические пути линейны в результате четырех последовательных ферментативных реакций предшественник А превращается в продукт Е, а продукт одной ферментативной реакции служит субстратом следующей:
A El > B Д2 > C ЕЪ > D Д4 > E
Кроме линейных выделяют циклические метаболические пути. Обычно они имеют разветвления, в которых какие-нибудь продукты реакций выходят из цепи реакций данного метаболического пути или, наоборот, вливаются в нее. Именно таким путем происходит окисление ацетильных групп до СО2 и Н2О в цикле лимонной кислоты.
Все метаболические пути делят на:
- центральные
- специальные (вторичные).
Центральные метаболические пути — пути превращения основных пищевых веществ в клетке (углеводов, жиров, белков и нуклеиновых кислот). На этих путях потоки метаболитов довольно внушительны. Например, в организме взрослого человека ежесуточно окисляется несколько сотен граммов глюкозы до СО2 и воды. Последовательности химических превращений на каждом из центральных метаболических путей, в принципе, у всех живых форм едины. Кроме центральных путей есть и другие метаболические пути со значительно меньшим потоком метаболитов (ежесуточный синтез или распад при этом измеряется миллиграммами).
Эти специальные метаболические пути составляют так называемый вторичный метаболизм, роль которого — в образовании различных специализированных веществ, требующихся клеткам в малых количествах. К вторичным метаболическим путям принадлежит, например, биосинтез коферментов и гормонов, потому что эти соединения вырабатываются и используются только в следовых количествах.
Промежуточный метаболизм складывается из двух фаз:
- катаболизма,
- анаболизма.
Катаболизм — это фаза, на которой происходит расщепление сложных органических молекул до более простых конечных продуктов. Углеводы, жиры и белки, поступившие извне с пищей или присутствующие в самой клетке в качестве запасных веществ, распадаются в серии последовательных реакций до таких соединений, как молочная кислота, СО2 и аммиак. Катаболические процессы сопровождаются высвобождением свободной энергии, заключенной в сложной структуре больших органических молекул. На определенных этапах соответствующих катаболических путей значительная часть свободной энергии запасается в форме высокоэнергетического соединения — АТФ (благодаря сопряженным ферментативным реакциям). Часть ее запасается также в богатых энергией водородных атомах кофермента КЛОН (КАОРН), находящегося в восстановленной форме катаболические пути поставляют химическую энергию в форме АТФ и НАДФH. Эта энергия используется на анаболических путях для биосинтеза макромолекул из небольших молекул — предшественников.
Ферментативное расщепление тех главных питательных веществ, которые служат клетке источником энергии, а именно углеводов, жиров и белков, совершается постепенно, т.е. через ряд последовательных ферментативных реакций. В аэробном катаболизме различают три главные стадии:
- На первой стадии макромолекулы клетки распадаются на свои основные «строительные блоки»: полисахариды до гексоз или пентоз, жиры □ до жирных кислот, глицерола и других компонентов, белки — до аминокислот.
- На второй стадии эти «строительные блоки» превращаются в один общий продукт — ацетильную группу ацетил-СоА.
- На третьей стадии различные катаболические пути сливаются в один общий путь — цикл лимонной кислоты; в результате всех этих превращений образуются только три конечных продукта.
Все продукты, образовавшиеся на первой стадии катаболизма, на второй стадии превращаются в еще более простые соединения, число которых сравнительно невелико. Гексозы, пентозы и глицерол расщепляются до одного и того же трехуглеродного промежуточного продукта (пирувата), а затем до единственной двухуглеродной формы ацетильной группы ацетилкофермента А (ацетил-СоА). Аналогичное превращение претерпевают жирные кислоты и углеродные скелеты большей части аминокислот: их расщепление также завершается образованием ацетильных групп в форме ацетил-СоА. Таким образом, ацетил-СоА представляет собой общий конечный продукт второй стадии катаболизма.
На третьей стадии ацетильная группа ацетил-СоА вступает в цикл лимонной кислоты — общий конечный путь, на котором почти все виды клеточного «топлива» в конце концов, окисляются до двуокиси углерода. Конечными продуктами метаболизма являются также вода и аммиак (или другие азотсодержащие соединения). Важно отметить, что катаболические пути сходятся, вливаясь на третьей стадии в общий путь — цикл лимонной кислоты.
Анаболизм, называемый также биосинтезом, — та фаза метаболизма, в которой из малых молекул-предшественников, или «строительных блоков», синтезируются белки, нуклеиновые кислоты и другие макромолекулярные компоненты клеток. Поскольку биосинтез — процесс, в результате которого увеличиваются размеры молекул и усложняется их структура, он требует затраты свободной энергии. Источником энергии служит распад АТФ до АДФ и неорганического фосфата. Для биосинтеза некоторых клеточных компонентов требуются также богатые энергией водородные атомы, донором которых является НАДФH.
Анаболизм, или биосинтез, начинающийся с малых молекул — предшественников, протекает также в три стадии:
- Синтез белков, например, начинается с образования а-кетокислот и других предшественников.
- На второй стадии происходит аминирование а-кетокислот в реакциях с донорами аминогрупп. Образуются а-аминокислоты.
- На последней, завершающей, стадии анаболизма из аминокислот строятся полипептидные цепи и образуются различные белки.
Сходным образом синтезируются липиды. Их синтез начинается с включения ацетильных групп в жирные кислоты и завершается сборкой различных липидных молекул из этих жирных кислот. В отличие от катаболизма для анаболизма характерно расхождение метаболических путей.
Тесная связь между анаболизмом и катаболизмом протекает на уровнях:
- источников атома углерода — продукты катаболизма являются исходными субстратами для анаболических реакций;
- на энергетическом уровне — в процессах катаболизма образуется АТФ и другие макроэргические соединения, энергия которых затрачивается в анаболических процессах;
- на уровне восстановленных эквивалентов — реакции катаболизма в основном окислительные, а анаболические реакции потребляют восстановленные эквиваленты.
Катаболизм сопровождается освобождением энергии, которая может аккумулироваться в виде АТФ. При анаболических процессах происходит потребление энергии, которая освобождается при распаде АТФ до АДФ и фосфорной кислоты или АМФ и пирофосфорной кислоты. Следовательно, АТФ является сопрягающим энергетическим звеном катаболизма и анаболизма. Кроме АТФ связующим звеном могут служить специфические метаболические пути или циклы. Связующий путь (цикл), объединяющий пути распада и синтеза веществ, называется амфиболическим. Примером амфиболического цикла может служить цикл Кребса. Амфиболические пути связаны, как правило, с окислением веществ до углекислого газа и воды.
Функции метаболизма:
- снабжение энергией, которая выделяется при распаде веществ корма;
- превращение молекул пищевых веществ в строительные блоки, которые используются клеткой для синтеза макромолекул;
- сборку собственных макромолекул из этих строительных блоков;
- синтез и разрушение биомолекул, необходимых для выполнения специфических функций клетки (гормонов).
Метаболические пути необратимы. Распад никогда не идет по пути, который являлся бы простым обращением реакций синтеза. В нем участвуют другие ферменты и другие промежуточные продукты. Нередко противоположно направленные процессы протекают в разных отсеках клетки. Так, жирные кислоты синтезируются в цитоплазме при участии одного набора ферментов, а окисляются в митохондриях при участии совсем другого набора.
vseobiology.ru
Обмен веществ (метаболизм) — схема, таблица — Схемо.РФ
- Войти
- Регистрация
- Схемы
- Биология
- География
- История
- Математика и алгебра
- Медицина
- Обществознание
- Педагогика
- Политология
- Право
- Психология
- Русский язык
- Социология
- Физика
- Философия
- Химия
- Экономика
- Прочее
- Книги
- Биология
- География
- История
- Математика и алгебра
- Медицина
- Обществознание
- Педагогика
- Политология
- Право
- Психология
- Русский язык
- Социология
- Физика
- Философия
- Химия
- Экономика
- Прочее
- Комментарии
- Люди
xn--e1aogju.xn--p1ai
Как улучшить метаболизм для похудения дома – 7 способов повышения обмена веществ
Вопрос ускорения метаболизма или улучшения обмена веществ актуальный. Каждая девушка сталкивается с проблемой избыточного веса, причиной которого как раз является плохой или медленный метаболизм. Так и я, смотря очередной раз на стрелку весов, задумалась об этом свойстве нашего человеческого организма и решила рассказать вам о нем много интересного.
Содержание статьи:
Метаболизм и его роль – изучаем суть обмена веществ в организме человека
Обмен веществ играет огромную роль в создании стройной фигуры. Этот биохимический процесс, протекающий в организме любого живого существа, в том числе и меня с вами, необходим для поддержания жизни. Благодаря ему мы может расти и восстанавливаться после полученных травм и реагировать на окружающий мир.
Метаболизм функционирует как отдельный процесс. Его суть преобразовывать поступающие калории, пищу, напитки в энергию. А если у человека есть энергия, то он способен жить.
Различают два типа метаболизма:
- Первый – катаболизм (диссимиляция) протекает быстро, при нем происходит процесс распада всех веществ, поступающих в организм.
- Второй – анаболизм (ассимиляция) наоборот собирает частички в единое целое и помогает клеткам впитать их.
По отдельности эти два процесса неразлучны. Они не могут действовать самостоятельно друг от друга – либо присутствует больше первого, либо второго.
Заметьте, что от процессов обмена веществ зависит ваш вес и строение тела. Когда больше функционирует процесс катаболизма, то человек худеет. А если действует анаболизм, то поправляется.
Схема метаболизма выглядит так:
Регулирует процессы впитываемости веществ и восстановления энергии центральная нервная система – один из отделов головного мозга под названием гипотоламус. В свою очередь его деятельность зависит от сна, отдыха, времени бодрствования, физических нагрузок, рациона питания. Кроме того, деятельность мозга и обменные процессы напрямую связаны с гормональным фоном, а также заболеваниями, которые могут протекать в организме человека.
Когда необходимо ускорить процесс метаболизма – нарушение обмена веществ в организме
Скорость обмена веществ в каждом организме своя, поэтому ускорять этот процесс можно не всем. Нарушение метаболизма, как правило, должен определять врач, так как причинами лишней массы тела могут быть заболевания, психологические расстройства, нарушения гормонального фона и т.п. Без мнения специалиста, конечно, можно ставить на себе эксперименты, а так делают многие женщины с лишним весом, но всегда стоит прислушиваться к себе, к своему самочувствию.
Итак, можно улучшать метаболизм, если вы:
- Ведете сидячий, неактивный образ жизни. Зачастую это первая причина, от чего страдает обмен веществ.
- Неправильно питаетесь.
- Сидите или сидели хоть раз на диете.
- Страдаете от ожирения.
- Имеете пожилой возраст. Обычно с возрастом процессы организма замедляются.
Мне, как работающей девушке, не хватало времени покушать. Зачастую утром, перекусив то, что было в холодильнике, я убегала на работу. На обед, если повезет, тратила минут 20. За это время кушала то, что успевала купить по дороге. А вечером, придя домой, у меня по плану был плотный ужин. Поэтому могла и переесть.
Конечно же я понимала, что с таким режимом и расписанием я никогда не смогу улучшить свой метаболизм. Поэтому решила проанализировать свою жизнь. Итак, я вела сидячий образ жизни, плохо питалась и из-за этого набирала лишние килограммы. Посмотрите и вы на себя со стороны, определите свои недостатки.
Как определить скорость метаболизма в организме – расчет уровня обмена веществ
От потребляемой пищи всего лишь 60-70% сжигается ежедневно.
Заметьте, что скорость метаболизма после 30 лет снижается на 6%, поэтому женщинам приходится все сложнее приводить себя в порядок и худеть.
Чтобы рассчитать количество энергии, которое создает ваш организм, следует:
- Измерить свой рост.
- Взвеситься.
- Полученные результаты подставить в формулу.
Для женщин она такова:
65,5 + (9.6 x вес в кг.) + (1.8 x рост в см.) — (4.7 x возраст в годах).
Для мужчин:
66,0 + (13.7 x вес в кг.) + (5,0 x рост в см.) — (6.8 x возраст в годах)
Итак, теперь вы можете понять, сколько калорий вы тратите в сутки. Примерно такое же количество вы должны съедать.
Если разница большая, то стоит пересмотреть свой рацион питания, иначе похудеть будет очень сложно.
Как повысить метаболизм в организме – эффективные способы улучшения обмена веществ для похудения
Существуют главные способы, которые помогут улучшить ваш метаболизм:
1. Ведите активный образ жизни. Если вы провели целый день в офисе, не засиживайтесь вечером дома, идите прогуливаться на улицу. Даже пешие прогулки помогут вам сжечь необходимое количество калорий. Либо отправляйтесь на тренировку в спортивный зал. Только физическая активность способна избавить вас от лишнего веса, даже в том случае, если вы съедите чего-нибудь лишнего.
2. Начните правильно питаться.
Запомните несколько правил:
- Питайтесь несколько раз в день. В идеале у вас должны быть 3 основных приема пищи и 2 дополнительных.
- Кушайте маленькими порциями. Чтобы измерить размер вашего желудка и узнать, сколько еды в него вмещается, сожмите свой кулак – именно столько вы должны съедать за 1 прием пищи.
- Включите в свой рацион овощи, фрукты (особенно цитрусовые), супы, красный перец, овсянку, коричневый рис, а также пищу, богатую кальцием, омегой-3.
Вам помогут следующие продукты:
- Никогда не придерживайтесь диет. Сидя на диете, в вашем организме возникает недостаток полезных веществ. После выхода из любой диеты, вы снова наберете тот вес, который сбросили, так как организм будет восстанавливаться, впитывая еще больше еды.
3. Пейте больше воды, ведь выходит из организма ее очень много.
В сутки взрослый человек должен выпивать минимум 2 литра воды.
4. Высыпайтесь. Здоровый сон – залог отличного метаболизма в организме. Научитесь ложиться вовремя и спать минимум 8 часов в сутки.
5. Откажитесь от вредных привычек. Запомните, что сигареты и алкоголь не для вас!
6. Посещайте сауну и баню. Жара, горячий воздух помогают вывести из организма ненужное количество воды, токсинов, шлаков.
7. Не нервничайте. Чаще всего стрессовые ситуации выбивают нас из колеи, и мы начинаем заедать эмоциональные переживания. Постарайтесь не связывать свои чувства и еду.
Я начала придерживаться таких правил не сразу, добавляла по одному пункту в день. Спустя время они вошли в привычку, и мне стало легче!
Вес стал потихоньку снижаться, а это главный показатель восстановления обмена веществ.
Итак, если вы мечтаете похудеть, то начните следить за собой с сегодняшнего дня. Не откладывайте правила на завтра. Я перечислила все важные аспекты улучшения метаболизма для похудения. Важно не только о них знать, но и действовать, чтобы увидеть положительный результат.
www.odnadama.ru
Глава 8 введение в метаболизм
Обмен веществ или метаболизм – это совокупность химических реакций в организме, которые обеспечивают его веществами и энергией, необходимыми для жизнедеятельности. Процесс метаболизма, сопровождающийся образованием более простых соединений из сложных, обозначают термином —катаболизм. Процесс, идущий в обратном направлении и приводящий, в конечном счете, к образованию сложного продукта из относительно более простых –анаболизм. Анаболические процессы сопровождаются потреблением энергии, катаболические – высвобождением.
Анаболизм и катаболизм не являются простым обращением реакций. Анаболические пути должны отличаться от путей катаболизма хотя бы одной из ферментативных реакций, чтобы регулироваться независимо, и за счет контроля активности этих ферментов регулируется суммарная скорость распада и синтеза веществ. Ферменты, которые определяют скорость всего процесса в целом, называются ключевыми.
Более того, путь по которому идет катаболизм той или иной молекулы, может быть непригодным для ее синтеза по энергетическим соображениям. Например, протекающие в печени расщепление глюкозы до пирувата представляет собой процесс, состоящий из 11 последовательных стадий, катализируемых специфическими ферментами. Казалось бы, синтез глюкозы из пирувата должен быть простым обращением всех этих ферментативных стадий её распада. Такой путь представляется на первый взгляд и самым естественным, и наиболее экономичным. Однако в действительности биосинтез глюкозы (глюконеогенез) в печени протекает иначе. Он включает лишь 8 из 11 ферментативных стадий, участвующих в ее распаде, а 3 недостающие стадии заменены в нем совсем другим набором ферментативных реакций, свойственным только этому биосинтетическому пути. Кроме того, реакции катаболизма и анаболизма часто разделены мембранами и протекают в разных компартментах клеток.
Таблица 8.1.
Компартментализация некоторых метаболических путей в гепатоците
Цитозоль | Гликолиз, многие реакции глюконеогенеза, активация аминокислот, синтез жирных кислот |
Плазматическая мембрана | Энергозависимые транспортные системы |
Ядро | Репликация ДНК, синтез различных видов РНК |
Рибосомы | Синтез белка |
Лизосомы | Изоляция гидролитических ферментов |
Комплекс Гольджи | Образование плазматической мембраны и секреторных пузырьков |
Микросомы | Локализация каталазы и оксидаз аминокислот |
Эндоплазмати-ческая сеть | Синтез липидов |
Митохондрии | Цикл трикарбоновых кислот, цепь тканевого дыхания, окисление жирных кислот, окислительное фосфорилирование |
Метаболизм выполняет 4 функции:
1) снабжение организма химической энергией, полученной при расщеплении богатых энергией пищевых веществ;
2) превращение пищевых веществ в строительные блоки, которые используются в клетке для биосинтеза макромолекул;
3) cборка макромолекулярных (биополимеры) и надмолекулярных структур живого организма, пластическое и энергетическое поддержание его структуры;
4) синтез и разрушение тех биомолекул, которые необходимы для выполнения специфических функций клетки и организма.
Метаболический путь– это последовательность химических превращений конкретного вещества в организме. Промежуточные продукты, образующиеся в процессе превращения, называютметаболитами, а последнее соединение метаболического пути – конечным продукт. Примером метаболического пути является гликолиз, синтез холестерина.
Метаболический цикл– это такой метаболический путь, один из конечных продуктов которого идентичен одному из соединений вовлеченных в этот процесс. Наиболее важными в организме человека метаболическими циклами являются цикл трикарбоновых кислот (цикл Кребса) и орнитиновый цикл мочевинообразования.
Почти все метаболические реакции в конечном итоге связаны между собой, поскольку продукт одной ферментативной реакции служит субстратом для другой, которая в данном процессе играет роль следующей стадии. Таким образом, метаболизм можно представить в виде чрезвычайно сложной сети ферментативных реакций. Если поток питательных веществ в какой-нибудь одной части этой сети уменьшится или нарушится, то в ответ могут произойти изменения в другой части сети, для того чтобы это первое изменение было как-то уравновешено или скомпенсировано. Более того, и катаболические и анаболические реакции отрегулированы таким образом, чтобы они протекали наиболее экономично, то есть с наименьшей затратой энергии и веществ. Например, окисление питательных веществ в клетке совершается со скоростью, как раз достаточной для того, чтобы удовлетворить ее энергетические потребности в данный момент.
studfile.net
