как укрепить иммунитет и увеличить объем легких
Если о влиянии закаливания на иммунитет знает каждый, то о пользе «кислородного голодания» слышали не все, хотя механизмы этих процессов похожи. Оказывается, такая практика как задержка дыхания может оказать благоприятное влияние на организм.
«При задержке дыхания наблюдается увеличение углекислого газа в организме и так называемое состояние гипоксии. В состоянии искусственного стресса наш организм начинает синтезировать клетки, которые будут его защищать, в частности, от вирусных и бактериальных агентов», – рассказала преподаватель кафедры спортивной медицины и медицинской реабилитации Сеченовского университета Кристина Володина.
Лучше всего кратковременное отсутствие воздуха активирует иммунитет именно в комбинации с активными дыхательными практиками. Ведь поверхностного дыхания, на которое мы часто переходим в быту, не хватает, чтобы обеспечить должным питанием все системы организма.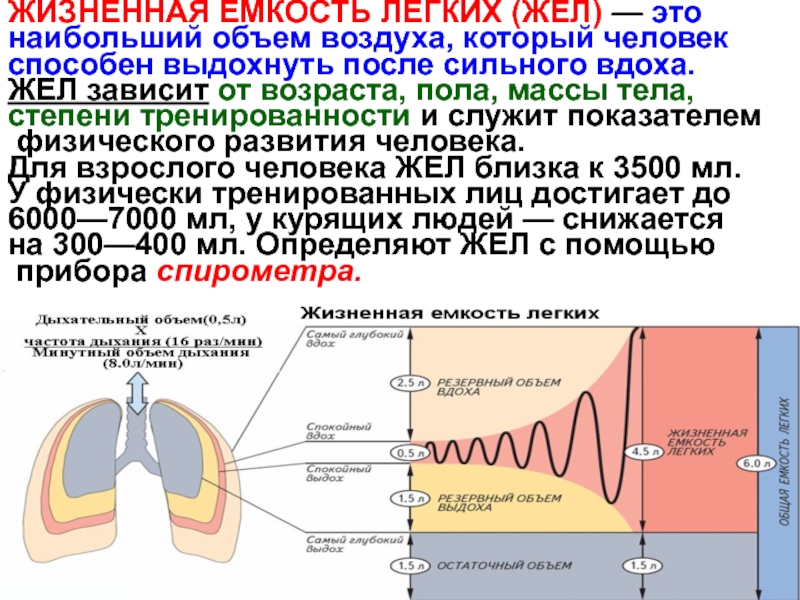
«В нашей легочной ткани, в частности, в бронхах есть специальный эпителий. Благодаря дыхательной гимнастике увеличивается кровоснабжение данных клеток и, как следствие, все иммунные процессы получают лучшее питание», – говорит Кристина Володина.
Как понять, что во время упражнений вы дышите достаточно глубоко? Индикатором могут послужить ладони, размещенные на нижних ребрах. Во время дыхания они должны двигаться в стороны.
Помочь легким полностью заполниться кислородом можно и другим способом, если во время дыхания сделать акцент на сокращении и расслаблении мышц, окружающих легкие.
«Сделаем спокойный вдох, при этом отводим плечи назад и сводим локти за спиной. Далее делаем выдох плавный, более продолжительный, и прогибаемся максимально в спине», – показывает доцент кафедры физиологии РНИМУ имени Пирогова Ирина Бабкина.
Ключевое правило выполнение упражнений: выдох должен быть вдвое длиннее вдоха, а вдох – исключительно через нос. Регулярное выполнение такой гимнастики увеличивает объем легких и мощь дыхательной мускулатуры. На продвинутом уровне люди с сильными легкими без труда надувают резиновую грелку. Правда, столь агрессивные упражнения не подойдут людям, страдающим от серьезных заболеваний дыхательных путей или тем, кто совсем недавно перенес коронавирус.
На продвинутом уровне люди с сильными легкими без труда надувают резиновую грелку. Правда, столь агрессивные упражнения не подойдут людям, страдающим от серьезных заболеваний дыхательных путей или тем, кто совсем недавно перенес коронавирус.
«Коронавирусная инфекция сопряжена с уплотнением легочной ткани, в связи с этим классические упражнения не подходят, они даже могут привести к разрыву легочной ткани, поэтому хорошей альтернативой будет подуть через трубочку в стакан с водой», – говорит Ирина Бабкина.
Вода обеспечивает сравнительно легкое сопротивление, достаточное для того, чтобы постепенно укрепить легкие.
Немало щадящих дыхательные пути упражнений есть и в йоге, одно из самых полезных – ритмическое дыхание.
«Мы делаем вдох на два, потом на четыре счета делаем задержку, и на семь счетов выдох. Таким образом мы очень плавно увеличиваем объем легких», – рассказала сертифицированный тренер по йоге Алина Капитонова.
Еще одна интересная мягкая дыхательная практика, которую йоги советуют включить в дыхательную гимнастику, это попеременное дыхание правой и левой ноздрей, где вдох и выдох делаются разными сторонами носа.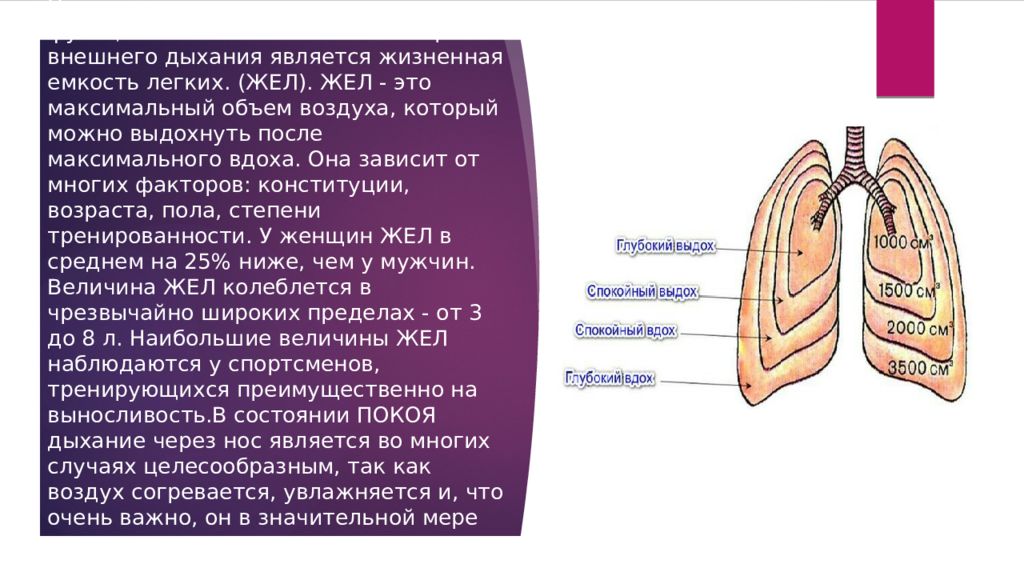 Йоги верят, что такие практики, где приходится дополнительно фокусироваться на ритме дыхания, активируют мышление и увеличивают объем активного внимания. Если это так, то это тоже плюс. Значит, будет больше внимания, чтобы уделить его своему здоровью.
Йоги верят, что такие практики, где приходится дополнительно фокусироваться на ритме дыхания, активируют мышление и увеличивают объем активного внимания. Если это так, то это тоже плюс. Значит, будет больше внимания, чтобы уделить его своему здоровью.
Страница не найдена |
Страница не найдена |404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
6789101112
13141516171819
20212223242526
2728293031
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Метки
Настройки
для слабовидящих
Внешнее дыхание и объемы легких
Для фридайвера легкие явлются основным «рабочим инстументом» (конечно, после головного мозга), поэтому нам важно понимать устройство легких и весь процесс дыхания.
Строение легких и грудной клетки
Легкие представляют собой пористый орган, похожий на губку, напоминающий в своем строении скопление отдельных пузырьков или виноградную гроздь с большим количеством ягод. Каждая «ягода» — это легочная альвеола (легочный пузырек) — место, где происходит выполнение основной функции легких — газообмен. Между воздухом альвеол и кровью лежит воздушно-кровяной барьер, образованный очень тонкими стенками альвеолы и кровеносного капилляра. Именно через этот барьер происходит диффузия газов: из альвеолы в кровь поступает кислород, а из крови в альвеолу углекислый газ.
Воздух к альвеолам поступает по воздухоносным путям — трохея, бронхи и более мелкие бронхиолы, которые завершаются альвеолярными мешками. Ветвление бронхов и бронхиол формирует доли (правое легкое имеет 3 доли, левое — 2 доли). В среднем в обоих легких имеется около 500-700 млн альвеол, дыхательная поверхность которых составляет от 40 м
В среднем в обоих легких имеется около 500-700 млн альвеол, дыхательная поверхность которых составляет от 40 м
Бронхи и трахея имеют в своих стенках хрящевое основание и поэтому достаточно жестки. Бронхиолы и альвеолы имеют мягкие стенки и поэтому могут спадаться, то есть слипаться, как спустивший воздушный шарик, если в них не поддерживать некое давление воздуха. Чтобы этого не произошло, легкие, как единый орган, со всех сторон покрытый плеврой — прочной герметичной оболочкой.
Плевра имеет два слоя — два листка. Один листок плотно прилежит к внутренней поверхности жесткой грудной клетки, другой — окружает легкие. Между ними находится плевральная полость, в которой поддерживается отрицательное давление. Благодаря этому легкие находятся в расправленном состоянии. Отрицательное давление в плевральной щели обусловлено эластической тягой легких, то есть постоянным стремлением легких уменьшить свой объем.
Эластическая тяга легких обусловлена тремя факторами:
1) упругостью ткани стенок альвеол вследствие наличия в них эластичных волокон
2) тонусом бронхиальных мышц
3) поверхностным натяжением пленки жидкости, покрывающей внутреннюю поверхность альвеол.
Жесткий каркас грудной клетки составляют ребра, которые гибко, благодаря хрящам и суставам, присоединяются к позвоночнику и суставам. Благодаря этому грудная клетка увеличивает и уменьшает свой объем, сохраняя при этом жесткость, необходимую для защиты находящихся в грудной полости органов.
Дыхательные мышцы
Для того, чтобы вдохнуть воздух, нам необходимо создать в легких давление более низкое, чем атмосферное, а чтобы выдохнуть более высокое. Таким образом, для вдоха необходимо увеличение объема грудной клетки, для выдоха — уменьшением объема. На самом деле большая часть усилий дыхания расходуется на вдох, в обычных условиях выдох осуществляется за счет упругих свойств легких.
Основной дыхательной мышцей является диафрагма — куполообразная мышечная перегородка между полостью грудной клетки и брюшной полостью.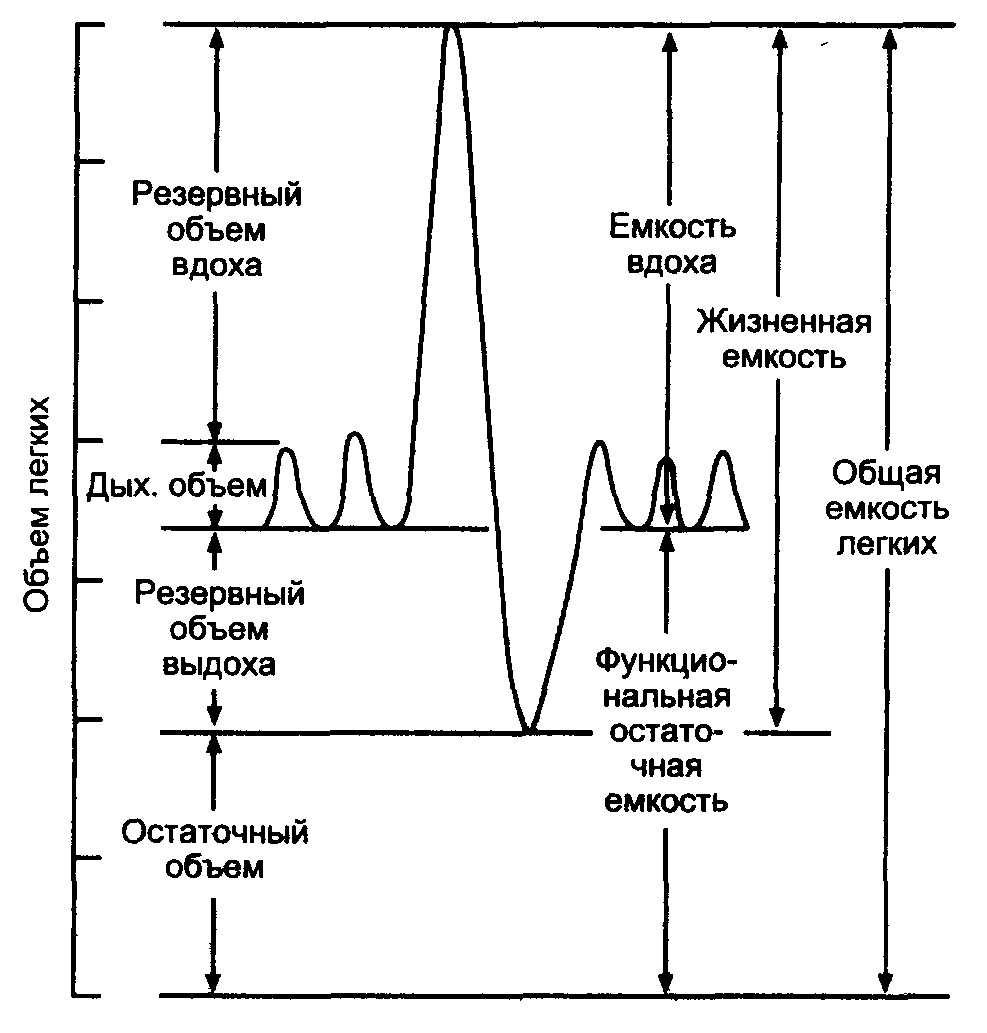
При вдохе диафрагма сокращается, растягиваясь активным действием в сторону нижних внутренних органов. При этом несжимаемые органы брюшной полости оттесняются вниз и в стороны, растягивая стенки брюшной полости. При спокойном вдохе купол диафрагмы спускается приблизительно на 1.5 см, соответственно увеличивается вертикальный размер грудной полости. При этом нижние ребра несколько расходятся, увеличивая и обхват грудной клетки, что особенно заметно в нижних отделах. При выдохе диафрагма пассивно расслабляется и подтягивается, удерживающими её сухожилиями, в своё спокойное состояние.
Кроме диафрагмы, в увеличении объема грудной клетки принимают участие также наружные косые межреберные и межхрящевые мышцы. В результате подъема ребер увеличивается смещение грудины вперед и отхождение боковых частей ребер в стороны.
При очень глубоком интенсивном дыхании или при повышении сопротивления вдоху в процесс увеличения объема грудной клетки включается ряд вспомогательных дыхательных мышц, которые могут поднимать ребра: лестничные, большая и малая грудные, передняя зубчатая.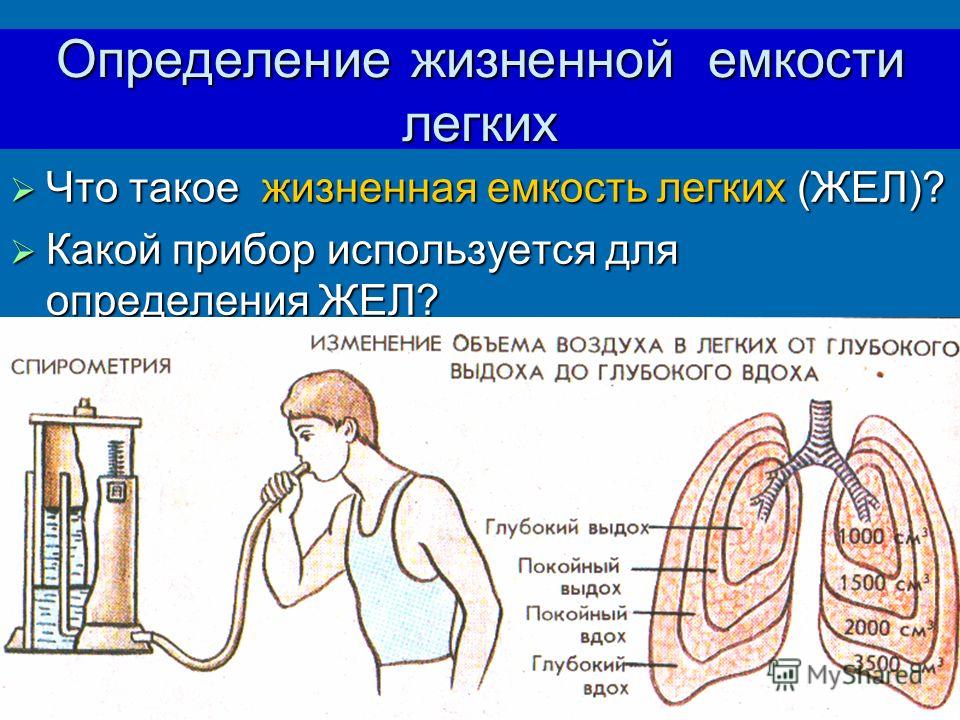 К вспомогательным мышцам вдоха относятся также мышцы, разгибающие грудной отдел позвоночника и фиксирующие плечевой пояс при опоре на откинутые назад руки(трапециевидная, ромбовидные, поднимающая лопатку).
К вспомогательным мышцам вдоха относятся также мышцы, разгибающие грудной отдел позвоночника и фиксирующие плечевой пояс при опоре на откинутые назад руки(трапециевидная, ромбовидные, поднимающая лопатку).
Как говорилось выше, спокойный вдох протекает пассивно, практически на фоне расслабления мышц вдоха. При активном интенсивном выдохе «подключаются» мышцы брюшной стенки, в результате чего объем брюшной полости уменьшается и повышается давление в ней. Давление передается на диафрагму и поднимает ее. Вследствие сокращения внутренних косых межреберных мышц происходит опускание ребер и сближение их краев.
Дыхательные движения
В обычной жизни, понаблюдав за собой и своими знакомыми, можно увидеть как дыхание, обеспечиваемое в основном диафрагмой, так и дыхание, обеспечиваемое в основном работой межреберных мышц. И это в пределах нормы. Мышцы плечевого пояса чаще подключаются при серьезных заболеваниях или интенсивной работе, но почти никогда — у относительно здоровых людей в нормальном состоянии.
Считается, что дыхание, обеспечиваемое в основном движениями диафрагмы, характерно больше для мужчин. В норме вдох сопровождается незначительным выпячиванием брюшной стенки, выдох — незначительным ее втяжением. Это брюшной тип дыхания.
У женщин чаще всего встречается грудной тип дыхания, обеспечиваемый в основном работой межреберных мышц. Это может быть связано с биологической готовностью женщины к материнству и, как следствие, с затрудненностью брюшного дыхания при беременности. При этом типе дыхания наиболее заметные движения совершает грудина и ребра.
Дыхание, при котором активно движутся плечи и ключицы, обеспечивается работой мышц плечевого пояса. Вентиляция легких при этом малоэффективна и касается только верхушек легких. Поэтому такой тип дыхания называется верхушечным. В обычных условиях такой тип дыхания практически не встречается и используется либо в ходе тех или иных гимнастик или развивается при серьезных заболеваниях.
Во фридайвинге мы считаем, что брюшной тип дыхания или дыхание животом является наиболее естественным и продуктивным. Об этом же говорится при занятиях йогой и пранаямой.
Об этом же говорится при занятиях йогой и пранаямой.
Во-первых, потому, что в нижних долях легких находится больше альвеол. Во-вторых, дыхательные движения связаны с нашей вегетативной нервной системой. Дыхание животом активирует парасимпатическую нервную систему — педаль тормоза для организма. Грудное дыхание активирует симпатическую нервную систему — педаль газа. При активном и долгом верхушечном дыхании происходит перестимуляция симпатической нервной системы. Это работает в обе стороны. Так паникующие люди всегда дышат верхушечным дыханием. И наоборот, если какое-то время спокойно дышать животом, происходит успокоение неврной системы и замедление всех процессов.
Легочные объемы
При спокойном дыхании человек вдыхает и выдыхает около 500 мл (от 300 до 800 мл) воздуха, этот объем воздуха называется дыхательным объемом. Кроме обычного дыхательного объема при максимально глубоком вдохе человек может вдохнуть еще приблизительно 3000 мл воздуха — это резервный объем вдоха.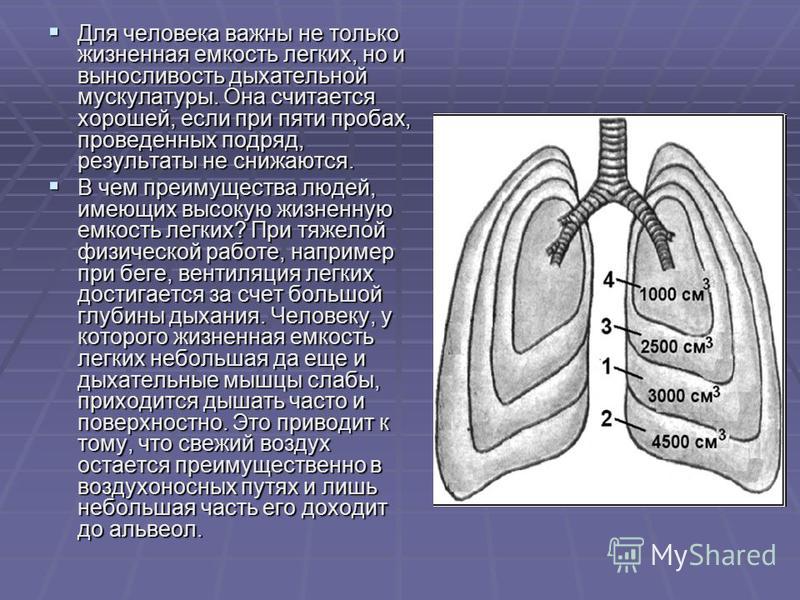 После обычного спокойного выдоха обычный здоровый человек напряжением мышц выдоха способен «выдавить» из легких еще около 1300 мл воздуха — это резервный объем выдоха.
После обычного спокойного выдоха обычный здоровый человек напряжением мышц выдоха способен «выдавить» из легких еще около 1300 мл воздуха — это резервный объем выдоха.
Сумма указанных объемов составляет жизненную емкость легких (ЖЭЛ): 500 мл + 3000 мл + 1300 мл = 4800 мл.
Как видим, природа подготовила для нас почти десятикратный запас по возможности «прокачивать» воздух через легкие.
Дыхательный объем — количественное выражение глубины дыхания. Жизненная емкость легких определяет собой максимальный объем воздуха, который может быть введен или выведен из легких в течение одного вдоха или выдоха. Средняя жизненная емкость легких у мужчин составляет 4000 — 5500 мл, у женщин — 3000 — 4500 мл. Физические тренировки и различные растяжки грудной клетки позволяют увеличить ЖЭЛ.
После максимального глубокого выдоха в легких остается около 1200 мл воздуха. Это — остаточный объем. Большая его часть может быть удалена из легких только при открытом пневмотораксе.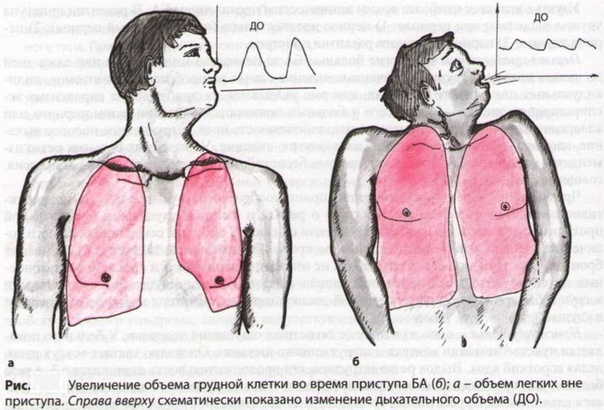
Остаточный объем определяется в первую очередь эластичностью диафрагмы и межреберных мышц. Увеличение подвижности грудной клетки и уменьшение остаточного объема — важная задача при подготовке к нырянию на большие глубины. Погружения ниже остаточного объема для обычного нетренированного человека — это погружения глубже 30-35 метров. Один из популярных способов увеличения эластичности диафрагмы и уменьшения остаточного объема легких — регулярное выполнение уддияна бандхи.
Максимальное количество воздуха, которое может находиться в легких, называется общей емкостью легких, она равна сумме остаточного объема и жизненной емкости легких (в использованном примере: 1200 мл + 4800 мл = 6000 мл).
Объем воздуха, находящийся в легких в конце спокойного выдоха (при расслабленной дыхательной мускулатуре) называется функциональной остаточной емкостью легких. Она равна сумме остаточного объема и резервного объема выдоха (в использованном примере: 1200 мл + 1300 мл = 2500 мл). Функциональная остаточная емкость легких близка к объему альвеолярного воздуха перед началом вдоха.
Функциональная остаточная емкость легких близка к объему альвеолярного воздуха перед началом вдоха.
Вентиляция легких определяется объемом воздуха, вдыхаемого или выдыхаемого в единицу времени. Обычно измеряют минутный объем дыхания. Вентиляция легких зависит от глубины и частоты дыхания, которая в состоянии покоя составляет от 12 до 18 вдохов в минуту. Минутный объем дыхания равен произведению дыхательного объема на частоту дыхания, т.е. примерно 6-9 л.
Для оценки легочных объемов используется спирометрия — метод исследования функции внешнего дыхания, включающий в себя измерение объёмных и скоростных показателей дыхания. Мы рекомендуем пройти это исследование всем, кто планирует серьезно заниматься фридайвингом.
Мертвое пространство
Воздух находится не только в альвеолах, но и в воздухоносных путях. К ним относятся полость носа (или рта при ротовом дыхании), носоглотка, гортань, трахея, бронхи. Воздух, находящийся в воздухоносных путях (за исключением дыхательных бронхиол), не участвует в газообмене. Поэтому просвет воздухоносных путей называют анатомическим мертвым пространством. При вдохе последние порции атмосферного воздуха входят в мертвое пространство и, не изменив своего состава, покидают его при выдохе.
Поэтому просвет воздухоносных путей называют анатомическим мертвым пространством. При вдохе последние порции атмосферного воздуха входят в мертвое пространство и, не изменив своего состава, покидают его при выдохе.
Объем анатомического мертвого пространства около 150 мл или примерно 1/3 дыхательного объема при спокойном дыхании. Т.е. из 500 мл вдыхаемого воздуха в альвеолы поступает лишь около 350 мл. В альвеолах в конце спокойного выдоха находится около 2500 мл воздуха, поэтому при каждом спокойном вдохе обновляется лишь 1/7 часть альвеолярного воздуха.
«ПОЛНОЕ ДЫХАНИЕ». Положительные свойства упражнения -Наши новости
«ПОЛНОЕ ДЫХАНИЕ». Положительные свойства упражненияСеу Лилия Витальевна инструктор-методист по ЛФК
С помощью «полного дыхания» мы начинаем дышать более глубоко, увеличивать вдох и выдох, активизировать все части легких. Благодаря этому постепенно углекислый газ начинает накапливаться в легких, а газообмен будет стремиться к равновесию. А увеличение углекислого газа уже способствует выведению слизи в легких и освобождению дыхательных путей.
А увеличение углекислого газа уже способствует выведению слизи в легких и освобождению дыхательных путей.
Воздействие на организм в целом. Во время упражнения происходит замедление нашего дыхания и расслабление тела. За счет этого успокаивается ум, появляется внутренняя гармония, снимается психоэмоциональное напряжение. Также ускоряется обмен веществ, укрепляется иммунитет и повышается концентрация. Дыхание животом также способствует укреплению мышц пресса, стимулирует правильную работу желудочно-кишечного тракта, способствует снижению аппетита и нормализации веса.
ТРЕНИРОВКА ДИАФРАГМАЛЬНОЙ МЫШЦЫ. При дыхании грудью воздух наполняет только верхние отделы легких, мы начинаем вдыхать меньше кислорода, что в итоге приводит к ослаблению здоровья и ухудшению работы головного мозга. А при дыхании диафрагмой в наши легкие набирается гораздо больше воздуха, и организм получает больше кислорода. Поэтому важно развивать свою диафрагму и учиться правильно дышать.
РЕГЕНЕРАЦИЯ И ТРЕНИРОВКА ЛЕГОЧНЫХ ТКАНЕЙ. При малоподвижности наши мышцы начинают ослабевать и атрофироваться. При неполноценном использовании легких, происходит тоже самое с легочными тканями: они начинают терять свою функциональность. Даже при коронавирусе страдают, в первую очередь, нижние отделы легких и может начаться активное воспаление, потому что эта часть легких меньше всего используется при дыхании.
При малоподвижности наши мышцы начинают ослабевать и атрофироваться. При неполноценном использовании легких, происходит тоже самое с легочными тканями: они начинают терять свою функциональность. Даже при коронавирусе страдают, в первую очередь, нижние отделы легких и может начаться активное воспаление, потому что эта часть легких меньше всего используется при дыхании.
Во время упражнения «полное дыхание» мы начинаем активизировать все ткани легких, в том числе нижнюю часть. Происходит насыщение кислородом и развитие всех легочных тканей.
УВЕЛИЧЕНИЕ ОБЪЕМА. Данное свойство вытекает из вышеупомянутого. При развитии и тренировке легких увеличивается их объем, что сделает нас более сильными, выносливыми и здоровыми. Также при увеличении объема легких правильно используется энергия нашего тела и экономится расход энергии, так как мы начинаем медленнее и глубже вдыхать и выдыхать воздух.
ПРЕДОТВРАЩЕНИЕ ГИПЕРВЕНТИЛЯЦИИ. С помощью упражнения улучшается газообмен в легких и предотвращается избыток кислорода. При дыхании грудью мы активизируем верхнюю часть легких, из-за чего снижается количество углекислого газа и может возникнуть преизбыток кислорода в легких.
При дыхании грудью мы активизируем верхнюю часть легких, из-за чего снижается количество углекислого газа и может возникнуть преизбыток кислорода в легких.
Лечение дыхательной системы | Санаторно-курортный комплекс «Русь»
Заболевания органов дыхания достаточно многообразны и довольно часто встречающиеся.
Рассмотрим основные причины, в результате которых возникают заболевания органов дыхательной системы. Основная причина — микроорганизмы (бактерии, вирусы, грибы, реже паразиты). Ведущая роль относится таким бактериальным возбудителям, как: пневмококки, гемофильная палочка, микоплазмы, хламидии, легионеллы (эти возбудители вызывают в основном пневмонии), микобактерия туберкулеза, вирусы гриппа типа А и В, респираторные вирусные инфекции.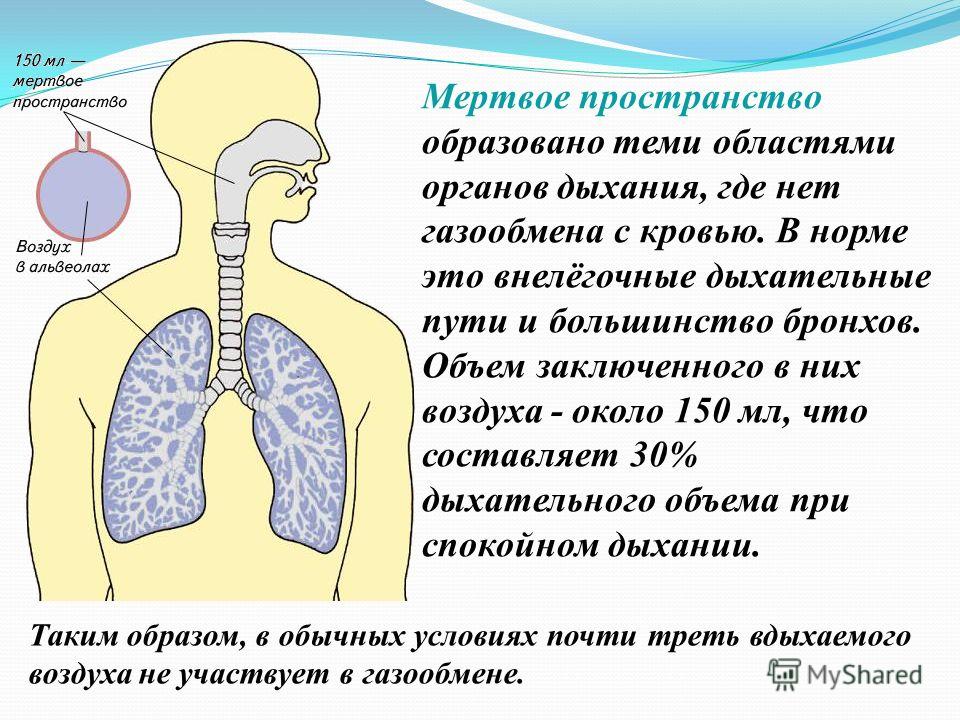 Чаще заболевание вызывается одним типом возбудителя (моноинфекция), но иногда (пожилой возраст, СПИД и другие иммунодефицитные заболевания) их может быть несколько (микстинфекции).
Чаще заболевание вызывается одним типом возбудителя (моноинфекция), но иногда (пожилой возраст, СПИД и другие иммунодефицитные заболевания) их может быть несколько (микстинфекции).
Также довольно часто причиной поражения органов дыхательной системы являются внешние аллергены. К ним относятся:
- Бытовые аллергены — домашняя пыль, которая содержит аллергены грибов, насекомых, домашних животных, частицы кожи человека и другие. Наибольшими аллергенными свойствами обладают домашние клещи (основная причина бронхиальной астмы).
- Аллергены животных, они содержатся в слюне, перхоти и моче животных.
- Аллергены плесневых и дрожжевых грибов, а именно их споры.
- Пыльца растений (травы: крапива, подорожник, полынь цветы: лютик, одуванчик, мак, кустарники: шиповник, сирень, деревья: береза, тополь и другие), споры грибов, аллергены насекомых.
- Профессиональные факторы (электросварка – соли никеля, испарения стали).

- Пищевые аллергены (коровье молоко).
- Лекарственные препараты (антибиотики, ферменты).
Провоцируют возникновение заболеваний органов дыхательной системы загрязнения воздуха (двуокись азота, двуокись серы, бензпирен и многие другие), бытовые загрязнения, которые содержатся в современных жилых помещениях (продукты бытовой химии, синтетические материалы, лаки, краски, клей), курение (активное, пассивное) за счет негативного действия табачного дыма, неблагоприятные климатические условия (низкая температура, высокая влажность, сильные колебания атмосферного давления).
Также к провоцирующим факторам относится злоупотребление алкоголем, переохлаждение, наличие заболеваний других органов и систем (сахарный диабет, заболевания сердца), наличие очагов хронической инфекции, наследственные и генетические аномалии и многие другие.
Симптомы при заболеваниях органов дыхательной системы.
Одышка, она может быть субъективной (ощущение больным затруднения дыхания при неврозах, истерии), объективной (определяется методами исследования и характеризуется изменениями ритма дыхания и продолжительностью вдоха и выдоха при эмфиземе легких) и сочетанной (к объективной одышке присоединяется и субъективный компонент с увеличением частоты дыхания при воспалениях легких, бронхогенном раке легкого, туберкулёзе). Одышка бывает физиологической (при повышенной физической нагрузке), патологической (при заболеваниях). Также она бывает инспираторной при затруднении вдоха (заболевания гортани, трахеи), экспираторной при затруднении выдоха (при поражении бронхов) и смешанной (тромбоэмболия легочной артерии).
Одышка бывает физиологической (при повышенной физической нагрузке), патологической (при заболеваниях). Также она бывает инспираторной при затруднении вдоха (заболевания гортани, трахеи), экспираторной при затруднении выдоха (при поражении бронхов) и смешанной (тромбоэмболия легочной артерии).
Наиболее тяжелая форма одышки – это удушье (при остром отеке легких). Если удушье возникает в виде внезапного приступа, то это астма (бронхиальная – спазм мелких бронхов, сердечная – вследствие ослабления работы сердца).
Следующий симптом болезней органов дыхания – это кашель (рефлекторная защитная реакция на скопление в гортани, трахее или бронхах слизи, а также на инородное тело, попавшее в дыхательную систему). По своему характеру кашель может быть сухим, без выделения мокроты (ларингит, сухой плеврит) и влажным, с выделением мокроты различного количества и качества (утренний кашель при хроническом бронхите, вечерний кашель при пневмонии, ночной кашель при туберкулезе, онкологических заболеваниях). Также он может быть постоянным (при воспалении гортани, бронхов) и периодическим (при гриппе, ОРЗ, пневмонии).
Также он может быть постоянным (при воспалении гортани, бронхов) и периодическим (при гриппе, ОРЗ, пневмонии).
Ещё один симптом – кровохарканье (выделение крови с мокротой при кашле). Оно может проявляться как при заболеваниях органов дыхательной системы (рак легкого, туберкулез, абсцесс легкого), так и при заболеваниях сердечно-сосудистой системы (пороки сердца). Кровь, выделяемая при кашле с мокротой, может быть свежей (алой) или измененной. Алая встречается при туберкулезе, аскаридозе. При крупозной пневмонии во 2 стадии заболевания она бывает ржавого цвета (ржавая мокрота).
Ещё на что могут жаловаться пациенты – это боль. Она может быть разной по происхождению и локализации, по характеру, интенсивности, продолжительности, по связи с актом дыхания, кашля и положением тела.
Методы исследования.
Правильно собранные жалобы, осмотр и грамотно проведенное обследование (пальпация, аускультация, перкуссия) – залог правильно поставленного диагноза. При всем этом можно выявить дополнительные признаки заболеваний.
При всем этом можно выявить дополнительные признаки заболеваний.
Осмотр – выявляются патологические формы грудной клетки (бочкообразная при эмфиземе, увеличение объема одной половины грудной клетки при плеврите, уменьшение половины грудной клетки при пневмосклерозе, пневмонии), тип дыхания, частота, глубина, ритм дыхания.
При пальпации оценивают голосовое дрожание, оно может быть усиленным (воспаление легких), ослабленным (плевриты).
При перкуссии можно выявить уменьшение количества воздуха в легких (фиброз, отек легких), полное отсутствие воздуха в целой доле или её части (абсцесс), увеличение содержания воздуха (эмфизема), также определить границы легких.
Аускультация позволяет оценить дыхание (в норме оно везикулярное, при бронхитах жесткое), выслушать хрипы ( сухие при бронхиальной астме, влажные при пневмонии, абсцессе легкого).
Инструментальные и лабораторные методы исследования.

Рентгенологические методы исследования (рентгеноскопия, рентгенография, томография, бронхография, флюорография) являются самыми важными в диагностике заболеваний органов дыхания.
Эндоскопические методы исследования (бронхоскопия, торакоскопия). Бронхоскопия важна для диагностики гнойных и опухолевых заболеваний. Но она применяется не только как диагностическая, но и как лечебная (например, для удаления инородных тел).
Методы функциональной диагностики.
Эти методы не позволяют диагностировать заболевание, которое привело к дыхательной недостаточности, однако дают возможность выявить её наличие, нередко задолго до появления первых симптомов.
Измерение легочных объемов.
Дыхательный объем – объем воздуха, вдыхаемого и выдыхаемого при нормальном дыхании, в норме 300 – 900 мл; резервный объем выдоха – объем воздуха, который человек может выдохнуть, если после нормального выдоха сделает максимальный выдох, равен 1500 – 2000 мл; резервный объем вдоха – объем воздуха, который человек может вдохнуть, если после обычного вдоха сделает максимальный вдох, равен 1500 – 2000 мл; жизненная емкость легких – равна сумме резервных вдоха и выдоха, примерно 3700 мл; остаточный объем – объем воздуха, остающегося в легких после максимального выдоха, равен 1000 – 1500 мл; общая ёмкость легких является суммой дыхательного, резервных и остаточного объемов 5000-6000 мл. Все эти объемы проверяются при помощи спирографии. Также проводят исследования интенсивности легочной вентиляции. Определяют следующие величины: минутный объем дыхания (примерно 5000 мл), максимальная вентиляция легких (предел дыхания), резерв дыхания (в норме он в 15 – 20 раз больше минутного объёма дыхания). Все эти пробы позволяют изучить состояние легочной вентиляции и её резервы, необходимость в которых может возникнуть при выполнении тяжелой физической работы или при заболевании органов дыхания.
Все эти объемы проверяются при помощи спирографии. Также проводят исследования интенсивности легочной вентиляции. Определяют следующие величины: минутный объем дыхания (примерно 5000 мл), максимальная вентиляция легких (предел дыхания), резерв дыхания (в норме он в 15 – 20 раз больше минутного объёма дыхания). Все эти пробы позволяют изучить состояние легочной вентиляции и её резервы, необходимость в которых может возникнуть при выполнении тяжелой физической работы или при заболевании органов дыхания.
Пробы на выявление явной или скрытой дыхательной недостаточности (определение кислородного дефицита и кислородного потребления).
Эргоспирография – метод, позволяющий определить количество работы, которое может совершить обследуемый без появления признаков дыхательной недостаточности. Исследование газов крови, определяют содержание кислорода в данном объеме, количество кислорода, которое может связать единица данной крови, процент насыщения кислородом крови, содержание оксида углерода (СО2). Ещё один важный метод – она предназначена для того, чтобы определить состав плевральной жидкости, это нужно для того, чтобы уточнить диагноз (микроскопическое исследование жидкости), а также её используют как лечебную процедуру: удаляют жидкость из плевральной полости и (при необходимости) вводят в полость лекарственные вещества (обычно антибиотики, ферменты)
Ещё один важный метод – она предназначена для того, чтобы определить состав плевральной жидкости, это нужно для того, чтобы уточнить диагноз (микроскопическое исследование жидкости), а также её используют как лечебную процедуру: удаляют жидкость из плевральной полости и (при необходимости) вводят в полость лекарственные вещества (обычно антибиотики, ферменты)
Лабораторные методы исследования.
Микроскопическое исследование мокроты, для определения ее состава, это может быть слизь, серозная жидкость, клетки крови и воздухоносных путей, простейшие, гельминты и их яйца.
Слизистая мокрота (вязкая, бесцветная) встречается при остром бронхите.
Серозная мокрота (бесцветная, жидкая, пенистая) бывает при отеке легких.
Слизисто-гнойная (желтая или зеленоватая, вязкая) может быть при хроническом бронхите, туберкулезе.
Чисто гнойная мокрота (однородная, полужидкая, зеленоватая) характерна для абсцесса легкого при его прорыве.
Кровянистая мокрота может состоять только из крови, обычно при легочных кровотечениях, или может быть смешанной, например, слизисто-гнойная с прожилками крови (при бронхоэктазах), серозно-кровянисая пенистая (при отеке легких), слизисто-кровянистая (при инфаркте легкого), гнойно-кровянистая (при гангрене легкого).
Затем проводится микроскопическое исследование мокроты для определения клеточного состава. Из других лабораторных методов проводят общий и биохимический анализ крови, общий анализ мочи.
Профилактика заболеваний органов дыхания
Главное – это ведение здорового образа жизни: отказ от вредных привычек (курение, алкоголь и прочие), регулярные занятия физической культурой, соблюдение режимов труда и отдыха, полноценный сон и другое. К профилактическим мерам относятся ежегодные медицинские осмотры, даже если ничего не беспокоит, необходимо сдавать общие анализы и обязательно проходить каждый год флюорографическое обследование.
При появлении симптомов необходимо обратиться к врачу, а не заниматься самолечением.
При уже имеющихся хронических заболевания (хронический бронхит, бронхиальная астма) стараться устранить аллергены из воздуха, тщательная санация очагов хронической инфекции и соблюдать назначения врача.
Соблюдение этих мер поможет избежать или во время выявить и своевременно начать лечение заболеваний или добиться стабильной ремиссии хронической патологии.
Болезни органов дыхания:
- Острые респираторные инфекции верхних дыхательных путей
- Грипп и пневмония
- Другие острые респираторные инфекции нижних дыхательных путей
- Другие болезни верхних дыхательных путей
- Хронические болезни нижних дыхательных путей
- Болезни легкого, вызванные внешними агентами
- Другие респираторные болезни, поражающие главным образом интерстициальную ткань
- Гнойные и некротические состояния нижних дыхательных путей
- Другие болезни плевры
- Другие болезни органов дыхания
Как увеличить объем легких?
Этот показатель особенно важен для тех, кто занимается спортом или вокалом. Рано или поздно такие люди замечают, что им просто не хватает дыхания на то, чтобы выполнить упражнение или «взять длинную ноту». Но, знать, как увеличить объем легких будет полезно всем людям, ведь этот показатель будет влиять и на самочувствие человека. Если вы чувствуете периодические головокружения при быстрой ходьбе или другом подобном занятии, или то, что воздуха по ощущениям «не хватает», то, возможно, дело в малом объеме легких.
Рано или поздно такие люди замечают, что им просто не хватает дыхания на то, чтобы выполнить упражнение или «взять длинную ноту». Но, знать, как увеличить объем легких будет полезно всем людям, ведь этот показатель будет влиять и на самочувствие человека. Если вы чувствуете периодические головокружения при быстрой ходьбе или другом подобном занятии, или то, что воздуха по ощущениям «не хватает», то, возможно, дело в малом объеме легких.
Как увеличить объем легких в домашних условиях?
Для начала можно попробовать заняться спортом. Только не все упражнения подойдут для выполнения поставленной задачи. Особенно эффективными будут следующие занятия:
- Приседания с отягощением.
- Отжимания.
Но все-таки, наиболее эффективны упражнения вне помещения:
- Плавание, особенно подводное.
- Бег, особенно на свежем воздухе.
- Катание на велосипеде.
Эти упражнения, если выполнять их регулярно помогут, как увеличить жизненный объем легких, так и достичь хорошей физической формы. Только запомните несколько правил. Во-первых, тренируйтесь не реже двух раз в неделю, во-вторых, обязательно устанавливайте тот уровень нагрузки, который будет для вас приемлем, то есть последние повторы упражнения или минуты бега или плавания должны переноситься нелегко. Тяжелое дыхание, небольшая дрожь и усталость в мышцах, вот на что надо ориентироваться. И, наконец, вдох при тренировке (кроме плавания, там надо руководствоваться советами тренера) должен совершаться только через нос, выдыхать можно и ртом.
Только запомните несколько правил. Во-первых, тренируйтесь не реже двух раз в неделю, во-вторых, обязательно устанавливайте тот уровень нагрузки, который будет для вас приемлем, то есть последние повторы упражнения или минуты бега или плавания должны переноситься нелегко. Тяжелое дыхание, небольшая дрожь и усталость в мышцах, вот на что надо ориентироваться. И, наконец, вдох при тренировке (кроме плавания, там надо руководствоваться советами тренера) должен совершаться только через нос, выдыхать можно и ртом.
Как увеличить объем легких с помощью шарика?
Существует и еще один способ, при помощи которого можно как увеличить объем легких, так и не тратить время на занятия спортом. Он отлично подойдет тем, кто по какой-то причине не может тренироваться. Потребуется всего лишь купить воздушные шарики и надувать их, только прекращайте заниматься этим при ощущении головокружения. Специалисты рекомендуют ежедневно уделять внимание этому упражнению, и уже через 2-3 недели можно будет увидеть первые результаты. Человек сможет надувать все больше шариков, что и будет сигнализировать об увеличении объема легких.
Человек сможет надувать все больше шариков, что и будет сигнализировать об увеличении объема легких.
Неважно, что именно выберете вы для себя, спорт, шарики, или совместите оба метода, главное, даже по достижении нужного результата не бросать занятия, иначе эффект может исчезнуть. Интенсивность тренировок можно снизить и до 1 раза в неделю, а вот прекращать их нельзя.
Лечение хронического ринита и гайморита, проблем с дыханием дыхательной гимнастикой по Стрельниковой
Дыхательная гимнастика по Стрельниковой известна далеко за пределами страны благодаря своей эффективности в лечении и профилактике многих заболеваний. Первоначально упражнения были разработаны для оперных певцов, вокалистов, в дальнейшем гимнастику стали внедрять в медицинскую практику.
Механизм воздействия
Гимнастика по Стрельниковой уникальна отсутствием аналогов в мире. Система дыхательных актов предусматривает необычный вдох носом наряду с активными движениями, сжимающими грудную клетку. В этом случае воздухом насыщаются даже глубинные отделы легких. Именно этим методом можно добиться абсолютного диафрагмального дыхания.
Эффективность гимнастики в лечении хронического ринита и гайморита связана с повышением объема поступающего кислорода. Чем лучше вентиляция органов дыхания, тем быстрее происходит восстановление и оздоровление эпителия.
Эффективность дыхательной гимнастики по Стрельниковой при лор-заболеваниях связывают с выравниванием процессов возбуждения и торможения в коре головного мозга, а также с положительным воздействием практики на нервно-регуляторные рычаги, управляющие процессом дыхания.
Гимнастические упражнения основаны на динамичных дыхательных актах с вовлечением движений рук, тела, ног. Для достижения результатов гимнастику по Стрельниковой следует выполнять регулярно и согласно инструкции. Следует учесть и возможные противопоказания, чтобы избежать негативных реакций.
Преимущества
Неоспоримыми преимуществами дыхательной гимнастики по Стрельниковой являются:
- отличное сочетание с другими упражнениями и спортивными занятиями;
- восстановление функции лор-органов;
- профилактика и лечение различных заболеваний;
- увеличение объема легких, что важно при деформации грудной клетки, после воспалительных процессов;
- доступность и легкость выполнения упражнений.
Многие клиницисты считают метод Стрельниковой парадоксальным. С одной стороны, грудная клетка находится в постоянном напряжении и сжатии. С другой, гимнастика не вызывает утомления, а вентиляция легких существенно возрастает.
Сам акт дыхания осуществляется во время движения. Именно это позволяет восстановить энергетический баланс организма, активизировать кровообращение в головном мозге и улучшить состояние при ряде неврологических нарушений.
Показания и противопоказания
Учитывая, что методика дыхания по Стрельниковой положительно воздействует практически на все обменные процессы в организме, на практике способ можно использовать для укрепления сосудов, улучшения кровоснабжения органов и систем. Гимнастика приносит особую пользу в период беременности, при сердечно-сосудистых патологиях, вегетососудистой дистонии.
Ограничения
Упражнения не выполняются при тяжелой форме тромбофлебита, органических патологиях внутренних органов и систем, высокой температуре.
Лечение
Выполнение упражнений не требует особых навыков, физической подготовки. Комплекс простой, включает вазомоторного ринита и хронического гайморита методом гимнастики Стрельниковой назначается только врачом с учетом противопоказаний. Курс лечения ‒ 7-14 дней ежедневно.
При облегчении самочувствия и купирования симптомов можно продолжить терапию несколько раз в неделю.такие элементы, как «ладошки», «насос», «погончики», «кошки», «ушки» и другие. Эти упражнения можно делать на работе, дома, в гостях и на даче.
Показать технику выполнения может лечащий врач или врач-физиотерапевт. В дальнейшем можно проводить тренировки в домашних условиях. Также освоить основной комплекс упражнений поможет видеозанятие.
Влияние увеличения объема легких при хронической обструктивной болезни легких на обструкцию верхних дыхательных путей во время сна
У пациентов с хронической обструктивной болезнью легких (ХОБЛ) наблюдается увеличение объема легких из-за ограничения потока воздуха на выдохе. Увеличение объема легких может повлиять на проходимость верхних дыхательных путей и компенсаторные реакции на ограничение инспираторного потока (IFL) во время сна. Мы предположили, что пациенты с ХОБЛ имеют менее гибкие дыхательные пути, обратно пропорциональные объему их легких, и что наличие ограничения потока выдыхаемого воздуха ограничивает реакции рабочего цикла для защиты вентиляции в присутствии ИФЛ.Мы включили 18 пациентов с ХОБЛ и 18 пациентов контрольной группы, сопоставимых по возрасту, индексу массы тела, полу и тяжести синдрома обструктивного апноэ во сне. Исследования сна, включая количественную оценку воздушного потока при различных уровнях назального давления, были проведены для определения механических свойств верхних дыхательных путей [критическое пассивное давление закрытия (Pcrit)] и для количественной оценки респираторных временных реакций на экспериментально индуцированный IFL. Пациенты с ХОБЛ имели более низкий пассивный Pcrit, чем их контрольная группа (ХОБЛ: -2,8 ± 0,9 см вод. Ст.; Контроль: -0.5 ± 0,5 см вод. Ст., P = 0,03), и наблюдалась обратная зависимость функциональной остаточной емкости испытуемого и пассивного Pcrit (увеличение функциональной остаточной емкости -1,7 см вод. Ст. / Л, r (2) = 0,27, P = 0,002). В ответ на IFL рабочий цикл вдоха увеличился больше (P = 0,03) у пациентов с ХОБЛ (от 0,40 до 0,54), чем в контрольной группе (от 0,41 до 0,51), и привел к заметному сокращению времени выдоха с 2,5 до 1,5 с (P <0,01). . Пациенты с ХОБЛ имеют менее гибкие дыхательные пути и большую, а не сокращенную компенсационную временную реакцию при обструкции верхних дыхательных путей.Хотя эти временные реакции могут снизить гиповентиляцию, они также могут увеличить риск развития динамической гиперинфляции из-за значительного сокращения времени выдоха.
Ключевые слова: ХОБЛ; ограничение инспираторного потока; объем легких; обструктивное апноэ сна; обструкция верхних дыхательных путей.
Влияние увеличения объема легких при хронической обструктивной болезни легких на обструкцию верхних дыхательных путей во время сна
J Appl Physiol (1985).2015 1 августа; 119 (3): 266–271.
, 1, 2 , 1 , 1 , 1 , 1 , 1 и 1Паоло Биселли
1 Центр расстройств сна Джонса Хопкинса, Подразделение отделения легочной медицины и реанимации, Центр астмы и аллергии Джонса Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Питер Р.Grossman
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Джейсон П. Киркнесс
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Сушил П. Патил
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Филип Л.Smith
1 Центр болезней сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Алан Р. Шварц
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Hartmut Schneider
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Автор, ответственный за переписку.Адрес для запросов на перепечатку и другой корреспонденции: Х. Шнайдер, Центр расстройств сна Джонса Хопкинса, Отделение легочной и интенсивной терапии, Центр астмы и аллергии Джонса Хопкинса, 5501 Hopkins Bayview Circle, Балтимор, Мэриленд 21224 (электронная почта: ude.imhj @ 3ienhcsh).Поступила в редакцию 29 мая 2014 г .; Принята к печати 31 мая 2015 г.
Авторские права © Американское физиологическое общество, 2015 г. Эта статья цитируется в других статьях PMC.Abstract
У пациентов с хронической обструктивной болезнью легких (ХОБЛ) наблюдается увеличение объема легких из-за ограничения потока воздуха на выдохе.Увеличение объема легких может повлиять на проходимость верхних дыхательных путей и компенсаторные реакции на ограничение инспираторного потока (IFL) во время сна. Мы предположили, что пациенты с ХОБЛ имеют менее гибкие дыхательные пути, обратно пропорциональные объему их легких, и что наличие ограничения потока выдыхаемого воздуха ограничивает реакции рабочего цикла для защиты вентиляции в присутствии ИФЛ. Мы включили 18 пациентов с ХОБЛ и 18 пациентов контрольной группы, сопоставимых по возрасту, индексу массы тела, полу и тяжести синдрома обструктивного апноэ во сне.Исследования сна, включая количественную оценку воздушного потока при различных уровнях назального давления, были проведены для определения механических свойств верхних дыхательных путей [критическое пассивное давление закрытия (Pcrit)] и для количественной оценки респираторных временных реакций на экспериментально индуцированный IFL. Пациенты с ХОБЛ имели более низкий пассивный Pcrit, чем их контрольная группа (ХОБЛ: -2,8 ± 0,9 см вод.ст. 2 O; контроль: -0,5 ± 0,5 см вод. функциональная остаточная емкость и пассивный Pcrit (−1.7 cmH 2 O / l увеличение функциональной остаточной емкости, r 2 = 0,27, P = 0,002). В ответ на IFL рабочий цикл вдоха увеличился больше ( P = 0,03) у пациентов с ХОБЛ (от 0,40 до 0,54), чем в контроле (от 0,41 до 0,51), и привел к заметному сокращению времени выдоха с 2,5 до 1,5 с ( P <0,01). Пациенты с ХОБЛ имеют менее гибкие дыхательные пути и большую, а не сокращенную компенсационную временную реакцию при обструкции верхних дыхательных путей.Хотя эти временные реакции могут снизить гиповентиляцию, они также могут увеличить риск развития динамической гиперинфляции из-за значительного сокращения времени выдоха.
Ключевые слова: обструкция верхних дыхательных путей, ХОБЛ, обструктивное апноэ во сне, ограничение потока вдоха, объем легких
Хроническая обструктивная болезнь легких (ХОБЛ) является ведущей причиной смерти, инвалидности и снижения качества жизни. Одышка при физической нагрузке остается основной причиной ухудшения качества жизни, а нарушение сна и утренняя усталость являются вторыми по частоте жалобами у этих пациентов (3, 18).В то время как обструктивное апноэ во сне (СОАС) является общепризнанным источником нарушений сна и утренней усталости у пациентов с ХОБЛ, другие маркеры ХОБЛ, такие как гиперинфляция легких (20), усиление дыхательных усилий (9, 12, 26), изменения в газообмен (6, 15, 21, 27, 34) и ограничение потока вдоха также были связаны с нарушениями сна. Понимание того, как эти факторы вызывают нарушения сна, может позволить исследователям разработать конкретные стратегии профилактики и лечения нарушений сна у пациентов с ХОБЛ.
Ограничение потока вдоха является признаком обструкции верхних дыхательных путей, которая возникает у людей с нарушенными механическими свойствами верхних дыхательных путей (10, 25). Механические свойства верхних дыхательных путей лучше всего количественно оценить, определив критическое давление закрытия (Pcrit) во время пассивного состояния нервной системы (пассивное Pcrit) (19, 25). Наша лаборатория недавно показала, что пассивный Pcrit предсказывает восприимчивость к заболеванию апноэ во сне и возрастает с увеличением индекса массы тела (ИМТ) и возраста (19).Более того, наша и другие лаборатории недавно продемонстрировали, что увеличение объема легких снижает пассивный Pcrit у нормальных людей и у пациентов с апноэ во сне (23, 31, 32). Эффект увеличения объема легких у пациентов с ХОБЛ на механические свойства верхних дыхательных путей не был продемонстрирован.
Обструкция верхних дыхательных путей вызывает компенсаторные реакции, которые помогают предотвратить гиповентиляцию. В частности, рабочий цикл вдоха [отношение времени вдоха (Ti) к длине дыхательного цикла] увеличивается в ответ на обструкцию верхних дыхательных путей, и это повышение Ti происходит за счет времени выдоха (Te) (5, 14, 28) .Однако пациенты с ХОБЛ часто демонстрируют длинное Те, чтобы справиться с ограничением потока выдоха и внутренним положительным давлением в конце выдоха (11, 13). Возможно, что наличие ограничения потока выдоха ухудшает реакцию рабочего цикла на обструкцию верхних дыхательных путей у пациентов с ХОБЛ. В настоящем исследовании мы набрали пациентов с ХОБЛ и сопоставили ИМТ, возраст, пол и индекс апноэ и гипопноэ (AHI), чтобы определить 1 ) пассивный Pcrit и 2 ) респираторный временной ответ на экспериментально индуцированную обструкцию верхних дыхательных путей.Мы предполагаем, что 1 ) пациенты с ХОБЛ имеют более низкий пассивный Pcrit (и, следовательно, более низкий риск обструкции верхних дыхательных путей) в сочетании с увеличением объема легких; и что 2 ) компенсаторные временные реакции на обструкцию верхних дыхательных путей снижены у пациентов с ХОБЛ по сравнению с нормальными людьми; и 3 ), что уменьшение временных реакций пропорционально степени ограничения потока выдоха [объем форсированного выдоха за 1 с (FEV 1 )].
МЕТОДЫ
Субъекты
Субъекты были набраны из группы лиц, участвовавших в испытании, изучающем влияние сна на исходы ХОБЛ. В общей сложности 96 пациентов с ХОБЛ и 41 курильщик, не страдающий ХОБЛ, прошли предыдущее исследование сна и были доступны для нашего исследования. Из этой группы было набрано 36 человек (). И мужчины ( n = 12), и женщины ( n = 6), которым был поставлен диагноз ХОБЛ [FEV 1 / форсированная жизненная емкость легких (FVC) <70%], были индивидуально сопоставлены по возрасту, полу, ИМТ и ИАГ. с восемнадцатью субъектами без ХОБЛ.Кроме того, анализ подгруппы был проведен на 12 пациентах с ХОБЛ и 12 контрольной группе, сопоставимых по их механическим свойствам верхних дыхательных путей (пассивный Pcrit) и ИМТ. Исключались пациенты, принимавшие респираторные депрессанты, седативные средства или пероральные стероиды. Субъектов также обследовали на наличие нестабильных сердечно-сосудистых заболеваний, неконтролируемой гипертензии, недавних операций на ротоглотке, неврологических расстройств, почечной и печеночной недостаточности, текущей беременности, нарушений свертываемости крови, психических проблем, среднего состояния покоя O 2 , насыщения гемоглобина <88% и аллергии на лидокаин.Письменное информированное согласие было получено от каждого участника этого исследования, которое было одобрено Наблюдательным советом по исследованиям в области человека Медицинского института Джонса Хопкинса.
Таблица 1.
| Переменная | Контроли | Пациенты с ХОБЛ | P Значение | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| n | 18 | 1816 | 9016 9016 9016 9016|||||||||
| Возраст, лет | 50.3 ± 1,6 | 57,1 ± 1,9 | <0,05 | ||||||||
| Высота, см | 170,0 ± 2,7 | 174,2 ± 2,1 | НС | ||||||||
| Масса, кг | 97,9 ± 6,6 86,5 | 4,1NS | |||||||||
| BMI, кг / м 2 | 31,6 ± 1,6 | 28,6 ± 1,2 | NS | ||||||||
| Пол | 12M; 6 Ф | 12М; 6 F | NS | ||||||||
| Объем легких | |||||||||||
| FEV 1 , литры | 3.1 ± 0,2 | 1,9 ± 0,2 | <0,05 | ||||||||
| ОФВ 1 / ФЖЕЛ,% | 79 ± 1,2 | 54 ± 2,6 | <0,05 | ||||||||
| TLC, литры | 5 | 6,7 ± 0,2 | <0,05 | ||||||||
| RV, литры | 1,9 ± 0,1 | 3,0 ± 0,2 | <0,05 | ||||||||
| FRC, литры | 2,8 ± 0,2 | 4,0 ± 0,2 0.05 | |||||||||
| RV / TLC,% | 33,8 ± 1,8 | 45,5 ± 2,4 | <0,05 | ||||||||
| Полисомнография | мин. ± 15,9 | NS | |||||||||
| Эффективность сна,% TST | 86,9 ± 2,0 | 79,4 ± 3,0 | <0,05 | ||||||||
| NREM,% TST | 84,7 ± 1,5 | 83.9 ± 1,9 | NS | ||||||||
| 1-й этап | 19,2 ± 2,4 | 27,1 ± 5,2 | NS | ||||||||
| 2-й этап | 60,2 ± 2,5 | 50,8 ± 4,3 | NS | 5,2 ± 1,8 | 6,0 ± 2,3 | NS | |||||
| REM,% TST | 15,3 ± 1,5 | 16,1 ± 1,9 | NS | ||||||||
| Всего AHI, событий / ч 28 | 9 ± 8,1 | 28,9 ± 8,6 | NS | ||||||||
| NREM AHI, событий / ч | 27,8 ± 8,1 | 28,2 ± 8,6 | NS | ||||||||
| REM AHI, событий165 | 733,3 ± 10,0 | NS | |||||||||
| % Гипопноэ NREM | 76,9 ± 6,1 | 75,9 ± 6,7 | NS | ||||||||
| % Гипопноэ REM | 7316 ± 7.3 | Артериальная Sa O 2 ,% | |||||||||
| Среднее базовое значение | 96.4 ± 0,4 | 93,9 ± 0,5 | <0,05 | ||||||||
| Среднее низкое значение | 91,5 ± 0,7 | 90,2 ± 0,6 | NS |
Экспериментальные методы
Тестирование функции легких.
Стандартные методы исследования функции легких (CPL Lung Function Analyzer; W.E. Collins, Braintree MA.) Были применены на следующее утро после диагностического исследования сна (2). ОФВ 1 и ФЖЕЛ определяли с помощью спирометрии.Функциональная остаточная емкость (FRC) измерялась с использованием разведения гелия в замкнутом контуре с несколькими вдохами, с медленной жизненной емкостью и резервным объемом выдоха, определяемыми в конце процедуры. Остаточный объем (RV) рассчитывали путем вычитания резервного объема выдоха из FRC. Затем можно определить общую емкость легких, добавив к ПЖ медленную жизненную емкость легких.
Полисомнография.
Стандартные диагностические методы использовались для определения исходных характеристик сна. Для контроля сна и слежения за сном электроды электроэнцефалографа помещали в точки F3-A2, C3-A2 и O1-A2, в дополнение к электродам электромиограммы под подбородком и левому и правому электродам электрокулограммы.Респираторные события оценивались с использованием импедансных торакоабдоминальных ремней для измерения дыхательного усилия, назальная канюля использовалась для количественного определения воздушного потока, а пульсоксиметрия использовалась для мониторинга насыщения гемоглобина кислородом. Апноэ определяли как остановку дыхания на 10 с, в то время как гипопноэ оценивали, когда снижение потока воздуха на 30% сопровождалось десатурацией кислорода ≥4%. Стандартные полисомнографические методы и правила оценки использовались для определения стадии сна и классификации нарушений дыхания во сне в соответствии с рекомендованными в 2007 г. руководящими принципами оценки, установленными Американской академией медицины сна (1).
Установка физиологии дыхания.
В дополнение к стандартным методам полисомнографии, субъект был снабжен гелевой маской, прикрепленной к специально разработанному устройству постоянного положительного давления в дыхательных путях, способному обеспечивать давление от -20 до +20 см вод. Ст. 2 O (Resmed, Bella Vista, NSW, Австралия). Расход воздуха измеряли с помощью пневмотахографа (модель 4830, 0-400 л / мин; Ханс Рудольф, Канзас-Сити, Миссури). Расход и давление регистрировались с частотой дискретизации 100 Гц. Все физиологические сигналы регистрировались и контролировались на компьютерной станции с использованием программного обеспечения Somnologica (Medcare, Buffalo, NY).
Протокол исследования
Первоначально испытуемые прошли диагностическое исследование сна для определения степени нарушения дыхания во сне, которое требовалось для сопоставления людей по AHI и антропометрическим данным (см.). Кроме того, на следующий день после исследования сна проводились функциональные тесты легких для определения общего объема легких и статуса заболевания. Затем мы выполнили последующее исследование сна в течение периода от 2 до 4 недель, чтобы определить механические свойства верхних дыхательных путей пациентов (пассивный Pcrit) и компенсаторные временные реакции на обструкцию верхних дыхательных путей.Процедуры определения Pcrit были подробно описаны ранее (24), проиллюстрированы и кратко описаны ниже.
Протокол эксперимента. Схематическая диаграмма экспериментальных протоколов ( вверху, ) и полисомнографических ответов ( внизу, ) во время сна с медленным движением глаз у мужчины с апноэ. Исходный уровень ( слева, ): назальное давление было отрегулировано до эффективного постоянного положительного давления в дыхательных путях и удерживалось не менее 3 минут (удерживающее давление) для установления стабильной модели дыхания без ограничения потока (см. График потока, внизу слева, ).Пассивная обструкция верхних дыхательных путей (, посередине слева, ): была проведена серия кратковременных (5 вдохов) падений назального давления в результате удержания давления без одновременной активации ЭМГ. Во время этих капель возникла обструкция верхних дыхательных путей, на что указывает ограничение потока вдоха, как показано на графике потока ниже. Sa O 2 , артериальный O 2 насыщение; Vi max , максимальный инспираторный поток.
Пассивное состояние: кратковременные периоды обструкции верхних дыхательных путей.
Мы использовали пассивный Pcrit для определения свойств верхних дыхательных путей при низкой гипотонической нервно-мышечной активности. Во время стабильного сна с медленным движением глаз назальное давление постепенно повышалось до тех пор, пока не было достигнуто носовое дыхание без ограничения потока. Затем назальное давление снижали ступенчато с шагом от 1 до 2 см вод. Падение давления будет прервано и повторено, если возникнет возбуждение или повышение активности ЭМГ без возбуждения.Периоды дыхания исключались, если были пробуждения от стабильного сна.
Сжимаемость верхних дыхательных путей.
Зависимость «давление-поток» (максимальный инспираторный поток в условиях ограниченного потока) была создана для каждого субъекта путем построения графика максимального воздушного потока из вдохов 3–5 каждого перепада давления, как описано ранее (30). Линейная регрессия использовалась для определения назального давления, при котором поток был нулевым, что указывает на закупорку верхних дыхательных путей (пассивный Pcrit), как показано на рис.
Ответы по времени дыхания.
Ti, Te, общее время каждого вдоха (Ttot) и частота дыхания были определены. Рабочий цикл вдоха (Ti / Tобщ) был зарегистрирован в условиях без ограничения потока, а также во время вдохов с острым умеренным или сильным ограничением потока, определяемым как средняя пиковая скорость потока воздуха на вдохе 50–150 мл / с () ( 28). Изменение временных параметров от исходного уровня до состояния обструкции верхних дыхательных путей использовалось для определения индивидуальной силы респираторных временных реакций на обструкцию верхних дыхательных путей.
Статистический анализ
Отдельные значения были усреднены и сравнены как для ХОБЛ, так и для контрольной группы с использованием непарного критерия Стьюдента t . Дальнейший анализ подгрупп проводился у пациентов с ОАС и без него. Изменения в ответе рабочего цикла сравнивали между группами пациентов с ХОБЛ и контрольной группой с помощью непарного t -теста. Сравнения до и после индукции ограничения инспираторного потока были выполнены с использованием парного теста t . Регрессионный анализ между FRC и пассивным Pcrit был выполнен для определения связи между объемом легких и сжимаемостью верхних дыхательных путей.Значение P 0,05 считалось статистически значимым. Все данные представлены как средние значения ± SE, если не указано иное.
РЕЗУЛЬТАТЫ
Характеристики субъектов
Демографические, антропометрические, полисомнографические и легочные статистические данные для всех 18 участников ХОБЛ и 18 контрольных групп, соответствующих AHI, отображаются в. Сравнение антропометрических переменных для субъектов, индивидуально подобранных по возрасту (57,1 ± 1,9 против 50,3 ± 1,6 года), полу (12 мужчин; 6 женщин), ИМТ (28.8 ± 1,3 против 31,6 ± 1,6 кг / м 2 ), и AHI (29 ± 8 против 29 ± 9 событий / ч) показаны на. У половины испытуемых (7 мужчин и 2 женщины из каждой группы) было нарушение дыхания во сне с частотой событий> 10 событий / час. Субъекты с ХОБЛ, по сравнению с контрольными субъектами, имели ОФВ 1 1,9 ± 0,2 против 3,1 ± 0,2 литра и ОФВ 1 / ФЖЕЛ 54 ± 0,0 против 79 ± 1,2%. Точно так же объемы легких были увеличены у пациентов с ХОБЛ по сравнению с контрольной группой: общая емкость легких составляла 6,7 ± 0,2 против 5,9 ± 0.3 литра, RV составляла 3,0 ± 0,2 против 1,9 ± 0,1 литра, а FRC составляла 4,0 ± 0,2 против 2,8 ± 0,2 литра.
Острые (пассивные) механические свойства верхних дыхательных путей
Субъекты с ХОБЛ имели средний пассивный Pcrit -2,8 см вод. t -тест;). Для подгруппы без ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -4,6 см вод.ст. 2 O по сравнению с -0,8 см вод.02; непарный т -тест). Для подгруппы с ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -1,0 см вод. Ст. 2 O по сравнению с -0,2 см вод. Была обнаружена значимая связь между FRC и пассивным Pcrit ( r 2 = 0,27, P = 0,002), как показано на рисунке, что указывает на то, что пациенты с более высокими объемами легких имели более низкие значения пассивного Pcrit.
Измерения пассивного критического давления закрытия (Pcrit) у пациентов с хронической обструктивной болезнью легких (ХОБЛ) и контрольной группы.График представляет средние значения пассивного Pcrit для пациентов с ХОБЛ и подобранной контрольной группы. Слева : все пациенты. Средний : пациенты с необструктивным апноэ сна (СОАС). Справа : пациенты с СОАС. Значения представляют собой средние значения ± SE. Коллапсируемость верхних дыхательных путей (пассивный Pcrit) ниже у пациентов с ХОБЛ по сравнению с субъектами, подобранными по возрасту, полу, индексу массы тела и индексу респираторных нарушений ( P = 0,03). Эта разница кажется более значительной у пациентов, не страдающих апноэ, но больше не заметна у пациентов с апноэ.NS, незначительно.
Пассивная зависимость Pcrit от функциональной остаточной емкости (FRC). График представляет пассивную зависимость Pcrit и FRC с линейной регрессией с использованием всех значений предмета. □, средства контроля, не относящиеся к OSA; ◇, органы управления OSA; ■ ХОБЛ без ОАС; ⧫ OSA ХОБЛ. Была статистически значимая связь между FRC и коллапсируемостью верхних дыхательных путей (пассивный Pcrit) у всех субъектов ( P = 0,002, r 2 = 0,27). Увеличение FRC на 1 литр было связано со снижением пассивного Pcrit на ~ 2 см вод. Ст.
При одномерном анализе была выявлена статистически значимая связь между значениями пассивного Pcrit и как FRC ( P = 0,002), так и ИМТ ( P = 0,003). В многомерном анализе оба фактора оставались определяющими для уровня пассивного Pcrit (FRC, P = 0,021; BMI, P = 0,041;).
Таблица 2.
Связь пассивного Pcrit с BMI и FRC
| Модель 1 | Модель 2 | Модель 3 | P значение | β-коэффициент | P значение | β-коэффициент | P Значение | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| FRC, см вод. Ст. 2 O / l | −1.66 ± 0,50 | 0,002 | −1,25 ± 0,51 | 0,021 | |||||||||||||
| ИМТ, кг / м 2 | 0,25 ± 0,08 | 9080,042 | |||||||||||||||
Острые респираторные временные ответы
В подгруппе из 12 пациентов, спаренных для анализа временных ответов, контрольная группа имела ИАГ 29,8 ± 7,5 событий / ч, а группа ХПК имела ИАГ 31.2 ± 6,8 событий / час. Среднее удерживающее давление составляло 8,8 ± 0,8 см вод. Ст. 2 O в контроле и 8,1 ± 1,0 см вод. Ст. 2 O у пациентов с ХОБЛ. Среднее дельта-давление, необходимое для серьезного ограничения потока вдоха, составляло 6,4 ± 0,8 см вод. Ст. 2 O для контроля и 7,0 ± 0,9 см вод.
Респираторные реакции по времени оценивались путем сравнения состояния без ограничения потока (исходный уровень) с периодами тяжелой обструкции верхних дыхательных путей. Пик инспираторного потока воздуха на исходном уровне и тяжелая обструкция верхних дыхательных путей были одинаковыми в обеих группах, снизившись с 383 ± 49 до 105 ± 11 мл / с в контроле и с 387 ± 47 до 111 ± 12 мл / с у пациентов с ХОБЛ.Параметры времени дыхания при исходном уровне, дыхании без ограничения потока и в ответ на серьезную степень ограничения потока вдоха суммированы в. Как в условиях без ограничения потока, так и в условиях с ограниченным потоком пациенты с ХОБЛ и контрольная группа имели одинаковые временные индексы. В то время как в контрольной группе увеличение рабочего цикла на ~ 25% с 0,41 до 0,51, у пациентов с ХОБЛ было увеличение на ~ 40% с 0,40 до 0,55 ( P = 0,03 для сравнения увеличения рабочего цикла). Те снизились в среднем с 2.От 5 до 1,5 с в группе ХОБЛ ( P <0,01) и в согласованном контроле от 2,4 до 1,8 с ( P <0,01). Ttot снизился при ХОБЛ с 4,1 до 3,3 с ( P <0,05) и в контроле с 3,9 до 3,6 с (незначительно). Ti увеличился с 1,5 до 1,8 с ( P <0,01) у пациентов с ХОБЛ и с 1,6 до 1,8 с в контроле ( P <0,05). Ни один из ответов по времени вдоха или выдоха не коррелировал с уровнем обструкции (FEV 1 ) у пациентов с ХОБЛ.
Таблица 3.
Временные реакции на индуцированное ограничение потока
| Время вдоха, с | Время выдоха, с | Общее время, с | Рабочий цикл, частота дыхания | 906 / мин||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Control | COPD | Control | COPD | Control | COPD | Control | COPD | Control Base | 9016 9016 ± 0,1| 1,5 ± 0,1 | 2,4 ± 0,2 | 2,5 ± 0,3 | 3,9 ± 0,2 | 4,1 ± 0,3 | 0,41 ± 0,02 | 0,40 ± 0,02 | 16,0 ± 0,9 | 15,5 ± 0,9 | | |
| IFL | 1,8 ± 0,1 * | 1,8 ± 0,1 * | 1,8 ± 0,2 * | 1,5 ± 0,1 * | 3,6 ± 0,3 | 3,3 ± 0,2 * | 0,51 ± 0,02 * | 0.55 ± 0,02 * † | 18,1 ± 1,6 | 18,9 ± 1,1 * | |||||||||
ОБСУЖДЕНИЕ
Основные результаты настоящего исследования заключаются в том, что пациенты с ХОБЛ имеют менее гибкие верхние дыхательные пути, чем их возраст. пол, ИМТ и AHI соответствовали контрольным субъектам, и что пассивный Pcrit обратно коррелировал с остаточным объемом легких. Проходимость дыхательных путей была увеличена у пациентов с ХОБЛ по сравнению с подобранной контрольной группой, но эта разница была намного меньше и несущественной в подгруппе пациентов с апноэ во сне, что указывает на то, что статус болезни апноэ во сне влияет на механизмы, которые опосредуют объем легких и пассивную взаимосвязь Pcrit.Во-вторых, в отличие от нашей гипотезы, пациенты с ХОБЛ продемонстрировали повышенную, а не пониженную реакцию рабочего цикла на обструкцию верхних дыхательных путей по сравнению с подобранной контрольной группой. Это увеличение рабочего цикла было связано с увеличением частоты дыхания и заметным снижением Те, которые являются известными факторами риска динамической гиперинфляции. Взятые вместе, наши данные показывают, что, хотя увеличение объема легких может снизить восприимчивость к OSA у пациентов с ХОБЛ, временные реакции на обструкцию верхних дыхательных путей могут способствовать динамической гиперинфляции.
Одним из основных клинических признаков ХОБЛ является прогрессирующее увеличение объема легких. У нашей популяции пациентов была умеренная степень ХОБЛ с FEV 1 / FVC в диапазоне от 50 до 70% от прогнозируемого и средним увеличением FRC на 1,2 литра по сравнению с контролем. Увеличение объема легких снижает разрушаемость верхних дыхательных путей у здоровых людей и пациентов с СОАС (23, 31, 32). Предлагаемый механизм этой связи — усиление тракции каудальной трахеи во время раздувания легких, в результате чего верхние дыхательные пути становятся более жесткими и менее гибкими (16).Теперь мы распространили эти результаты на пациентов с ХОБЛ с увеличенным объемом легких и обнаружили аналогичную взаимосвязь между FRC и верхней коллапсируемостью на ~ 2 см вод. Ст. 2 O снижение пассивного Pcrit на увеличение FRC на литр. Более низкий пассивный Pcrit связан с меньшим риском развития ОАС. Таким образом, оказывается, что пациенты с ХОБЛ с увеличенным объемом легких менее подвержены развитию ОАС.
Мы наблюдали более низкий пассивный Pcrit у пациентов с ХОБЛ, не страдающих апноэ, по сравнению с их сопоставимой группой контроля без апноэ.Можно предположить, что это различие связано с аномально высоким пассивным Pcrit в контрольной группе, а не со снижением пассивного Pcrit в группе ХОБЛ. Наша лаборатория ранее продемонстрировала, что пассивный Pcrit может быть одинаковым у лиц без OSA и OSA, в то время как активный Pcrit ниже у здоровых людей по сравнению с пациентами с апноэ, даже при сопоставлении с пассивным Pcrit (19, 25). Пассивный Pcrit выявляет механические свойства дыхательных путей в ненейронно активированном состоянии и приближается к измерениям Pcrit под анестезией.Фактически, некоторые отчеты во время анестезии также показали значения Pcrit, близкие к атмосферным, особенно при изучении пациентов старшего возраста (7, 8). Таким образом, мы предполагаем, что разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и контрольной группой не связана с аномально высоким Pcrit в нормальном контроле, а, скорее, из-за снижения пассивного Pcrit у пациентов с неапнеическим ХОБЛ.
Хотя имелась разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и их контрольной группой, мы больше не наблюдали этой разницы при сравнении пациентов с апноэ с ХОБЛ и их контрольной группы.Мы предлагаем несколько механизмов для объяснения этой дифференциальной реакции. Во-первых, несколько исследователей продемонстрировали, что пассивный Pcrit снижается с увеличением объема легких, что связано с каудальным трактом верхних дыхательных путей (31, 33, 35). Люди с апноэ имеют более крупный язык (29) и часто узкое, высоко дугообразное твердое небо (17), оба из которых могли притупить эффект растяжения, обеспечиваемый увеличением объема легких. Во-вторых, также возможно, что увеличение объема легких снижает пассивный Pcrit за счет нервной стимуляции внутри- или внелегочных рецепторов растяжения.Люди с апноэ могут иметь ослабленную нервную реакцию на увеличение объема легких, аналогичную ослаблению нервного контроля над верхними дыхательными путями в ответ на обструкцию верхних дыхательных путей (22, 25). В качестве альтернативы, подобно рефлексу Геринга-Брейера, который требует больших объемов вдоха для вызова рефлекторного ответа, пассивные ответы Pcrit также могут зависеть от степени гиперинфляции. У некоторых пациентов с апноэ с ХОБЛ увеличение объема легких могло быть недостаточно большим для снижения пассивного Pcrit.Чтобы определить, почему пациенты с неапноэ с ХОБЛ имеют более низкий пассивный Pcrit по сравнению с контрольной группой, в то время как пациенты с апноэ с ХОБЛ имеют такой же пассивный Pcrit, чем пациенты с апноэ, необходимы механические эксперименты, включающие оценку нервной и мышечной активности.
При обструкции верхних дыхательных путей увеличение рабочего цикла является одним из основных способов поддержания вентиляции. Чем больше увеличение рабочего цикла, тем лучше люди поддерживают минутную вентиляцию (5, 28, 36).В нашей настоящей работе мы наблюдали, что пациенты с ХОБЛ, по сравнению с подобранной контрольной группой, имеют большее увеличение рабочего цикла при обструкции верхних дыхательных путей. Таким образом, пациенты с ХОБЛ, по-видимому, лучше защищены от развития гиповентиляции по сравнению с контрольной группой, когда сталкиваются с обструкцией верхних дыхательных путей. Напротив, пациенты с ХОБЛ нуждаются в очень длительном Те, чтобы предотвратить динамическую гиперинфляцию легких. В настоящей работе мы наблюдали, что пациенты с ХОБЛ, а также контрольная группа, снижали Те при ограничении инспираторного потока.Хотя умеренное снижение Те обычно не влияет на механику дыхания, наблюдаемого снижения Те на ~ 50% может быть достаточно, чтобы вызвать динамическую гиперинфляцию. Фактически, подобное снижение Те при использовании метронома во время бодрствования вызывало динамическую гиперинфляцию у пациентов с умеренной ХОБЛ (4). Субъекты с нормальной функцией легких могут хорошо переносить снижение Те. Однако у субъектов с ограничением потока вдоха при ХОБЛ наблюдаемое снижение Те может вызывать динамическую гиперинфляцию во время сна.
У настоящего исследования есть несколько сильных сторон и ограничений. Первым преимуществом является наш подход к сопоставлению пациентов с ХОБЛ и контрольной группы по возрасту, тяжести апноэ во сне (AHI), полу и ИМТ, которые являются известными факторами риска разрушения верхних дыхательных путей. Когда мы проанализировали только пациентов без ОАС, различия в разборчивости верхних дыхательных путей были даже больше, чем при сравнении всей группы, что позволяет предположить, что мы, возможно, недооценили влияние повышенного объема легких на проходимость верхних дыхательных путей.Вторая сильная сторона — это наш экспериментальный план для определения временных параметров в ответ на обструкцию верхних дыхательных путей. В предыдущих исследованиях наша лаборатория продемонстрировала, что рабочий цикл увеличивается с тяжестью обструкции верхних дыхательных путей в зависимости от дозы. Поэтому мы установили одинаковую степень обструкции верхних дыхательных путей для всех участников нашего исследования. Этот экспериментальный план позволил нам уменьшить вариабельность временных ответов, наблюдая при этом дифференциальные ответы между пациентами с ХОБЛ и контрольной группой.Напротив, несмотря на лучшее соответствие пациентов с ХОБЛ и контрольной группы по статусу заболевания (AHI), возрасту и полу, у нас есть только перекрестные данные по пассивному Pcrit для участников нашего исследования. Возможно, мы недооценили влияние объема легких на сжимаемость верхних дыхательных путей из-за систематической ошибки отбора. Мы также не измеряли внутреннее положительное давление в конце выдоха, которое, вероятно, присутствует у многих наших пациентов с ХОБЛ и может быть изменено экспериментально вызванным ограничением потока.Мы признаем, что наши пациенты с ХОБЛ были значительно старше контрольной группы. Увеличение возраста связано либо с отсутствием изменений, либо с увеличением пассивного Pcrit (19). Поэтому мы считаем, что разница в возрасте не может объяснить более низкий пассивный Pcrit в группе ХОБЛ. Наконец, возможно, что мы не достигли аналогичной нервно-мышечной пассивности у контрольных пациентов с апноэ и пациентов с ХОБЛ с апноэ. Пациенты с ХОБЛ имеют более высокие респираторные нагрузки и, как следствие, более высокие усилия, что может привести к более сильному неврологическому воздействию как на дыхательные мышцы, так и на мышцы верхних дыхательных путей.Хотя пассивные измерения Pcrit предназначены для описания свойств дыхательных путей в пассивном состоянии, мы не можем исключить, что некоторые из наблюдаемых различий в верхних дыхательных путях отражают различные состояния активации мышц верхних дыхательных путей.
Значение
Настоящая работа имеет несколько клинических последствий. Во-первых, мы показываем, что увеличение объема легких связано с более низким Pcrit (пассивным Pcrit) верхних дыхательных путей. Аналогичным образом, изменения объема легких также могут влиять на пассивный Pcrit у пациентов с ХОБЛ.Операция по уменьшению объема легких (LVRS) — одна из стратегий лечения тяжелой ХОБЛ. Если LVRS повысит пассивный Pcrit, эффективность лечения LVRS может снизиться из-за возникновения OSA. Во-вторых, у пациентов с ХОБЛ короткие периоды тяжелой обструкции верхних дыхательных путей вызывали заметное снижение Те до уровней, сопоставимых с результатами предыдущих исследований, изучающих источники динамической гиперинфляции. Известно, что динамическая гиперинфляция увеличивает работу дыхания и снижает эффективность сна, что может быть связано с утренней усталостью, обычно наблюдаемой у пациентов с ХОБЛ.
ГРАНТЫ
Это исследование финансировалось Национальным институтом сердца, легких и крови, грант RO1-HL-105546 и Conselho Nacional de Desenvolvimento Científico e Tecnológico-Brasil.
РАСКРЫТИЕ ИНФОРМАЦИИ
Автор (ы) не заявляет о конфликте интересов, финансовом или ином.
ВЗНОС АВТОРОВ
Вклад авторов: P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. проанализированные данные; P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. интерпретированные результаты экспериментов; P.J.C.B., P.R.G. и H.S. подготовленные фигурки; P.J.C.B., P.R.G., A.R.S. и H.S. составленная рукопись; P.J.C.B., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. отредактированная и исправленная рукопись; P.J.C.B. и H.S. утвержденная финальная версия рукописи; P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. концепция и дизайн исследования; P.R.G., J.P.K. и H.S. проводил эксперименты.
СПИСОК ЛИТЕРАТУРЫ
1. Американская академия медицины сна. Руководство AASM по оценке сна и связанных с ним событий: правила, терминология и технические спецификации.Вестчестер, Иллинойс: Американская академия медицины сна, 2007. [Google Scholar] 2. Американское торакальное общество. Стандартизация спирометрии, обновление 1994 г. Американское торакальное общество. Am J Respir Crit Care Med 152: 1107–1136, 1995. [PubMed] [Google Scholar] 3. Бреслин Э, ван дер Сханс С., Бреукинк С., Мик П., Мерсер К., Фольц В., Луи С. Восприятие утомляемости и качества жизни у пациентов с ХОБЛ. Грудь 114: 958–964, 1998. [PubMed] [Google Scholar] 4. Каллигаро Г.Л., Рейн Р.И., Бейтман М.Э., Бейтман Э.Д., Купер С.Б.Сравнение динамической гиперинфляции и связанной с ней одышки, вызванной тахипноэ в метрономном ритме, с дополнительными упражнениями. ХОБЛ 11: 105–112, 2014. [PubMed] [Google Scholar] 5. Чин Ч., Киркнесс JP, Патил С.П., Макгинли Б.М., Смит П.Л., Шварц А.Р., Шнайдер Х. Компенсаторные реакции на обструкцию верхних дыхательных путей у мужчин и женщин с ожирением и апноэ. J Appl Physiol 112: 403–410, 2012. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Дуглас, штат Нью-Джерси, Calverley PMA, Leggett RJE, Brash DC, Flenley DC, Brezinova V. Преходящая гипоксемия во сне при хроническом бронхите и эмфиземе.Ланцет 1: 1–4, 1979. [PubMed] [Google Scholar] 7. Иствуд ПР, Платт ПР, Шеперд К., Мэддисон К., Хиллман ДР. Складываемость верхних дыхательных путей при различных концентрациях анестезии пропофолом. Анестезиология 103: 470–477, 2005. [PubMed] [Google Scholar] 8. Eastwood PR, Szollosi I, Platt PR, Hillman DR. Сравнение коллапса верхних дыхательных путей во время наркоза и сна. Ланцет 359: 1207–1209, 2002. [PubMed] [Google Scholar] 9. Gold AR, Gold MS, Харрис К.В., Эспелета В.Дж., Амин М.М., Бродерик Дж.Гиперсонливость, бессонница и патофизиология синдрома сопротивления верхних дыхательных путей. Сон Мед 9: 675–683, 2008. [PubMed] [Google Scholar] 10. Золото AR, Schwartz AR. Критическое давление в глотке. Почему и как использовать назальное постоянное положительное давление в дыхательных путях для диагностики. Грудь 110: 1077–1088, 1996. [PubMed] [Google Scholar] 11. Gorini M, Misuri G, Corrado A, Duranti R, Iandelli I, De Paola E, Scano G. Характер дыхания и задержка углекислого газа при тяжелой хронической обструктивной болезни легких.Грудная клетка 51: 677–683, 1996. [Бесплатная статья PMC] [PubMed] [Google Scholar] 12. Гийемино C, Stoohs R, Clerk A, Cetel M, Maistros P. Причина чрезмерной дневной сонливости. Синдром сопротивления верхних дыхательных путей. Грудь 104: 781–787, 1993. [PubMed] [Google Scholar] 13. Haluszka J, Chartrand DA, Grassino AE, Milic-Emili J. Внутренний ПДКВ и артериальный Pco 2 у стабильных пациентов с хронической обструктивной болезнью легких. Am Rev Respir Dis 141: 1194–1197, 1990. [PubMed] [Google Scholar] 14. Хосино Ю., Аюс Т., Курата С., Аюс Т., Шнайдер Х., Киркнесс Дж. П., Патил С.П., Шварц А.Р., Ои К.Компенсаторные реакции на обструкцию верхних дыхательных путей у здоровых людей под анестезией пропофолом. Респир Физиол Нейробиол 166: 24–31, 2009. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Хаджел Д.В., Мартин Р.Дж., Кейпхарт М., Джонсон Б., Хилл П. Вклад гиповентиляции в десатурацию кислорода во сне при хронической обструктивной болезни легких. J Appl Physiol 55: 669–677, 1983. [PubMed] [Google Scholar] 16. Кайрайтис К., Байт К., Парих Р., Ставрину Р., Уитли Дж. Р., Эмис Т.К. Влияние тракции трахеи на проходимость верхних дыхательных путей у кроликов: роль тканевого давления.Спать 30: 179–186, 2007. [PubMed] [Google Scholar] 17. Ким Дж. Х., Гийемино К. Назомаксиллярный комплекс, нижняя челюсть и нарушение дыхания во сне. Сон Дыхание 15: 185–193, 2011. [PubMed] [Google Scholar] 18. Kinsman RA, Yaroush RA, Fernandez E, Dirks JF, Schocket M, Fukuhara J. Симптомы и переживания при хроническом бронхите и эмфиземе. Грудь 83: 755–761, 1983. [PubMed] [Google Scholar] 19. Киркнесс Дж. П., Шварц А. Р., Шнайдер Х., Пенджаби Н. М., Малый Дж. Дж., Лаффан А. М., МакГинли Б. М., Магнусон Т., Швейцер М., Смит П. Л., Патил С. П..Вклад мужского пола, возраста и ожирения в механическую нестабильность верхних дыхательных путей во время сна. J Appl Physiol 104: 1618–1624, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Krachman SL, Chatila W., Martin UJ, Nugent T, Crocetti J, Gaughan J, Criner GJ. Влияние операции по уменьшению объема легких на качество сна и ночной газообмен у пациентов с тяжелой эмфиземой. Грудь 128: 3221–3228, 2005. [PubMed] [Google Scholar] 21. Leitch AG, Gloney LJ, Leggett RJE. Напряжение газов артериальной крови, ион водорода и электроэнцефалограмма во время сна у пациентов с хронической дыхательной недостаточностью.Грудная клетка 31: 730–735, 1976. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Макгинли Б.М., Шварц А.Р., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Патил С.П. Нервно-мышечная компенсация верхних дыхательных путей во время сна нарушается при обструктивном апноэ во сне. J Appl Physiol 105: 197–205, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Оуэнс Р.Л., Малхотра А., Эккерт Д.Д., Уайт Д.П., Джордан А.С. Влияние объема легких в конце выдоха на измерения гибкости глотки. J Appl Physiol 108: 455–451, 2010.[Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Патил С.П., Пенджаби Н.М., Шнайдер Х., О’Доннелл С.П., Смит П.Л., Шварц А.Р. Упрощенный метод измерения критического давления во время сна в клинических условиях. Am J Respir Crit Care Med 170: 86–93, 2004. [PubMed] [Google Scholar] 25. Патил С.П., Шнайдер Х., Маркс Дж.Дж., Гладмон Э., Шварц А.Р., Смит П.Л. Нейромеханический контроль проходимости верхних дыхательных путей во время сна. J Appl Physiol 102: 547–556, 2007. [PubMed] [Google Scholar] 26. Полномочия CR, Frey WC. Поддержание теста на бодрствование у военнослужащих с синдромом сопротивления верхних дыхательных путей и легким или умеренным апноэ во сне.Сон Дыхание 13: 253–258, 2009. [PubMed] [Google Scholar] 27. Сандерс MH, Ньюман AB, Haggerty CL, Redline S, Lebowitz M, Samet J, O’Connor GT, Punjabi NM, Shahar E. Сон и нарушение дыхания во сне у взрослых с преимущественно легкой формой обструктивного заболевания дыхательных путей. Am J Respir Crit Care Med 167: 7–14, 2003. [PubMed] [Google Scholar] 28. Шнайдер Х., Кришнан В., Пичард Л. Е., Патил С. П., Смит П. Л., Шварц А. Р.. Ответная реакция рабочего цикла вдоха на ограничение потока предсказывает ночную гиповентиляцию. Eur Respir J 33: 1068–1076, 2009.[PubMed] [Google Scholar] 29. Шваб Р.Дж., Пасирштейн М., Пирсон Р., Макли А., Хачадориан Р., Аренс Р., Мэйслин Г., Пак А.И. Выявление анатомических факторов риска обструктивного апноэ во сне верхних дыхательных путей с помощью объемной магнитно-резонансной томографии. Am J Respir Crit Care Med 168: 522–530, 2003. [PubMed] [Google Scholar] 30. Шварц А.Р., О’Доннел С.П., Барон Дж., Шуберт Н., Алам Д., Самади С.Д., Смит П.Л. Гипотонические верхние дыхательные пути при обструктивном апноэ во сне. Роль структур и нервно-мышечной деятельности.Am J Respir Crit Care Med 157: 1051–1057, 1998. [PubMed] [Google Scholar] 31. Сквайер С.Б., Патил С.П., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Шварц А.Р. Влияние объема легких в конце выдоха на сжимаемость верхних дыхательных путей у спящих мужчин и женщин. J Appl Physiol 109: 977–985, 2010. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Тагайто Ю., Исоно С., Реммерс Дж. Э., Танака А., Нишино Т. Объем легких и сжатие пассивной глотки у пациентов с нарушением дыхания во сне. J Appl Physiol 103: 1379–1385, 2007.[PubMed] [Google Scholar] 33. Тут Д.К., Шварц А.Р., Роуч Д., Мудрый Р.А., Пермутт С., Смит П.Л. Положение трахеи и шеи влияет на динамику воздушного потока в верхних дыхательных путях, изменяя длину дыхательных путей. J Appl Physiol 75: 2084–2090, 1993. [PubMed] [Google Scholar] 34. Траск CH, Gress EM. Оксиметрические исследования пациентов с хронической эмфиземой легких, бодрствования и сна. N Engl J Med 266: 639–642, 1962. [PubMed] [Google Scholar] 35. Ван де Грааф ВБ. Торакальное вытяжение за трахею: механизмы и масштабы. J Appl Physiol 70: 1328–1336, 1991.[PubMed] [Google Scholar] 36. Юнес М. Роль механизмов контроля дыхания в патогенезе обструктивных нарушений сна. J Appl Physiol 105: 1389–1405, 2008. [PubMed] [Google Scholar]Влияние увеличения объема легких при хронической обструктивной болезни легких на обструкцию верхних дыхательных путей во время сна
J Appl Physiol (1985). 2015 1 августа; 119 (3): 266–271.
, 1, 2 , 1 , 1 , 1 , 1 , 1 и 1Паоло Биселли
1 Центр расстройств сна Джонса Хопкинса, Подразделение отделения легочной медицины и реанимации, Центр астмы и аллергии Джонса Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Питер Р.Grossman
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Джейсон П. Киркнесс
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Сушил П. Патил
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Филип Л.Smith
1 Центр болезней сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Алан Р. Шварц
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Hartmut Schneider
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Автор, ответственный за переписку.Адрес для запросов на перепечатку и другой корреспонденции: Х. Шнайдер, Центр расстройств сна Джонса Хопкинса, Отделение легочной и интенсивной терапии, Центр астмы и аллергии Джонса Хопкинса, 5501 Hopkins Bayview Circle, Балтимор, Мэриленд 21224 (электронная почта: ude.imhj @ 3ienhcsh).Поступила в редакцию 29 мая 2014 г .; Принята к печати 31 мая 2015 г.
Авторские права © Американское физиологическое общество, 2015 г. Эта статья цитируется в других статьях PMC.Abstract
У пациентов с хронической обструктивной болезнью легких (ХОБЛ) наблюдается увеличение объема легких из-за ограничения потока воздуха на выдохе.Увеличение объема легких может повлиять на проходимость верхних дыхательных путей и компенсаторные реакции на ограничение инспираторного потока (IFL) во время сна. Мы предположили, что пациенты с ХОБЛ имеют менее гибкие дыхательные пути, обратно пропорциональные объему их легких, и что наличие ограничения потока выдыхаемого воздуха ограничивает реакции рабочего цикла для защиты вентиляции в присутствии ИФЛ. Мы включили 18 пациентов с ХОБЛ и 18 пациентов контрольной группы, сопоставимых по возрасту, индексу массы тела, полу и тяжести синдрома обструктивного апноэ во сне.Исследования сна, включая количественную оценку воздушного потока при различных уровнях назального давления, были проведены для определения механических свойств верхних дыхательных путей [критическое пассивное давление закрытия (Pcrit)] и для количественной оценки респираторных временных реакций на экспериментально индуцированный IFL. Пациенты с ХОБЛ имели более низкий пассивный Pcrit, чем их контрольная группа (ХОБЛ: -2,8 ± 0,9 см вод.ст. 2 O; контроль: -0,5 ± 0,5 см вод. функциональная остаточная емкость и пассивный Pcrit (−1.7 cmH 2 O / l увеличение функциональной остаточной емкости, r 2 = 0,27, P = 0,002). В ответ на IFL рабочий цикл вдоха увеличился больше ( P = 0,03) у пациентов с ХОБЛ (от 0,40 до 0,54), чем в контроле (от 0,41 до 0,51), и привел к заметному сокращению времени выдоха с 2,5 до 1,5 с ( P <0,01). Пациенты с ХОБЛ имеют менее гибкие дыхательные пути и большую, а не сокращенную компенсационную временную реакцию при обструкции верхних дыхательных путей.Хотя эти временные реакции могут снизить гиповентиляцию, они также могут увеличить риск развития динамической гиперинфляции из-за значительного сокращения времени выдоха.
Ключевые слова: обструкция верхних дыхательных путей, ХОБЛ, обструктивное апноэ во сне, ограничение потока вдоха, объем легких
Хроническая обструктивная болезнь легких (ХОБЛ) является ведущей причиной смерти, инвалидности и снижения качества жизни. Одышка при физической нагрузке остается основной причиной ухудшения качества жизни, а нарушение сна и утренняя усталость являются вторыми по частоте жалобами у этих пациентов (3, 18).В то время как обструктивное апноэ во сне (СОАС) является общепризнанным источником нарушений сна и утренней усталости у пациентов с ХОБЛ, другие маркеры ХОБЛ, такие как гиперинфляция легких (20), усиление дыхательных усилий (9, 12, 26), изменения в газообмен (6, 15, 21, 27, 34) и ограничение потока вдоха также были связаны с нарушениями сна. Понимание того, как эти факторы вызывают нарушения сна, может позволить исследователям разработать конкретные стратегии профилактики и лечения нарушений сна у пациентов с ХОБЛ.
Ограничение потока вдоха является признаком обструкции верхних дыхательных путей, которая возникает у людей с нарушенными механическими свойствами верхних дыхательных путей (10, 25). Механические свойства верхних дыхательных путей лучше всего количественно оценить, определив критическое давление закрытия (Pcrit) во время пассивного состояния нервной системы (пассивное Pcrit) (19, 25). Наша лаборатория недавно показала, что пассивный Pcrit предсказывает восприимчивость к заболеванию апноэ во сне и возрастает с увеличением индекса массы тела (ИМТ) и возраста (19).Более того, наша и другие лаборатории недавно продемонстрировали, что увеличение объема легких снижает пассивный Pcrit у нормальных людей и у пациентов с апноэ во сне (23, 31, 32). Эффект увеличения объема легких у пациентов с ХОБЛ на механические свойства верхних дыхательных путей не был продемонстрирован.
Обструкция верхних дыхательных путей вызывает компенсаторные реакции, которые помогают предотвратить гиповентиляцию. В частности, рабочий цикл вдоха [отношение времени вдоха (Ti) к длине дыхательного цикла] увеличивается в ответ на обструкцию верхних дыхательных путей, и это повышение Ti происходит за счет времени выдоха (Te) (5, 14, 28) .Однако пациенты с ХОБЛ часто демонстрируют длинное Те, чтобы справиться с ограничением потока выдоха и внутренним положительным давлением в конце выдоха (11, 13). Возможно, что наличие ограничения потока выдоха ухудшает реакцию рабочего цикла на обструкцию верхних дыхательных путей у пациентов с ХОБЛ. В настоящем исследовании мы набрали пациентов с ХОБЛ и сопоставили ИМТ, возраст, пол и индекс апноэ и гипопноэ (AHI), чтобы определить 1 ) пассивный Pcrit и 2 ) респираторный временной ответ на экспериментально индуцированную обструкцию верхних дыхательных путей.Мы предполагаем, что 1 ) пациенты с ХОБЛ имеют более низкий пассивный Pcrit (и, следовательно, более низкий риск обструкции верхних дыхательных путей) в сочетании с увеличением объема легких; и что 2 ) компенсаторные временные реакции на обструкцию верхних дыхательных путей снижены у пациентов с ХОБЛ по сравнению с нормальными людьми; и 3 ), что уменьшение временных реакций пропорционально степени ограничения потока выдоха [объем форсированного выдоха за 1 с (FEV 1 )].
МЕТОДЫ
Субъекты
Субъекты были набраны из группы лиц, участвовавших в испытании, изучающем влияние сна на исходы ХОБЛ. В общей сложности 96 пациентов с ХОБЛ и 41 курильщик, не страдающий ХОБЛ, прошли предыдущее исследование сна и были доступны для нашего исследования. Из этой группы было набрано 36 человек (). И мужчины ( n = 12), и женщины ( n = 6), которым был поставлен диагноз ХОБЛ [FEV 1 / форсированная жизненная емкость легких (FVC) <70%], были индивидуально сопоставлены по возрасту, полу, ИМТ и ИАГ. с восемнадцатью субъектами без ХОБЛ.Кроме того, анализ подгруппы был проведен на 12 пациентах с ХОБЛ и 12 контрольной группе, сопоставимых по их механическим свойствам верхних дыхательных путей (пассивный Pcrit) и ИМТ. Исключались пациенты, принимавшие респираторные депрессанты, седативные средства или пероральные стероиды. Субъектов также обследовали на наличие нестабильных сердечно-сосудистых заболеваний, неконтролируемой гипертензии, недавних операций на ротоглотке, неврологических расстройств, почечной и печеночной недостаточности, текущей беременности, нарушений свертываемости крови, психических проблем, среднего состояния покоя O 2 , насыщения гемоглобина <88% и аллергии на лидокаин.Письменное информированное согласие было получено от каждого участника этого исследования, которое было одобрено Наблюдательным советом по исследованиям в области человека Медицинского института Джонса Хопкинса.
Таблица 1.
| Переменная | Контроли | Пациенты с ХОБЛ | P Значение | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| n | 18 | 1816 | 9016 9016 9016 9016|||||||||
| Возраст, лет | 50.3 ± 1,6 | 57,1 ± 1,9 | <0,05 | ||||||||
| Высота, см | 170,0 ± 2,7 | 174,2 ± 2,1 | НС | ||||||||
| Масса, кг | 97,9 ± 6,6 86,5 | 4,1NS | |||||||||
| BMI, кг / м 2 | 31,6 ± 1,6 | 28,6 ± 1,2 | NS | ||||||||
| Пол | 12M; 6 Ф | 12М; 6 F | NS | ||||||||
| Объем легких | |||||||||||
| FEV 1 , литры | 3.1 ± 0,2 | 1,9 ± 0,2 | <0,05 | ||||||||
| ОФВ 1 / ФЖЕЛ,% | 79 ± 1,2 | 54 ± 2,6 | <0,05 | ||||||||
| TLC, литры | 5 | 6,7 ± 0,2 | <0,05 | ||||||||
| RV, литры | 1,9 ± 0,1 | 3,0 ± 0,2 | <0,05 | ||||||||
| FRC, литры | 2,8 ± 0,2 | 4,0 ± 0,2 0.05 | |||||||||
| RV / TLC,% | 33,8 ± 1,8 | 45,5 ± 2,4 | <0,05 | ||||||||
| Полисомнография | мин. ± 15,9 | NS | |||||||||
| Эффективность сна,% TST | 86,9 ± 2,0 | 79,4 ± 3,0 | <0,05 | ||||||||
| NREM,% TST | 84,7 ± 1,5 | 83.9 ± 1,9 | NS | ||||||||
| 1-й этап | 19,2 ± 2,4 | 27,1 ± 5,2 | NS | ||||||||
| 2-й этап | 60,2 ± 2,5 | 50,8 ± 4,3 | NS | 5,2 ± 1,8 | 6,0 ± 2,3 | NS | |||||
| REM,% TST | 15,3 ± 1,5 | 16,1 ± 1,9 | NS | ||||||||
| Всего AHI, событий / ч 28 | 9 ± 8,1 | 28,9 ± 8,6 | NS | ||||||||
| NREM AHI, событий / ч | 27,8 ± 8,1 | 28,2 ± 8,6 | NS | ||||||||
| REM AHI, событий165 | 733,3 ± 10,0 | NS | |||||||||
| % Гипопноэ NREM | 76,9 ± 6,1 | 75,9 ± 6,7 | NS | ||||||||
| % Гипопноэ REM | 7316 ± 7.3 | Артериальная Sa O 2 ,% | |||||||||
| Среднее базовое значение | 96.4 ± 0,4 | 93,9 ± 0,5 | <0,05 | ||||||||
| Среднее низкое значение | 91,5 ± 0,7 | 90,2 ± 0,6 | NS |
Экспериментальные методы
Тестирование функции легких.
Стандартные методы исследования функции легких (CPL Lung Function Analyzer; W.E. Collins, Braintree MA.) Были применены на следующее утро после диагностического исследования сна (2). ОФВ 1 и ФЖЕЛ определяли с помощью спирометрии.Функциональная остаточная емкость (FRC) измерялась с использованием разведения гелия в замкнутом контуре с несколькими вдохами, с медленной жизненной емкостью и резервным объемом выдоха, определяемыми в конце процедуры. Остаточный объем (RV) рассчитывали путем вычитания резервного объема выдоха из FRC. Затем можно определить общую емкость легких, добавив к ПЖ медленную жизненную емкость легких.
Полисомнография.
Стандартные диагностические методы использовались для определения исходных характеристик сна. Для контроля сна и слежения за сном электроды электроэнцефалографа помещали в точки F3-A2, C3-A2 и O1-A2, в дополнение к электродам электромиограммы под подбородком и левому и правому электродам электрокулограммы.Респираторные события оценивались с использованием импедансных торакоабдоминальных ремней для измерения дыхательного усилия, назальная канюля использовалась для количественного определения воздушного потока, а пульсоксиметрия использовалась для мониторинга насыщения гемоглобина кислородом. Апноэ определяли как остановку дыхания на 10 с, в то время как гипопноэ оценивали, когда снижение потока воздуха на 30% сопровождалось десатурацией кислорода ≥4%. Стандартные полисомнографические методы и правила оценки использовались для определения стадии сна и классификации нарушений дыхания во сне в соответствии с рекомендованными в 2007 г. руководящими принципами оценки, установленными Американской академией медицины сна (1).
Установка физиологии дыхания.
В дополнение к стандартным методам полисомнографии, субъект был снабжен гелевой маской, прикрепленной к специально разработанному устройству постоянного положительного давления в дыхательных путях, способному обеспечивать давление от -20 до +20 см вод. Ст. 2 O (Resmed, Bella Vista, NSW, Австралия). Расход воздуха измеряли с помощью пневмотахографа (модель 4830, 0-400 л / мин; Ханс Рудольф, Канзас-Сити, Миссури). Расход и давление регистрировались с частотой дискретизации 100 Гц. Все физиологические сигналы регистрировались и контролировались на компьютерной станции с использованием программного обеспечения Somnologica (Medcare, Buffalo, NY).
Протокол исследования
Первоначально испытуемые прошли диагностическое исследование сна для определения степени нарушения дыхания во сне, которое требовалось для сопоставления людей по AHI и антропометрическим данным (см.). Кроме того, на следующий день после исследования сна проводились функциональные тесты легких для определения общего объема легких и статуса заболевания. Затем мы выполнили последующее исследование сна в течение периода от 2 до 4 недель, чтобы определить механические свойства верхних дыхательных путей пациентов (пассивный Pcrit) и компенсаторные временные реакции на обструкцию верхних дыхательных путей.Процедуры определения Pcrit были подробно описаны ранее (24), проиллюстрированы и кратко описаны ниже.
Протокол эксперимента. Схематическая диаграмма экспериментальных протоколов ( вверху, ) и полисомнографических ответов ( внизу, ) во время сна с медленным движением глаз у мужчины с апноэ. Исходный уровень ( слева, ): назальное давление было отрегулировано до эффективного постоянного положительного давления в дыхательных путях и удерживалось не менее 3 минут (удерживающее давление) для установления стабильной модели дыхания без ограничения потока (см. График потока, внизу слева, ).Пассивная обструкция верхних дыхательных путей (, посередине слева, ): была проведена серия кратковременных (5 вдохов) падений назального давления в результате удержания давления без одновременной активации ЭМГ. Во время этих капель возникла обструкция верхних дыхательных путей, на что указывает ограничение потока вдоха, как показано на графике потока ниже. Sa O 2 , артериальный O 2 насыщение; Vi max , максимальный инспираторный поток.
Пассивное состояние: кратковременные периоды обструкции верхних дыхательных путей.
Мы использовали пассивный Pcrit для определения свойств верхних дыхательных путей при низкой гипотонической нервно-мышечной активности. Во время стабильного сна с медленным движением глаз назальное давление постепенно повышалось до тех пор, пока не было достигнуто носовое дыхание без ограничения потока. Затем назальное давление снижали ступенчато с шагом от 1 до 2 см вод. Падение давления будет прервано и повторено, если возникнет возбуждение или повышение активности ЭМГ без возбуждения.Периоды дыхания исключались, если были пробуждения от стабильного сна.
Сжимаемость верхних дыхательных путей.
Зависимость «давление-поток» (максимальный инспираторный поток в условиях ограниченного потока) была создана для каждого субъекта путем построения графика максимального воздушного потока из вдохов 3–5 каждого перепада давления, как описано ранее (30). Линейная регрессия использовалась для определения назального давления, при котором поток был нулевым, что указывает на закупорку верхних дыхательных путей (пассивный Pcrit), как показано на рис.
Ответы по времени дыхания.
Ti, Te, общее время каждого вдоха (Ttot) и частота дыхания были определены. Рабочий цикл вдоха (Ti / Tобщ) был зарегистрирован в условиях без ограничения потока, а также во время вдохов с острым умеренным или сильным ограничением потока, определяемым как средняя пиковая скорость потока воздуха на вдохе 50–150 мл / с () ( 28). Изменение временных параметров от исходного уровня до состояния обструкции верхних дыхательных путей использовалось для определения индивидуальной силы респираторных временных реакций на обструкцию верхних дыхательных путей.
Статистический анализ
Отдельные значения были усреднены и сравнены как для ХОБЛ, так и для контрольной группы с использованием непарного критерия Стьюдента t . Дальнейший анализ подгрупп проводился у пациентов с ОАС и без него. Изменения в ответе рабочего цикла сравнивали между группами пациентов с ХОБЛ и контрольной группой с помощью непарного t -теста. Сравнения до и после индукции ограничения инспираторного потока были выполнены с использованием парного теста t . Регрессионный анализ между FRC и пассивным Pcrit был выполнен для определения связи между объемом легких и сжимаемостью верхних дыхательных путей.Значение P 0,05 считалось статистически значимым. Все данные представлены как средние значения ± SE, если не указано иное.
РЕЗУЛЬТАТЫ
Характеристики субъектов
Демографические, антропометрические, полисомнографические и легочные статистические данные для всех 18 участников ХОБЛ и 18 контрольных групп, соответствующих AHI, отображаются в. Сравнение антропометрических переменных для субъектов, индивидуально подобранных по возрасту (57,1 ± 1,9 против 50,3 ± 1,6 года), полу (12 мужчин; 6 женщин), ИМТ (28.8 ± 1,3 против 31,6 ± 1,6 кг / м 2 ), и AHI (29 ± 8 против 29 ± 9 событий / ч) показаны на. У половины испытуемых (7 мужчин и 2 женщины из каждой группы) было нарушение дыхания во сне с частотой событий> 10 событий / час. Субъекты с ХОБЛ, по сравнению с контрольными субъектами, имели ОФВ 1 1,9 ± 0,2 против 3,1 ± 0,2 литра и ОФВ 1 / ФЖЕЛ 54 ± 0,0 против 79 ± 1,2%. Точно так же объемы легких были увеличены у пациентов с ХОБЛ по сравнению с контрольной группой: общая емкость легких составляла 6,7 ± 0,2 против 5,9 ± 0.3 литра, RV составляла 3,0 ± 0,2 против 1,9 ± 0,1 литра, а FRC составляла 4,0 ± 0,2 против 2,8 ± 0,2 литра.
Острые (пассивные) механические свойства верхних дыхательных путей
Субъекты с ХОБЛ имели средний пассивный Pcrit -2,8 см вод. t -тест;). Для подгруппы без ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -4,6 см вод.ст. 2 O по сравнению с -0,8 см вод.02; непарный т -тест). Для подгруппы с ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -1,0 см вод. Ст. 2 O по сравнению с -0,2 см вод. Была обнаружена значимая связь между FRC и пассивным Pcrit ( r 2 = 0,27, P = 0,002), как показано на рисунке, что указывает на то, что пациенты с более высокими объемами легких имели более низкие значения пассивного Pcrit.
Измерения пассивного критического давления закрытия (Pcrit) у пациентов с хронической обструктивной болезнью легких (ХОБЛ) и контрольной группы.График представляет средние значения пассивного Pcrit для пациентов с ХОБЛ и подобранной контрольной группы. Слева : все пациенты. Средний : пациенты с необструктивным апноэ сна (СОАС). Справа : пациенты с СОАС. Значения представляют собой средние значения ± SE. Коллапсируемость верхних дыхательных путей (пассивный Pcrit) ниже у пациентов с ХОБЛ по сравнению с субъектами, подобранными по возрасту, полу, индексу массы тела и индексу респираторных нарушений ( P = 0,03). Эта разница кажется более значительной у пациентов, не страдающих апноэ, но больше не заметна у пациентов с апноэ.NS, незначительно.
Пассивная зависимость Pcrit от функциональной остаточной емкости (FRC). График представляет пассивную зависимость Pcrit и FRC с линейной регрессией с использованием всех значений предмета. □, средства контроля, не относящиеся к OSA; ◇, органы управления OSA; ■ ХОБЛ без ОАС; ⧫ OSA ХОБЛ. Была статистически значимая связь между FRC и коллапсируемостью верхних дыхательных путей (пассивный Pcrit) у всех субъектов ( P = 0,002, r 2 = 0,27). Увеличение FRC на 1 литр было связано со снижением пассивного Pcrit на ~ 2 см вод. Ст.
При одномерном анализе была выявлена статистически значимая связь между значениями пассивного Pcrit и как FRC ( P = 0,002), так и ИМТ ( P = 0,003). В многомерном анализе оба фактора оставались определяющими для уровня пассивного Pcrit (FRC, P = 0,021; BMI, P = 0,041;).
Таблица 2.
Связь пассивного Pcrit с BMI и FRC
| Модель 1 | Модель 2 | Модель 3 | P значение | β-коэффициент | P значение | β-коэффициент | P Значение | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| FRC, см вод. Ст. 2 O / l | −1.66 ± 0,50 | 0,002 | −1,25 ± 0,51 | 0,021 | |||||||||||||
| ИМТ, кг / м 2 | 0,25 ± 0,08 | 9080,042 | |||||||||||||||
Острые респираторные временные ответы
В подгруппе из 12 пациентов, спаренных для анализа временных ответов, контрольная группа имела ИАГ 29,8 ± 7,5 событий / ч, а группа ХПК имела ИАГ 31.2 ± 6,8 событий / час. Среднее удерживающее давление составляло 8,8 ± 0,8 см вод. Ст. 2 O в контроле и 8,1 ± 1,0 см вод. Ст. 2 O у пациентов с ХОБЛ. Среднее дельта-давление, необходимое для серьезного ограничения потока вдоха, составляло 6,4 ± 0,8 см вод. Ст. 2 O для контроля и 7,0 ± 0,9 см вод.
Респираторные реакции по времени оценивались путем сравнения состояния без ограничения потока (исходный уровень) с периодами тяжелой обструкции верхних дыхательных путей. Пик инспираторного потока воздуха на исходном уровне и тяжелая обструкция верхних дыхательных путей были одинаковыми в обеих группах, снизившись с 383 ± 49 до 105 ± 11 мл / с в контроле и с 387 ± 47 до 111 ± 12 мл / с у пациентов с ХОБЛ.Параметры времени дыхания при исходном уровне, дыхании без ограничения потока и в ответ на серьезную степень ограничения потока вдоха суммированы в. Как в условиях без ограничения потока, так и в условиях с ограниченным потоком пациенты с ХОБЛ и контрольная группа имели одинаковые временные индексы. В то время как в контрольной группе увеличение рабочего цикла на ~ 25% с 0,41 до 0,51, у пациентов с ХОБЛ было увеличение на ~ 40% с 0,40 до 0,55 ( P = 0,03 для сравнения увеличения рабочего цикла). Те снизились в среднем с 2.От 5 до 1,5 с в группе ХОБЛ ( P <0,01) и в согласованном контроле от 2,4 до 1,8 с ( P <0,01). Ttot снизился при ХОБЛ с 4,1 до 3,3 с ( P <0,05) и в контроле с 3,9 до 3,6 с (незначительно). Ti увеличился с 1,5 до 1,8 с ( P <0,01) у пациентов с ХОБЛ и с 1,6 до 1,8 с в контроле ( P <0,05). Ни один из ответов по времени вдоха или выдоха не коррелировал с уровнем обструкции (FEV 1 ) у пациентов с ХОБЛ.
Таблица 3.
Временные реакции на индуцированное ограничение потока
| Время вдоха, с | Время выдоха, с | Общее время, с | Рабочий цикл, частота дыхания | 906 / мин||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Control | COPD | Control | COPD | Control | COPD | Control | COPD | Control Base | 9016 9016 ± 0,1| 1,5 ± 0,1 | 2,4 ± 0,2 | 2,5 ± 0,3 | 3,9 ± 0,2 | 4,1 ± 0,3 | 0,41 ± 0,02 | 0,40 ± 0,02 | 16,0 ± 0,9 | 15,5 ± 0,9 | | |
| IFL | 1,8 ± 0,1 * | 1,8 ± 0,1 * | 1,8 ± 0,2 * | 1,5 ± 0,1 * | 3,6 ± 0,3 | 3,3 ± 0,2 * | 0,51 ± 0,02 * | 0.55 ± 0,02 * † | 18,1 ± 1,6 | 18,9 ± 1,1 * | |||||||||
ОБСУЖДЕНИЕ
Основные результаты настоящего исследования заключаются в том, что пациенты с ХОБЛ имеют менее гибкие верхние дыхательные пути, чем их возраст. пол, ИМТ и AHI соответствовали контрольным субъектам, и что пассивный Pcrit обратно коррелировал с остаточным объемом легких. Проходимость дыхательных путей была увеличена у пациентов с ХОБЛ по сравнению с подобранной контрольной группой, но эта разница была намного меньше и несущественной в подгруппе пациентов с апноэ во сне, что указывает на то, что статус болезни апноэ во сне влияет на механизмы, которые опосредуют объем легких и пассивную взаимосвязь Pcrit.Во-вторых, в отличие от нашей гипотезы, пациенты с ХОБЛ продемонстрировали повышенную, а не пониженную реакцию рабочего цикла на обструкцию верхних дыхательных путей по сравнению с подобранной контрольной группой. Это увеличение рабочего цикла было связано с увеличением частоты дыхания и заметным снижением Те, которые являются известными факторами риска динамической гиперинфляции. Взятые вместе, наши данные показывают, что, хотя увеличение объема легких может снизить восприимчивость к OSA у пациентов с ХОБЛ, временные реакции на обструкцию верхних дыхательных путей могут способствовать динамической гиперинфляции.
Одним из основных клинических признаков ХОБЛ является прогрессирующее увеличение объема легких. У нашей популяции пациентов была умеренная степень ХОБЛ с FEV 1 / FVC в диапазоне от 50 до 70% от прогнозируемого и средним увеличением FRC на 1,2 литра по сравнению с контролем. Увеличение объема легких снижает разрушаемость верхних дыхательных путей у здоровых людей и пациентов с СОАС (23, 31, 32). Предлагаемый механизм этой связи — усиление тракции каудальной трахеи во время раздувания легких, в результате чего верхние дыхательные пути становятся более жесткими и менее гибкими (16).Теперь мы распространили эти результаты на пациентов с ХОБЛ с увеличенным объемом легких и обнаружили аналогичную взаимосвязь между FRC и верхней коллапсируемостью на ~ 2 см вод. Ст. 2 O снижение пассивного Pcrit на увеличение FRC на литр. Более низкий пассивный Pcrit связан с меньшим риском развития ОАС. Таким образом, оказывается, что пациенты с ХОБЛ с увеличенным объемом легких менее подвержены развитию ОАС.
Мы наблюдали более низкий пассивный Pcrit у пациентов с ХОБЛ, не страдающих апноэ, по сравнению с их сопоставимой группой контроля без апноэ.Можно предположить, что это различие связано с аномально высоким пассивным Pcrit в контрольной группе, а не со снижением пассивного Pcrit в группе ХОБЛ. Наша лаборатория ранее продемонстрировала, что пассивный Pcrit может быть одинаковым у лиц без OSA и OSA, в то время как активный Pcrit ниже у здоровых людей по сравнению с пациентами с апноэ, даже при сопоставлении с пассивным Pcrit (19, 25). Пассивный Pcrit выявляет механические свойства дыхательных путей в ненейронно активированном состоянии и приближается к измерениям Pcrit под анестезией.Фактически, некоторые отчеты во время анестезии также показали значения Pcrit, близкие к атмосферным, особенно при изучении пациентов старшего возраста (7, 8). Таким образом, мы предполагаем, что разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и контрольной группой не связана с аномально высоким Pcrit в нормальном контроле, а, скорее, из-за снижения пассивного Pcrit у пациентов с неапнеическим ХОБЛ.
Хотя имелась разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и их контрольной группой, мы больше не наблюдали этой разницы при сравнении пациентов с апноэ с ХОБЛ и их контрольной группы.Мы предлагаем несколько механизмов для объяснения этой дифференциальной реакции. Во-первых, несколько исследователей продемонстрировали, что пассивный Pcrit снижается с увеличением объема легких, что связано с каудальным трактом верхних дыхательных путей (31, 33, 35). Люди с апноэ имеют более крупный язык (29) и часто узкое, высоко дугообразное твердое небо (17), оба из которых могли притупить эффект растяжения, обеспечиваемый увеличением объема легких. Во-вторых, также возможно, что увеличение объема легких снижает пассивный Pcrit за счет нервной стимуляции внутри- или внелегочных рецепторов растяжения.Люди с апноэ могут иметь ослабленную нервную реакцию на увеличение объема легких, аналогичную ослаблению нервного контроля над верхними дыхательными путями в ответ на обструкцию верхних дыхательных путей (22, 25). В качестве альтернативы, подобно рефлексу Геринга-Брейера, который требует больших объемов вдоха для вызова рефлекторного ответа, пассивные ответы Pcrit также могут зависеть от степени гиперинфляции. У некоторых пациентов с апноэ с ХОБЛ увеличение объема легких могло быть недостаточно большим для снижения пассивного Pcrit.Чтобы определить, почему пациенты с неапноэ с ХОБЛ имеют более низкий пассивный Pcrit по сравнению с контрольной группой, в то время как пациенты с апноэ с ХОБЛ имеют такой же пассивный Pcrit, чем пациенты с апноэ, необходимы механические эксперименты, включающие оценку нервной и мышечной активности.
При обструкции верхних дыхательных путей увеличение рабочего цикла является одним из основных способов поддержания вентиляции. Чем больше увеличение рабочего цикла, тем лучше люди поддерживают минутную вентиляцию (5, 28, 36).В нашей настоящей работе мы наблюдали, что пациенты с ХОБЛ, по сравнению с подобранной контрольной группой, имеют большее увеличение рабочего цикла при обструкции верхних дыхательных путей. Таким образом, пациенты с ХОБЛ, по-видимому, лучше защищены от развития гиповентиляции по сравнению с контрольной группой, когда сталкиваются с обструкцией верхних дыхательных путей. Напротив, пациенты с ХОБЛ нуждаются в очень длительном Те, чтобы предотвратить динамическую гиперинфляцию легких. В настоящей работе мы наблюдали, что пациенты с ХОБЛ, а также контрольная группа, снижали Те при ограничении инспираторного потока.Хотя умеренное снижение Те обычно не влияет на механику дыхания, наблюдаемого снижения Те на ~ 50% может быть достаточно, чтобы вызвать динамическую гиперинфляцию. Фактически, подобное снижение Те при использовании метронома во время бодрствования вызывало динамическую гиперинфляцию у пациентов с умеренной ХОБЛ (4). Субъекты с нормальной функцией легких могут хорошо переносить снижение Те. Однако у субъектов с ограничением потока вдоха при ХОБЛ наблюдаемое снижение Те может вызывать динамическую гиперинфляцию во время сна.
У настоящего исследования есть несколько сильных сторон и ограничений. Первым преимуществом является наш подход к сопоставлению пациентов с ХОБЛ и контрольной группы по возрасту, тяжести апноэ во сне (AHI), полу и ИМТ, которые являются известными факторами риска разрушения верхних дыхательных путей. Когда мы проанализировали только пациентов без ОАС, различия в разборчивости верхних дыхательных путей были даже больше, чем при сравнении всей группы, что позволяет предположить, что мы, возможно, недооценили влияние повышенного объема легких на проходимость верхних дыхательных путей.Вторая сильная сторона — это наш экспериментальный план для определения временных параметров в ответ на обструкцию верхних дыхательных путей. В предыдущих исследованиях наша лаборатория продемонстрировала, что рабочий цикл увеличивается с тяжестью обструкции верхних дыхательных путей в зависимости от дозы. Поэтому мы установили одинаковую степень обструкции верхних дыхательных путей для всех участников нашего исследования. Этот экспериментальный план позволил нам уменьшить вариабельность временных ответов, наблюдая при этом дифференциальные ответы между пациентами с ХОБЛ и контрольной группой.Напротив, несмотря на лучшее соответствие пациентов с ХОБЛ и контрольной группы по статусу заболевания (AHI), возрасту и полу, у нас есть только перекрестные данные по пассивному Pcrit для участников нашего исследования. Возможно, мы недооценили влияние объема легких на сжимаемость верхних дыхательных путей из-за систематической ошибки отбора. Мы также не измеряли внутреннее положительное давление в конце выдоха, которое, вероятно, присутствует у многих наших пациентов с ХОБЛ и может быть изменено экспериментально вызванным ограничением потока.Мы признаем, что наши пациенты с ХОБЛ были значительно старше контрольной группы. Увеличение возраста связано либо с отсутствием изменений, либо с увеличением пассивного Pcrit (19). Поэтому мы считаем, что разница в возрасте не может объяснить более низкий пассивный Pcrit в группе ХОБЛ. Наконец, возможно, что мы не достигли аналогичной нервно-мышечной пассивности у контрольных пациентов с апноэ и пациентов с ХОБЛ с апноэ. Пациенты с ХОБЛ имеют более высокие респираторные нагрузки и, как следствие, более высокие усилия, что может привести к более сильному неврологическому воздействию как на дыхательные мышцы, так и на мышцы верхних дыхательных путей.Хотя пассивные измерения Pcrit предназначены для описания свойств дыхательных путей в пассивном состоянии, мы не можем исключить, что некоторые из наблюдаемых различий в верхних дыхательных путях отражают различные состояния активации мышц верхних дыхательных путей.
Значение
Настоящая работа имеет несколько клинических последствий. Во-первых, мы показываем, что увеличение объема легких связано с более низким Pcrit (пассивным Pcrit) верхних дыхательных путей. Аналогичным образом, изменения объема легких также могут влиять на пассивный Pcrit у пациентов с ХОБЛ.Операция по уменьшению объема легких (LVRS) — одна из стратегий лечения тяжелой ХОБЛ. Если LVRS повысит пассивный Pcrit, эффективность лечения LVRS может снизиться из-за возникновения OSA. Во-вторых, у пациентов с ХОБЛ короткие периоды тяжелой обструкции верхних дыхательных путей вызывали заметное снижение Те до уровней, сопоставимых с результатами предыдущих исследований, изучающих источники динамической гиперинфляции. Известно, что динамическая гиперинфляция увеличивает работу дыхания и снижает эффективность сна, что может быть связано с утренней усталостью, обычно наблюдаемой у пациентов с ХОБЛ.
ГРАНТЫ
Это исследование финансировалось Национальным институтом сердца, легких и крови, грант RO1-HL-105546 и Conselho Nacional de Desenvolvimento Científico e Tecnológico-Brasil.
РАСКРЫТИЕ ИНФОРМАЦИИ
Автор (ы) не заявляет о конфликте интересов, финансовом или ином.
ВЗНОС АВТОРОВ
Вклад авторов: P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. проанализированные данные; P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. интерпретированные результаты экспериментов; P.J.C.B., P.R.G. и H.S. подготовленные фигурки; P.J.C.B., P.R.G., A.R.S. и H.S. составленная рукопись; P.J.C.B., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. отредактированная и исправленная рукопись; P.J.C.B. и H.S. утвержденная финальная версия рукописи; P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. концепция и дизайн исследования; P.R.G., J.P.K. и H.S. проводил эксперименты.
СПИСОК ЛИТЕРАТУРЫ
1. Американская академия медицины сна. Руководство AASM по оценке сна и связанных с ним событий: правила, терминология и технические спецификации.Вестчестер, Иллинойс: Американская академия медицины сна, 2007. [Google Scholar] 2. Американское торакальное общество. Стандартизация спирометрии, обновление 1994 г. Американское торакальное общество. Am J Respir Crit Care Med 152: 1107–1136, 1995. [PubMed] [Google Scholar] 3. Бреслин Э, ван дер Сханс С., Бреукинк С., Мик П., Мерсер К., Фольц В., Луи С. Восприятие утомляемости и качества жизни у пациентов с ХОБЛ. Грудь 114: 958–964, 1998. [PubMed] [Google Scholar] 4. Каллигаро Г.Л., Рейн Р.И., Бейтман М.Э., Бейтман Э.Д., Купер С.Б.Сравнение динамической гиперинфляции и связанной с ней одышки, вызванной тахипноэ в метрономном ритме, с дополнительными упражнениями. ХОБЛ 11: 105–112, 2014. [PubMed] [Google Scholar] 5. Чин Ч., Киркнесс JP, Патил С.П., Макгинли Б.М., Смит П.Л., Шварц А.Р., Шнайдер Х. Компенсаторные реакции на обструкцию верхних дыхательных путей у мужчин и женщин с ожирением и апноэ. J Appl Physiol 112: 403–410, 2012. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Дуглас, штат Нью-Джерси, Calverley PMA, Leggett RJE, Brash DC, Flenley DC, Brezinova V. Преходящая гипоксемия во сне при хроническом бронхите и эмфиземе.Ланцет 1: 1–4, 1979. [PubMed] [Google Scholar] 7. Иствуд ПР, Платт ПР, Шеперд К., Мэддисон К., Хиллман ДР. Складываемость верхних дыхательных путей при различных концентрациях анестезии пропофолом. Анестезиология 103: 470–477, 2005. [PubMed] [Google Scholar] 8. Eastwood PR, Szollosi I, Platt PR, Hillman DR. Сравнение коллапса верхних дыхательных путей во время наркоза и сна. Ланцет 359: 1207–1209, 2002. [PubMed] [Google Scholar] 9. Gold AR, Gold MS, Харрис К.В., Эспелета В.Дж., Амин М.М., Бродерик Дж.Гиперсонливость, бессонница и патофизиология синдрома сопротивления верхних дыхательных путей. Сон Мед 9: 675–683, 2008. [PubMed] [Google Scholar] 10. Золото AR, Schwartz AR. Критическое давление в глотке. Почему и как использовать назальное постоянное положительное давление в дыхательных путях для диагностики. Грудь 110: 1077–1088, 1996. [PubMed] [Google Scholar] 11. Gorini M, Misuri G, Corrado A, Duranti R, Iandelli I, De Paola E, Scano G. Характер дыхания и задержка углекислого газа при тяжелой хронической обструктивной болезни легких.Грудная клетка 51: 677–683, 1996. [Бесплатная статья PMC] [PubMed] [Google Scholar] 12. Гийемино C, Stoohs R, Clerk A, Cetel M, Maistros P. Причина чрезмерной дневной сонливости. Синдром сопротивления верхних дыхательных путей. Грудь 104: 781–787, 1993. [PubMed] [Google Scholar] 13. Haluszka J, Chartrand DA, Grassino AE, Milic-Emili J. Внутренний ПДКВ и артериальный Pco 2 у стабильных пациентов с хронической обструктивной болезнью легких. Am Rev Respir Dis 141: 1194–1197, 1990. [PubMed] [Google Scholar] 14. Хосино Ю., Аюс Т., Курата С., Аюс Т., Шнайдер Х., Киркнесс Дж. П., Патил С.П., Шварц А.Р., Ои К.Компенсаторные реакции на обструкцию верхних дыхательных путей у здоровых людей под анестезией пропофолом. Респир Физиол Нейробиол 166: 24–31, 2009. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Хаджел Д.В., Мартин Р.Дж., Кейпхарт М., Джонсон Б., Хилл П. Вклад гиповентиляции в десатурацию кислорода во сне при хронической обструктивной болезни легких. J Appl Physiol 55: 669–677, 1983. [PubMed] [Google Scholar] 16. Кайрайтис К., Байт К., Парих Р., Ставрину Р., Уитли Дж. Р., Эмис Т.К. Влияние тракции трахеи на проходимость верхних дыхательных путей у кроликов: роль тканевого давления.Спать 30: 179–186, 2007. [PubMed] [Google Scholar] 17. Ким Дж. Х., Гийемино К. Назомаксиллярный комплекс, нижняя челюсть и нарушение дыхания во сне. Сон Дыхание 15: 185–193, 2011. [PubMed] [Google Scholar] 18. Kinsman RA, Yaroush RA, Fernandez E, Dirks JF, Schocket M, Fukuhara J. Симптомы и переживания при хроническом бронхите и эмфиземе. Грудь 83: 755–761, 1983. [PubMed] [Google Scholar] 19. Киркнесс Дж. П., Шварц А. Р., Шнайдер Х., Пенджаби Н. М., Малый Дж. Дж., Лаффан А. М., МакГинли Б. М., Магнусон Т., Швейцер М., Смит П. Л., Патил С. П..Вклад мужского пола, возраста и ожирения в механическую нестабильность верхних дыхательных путей во время сна. J Appl Physiol 104: 1618–1624, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Krachman SL, Chatila W., Martin UJ, Nugent T, Crocetti J, Gaughan J, Criner GJ. Влияние операции по уменьшению объема легких на качество сна и ночной газообмен у пациентов с тяжелой эмфиземой. Грудь 128: 3221–3228, 2005. [PubMed] [Google Scholar] 21. Leitch AG, Gloney LJ, Leggett RJE. Напряжение газов артериальной крови, ион водорода и электроэнцефалограмма во время сна у пациентов с хронической дыхательной недостаточностью.Грудная клетка 31: 730–735, 1976. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Макгинли Б.М., Шварц А.Р., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Патил С.П. Нервно-мышечная компенсация верхних дыхательных путей во время сна нарушается при обструктивном апноэ во сне. J Appl Physiol 105: 197–205, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Оуэнс Р.Л., Малхотра А., Эккерт Д.Д., Уайт Д.П., Джордан А.С. Влияние объема легких в конце выдоха на измерения гибкости глотки. J Appl Physiol 108: 455–451, 2010.[Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Патил С.П., Пенджаби Н.М., Шнайдер Х., О’Доннелл С.П., Смит П.Л., Шварц А.Р. Упрощенный метод измерения критического давления во время сна в клинических условиях. Am J Respir Crit Care Med 170: 86–93, 2004. [PubMed] [Google Scholar] 25. Патил С.П., Шнайдер Х., Маркс Дж.Дж., Гладмон Э., Шварц А.Р., Смит П.Л. Нейромеханический контроль проходимости верхних дыхательных путей во время сна. J Appl Physiol 102: 547–556, 2007. [PubMed] [Google Scholar] 26. Полномочия CR, Frey WC. Поддержание теста на бодрствование у военнослужащих с синдромом сопротивления верхних дыхательных путей и легким или умеренным апноэ во сне.Сон Дыхание 13: 253–258, 2009. [PubMed] [Google Scholar] 27. Сандерс MH, Ньюман AB, Haggerty CL, Redline S, Lebowitz M, Samet J, O’Connor GT, Punjabi NM, Shahar E. Сон и нарушение дыхания во сне у взрослых с преимущественно легкой формой обструктивного заболевания дыхательных путей. Am J Respir Crit Care Med 167: 7–14, 2003. [PubMed] [Google Scholar] 28. Шнайдер Х., Кришнан В., Пичард Л. Е., Патил С. П., Смит П. Л., Шварц А. Р.. Ответная реакция рабочего цикла вдоха на ограничение потока предсказывает ночную гиповентиляцию. Eur Respir J 33: 1068–1076, 2009.[PubMed] [Google Scholar] 29. Шваб Р.Дж., Пасирштейн М., Пирсон Р., Макли А., Хачадориан Р., Аренс Р., Мэйслин Г., Пак А.И. Выявление анатомических факторов риска обструктивного апноэ во сне верхних дыхательных путей с помощью объемной магнитно-резонансной томографии. Am J Respir Crit Care Med 168: 522–530, 2003. [PubMed] [Google Scholar] 30. Шварц А.Р., О’Доннел С.П., Барон Дж., Шуберт Н., Алам Д., Самади С.Д., Смит П.Л. Гипотонические верхние дыхательные пути при обструктивном апноэ во сне. Роль структур и нервно-мышечной деятельности.Am J Respir Crit Care Med 157: 1051–1057, 1998. [PubMed] [Google Scholar] 31. Сквайер С.Б., Патил С.П., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Шварц А.Р. Влияние объема легких в конце выдоха на сжимаемость верхних дыхательных путей у спящих мужчин и женщин. J Appl Physiol 109: 977–985, 2010. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Тагайто Ю., Исоно С., Реммерс Дж. Э., Танака А., Нишино Т. Объем легких и сжатие пассивной глотки у пациентов с нарушением дыхания во сне. J Appl Physiol 103: 1379–1385, 2007.[PubMed] [Google Scholar] 33. Тут Д.К., Шварц А.Р., Роуч Д., Мудрый Р.А., Пермутт С., Смит П.Л. Положение трахеи и шеи влияет на динамику воздушного потока в верхних дыхательных путях, изменяя длину дыхательных путей. J Appl Physiol 75: 2084–2090, 1993. [PubMed] [Google Scholar] 34. Траск CH, Gress EM. Оксиметрические исследования пациентов с хронической эмфиземой легких, бодрствования и сна. N Engl J Med 266: 639–642, 1962. [PubMed] [Google Scholar] 35. Ван де Грааф ВБ. Торакальное вытяжение за трахею: механизмы и масштабы. J Appl Physiol 70: 1328–1336, 1991.[PubMed] [Google Scholar] 36. Юнес М. Роль механизмов контроля дыхания в патогенезе обструктивных нарушений сна. J Appl Physiol 105: 1389–1405, 2008. [PubMed] [Google Scholar]Влияние увеличения объема легких при хронической обструктивной болезни легких на обструкцию верхних дыхательных путей во время сна
J Appl Physiol (1985). 2015 1 августа; 119 (3): 266–271.
, 1, 2 , 1 , 1 , 1 , 1 , 1 и 1Паоло Биселли
1 Центр расстройств сна Джонса Хопкинса, Подразделение отделения легочной медицины и реанимации, Центр астмы и аллергии Джонса Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Питер Р.Grossman
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Джейсон П. Киркнесс
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Сушил П. Патил
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Филип Л.Smith
1 Центр болезней сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Алан Р. Шварц
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Hartmut Schneider
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Автор, ответственный за переписку.Адрес для запросов на перепечатку и другой корреспонденции: Х. Шнайдер, Центр расстройств сна Джонса Хопкинса, Отделение легочной и интенсивной терапии, Центр астмы и аллергии Джонса Хопкинса, 5501 Hopkins Bayview Circle, Балтимор, Мэриленд 21224 (электронная почта: ude.imhj @ 3ienhcsh).Поступила в редакцию 29 мая 2014 г .; Принята к печати 31 мая 2015 г.
Авторские права © Американское физиологическое общество, 2015 г. Эта статья цитируется в других статьях PMC.Abstract
У пациентов с хронической обструктивной болезнью легких (ХОБЛ) наблюдается увеличение объема легких из-за ограничения потока воздуха на выдохе.Увеличение объема легких может повлиять на проходимость верхних дыхательных путей и компенсаторные реакции на ограничение инспираторного потока (IFL) во время сна. Мы предположили, что пациенты с ХОБЛ имеют менее гибкие дыхательные пути, обратно пропорциональные объему их легких, и что наличие ограничения потока выдыхаемого воздуха ограничивает реакции рабочего цикла для защиты вентиляции в присутствии ИФЛ. Мы включили 18 пациентов с ХОБЛ и 18 пациентов контрольной группы, сопоставимых по возрасту, индексу массы тела, полу и тяжести синдрома обструктивного апноэ во сне.Исследования сна, включая количественную оценку воздушного потока при различных уровнях назального давления, были проведены для определения механических свойств верхних дыхательных путей [критическое пассивное давление закрытия (Pcrit)] и для количественной оценки респираторных временных реакций на экспериментально индуцированный IFL. Пациенты с ХОБЛ имели более низкий пассивный Pcrit, чем их контрольная группа (ХОБЛ: -2,8 ± 0,9 см вод.ст. 2 O; контроль: -0,5 ± 0,5 см вод. функциональная остаточная емкость и пассивный Pcrit (−1.7 cmH 2 O / l увеличение функциональной остаточной емкости, r 2 = 0,27, P = 0,002). В ответ на IFL рабочий цикл вдоха увеличился больше ( P = 0,03) у пациентов с ХОБЛ (от 0,40 до 0,54), чем в контроле (от 0,41 до 0,51), и привел к заметному сокращению времени выдоха с 2,5 до 1,5 с ( P <0,01). Пациенты с ХОБЛ имеют менее гибкие дыхательные пути и большую, а не сокращенную компенсационную временную реакцию при обструкции верхних дыхательных путей.Хотя эти временные реакции могут снизить гиповентиляцию, они также могут увеличить риск развития динамической гиперинфляции из-за значительного сокращения времени выдоха.
Ключевые слова: обструкция верхних дыхательных путей, ХОБЛ, обструктивное апноэ во сне, ограничение потока вдоха, объем легких
Хроническая обструктивная болезнь легких (ХОБЛ) является ведущей причиной смерти, инвалидности и снижения качества жизни. Одышка при физической нагрузке остается основной причиной ухудшения качества жизни, а нарушение сна и утренняя усталость являются вторыми по частоте жалобами у этих пациентов (3, 18).В то время как обструктивное апноэ во сне (СОАС) является общепризнанным источником нарушений сна и утренней усталости у пациентов с ХОБЛ, другие маркеры ХОБЛ, такие как гиперинфляция легких (20), усиление дыхательных усилий (9, 12, 26), изменения в газообмен (6, 15, 21, 27, 34) и ограничение потока вдоха также были связаны с нарушениями сна. Понимание того, как эти факторы вызывают нарушения сна, может позволить исследователям разработать конкретные стратегии профилактики и лечения нарушений сна у пациентов с ХОБЛ.
Ограничение потока вдоха является признаком обструкции верхних дыхательных путей, которая возникает у людей с нарушенными механическими свойствами верхних дыхательных путей (10, 25). Механические свойства верхних дыхательных путей лучше всего количественно оценить, определив критическое давление закрытия (Pcrit) во время пассивного состояния нервной системы (пассивное Pcrit) (19, 25). Наша лаборатория недавно показала, что пассивный Pcrit предсказывает восприимчивость к заболеванию апноэ во сне и возрастает с увеличением индекса массы тела (ИМТ) и возраста (19).Более того, наша и другие лаборатории недавно продемонстрировали, что увеличение объема легких снижает пассивный Pcrit у нормальных людей и у пациентов с апноэ во сне (23, 31, 32). Эффект увеличения объема легких у пациентов с ХОБЛ на механические свойства верхних дыхательных путей не был продемонстрирован.
Обструкция верхних дыхательных путей вызывает компенсаторные реакции, которые помогают предотвратить гиповентиляцию. В частности, рабочий цикл вдоха [отношение времени вдоха (Ti) к длине дыхательного цикла] увеличивается в ответ на обструкцию верхних дыхательных путей, и это повышение Ti происходит за счет времени выдоха (Te) (5, 14, 28) .Однако пациенты с ХОБЛ часто демонстрируют длинное Те, чтобы справиться с ограничением потока выдоха и внутренним положительным давлением в конце выдоха (11, 13). Возможно, что наличие ограничения потока выдоха ухудшает реакцию рабочего цикла на обструкцию верхних дыхательных путей у пациентов с ХОБЛ. В настоящем исследовании мы набрали пациентов с ХОБЛ и сопоставили ИМТ, возраст, пол и индекс апноэ и гипопноэ (AHI), чтобы определить 1 ) пассивный Pcrit и 2 ) респираторный временной ответ на экспериментально индуцированную обструкцию верхних дыхательных путей.Мы предполагаем, что 1 ) пациенты с ХОБЛ имеют более низкий пассивный Pcrit (и, следовательно, более низкий риск обструкции верхних дыхательных путей) в сочетании с увеличением объема легких; и что 2 ) компенсаторные временные реакции на обструкцию верхних дыхательных путей снижены у пациентов с ХОБЛ по сравнению с нормальными людьми; и 3 ), что уменьшение временных реакций пропорционально степени ограничения потока выдоха [объем форсированного выдоха за 1 с (FEV 1 )].
МЕТОДЫ
Субъекты
Субъекты были набраны из группы лиц, участвовавших в испытании, изучающем влияние сна на исходы ХОБЛ. В общей сложности 96 пациентов с ХОБЛ и 41 курильщик, не страдающий ХОБЛ, прошли предыдущее исследование сна и были доступны для нашего исследования. Из этой группы было набрано 36 человек (). И мужчины ( n = 12), и женщины ( n = 6), которым был поставлен диагноз ХОБЛ [FEV 1 / форсированная жизненная емкость легких (FVC) <70%], были индивидуально сопоставлены по возрасту, полу, ИМТ и ИАГ. с восемнадцатью субъектами без ХОБЛ.Кроме того, анализ подгруппы был проведен на 12 пациентах с ХОБЛ и 12 контрольной группе, сопоставимых по их механическим свойствам верхних дыхательных путей (пассивный Pcrit) и ИМТ. Исключались пациенты, принимавшие респираторные депрессанты, седативные средства или пероральные стероиды. Субъектов также обследовали на наличие нестабильных сердечно-сосудистых заболеваний, неконтролируемой гипертензии, недавних операций на ротоглотке, неврологических расстройств, почечной и печеночной недостаточности, текущей беременности, нарушений свертываемости крови, психических проблем, среднего состояния покоя O 2 , насыщения гемоглобина <88% и аллергии на лидокаин.Письменное информированное согласие было получено от каждого участника этого исследования, которое было одобрено Наблюдательным советом по исследованиям в области человека Медицинского института Джонса Хопкинса.
Таблица 1.
| Переменная | Контроли | Пациенты с ХОБЛ | P Значение | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| n | 18 | 1816 | 9016 9016 9016 9016|||||||||
| Возраст, лет | 50.3 ± 1,6 | 57,1 ± 1,9 | <0,05 | ||||||||
| Высота, см | 170,0 ± 2,7 | 174,2 ± 2,1 | НС | ||||||||
| Масса, кг | 97,9 ± 6,6 86,5 | 4,1NS | |||||||||
| BMI, кг / м 2 | 31,6 ± 1,6 | 28,6 ± 1,2 | NS | ||||||||
| Пол | 12M; 6 Ф | 12М; 6 F | NS | ||||||||
| Объем легких | |||||||||||
| FEV 1 , литры | 3.1 ± 0,2 | 1,9 ± 0,2 | <0,05 | ||||||||
| ОФВ 1 / ФЖЕЛ,% | 79 ± 1,2 | 54 ± 2,6 | <0,05 | ||||||||
| TLC, литры | 5 | 6,7 ± 0,2 | <0,05 | ||||||||
| RV, литры | 1,9 ± 0,1 | 3,0 ± 0,2 | <0,05 | ||||||||
| FRC, литры | 2,8 ± 0,2 | 4,0 ± 0,2 0.05 | |||||||||
| RV / TLC,% | 33,8 ± 1,8 | 45,5 ± 2,4 | <0,05 | ||||||||
| Полисомнография | мин. ± 15,9 | NS | |||||||||
| Эффективность сна,% TST | 86,9 ± 2,0 | 79,4 ± 3,0 | <0,05 | ||||||||
| NREM,% TST | 84,7 ± 1,5 | 83.9 ± 1,9 | NS | ||||||||
| 1-й этап | 19,2 ± 2,4 | 27,1 ± 5,2 | NS | ||||||||
| 2-й этап | 60,2 ± 2,5 | 50,8 ± 4,3 | NS | 5,2 ± 1,8 | 6,0 ± 2,3 | NS | |||||
| REM,% TST | 15,3 ± 1,5 | 16,1 ± 1,9 | NS | ||||||||
| Всего AHI, событий / ч 28 | 9 ± 8,1 | 28,9 ± 8,6 | NS | ||||||||
| NREM AHI, событий / ч | 27,8 ± 8,1 | 28,2 ± 8,6 | NS | ||||||||
| REM AHI, событий165 | 733,3 ± 10,0 | NS | |||||||||
| % Гипопноэ NREM | 76,9 ± 6,1 | 75,9 ± 6,7 | NS | ||||||||
| % Гипопноэ REM | 7316 ± 7.3 | Артериальная Sa O 2 ,% | |||||||||
| Среднее базовое значение | 96.4 ± 0,4 | 93,9 ± 0,5 | <0,05 | ||||||||
| Среднее низкое значение | 91,5 ± 0,7 | 90,2 ± 0,6 | NS |
Экспериментальные методы
Тестирование функции легких.
Стандартные методы исследования функции легких (CPL Lung Function Analyzer; W.E. Collins, Braintree MA.) Были применены на следующее утро после диагностического исследования сна (2). ОФВ 1 и ФЖЕЛ определяли с помощью спирометрии.Функциональная остаточная емкость (FRC) измерялась с использованием разведения гелия в замкнутом контуре с несколькими вдохами, с медленной жизненной емкостью и резервным объемом выдоха, определяемыми в конце процедуры. Остаточный объем (RV) рассчитывали путем вычитания резервного объема выдоха из FRC. Затем можно определить общую емкость легких, добавив к ПЖ медленную жизненную емкость легких.
Полисомнография.
Стандартные диагностические методы использовались для определения исходных характеристик сна. Для контроля сна и слежения за сном электроды электроэнцефалографа помещали в точки F3-A2, C3-A2 и O1-A2, в дополнение к электродам электромиограммы под подбородком и левому и правому электродам электрокулограммы.Респираторные события оценивались с использованием импедансных торакоабдоминальных ремней для измерения дыхательного усилия, назальная канюля использовалась для количественного определения воздушного потока, а пульсоксиметрия использовалась для мониторинга насыщения гемоглобина кислородом. Апноэ определяли как остановку дыхания на 10 с, в то время как гипопноэ оценивали, когда снижение потока воздуха на 30% сопровождалось десатурацией кислорода ≥4%. Стандартные полисомнографические методы и правила оценки использовались для определения стадии сна и классификации нарушений дыхания во сне в соответствии с рекомендованными в 2007 г. руководящими принципами оценки, установленными Американской академией медицины сна (1).
Установка физиологии дыхания.
В дополнение к стандартным методам полисомнографии, субъект был снабжен гелевой маской, прикрепленной к специально разработанному устройству постоянного положительного давления в дыхательных путях, способному обеспечивать давление от -20 до +20 см вод. Ст. 2 O (Resmed, Bella Vista, NSW, Австралия). Расход воздуха измеряли с помощью пневмотахографа (модель 4830, 0-400 л / мин; Ханс Рудольф, Канзас-Сити, Миссури). Расход и давление регистрировались с частотой дискретизации 100 Гц. Все физиологические сигналы регистрировались и контролировались на компьютерной станции с использованием программного обеспечения Somnologica (Medcare, Buffalo, NY).
Протокол исследования
Первоначально испытуемые прошли диагностическое исследование сна для определения степени нарушения дыхания во сне, которое требовалось для сопоставления людей по AHI и антропометрическим данным (см.). Кроме того, на следующий день после исследования сна проводились функциональные тесты легких для определения общего объема легких и статуса заболевания. Затем мы выполнили последующее исследование сна в течение периода от 2 до 4 недель, чтобы определить механические свойства верхних дыхательных путей пациентов (пассивный Pcrit) и компенсаторные временные реакции на обструкцию верхних дыхательных путей.Процедуры определения Pcrit были подробно описаны ранее (24), проиллюстрированы и кратко описаны ниже.
Протокол эксперимента. Схематическая диаграмма экспериментальных протоколов ( вверху, ) и полисомнографических ответов ( внизу, ) во время сна с медленным движением глаз у мужчины с апноэ. Исходный уровень ( слева, ): назальное давление было отрегулировано до эффективного постоянного положительного давления в дыхательных путях и удерживалось не менее 3 минут (удерживающее давление) для установления стабильной модели дыхания без ограничения потока (см. График потока, внизу слева, ).Пассивная обструкция верхних дыхательных путей (, посередине слева, ): была проведена серия кратковременных (5 вдохов) падений назального давления в результате удержания давления без одновременной активации ЭМГ. Во время этих капель возникла обструкция верхних дыхательных путей, на что указывает ограничение потока вдоха, как показано на графике потока ниже. Sa O 2 , артериальный O 2 насыщение; Vi max , максимальный инспираторный поток.
Пассивное состояние: кратковременные периоды обструкции верхних дыхательных путей.
Мы использовали пассивный Pcrit для определения свойств верхних дыхательных путей при низкой гипотонической нервно-мышечной активности. Во время стабильного сна с медленным движением глаз назальное давление постепенно повышалось до тех пор, пока не было достигнуто носовое дыхание без ограничения потока. Затем назальное давление снижали ступенчато с шагом от 1 до 2 см вод. Падение давления будет прервано и повторено, если возникнет возбуждение или повышение активности ЭМГ без возбуждения.Периоды дыхания исключались, если были пробуждения от стабильного сна.
Сжимаемость верхних дыхательных путей.
Зависимость «давление-поток» (максимальный инспираторный поток в условиях ограниченного потока) была создана для каждого субъекта путем построения графика максимального воздушного потока из вдохов 3–5 каждого перепада давления, как описано ранее (30). Линейная регрессия использовалась для определения назального давления, при котором поток был нулевым, что указывает на закупорку верхних дыхательных путей (пассивный Pcrit), как показано на рис.
Ответы по времени дыхания.
Ti, Te, общее время каждого вдоха (Ttot) и частота дыхания были определены. Рабочий цикл вдоха (Ti / Tобщ) был зарегистрирован в условиях без ограничения потока, а также во время вдохов с острым умеренным или сильным ограничением потока, определяемым как средняя пиковая скорость потока воздуха на вдохе 50–150 мл / с () ( 28). Изменение временных параметров от исходного уровня до состояния обструкции верхних дыхательных путей использовалось для определения индивидуальной силы респираторных временных реакций на обструкцию верхних дыхательных путей.
Статистический анализ
Отдельные значения были усреднены и сравнены как для ХОБЛ, так и для контрольной группы с использованием непарного критерия Стьюдента t . Дальнейший анализ подгрупп проводился у пациентов с ОАС и без него. Изменения в ответе рабочего цикла сравнивали между группами пациентов с ХОБЛ и контрольной группой с помощью непарного t -теста. Сравнения до и после индукции ограничения инспираторного потока были выполнены с использованием парного теста t . Регрессионный анализ между FRC и пассивным Pcrit был выполнен для определения связи между объемом легких и сжимаемостью верхних дыхательных путей.Значение P 0,05 считалось статистически значимым. Все данные представлены как средние значения ± SE, если не указано иное.
РЕЗУЛЬТАТЫ
Характеристики субъектов
Демографические, антропометрические, полисомнографические и легочные статистические данные для всех 18 участников ХОБЛ и 18 контрольных групп, соответствующих AHI, отображаются в. Сравнение антропометрических переменных для субъектов, индивидуально подобранных по возрасту (57,1 ± 1,9 против 50,3 ± 1,6 года), полу (12 мужчин; 6 женщин), ИМТ (28.8 ± 1,3 против 31,6 ± 1,6 кг / м 2 ), и AHI (29 ± 8 против 29 ± 9 событий / ч) показаны на. У половины испытуемых (7 мужчин и 2 женщины из каждой группы) было нарушение дыхания во сне с частотой событий> 10 событий / час. Субъекты с ХОБЛ, по сравнению с контрольными субъектами, имели ОФВ 1 1,9 ± 0,2 против 3,1 ± 0,2 литра и ОФВ 1 / ФЖЕЛ 54 ± 0,0 против 79 ± 1,2%. Точно так же объемы легких были увеличены у пациентов с ХОБЛ по сравнению с контрольной группой: общая емкость легких составляла 6,7 ± 0,2 против 5,9 ± 0.3 литра, RV составляла 3,0 ± 0,2 против 1,9 ± 0,1 литра, а FRC составляла 4,0 ± 0,2 против 2,8 ± 0,2 литра.
Острые (пассивные) механические свойства верхних дыхательных путей
Субъекты с ХОБЛ имели средний пассивный Pcrit -2,8 см вод. t -тест;). Для подгруппы без ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -4,6 см вод.ст. 2 O по сравнению с -0,8 см вод.02; непарный т -тест). Для подгруппы с ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -1,0 см вод. Ст. 2 O по сравнению с -0,2 см вод. Была обнаружена значимая связь между FRC и пассивным Pcrit ( r 2 = 0,27, P = 0,002), как показано на рисунке, что указывает на то, что пациенты с более высокими объемами легких имели более низкие значения пассивного Pcrit.
Измерения пассивного критического давления закрытия (Pcrit) у пациентов с хронической обструктивной болезнью легких (ХОБЛ) и контрольной группы.График представляет средние значения пассивного Pcrit для пациентов с ХОБЛ и подобранной контрольной группы. Слева : все пациенты. Средний : пациенты с необструктивным апноэ сна (СОАС). Справа : пациенты с СОАС. Значения представляют собой средние значения ± SE. Коллапсируемость верхних дыхательных путей (пассивный Pcrit) ниже у пациентов с ХОБЛ по сравнению с субъектами, подобранными по возрасту, полу, индексу массы тела и индексу респираторных нарушений ( P = 0,03). Эта разница кажется более значительной у пациентов, не страдающих апноэ, но больше не заметна у пациентов с апноэ.NS, незначительно.
Пассивная зависимость Pcrit от функциональной остаточной емкости (FRC). График представляет пассивную зависимость Pcrit и FRC с линейной регрессией с использованием всех значений предмета. □, средства контроля, не относящиеся к OSA; ◇, органы управления OSA; ■ ХОБЛ без ОАС; ⧫ OSA ХОБЛ. Была статистически значимая связь между FRC и коллапсируемостью верхних дыхательных путей (пассивный Pcrit) у всех субъектов ( P = 0,002, r 2 = 0,27). Увеличение FRC на 1 литр было связано со снижением пассивного Pcrit на ~ 2 см вод. Ст.
При одномерном анализе была выявлена статистически значимая связь между значениями пассивного Pcrit и как FRC ( P = 0,002), так и ИМТ ( P = 0,003). В многомерном анализе оба фактора оставались определяющими для уровня пассивного Pcrit (FRC, P = 0,021; BMI, P = 0,041;).
Таблица 2.
Связь пассивного Pcrit с BMI и FRC
| Модель 1 | Модель 2 | Модель 3 | P значение | β-коэффициент | P значение | β-коэффициент | P Значение | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| FRC, см вод. Ст. 2 O / l | −1.66 ± 0,50 | 0,002 | −1,25 ± 0,51 | 0,021 | |||||||||||||
| ИМТ, кг / м 2 | 0,25 ± 0,08 | 9080,042 | |||||||||||||||
Острые респираторные временные ответы
В подгруппе из 12 пациентов, спаренных для анализа временных ответов, контрольная группа имела ИАГ 29,8 ± 7,5 событий / ч, а группа ХПК имела ИАГ 31.2 ± 6,8 событий / час. Среднее удерживающее давление составляло 8,8 ± 0,8 см вод. Ст. 2 O в контроле и 8,1 ± 1,0 см вод. Ст. 2 O у пациентов с ХОБЛ. Среднее дельта-давление, необходимое для серьезного ограничения потока вдоха, составляло 6,4 ± 0,8 см вод. Ст. 2 O для контроля и 7,0 ± 0,9 см вод.
Респираторные реакции по времени оценивались путем сравнения состояния без ограничения потока (исходный уровень) с периодами тяжелой обструкции верхних дыхательных путей. Пик инспираторного потока воздуха на исходном уровне и тяжелая обструкция верхних дыхательных путей были одинаковыми в обеих группах, снизившись с 383 ± 49 до 105 ± 11 мл / с в контроле и с 387 ± 47 до 111 ± 12 мл / с у пациентов с ХОБЛ.Параметры времени дыхания при исходном уровне, дыхании без ограничения потока и в ответ на серьезную степень ограничения потока вдоха суммированы в. Как в условиях без ограничения потока, так и в условиях с ограниченным потоком пациенты с ХОБЛ и контрольная группа имели одинаковые временные индексы. В то время как в контрольной группе увеличение рабочего цикла на ~ 25% с 0,41 до 0,51, у пациентов с ХОБЛ было увеличение на ~ 40% с 0,40 до 0,55 ( P = 0,03 для сравнения увеличения рабочего цикла). Те снизились в среднем с 2.От 5 до 1,5 с в группе ХОБЛ ( P <0,01) и в согласованном контроле от 2,4 до 1,8 с ( P <0,01). Ttot снизился при ХОБЛ с 4,1 до 3,3 с ( P <0,05) и в контроле с 3,9 до 3,6 с (незначительно). Ti увеличился с 1,5 до 1,8 с ( P <0,01) у пациентов с ХОБЛ и с 1,6 до 1,8 с в контроле ( P <0,05). Ни один из ответов по времени вдоха или выдоха не коррелировал с уровнем обструкции (FEV 1 ) у пациентов с ХОБЛ.
Таблица 3.
Временные реакции на индуцированное ограничение потока
| Время вдоха, с | Время выдоха, с | Общее время, с | Рабочий цикл, частота дыхания | 906 / мин||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Control | COPD | Control | COPD | Control | COPD | Control | COPD | Control Base | 9016 9016 ± 0,1| 1,5 ± 0,1 | 2,4 ± 0,2 | 2,5 ± 0,3 | 3,9 ± 0,2 | 4,1 ± 0,3 | 0,41 ± 0,02 | 0,40 ± 0,02 | 16,0 ± 0,9 | 15,5 ± 0,9 | | |
| IFL | 1,8 ± 0,1 * | 1,8 ± 0,1 * | 1,8 ± 0,2 * | 1,5 ± 0,1 * | 3,6 ± 0,3 | 3,3 ± 0,2 * | 0,51 ± 0,02 * | 0.55 ± 0,02 * † | 18,1 ± 1,6 | 18,9 ± 1,1 * | |||||||||
ОБСУЖДЕНИЕ
Основные результаты настоящего исследования заключаются в том, что пациенты с ХОБЛ имеют менее гибкие верхние дыхательные пути, чем их возраст. пол, ИМТ и AHI соответствовали контрольным субъектам, и что пассивный Pcrit обратно коррелировал с остаточным объемом легких. Проходимость дыхательных путей была увеличена у пациентов с ХОБЛ по сравнению с подобранной контрольной группой, но эта разница была намного меньше и несущественной в подгруппе пациентов с апноэ во сне, что указывает на то, что статус болезни апноэ во сне влияет на механизмы, которые опосредуют объем легких и пассивную взаимосвязь Pcrit.Во-вторых, в отличие от нашей гипотезы, пациенты с ХОБЛ продемонстрировали повышенную, а не пониженную реакцию рабочего цикла на обструкцию верхних дыхательных путей по сравнению с подобранной контрольной группой. Это увеличение рабочего цикла было связано с увеличением частоты дыхания и заметным снижением Те, которые являются известными факторами риска динамической гиперинфляции. Взятые вместе, наши данные показывают, что, хотя увеличение объема легких может снизить восприимчивость к OSA у пациентов с ХОБЛ, временные реакции на обструкцию верхних дыхательных путей могут способствовать динамической гиперинфляции.
Одним из основных клинических признаков ХОБЛ является прогрессирующее увеличение объема легких. У нашей популяции пациентов была умеренная степень ХОБЛ с FEV 1 / FVC в диапазоне от 50 до 70% от прогнозируемого и средним увеличением FRC на 1,2 литра по сравнению с контролем. Увеличение объема легких снижает разрушаемость верхних дыхательных путей у здоровых людей и пациентов с СОАС (23, 31, 32). Предлагаемый механизм этой связи — усиление тракции каудальной трахеи во время раздувания легких, в результате чего верхние дыхательные пути становятся более жесткими и менее гибкими (16).Теперь мы распространили эти результаты на пациентов с ХОБЛ с увеличенным объемом легких и обнаружили аналогичную взаимосвязь между FRC и верхней коллапсируемостью на ~ 2 см вод. Ст. 2 O снижение пассивного Pcrit на увеличение FRC на литр. Более низкий пассивный Pcrit связан с меньшим риском развития ОАС. Таким образом, оказывается, что пациенты с ХОБЛ с увеличенным объемом легких менее подвержены развитию ОАС.
Мы наблюдали более низкий пассивный Pcrit у пациентов с ХОБЛ, не страдающих апноэ, по сравнению с их сопоставимой группой контроля без апноэ.Можно предположить, что это различие связано с аномально высоким пассивным Pcrit в контрольной группе, а не со снижением пассивного Pcrit в группе ХОБЛ. Наша лаборатория ранее продемонстрировала, что пассивный Pcrit может быть одинаковым у лиц без OSA и OSA, в то время как активный Pcrit ниже у здоровых людей по сравнению с пациентами с апноэ, даже при сопоставлении с пассивным Pcrit (19, 25). Пассивный Pcrit выявляет механические свойства дыхательных путей в ненейронно активированном состоянии и приближается к измерениям Pcrit под анестезией.Фактически, некоторые отчеты во время анестезии также показали значения Pcrit, близкие к атмосферным, особенно при изучении пациентов старшего возраста (7, 8). Таким образом, мы предполагаем, что разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и контрольной группой не связана с аномально высоким Pcrit в нормальном контроле, а, скорее, из-за снижения пассивного Pcrit у пациентов с неапнеическим ХОБЛ.
Хотя имелась разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и их контрольной группой, мы больше не наблюдали этой разницы при сравнении пациентов с апноэ с ХОБЛ и их контрольной группы.Мы предлагаем несколько механизмов для объяснения этой дифференциальной реакции. Во-первых, несколько исследователей продемонстрировали, что пассивный Pcrit снижается с увеличением объема легких, что связано с каудальным трактом верхних дыхательных путей (31, 33, 35). Люди с апноэ имеют более крупный язык (29) и часто узкое, высоко дугообразное твердое небо (17), оба из которых могли притупить эффект растяжения, обеспечиваемый увеличением объема легких. Во-вторых, также возможно, что увеличение объема легких снижает пассивный Pcrit за счет нервной стимуляции внутри- или внелегочных рецепторов растяжения.Люди с апноэ могут иметь ослабленную нервную реакцию на увеличение объема легких, аналогичную ослаблению нервного контроля над верхними дыхательными путями в ответ на обструкцию верхних дыхательных путей (22, 25). В качестве альтернативы, подобно рефлексу Геринга-Брейера, который требует больших объемов вдоха для вызова рефлекторного ответа, пассивные ответы Pcrit также могут зависеть от степени гиперинфляции. У некоторых пациентов с апноэ с ХОБЛ увеличение объема легких могло быть недостаточно большим для снижения пассивного Pcrit.Чтобы определить, почему пациенты с неапноэ с ХОБЛ имеют более низкий пассивный Pcrit по сравнению с контрольной группой, в то время как пациенты с апноэ с ХОБЛ имеют такой же пассивный Pcrit, чем пациенты с апноэ, необходимы механические эксперименты, включающие оценку нервной и мышечной активности.
При обструкции верхних дыхательных путей увеличение рабочего цикла является одним из основных способов поддержания вентиляции. Чем больше увеличение рабочего цикла, тем лучше люди поддерживают минутную вентиляцию (5, 28, 36).В нашей настоящей работе мы наблюдали, что пациенты с ХОБЛ, по сравнению с подобранной контрольной группой, имеют большее увеличение рабочего цикла при обструкции верхних дыхательных путей. Таким образом, пациенты с ХОБЛ, по-видимому, лучше защищены от развития гиповентиляции по сравнению с контрольной группой, когда сталкиваются с обструкцией верхних дыхательных путей. Напротив, пациенты с ХОБЛ нуждаются в очень длительном Те, чтобы предотвратить динамическую гиперинфляцию легких. В настоящей работе мы наблюдали, что пациенты с ХОБЛ, а также контрольная группа, снижали Те при ограничении инспираторного потока.Хотя умеренное снижение Те обычно не влияет на механику дыхания, наблюдаемого снижения Те на ~ 50% может быть достаточно, чтобы вызвать динамическую гиперинфляцию. Фактически, подобное снижение Те при использовании метронома во время бодрствования вызывало динамическую гиперинфляцию у пациентов с умеренной ХОБЛ (4). Субъекты с нормальной функцией легких могут хорошо переносить снижение Те. Однако у субъектов с ограничением потока вдоха при ХОБЛ наблюдаемое снижение Те может вызывать динамическую гиперинфляцию во время сна.
У настоящего исследования есть несколько сильных сторон и ограничений. Первым преимуществом является наш подход к сопоставлению пациентов с ХОБЛ и контрольной группы по возрасту, тяжести апноэ во сне (AHI), полу и ИМТ, которые являются известными факторами риска разрушения верхних дыхательных путей. Когда мы проанализировали только пациентов без ОАС, различия в разборчивости верхних дыхательных путей были даже больше, чем при сравнении всей группы, что позволяет предположить, что мы, возможно, недооценили влияние повышенного объема легких на проходимость верхних дыхательных путей.Вторая сильная сторона — это наш экспериментальный план для определения временных параметров в ответ на обструкцию верхних дыхательных путей. В предыдущих исследованиях наша лаборатория продемонстрировала, что рабочий цикл увеличивается с тяжестью обструкции верхних дыхательных путей в зависимости от дозы. Поэтому мы установили одинаковую степень обструкции верхних дыхательных путей для всех участников нашего исследования. Этот экспериментальный план позволил нам уменьшить вариабельность временных ответов, наблюдая при этом дифференциальные ответы между пациентами с ХОБЛ и контрольной группой.Напротив, несмотря на лучшее соответствие пациентов с ХОБЛ и контрольной группы по статусу заболевания (AHI), возрасту и полу, у нас есть только перекрестные данные по пассивному Pcrit для участников нашего исследования. Возможно, мы недооценили влияние объема легких на сжимаемость верхних дыхательных путей из-за систематической ошибки отбора. Мы также не измеряли внутреннее положительное давление в конце выдоха, которое, вероятно, присутствует у многих наших пациентов с ХОБЛ и может быть изменено экспериментально вызванным ограничением потока.Мы признаем, что наши пациенты с ХОБЛ были значительно старше контрольной группы. Увеличение возраста связано либо с отсутствием изменений, либо с увеличением пассивного Pcrit (19). Поэтому мы считаем, что разница в возрасте не может объяснить более низкий пассивный Pcrit в группе ХОБЛ. Наконец, возможно, что мы не достигли аналогичной нервно-мышечной пассивности у контрольных пациентов с апноэ и пациентов с ХОБЛ с апноэ. Пациенты с ХОБЛ имеют более высокие респираторные нагрузки и, как следствие, более высокие усилия, что может привести к более сильному неврологическому воздействию как на дыхательные мышцы, так и на мышцы верхних дыхательных путей.Хотя пассивные измерения Pcrit предназначены для описания свойств дыхательных путей в пассивном состоянии, мы не можем исключить, что некоторые из наблюдаемых различий в верхних дыхательных путях отражают различные состояния активации мышц верхних дыхательных путей.
Значение
Настоящая работа имеет несколько клинических последствий. Во-первых, мы показываем, что увеличение объема легких связано с более низким Pcrit (пассивным Pcrit) верхних дыхательных путей. Аналогичным образом, изменения объема легких также могут влиять на пассивный Pcrit у пациентов с ХОБЛ.Операция по уменьшению объема легких (LVRS) — одна из стратегий лечения тяжелой ХОБЛ. Если LVRS повысит пассивный Pcrit, эффективность лечения LVRS может снизиться из-за возникновения OSA. Во-вторых, у пациентов с ХОБЛ короткие периоды тяжелой обструкции верхних дыхательных путей вызывали заметное снижение Те до уровней, сопоставимых с результатами предыдущих исследований, изучающих источники динамической гиперинфляции. Известно, что динамическая гиперинфляция увеличивает работу дыхания и снижает эффективность сна, что может быть связано с утренней усталостью, обычно наблюдаемой у пациентов с ХОБЛ.
ГРАНТЫ
Это исследование финансировалось Национальным институтом сердца, легких и крови, грант RO1-HL-105546 и Conselho Nacional de Desenvolvimento Científico e Tecnológico-Brasil.
РАСКРЫТИЕ ИНФОРМАЦИИ
Автор (ы) не заявляет о конфликте интересов, финансовом или ином.
ВЗНОС АВТОРОВ
Вклад авторов: P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. проанализированные данные; P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. интерпретированные результаты экспериментов; P.J.C.B., P.R.G. и H.S. подготовленные фигурки; P.J.C.B., P.R.G., A.R.S. и H.S. составленная рукопись; P.J.C.B., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. отредактированная и исправленная рукопись; P.J.C.B. и H.S. утвержденная финальная версия рукописи; P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. концепция и дизайн исследования; P.R.G., J.P.K. и H.S. проводил эксперименты.
СПИСОК ЛИТЕРАТУРЫ
1. Американская академия медицины сна. Руководство AASM по оценке сна и связанных с ним событий: правила, терминология и технические спецификации.Вестчестер, Иллинойс: Американская академия медицины сна, 2007. [Google Scholar] 2. Американское торакальное общество. Стандартизация спирометрии, обновление 1994 г. Американское торакальное общество. Am J Respir Crit Care Med 152: 1107–1136, 1995. [PubMed] [Google Scholar] 3. Бреслин Э, ван дер Сханс С., Бреукинк С., Мик П., Мерсер К., Фольц В., Луи С. Восприятие утомляемости и качества жизни у пациентов с ХОБЛ. Грудь 114: 958–964, 1998. [PubMed] [Google Scholar] 4. Каллигаро Г.Л., Рейн Р.И., Бейтман М.Э., Бейтман Э.Д., Купер С.Б.Сравнение динамической гиперинфляции и связанной с ней одышки, вызванной тахипноэ в метрономном ритме, с дополнительными упражнениями. ХОБЛ 11: 105–112, 2014. [PubMed] [Google Scholar] 5. Чин Ч., Киркнесс JP, Патил С.П., Макгинли Б.М., Смит П.Л., Шварц А.Р., Шнайдер Х. Компенсаторные реакции на обструкцию верхних дыхательных путей у мужчин и женщин с ожирением и апноэ. J Appl Physiol 112: 403–410, 2012. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Дуглас, штат Нью-Джерси, Calverley PMA, Leggett RJE, Brash DC, Flenley DC, Brezinova V. Преходящая гипоксемия во сне при хроническом бронхите и эмфиземе.Ланцет 1: 1–4, 1979. [PubMed] [Google Scholar] 7. Иствуд ПР, Платт ПР, Шеперд К., Мэддисон К., Хиллман ДР. Складываемость верхних дыхательных путей при различных концентрациях анестезии пропофолом. Анестезиология 103: 470–477, 2005. [PubMed] [Google Scholar] 8. Eastwood PR, Szollosi I, Platt PR, Hillman DR. Сравнение коллапса верхних дыхательных путей во время наркоза и сна. Ланцет 359: 1207–1209, 2002. [PubMed] [Google Scholar] 9. Gold AR, Gold MS, Харрис К.В., Эспелета В.Дж., Амин М.М., Бродерик Дж.Гиперсонливость, бессонница и патофизиология синдрома сопротивления верхних дыхательных путей. Сон Мед 9: 675–683, 2008. [PubMed] [Google Scholar] 10. Золото AR, Schwartz AR. Критическое давление в глотке. Почему и как использовать назальное постоянное положительное давление в дыхательных путях для диагностики. Грудь 110: 1077–1088, 1996. [PubMed] [Google Scholar] 11. Gorini M, Misuri G, Corrado A, Duranti R, Iandelli I, De Paola E, Scano G. Характер дыхания и задержка углекислого газа при тяжелой хронической обструктивной болезни легких.Грудная клетка 51: 677–683, 1996. [Бесплатная статья PMC] [PubMed] [Google Scholar] 12. Гийемино C, Stoohs R, Clerk A, Cetel M, Maistros P. Причина чрезмерной дневной сонливости. Синдром сопротивления верхних дыхательных путей. Грудь 104: 781–787, 1993. [PubMed] [Google Scholar] 13. Haluszka J, Chartrand DA, Grassino AE, Milic-Emili J. Внутренний ПДКВ и артериальный Pco 2 у стабильных пациентов с хронической обструктивной болезнью легких. Am Rev Respir Dis 141: 1194–1197, 1990. [PubMed] [Google Scholar] 14. Хосино Ю., Аюс Т., Курата С., Аюс Т., Шнайдер Х., Киркнесс Дж. П., Патил С.П., Шварц А.Р., Ои К.Компенсаторные реакции на обструкцию верхних дыхательных путей у здоровых людей под анестезией пропофолом. Респир Физиол Нейробиол 166: 24–31, 2009. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Хаджел Д.В., Мартин Р.Дж., Кейпхарт М., Джонсон Б., Хилл П. Вклад гиповентиляции в десатурацию кислорода во сне при хронической обструктивной болезни легких. J Appl Physiol 55: 669–677, 1983. [PubMed] [Google Scholar] 16. Кайрайтис К., Байт К., Парих Р., Ставрину Р., Уитли Дж. Р., Эмис Т.К. Влияние тракции трахеи на проходимость верхних дыхательных путей у кроликов: роль тканевого давления.Спать 30: 179–186, 2007. [PubMed] [Google Scholar] 17. Ким Дж. Х., Гийемино К. Назомаксиллярный комплекс, нижняя челюсть и нарушение дыхания во сне. Сон Дыхание 15: 185–193, 2011. [PubMed] [Google Scholar] 18. Kinsman RA, Yaroush RA, Fernandez E, Dirks JF, Schocket M, Fukuhara J. Симптомы и переживания при хроническом бронхите и эмфиземе. Грудь 83: 755–761, 1983. [PubMed] [Google Scholar] 19. Киркнесс Дж. П., Шварц А. Р., Шнайдер Х., Пенджаби Н. М., Малый Дж. Дж., Лаффан А. М., МакГинли Б. М., Магнусон Т., Швейцер М., Смит П. Л., Патил С. П..Вклад мужского пола, возраста и ожирения в механическую нестабильность верхних дыхательных путей во время сна. J Appl Physiol 104: 1618–1624, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Krachman SL, Chatila W., Martin UJ, Nugent T, Crocetti J, Gaughan J, Criner GJ. Влияние операции по уменьшению объема легких на качество сна и ночной газообмен у пациентов с тяжелой эмфиземой. Грудь 128: 3221–3228, 2005. [PubMed] [Google Scholar] 21. Leitch AG, Gloney LJ, Leggett RJE. Напряжение газов артериальной крови, ион водорода и электроэнцефалограмма во время сна у пациентов с хронической дыхательной недостаточностью.Грудная клетка 31: 730–735, 1976. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Макгинли Б.М., Шварц А.Р., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Патил С.П. Нервно-мышечная компенсация верхних дыхательных путей во время сна нарушается при обструктивном апноэ во сне. J Appl Physiol 105: 197–205, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Оуэнс Р.Л., Малхотра А., Эккерт Д.Д., Уайт Д.П., Джордан А.С. Влияние объема легких в конце выдоха на измерения гибкости глотки. J Appl Physiol 108: 455–451, 2010.[Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Патил С.П., Пенджаби Н.М., Шнайдер Х., О’Доннелл С.П., Смит П.Л., Шварц А.Р. Упрощенный метод измерения критического давления во время сна в клинических условиях. Am J Respir Crit Care Med 170: 86–93, 2004. [PubMed] [Google Scholar] 25. Патил С.П., Шнайдер Х., Маркс Дж.Дж., Гладмон Э., Шварц А.Р., Смит П.Л. Нейромеханический контроль проходимости верхних дыхательных путей во время сна. J Appl Physiol 102: 547–556, 2007. [PubMed] [Google Scholar] 26. Полномочия CR, Frey WC. Поддержание теста на бодрствование у военнослужащих с синдромом сопротивления верхних дыхательных путей и легким или умеренным апноэ во сне.Сон Дыхание 13: 253–258, 2009. [PubMed] [Google Scholar] 27. Сандерс MH, Ньюман AB, Haggerty CL, Redline S, Lebowitz M, Samet J, O’Connor GT, Punjabi NM, Shahar E. Сон и нарушение дыхания во сне у взрослых с преимущественно легкой формой обструктивного заболевания дыхательных путей. Am J Respir Crit Care Med 167: 7–14, 2003. [PubMed] [Google Scholar] 28. Шнайдер Х., Кришнан В., Пичард Л. Е., Патил С. П., Смит П. Л., Шварц А. Р.. Ответная реакция рабочего цикла вдоха на ограничение потока предсказывает ночную гиповентиляцию. Eur Respir J 33: 1068–1076, 2009.[PubMed] [Google Scholar] 29. Шваб Р.Дж., Пасирштейн М., Пирсон Р., Макли А., Хачадориан Р., Аренс Р., Мэйслин Г., Пак А.И. Выявление анатомических факторов риска обструктивного апноэ во сне верхних дыхательных путей с помощью объемной магнитно-резонансной томографии. Am J Respir Crit Care Med 168: 522–530, 2003. [PubMed] [Google Scholar] 30. Шварц А.Р., О’Доннел С.П., Барон Дж., Шуберт Н., Алам Д., Самади С.Д., Смит П.Л. Гипотонические верхние дыхательные пути при обструктивном апноэ во сне. Роль структур и нервно-мышечной деятельности.Am J Respir Crit Care Med 157: 1051–1057, 1998. [PubMed] [Google Scholar] 31. Сквайер С.Б., Патил С.П., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Шварц А.Р. Влияние объема легких в конце выдоха на сжимаемость верхних дыхательных путей у спящих мужчин и женщин. J Appl Physiol 109: 977–985, 2010. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Тагайто Ю., Исоно С., Реммерс Дж. Э., Танака А., Нишино Т. Объем легких и сжатие пассивной глотки у пациентов с нарушением дыхания во сне. J Appl Physiol 103: 1379–1385, 2007.[PubMed] [Google Scholar] 33. Тут Д.К., Шварц А.Р., Роуч Д., Мудрый Р.А., Пермутт С., Смит П.Л. Положение трахеи и шеи влияет на динамику воздушного потока в верхних дыхательных путях, изменяя длину дыхательных путей. J Appl Physiol 75: 2084–2090, 1993. [PubMed] [Google Scholar] 34. Траск CH, Gress EM. Оксиметрические исследования пациентов с хронической эмфиземой легких, бодрствования и сна. N Engl J Med 266: 639–642, 1962. [PubMed] [Google Scholar] 35. Ван де Грааф ВБ. Торакальное вытяжение за трахею: механизмы и масштабы. J Appl Physiol 70: 1328–1336, 1991.[PubMed] [Google Scholar] 36. Юнес М. Роль механизмов контроля дыхания в патогенезе обструктивных нарушений сна. J Appl Physiol 105: 1389–1405, 2008. [PubMed] [Google Scholar]Влияние увеличения объема легких при хронической обструктивной болезни легких на обструкцию верхних дыхательных путей во время сна
J Appl Physiol (1985). 2015 1 августа; 119 (3): 266–271.
, 1, 2 , 1 , 1 , 1 , 1 , 1 и 1Паоло Биселли
1 Центр расстройств сна Джонса Хопкинса, Подразделение отделения легочной медицины и реанимации, Центр астмы и аллергии Джонса Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Питер Р.Grossman
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Джейсон П. Киркнесс
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Сушил П. Патил
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Филип Л.Smith
1 Центр болезней сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Алан Р. Шварц
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
Hartmut Schneider
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
1 Центр расстройств сна Джонса Хопкинса, отделение легочной медицины и реанимации, Центр астмы и аллергии Джона Хопкинса, Балтимор, Мэриленд; и
2 Hospital Universitário, Университет Сан-Паулу, Сан-Паулу, Бразилия
Автор, ответственный за переписку.Адрес для запросов на перепечатку и другой корреспонденции: Х. Шнайдер, Центр расстройств сна Джонса Хопкинса, Отделение легочной и интенсивной терапии, Центр астмы и аллергии Джонса Хопкинса, 5501 Hopkins Bayview Circle, Балтимор, Мэриленд 21224 (электронная почта: ude.imhj @ 3ienhcsh).Поступила в редакцию 29 мая 2014 г .; Принята к печати 31 мая 2015 г.
Авторские права © Американское физиологическое общество, 2015 г. Эта статья цитируется в других статьях PMC.Abstract
У пациентов с хронической обструктивной болезнью легких (ХОБЛ) наблюдается увеличение объема легких из-за ограничения потока воздуха на выдохе.Увеличение объема легких может повлиять на проходимость верхних дыхательных путей и компенсаторные реакции на ограничение инспираторного потока (IFL) во время сна. Мы предположили, что пациенты с ХОБЛ имеют менее гибкие дыхательные пути, обратно пропорциональные объему их легких, и что наличие ограничения потока выдыхаемого воздуха ограничивает реакции рабочего цикла для защиты вентиляции в присутствии ИФЛ. Мы включили 18 пациентов с ХОБЛ и 18 пациентов контрольной группы, сопоставимых по возрасту, индексу массы тела, полу и тяжести синдрома обструктивного апноэ во сне.Исследования сна, включая количественную оценку воздушного потока при различных уровнях назального давления, были проведены для определения механических свойств верхних дыхательных путей [критическое пассивное давление закрытия (Pcrit)] и для количественной оценки респираторных временных реакций на экспериментально индуцированный IFL. Пациенты с ХОБЛ имели более низкий пассивный Pcrit, чем их контрольная группа (ХОБЛ: -2,8 ± 0,9 см вод.ст. 2 O; контроль: -0,5 ± 0,5 см вод. функциональная остаточная емкость и пассивный Pcrit (−1.7 cmH 2 O / l увеличение функциональной остаточной емкости, r 2 = 0,27, P = 0,002). В ответ на IFL рабочий цикл вдоха увеличился больше ( P = 0,03) у пациентов с ХОБЛ (от 0,40 до 0,54), чем в контроле (от 0,41 до 0,51), и привел к заметному сокращению времени выдоха с 2,5 до 1,5 с ( P <0,01). Пациенты с ХОБЛ имеют менее гибкие дыхательные пути и большую, а не сокращенную компенсационную временную реакцию при обструкции верхних дыхательных путей.Хотя эти временные реакции могут снизить гиповентиляцию, они также могут увеличить риск развития динамической гиперинфляции из-за значительного сокращения времени выдоха.
Ключевые слова: обструкция верхних дыхательных путей, ХОБЛ, обструктивное апноэ во сне, ограничение потока вдоха, объем легких
Хроническая обструктивная болезнь легких (ХОБЛ) является ведущей причиной смерти, инвалидности и снижения качества жизни. Одышка при физической нагрузке остается основной причиной ухудшения качества жизни, а нарушение сна и утренняя усталость являются вторыми по частоте жалобами у этих пациентов (3, 18).В то время как обструктивное апноэ во сне (СОАС) является общепризнанным источником нарушений сна и утренней усталости у пациентов с ХОБЛ, другие маркеры ХОБЛ, такие как гиперинфляция легких (20), усиление дыхательных усилий (9, 12, 26), изменения в газообмен (6, 15, 21, 27, 34) и ограничение потока вдоха также были связаны с нарушениями сна. Понимание того, как эти факторы вызывают нарушения сна, может позволить исследователям разработать конкретные стратегии профилактики и лечения нарушений сна у пациентов с ХОБЛ.
Ограничение потока вдоха является признаком обструкции верхних дыхательных путей, которая возникает у людей с нарушенными механическими свойствами верхних дыхательных путей (10, 25). Механические свойства верхних дыхательных путей лучше всего количественно оценить, определив критическое давление закрытия (Pcrit) во время пассивного состояния нервной системы (пассивное Pcrit) (19, 25). Наша лаборатория недавно показала, что пассивный Pcrit предсказывает восприимчивость к заболеванию апноэ во сне и возрастает с увеличением индекса массы тела (ИМТ) и возраста (19).Более того, наша и другие лаборатории недавно продемонстрировали, что увеличение объема легких снижает пассивный Pcrit у нормальных людей и у пациентов с апноэ во сне (23, 31, 32). Эффект увеличения объема легких у пациентов с ХОБЛ на механические свойства верхних дыхательных путей не был продемонстрирован.
Обструкция верхних дыхательных путей вызывает компенсаторные реакции, которые помогают предотвратить гиповентиляцию. В частности, рабочий цикл вдоха [отношение времени вдоха (Ti) к длине дыхательного цикла] увеличивается в ответ на обструкцию верхних дыхательных путей, и это повышение Ti происходит за счет времени выдоха (Te) (5, 14, 28) .Однако пациенты с ХОБЛ часто демонстрируют длинное Те, чтобы справиться с ограничением потока выдоха и внутренним положительным давлением в конце выдоха (11, 13). Возможно, что наличие ограничения потока выдоха ухудшает реакцию рабочего цикла на обструкцию верхних дыхательных путей у пациентов с ХОБЛ. В настоящем исследовании мы набрали пациентов с ХОБЛ и сопоставили ИМТ, возраст, пол и индекс апноэ и гипопноэ (AHI), чтобы определить 1 ) пассивный Pcrit и 2 ) респираторный временной ответ на экспериментально индуцированную обструкцию верхних дыхательных путей.Мы предполагаем, что 1 ) пациенты с ХОБЛ имеют более низкий пассивный Pcrit (и, следовательно, более низкий риск обструкции верхних дыхательных путей) в сочетании с увеличением объема легких; и что 2 ) компенсаторные временные реакции на обструкцию верхних дыхательных путей снижены у пациентов с ХОБЛ по сравнению с нормальными людьми; и 3 ), что уменьшение временных реакций пропорционально степени ограничения потока выдоха [объем форсированного выдоха за 1 с (FEV 1 )].
МЕТОДЫ
Субъекты
Субъекты были набраны из группы лиц, участвовавших в испытании, изучающем влияние сна на исходы ХОБЛ. В общей сложности 96 пациентов с ХОБЛ и 41 курильщик, не страдающий ХОБЛ, прошли предыдущее исследование сна и были доступны для нашего исследования. Из этой группы было набрано 36 человек (). И мужчины ( n = 12), и женщины ( n = 6), которым был поставлен диагноз ХОБЛ [FEV 1 / форсированная жизненная емкость легких (FVC) <70%], были индивидуально сопоставлены по возрасту, полу, ИМТ и ИАГ. с восемнадцатью субъектами без ХОБЛ.Кроме того, анализ подгруппы был проведен на 12 пациентах с ХОБЛ и 12 контрольной группе, сопоставимых по их механическим свойствам верхних дыхательных путей (пассивный Pcrit) и ИМТ. Исключались пациенты, принимавшие респираторные депрессанты, седативные средства или пероральные стероиды. Субъектов также обследовали на наличие нестабильных сердечно-сосудистых заболеваний, неконтролируемой гипертензии, недавних операций на ротоглотке, неврологических расстройств, почечной и печеночной недостаточности, текущей беременности, нарушений свертываемости крови, психических проблем, среднего состояния покоя O 2 , насыщения гемоглобина <88% и аллергии на лидокаин.Письменное информированное согласие было получено от каждого участника этого исследования, которое было одобрено Наблюдательным советом по исследованиям в области человека Медицинского института Джонса Хопкинса.
Таблица 1.
| Переменная | Контроли | Пациенты с ХОБЛ | P Значение | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| n | 18 | 1816 | 9016 9016 9016 9016|||||||||
| Возраст, лет | 50.3 ± 1,6 | 57,1 ± 1,9 | <0,05 | ||||||||
| Высота, см | 170,0 ± 2,7 | 174,2 ± 2,1 | НС | ||||||||
| Масса, кг | 97,9 ± 6,6 86,5 | 4,1NS | |||||||||
| BMI, кг / м 2 | 31,6 ± 1,6 | 28,6 ± 1,2 | NS | ||||||||
| Пол | 12M; 6 Ф | 12М; 6 F | NS | ||||||||
| Объем легких | |||||||||||
| FEV 1 , литры | 3.1 ± 0,2 | 1,9 ± 0,2 | <0,05 | ||||||||
| ОФВ 1 / ФЖЕЛ,% | 79 ± 1,2 | 54 ± 2,6 | <0,05 | ||||||||
| TLC, литры | 5 | 6,7 ± 0,2 | <0,05 | ||||||||
| RV, литры | 1,9 ± 0,1 | 3,0 ± 0,2 | <0,05 | ||||||||
| FRC, литры | 2,8 ± 0,2 | 4,0 ± 0,2 0.05 | |||||||||
| RV / TLC,% | 33,8 ± 1,8 | 45,5 ± 2,4 | <0,05 | ||||||||
| Полисомнография | мин. ± 15,9 | NS | |||||||||
| Эффективность сна,% TST | 86,9 ± 2,0 | 79,4 ± 3,0 | <0,05 | ||||||||
| NREM,% TST | 84,7 ± 1,5 | 83.9 ± 1,9 | NS | ||||||||
| 1-й этап | 19,2 ± 2,4 | 27,1 ± 5,2 | NS | ||||||||
| 2-й этап | 60,2 ± 2,5 | 50,8 ± 4,3 | NS | 5,2 ± 1,8 | 6,0 ± 2,3 | NS | |||||
| REM,% TST | 15,3 ± 1,5 | 16,1 ± 1,9 | NS | ||||||||
| Всего AHI, событий / ч 28 | 9 ± 8,1 | 28,9 ± 8,6 | NS | ||||||||
| NREM AHI, событий / ч | 27,8 ± 8,1 | 28,2 ± 8,6 | NS | ||||||||
| REM AHI, событий165 | 733,3 ± 10,0 | NS | |||||||||
| % Гипопноэ NREM | 76,9 ± 6,1 | 75,9 ± 6,7 | NS | ||||||||
| % Гипопноэ REM | 7316 ± 7.3 | Артериальная Sa O 2 ,% | |||||||||
| Среднее базовое значение | 96.4 ± 0,4 | 93,9 ± 0,5 | <0,05 | ||||||||
| Среднее низкое значение | 91,5 ± 0,7 | 90,2 ± 0,6 | NS |
Экспериментальные методы
Тестирование функции легких.
Стандартные методы исследования функции легких (CPL Lung Function Analyzer; W.E. Collins, Braintree MA.) Были применены на следующее утро после диагностического исследования сна (2). ОФВ 1 и ФЖЕЛ определяли с помощью спирометрии.Функциональная остаточная емкость (FRC) измерялась с использованием разведения гелия в замкнутом контуре с несколькими вдохами, с медленной жизненной емкостью и резервным объемом выдоха, определяемыми в конце процедуры. Остаточный объем (RV) рассчитывали путем вычитания резервного объема выдоха из FRC. Затем можно определить общую емкость легких, добавив к ПЖ медленную жизненную емкость легких.
Полисомнография.
Стандартные диагностические методы использовались для определения исходных характеристик сна. Для контроля сна и слежения за сном электроды электроэнцефалографа помещали в точки F3-A2, C3-A2 и O1-A2, в дополнение к электродам электромиограммы под подбородком и левому и правому электродам электрокулограммы.Респираторные события оценивались с использованием импедансных торакоабдоминальных ремней для измерения дыхательного усилия, назальная канюля использовалась для количественного определения воздушного потока, а пульсоксиметрия использовалась для мониторинга насыщения гемоглобина кислородом. Апноэ определяли как остановку дыхания на 10 с, в то время как гипопноэ оценивали, когда снижение потока воздуха на 30% сопровождалось десатурацией кислорода ≥4%. Стандартные полисомнографические методы и правила оценки использовались для определения стадии сна и классификации нарушений дыхания во сне в соответствии с рекомендованными в 2007 г. руководящими принципами оценки, установленными Американской академией медицины сна (1).
Установка физиологии дыхания.
В дополнение к стандартным методам полисомнографии, субъект был снабжен гелевой маской, прикрепленной к специально разработанному устройству постоянного положительного давления в дыхательных путях, способному обеспечивать давление от -20 до +20 см вод. Ст. 2 O (Resmed, Bella Vista, NSW, Австралия). Расход воздуха измеряли с помощью пневмотахографа (модель 4830, 0-400 л / мин; Ханс Рудольф, Канзас-Сити, Миссури). Расход и давление регистрировались с частотой дискретизации 100 Гц. Все физиологические сигналы регистрировались и контролировались на компьютерной станции с использованием программного обеспечения Somnologica (Medcare, Buffalo, NY).
Протокол исследования
Первоначально испытуемые прошли диагностическое исследование сна для определения степени нарушения дыхания во сне, которое требовалось для сопоставления людей по AHI и антропометрическим данным (см.). Кроме того, на следующий день после исследования сна проводились функциональные тесты легких для определения общего объема легких и статуса заболевания. Затем мы выполнили последующее исследование сна в течение периода от 2 до 4 недель, чтобы определить механические свойства верхних дыхательных путей пациентов (пассивный Pcrit) и компенсаторные временные реакции на обструкцию верхних дыхательных путей.Процедуры определения Pcrit были подробно описаны ранее (24), проиллюстрированы и кратко описаны ниже.
Протокол эксперимента. Схематическая диаграмма экспериментальных протоколов ( вверху, ) и полисомнографических ответов ( внизу, ) во время сна с медленным движением глаз у мужчины с апноэ. Исходный уровень ( слева, ): назальное давление было отрегулировано до эффективного постоянного положительного давления в дыхательных путях и удерживалось не менее 3 минут (удерживающее давление) для установления стабильной модели дыхания без ограничения потока (см. График потока, внизу слева, ).Пассивная обструкция верхних дыхательных путей (, посередине слева, ): была проведена серия кратковременных (5 вдохов) падений назального давления в результате удержания давления без одновременной активации ЭМГ. Во время этих капель возникла обструкция верхних дыхательных путей, на что указывает ограничение потока вдоха, как показано на графике потока ниже. Sa O 2 , артериальный O 2 насыщение; Vi max , максимальный инспираторный поток.
Пассивное состояние: кратковременные периоды обструкции верхних дыхательных путей.
Мы использовали пассивный Pcrit для определения свойств верхних дыхательных путей при низкой гипотонической нервно-мышечной активности. Во время стабильного сна с медленным движением глаз назальное давление постепенно повышалось до тех пор, пока не было достигнуто носовое дыхание без ограничения потока. Затем назальное давление снижали ступенчато с шагом от 1 до 2 см вод. Падение давления будет прервано и повторено, если возникнет возбуждение или повышение активности ЭМГ без возбуждения.Периоды дыхания исключались, если были пробуждения от стабильного сна.
Сжимаемость верхних дыхательных путей.
Зависимость «давление-поток» (максимальный инспираторный поток в условиях ограниченного потока) была создана для каждого субъекта путем построения графика максимального воздушного потока из вдохов 3–5 каждого перепада давления, как описано ранее (30). Линейная регрессия использовалась для определения назального давления, при котором поток был нулевым, что указывает на закупорку верхних дыхательных путей (пассивный Pcrit), как показано на рис.
Ответы по времени дыхания.
Ti, Te, общее время каждого вдоха (Ttot) и частота дыхания были определены. Рабочий цикл вдоха (Ti / Tобщ) был зарегистрирован в условиях без ограничения потока, а также во время вдохов с острым умеренным или сильным ограничением потока, определяемым как средняя пиковая скорость потока воздуха на вдохе 50–150 мл / с () ( 28). Изменение временных параметров от исходного уровня до состояния обструкции верхних дыхательных путей использовалось для определения индивидуальной силы респираторных временных реакций на обструкцию верхних дыхательных путей.
Статистический анализ
Отдельные значения были усреднены и сравнены как для ХОБЛ, так и для контрольной группы с использованием непарного критерия Стьюдента t . Дальнейший анализ подгрупп проводился у пациентов с ОАС и без него. Изменения в ответе рабочего цикла сравнивали между группами пациентов с ХОБЛ и контрольной группой с помощью непарного t -теста. Сравнения до и после индукции ограничения инспираторного потока были выполнены с использованием парного теста t . Регрессионный анализ между FRC и пассивным Pcrit был выполнен для определения связи между объемом легких и сжимаемостью верхних дыхательных путей.Значение P 0,05 считалось статистически значимым. Все данные представлены как средние значения ± SE, если не указано иное.
РЕЗУЛЬТАТЫ
Характеристики субъектов
Демографические, антропометрические, полисомнографические и легочные статистические данные для всех 18 участников ХОБЛ и 18 контрольных групп, соответствующих AHI, отображаются в. Сравнение антропометрических переменных для субъектов, индивидуально подобранных по возрасту (57,1 ± 1,9 против 50,3 ± 1,6 года), полу (12 мужчин; 6 женщин), ИМТ (28.8 ± 1,3 против 31,6 ± 1,6 кг / м 2 ), и AHI (29 ± 8 против 29 ± 9 событий / ч) показаны на. У половины испытуемых (7 мужчин и 2 женщины из каждой группы) было нарушение дыхания во сне с частотой событий> 10 событий / час. Субъекты с ХОБЛ, по сравнению с контрольными субъектами, имели ОФВ 1 1,9 ± 0,2 против 3,1 ± 0,2 литра и ОФВ 1 / ФЖЕЛ 54 ± 0,0 против 79 ± 1,2%. Точно так же объемы легких были увеличены у пациентов с ХОБЛ по сравнению с контрольной группой: общая емкость легких составляла 6,7 ± 0,2 против 5,9 ± 0.3 литра, RV составляла 3,0 ± 0,2 против 1,9 ± 0,1 литра, а FRC составляла 4,0 ± 0,2 против 2,8 ± 0,2 литра.
Острые (пассивные) механические свойства верхних дыхательных путей
Субъекты с ХОБЛ имели средний пассивный Pcrit -2,8 см вод. t -тест;). Для подгруппы без ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -4,6 см вод.ст. 2 O по сравнению с -0,8 см вод.02; непарный т -тест). Для подгруппы с ОАС у субъектов с ХОБЛ средний пассивный Pcrit составлял -1,0 см вод. Ст. 2 O по сравнению с -0,2 см вод. Была обнаружена значимая связь между FRC и пассивным Pcrit ( r 2 = 0,27, P = 0,002), как показано на рисунке, что указывает на то, что пациенты с более высокими объемами легких имели более низкие значения пассивного Pcrit.
Измерения пассивного критического давления закрытия (Pcrit) у пациентов с хронической обструктивной болезнью легких (ХОБЛ) и контрольной группы.График представляет средние значения пассивного Pcrit для пациентов с ХОБЛ и подобранной контрольной группы. Слева : все пациенты. Средний : пациенты с необструктивным апноэ сна (СОАС). Справа : пациенты с СОАС. Значения представляют собой средние значения ± SE. Коллапсируемость верхних дыхательных путей (пассивный Pcrit) ниже у пациентов с ХОБЛ по сравнению с субъектами, подобранными по возрасту, полу, индексу массы тела и индексу респираторных нарушений ( P = 0,03). Эта разница кажется более значительной у пациентов, не страдающих апноэ, но больше не заметна у пациентов с апноэ.NS, незначительно.
Пассивная зависимость Pcrit от функциональной остаточной емкости (FRC). График представляет пассивную зависимость Pcrit и FRC с линейной регрессией с использованием всех значений предмета. □, средства контроля, не относящиеся к OSA; ◇, органы управления OSA; ■ ХОБЛ без ОАС; ⧫ OSA ХОБЛ. Была статистически значимая связь между FRC и коллапсируемостью верхних дыхательных путей (пассивный Pcrit) у всех субъектов ( P = 0,002, r 2 = 0,27). Увеличение FRC на 1 литр было связано со снижением пассивного Pcrit на ~ 2 см вод. Ст.
При одномерном анализе была выявлена статистически значимая связь между значениями пассивного Pcrit и как FRC ( P = 0,002), так и ИМТ ( P = 0,003). В многомерном анализе оба фактора оставались определяющими для уровня пассивного Pcrit (FRC, P = 0,021; BMI, P = 0,041;).
Таблица 2.
Связь пассивного Pcrit с BMI и FRC
| Модель 1 | Модель 2 | Модель 3 | P значение | β-коэффициент | P значение | β-коэффициент | P Значение | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| FRC, см вод. Ст. 2 O / l | −1.66 ± 0,50 | 0,002 | −1,25 ± 0,51 | 0,021 | |||||||||||||
| ИМТ, кг / м 2 | 0,25 ± 0,08 | 9080,042 | |||||||||||||||
Острые респираторные временные ответы
В подгруппе из 12 пациентов, спаренных для анализа временных ответов, контрольная группа имела ИАГ 29,8 ± 7,5 событий / ч, а группа ХПК имела ИАГ 31.2 ± 6,8 событий / час. Среднее удерживающее давление составляло 8,8 ± 0,8 см вод. Ст. 2 O в контроле и 8,1 ± 1,0 см вод. Ст. 2 O у пациентов с ХОБЛ. Среднее дельта-давление, необходимое для серьезного ограничения потока вдоха, составляло 6,4 ± 0,8 см вод. Ст. 2 O для контроля и 7,0 ± 0,9 см вод.
Респираторные реакции по времени оценивались путем сравнения состояния без ограничения потока (исходный уровень) с периодами тяжелой обструкции верхних дыхательных путей. Пик инспираторного потока воздуха на исходном уровне и тяжелая обструкция верхних дыхательных путей были одинаковыми в обеих группах, снизившись с 383 ± 49 до 105 ± 11 мл / с в контроле и с 387 ± 47 до 111 ± 12 мл / с у пациентов с ХОБЛ.Параметры времени дыхания при исходном уровне, дыхании без ограничения потока и в ответ на серьезную степень ограничения потока вдоха суммированы в. Как в условиях без ограничения потока, так и в условиях с ограниченным потоком пациенты с ХОБЛ и контрольная группа имели одинаковые временные индексы. В то время как в контрольной группе увеличение рабочего цикла на ~ 25% с 0,41 до 0,51, у пациентов с ХОБЛ было увеличение на ~ 40% с 0,40 до 0,55 ( P = 0,03 для сравнения увеличения рабочего цикла). Те снизились в среднем с 2.От 5 до 1,5 с в группе ХОБЛ ( P <0,01) и в согласованном контроле от 2,4 до 1,8 с ( P <0,01). Ttot снизился при ХОБЛ с 4,1 до 3,3 с ( P <0,05) и в контроле с 3,9 до 3,6 с (незначительно). Ti увеличился с 1,5 до 1,8 с ( P <0,01) у пациентов с ХОБЛ и с 1,6 до 1,8 с в контроле ( P <0,05). Ни один из ответов по времени вдоха или выдоха не коррелировал с уровнем обструкции (FEV 1 ) у пациентов с ХОБЛ.
Таблица 3.
Временные реакции на индуцированное ограничение потока
| Время вдоха, с | Время выдоха, с | Общее время, с | Рабочий цикл, частота дыхания | 906 / мин||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Control | COPD | Control | COPD | Control | COPD | Control | COPD | Control Base | 9016 9016 ± 0,1| 1,5 ± 0,1 | 2,4 ± 0,2 | 2,5 ± 0,3 | 3,9 ± 0,2 | 4,1 ± 0,3 | 0,41 ± 0,02 | 0,40 ± 0,02 | 16,0 ± 0,9 | 15,5 ± 0,9 | | |
| IFL | 1,8 ± 0,1 * | 1,8 ± 0,1 * | 1,8 ± 0,2 * | 1,5 ± 0,1 * | 3,6 ± 0,3 | 3,3 ± 0,2 * | 0,51 ± 0,02 * | 0.55 ± 0,02 * † | 18,1 ± 1,6 | 18,9 ± 1,1 * | |||||||||
ОБСУЖДЕНИЕ
Основные результаты настоящего исследования заключаются в том, что пациенты с ХОБЛ имеют менее гибкие верхние дыхательные пути, чем их возраст. пол, ИМТ и AHI соответствовали контрольным субъектам, и что пассивный Pcrit обратно коррелировал с остаточным объемом легких. Проходимость дыхательных путей была увеличена у пациентов с ХОБЛ по сравнению с подобранной контрольной группой, но эта разница была намного меньше и несущественной в подгруппе пациентов с апноэ во сне, что указывает на то, что статус болезни апноэ во сне влияет на механизмы, которые опосредуют объем легких и пассивную взаимосвязь Pcrit.Во-вторых, в отличие от нашей гипотезы, пациенты с ХОБЛ продемонстрировали повышенную, а не пониженную реакцию рабочего цикла на обструкцию верхних дыхательных путей по сравнению с подобранной контрольной группой. Это увеличение рабочего цикла было связано с увеличением частоты дыхания и заметным снижением Те, которые являются известными факторами риска динамической гиперинфляции. Взятые вместе, наши данные показывают, что, хотя увеличение объема легких может снизить восприимчивость к OSA у пациентов с ХОБЛ, временные реакции на обструкцию верхних дыхательных путей могут способствовать динамической гиперинфляции.
Одним из основных клинических признаков ХОБЛ является прогрессирующее увеличение объема легких. У нашей популяции пациентов была умеренная степень ХОБЛ с FEV 1 / FVC в диапазоне от 50 до 70% от прогнозируемого и средним увеличением FRC на 1,2 литра по сравнению с контролем. Увеличение объема легких снижает разрушаемость верхних дыхательных путей у здоровых людей и пациентов с СОАС (23, 31, 32). Предлагаемый механизм этой связи — усиление тракции каудальной трахеи во время раздувания легких, в результате чего верхние дыхательные пути становятся более жесткими и менее гибкими (16).Теперь мы распространили эти результаты на пациентов с ХОБЛ с увеличенным объемом легких и обнаружили аналогичную взаимосвязь между FRC и верхней коллапсируемостью на ~ 2 см вод. Ст. 2 O снижение пассивного Pcrit на увеличение FRC на литр. Более низкий пассивный Pcrit связан с меньшим риском развития ОАС. Таким образом, оказывается, что пациенты с ХОБЛ с увеличенным объемом легких менее подвержены развитию ОАС.
Мы наблюдали более низкий пассивный Pcrit у пациентов с ХОБЛ, не страдающих апноэ, по сравнению с их сопоставимой группой контроля без апноэ.Можно предположить, что это различие связано с аномально высоким пассивным Pcrit в контрольной группе, а не со снижением пассивного Pcrit в группе ХОБЛ. Наша лаборатория ранее продемонстрировала, что пассивный Pcrit может быть одинаковым у лиц без OSA и OSA, в то время как активный Pcrit ниже у здоровых людей по сравнению с пациентами с апноэ, даже при сопоставлении с пассивным Pcrit (19, 25). Пассивный Pcrit выявляет механические свойства дыхательных путей в ненейронно активированном состоянии и приближается к измерениям Pcrit под анестезией.Фактически, некоторые отчеты во время анестезии также показали значения Pcrit, близкие к атмосферным, особенно при изучении пациентов старшего возраста (7, 8). Таким образом, мы предполагаем, что разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и контрольной группой не связана с аномально высоким Pcrit в нормальном контроле, а, скорее, из-за снижения пассивного Pcrit у пациентов с неапнеическим ХОБЛ.
Хотя имелась разница в пассивном Pcrit между пациентами с ХОБЛ, не страдающими апноэ, и их контрольной группой, мы больше не наблюдали этой разницы при сравнении пациентов с апноэ с ХОБЛ и их контрольной группы.Мы предлагаем несколько механизмов для объяснения этой дифференциальной реакции. Во-первых, несколько исследователей продемонстрировали, что пассивный Pcrit снижается с увеличением объема легких, что связано с каудальным трактом верхних дыхательных путей (31, 33, 35). Люди с апноэ имеют более крупный язык (29) и часто узкое, высоко дугообразное твердое небо (17), оба из которых могли притупить эффект растяжения, обеспечиваемый увеличением объема легких. Во-вторых, также возможно, что увеличение объема легких снижает пассивный Pcrit за счет нервной стимуляции внутри- или внелегочных рецепторов растяжения.Люди с апноэ могут иметь ослабленную нервную реакцию на увеличение объема легких, аналогичную ослаблению нервного контроля над верхними дыхательными путями в ответ на обструкцию верхних дыхательных путей (22, 25). В качестве альтернативы, подобно рефлексу Геринга-Брейера, который требует больших объемов вдоха для вызова рефлекторного ответа, пассивные ответы Pcrit также могут зависеть от степени гиперинфляции. У некоторых пациентов с апноэ с ХОБЛ увеличение объема легких могло быть недостаточно большим для снижения пассивного Pcrit.Чтобы определить, почему пациенты с неапноэ с ХОБЛ имеют более низкий пассивный Pcrit по сравнению с контрольной группой, в то время как пациенты с апноэ с ХОБЛ имеют такой же пассивный Pcrit, чем пациенты с апноэ, необходимы механические эксперименты, включающие оценку нервной и мышечной активности.
При обструкции верхних дыхательных путей увеличение рабочего цикла является одним из основных способов поддержания вентиляции. Чем больше увеличение рабочего цикла, тем лучше люди поддерживают минутную вентиляцию (5, 28, 36).В нашей настоящей работе мы наблюдали, что пациенты с ХОБЛ, по сравнению с подобранной контрольной группой, имеют большее увеличение рабочего цикла при обструкции верхних дыхательных путей. Таким образом, пациенты с ХОБЛ, по-видимому, лучше защищены от развития гиповентиляции по сравнению с контрольной группой, когда сталкиваются с обструкцией верхних дыхательных путей. Напротив, пациенты с ХОБЛ нуждаются в очень длительном Те, чтобы предотвратить динамическую гиперинфляцию легких. В настоящей работе мы наблюдали, что пациенты с ХОБЛ, а также контрольная группа, снижали Те при ограничении инспираторного потока.Хотя умеренное снижение Те обычно не влияет на механику дыхания, наблюдаемого снижения Те на ~ 50% может быть достаточно, чтобы вызвать динамическую гиперинфляцию. Фактически, подобное снижение Те при использовании метронома во время бодрствования вызывало динамическую гиперинфляцию у пациентов с умеренной ХОБЛ (4). Субъекты с нормальной функцией легких могут хорошо переносить снижение Те. Однако у субъектов с ограничением потока вдоха при ХОБЛ наблюдаемое снижение Те может вызывать динамическую гиперинфляцию во время сна.
У настоящего исследования есть несколько сильных сторон и ограничений. Первым преимуществом является наш подход к сопоставлению пациентов с ХОБЛ и контрольной группы по возрасту, тяжести апноэ во сне (AHI), полу и ИМТ, которые являются известными факторами риска разрушения верхних дыхательных путей. Когда мы проанализировали только пациентов без ОАС, различия в разборчивости верхних дыхательных путей были даже больше, чем при сравнении всей группы, что позволяет предположить, что мы, возможно, недооценили влияние повышенного объема легких на проходимость верхних дыхательных путей.Вторая сильная сторона — это наш экспериментальный план для определения временных параметров в ответ на обструкцию верхних дыхательных путей. В предыдущих исследованиях наша лаборатория продемонстрировала, что рабочий цикл увеличивается с тяжестью обструкции верхних дыхательных путей в зависимости от дозы. Поэтому мы установили одинаковую степень обструкции верхних дыхательных путей для всех участников нашего исследования. Этот экспериментальный план позволил нам уменьшить вариабельность временных ответов, наблюдая при этом дифференциальные ответы между пациентами с ХОБЛ и контрольной группой.Напротив, несмотря на лучшее соответствие пациентов с ХОБЛ и контрольной группы по статусу заболевания (AHI), возрасту и полу, у нас есть только перекрестные данные по пассивному Pcrit для участников нашего исследования. Возможно, мы недооценили влияние объема легких на сжимаемость верхних дыхательных путей из-за систематической ошибки отбора. Мы также не измеряли внутреннее положительное давление в конце выдоха, которое, вероятно, присутствует у многих наших пациентов с ХОБЛ и может быть изменено экспериментально вызванным ограничением потока.Мы признаем, что наши пациенты с ХОБЛ были значительно старше контрольной группы. Увеличение возраста связано либо с отсутствием изменений, либо с увеличением пассивного Pcrit (19). Поэтому мы считаем, что разница в возрасте не может объяснить более низкий пассивный Pcrit в группе ХОБЛ. Наконец, возможно, что мы не достигли аналогичной нервно-мышечной пассивности у контрольных пациентов с апноэ и пациентов с ХОБЛ с апноэ. Пациенты с ХОБЛ имеют более высокие респираторные нагрузки и, как следствие, более высокие усилия, что может привести к более сильному неврологическому воздействию как на дыхательные мышцы, так и на мышцы верхних дыхательных путей.Хотя пассивные измерения Pcrit предназначены для описания свойств дыхательных путей в пассивном состоянии, мы не можем исключить, что некоторые из наблюдаемых различий в верхних дыхательных путях отражают различные состояния активации мышц верхних дыхательных путей.
Значение
Настоящая работа имеет несколько клинических последствий. Во-первых, мы показываем, что увеличение объема легких связано с более низким Pcrit (пассивным Pcrit) верхних дыхательных путей. Аналогичным образом, изменения объема легких также могут влиять на пассивный Pcrit у пациентов с ХОБЛ.Операция по уменьшению объема легких (LVRS) — одна из стратегий лечения тяжелой ХОБЛ. Если LVRS повысит пассивный Pcrit, эффективность лечения LVRS может снизиться из-за возникновения OSA. Во-вторых, у пациентов с ХОБЛ короткие периоды тяжелой обструкции верхних дыхательных путей вызывали заметное снижение Те до уровней, сопоставимых с результатами предыдущих исследований, изучающих источники динамической гиперинфляции. Известно, что динамическая гиперинфляция увеличивает работу дыхания и снижает эффективность сна, что может быть связано с утренней усталостью, обычно наблюдаемой у пациентов с ХОБЛ.
ГРАНТЫ
Это исследование финансировалось Национальным институтом сердца, легких и крови, грант RO1-HL-105546 и Conselho Nacional de Desenvolvimento Científico e Tecnológico-Brasil.
РАСКРЫТИЕ ИНФОРМАЦИИ
Автор (ы) не заявляет о конфликте интересов, финансовом или ином.
ВЗНОС АВТОРОВ
Вклад авторов: P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. проанализированные данные; P.J.C.B., P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. интерпретированные результаты экспериментов; P.J.C.B., P.R.G. и H.S. подготовленные фигурки; P.J.C.B., P.R.G., A.R.S. и H.S. составленная рукопись; P.J.C.B., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. отредактированная и исправленная рукопись; P.J.C.B. и H.S. утвержденная финальная версия рукописи; P.R.G., J.P.K., S.P.P., P.L.S., A.R.S. и H.S. концепция и дизайн исследования; P.R.G., J.P.K. и H.S. проводил эксперименты.
СПИСОК ЛИТЕРАТУРЫ
1. Американская академия медицины сна. Руководство AASM по оценке сна и связанных с ним событий: правила, терминология и технические спецификации.Вестчестер, Иллинойс: Американская академия медицины сна, 2007. [Google Scholar] 2. Американское торакальное общество. Стандартизация спирометрии, обновление 1994 г. Американское торакальное общество. Am J Respir Crit Care Med 152: 1107–1136, 1995. [PubMed] [Google Scholar] 3. Бреслин Э, ван дер Сханс С., Бреукинк С., Мик П., Мерсер К., Фольц В., Луи С. Восприятие утомляемости и качества жизни у пациентов с ХОБЛ. Грудь 114: 958–964, 1998. [PubMed] [Google Scholar] 4. Каллигаро Г.Л., Рейн Р.И., Бейтман М.Э., Бейтман Э.Д., Купер С.Б.Сравнение динамической гиперинфляции и связанной с ней одышки, вызванной тахипноэ в метрономном ритме, с дополнительными упражнениями. ХОБЛ 11: 105–112, 2014. [PubMed] [Google Scholar] 5. Чин Ч., Киркнесс JP, Патил С.П., Макгинли Б.М., Смит П.Л., Шварц А.Р., Шнайдер Х. Компенсаторные реакции на обструкцию верхних дыхательных путей у мужчин и женщин с ожирением и апноэ. J Appl Physiol 112: 403–410, 2012. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Дуглас, штат Нью-Джерси, Calverley PMA, Leggett RJE, Brash DC, Flenley DC, Brezinova V. Преходящая гипоксемия во сне при хроническом бронхите и эмфиземе.Ланцет 1: 1–4, 1979. [PubMed] [Google Scholar] 7. Иствуд ПР, Платт ПР, Шеперд К., Мэддисон К., Хиллман ДР. Складываемость верхних дыхательных путей при различных концентрациях анестезии пропофолом. Анестезиология 103: 470–477, 2005. [PubMed] [Google Scholar] 8. Eastwood PR, Szollosi I, Platt PR, Hillman DR. Сравнение коллапса верхних дыхательных путей во время наркоза и сна. Ланцет 359: 1207–1209, 2002. [PubMed] [Google Scholar] 9. Gold AR, Gold MS, Харрис К.В., Эспелета В.Дж., Амин М.М., Бродерик Дж.Гиперсонливость, бессонница и патофизиология синдрома сопротивления верхних дыхательных путей. Сон Мед 9: 675–683, 2008. [PubMed] [Google Scholar] 10. Золото AR, Schwartz AR. Критическое давление в глотке. Почему и как использовать назальное постоянное положительное давление в дыхательных путях для диагностики. Грудь 110: 1077–1088, 1996. [PubMed] [Google Scholar] 11. Gorini M, Misuri G, Corrado A, Duranti R, Iandelli I, De Paola E, Scano G. Характер дыхания и задержка углекислого газа при тяжелой хронической обструктивной болезни легких.Грудная клетка 51: 677–683, 1996. [Бесплатная статья PMC] [PubMed] [Google Scholar] 12. Гийемино C, Stoohs R, Clerk A, Cetel M, Maistros P. Причина чрезмерной дневной сонливости. Синдром сопротивления верхних дыхательных путей. Грудь 104: 781–787, 1993. [PubMed] [Google Scholar] 13. Haluszka J, Chartrand DA, Grassino AE, Milic-Emili J. Внутренний ПДКВ и артериальный Pco 2 у стабильных пациентов с хронической обструктивной болезнью легких. Am Rev Respir Dis 141: 1194–1197, 1990. [PubMed] [Google Scholar] 14. Хосино Ю., Аюс Т., Курата С., Аюс Т., Шнайдер Х., Киркнесс Дж. П., Патил С.П., Шварц А.Р., Ои К.Компенсаторные реакции на обструкцию верхних дыхательных путей у здоровых людей под анестезией пропофолом. Респир Физиол Нейробиол 166: 24–31, 2009. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Хаджел Д.В., Мартин Р.Дж., Кейпхарт М., Джонсон Б., Хилл П. Вклад гиповентиляции в десатурацию кислорода во сне при хронической обструктивной болезни легких. J Appl Physiol 55: 669–677, 1983. [PubMed] [Google Scholar] 16. Кайрайтис К., Байт К., Парих Р., Ставрину Р., Уитли Дж. Р., Эмис Т.К. Влияние тракции трахеи на проходимость верхних дыхательных путей у кроликов: роль тканевого давления.Спать 30: 179–186, 2007. [PubMed] [Google Scholar] 17. Ким Дж. Х., Гийемино К. Назомаксиллярный комплекс, нижняя челюсть и нарушение дыхания во сне. Сон Дыхание 15: 185–193, 2011. [PubMed] [Google Scholar] 18. Kinsman RA, Yaroush RA, Fernandez E, Dirks JF, Schocket M, Fukuhara J. Симптомы и переживания при хроническом бронхите и эмфиземе. Грудь 83: 755–761, 1983. [PubMed] [Google Scholar] 19. Киркнесс Дж. П., Шварц А. Р., Шнайдер Х., Пенджаби Н. М., Малый Дж. Дж., Лаффан А. М., МакГинли Б. М., Магнусон Т., Швейцер М., Смит П. Л., Патил С. П..Вклад мужского пола, возраста и ожирения в механическую нестабильность верхних дыхательных путей во время сна. J Appl Physiol 104: 1618–1624, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Krachman SL, Chatila W., Martin UJ, Nugent T, Crocetti J, Gaughan J, Criner GJ. Влияние операции по уменьшению объема легких на качество сна и ночной газообмен у пациентов с тяжелой эмфиземой. Грудь 128: 3221–3228, 2005. [PubMed] [Google Scholar] 21. Leitch AG, Gloney LJ, Leggett RJE. Напряжение газов артериальной крови, ион водорода и электроэнцефалограмма во время сна у пациентов с хронической дыхательной недостаточностью.Грудная клетка 31: 730–735, 1976. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Макгинли Б.М., Шварц А.Р., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Патил С.П. Нервно-мышечная компенсация верхних дыхательных путей во время сна нарушается при обструктивном апноэ во сне. J Appl Physiol 105: 197–205, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Оуэнс Р.Л., Малхотра А., Эккерт Д.Д., Уайт Д.П., Джордан А.С. Влияние объема легких в конце выдоха на измерения гибкости глотки. J Appl Physiol 108: 455–451, 2010.[Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Патил С.П., Пенджаби Н.М., Шнайдер Х., О’Доннелл С.П., Смит П.Л., Шварц А.Р. Упрощенный метод измерения критического давления во время сна в клинических условиях. Am J Respir Crit Care Med 170: 86–93, 2004. [PubMed] [Google Scholar] 25. Патил С.П., Шнайдер Х., Маркс Дж.Дж., Гладмон Э., Шварц А.Р., Смит П.Л. Нейромеханический контроль проходимости верхних дыхательных путей во время сна. J Appl Physiol 102: 547–556, 2007. [PubMed] [Google Scholar] 26. Полномочия CR, Frey WC. Поддержание теста на бодрствование у военнослужащих с синдромом сопротивления верхних дыхательных путей и легким или умеренным апноэ во сне.Сон Дыхание 13: 253–258, 2009. [PubMed] [Google Scholar] 27. Сандерс MH, Ньюман AB, Haggerty CL, Redline S, Lebowitz M, Samet J, O’Connor GT, Punjabi NM, Shahar E. Сон и нарушение дыхания во сне у взрослых с преимущественно легкой формой обструктивного заболевания дыхательных путей. Am J Respir Crit Care Med 167: 7–14, 2003. [PubMed] [Google Scholar] 28. Шнайдер Х., Кришнан В., Пичард Л. Е., Патил С. П., Смит П. Л., Шварц А. Р.. Ответная реакция рабочего цикла вдоха на ограничение потока предсказывает ночную гиповентиляцию. Eur Respir J 33: 1068–1076, 2009.[PubMed] [Google Scholar] 29. Шваб Р.Дж., Пасирштейн М., Пирсон Р., Макли А., Хачадориан Р., Аренс Р., Мэйслин Г., Пак А.И. Выявление анатомических факторов риска обструктивного апноэ во сне верхних дыхательных путей с помощью объемной магнитно-резонансной томографии. Am J Respir Crit Care Med 168: 522–530, 2003. [PubMed] [Google Scholar] 30. Шварц А.Р., О’Доннел С.П., Барон Дж., Шуберт Н., Алам Д., Самади С.Д., Смит П.Л. Гипотонические верхние дыхательные пути при обструктивном апноэ во сне. Роль структур и нервно-мышечной деятельности.Am J Respir Crit Care Med 157: 1051–1057, 1998. [PubMed] [Google Scholar] 31. Сквайер С.Б., Патил С.П., Шнайдер Х., Киркнесс Дж. П., Смит П.Л., Шварц А.Р. Влияние объема легких в конце выдоха на сжимаемость верхних дыхательных путей у спящих мужчин и женщин. J Appl Physiol 109: 977–985, 2010. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Тагайто Ю., Исоно С., Реммерс Дж. Э., Танака А., Нишино Т. Объем легких и сжатие пассивной глотки у пациентов с нарушением дыхания во сне. J Appl Physiol 103: 1379–1385, 2007.[PubMed] [Google Scholar] 33. Тут Д.К., Шварц А.Р., Роуч Д., Мудрый Р.А., Пермутт С., Смит П.Л. Положение трахеи и шеи влияет на динамику воздушного потока в верхних дыхательных путях, изменяя длину дыхательных путей. J Appl Physiol 75: 2084–2090, 1993. [PubMed] [Google Scholar] 34. Траск CH, Gress EM. Оксиметрические исследования пациентов с хронической эмфиземой легких, бодрствования и сна. N Engl J Med 266: 639–642, 1962. [PubMed] [Google Scholar] 35. Ван де Грааф ВБ. Торакальное вытяжение за трахею: механизмы и масштабы. J Appl Physiol 70: 1328–1336, 1991.[PubMed] [Google Scholar] 36. Юнес М. Роль механизмов контроля дыхания в патогенезе обструктивных нарушений сна. J Appl Physiol 105: 1389–1405, 2008. [PubMed] [Google Scholar]объемов легких — Physiopedia
Объем легких также известен как объем дыхания. Это относится к объему газа в легких в данный момент дыхательного цикла. Емкость легких определяется суммированием различных объемов легких. Средняя общая емкость легких взрослого мужчины составляет около 6 литров воздуха.Измерение объема легких является неотъемлемой частью исследования функции легких. Эти объемы имеют тенденцию меняться в зависимости от глубины дыхания, этнической принадлежности, пола, возраста, состава тела [1] и некоторых респираторных заболеваний. Некоторые объемы легких можно измерить с помощью спирометрии — дыхательный объем, резервный объем вдоха и резервный объем выдоха. Однако измерение остаточного объема, функциональной остаточной емкости и общей емкости легких осуществляется с помощью плетизмографии тела, азотного вымывания и разбавления гелием.
Это количество воздуха, которое можно вдохнуть или выдохнуть в течение одного дыхательного цикла. [2] . На нем изображены функции дыхательных центров, дыхательных мышц и механика легких и грудной стенки [3] .
Нормальное значение для взрослых составляет 10% жизненной емкости легких (ЖЕЛ), приблизительно 300–500 мл (6-8 мл / кг) [3] ; но может увеличить VC до 50% на упражнении [4]
- Резервный объем вдоха (IRV)
Это количество воздуха, которое можно принудительно вдохнуть после нормального дыхательного объема.ИРВ обычно оставляют в резерве, но используют при глубоком дыхании. Нормальное значение для взрослых — 1900-3300 мл.
- Резервный объем выдоха (ERV)
Это объем воздуха, который можно принудительно выдохнуть после выдоха нормального дыхательного объема. Нормальное значение для взрослых составляет 700-1200 мл. ERV снижается при ожирении, асците или после операции на верхних отделах брюшной полости [3]
Это объем воздуха, остающийся в легких после максимального выдоха. Нормальное значение для взрослых составляет 1200 мл (20-25 мл / кг).Он косвенно измеряется путем суммирования FRC и ERV и не может быть измерен спирометрией.
При обструктивных заболеваниях легких с особенностями неполного опорожнения легких и захвата воздуха ПЖ может быть значительно высоким. ПЖ также можно выразить в виде процента от общей емкости легких, и значения, превышающие 140%, значительно увеличивают риски баротравмы, пневмоторакса, инфекции и снижения венозного возврата из-за высокого внутригрудного давления, как это было замечено у пациентов с высоким ПЖ, которым требуется хирургическое вмешательство. Таким образом, механическая вентиляция требует высокого давления в периоперационном периоде. [5]
Это максимальный объем воздуха, который можно вдохнуть после состояния покоя. Он рассчитывается как сумма резервного объема вдоха и дыхательного объема. IC = IRV + TV
Это максимальный объем воздуха, который могут вместить легкие, или сумма всех отсеков объема или объем воздуха в легких после максимального вдоха. Нормальное значение составляет около 6000 мл (4-6 л). TLC рассчитывается путем суммирования четырех основных объемов легких (TV, IRV, ERV, RV).
TLC может увеличиваться у пациентов с обструктивными дефектами, такими как эмфизема, и снижаться у пациентов с рестриктивными аномалиями, включая аномалии грудной стенки и кифосколиоз. [6] .
Это общее количество выдыхаемого воздуха после максимального вдоха. Ценность составляет около 4800 мл, и она варьируется в зависимости от возраста и размера тела. Он рассчитывается путем суммирования дыхательного объема, резервного объема вдоха и резервного объема выдоха. ВК = TV + IRV + ERV.
VC указывает на способность глубоко дышать и кашлять, отражая силу мышц на вдохе и выдохе. VC должен быть в 3 раза больше, чем TV для эффективного кашля. [7] . VC иногда снижается при обструктивных расстройствах и всегда при рестриктивных расстройствах [7]
- Функция Остаточная емкость (FRC)
Это количество воздуха, остающегося в легких в конце нормального выдоха.Он рассчитывается путем сложения остаточного объема и объема выдоха. Нормальное значение — около 1800 — 2200 мл. FRC = RV + ERV.
FRC не полагается на усилие и выделяет положение покоя, когда внутренняя и внешняя упругая отдача уравновешены. FRC снижается при рестриктивных расстройствах. Отношение FRC к TLC — это индекс гиперинфляции [8] . При ХОБЛ FRC составляет до 80% от TLC [3] .
Измерение объема легких [править | править источник]
Измерения объема легких важны для правильного физиологического диагноза, однако его роль в оценке тяжести заболевания, функциональной инвалидности, течения заболевания и реакции на лечение остается спорной. [9] Измерение может быть выполнено с помощью спирометрии, см.…, Плетизмографии тела, вымывания азотом и разбавления гелием с последними тремя методами, используемыми для измерения статических объемов легких [6] .
Плетизмография тела [править | править источник]
Плетизмография происходит от греческого слова, означающего «увеличение». Плетизмография тела в первую очередь измеряет FRC с помощью закона Бойля. Это особенно подходит для пациентов, у которых есть воздушные пространства в легких, которые не сообщаются с бронхиальным деревом.
Человек удобно сидит в герметичном боксе (статические объемы легких могут быть получены путем измерения изменений давления в боксе постоянного объема или объема в боксе постоянного давления), в котором можно точно измерить изменения давления и объема.
Вымывание азота [править | править источник]
Этот метод основан на вымывании N2 из легких, когда пациент дышит 100% O2, используя свойства разбавления газов.
- Пациент дышит 100% кислородом, и весь азот в легких вымывается.
- Измеряется выдыхаемый объем и концентрация азота в этом объеме.
- Разница в объеме азота при исходной концентрации и конечной выдыхаемой концентрации позволяет рассчитать внутригрудной объем, обычно FRC.
Разбавление гелием [редактировать | править источник]
Метод измерения объема легких основан на уравновешивании газа в легких с известным объемом газа, содержащего гелий.В этом методе испытуемого подключают к спирометру, заполненному 10% гелия в кислороде. После того, как испытуемый повторно вдохнет гелий-кислородную смесь и уравновесится со спирометром, концентрация гелия в легких станет такой же, как в спирометре. Исходя из принципа сохранения массы, мы можем записать, что: C1 × V1 = C2 (V1 + V2), где C1 равно начальной концентрации гелия в спирометре,
- V1 равняется начальному объему гелий-кислородной смеси в спирометре,
- C2 соответствует концентрации гелия после уравновешивания,
- V2 соответствует неизвестному объему в легких.
- V2 = V1 (C1-C2) / C2
- Если тест начинается в конце нормального дыхательного объема (конец выдоха), объем воздуха, остающийся в легких, представляет FRC.
- Если тест начинается в конце FVC, то тест измеряет RV.
- Точно так же, если тест начинается после максимального вдоха, тогда V2 будет равняться общей емкости легких.
Чтобы лучше понять методику оценки объема легких, посмотрите видео ниже.
Европейский респираторный журнал http: // erj.ersjournals.com/content/26/3/511
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC32298
Lutfi MF. Физиологические основы и клиническое значение измерения объема легких. Междисциплинарная респираторная медицина, 2017; 12: 3
Руппель ГЛ. Какова клиническая ценность объема легких? Респираторная помощь, 2012; 57 (1): 126–35.
- ↑ Maiolo C, Mohamed EI, Carbonelli MG Состав тела и респираторная функция. Acta Diabetologica, 2003; 40 Дополнение 1 (1): S32-8 · DOI: 10.1007 / s00592-003-0023-0
- ↑ Guyton C, Hall, E. Контрольная книга по медицинской физиологии. Elsevier Inc. Филадельфия, Пенсильвания. 2006; с.475-477.
- ↑ 3,0 3,1 3,2 3,3 Hough, A. Физиотерапия в респираторной терапии; Доказательный подход к лечению респираторных и сердечных заболеваний. 3 rd ред. Соединенное Королевство: Nelson Thomes Ltd, 2001, стр.69.
- ↑ Люс Дж. М., Пирсон Д. Д., Тайлер М. Т.. Интенсивная респираторная терапия, У. Б. Сондерс, Филадельфия, Пенсильвания.стр.21
- ↑ Wilde M, Nair S, Madden B. Тесты функции легких — обзор. Уход за тяжелобольными. 2007; 23 декабря (6): 173-7.
- ↑ 6,0 6,1 Рану Х., Уайлд М., Мэдден Б. Тест функции легких. Ольстерский медицинский журнал, 2011 г .; 80 (2): 84–90. PMC3229853
- ↑ 7,0 7,1 Прайор Дж. А., Уэббер Б. А.. Ред. Физиотерапия при респираторных и сердечных проблемах. 2 nd издание. Черчилль Ливингстон, Лондон. 1998; p53-54
- ↑ Прайор Дж. А., Уэббер Б. А..Ред. Физиотерапия при респираторных и сердечных проблемах. 2 nd издание. Черчилль Ливингстон, Лондон. 1998; p52-63
- ↑ Pellegrino R, Viegi G, Enright P, et al. Стратегии интерпретации для тестирования функции легких. Eur Respir J 2005; (Под давлением).
Объемы легких — Physiopedia
Объем легких также известен как объем дыхания. Это относится к объему газа в легких в данный момент дыхательного цикла. Емкость легких определяется суммированием различных объемов легких.Средняя общая емкость легких взрослого мужчины составляет около 6 литров воздуха. Измерение объема легких является неотъемлемой частью исследования функции легких. Эти объемы имеют тенденцию меняться в зависимости от глубины дыхания, этнической принадлежности, пола, возраста, состава тела [1] и некоторых респираторных заболеваний. Некоторые объемы легких можно измерить с помощью спирометрии — дыхательный объем, резервный объем вдоха и резервный объем выдоха. Однако измерение остаточного объема, функциональной остаточной емкости и общей емкости легких осуществляется с помощью плетизмографии тела, азотного вымывания и разбавления гелием.
Это количество воздуха, которое можно вдохнуть или выдохнуть в течение одного дыхательного цикла. [2] . На нем изображены функции дыхательных центров, дыхательных мышц и механика легких и грудной стенки [3] .
Нормальное значение для взрослых составляет 10% жизненной емкости легких (ЖЕЛ), приблизительно 300–500 мл (6-8 мл / кг) [3] ; но может увеличить VC до 50% на упражнении [4]
- Резервный объем вдоха (IRV)
Это количество воздуха, которое можно принудительно вдохнуть после нормального дыхательного объема.ИРВ обычно оставляют в резерве, но используют при глубоком дыхании. Нормальное значение для взрослых — 1900-3300 мл.
- Резервный объем выдоха (ERV)
Это объем воздуха, который можно принудительно выдохнуть после выдоха нормального дыхательного объема. Нормальное значение для взрослых составляет 700-1200 мл. ERV снижается при ожирении, асците или после операции на верхних отделах брюшной полости [3]
Это объем воздуха, остающийся в легких после максимального выдоха. Нормальное значение для взрослых составляет 1200 мл (20-25 мл / кг).Он косвенно измеряется путем суммирования FRC и ERV и не может быть измерен спирометрией.
При обструктивных заболеваниях легких с особенностями неполного опорожнения легких и захвата воздуха ПЖ может быть значительно высоким. ПЖ также можно выразить в виде процента от общей емкости легких, и значения, превышающие 140%, значительно увеличивают риски баротравмы, пневмоторакса, инфекции и снижения венозного возврата из-за высокого внутригрудного давления, как это было замечено у пациентов с высоким ПЖ, которым требуется хирургическое вмешательство. Таким образом, механическая вентиляция требует высокого давления в периоперационном периоде. [5]
Это максимальный объем воздуха, который можно вдохнуть после состояния покоя. Он рассчитывается как сумма резервного объема вдоха и дыхательного объема. IC = IRV + TV
Это максимальный объем воздуха, который могут вместить легкие, или сумма всех отсеков объема или объем воздуха в легких после максимального вдоха. Нормальное значение составляет около 6000 мл (4-6 л). TLC рассчитывается путем суммирования четырех основных объемов легких (TV, IRV, ERV, RV).
TLC может увеличиваться у пациентов с обструктивными дефектами, такими как эмфизема, и снижаться у пациентов с рестриктивными аномалиями, включая аномалии грудной стенки и кифосколиоз. [6] .
Это общее количество выдыхаемого воздуха после максимального вдоха. Ценность составляет около 4800 мл, и она варьируется в зависимости от возраста и размера тела. Он рассчитывается путем суммирования дыхательного объема, резервного объема вдоха и резервного объема выдоха. ВК = TV + IRV + ERV.
VC указывает на способность глубоко дышать и кашлять, отражая силу мышц на вдохе и выдохе. VC должен быть в 3 раза больше, чем TV для эффективного кашля. [7] . VC иногда снижается при обструктивных расстройствах и всегда при рестриктивных расстройствах [7]
- Функция Остаточная емкость (FRC)
Это количество воздуха, остающегося в легких в конце нормального выдоха.Он рассчитывается путем сложения остаточного объема и объема выдоха. Нормальное значение — около 1800 — 2200 мл. FRC = RV + ERV.
FRC не полагается на усилие и выделяет положение покоя, когда внутренняя и внешняя упругая отдача уравновешены. FRC снижается при рестриктивных расстройствах. Отношение FRC к TLC — это индекс гиперинфляции [8] . При ХОБЛ FRC составляет до 80% от TLC [3] .
Измерение объема легких [править | править источник]
Измерения объема легких важны для правильного физиологического диагноза, однако его роль в оценке тяжести заболевания, функциональной инвалидности, течения заболевания и реакции на лечение остается спорной. [9] Измерение может быть выполнено с помощью спирометрии, см.…, Плетизмографии тела, вымывания азотом и разбавления гелием с последними тремя методами, используемыми для измерения статических объемов легких [6] .
Плетизмография тела [править | править источник]
Плетизмография происходит от греческого слова, означающего «увеличение». Плетизмография тела в первую очередь измеряет FRC с помощью закона Бойля. Это особенно подходит для пациентов, у которых есть воздушные пространства в легких, которые не сообщаются с бронхиальным деревом.
Человек удобно сидит в герметичном боксе (статические объемы легких могут быть получены путем измерения изменений давления в боксе постоянного объема или объема в боксе постоянного давления), в котором можно точно измерить изменения давления и объема.
Вымывание азота [править | править источник]
Этот метод основан на вымывании N2 из легких, когда пациент дышит 100% O2, используя свойства разбавления газов.
- Пациент дышит 100% кислородом, и весь азот в легких вымывается.
- Измеряется выдыхаемый объем и концентрация азота в этом объеме.
- Разница в объеме азота при исходной концентрации и конечной выдыхаемой концентрации позволяет рассчитать внутригрудной объем, обычно FRC.
Разбавление гелием [редактировать | править источник]
Метод измерения объема легких основан на уравновешивании газа в легких с известным объемом газа, содержащего гелий.В этом методе испытуемого подключают к спирометру, заполненному 10% гелия в кислороде. После того, как испытуемый повторно вдохнет гелий-кислородную смесь и уравновесится со спирометром, концентрация гелия в легких станет такой же, как в спирометре. Исходя из принципа сохранения массы, мы можем записать, что: C1 × V1 = C2 (V1 + V2), где C1 равно начальной концентрации гелия в спирометре,
- V1 равняется начальному объему гелий-кислородной смеси в спирометре,
- C2 соответствует концентрации гелия после уравновешивания,
- V2 соответствует неизвестному объему в легких.
- V2 = V1 (C1-C2) / C2
- Если тест начинается в конце нормального дыхательного объема (конец выдоха), объем воздуха, остающийся в легких, представляет FRC.
- Если тест начинается в конце FVC, то тест измеряет RV.
- Точно так же, если тест начинается после максимального вдоха, тогда V2 будет равняться общей емкости легких.
Чтобы лучше понять методику оценки объема легких, посмотрите видео ниже.
Европейский респираторный журнал http: // erj.ersjournals.com/content/26/3/511
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC32298
Lutfi MF. Физиологические основы и клиническое значение измерения объема легких. Междисциплинарная респираторная медицина, 2017; 12: 3
Руппель ГЛ. Какова клиническая ценность объема легких? Респираторная помощь, 2012; 57 (1): 126–35.
- ↑ Maiolo C, Mohamed EI, Carbonelli MG Состав тела и респираторная функция. Acta Diabetologica, 2003; 40 Дополнение 1 (1): S32-8 · DOI: 10.1007 / s00592-003-0023-0
- ↑ Guyton C, Hall, E. Контрольная книга по медицинской физиологии. Elsevier Inc. Филадельфия, Пенсильвания. 2006; с.475-477.
- ↑ 3,0 3,1 3,2 3,3 Hough, A. Физиотерапия в респираторной терапии; Доказательный подход к лечению респираторных и сердечных заболеваний. 3 rd ред. Соединенное Королевство: Nelson Thomes Ltd, 2001, стр.69.
- ↑ Люс Дж. М., Пирсон Д. Д., Тайлер М. Т.. Интенсивная респираторная терапия, У. Б. Сондерс, Филадельфия, Пенсильвания.стр.21
- ↑ Wilde M, Nair S, Madden B. Тесты функции легких — обзор. Уход за тяжелобольными. 2007; 23 декабря (6): 173-7.
- ↑ 6,0 6,1 Рану Х., Уайлд М., Мэдден Б. Тест функции легких. Ольстерский медицинский журнал, 2011 г .; 80 (2): 84–90. PMC3229853
- ↑ 7,0 7,1 Прайор Дж. А., Уэббер Б. А.. Ред. Физиотерапия при респираторных и сердечных проблемах. 2 nd издание. Черчилль Ливингстон, Лондон. 1998; p53-54
- ↑ Прайор Дж. А., Уэббер Б. А..Ред. Физиотерапия при респираторных и сердечных проблемах. 2 nd издание. Черчилль Ливингстон, Лондон. 1998; p52-63
- ↑ Pellegrino R, Viegi G, Enright P, et al. Стратегии интерпретации для тестирования функции легких. Eur Respir J 2005; (Под давлением).

