Википедия — свободная энциклопедия
Избранная статья
Первое сражение при реке Булл-Ран (англ. First Battle of Bull Run), также Первое сражение при Манассасе) — первое крупное сухопутное сражение Гражданской войны в США. Состоялось 21 июля 1861 года возле Манассаса (штат Виргиния). Федеральная армия под командованием генерала Ирвина Макдауэлла атаковала армию Конфедерации под командованием генералов Джонстона и Борегара, но была остановлена, а затем обращена в бегство. Федеральная армия ставила своей целью захват важного транспортного узла — Манассаса, а армия Борегара заняла оборону на рубеже небольшой реки Булл-Ран. 21 июля Макдауэлл отправил три дивизии в обход левого фланга противника; им удалось атаковать и отбросить несколько бригад конфедератов. Через несколько часов Макдауэлл отправил вперёд две артиллерийские батареи и несколько пехотных полков, но южане встретили их на холме Генри и отбили все атаки. Федеральная армия потеряла в этих боях 11 орудий, и, надеясь их отбить, командование посылало в бой полк за полком, пока не были израсходованы все резервы. Между тем на поле боя подошли свежие бригады армии Юга и заставили отступить последний резерв северян — бригаду Ховарда. Отступление Ховарда инициировало общий отход всей федеральной армии, который превратился в беспорядочное бегство. Южане смогли выделить для преследования всего несколько полков, поэтому им не удалось нанести противнику существенного урона.
Хорошая статья
«Хлеб» (укр. «Хліб») — одна из наиболее известных картин украинской советской художницы Татьяны Яблонской, созданная в 1949 году, за которую ей в 1950 году была присуждена Сталинская премия II степени. Картина также была награждена бронзовой медалью Всемирной выставки 1958 года в Брюсселе, она экспонировалась на многих крупных международных выставках.
В работе над полотном художница использовала наброски, сделанные летом 1948 года в одном из наиболее благополучных колхозов Советской Украины — колхозе имени В. И. Ленина Чемеровецкого района Каменец-Подольской области, в котором в то время было одиннадцать Героев Социалистического Труда. Яблонская была восхищена масштабами сельскохозяйственных работ и людьми, которые там трудились. Советские искусствоведы отмечали, что Яблонская изобразила на своей картине «новых людей», которые могут существовать только в социалистическом государстве. Это настоящие хозяева своей жизни, которые по-новому воспринимают свою жизнь и деятельность. Произведение было задумано и создано художницей как «обобщённый образ радостной, свободной творческой работы». По мнению французского искусствоведа Марка Дюпети, эта картина стала для своего времени программным произведением и образцом украинской реалистической живописи XX столетия.
Изображение дня
Рассвет в деревне Бёрнсте в окрестностях Дюльмена, Северный Рейн-Вестфалия
Биотин — SportWiki энциклопедия
Содержание витаминa Н в некоторых пищевых продуктахБиоти́н (витамин Н, витамин B7, кофермент R) — водорастворимый витамин группы В. Биотин является кофактором в метаболизме жирных кислот, лейцина и в процессе глюконеогенеза.
Эффекты биотина[править | править код]
Биотин входит в состав ферментов, регулирующих белковый и жировой обмен, обладает высокой активностью. Участвует в синтезе глюкокиназы. Является коферментом различных ферментов, в том числе и транскарбоксилаз. С участием биотина протекают реакции активирования и переноса СО2.
Биотин в бодибилдинге[править | править код]
Биотин часто применяется в спорте, так как играет огромную роль в метаболизме аминокислот, а также в процессах, обеспечивающих мышцы энергией. Нередко именно дефицит биотина служит причиной медленного роста мышечной массы. Нехватка биотина может возникнуть в силу распространенной среди культуристов привычки есть яйца сырыми. В кишечнике человека биотин вступает в связь с другим соединением яичного белка — авиданом. В итоге образуется трудноперевариваемое соединение, которое лишает прием биотина всякого смысла.
Дозы и режим приема[править | править код]
Передозировка биотина не возникает даже в случае употребления больших количеств. [1] Рекомендуемые дозы — 30 мкг, в бодибилдинге требуются более высокие дозы — 200 мкг и выше.
Суточная норма биотина для разных возрастов[править | править код]
| Возраст | 0-6 месяцев | 7-12 месяцев | 1-3 года | 4-8 лет | 9-13 лет | 14 -18 лет | 19 лет и старше |
|---|---|---|---|---|---|---|---|
| Суточная норма биотина [2], мкг/день | 6 | 8 | 12 | 20 | 25 | 30 |
В 1916 г. Бейтмен обнаружил, что у крыс, в рационе которых единственным источником белка служил яичный белок, развивается синдром, характеризующийся нервно-мышечными расстройствами, тяжелым дерматитом и алопецией. Этот синдром не развивался, если крыс кормили вареным яичным белком, добавляли в корм дрожжевые грибы, печень или экстракты из них. В 1936 г. Кегль и Теннис из яичного желтка выделили в кристаллическом виде необходимый для роста дрожжевых грибов фактор, который они назвали биотином. Биотин оказался тем самым веществом, которое защищало крыс от токсического действия яичного белка (Gyorgy, 1940).
В 1942 г. Дю Виньо установил структурную формулу биотина, вскоре после этого он был синтезирован.
Одновременно активно исследовали природу присутствующего в яичном белке антагониста биотина. В 1940 г. Эйкин и сотр. впервые выделили его и назвали авидином. Авидин представляет собой гликопротеид, который с высоким сродством связывает биотин, препятствуя тем самым его всасыванию.
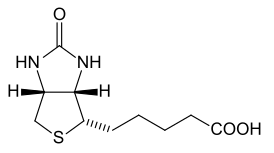
Структурная формула биотина следующая:
Структурная формула биотинаВ природных продуктах помимо свободного биотина обнаружены еще три его формы: биоцитин (e-биотинил-L-лизин), d- и l-сульфоксиды биотина. Значение этих веществ в качестве заменителей биотина для человека не известно, хотя они поддерживают пролиферацию некоторых микроорганизмов. Биоцитин может быть продуктом распада комплекса биотина с белком, поскольку, выполняя роль простетической группы, биотин ковалентно связан с s-аминогруппой остатка лизина соответствующего фермента.
Действию биотина препятствует ряд соединений, в том числе сульфон биотина, дестиобиотин и некоторые имидазолидон-карбоновые кислоты. Антагонизм между авидином и биотином описан выше.
Биотин не оказывает побочного действия у человека даже при приеме больших доз в течение нескольких месяцев.
У человека биотин играет важную роль в углеводном и жировом обмене, участвуя в карбоксилировании четырех субстратов: пировиноградной кислоты, ацетил-КоА, пропионил-КоАи Р-метилкротонил-КоА. Карбоксилирование протекает в две стадии: на первой С02 активируется, ковалентно связываясь с биотином в активном центре фермента, а затем активированный С02 переносится с биотина на соответствующий акцептор.
У большинства животных для воспроизведения дефицита биотина необходимо либо уничтожить кишечную микрофлору (которая, по-видимому, синтезирует биотин), либо скармливать им сырой яичный белок, либо вводить антагонисты биотина. Дефицит биотина у человека проявляется дерматитом, атрофическим глосситом, гиперестезией, миалгией, потерей аппетита, легкой анемией и изменениями ЭКГ. Дефицит биотина наблюдался в отдельных случаях длительного потребления в пищу сырых яиц. Описаны врожденные дефекты биотинзависимых ферментов, которые удается компенсировать введением больших доз биотина (Baumgartner et al., 1984).
Симптомы дефицита биотина наблюдались у детей и взрослых с хроническими воспалительными заболеваниями кишечника, длительно получавших парентеральное питание без добавок биотина. В таких случаях дополнительным фактором был, вероятно, недостаточный синтез биотина кишечной микрофлорой. Авитаминоз проявлялся тяжелой эритродермией и алопецией, напоминающими симптомы дефицита цинка, но исчезающими при приеме даже небольших доз биотина. Биохимические подтверждения дефицита биотина приводятся лишь в немногих работах, но в одном случае биотин снижал повышенную экскрецию с мочой β-гидроксиизовалериановой кислоты, что указывало на нарушение функции биотинзависимой метилкротонил-КоА-карбоксилазы (Gillis et al., 1982).
Ориентировочная суточная потребность в биотине для взрослого человека составляет 30 мкг/сут (табл. XIII.2). Американцы в среднем потребляют биотин в количестве 100— 300 мкг/сут. Частично всасывается и биотин, синтезируемый микрофлорой кишечника. При дефиците биотина в организме и для борьбы с его последствиями нередко применяются дозировки от 2500 мкг до 15-20 тыс. мкг.
Пищевые источники[править | править код]
Биотином богаты субпродукты (печень, почки), яичный желток, молоко, рыба и орехи. Биотин устойчив к нагреванию, но относительно быстро разрушается в щелочной среде.
Биотин легко всасывается в ЖКТ и появляется в моче преимущественно в неизмененном виде, а также в виде метаболитов: бис-норбиотина и сульфоксидов биотина. Система колец в молекуле биотина в организме млекопитающих не разрушается. Применение. Большие дозы биотина (5—10 мг/сут) применяют при себорейном дерматите у новорожденных, а также при генетических дефектах биотинзависимых ферментов. При длительном парентеральном питании в питательные растворы следует добавлять витаминные препараты, содержащие биотин.
Витамины и минералы
Витаминно-минеральный комплекс
| Биотин | |
|---|---|
 ( {{{картинка}}}) ( ({{{картинка3D}}}) | |
| Хим. формула | C10H16N2O3S |
| Молярная масса | 244.31 г/моль |
| Температура | |
| • плавления | 230 °C[1] |
| Рег. номер CAS | 58-85-5 |
| PubChem | 171548 |
| Рег. номер EINECS | 200-399-3 |
| SMILES | |
| InChI | 1S/C10h26N2O3S/c13-8(14)4-2-1-3-7-9-6(5-16-7)11-10(15)12-9/h6-7,9H,1-5h3,(H,13,14)(h3,11,12,15)/t6-,7-,9-/m0/s1 |
| ChEBI | 15956 |
| ChemSpider | 149962 |
| NFPA 704 |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Метионин — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 июля 2017; проверки требуют 8 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 июля 2017; проверки требуют 8 правок.| Метионин | |
|---|---|
 ( {{{картинка}}}) | |
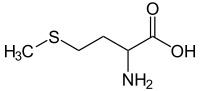
| Систематическое наименование | 2-амино-4-(метилтио)бутановая кислота |
| Сокращения | Met, AUG |
| Традиционные названия | Метионин |
| Хим. формула | HO2CCH(NH2)CH2CH2SCH3 |
| Рац. формула | C5H11NO2S |
| Молярная масса | 149.21 г/моль |
| Плотность | 1.340 г/см³ |
| Температура | |
| • плавления | L- или D- 281 (разл.) |
| Константа диссоциации кислоты pKa{\displaystyle pK_{a}} | 2.28 (карбоксил) 9.21 (аминогруппа)[1] |
| Рег. номер CAS | 59-51-8, 63-68-3 (L-энантиомер) |
| PubChem | 876 |
| Рег. номер EINECS | 200-432-1 |
| SMILES | |
| InChI | |
| ChEBI | 16811 |
| ChemSpider | 853 |
| ЛД50 | L-метионин, крысы, перорально[2] — 36 000 мг/кг |
| Токсичность | нетоксичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Метионин — алифатическая серосодержащая α-аминокислота, бесцветные кристаллы со специфическим неприятным запахом, растворимые в воде, входит в число незаменимых аминокислот. Содержится во многих белках и пептидах (метионин-энкефалин, метионин-окситоцин). Значительное количество метионина содержится в казеине.
Метионин также служит в организме донором метильных групп (в составе S-аденозил-метионина) при биосинтезе холина, адреналина и др., а также источником серы при биосинтезе цистеина.
Метионин по своим свойствам является типичной алифатической аминокислотой, метилсульфидный фрагмент при восстановлении красным фосфором в йодистоводородной кислоте деметилируется с образованием гомоцистеина; в мягких условиях окисляется до метионинсульфоксида, под действием перекиси водорода, хлорной кислоты и других сильных окислителей — до соответствующего сульфона.
Первоначально в промышленности метионин выделяли из гидролизатов казеина, однако в настоящее время метионин получают синтетически. Промышленный синтез DL-метионина осуществляют исходя из акролеина. На первой стадии присоединением метилмеркаптана к акролеину синтезируют 3-метилтиопропионовый альдегид:
- Ch4SH+h3C=CH-CHO→Ch4SCh3Ch3CHO{\displaystyle {\mathsf {CH_{3}SH+H_{2}C{\text{=}}CH{\text{-}}CHO\rightarrow CH_{3}SCH_{2}CH_{2}CHO}}}
который далее используется в качестве карбонильного компонента синтеза Штреккера:
- Ch4SCh3Ch3CHO+HCN+Nh4→Ch4SCh3Ch3CH(Nh3)CN{\displaystyle {\mathsf {CH_{3}SCH_{2}CH_{2}CHO+HCN+NH_{3}\rightarrow CH_{3}SCH_{2}CH_{2}CH(NH_{2})CN}}}
- Ch4SCh3Ch3CH(Nh3)CN+h3O→Ch4SCh3Ch3CH(Nh3)COOH{\displaystyle {\mathsf {CH_{3}SCH_{2}CH_{2}CH(NH_{2})CN+H_{2}O\rightarrow CH_{3}SCH_{2}CH_{2}CH(NH_{2})COOH}}}
Метионин является незаменимой аминокислотой, то есть не синтезируется в организме человека. Содержится в следующих продуктах питания:
| Вид пищи | г/100 г |
|---|---|
| Яйцо, высушенный белок, порошок с пониженным содержанием глюкозы | 3.204 |
| Семя кунжута, мука (пониженное содержание жира) | 1.656 |
| Бразильский орех | 1.008 |
| Изолят соевого белка | 0.814 |
| Курица, жареная | 0.801 |
| Тунец, консервированный в воде | 0.755 |
| Ростки пшеницы | 0.456 |
| Овёс | 0.312 |
| Арахис | 0.309 |
| Нут | 0.253 |
| Кукуруза, жёлтая | 0.197 |
| Миндаль | 0.151 |
| Фасоль пинто, приготовленная | 0.117 |
| Чечевица, приготовленная | 0.077 |
| Рис, неочищенный, среднее зерно, приготовленный | 0.052 |
| Капуста |
| Продукт | Белок | Метионин | М/Б |
|---|---|---|---|
| Свинина сырая | 21,26 г | 0 554 мг | 2,6 % |
| Сырое куриное филе | 21,23 г | 0 552 мг | 2,6 % |
| Сырое филе лосося | 20,42 г | 0 626 мг | 3,1 % |
| Куриное яйцо | 12,57 г | 0 380 мг | 3,0 % |
| Коровье молоко, 3,7 % жирности | 0 3,28 г | 0 0 82 мг | 2,5 % |
| Кунжут | 17,73 г | 0 586 мг | 3,3 % |
| Бразильский орех | 14,32 г | 1008 мг | 7,0 % |
| Грецкие орехи | 15,23 г | 0 236 мг | 1,5 % |
| Мука пшеничная г/п | 13,70 г | 0 212 мг | 1,5 % |
| Кукурузная мука | 0 6,93 г | 0 145 мг | 2,1 % |
| Рис неочищенный | 0 7,94 г | 0 179 мг | 2,3 % |
| Соя высушенная | 36,49 г | 0 547 мг | 1,5 % |
| Горох цельный лущенный | 24,55 г | 0 251 мг | 1,0 % |
Метионин используется в качестве аминокислотной добавки к кормам в птицеводстве и скотоводстве.
Метионин и его производные в фармакологии[править | править код]
Фармакологический препарат метионина оказывает некоторое липотропное действие, повышает синтез холина, лецитина и других фосфолипидов, в некоторой степени способствует снижению содержания холестерина в крови и улучшению соотношения фосфолипиды/холестерин, уменьшению отложения нейтрального жира в печени и улучшению функции печени, может оказывать умеренное антидепрессивное действие (по-видимому, за счёт влияния на биосинтез адреналина).
S-аденозил-метионин (Адеметионин, SAMe, гептрал, гептор) оказывает более сильное положительное действие на функцию печени и более выраженное антидепрессивное действие, чем метионин. В фармакологии используется как стимулятор регенерации печени, антифибротик, антихолестатик, антидепрессант. В эксперименте показана антифибротическая (противорубцовая) активность адеметионина.
Метил-метионин-сульфоний (в фармакологии известен как «метиосульфония хлорид»), иногда условно называемый «витамином U» (от лат. ulcus — язва)[4], обладает выраженным цитопротективным действием на слизистую желудка и двенадцатиперстной кишки, способствует заживлению язвенных и эрозивных поражений слизистой желудка и двенадцатиперстной кишки.
Метионин, меченый углеродом 11, обладает свойством избирательно накапливаться в опухолевой ткани. Это позволяет использовать его в качестве радиофармпрепарата при онкологических исследованиях головного мозга.[5]
- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ L-Methionine // MSDS
- ↑ National Nutrient Database for Standard Reference, U.S. Department of Agriculture, <http://www.nal.usda.gov/fnic/foodcomp/search/>. Проверено 7 сентября 2009. Архивная копия от 3 марта 2015 на Wayback Machine.
- ↑ Витамин U
- ↑ Нейроонкология, Институт мозга человека им. Н.П.Бехтеревой РАН, <http://www.ihb.spb.ru/petindex.htm>. Проверено 13 июля 2002. Архивная копия от 13 июля 2009 на Wayback Machine.
