Основной обмен — Википедия
Материал из Википедии — свободной энциклопедии
Основной обмен — это минимальное количество энергии, необходимое для обеспечения нормальной жизнедеятельности организма в стандартных условиях[1][2]. Под стандартными условиями обычно подразумевают[2][3]:
- бодрствование,
- утром,
- натощак (после 12 — 16 часов голодания),
- в лежачем положении,
- в условиях психологического и эмоционального покоя,
- температура комфорта (18 — 20 °C).
Интенсивность основного обмена у мужчин в среднем составляет 1 ккал/кг/ч, то есть за сутки на основной обмен расходуется 1700 ккал для мужчины весом 70 кг[1]. Для женщин эта величина на 10 % меньше[4].
Величина основного обмена зависит от соотношения в организме процессов анаболизма и катаболизма.
Освобождаемая в ходе метаболизма тепловая энергия расходуется на поддержание постоянства температуры тела. Эта энергия также расходуется на процессы клеточного метаболизма, кровообращение, дыхание, выделение, поддержание температуры тела, функционирование жизненно важных нервных центров мозга, постоянную секрецию эндокринных желёз. Энергозатраты организма возрастают при физической и умственной работе, психоэмоциональном напряжении, после приема пищи, при понижении температуры.
| Пол | Возраст (лет) | Уравнение для расчёта (ккал/сутки) |
|---|---|---|
| М | 10—18 | 16,6 мт + 119Р + 572 |
| Ж | 10—18 | 7,4 мт + 482Р + 217 |
| М | 18—30 | 15,4 мт + 27Р + 717 |
| Ж | 18—30 | 13,3 мт + 334Р + 35 |
| М | 30—60 | 11,3 мт + 16Р + 901 |
| Ж | 30—60 | 8,7 мт + 25Р + 865 |
| М | >60 | 8,8 мт + 1128Р — 1071 |
| Ж | >60 | 9,2 мт + 637Р — 302 |
мт — масса тела (кг), Р — рост (м)
- ↑ 1 2 Нормальная физиология человека / Ткаченко Б. И.. — 2-е. — Москва: Медицина, 2005. — С. 575—576. — 928 с. — ISBN 5-225-04240-6.
- ↑ 1 2 Агаджанян Н. А., Смирнов В. М. Нормальная физиология:Учебник для студентов медицинских вузов. — Москва: Медицинское информационное агентство, 2009. — С. 361. — 520 с. — ISBN 978-5-9986-0001-2.
- ↑ Гайтон А. К., Холл Д. Э. Медицинская физиология = Textbook of Medical Physiology / Кобрин В.И.. — Москва: Логосфера, 2008. — С. 112. — 1296 с. — ISBN 978-5-98657-013-6.
- ↑ Судаков К. В. Нормальная физиология. — Москва: Медицинское информационное агентство, 2006. — С. 75—78. — 920 с. — ISBN 5894812941.
Обсуждение:Обмен веществ — Википедия
Материал из Википедии — свободной энциклопедии
| | Эта статья была переименована по результатам обсуждения от 8 июня 2013 года. Для повторного выставления статьи на переименование нужны веские основания, иначе такое действие будет нарушать правила (см. п. 8). |
Неспешно делаю перевод английской статьи у себя в песочнице Meddoc13 08:35, 19 августа 2010 (UTC)
Вывел на всеобщее обозрение основную часть перевода. Продолжение следует. Meddoc13 09:47, 23 августа 2010 (UTC)
Ну уж магний-то надо бы упомянуть. Вставил. Shenikolaj2008 14:26, 5 сентября 2010 (UTC)
- Отлично —Sirozha.ru 14:33, 6 сентября 2010 (UTC)
Цитирую «Неорганические элементы играют важнейшую роль в обмене веществ.» Можно поподробнее про
Алхимия в названии[править код]
Минералы уж никак не могут быть биогенными веществами, а тем более молекулами, так как они — ГЕОгенные вещества. С гораздо большим основанием к биогенным минералам можно было бы отнести нефтепродукты и янтарь, но их-то как раз к минералам и не относят. Очевидно появление в названии термина «минералы» связано с каким-то источником 18 — начала 19 века, задолго до Брокгауза и Ефрона, когда о природе органических веществ было очень мало что известно, но были широко распространены представления о гомункулусе и зарождении жизни в камнях, пыли и т.д. Переименовал в «Неорганические вещества и кофакторы». 109.188.127.36 18:10, 20 июля 2016 (UTC)
- for example, a decrease in the amount of product can increase the flux through the pathway to compensate.
- при переводе откуда-то появился «поток энергии» —Sirozha.ru 10:06, 23 сентября 2010 (UTC)
Почему метаболизм, а не обмен веществ?[править код]
Откуда взялся метаболизм? По-русски эти процессы всегда назывались обмен веществ, по-немецки тоже (Stoffwechsel). Ural X 08:03, 5 сентября 2011 (UTC)
- Это очевидные синонимы—Meddoc13 10:33, 5 сентября 2011 (UTC)
- Это понятно, поэтому и вопрос, по каким причинам выбран именно метаболизм в качестве названия. 69.76.218.241 11:05, 5 сентября 2011 (UTC)
- Для меня это не принципиально. Можете запустить КПМ—Meddoc13 11:55, 5 сентября 2011 (UTC)
- на русском языке это называется и так, и так —Sirozha.ru 03:38, 6 сентября 2011 (UTC)
- Так давайте придерживаться русского варианта, раз оба термина синонимы, всё-таки без нужды не имеет смысла браться за метаболизм. С ув. Ural X 14:46, 14 сентября 2011 (UTC)
- на русском языке это называется и так, и так —Sirozha.ru 03:38, 6 сентября 2011 (UTC)
- Для меня это не принципиально. Можете запустить КПМ—Meddoc13 11:55, 5 сентября 2011 (UTC)
- Это понятно, поэтому и вопрос, по каким причинам выбран именно метаболизм в качестве названия. 69.76.218.241 11:05, 5 сентября 2011 (UTC)
Метаболизм конечно хорошее слово, но давайте придерживаться словаря славянских языков когда при этом есть такая хорошая возможность. Extreemator 14:40, 8 июня 2013 (UTC)
Википедия:Рецензирование/Обмен веществ.
обмен веществ происходит В КЛЕТКЕ. об этом написано в любом учебнике. капилляр — это посредник между кровью и межклеточным веществом. органические молекулы движутся из крови через капилляр в межклеточное вещество, откуда захватываются клетками, и туда же попадают продукты катаболизма —Sirozha.ru 06:25, 25 июля 2011 (UTC)
- Обмен веществ происходит между клетками организма и межклеточной жидкостью, постоянство состава которой поддерживается кровообращением: за время прохождении крови в капиллярах через проницаемые стенки капилляров плазма крови 40 раз полностью обновляется с интерстициальной жидкостью Физиологию человека под редакцией Р.Шмидта и Г.Тевса в 3-х томах. М.:Мир,1996 с. 521. // golfi w
- В этот раз вы почти правы… —Sirozha.ru 02:25, 27 июля 2011 (UTC)
Интересно, почему «вы почти правы»? а как метаболизм может преобразовывать продукты жизнедеятельности клеток, тем более доставлять их к месту назначения?—Golfi w 19:59, 13 августа 2012 (UTC)
Скорость обмена веществ[править код]
Мне кажется, в статье необходимо рассмотреть понятие скорости обмена веществ (сейчас она упоминается единожды во введении, в виде красной ссылки), т. к. это, возможно, самый популярный в бытовом общении контекст употребления слова «метаболизм». LoKi 14:50, 4 июня 2012 (UTC)
Обмен веществ Википедия
Метаболи́зм или обме́н веще́ств — набор химических реакций, которые возникают в живом организме для поддержания жизни. Эти процессы позволяют организмам расти и размножаться, сохранять свои структуры и отвечать на воздействия окружающей среды.
Метаболизм обычно делят на 2 стадии: катаболизм и анаболизм. В ходе катаболизма сложные органические вещества деградируют до более простых, обычно выделяя энергию. А в процессах анаболизма — из более простых синтезируются более сложные вещества и это сопровождается затратами энергии.
Серии химических реакций обмена веществ называют метаболическими путями. В них, при участии ферментов, одни биологически значимые молекулы последовательно превращаются в другие.
Ферменты играют важную роль в метаболических процессах потому, что:
- действуют как биологические катализаторы и снижают энергию активации химической реакции;
- позволяют регулировать метаболические пути в ответ на изменения среды клетки или сигналы от других клеток.
Особенности метаболизма влияют на то, будет ли пригодна определённая молекула для использования организмом в качестве источника энергии. Так, например, некоторые прокариоты используют сероводород в качестве источника энергии, однако этот газ ядовит для животных[1]. Скорость обмена веществ также влияет на количество пищи, необходимой для организма.
Органические вещества, входящие в состав всех живых существ (животных, растений, грибов и микроорганизмов), представлены в основном аминокислотами, углеводами, липидами (часто называемые жирами) и нуклеиновыми кислотами. Так как эти молекулы имеют важное значение для жизни, метаболические реакции сосредоточены на создании этих молекул при строительстве клеток и тканей или разрушении их с целью использования в качестве источника энергии. Многие важные биохимические реакции объединяются вместе для синтеза ДНК и белков.
Наследственные болезни обмена веществ — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 июня 2019; проверки требуют 2 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 июня 2019; проверки требуют 2 правки.Наследственные нарушения обмена веществ включают в себя большую группу наследственных заболеваний, затрагивающих расстройства метаболизма. Такие нарушения составляют значительную часть группы метаболических расстройств (метаболические заболевания). Наследственными называются такие заболевания человека, которые вызваны перестройками и нарушениями в генетическом материале организма – хромосомах и генах. Среди наследственных заболеваний человека одно из самых значительных мест занимают наследственные болезни обмена. В настоящее время[когда?] эта группа включает около 700 различных заболеваний[источник не указан 195 дней].
Развитие большинства из них является следствием дефекта единичных генов, кодирующих индивидуальные ферменты, которые обеспечивают превращение одних веществ (субстраты) в другие (продукты). В большинстве случаев таких расстройств патогенным является накопление веществ, обладающих токсическим действием или нарушающих способность синтеза других жизненно важных соединений. Для наследственных болезней обмена веществ иногда используется синонимичный термин «врождённые ошибки метаболизма» ферментопатии.
Термин врожденное нарушение обмена веществ был предложен в начале XXI века британским врачом сэром Арчибальдом Гародом (1857—1936), который известен благодаря разработанной им классической концепции метаболического блока как основы патогенеза наследственных нарушений обмена веществ.
Его труд «Врождённые нарушения обмена веществ»[1], написанный по результатам многолетнего изучения природы и наследования алкаптонурии лёг в основу дальнейших исследований генетически обусловленных врождённых нарушений обмена веществ.
Традиционно наследственные болезни обмена веществ разделялись на нарушения обмена углеводов, аминокислот, органических кислот, или лизосомные болезни накопления. Однако в последние десятилетия были открыты сотни новых наследственных нарушений обмена, и эти категории сильно разрослись.
В настоящее время выделяют следующие основные классы наследственных метаболических расстройств. Приведены характерные примерами для каждого класса, однако многие другие не попали в эти категории. Где возможно, приведён шифр по МКБ-10.
С развитием метабономики и метаболомики, а также фармакогенетики, всё большее и большее значение приобретает исследование роли отдельных генов в формировании наследственных нарушений обмена, ферментопатий
метаболизм — Викисловарь
Морфологические и синтаксические свойства[править]
| падеж | ед. ч. | мн. ч. |
|---|---|---|
| Им. | метаболи́зм | метаболи́змы |
| Р. | метаболи́зма | метаболи́змов |
| Д. | метаболи́зму | метаболи́змам |
| В. | метаболи́зм | метаболи́змы |
| Тв. | метаболи́змом | метаболи́змами |
| Пр. | метаболи́зме | метаболи́змах |
ме-та-бо-ли́зм
Существительное, неодушевлённое, мужской род, 2-е склонение (тип склонения 1a по классификации А. А. Зализняка).
Корень: -мета-; корень: -бол-; суффикс: -изм [Тихонов, 1996].
Произношение[править]
- МФА: [mʲɪtəbɐˈlʲizm]
Семантические свойства[править]
Значение[править]
- биол., мед. обмен веществ; совокупность процессов биохимических превращений веществ и энергии в живых организмах ◆ Во много раз возрастает сопротивление ядам, инфекциям и радиации, значительно улучшается метаболизм, усиливается выносливость. Ярослав Кудлак, «Симбиоз», 2009 г. // «Наука и жизнь» (цитата из Национального корпуса русского языка, см. Список литературы)
- биохим. превращение определённых веществ внутри клеток с момента их поступления до образования конечных продуктов ◆ Отсутствует пример употребления (см. рекомендации).
Синонимы[править]
- обмен веществ
Антонимы[править]
Гиперонимы[править]
Гипонимы[править]
- анаболизм, катаболизм
Родственные слова[править]
Этимология[править]
Происходит от др.-греч. μεταβολή «превращение, изменение».
Фразеологизмы и устойчивые сочетания[править]
Перевод[править]
| Список переводов | |
Библиография[править]
Липидный обмен — Википедия
Липидный обмен, или метаболизм липидов — сложный биохимический и физиологический процесс, происходящий в некоторых клетках живых организмов.
Липидный обмен включает в себя следующие процессы:
Термин «липиды» объединяет вещества, обладающие общим физическим свойством — гидрофобностью, то есть нерастворимостью в воде. Однако такое определение в настоящее время является не совсем корректным ввиду, того, что некоторые группы (триацилглицерины, фосфолипиды, сфинголипиды и др.) проявляют себя как амфифильные или дифильные соединения, то есть способные растворяться как в полярных веществах (гидрофильность), так и в неполярных (гидрофобность). По структуре липиды настолько разнообразны, что у них отсутствует общий признак химического строения. Липиды разделяют на классы, в которые объединяют молекулы, имеющие сходное химическое строение и общие биологические свойства.
Основную массу липидов в организме составляют жиры — триацилглицеролы, служащие формой депонирования энергии. Жиры располагаются преимущественно в подкожной жировой ткани и выполняют также функции теплоизоляционной и механической защиты.
Фосфолипиды — большой класс липидов, получивший своё название из-за остатка фосфорной кислоты, придающего им свойства амфифильности. Благодаря этому свойству фосфолипиды формируют бислойную структуру мембран, в которую погружены белки. Клетки или отделы клеток, окружённые мембранами, отличаются по составу и набору молекул от окружающей среды, поэтому химические процессы в клетке разделены и ориентированы в пространстве, что необходимо для регуляции метаболизма.
Стероиды, представленные в животном мире холестеролом и его производными, выполняют разнообразные функции. Холестерол — важный компонент мембран и регулятор свойств гидрофобного слоя. Производные холестерола (жёлчные кислоты) необходимы для переваривания жиров. Стероидные гормоны, синтезируемые из холестерола, участвуют в регуляции энергетического, водно-солевого обменов, половых функций. Кроме стероидных гормонов, многие производные липидов выполняют регуляторные функции и действуют, как и гормоны, в очень низких концентрациях. Например, тромбоцитактивирующий фактор — фосфолипид особой структуры — оказывает сильное влияние на агрегацию тромбоцитов в концентрации 10-12 М; эйкозаноиды, производные полиеновых жирных кислот, вырабатываемые почти всеми типами клеток, вызывают разнообразные биологические эффекты в концентрациях не более 10-9 М. Из приведённых примеров следует, что липиды обладают широким спектром биологических функций.
В тканях человека количество разных классов липидов существенно различается. В жировой ткани жиры составляют до 75 % сухого веса. В нервной ткани липидов содержится до 50 % сухого веса, основные из них фосфолипиды и сфингомиелины (30 %), холестерол (10 %), ганглиозиды и цереброзиды (7 %). В печени общее количество липидов в норме не превышает 10—13 %.
Нарушения обмена липидов приводят к развитию многих заболеваний, но среди людей наиболее распространены два из них — ожирение и атеросклероз.
Расщепление, переваривание и всасывание пищевых липидов[править | править код]
Суточная потребность человека в жирах составляет 70—80 г, хотя в пищевом рационе их содержание может колебаться от 80 до 130 г.
Переваривание липидов в желудке[править | править код]
В желудке имеется фермент липаза, способный катализировать расщепление триацилглицеролов. Однако оптимальной средой её действия является среда, близкая к нейтральной. Поэтому липаза в желудке у взрослых людей практически неактивна из-за малых значений pH.
Однако у детей ситуация обстоит несколько по-другому: желудок детей имеет при рождении среду, близкую к нейтральной (pH (среднее) = 5,5). Это явление обусловлено основным продуктом питания детей — молоком (содержит белки и жирных кислоты (количество углерода меньше 14)). Так, фермент липаза выполняет ключевую роль в метаболизме липидов у детей[источник не указан 217 дней].
Переваривание липидов в кишечнике[править | править код]
В двенадцатиперстной кишке пища подвергается действию желчи и сока поджелудочной железы. На первом этапе там происходит эмульгирование жиров.
Эмульгирование жиров[править | править код]
Жиры составляют до 90 % липидов, поступающих с пищей. Переваривание жиров происходит в тонком кишечнике, однако уже в желудке небольшая часть жиров гидролизуется под действием «липазы языка» (лингвальная (лат. lingua — язык) липаза). Этот фермент синтезируется железами на дорсальной поверхности языка и относительно устойчив при кислых значениях рН желудочного сока. Поэтому он действует в течение 1—2 ч на жиры пищи в желудке. Однако вклад этой липазы в переваривание жиров у взрослых людей незначителен. Основной процесс переваривания происходит в тонкой кишке.
Так как жиры — нерастворимые в воде соединения, то они могут подвергаться действию ферментов, растворённых в воде только на границе раздела фаз вода/жир. Поэтому действию панкреатической липазы, гидролизующей жиры, предшествует эмульгирование жиров. Эмульгирование (смешивание жира с водой) происходит в тонком кишечнике под действием солей жёлчных кислот. Жёлчные кислоты в основном конъюгированные: таурохолевая, гликохолевая и другие кислоты.
Гормоны, активирующие переваривание жиров[править | править код]
При поступлении пищи в желудок, а затем в кишечник клетки слизистой оболочки тонкого кишечника начинают секретировать в кровь пептидный гормон холецистокинин (панкреозимин). Этот гормон действует на жёлчный пузырь, стимулируя его сокращение, и на экзокринные клетки поджелудочной железы, стимулируя секрецию пищеварительных ферментов, в том числе панкреатической липазы. Другие клетки слизистой оболочки тонкого кишечника в ответ на поступление из желудка кислого содержимого выделяют гормон секретин. Секретин — гормон пептидной природы, стимулирующий секрецию гидрокарбоната (НСО3—) в сок поджелудочной железы.
Нарушения переваривания и всасывания жиров[править | править код]
Нарушение переваривания жиров может быть следствием нескольких причин. Одна из них — нарушение секреции жёлчи из жёлчного пузыря при механическом препятствии оттоку жёлчи. Это состояние может быть результатом сужения просвета жёлчного протока камнями, образующимися в жёлчном пузыре, или сдавлением жёлчного протока опухолью, развивающейся в окружающих тканях. Уменьшение секреции жёлчи приводит к нарушению эмульгирования пищевых жиров и, следовательно, к снижению способности панкреатической липазы гидролизовать жиры.
Нарушение секреции сока поджелудочной железы и, следовательно, недостаточная секреция панкреатической липазы также приводят к снижению скорости гидролиза жиров. В обоих случаях нарушение переваривания и всасывания жиров приводит к увеличению количества жиров в фекалиях — возникает стеаторея (жирный стул). В норме содержание жиров в фекалиях составляет не более 5 %. При стеаторее нарушается всасывание жирорастворимых витаминов (A, D, E, К) и незаменимых жирных кислот, поэтому при длительно текущей стеаторее развивается недостаточность этих незаменимых факторов питания с соответствующими клиническими симптомами. При нарушении переваривания жиров плохо перевариваются и вещества нелипидной природы, так как жир обволакивает частицы пищи и препятствует действию на них ферментов.
Всасывание липидов в кишечнике[править | править код]
Ресинтез жиров в слизистой оболочке тонкого кишечника[править | править код]
Основная часть всосавшихся в тонком кишечнике липидов принимает участие в ресинтезе триацилглицеринов. Для этого в эндоплазматическом ретикулуме энтероцитов работают специальные ферменты
Факторы, влияющие на всасывание липидов[править | править код]
Катаболизм липидов[править | править код]
Катаболизм липидов — совокупность всех катаболических процессов липидов, включающая несколько стадий:
Липолиз[править | править код]
Липолиз — катаболический процесс, результатом которого является расщепление жиров, происходящее под действием фермента липазы.
β-Окисление жирных кислот[править | править код]
Процесс β-окисления высших жирных кислот (ВЖК) складывается из следующих этапов:
- активация ВЖК на наружной поверхности мембраны митохондрий при участии АТФ, кофермента А и ионов магния с образованием активной формы ВЖК (ацил — КоА).
- транспорт жирных кислот внутрь митохондрий возможен при присоединении активной формы жирной кислоты к карнитину, находящемуся на наружной поверхности внутренней мембраны митохондрий. Образуется ацил-карнитин, обладающий способностью проходить через мембрану. На внутренней поверхности комплекс распадается и карнитин возвращается на наружную поверхность мембраны.
- внутримитохондриальное окисление жирных кислот состоит из последовательных ферментативных реакций. В результате одного завершенного цикла окисления происходит отщепление от жирной кислоты одной молекулы ацетил-КоА, то есть укорочение жирнокислотной цепи на два углеродных атома. При этом в результате двух дегидрогеназных реакций восстанавливается ФАД до ФАДН2 и НАД+ до НАДН2. Таким образом завершая 1 цикл β—окисления ВЖК, в результате которого ВЖК укоротилось на 2 углеродных звена. При β-окислении выделилось 5АТФ и 12АТФ выделилось при окислении ацетил-КоА в цикле Кребса и сопряженных с ним ферментов дыхательной цепи. Окисление ВЖК будет происходить циклически одинаково, но только до последней стадии — стадии превращения масляной кислоты (бутирил-КоА), которая имеет свои особенности, которые необходимо учитывать при подсчёте суммарного энергетического эффекта окисления ВЖК, когда в результате одного цикла образуется 2 молекулы ацетил-КоА, одна из них проходила β-окисление с выделением 5АТФ, а другая нет.
ω-Окисление жирных кислот[править | править код]
Хотя для жирных кислот наиболее характерно β-окисление, встречаются также два других типа окисления: α-и ω-окисления. Окисление жирных кислот с длинной цепью до 2-оксикислот и затем до жирных кислот с числом атомов углерода на один меньше, чем в исходном субстрате, было показано в микросомах мозга и других тканях, а также в растениях. 2-Оксикислоты с длинной цепью являются компонентами липидов мозга.
Окисление ненасыщенных жирных кислот[править | править код]
Около половины жирных кислот в организме человека ненасыщенные. β-Окисление этих кислот идёт обычным путём до тех пор, пока двойная связь не окажется между третьим и четвёртым атомами углерода. Затем фермент еноил-КоА изомераза перемещает двойную связь из положения 3-4 в положение 2-3 и изменяет цис-конформацию двойной связи на транс-, которая требуется для β-окисления. В этом цикле β-окисления первая реакция дегидрирования не происходит, так как двойная связь в радикале жирной кислоты уже имеется. Далее циклы β-окисления продолжаются, не отличаясь от обычного пути.
Нарушения окисления жирных кислот[править | править код]
Нарушение переноса жирных кислот в митохондрии.
Скорость переноса жирных кислот внутрь митохондрий, а следовательно и скорость процесса β-окисления, зависит от доступности карнитина и скорости работы фермента карнитинацилтрансферазы I.
β-Окисление могут нарушать следующие факторы:
- длительный гемодиализ, в ходе которого организм теряет карнитин;
- длительная ацидурия, при которой карнитин выводится как основание с органическими кислотами;
- лечение больных сахарным диабетом препаратами сульфонилмочевины, ингибирующими карнитинацилтрансферазу I;
- низкая активность ферментов, синтезирующих карнитин;
- наследственные дефекты карнитинацил-трансферазы I.
При длительном голодании кетоновые тела становятся основным источником энергии для скелетных мышц, сердца и почек. Таким образом глюкоза сохраняется для окисления в мозге и эритроцитах. Уже через 2-3 дня после начала голодания концентрация кетоновых тел в крови достаточна для того, чтобы они проходили в клетки мозга и окислялись, снижая его потребности в глюкозе.
Кислород, необходимый организму для функционирования ЦПЭ и многих других реакций, является одновременно и токсическим веществом, если из него образуются так называемые активные формы.
К активным формам кислорода относят:
Липогенез[править | править код]
Липогенез — процесс синтеза жирных кислот, основным источником которого является углеводы.
С пищей в организм поступают разнообразные жирные кислоты, в том числе и незаменимые. Значительная часть заменимых жирных кислот синтезируется в печени, в меньшей степени — в жировой ткани и лактирующей молочной железе. Источником углерода для синтеза жирных кислот служит ацетил-КоА, образующийся при распаде глюкозы в абсорбтивном периоде. Таким образом, избыток углеводов, поступающих в организм, трансформируется в жирные кислоты, а затем в жиры.
Синтез кетоновых тел[править | править код]
Все кетоновые тела берут начало от ацетоацетил-КоА, который образуется при конденсации 2-х молекул ацетил-КоА по принципу «голова в хвост». Реакция конденсации происходит в митохондриях. В печени ацетоацетил-КоА взаимодействует ещё с одной молекулой ацетил-КоА и превращается в ГОМГ-КоА- важное промежуточное вещество для синтеза холестерола и стероидов.
Организм получает жирные кислоты из пищи и путём липогенеза из ацетил-КоА, образующегося из углеводов и некоторых аминокислот. Состав смеси жирных кислот пищи существенно варьирует по степени ненасыщенности и длине цепи. Липогенез у высших животных включает только образование пальмитата, из которого образуются другие насыщенные и мононенасыщенные кислоты. Из смеси имеющихся жирных кислот в печени животного образуется свойственный данному виду набор жирных кислот; однако на характере синтезируемых жирных кислот сказывается также и диета. Процессы утилизации жирных кислот пищи включают укорочение и удлинение углеродного скелета, так же как и введение двойной связи.
Фосфолипиды выполняют ряд важных биологических функций. Как большинство полярных липидов, они являются амфифильными соединениями, несущими гидрофобные и гидрофильные группы. Некоторые фосфолипиды, например фосфатидилхолин, представляют собой диполярные ионы, обладающие катионной и анионной группами, и являются основными компонентами клеточных мембранных систем. Например, в миелиновом волокне нерва фосфолипиды и цереброзиды составляют приблизительно 60 % сухого веса.
Распределение и обмен[править | править код]
Среди липидов тела фосфолипиды распределены неравномерно. Богатыми источниками фосфолипидов являются липиды тканей различных желез, в особенности печени, а также плазма крови, где они могут составлять до половины всех липидов. Фосфолипиды являются также преобладающими липидами в желтках птичьих яиц и в семенах бобовых растений. Обмен различных фосфолипидов в определённых местах животного организма изучали с использованием различных изотопов, наиболее часто 32Р. Период полупревращения этих липидов колеблется от менее одного дня для фосфатидилхолина печени до более 200 сут для фосфатидилэтаноламина мозга.
Образование[править | править код]
Холестерол — основной стероид организма животных. У взрослого человека содержание холестерола составляет 140—150 г. Около 93 % стероида входит в состав мембран и 7 % находится в жидкостях организма. Холестерол увеличивает микровязкость мембран и снижает их проницаемость для Н2О и водорастворимых веществ. В крови он представлен в виде свободного холестерола, входящего в оболочку липопротеинов, и его эфиров, которые вместе с ТАГ составляют внутреннее содержимое этих частиц. Содержание холестерола и его эфиров в составе хиломикронов составляет ~ 5 %, в ЛПОНП ~10 %, в ЛПНП ~ 50—60 % и в ЛПВП ~ 20—30 %. Концентрация холестерола в сыворотке крови взрослого человека в норме равна ~ 200 мг/дл или 5,2 ммоль/л, что соответствует холестериновому равновесию, когда количество холестерола, поступающего в организм, равно количеству холестерола выводимому из организма. Если концентрация холестерола в крови выше нормы, то это указывает на задержку его в организме и является фактором риска развития атеросклероза.
Холестерол является предшественником всех стероидов животного организма:
Холестериновое равновесие поддерживается благодаря тому, что с одной стороны холестерол поступает с пищей (~ 0,3—0,5 г/с) и синтезируется в печени или других тканях (~ 0,5 г/с), а с другой — выводится с калом в виде жёлчных кислот, холестерола желчи, продуктов катаболизма стероидных гормонов, с кожным салом, в составе мембран слущенного эпителия (~ 1,0 г/с)
Биосинтез холестерола[править | править код]
Транспорт холестерола[править | править код]
Эйкозаноиды, включающие в себя простагландины, тромбоксаны, лейкотриены и ряд других веществ, — высокоактивные регуляторы клеточных функций. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как «гормоны местного действия», влияя на метаболизм продуцирующей их клетки по аутокринному механизму, и на окружающие клетки — по паракринному механизму. Эйкозаноиды участвуют во многих процессах: регулируют тонус гладкомышечных клеток и вследствие этого влияют на АД, состояние бронхов, кишечника, матки. Эйкозаноиды регулируют секрецию воды и натрия почками, влияют на образование тромбов. Разные типы эйкозаноидов участвуют в развитии воспалительного процесса, происходящего после повреждения тканей или инфекции. Такие признаки воспаления, как боль, отёк, лихорадка, в значительной мере обусловлены действием эйкозаноидов. Избыточная секреция эйкозаноидов приводит к ряду заболеваний, например, бронхиальной астме и аллергическим реакциям.
Субстраты для синтеза эйкозаноидов[править | править код]
Основным субстратом для синтеза эйкозаноидов является арахидоновая (ω-6-эйкозатетраеновая) кислота, содержащая 4 двойные связи при углеродных атомах (5, 8, 11, 14). Она может поступать с пищей или синтезироваться из линолевой кислоты. В небольших количествах для синтеза эйкозаноидов могут использоваться ω-6-эйкозатриеновая кислота с тремя двойными связями (5, 8, 11) и ω-3-эйкозапентаеновая кислота, в составе которой имеется 5 двойных связей в положениях 5, 8, 11, 14, 17. Обе минорные эйкозановые кислоты либо поступают с пищей, либо синтезируются из олеиновой и линоленовой кислот соответственно.
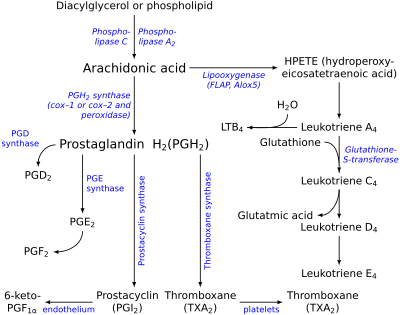
Синтез лейкотриенов, ГЭТЕ(гидроксиэйкозатетроеноатов), липоксинов[править | править код]
Синтез лейкотриенов идёт по пути, отличному от пути синтеза простагландинов, и начинается с образования гидроксипероксидов — гидропероксидэйкозатетраеноатов (ГПЭТЕ). Эти вещества или восстанавливаются с образованием гидроксиэйкозатетроеноатов (ГЭТЕ) или превращаются в лейкотриены или липоксины. ГЭТЕ отличаются по положению гидроксильной группы у 5-го, 12-го или 15-го атома углерода, например: 5-ГЭТЕ, 12-ГЭТЕ.
Липоксины (например, основной липоксин А4) включают 4 сопряжённых двойных связи и 3 гидроксильных группы.
Синтез липоксинов начинается с действия на арахидоновую кислоту 15-липоксигеназы, затем происходит ряд реакций, приводящих к образованию липоксина А4
Клинические аспекты обмена эйкозаноидов[править | править код]
Медленно реагирующая субстанция при анафилаксии (МРВ-А) представляет собой смесь лейкотриенов С4, D4 и Е4. Эта смесь в 100—1000 раз более эффективна, чем гистамин или простагландины как фактор, вызывающий сокращение гладкой мускулатуры бронхов. Эти лейкотриены вместе с лейкотрином В4 повышают проницаемость кровеносных сосудов и вызывают приток и активацию лейкоцитов, а также, являются важными регуляторами при многих заболеваниях, в развитии которых участвуют воспалительные процессы или быстрые аллергические реакции (например, при бронхиальной астме).
Использование производных эйкозаноидов в качестве лекарственных средств[править | править код]
Хотя действие всех типов эйкозаноидов до конца не изучено, имеются примеры успешного использования лекарств — аналогов эйкозаноидов для лечения различных заболеваний. Например, аналоги PG Е1 и PG Е2 подавляют секрецию соляной кислоты в желудке, блокируя гистаминовые рецепторы II типа в клетках слизистой оболочки желудка. Эти лекарства, известные как Н2-блокаторы, ускоряют заживление язв желудка и двенадцатиперстной кишки. Способность PG Е2 и PG F2α стимулировать сокращение мускулатуры матки используют для стимуляции родовой деятельности.
Сфинголипиды — производные церамида, образующегося в результате соединения аминоспирта сфингозина и жирной кислоты. В группу сфинголипидов входят сфингомиелины и гликосфинголипиды.
Сфингомиелины находятся в мембранах клеток различных тканей, но наибольшее их количество содержится в нервной ткани. Сфингомиелины миелиновых оболочек содержат в основном жирные кислоты с длинной цепью: лигноцериновую и нервоновую кислоты, а сфингомиелин серого вещества мозга содержит преимущественно стеариновую кислоту.
Синтез церамида и его производных[править | править код]
Катаболизм сфингомиелина и его нарушения[править | править код]
В лизосомах находятся ферменты, способные гидролизовать любые компоненты клеток. Эти ферменты называют кислыми гидролазами, так как они активны в кислой среде.
В условиях положительного калорийного баланса значительная часть потенциальной энергии пищевых продуктов запасается в виде энергии гликогена или жира. Во многих тканях даже при нормальном питании, не говоря уже о состояниях калорийного дефицита или голодания, окисляются преимущественно жирные кислоты, а не глюкоза. Причина этого — необходимость сохранения глюкозы для тех тканей (например, для мозга или эритроцитов), которые постоянно в ней нуждаются. Следовательно, регуляторные механизмы, часто с участием гормонов, должны обеспечивать постоянное снабжение всех тканей подходящим топливом в условиях как нормального питания, так и голодания. Сбой в этих механизмах происходит при гормональном дисбалансе (например, в условиях недостатка инсулина при диабете), при нарушении метаболизма в период интенсивной лактации (например, при кетозе крупного рогатого скота) или из-за усиления обменных процессов при беременности (например, при токсикозе беременности у овец). Такие состояния представляют собой патологические отклонения при синдроме голодания; он наблюдается при многих заболеваниях, сопровождающихся снижением аппетита.
Тучность[править | править код]
Абеталипопротеинемия[править | править код]
Это относительно редкое генетическое заболевание характеризуется отсутствием в плазме β-липопротеидов плотности, меньшей чем 1,063 и связано с интенсивной демиелинизацией нервных волокон. Апо-В отсутствует в плазме, так же как и в хиломикронах, ЛПОНП и ЛПНП. Уровень триацилглицеринов и холестерина плазмы очень низок. Это свидетельствует о необходимости апо-В для нормального всасывания, синтеза и транспорта триацилглицеринов и холестерина из кишечника и печени. Липиды накапливаются в клетках слизистой оболочки кишечных ворсинок, при этом наблюдается акантоцитоз — сферическая деформация эритроцитов. Более 80 % эритроцитов являются акантоцитами, или, как их иначе называют, зубчатыми эритроцитами (от греч. akantha — зубец, шип).
Кахексия[править | править код]
Недостаточное потребление калорий может привести и к полному исчезновению жировой ткани из подкожного и сальникового депо. Это может происходить при опухолях или хроническом инфекционном заболевании, при недостаточном питании или при метаболических нарушениях, таких, как диабет или увеличение щитовидной железы. В экспериментах было показано, что повреждение определённых областей гипоталамуса вызывает анорексию даже у предварительно голодавшего животного. Для анорексии, в происхождении которой имеет значение психогенный компонент, используют термин «anorexia nervosa» (нейрогенная анорексия).
В то время как потеря липидов тела при болезни щитовидной железы связана частично с избыточной мобилизацией резервных липидов, существенной причиной кахексии при голодании, недостаточности тиамина или диабете является сниженная способность организма синтезировать жирные кислоты из углеводных предшественников.
Атеросклероз[править | править код]
Атеросклероз (от греч. ἀθέρος — мякина, кашица + σκληρός — твёрдый, плотный) — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов. Отложения формируются в виде атероматозных бляшек. Последующее разрастание в них соединительной ткани (склероз), и кальциноз стенки сосуда приводят к деформации и сужению просвета вплоть до облитерации (закупорки). Важно различать атеросклероз от артериосклероза Менкеберга, другой формы склеротических поражений артерий, для которой характерно отложение солей кальция в средней оболочке артерий, диффузность поражения (отсутствие бляшек), развитие аневризм (а не закупорки) сосудов. Атеросклероз сосудов ведет к развитию ишемической болезни сердца.
Молекулярные механизмы патогенеза атеросклероза[править | править код]
Таганович и др. Биологическая химия. — Минск: Высшая школа, 2013. — ISBN 978-985-06-2321-8.
