Гликозаминогликаны (мукополисахариды). «БИОЛОГИЧЕСКАЯ ХИМИЯ», Березов Т.Т., Коровкин Б.Ф.
Гликозаминогликаны соединительной ткани – это линейные неразветвлен-ные полимеры, построенные из повторяющихся дисахаридных единиц. В организме гликозаминогликаны не встречаются в свободном состоянии, т.е. в виде «чистых» углеводов. Они всегда связаны с большим или меньшим количеством белка. В их состав обязательно входят остатки мономера либо глюкозамина, либо галактозамина. Второй главный мономер дисахаридных единиц также представлен двумя разновидностями: D-глюкуроновой и L-идуроновой кислотами. В настоящее время четко расшифрована структура шести основных классов гликозаминогликанов (табл. 21.2).
Гиалуроновая кислота впервые была обнаружена в стекловидном теле глаза. Из всех гликозаминогликанов гиалуроновая кислота имеет большую мол. массу (100000–10000000). Доля связанного с гиалуроновой кислотой белка в молекуле (частице) протеогликана составляет не более 1–2% от его общей массы. Считают, что основная функция гиалуроновой кислоты в соединительной ткани – связывание воды.
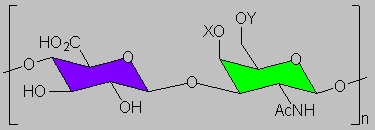
В результате такого связывания межклеточное вещество приобретает характер желеобразного матрикса, способного «поддерживать» клетки. Важна также роль гиалуроновой кислоты в регуляции проницаемости тканей. Приводим структуру повторяющейся дисахаридной единицы в молекуле гиалуроновой кислоты:
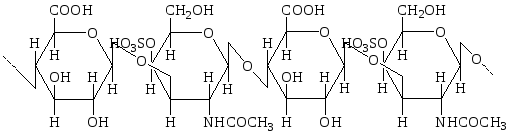
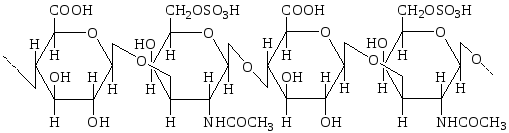
Хондроитин-4-сульфат и хондроитин-6-сульфат построены по одному плану. Отличие между ними заключается в локализации сульфатной группы. Несмотря на минимальные различия в химической структуре, физико-химические свойства хондроитин-4-сульфата и хондроитин-6-сульфата существенно различаются; последние различаются также распределением в разных видах соединительной ткани (табл. 21.3).
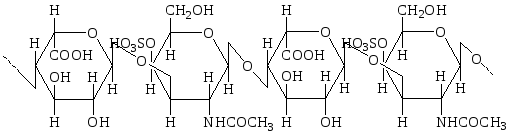
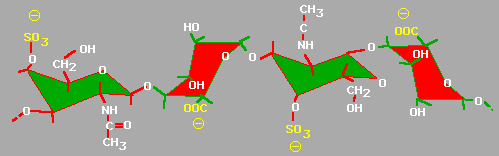
Дерматансульфат особенно характерен для дермы (кожи). Он резистентен к действию гиалуронидаз (тестикулярной и бактериальной). В этом одно из отличий дерматансульфата от хондроитинсульфатов. Кроме того, в состав дисахаридной единицы дерматансульфата входит L-идуроновая, а не D-глюкуроновая кислота (в малом количестве D-глюкуроновую кислоту можно обнаружить в повторяющихся единицах дерматансульфата):
О биологической роли дерматансульфата почти ничего неизвестно. Роль этого гликозаминогликана не может быть сведена только к стабилизации коллагеновых пучков, так как дерматансульфат обнаруживается и в тканях эктодермального происхождения, не содержащих коллагена.
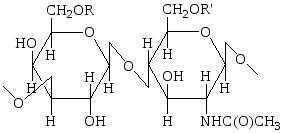
Кератансульфат впервые был выделен из роговой оболочки глаза быка, отсюда и название этого гликозаминогликана. В противоположность всем остальным гликозаминогликанам кератансульфат не содержит ни D-глю-куроновой, ни L-идуроновой кислоты:
Установлено, что кератансульфат, выделенный из роговицы глаза (кера-тансульфат I), и кератансульфат, полученный из хрящевой ткани (кера-тансульфат II), различаются по степени сульфатированности и строению связи между кератансульфатом и пептидной частью протеогликана.
Гепарин известен прежде всего как антикоагулянт. Однако его следует относить к гликозаминогликанам, так как он синтезируется тучными клетками, которые являются разновидностью клеточных элементов соединительной ткани. Он может входить в состав протеогликанов; с гликоз-аминогликанами его объединяет и химическая структура.
Гепаринсульфат в отличие от гепарина в дисахаридных единицах чаще содержит N-ацетильные группы, чем N-сульфатные. Кроме того, степень О-сульфатирования гепаринсульфата ниже, чем гепарина.
Биосинтез гликозаминогликанов. Известно, что синтез глюкозамина и глюкуроновой кислоты, входящих в состав гиалуроновой кислоты, происходит из D-глюкозы. Непосредственные предшественники гиалуро-новой кислоты – нуклеотидные (уридиндифосфонуклеотидные) производные N-ацетилглюкозамина и глюкуроновой кислоты.
Предшественником углеводных остатков сульфатированных гликоза-миногликанов, как и у гиалуроновой кислоты, является молекула D-глю-козы. Далее происходит эпимеризация глюкозамина в галактозамин, а глюкуроновой кислоты при синтезе дерматансульфата – в идуроновую кислоту. Нуклеотидные производные этих соединений утилизируются при биосинтезе сульфатированных гликозаминогликанов, при этом сульфат включается в биосинтез гликозаминогликанов в виде 3′-фосфоаденозин-5′-фосфосульфата (ФАФС). В процессе биосинтеза гликозаминогликанов принимает участие большое количество различных ферментов, в том числе трансфераз.
Предыдущая страница | Следующая страница
СОДЕРЖАНИЕ
Еще по теме:Хондроитинсульфаты Распространение в природе
Хондроитинсульфаты– самые распространенные представители гликозаминогли-канов в живом организме. Они являются главными компонентами многих тканей, включая хрящи, кожу, сухожилия, связки. Хондроитинсульфаты были обнаружены в пупочном канатике, артерии, роговице глаза, в клапанах сердца и аорте, селезенке, мозге, слюне. Известно несколько типов хондроитинсульфатов. Наиболее изучены 4 представителя, которые принято обозначать буквами латинского алфавита:
Химическое строение и молекулярная структура
Макромолекулы хондроитинсульфата А(хондроитин-4-сульфата) состоят из чередующихся звеньев остатковβ-D-глюкуроновой кислоты
|
Рис.1.Структурная формула макромолекулы хондроитинсульфата А. |
Хондроитинсульфат С(хондроитин-6-сульфат) и хондроитинсульфат А (хондроитин-4-сульфат) построены по одному принципу. Отличие между ними заключается в локализации сульфатной группы. Дисахаридный фрагмент хондроитин-6-сульфата включает звенья остатков
|
Рис.2.Структурная формула макромолекулы хондроитинсульфата С. |
Хондроитинсульфат В (дерматансульфат) построен из чередующихся остатковα-L-идуроновой кислотыи4-сульфат-N-ацетил-β-D-галактозамина, соединенныхβ-(1→3)-гликозидными связями. Дисахаридные фрагменты связаныβ-(1→4)-гликозидными связями. Структурная формула дерматансульфата представлена на рисунке 3.
|
Рис. 3. Структурная формула макромолекулы хондроитинсульфата В. |
В отличие от остальных гликозаминогликанов макромолекулы хондроитинсульфата D (кератансульфата) не содержат звенья остатков глюкуроновой и идуроновой кислот. Дисахаридная единица состоит из звеньев остатковβ-D-галактопиранозыиN-ацетил-D-глюкозамин-6-сульфата, соединенных β-(1→4)-гликозидными связями. Дисахаридные фрагменты соединены β-(1→3)-гликозидными связями (рис.4.).
|
Кератансульфаты – сложные гетерогенные гликозаминогликаны. Различают два типа кератансульфатов: кератансульфат I и кератансульфат II. Они отличаются друг от друга суммарным содержанием остатков низкомолекулярных углеводов и локализацией в живом организме.Кератансульфат Iприсутствует главным образом в роговице глаза и содержит кроме вышеуказанной повторяющейся дисахаридной единицы (см. рис.4) звенья остатковL-фукозы,D-маннозы и сиаловой кислоты.Кератансульфат
Энергетически выгодной конформацией пиранозных циклов макромолекул всех хондроитинсульфатов является конформация кресла С1(рис.5).
(а) |
|
(б) |
|
Рис.5. Конформация повторяющихся единиц макромолекул хондроитинсульфатов (а) и дерматансульфата (б). На (а): X= –H, –SO3—;Y= –H, –SO3—. |
На рис.5 б на примере дерматансульфата показаны также функциональные группы звеньев макромолекул, несущие отрицательный заряд и определяющие полиэлектролитный характер данного класса полисахаридов.
Получение
Один из наиболее богатых источников хондроитинсульфатов – хрящ носовой перегородки(20-40%). Поскольку ткань хряща наряду с хондроитинсульфатами содержит большое количество коллагена, при получении полисахаридов из биомассы необходимо отделить белковую часть. Наилучший метод выделения – экстракция хлоридом калия. В полученный экстракт добавляют ацетатный буфер для осаждения коллагена. Затем уделяют примеси адсорбцией на каолине. Полученный фильтрат подвергают диализу от низкомолекулярных соединений. К диализованному раствору вновь добавляют ацетатный буфер и пропускают через колонку с коалином. (Для очистки хондроитинсульфатов от низкомолекулярных примесей можно использовать также препаративный электрофорез.) Фильтрат упаривают в вакууме и осаждают хондроитинсульфат концентрированным раствором этилового спирта.
Физические свойства
Хондроитинсульфаты построены из макромолекул преимущественно линейного строения. Относятся к классу полужесткоцепных полимеров. Считается, что макромолекулы хондроитинсульфатов в разбавленных растворах имеют форму палочек длиной ~3700 Å.
Молекулярная масса различных типов хондроитинсульфатов лежит в пределах (20-50)∙103Да.
Хондроитинсульфаты растворимы в воде и нерастворимы в органических растворителях.
Хондроитинсульфаты – оптически активные
полимеры. Их водные растворы обладают
отрицательными величинами удельного
оптического вращения 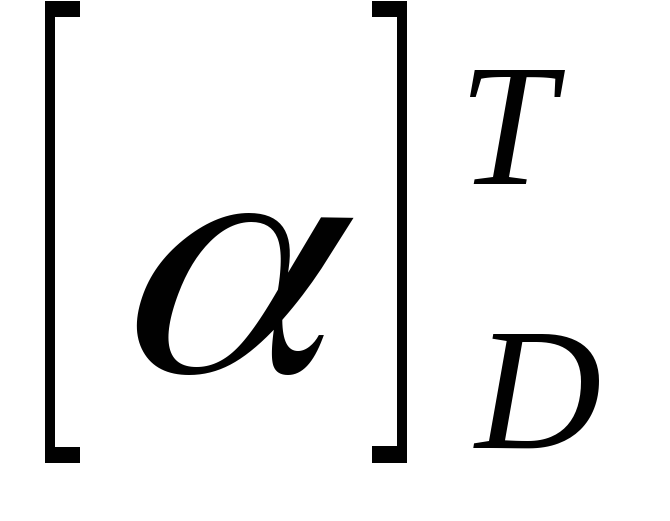 .
Для хондроитин-4-сульфата –
.
Для хондроитин-4-сульфата –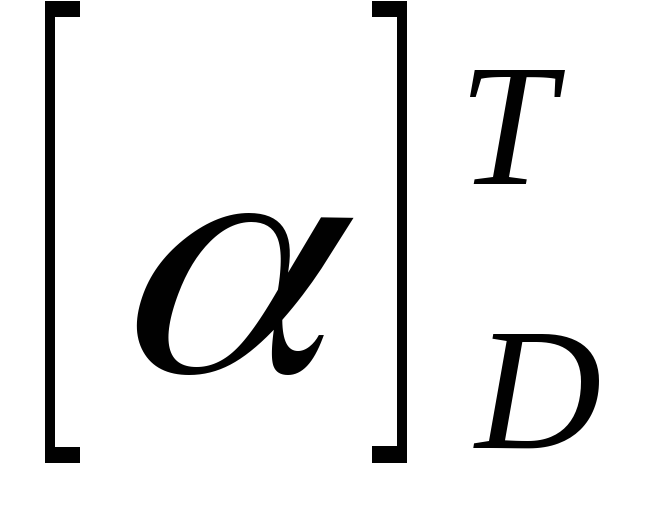 = (–28) — (–33)
град., хондроитин-6-сульфата –
= (–28) — (–33)
град., хондроитин-6-сульфата –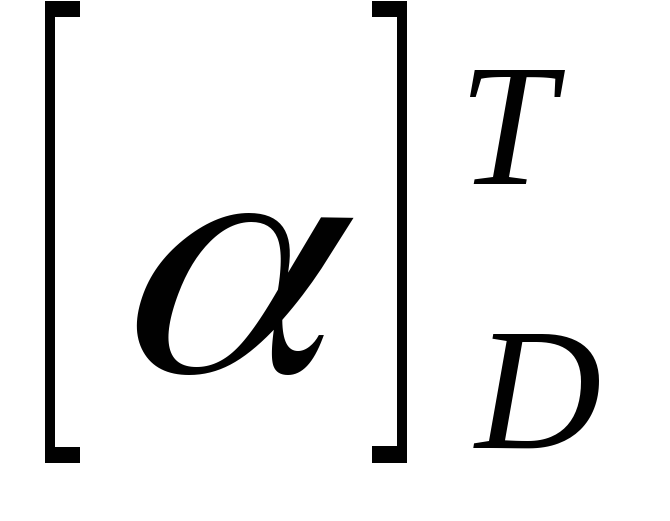 = (–12) — (–22)
град., дерматансульфата –
= (–12) — (–22)
град., дерматансульфата –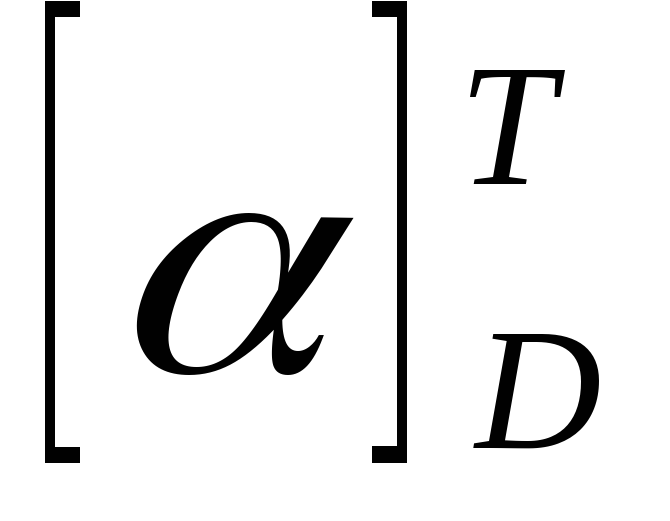 = (–55) — (–76)
град.
= (–55) — (–76)
град.
Химические свойства
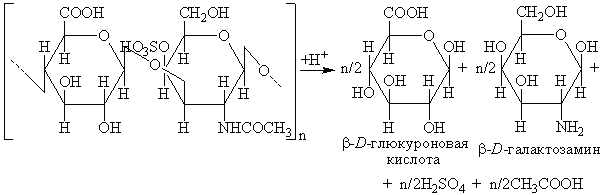
Гидролиз в кислой среде. Продуктами полного кислотного гидролиза хондроитинсульфатов (кроме кератансульфата) являютсяβ-D-глюкуроновая (или α-L-идуроновая кислота),β-D-галактозамин, серная и уксусная кислоты.В качестве примера на рис.6 приведена схема реакции кислотного гидролиза хондроитинсульфата А.
|
Рис.6. Кислотный гидролиз хондроитин-4-сульфата. |
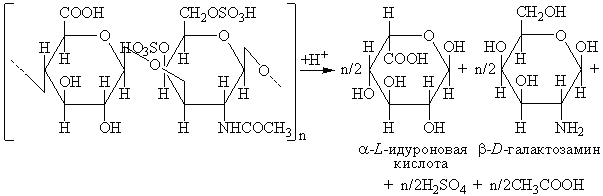
Реакция гидролиза дерматансульфата в кислой среде представлена на рис.7.
|
Рис.7.Кислотный гидролиз дерматансульфата. |
Ферментативный гидролиз.Продуктами ферментативного гидролиза хондроитинсульфатов под действиемгиалуронидазразличного типа являются ди- и тетрасахариды. Может образовываться также ненасыщенный дисульфатированный дисахарид.
Биологическая активность и применение хондроитинсульфатов
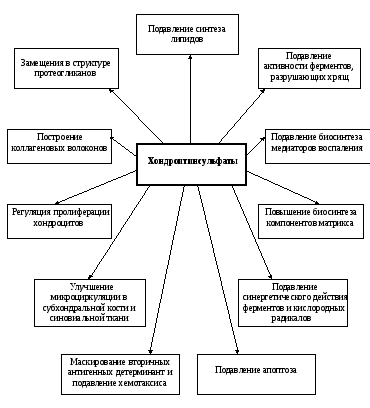
Хондроитинсульфаты оказывают разнообразное влияние на живой организм (рис.8).
Рис.8.Направления влияния хондроитинсульфатов на показатели обмена соединительного матрикса. |
Хондроитинсульфаты относятся к группе так называемых хондропротекторов– веществ, обладающих структурно-модифицирующим действием и являющихся дополнительным субстратом для образования тканей, особенно хрящевой и кожной. Они ингибируют специфические ферменты, разрушающие хрящевую ткань и кожу над воспаленными суставами,замедляют резорбцию костной ткани и снижают потерю кальция.Хондроитинсульфаты улучшают фосфорно-кальциевый обмен в хрящевой ткани, стимулируютнакопление жидкостив глубоких слоях кожи.
Хондроитинсульфаты успешно применяются при лечении остеоартроза,остеохандроза, коксартроза. Ткань хряща состоит, главным образом, из коллагена, протеогликанов, воды и специализированных клетокхондроцитов, содержащих в основном хондроитинсульфаты.При остеоартрозе в патологический процесс вовлечен суставной хрящ и прилежащая к нему кость (рис.9). По разным причинам (нарушение обмена веществ), травма, физические перегрузки суставов и др. возможно разрушение хрящевой ткани: теряется способность удерживать влагу, сохранять упругость и эластичность. Первый признак этого – хруст в суставах.
|
Рис.9. Иллюстрация патологических процессов при остеоартрозе и остеохандрозе. |
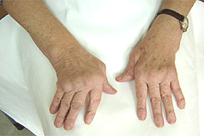
Аналогичные изменения происходят и в позвоночнике. При остеохондрозе межпозвонковые диски («прокладки» между позвонками) теряют до 50% хондроитинсульфата (рис.9). Исчезает гибкость, на смену приходят хруст, утренняя скованность, «усталость, слабость», боль в спине и голове, которая замечается при длительном пребывании в одном положении (долгая работа за компьютером, за рулем автомобиля, длительное стояние за прилавком магазина). При повышенной нагрузке на позвоночник (садово-огородные работы, перенос тяжестей) в хрящевой ткани межпозвонковых дисков появляются трещинки и разрушения. Как результат – ущемление нервов и сосудов, припухлость пораженного сустава, развитие типичных деформаций суставов, наличие костных разрастаний (рис.10).
|
Рис.10. Костные разрастания (узелки Гебердена и Бушара) суставов. |
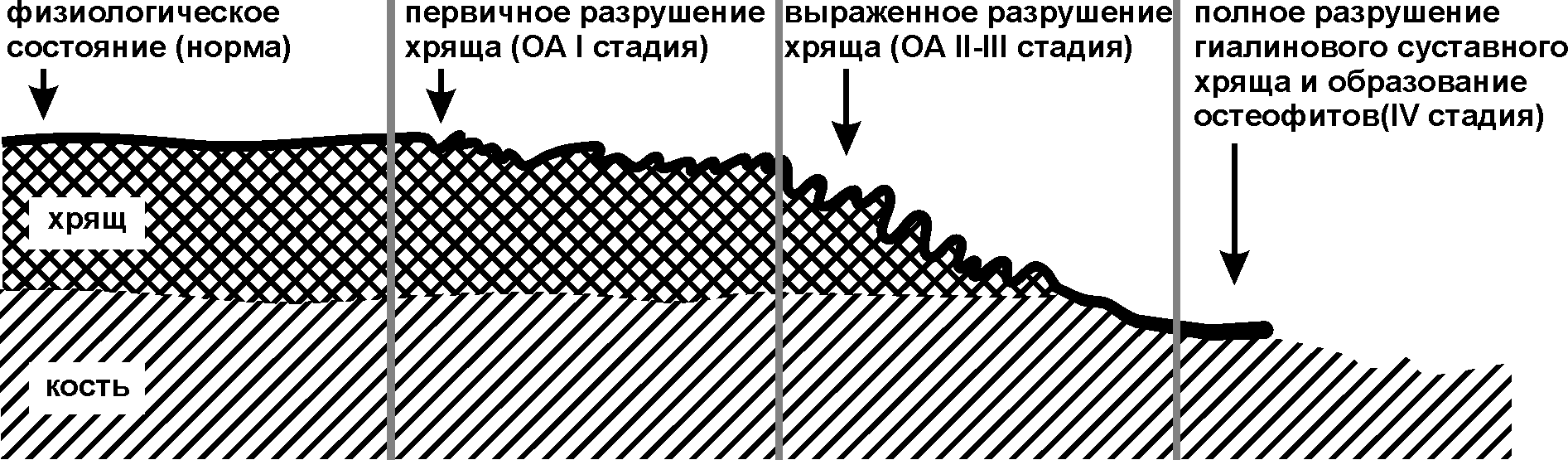
Хондроитинсульфаты воздействуют на причину болезни. Они стимулируют деятельность клеток-хондроцитови служат сырьем для синтеза молекулпротеогликанов.При наличии большого количества хондроитинсульфатов в хряще синтезируется больше протеогликанов, которые удерживают значительное количество воды, улучшая образование суставной жидкости, стимулируя образование белка-коллагена и делая хрящевую ткань влажной и упругой. Таким образом, гликозаминогликаны участвуют как в процессах образования, так и регенерации тканей суставов (рис.11).
|
Рис.11. Стадии разрушения хрящевых тканей. |
Подобное комплексное воздействие хондропротекторов на сустав делает их незаменимыми в лечебной практике.
На основе хондроитинсульфатов созданы многочисленные лекарственные препараты (хондропротекторы) ибиологически активные добавки (БАД), такие как «Глюкозамин хондроитин», «Артрин», «Хондролон», «Мукосат», «Амфлутол», «Структум», «Хонсурид», «Хонда хондропротектор», «Хондроксид», «Сустанорм», «Флексалис», «Сустафорт гель для тела», «Элемент 5 формула С», «Анавита+» и др. (рис.12).
(а) | (б) | (в) |
|
|
|
Рис.12. БАДы (а,б) и лекарственный препарат «Структум» (в) на основе хондроитинсульфатов. | ||
Они регулируют обмен в хрящевой ткани, оказывают питательную поддержку суставам, препятствуют разрушению и способствуют восстановлению хрящевой ткани, оказывают противовоспалительное действие, участвуют в формировании связок, костей
Хондроитин | Info-Farm.RU
Хондроитинсульфат — биологическая макромолекула, что синтезируется фибробластами и является важной составляющей хрящевой ткани, которая сопротивляется при сжатии. Представляет собой полимерный сульфатированные гликозаминогликаны. Входят в состав синовиальной жидкости. Представляет собой сульфатированные гликозаминогликаны (ГАГ), содержащий два вида углеводных остатков N-ацетилгалактозамин и глюкуроновую кислоту, поочередно чередуются в цепи хондроитин сульфата.
В медицине хондроитина сульфат применяется как лекарственное средство группы нестероидных противовоспалительных препаратов.
Химическое строение
Цепи хондроитин сульфата является неразветвлёнными полисахаридами без фиксированной длины. Хондроитин сульфат состоит только из двух простых сахаров, постоянно меняют одно одного D-глюкуроновой кислоты и N-ацетилгалактозамину. Глюкуроновая кислота сочетается с N-ацетилгалактозамином гликозидной связью β-1,3, а N-ацетилгалактозамину к глюкуроновой кислоты β-1,4. Цепь хондроитин сульфата может содержать более 100 сахарных остатков, которые могут достаточно сильно отличаться между собой. Атомы N-ацетилгалактозамину C 6 и / или C 4 могут быть сульфатированных. Если глюкуроновая кислота епимеризована на С5 в индуроновой кислоты, то такой ГАГ называется дерматансульфат.
Сульфатирования
Каждый простой углевод может содержать одну или две сульфогруппы, или не содержать никакой. Чаще всего сульфогруппы приеднануються к гидроксигруппы 4 и 6 атома углерода. Сульфатирования катализируется различными сульфотрансферазамы. Степень сульфатизации в среднем составляет 0.8 на дисахарид.
Различают такие типы хондроитин сульфата:
| Тип хондроитин сульфата | Систематическая название | Дисахаридного остаток | Детальное описание |
|---|---|---|---|
| хондроитин сульфат А | хондроитин-4-сульфат | Пример | сульфатная группа размещена преимущественно на 4 атоме углерода N-ацетилхолина |
| хондроитин сульфат B | дерматансульфат | Пример | сульфатная группа размещена преимущественно на 2 атоме углерода индуроновой кислоты и на 4 атоме углерода N-ацетилхолина |
| хондроитин сульфат C | хондроитин-6-сульфат | Пример | сульфатная группа размещена преимущественно на 6 атоме углерода N-ацетилхолина |
| хондроитин сульфат D | хондроитин-2,6-сульфат, дерматан сульфат | Пример | сульфатная группа размещена преимущественно на 2 глюкуроновой кислоты и на 4 атоме углерода N-ацетилхолина (Хондроитин-2,6-сульфат) |
| хондроитин сульфат E | хондроитин-4,6-сульфат | Пример | сульфатная группа размещена преимущественно на 4 и 6 атомах углерода N-ацетилхолина |
Типирование по буквами от А до Е применялось еще в те времена, когда хондроитин сульфат был изолирован (выделенный), но его формула не была известна. Отнесение дерматансульфата к хондроитин сульфатов как хондроитин сульфата В рассматривается сейчас как ошибочное, поскольку эта молекула не содержит ни глюкуроновой, ни индуроновой кислоты. Чаще всего встречается хондроитин сульфат А, В и С типов. Ранее название хондроитин (без сульфат) использовали для названия цепи с небольшим количеством сульфатных групп или вовсе без них, на сегодня этот срок больше не используется.
Связывание белка
В живых организмах хондроитин сульфат связан с белком, оба являются частью одного протеогликана. Связывание цепей хондроитин сульфата осуществляется сериновых остаток гидроксигруппы определенного белка. Неизвестно, каким образом выбираются белки для связывания с гликозаминогликанами. Гликозилированы сериновые остатки часто следуют за глициновыми остатками, по соседству находится кислые остатки аминокислот. Связующим агентом ГАГ-цепи постоянно служит одинаковый сахарный цепь из трех углеводов:
Ser-O- Xyl-Gal-Gal -GlcA -...
Каждый углевод связывается специфическим ферментом, из-за чего возможен многоуровневый контроль на синтез ГАГ. Ксилоза связывается эндоплазматической сетью белками, в то время как остаток углевода переносится в аппарат Гольджи.
Функции хондроитин сульфата
Функция хондроитина очень зависит от свойств целого протеогликана, частью которого она является. Протеогликан хондроитина имеет как структурную так и регулирующую функции.
Структурная функция
Протеогликан-хондроитина, представляет собой вместе с коллагеном значительную составляющую часть внеклеточной вещества. Они оказывают структурную целостность тканей. Типичными представителями являются агрекан, версикан, бревикан и нейрокан.
Хондроитин сульфат как составная часть агрекану формирует большую часть хрящевой массы. Плотно размещены, сильно заряженные сульфатные группы ведут к электростатического отталкивания отдельных цепей, который и обусловливает значительную часть сопротивления хряща на сжатие. Снижение количества хондроитина сульфата в хрящи — частая причина артроза.
Биологическая роль
Хондроитинсульфат имеет тропность к хрящевой ткани, инициирует процесс фиксации серы в процессе синтеза хондроитин-серной кислоты, что, в свою очередь, способствует отложению кальция в костях. Стимулирует синтез гиалуроновой кислоты, укрепляя соединительнотканные структуры: хряща, сухожилий, связок, кожи. Оказывает анальгетическое и противовоспалительное действие, является хондропротектором, способствует активной регенерации хряща.
Особенностью хондроитин среди протеогликаниив является его способность сохранять воду в толще хряща в виде водных полостей, создающих хорошую амортизацию и поглощающие удары, что в итоге повышает прочность соединительной ткани. Важной действием хондроитина является его способность угнетать действие специфических ферментов, разрушающих соединительную ткань, в том числе лизосомальных ферментов, высвобождающихся в результате разрушения хондроцитов (эластаза, пептидаза, катепсин, интерлейкин-1 и др.)
Естественное потребление хондроитинсульфата и других хондропротекторных веществ осуществлялось с употреблением в пищу сухожилий, кожи и хрящей животных, особенно рыб. В связи с уменьшением доли этих продуктов в рационе современного человека (иногда и с полным исключением), а также при метаболических нарушениях, чрезмерных функциональных нагрузках и особенно возрастном снижении активности синтетических процессов хондроитинсульфат должен поступать уже в готовом виде (или в виде предшественников синтеза ) извне в том числе с пищей.
Фармакология
По данным разработчиков лекарственных средств хондроитина сульфат замедляет резорбцию костной ткани и снижает потерю Ca 2+. Улучшает фосфорно-кальциевый обмен в хрящевой ткани, ускоряет процессы ее восстановления, тормозит процессы дегенерации хрящевой и соединительной ткани. Подавляет активность ферментов, вызывающих поражение хрящевой ткани, стимулирует синтез гликозаминогликанов, способствует регенерации суставной сумки и хрящевых поверхностей суставов, увеличивает продукцию внутрисуставной жидкости. Уменьшает болезненность и увеличивает подвижность пораженных суставов. Структура хондроитин сульфата схожа с гепарином, поэтому данное соединение, потенциально, может препятствовать образованию фибриновых тромбов в синовиальной и субхондральной микроциркуляторном русле.