| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
| ||||
|
Пиридоксина гидрохлорид — это… Что такое Пиридоксина гидрохлорид?
Пиридоксина гидрохлоридДействующее вещество
›› Пиридоксин* (Pyridoxine*)
Латинское название
Pyridoxini hydrochloridum
АТХ:
›› A11HA02 Пиридоксин (витамин В6)Фармакологическая группа: Витамины и витаминоподобные средства
Нозологическая классификация (МКБ-10)
›› D50 Железодефицитная анемия›› E53.
 1 Недостаточность пиридоксина
1 Недостаточность пиридоксина›› G21 Вторичный паркинсонизм
›› G25 Другие экстрапирамидные и двигательные нарушения
›› K25 Язва желудка
›› K26 Язва двенадцатиперстной кишки
›› K73 Хронический гепатит, не классифицированный в других рубриках
›› L20 Атопический дерматит
›› L30.9 Дерматит неуточненный
›› L40 Псориаз
›› O14.9 Преэклампсия [нефропатия] неуточненная
Состав и форма выпуска
1 ампула с 1 мл раствора для инъекций содержит пиридоксина гидрохлорида 0,01 или 0,05 г; в коробке 10 шт.
1 таблетка — 0,002, 0,005 или 0,01 г; в банке 50 шт.
Фармакологическое действие
Фармакологическое действие — восполняющее дефицит витамина B6.
Показания
Гиповитаминоз, язвенная болезнь желудка и двенадцатиперстной кишки, гипохромная и микроцитарная анемии, паркинсонизм, хорея, токсикоз беременных, гепатит, дерматит, экссудативный диатез, нейродермиты, псориаз.
Противопоказания
Гиперчувствительность.
Побочные действия
Аллергические реакции.
Способ применения и дозы
Внутрь, после еды; профилактически — 0,002–0,005 г (детям — 0,002 г) в день; лечебные дозы — 0,02–0,03 г 1–2 раза в день (детям дозу уменьшают соответственно возрасту). В/м — 0,05–0,1 г (детям — 0,02 г) в сутки (в 1–2 приема). Курс лечения — 1 мес (для детей — 2 нед). При паркинсонизме — по 2 мл 5% раствора в день (курс 20–25 инъекций).
Срок годности
3 года
Условия хранения
Список Б.: В защищенном от света месте.
Словарь медицинских препаратов. 2005.
ПИКОВИТ сироп — инструкция по применению, цена, дозировки, аналоги, противопоказания
Действующие вещества
— декспантенол (dexpanthenol)— пиридоксина гидрохлорид (вит. B6) (pyridoxine)
— цианокобаламин (вит. B12) (cyanocobalamin)
— аскорбиновая кислота (вит. С) (ascorbic acid)
— ретинол (в форме пальмитата) (вит. А) (retinol)
— никотинамид (вит.
 PP) (nicotinamide)
PP) (nicotinamide)— тиамина гидрохлорид (вит. B1) (thiamine)
— рибофлавин (в форме фосфата натрия) (riboflavin)
— колекальциферол (вит. D3) (colecalciferol)
Состав и форма выпуска препарата
◊ Сироп для детей в виде густой, вязкой жидкости, от светло-желтого до коричневато-оранжевого цвета, с запахом цитрусовых и кислым вкусом; допустимо присутствие едва видимых включений.
| 5 мл | |
| ретинол (в форме пальмитата) (вит. А) | 900 МЕ |
| колекальциферол (вит. D3) | 100 МЕ |
| аскорбиновая кислота (вит. С) | 50 мг |
| тиамина гидрохлорид (вит. B1) | 1 мг |
| рибофлавин (в форме натрия фосфата) (вит. В2) | 1 мг |
| декспантенол (D-пантенол) (вит. В5) | 2 мг |
| пиридоксина гидрохлорид (вит. B6) | 600 мкг |
цианокобаламин (вит. B12) B12) | 1 мкг |
| никотинамид (вит. PP) | 5 мг |
Вспомогательные вещества: агар, камедь трагакантовая, сахароза, декстроза (глюкоза) жидкая, масло апельсиновое, ароматизатор грейпфрутовый, ароматизатор апельсиновый, полисорбат 80 (твин 80), лимонной кислоты моногидрат, краситель пунцовый (Понсо 4R) (Е124), натрия бензоат, вода очищенная.
150 мл — флаконы темного стекла (1) в комплекте с дозирующей ложкой — пачки картонные.
Фармакологическое действие
Поливитаминное лекарственное средство. Содержит комплекс витаминов, являющихся важными факторами метаболических процессов в организме.
Ретинол (витамин А) участвует в синтезе различных веществ (белков, липидов, мукополисахаридов) и обеспечивает нормальную функцию кожи, слизистых оболочек, а также органа зрения.
Колекальциферол (витамин D3) играет важную роль в поддержании баланса кальция и фосфора в организме. При его недостатке в костной ткани уменьшается содержание кальция (остеопороз).
Тиамин (витамин В1) нормализует деятельность сердца и способствует нормальному функционированию нервной системы.
Рибофлавин (витамин В2) способствует регенерации тканей, в т.ч. клеток кожи.
Пиридоксин (витамин В6) способствует поддержанию структуры и функции костей, зубов, десен; оказывает влияние на эритропоэз, способствует нормальному функционированию нервной системы.
Цианокобаламин (витамин В12) участвует в эритропоэзе, способствует нормальному функционированию нервной системы.
Витамины группы В участвуют в образовании различных ферментов, которые регулируют обмен веществ в организме.
Аскорбиновая кислота (витамин С) участвует в окислении ряда биологически активных веществ, регуляции обмена в соединительной ткани, углеводного обмена, свертываемости крови и регенерации тканей, стимулирует образование стероидных гормонов, нормализует проницаемость капилляров. Витамин С повышает устойчивость организма к инфекциям, снижает воспалительные реакции.
Никотинамид (витамин РР) и D-пантенол (витамин В5) — коферменты, участвующие в метаболизме белка, синтезе жирных кислот и холестерина, продуцировании энергии и необходимы для нормального функционирования ЦНС.
Новости по теме
Показания
Применяют у детей в качестве профилактического средства при состояниях, сопровождающихся повышением потребности в витаминах: переутомление у детей школьного возраста; повышенная физическая и нервно-психическая нагрузка; при отсутствии аппетита и нерегулярном, неполноценном или однообразном рационе питания; в период выздоровления после перенесенных заболеваний, для повышения сопротивляемости организма к инфекционным и простудным заболеваниям. В составе комплексной терапии при применении химиотерапевтических средств.
Противопоказания
Гипервитаминоз А и D; повышенная чувствительность к компонентам препарата.
Дозировка
Внутрь. Режим дозирования индивидуальный, в зависимости от показаний и возраста пациента.
Побочные действия
Со стороны пищеварительной системы: диарея.
Со стороны нервной системы: головная боль.
Прочие: аллергические реакции, анафилактический шок.
Лекарственное взаимодействие
Витамин С усиливает действие и побочные эффекты противомикробных средств из группы сульфаниламидов (в т.ч. появление кристаллов в моче).
Нельзя принимать одновременно с препаратами тетрациклинового ряда и натрия фторидом, т.к. кальций снижает абсорбцию этих препаратов. При необходимости применения данной комбинации с антибиотиками тетрациклинового ряда и натрия фторидом, интервал между приемами этих препаратов должен составлять не менее 3 ч.
Пиридоксин угнетает активность леводопы.
Особые указания
На фоне применения возможно окрашивание мочи в желтый цвет, что не имеет клинического значения и объясняется наличием в препарате рибофлавина.
Не рекомендуется принимать совместно с другими препаратами, содержащими витамины.
Описание препарата ПИКОВИТ основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
ПИКОВИТ таблетки — инструкция по применению, цена, дозировки, аналоги, противопоказания
Действующие вещества
— рибофлавин (вит. B2) (riboflavin)— пиридоксина гидрохлорид (вит. B6) (pyridoxine)
— цианокобаламин (вит. B12) (cyanocobalamin)
— аскорбиновая кислота (вит. С) (ascorbic acid)
— ретинола пальмитат (вит. А) (retinol)
— кальция пантотенат (вит. B5) (calcium pantothenate)
— никотинамид (вит. PP) (nicotinamide)
— колекальциферол (вит.
 D3) (colecalciferol)
D3) (colecalciferol)— тиамина мононитрат (вит. B1) (thiamine)
— кальций (Ca2+)
— фосфор (P5+)
— фолиевая кислота (вит. Bc) (folic acid)
Состав и форма выпуска препарата
◊ Таблетки, покрытые оболочкой интенсивно розового, желтого, зеленого и оранжевого цвета, круглые, двояковыпуклые; допускаются вкрапления.
| 1 таб. | |
| ретинола пальмитат (вит. А) | 600 МЕ |
| колекальциферол (вит. D3) | 80 МЕ |
| аскорбиновая кислота (вит. С) | 10 мг |
| тиамина мононитрат (вит. B1) | 250 мкг |
| рибофлавин (вит. B2) | 300 мкг |
| кальция пантотенат (вит. B5) | 1.2 мг |
| пиридоксина гидрохлорид (вит. B6) | 300 мкг |
| фолиевая кислота (вит. Bc) | 40 мкг |
цианокобаламин (вит. B12) B12) | 0.2 мкг |
| никотинамид (вит. PP) | 3 мг |
| кальций (Ca2+) | 12.5 мг |
| фосфор (P5+) | 10 мг |
Вспомогательные вещества: лактозы моногидрат, ароматизатор апельсиновое масло 05073, полисорбат 80 (твин 80), глицерол, масло касторовое неощищенное, лимонная кислота безводная, сорбитол, декстроза жидкая (сухое вещество), магния стеарат, воск эмульсионный, масло вазелиновое, повидон, пеногаситель 1510, сахароза.
1 таблетка розового цвета дополнительно содержит: краситель пунцовый Понсо 4 R (Е124), титана диоксид (Е171).
1 таблетка желтого цвета дополнительно содержит: краситель солнечный закат желтый 06080 (Е110), краситель хинолиновый желтый (Е104), титана диоксид (Е171).
1 таблетка оранжевого цвета дополнительно содержит: краситель солнечный закат желтый 06080 (Е110), титана диоксид (Е171).
1 таблетка зеленого цвета дополнительно содержит: краситель индигокармин (Е132), краситель хинолиновый желтый (Е104), титана диоксид (Е171).
15 шт. — блистеры (2) — пачки картонные.
15 шт. — блистеры (4) — пачки картонные.
Фармакологическое действие
Комбинированное лекарственное средство, содержащее комплекс витаминов и минералов, являющихся важными факторами метаболических процессов.
Ретинол (витамин А) участвует в синтезе различных веществ (белков, липидов, мукополисахаридов) и обеспечивает нормальную функцию кожи, слизистых оболочек, а также органа зрения.
Колекальциферол (витамин D3) поддерживает баланс кальция и фосфора в организме.
Тиамин (витамин В1) нормализует деятельность сердца, способствует нормальному функционированию нервной системы.
Рибофлавин (витамин В2) способствует процессам регенерации тканей, в т.ч. клеток кожи.
Пиридоксин (витамин В6) способствует поддержанию структуры и функции костей, зубов, десен; оказывает влияние на эритропоэз, способствует нормальному функционированию нервной системы.
Цианокобаламин (витамин В12) участвует в эритропоэзе, способствует нормальному функционированию нервной системы.
Витамины группы В участвуют в образовании различных ферментов, которые регулируют обмен веществ в организме.
Аскорбиновая кислота (витамин С) участвует в окислении ряда биологически активных веществ, регуляции обмена в соединительной ткани, углеводного обмена, свертываемости крови и регенерации тканей, стимулирует образование стероидных гормонов, нормализует проницаемость капилляров. Витамин С повышает устойчивость организма к инфекциям, снижает воспалительные реакции.
Фолиевая кислота (витамин Вс) стимулирует эритропоэз.
Кальций участвует в формировании костной ткани, свертывании крови, передаче нервных импульсов, сокращении скелетных и гладких мышц.
Фосфор, наряду с кальцием, участвует в формировании костей и зубов, а также участвует в процессах энергетического обмена.
Новости по теме
Показания
Профилактика дефицита витаминов и минералов: при неполноценном и несбалансированном питании; вследствие отсутствия аппетита; при переутомлении у детей школьного возраста.
Противопоказания
Гипервитаминоз А; гипервитаминоз D; повышенная чувствительность к компонентам препарата; детский возраст до 4 лет.
Дозировка
Внутрь. Режим дозирования индивидуальный, в зависимости от показаний, возраста пациента и клинической ситуации.
Побочные действия
Со стороны пищеварительной системы: диарея.
Со стороны нервной системы: головная боль.
Прочие: аллергические реакции, анафилактический шок.
Лекарственное взаимодействие
Наличие в препарате кальция обусловливает задержку всасывания в кишечнике антибиотиков из группы тетрациклинов, а также противомикробных средств — производных фторхинолонов. Следует соблюдать между приемами препаратов интервал не менее 2 ч.
Витамин С усиливает действие и побочные эффекты сульфаниламидов (в т.ч. кристаллурию).
При одновременном применении диуретиков из группы тиазидов увеличивается вероятность гиперкальциемии.
Особые указания
При применении возможное окрашивание мочи в желтый цвет совершенно безвредно и объясняется наличием в препарате рибофлавина.
Не рекомендуется принимать совместно с другими препаратами, содержащими витамины и минералы.
Высокие дозы глицерола могут вызвать головную боль, нарушения со стороны ЖКТ (диарея).
Применение в детском возрасте
Противопоказан детям до 4 лет.
Описание препарата ПИКОВИТ основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Витамин B6 (пиридоксин) — StatPearls
Непрерывное обучение
Пиридоксин — это витамин и лекарство, используемое для лечения дефицита витамина B6 и лечения тошноты и рвоты во время беременности. Он также используется при синдромах зависимости от витамина B6 и спорно используется при некоторых других расстройствах. В этом упражнении будут освещены показания, механизм действия, пути введения, побочные эффекты, мониторинг и противопоказания, связанные с использованием пиридоксина у пациентов с дефицитом витамина B6 и другими заболеваниями.
Он также используется при синдромах зависимости от витамина B6 и спорно используется при некоторых других расстройствах. В этом упражнении будут освещены показания, механизм действия, пути введения, побочные эффекты, мониторинг и противопоказания, связанные с использованием пиридоксина у пациентов с дефицитом витамина B6 и другими заболеваниями.
Целей:
Определите механизм действия витамина B6.
Опишите возможные побочные эффекты витамина B6.
Оцените важность витамина B6 в лечении нескольких заболеваний.
Подчеркните важность улучшения координации помощи между межпрофессиональной командой для улучшения оказания помощи пациентам, получающим пиридоксин.
Показания
Витамин B6 (пиридоксин) — это водорастворимое вещество, которое внутри организма превращается в необходимые коферменты более чем 100 ферментов в организме человека.
Витамин B6 имеет три естественные формы: пиридоксин (PN), пиридоксаль (PL) и пиридоксамин (PM), все из которых превращаются в своих активных формах в организме, которые представляют собой кофермент пиридоксаль-5-фосфат (PLP или P5P). . [1] [2]
PLP, функциональная структура в организме, в основном служит коферментом в метаболизме аминокислот, белков, углеводов и липидов, помимо синтеза нейромедиаторов.[1] Он также участвует в гликогенолизе и глюконеогенезе. [3] [4]
Есть только два одобренных FDA препарата, содержащих пиридоксин или его аналоги; первый представляет собой комбинацию нескольких витаминов, включая B6, показанных для профилактики авитаминоза у детей и взрослых пациентов, получающих парентеральное питание, а второй представляет собой комбинацию сукцината доксиламина и гидрохлорида пиридоксина (аналог витамина B6) в форме таблеток для перорального применения. для лечения тошноты и рвоты при беременности, не поддающейся консервативному лечению.[5] [6]
Витамин B6 показан в случаях его дефицита, который может быть вызван плохой функцией почек, аутоиммунными заболеваниями, повышенным потреблением алкоголя или изониазида, циклосерина, вальпроевой кислоты, фенитоина, карбамазепина, примидона, гидралазина, и теофиллиновая терапия. [7] [8] [9] [10] [11] [12] [13]] Недостаточное потребление витамина B6 — редкая причина его дефицита.
[7] [8] [9] [10] [11] [12] [13]] Недостаточное потребление витамина B6 — редкая причина его дефицита.
Дефицит витамина B6 клинически проявляется в виде себорейного дерматита, микроцитарной анемии, кариеса, глоссита, эпилептиформных судорог, периферической невропатии, электроэнцефалографических аномалий, депрессии, спутанности сознания и ослабления иммунной функции.[7] [14] [15] [16] [17]
Некоторые редкие врожденные ошибки метаболизма являются результатом дефектов в сайтах связывания кофермента ответственных ферментов, где прикрепляется PLP, и введение очень высоких доз витамина B6 имеет решающее значение. для функционирования этих ферментов. Эти расстройства называются синдромами зависимости от витамина B6. Примерами этих синдромов являются судороги новорожденного, ксантуреновая ацидурия, цистатионинурия, первичная гипероксалурия, гомоцистинурия, сидеробластная анемия и спиральная атрофия с орнитинурией.[18]
Кроме того, некоторые токсикологические применения пиридоксина включают передозировку изониазида, отравление грибами ложных сморчков (гиромитра), воздействие гидразина, токсичность этиленгликоля и токсичность кримидина. [13]
[13]
Существуют некоторые доказательства эффективности витамина B6 в подавлении лактации и облегчении побочных эффектов пероральных контрацептивов, таких как депрессия и тошнота. [19]
Исследования показали противоречивые результаты относительно использования добавок витамина B6 для лечения гестационного диабета, предменструального синдрома, синдрома запястного канала, утреннего недомогания, а также лечения и профилактики гипертонической болезни.[19]
Несмотря на то, что существуют скудные доказательства эффективности пиридоксина в отношении этих применений, он использовался эмпирически для лечения некоторых состояний, включая атопический дерматит, кариес зубов, острую алкогольную интоксикацию, аутизм, диабетические осложнения, синдром Дауна, шизофрению, хорею Хантингтона. , и стероид-зависимая астма. [14] [16] [7] [20] [7] [19]
Исследования показывают снижение риска колоректального рака при увеличении потребления B6 людьми. [21] Некоторые исследования показали, что высокие уровни B6 препятствуют размножению опухолевых клеток печени in vitro у крыс.[22]
Механизм действия
PLP катализирует различные реакции, такие как трансаминирование, декарбоксилирование, рацемизация и отщепление, как в связанной с ферментом, так и в свободной форме. Эти реакции значительно облегчаются и ускоряются в присутствии PLP из-за электроноакцепторной природы молекулы, которая нестабилизирует связи вокруг альфа-углеродного атома через систему, образованную аминокислотами. [23]
Метаболизм витамина B6
Пиридоксин, пиридоксамин и пиридоксаль быстро всасываются из пищи и пероральных препаратов клетками слизистой оболочки тонкого кишечника, в то время как их фосфорилированные аналоги сначала подвергаются дефосфорилированию, а затем абсорбируются.[24]
Аналоги витамина B6 всасываются в кишечнике путем пассивной диффузии, что означает, что значительное количество соединения легко абсорбируется без насыщения клеток. [25] [26]
После поглощения PM и PN воздействуют на пиридоксалкиназу с образованием PMP и PNP соответственно; затем эти соединения превращаются ферментом оксидазой пиридоксин (пиридоксамин) фосфат (PNP) в кофермент PLP. Этот процесс происходит только в гепатоцитах и, в меньшей степени, в клетках слизистой оболочки тонкого кишечника из-за недостатка PNP-оксидазы в большинстве тканей.Поскольку клеточные мембраны непроницаемы для PLP, он либо дефосфорилируется ферментом фосфогидролазой, так что PL может высвобождаться в кровоток, либо напрямую присоединяется к альбумину и высвобождается гепатоцитами в кровоток в виде комплекса PLP-альбумин [25] [27]. ] PLP также захватывается эритроцитами и переносится гемоглобином в другие ткани. [28]
Наконец, связанный с белком PLP дефосфорилируется, и PLP конечного продукта в сочетании со свободной PL в плазме затем трансформируется внутри тканей-мишеней под действием фермента пиридоксалкиназы в кофермент PLP, который является активной формой витамина. B6.PLP связывается с различными белками внутри тканей, чтобы защитить его от ферментов фосфатазы. [29]
Введение
Витамин B6 может вводиться как перорально, так и внутривенно. Пероральная форма витамина B6 является наиболее распространенной доступной формой, тогда как внутривенная форма полезна в некоторых особых случаях, таких как синдромы мальабсорбции, анорексия и у пациентов, находящихся на парентеральном питании. Он также присутствует во внутримышечной и подкожной формах.
Побочные эффекты
Наиболее известным побочным эффектом от приема витамина B6 является сенсорная нейропатия, но эта патология редко возникает при дозах ниже токсичных, которые для взрослых составляют 1 г / день или более, и нет никаких доказательств ее возникновения в более низких дозах. чем 100 мг / день менее 30 недель у взрослых.[20] Стоит отметить, что средняя диетическая потребность взрослых в витамине B6 составляет 1,75 мг / день. [18]
Не сообщалось о побочных эффектах, вызванных диетическими концентрациями или регулярными дополнительными дозами витамина B6, в то время как более высокие дозы ниже уровня токсичности могут вызвать расстройство желудка, тошноту, болезненность груди, светочувствительность и везикулярные дерматозы. [20]
Противопоказания
Единственными двумя противопоказаниями для приема витамина B6 являются гипервитаминоз B6, поскольку токсические уровни могут вызывать сенсорную невропатию и гиперчувствительность к пиридоксину.
Мониторинг
Терапевтический индекс B6 варьируется между людьми, поскольку отмечается индивидуальная восприимчивость к токсическим побочным эффектам, но в некоторых исследованиях указывается пороговое значение 100 граммов в течение 20 месяцев, ниже которого не возникает нейропатии, связанной с токсичностью [30]. ] [20]
Витамин B6 хорошо усваивается из пищи и лекарств, и его высокая концентрация может быть быстро достигнута; однако человеческий организм выводит избыток с мочой в виде 4-пиридоксической кислоты, и она также выводится в неизменном виде при приеме очень высоких доз.[31] Контроль количества витамина B6 в организме осуществляется по трем причинам; для подтверждения истощения, токсичности и в исследованиях, связанных с витамином B6.
Мониторинг витамина B6 делится на прямые и функциональные методы. Прямые методы — это измерение концентрации витамина в плазме, клетках крови или моче. Концентрация PLP в плазме — лучший метод мониторинга, поскольку она отражает запасы B6 во всем организме. [32]
Функциональные методы, такие как нагрузочный тест триптофана, уровни гомоцистеина в плазме и активность трансаминаз в крови, также используются для выявления дефицита B6.Тесты на стимуляцию аспартатаминотрансферазы эритроцитов и аланинаминотрансферазы позволяют оценить долгосрочный статус витамина B6, и их значения увеличиваются с истощением B6. [32]
Токсичность
Витамин B6 может быть токсичным, если его концентрация в организме слишком высока, вызывая сенсорную невропатию, механизм которой неизвестен. Дегенерация сенсорных волокон периферических нервов и их миелина, а также дорсальных столбов спинного мозга вызывает двустороннюю потерю периферической чувствительности или гиперестезию, сопровождающуюся болью в конечностях, атаксией и потерей равновесия.Состояние постепенно регрессирует после прекращения приема добавки до восстановления нормальной активности. [13] Более высокие дозы могут вызвать атрофию яичек и снижение подвижности сперматозоидов [33].
Исследования по данному вопросу показали, что продолжительность приема витамина прямо пропорциональна риску клинически очевидной токсичности по отношению к общей введенной дозе. [20]
Улучшение результатов команды здравоохранения
Адекватное питание необходимо для любой витаминной профилактики.Медицинские работники должны посоветовать пациентам употреблять в пищу продукты, богатые витамином B6, такие как нут, печень, птица и обогащенные готовые к употреблению злаки. Дефицит B6 обычно встречается редко из-за несоответствия питания.
Гинекологам, акушерам, неврологам, гематологам и дерматологам часто требуется диагностировать, лечить и сотрудничать с пациентами с дефицитом или избытком витамина B6. Клиническая картина, сопровождающая дефицит витамина B6, не является уникальной характеристикой дефицита B6, поэтому для выявления проблемы необходимы тщательный анализ и хорошие навыки наблюдения.Уязвимые группы населения, такие как пациенты с хроническими заболеваниями и некачественным питанием, должны выявляться и управляться соответствующим образом.
Клиническое использование витамина B6 при некоторых заболеваниях вызывает споры, поскольку нет определенных доказательств его использования в этих условиях. Но из-за относительной безопасности высоких доз водорастворимых витаминов строгий контроль за пациентами не требуется. Некоторые состояния требуют гораздо более высоких доз, чем обычно необходимо, например синдромы зависимости, и необходимо наблюдение за побочными эффектами.
Независимо от того, используется ли витамин B6 для лечения заболевания или просто в качестве пищевой добавки, все члены межпрофессиональной команды, включая клиницистов, практикующих среднего звена, медсестер, фармацевтов и диетологов / диетологов, должны работать как единое целое и иметь доступ к той же клинической информации, чтобы они могли внедрять вмешательства, которые оптимизируют результаты лечения пациентов и минимизируют нежелательные явления. [Уровень 5]
Ссылки
- 1.
- SNELL EE. Химическая структура относительно биологической активности витамина B6.Vitam Horm. 1958; 16: 77-125. [PubMed: 13625598]
- 2.
- RABINOWITZ JC, SNELL EE. Группа витаминов B6; микробиологическое и естественное происхождение пиридоксаминфосфата. J Biol Chem. 1947 Август; 169 (3): 643-50. [PubMed: 20259097]
- 3.
- SNELL EE. Резюме известных метаболических функций никотиновой кислоты, рибофлавина и витамина B6. Physiol Rev.1953, октябрь; 33 (4): 509-24. [PubMed: 13100067]
- 4.
- Эбади М. Регулирование и функция пиридоксальфосфата в ЦНС.Neurochem Int. 1981; 3 (3-4): 181-205. [PubMed: 1
- 63]
- 5.
- Wibowo N, Purwosunu Y, Sekizawa A, Farina A, Tambunan V, Bardosono S. Добавление витамина B₆ беременным женщинам с тошнотой и рвотой. Int J Gynaecol Obstet. 2012 Март; 116 (3): 206-10. [PubMed: 22189065]
- 6.
- Мэтьюз А., Хаас Д.П., О’Матуна Д.П., Доусвелл Т., Дойл М. Вмешательства при тошноте и рвоте на ранних сроках беременности. Кокрановская база данных Syst Rev.2014, 21 марта; (3): CD007575. [PubMed: 24659261]
- 7.
- Vech RL, Lumeng L, Li TK. Метаболизм витамина B6 при хроническом злоупотреблении алкоголем Влияние окисления этанола на метаболизм пиридоксаль-5′-фосфата в печени. J Clin Invest. 1975 Май; 55 (5): 1026-32. [Бесплатная статья PMC: PMC301849] [PubMed: 1168205]
- 8.
- Snider DE. Добавки пиридоксина во время терапии изониазидом. Бугорок. 1980 декабрь; 61 (4): 191-6. [PubMed: 6269259]
- 9.
- Раскин Н.Х., Фишман Р.А. Пиридоксин-дефицитная нейропатия, вызванная гидралазином. N Engl J Med.1965 25 ноября; 273 (22): 1182-5. [PubMed: 5847557]
- 10.
- Наир С., Магуайр В., Барон Х., Имбрус Р. Влияние циклосерина на пиридоксин-зависимый метаболизм при туберкулезе. J Clin Pharmacol. 1976 август-сентябрь; 16 (8-9): 439-43. [PubMed: 972198]
- 11.
- Clayton PT. B6-ответные расстройства: модель витаминной зависимости. J Inherit Metab Dis. 2006 апрель-июнь; 29 (2-3): 317-26. [PubMed: 16763894]
- 12.
- Апеланд Т., Фрейланд ЭС, Кристенсен О., Странджорд Р. Э., Мансур Массачусетс.Лекарственное нарушение окислительно-восстановительного статуса аминотиола у пациентов с эпилепсией: улучшение за счет витаминов группы B. Epilepsy Res. 2008 ноя; 82 (1): 1-6. [PubMed: 18644700]
- 13.
- Lheureux P, Penaloza A, Gris M. Пиридоксин в клинической токсикологии: обзор. Eur J Emerg Med. 2005 Апрель; 12 (2): 78-85. [PubMed: 15756083]
- 14.
- MUELLER JF, VILTER RW. Дефицит пиридоксина у людей вызван дезоксипиридоксином. J Clin Invest. 1950 Февраль; 29 (2): 193-201. [Бесплатная статья PMC: PMC439740] [PubMed: 15403983]
- 15.
- Хокинс В.В., Барски Дж. Эксперимент по лишению человека витамина B6. Наука. 1948 10 сентября; 108 (2802): 284-6. [PubMed: 17842719]
- 16.
- Salam RA, Zuberi NF, Bhutta ZA. Добавки пиридоксина (витамина B6) во время беременности или родов для исходов у матери и новорожденного. Кокрановская база данных Syst Rev.2015, 3 июня; (6): CD000179. [PubMed: 26039815]
- 17.
- Рииконен Р., Манкинен К., Гейли Э. Долгосрочный исход пиридоксин-зависимой детской эпилепсии.Eur J Paediatr Neurol. 2015 ноя; 19 (6): 647-51. [PubMed: 26310861]
- 18.
- Frimpter GW, Andelman RJ, George WF. Синдромы зависимости от витамина В6. Новые горизонты в питании. Am J Clin Nutr. 1969 июн; 22 (6): 794-805. [PubMed: 48]
- 19.
- Бендер Д.А. Использование витамина B6 в непищевых целях. Br J Nutr. 1999 Янв; 81 (1): 7-20. [PubMed: 10341670]
- 20.
- Бендич А., Коэн М. Проблемы безопасности витамина B6. Ann N Y Acad Sci. 1990; 585: 321-30. [PubMed: 21]
- 21.
- Larsson SC, Orsini N, Wolk A. Витамин B6 и риск колоректального рака: метаанализ проспективных исследований. ДЖАМА. 17 марта 2010 г .; 303 (11): 1077-83. [PubMed: 20233826]
- 22.
- Tryfiates GP. Влияние пиридоксина на экспрессию сывороточного белка у крыс с гепатомой. J Natl Cancer Inst. 1981 Февраль; 66 (2): 339-44. [PubMed: 62]
- 23.
- Хаяси Х, Вада Х, Йошимура Т., Эсаки Н., Сода К. Последние темы в исследованиях пиридоксаль-5′-фосфатного фермента. Анну Рев Биохим.1990; 59: 87-110. [PubMed: 2197992]
- 24.
- Hamm MW, Mehansho H, Henderson LM. Транспорт и метаболизм пиридоксамина и пиридоксаминфосфата в тонком кишечнике крысы. J Nutr. 1979 сентябрь; 109 (9): 1552-9. [PubMed: 479950]
- 25.
- Бусс Д.Д., Хамм М.В., Механшо Х., Хендерсон Л.М. Транспорт и метаболизм пиридоксина в перфузируемой тонкой кишке и задних конечностях крысы. J Nutr. 1980 августа; 110 (8): 1655-63. [PubMed: 7400856]
- 26.
- Цудзи Т., Ямада Р., Нос Ю.Всасывание витамина B6 в кишечнике. I. Поглощение пиридоксола тканью кишечника крыс. J Nutr Sci Vitaminol (Токио). 1973 Октябрь; 19 (5): 401-17. [PubMed: 47
] 2]- 27.
- Механшо Х., Бусс Д.Д., Хамм М.В., Хендерсон Л.М. Транспорт и метаболизм пиридоксина в печени крыс. Biochim Biophys Acta. 1980, 1 августа; 631 (1): 112-23. [PubMed: 7397240]
- 28.
- Mehansho H, Henderson LM. Транспорт и накопление пиридоксина и пиридоксаля эритроцитами. J Biol Chem. 1980 25 декабря; 255 (24): 11901-7.[PubMed: 7440576]
- 29.
- Li TK, Lumeng L, Veitch RL. Регуляция метаболизма пиридоксаль-5′-фосфата в печени. Biochem Biophys Res Commun. 1974, 27 ноября; 61 (2): 677-84. [PubMed: 4375996]
- 30.
- Сенсорная невропатия от злоупотребления пиридоксином. N Engl J Med. 19 января 1984; 310 (3): 197-8. [PubMed: 6318110]
- 31.
- Ink SL, Henderson LM. Метаболизм витамина B6. Анну Рев Нутр. 1984; 4: 455-70. [PubMed: 6380540]
- 32.
- Ueland PM, Ulvik A, Rios-Avila L, Midttun Ø, Gregory JF.Прямые и функциональные биомаркеры статуса витамина B6. Анну Рев Нутр. 2015; 35: 33-70. [Бесплатная статья PMC: PMC5988249] [PubMed: 25974692]
- 33.
- Цуцуми С., Танака Т., Гото К., Акаике М. Влияние пиридоксина на мужскую фертильность. J Toxicol Sci. 1995 августа; 20 (3): 351-65. [PubMed: 8667459]
Витамин B6 (пиридоксин) — StatPearls
Непрерывное обучение
Пиридоксин — это витамин и лекарство, используемое для лечения дефицита витамина B6 и лечения тошноты и рвоты во время беременности.Он также используется при синдромах зависимости от витамина B6 и спорно используется при некоторых других расстройствах. В этом упражнении будут освещены показания, механизм действия, пути введения, побочные эффекты, мониторинг и противопоказания, связанные с использованием пиридоксина у пациентов с дефицитом витамина B6 и другими заболеваниями.
Целей:
Определите механизм действия витамина B6.
Опишите возможные побочные эффекты витамина B6.
Оцените важность витамина B6 в лечении нескольких заболеваний.
Подчеркните важность улучшения координации помощи между межпрофессиональной командой для улучшения оказания помощи пациентам, получающим пиридоксин.
Показания
Витамин B6 (пиридоксин) — это водорастворимое вещество, которое внутри организма превращается в необходимые коферменты более чем 100 ферментов в организме человека.
Витамин B6 имеет три естественные формы: пиридоксин (PN), пиридоксаль (PL) и пиридоксамин (PM), все из которых превращаются в своих активных формах в организме, которые представляют собой кофермент пиридоксаль-5-фосфат (PLP или P5P). . [1] [2]
PLP, функциональная структура в организме, в основном служит коферментом в метаболизме аминокислот, белков, углеводов и липидов, в дополнение к синтезу нейротрансмиттеров. [1] Он также участвует в гликогенолизе и глюконеогенезе. [3] [4]
Есть только два одобренных FDA препарата, содержащих пиридоксин или его аналоги; первый представляет собой комбинацию нескольких витаминов, включая B6, показанных для профилактики авитаминоза у детей и взрослых пациентов, получающих парентеральное питание, а второй представляет собой комбинацию сукцината доксиламина и гидрохлорида пиридоксина (аналог витамина B6) в форме таблеток для перорального применения. для лечения тошноты и рвоты при беременности, не поддающейся консервативному лечению.[5] [6]
Витамин B6 показан в случаях его дефицита, который может быть вызван плохой функцией почек, аутоиммунными заболеваниями, повышенным потреблением алкоголя или изониазида, циклосерина, вальпроевой кислоты, фенитоина, карбамазепина, примидона, гидралазина, и теофиллиновая терапия. [7] [8] [9] [10] [11] [12] [13]] Недостаточное потребление витамина B6 — редкая причина его дефицита.
Дефицит витамина B6 клинически проявляется в виде себорейного дерматита, микроцитарной анемии, кариеса, глоссита, эпилептиформных судорог, периферической невропатии, электроэнцефалографических аномалий, депрессии, спутанности сознания и ослабления иммунной функции.[7] [14] [15] [16] [17]
Некоторые редкие врожденные ошибки метаболизма являются результатом дефектов в сайтах связывания кофермента ответственных ферментов, где прикрепляется PLP, и введение очень высоких доз витамина B6 имеет решающее значение. для функционирования этих ферментов. Эти расстройства называются синдромами зависимости от витамина B6. Примерами этих синдромов являются судороги новорожденного, ксантуреновая ацидурия, цистатионинурия, первичная гипероксалурия, гомоцистинурия, сидеробластная анемия и спиральная атрофия с орнитинурией.[18]
Кроме того, некоторые токсикологические применения пиридоксина включают передозировку изониазида, отравление грибами ложных сморчков (гиромитра), воздействие гидразина, токсичность этиленгликоля и токсичность кримидина. [13]
Существуют некоторые доказательства эффективности витамина B6 в подавлении лактации и облегчении побочных эффектов пероральных контрацептивов, таких как депрессия и тошнота. [19]
Исследования показали противоречивые результаты относительно использования добавок витамина B6 для лечения гестационного диабета, предменструального синдрома, синдрома запястного канала, утреннего недомогания, а также лечения и профилактики гипертонической болезни.[19]
Несмотря на то, что существуют скудные доказательства эффективности пиридоксина в отношении этих применений, он использовался эмпирически для лечения некоторых состояний, включая атопический дерматит, кариес зубов, острую алкогольную интоксикацию, аутизм, диабетические осложнения, синдром Дауна, шизофрению, хорею Хантингтона. , и стероид-зависимая астма. [14] [16] [7] [20] [7] [19]
Исследования показывают снижение риска колоректального рака при увеличении потребления B6 людьми. [21] Некоторые исследования показали, что высокие уровни B6 препятствуют размножению опухолевых клеток печени in vitro у крыс.[22]
Механизм действия
PLP катализирует различные реакции, такие как трансаминирование, декарбоксилирование, рацемизация и отщепление, как в связанной с ферментом, так и в свободной форме. Эти реакции значительно облегчаются и ускоряются в присутствии PLP из-за электроноакцепторной природы молекулы, которая нестабилизирует связи вокруг альфа-углеродного атома через систему, образованную аминокислотами. [23]
Метаболизм витамина B6
Пиридоксин, пиридоксамин и пиридоксаль быстро всасываются из пищи и пероральных препаратов клетками слизистой оболочки тонкого кишечника, в то время как их фосфорилированные аналоги сначала подвергаются дефосфорилированию, а затем абсорбируются.[24]
Аналоги витамина B6 всасываются в кишечнике путем пассивной диффузии, что означает, что значительное количество соединения легко абсорбируется без насыщения клеток. [25] [26]
После поглощения PM и PN воздействуют на пиридоксалкиназу с образованием PMP и PNP соответственно; затем эти соединения превращаются ферментом оксидазой пиридоксин (пиридоксамин) фосфат (PNP) в кофермент PLP. Этот процесс происходит только в гепатоцитах и, в меньшей степени, в клетках слизистой оболочки тонкого кишечника из-за недостатка PNP-оксидазы в большинстве тканей.Поскольку клеточные мембраны непроницаемы для PLP, он либо дефосфорилируется ферментом фосфогидролазой, так что PL может высвобождаться в кровоток, либо напрямую присоединяется к альбумину и высвобождается гепатоцитами в кровоток в виде комплекса PLP-альбумин [25] [27]. ] PLP также захватывается эритроцитами и переносится гемоглобином в другие ткани. [28]
Наконец, связанный с белком PLP дефосфорилируется, и PLP конечного продукта в сочетании со свободной PL в плазме затем трансформируется внутри тканей-мишеней под действием фермента пиридоксалкиназы в кофермент PLP, который является активной формой витамина. B6.PLP связывается с различными белками внутри тканей, чтобы защитить его от ферментов фосфатазы. [29]
Введение
Витамин B6 может вводиться как перорально, так и внутривенно. Пероральная форма витамина B6 является наиболее распространенной доступной формой, тогда как внутривенная форма полезна в некоторых особых случаях, таких как синдромы мальабсорбции, анорексия и у пациентов, находящихся на парентеральном питании. Он также присутствует во внутримышечной и подкожной формах.
Побочные эффекты
Наиболее известным побочным эффектом от приема витамина B6 является сенсорная нейропатия, но эта патология редко возникает при дозах ниже токсичных, которые для взрослых составляют 1 г / день или более, и нет никаких доказательств ее возникновения при более низких дозах. чем 100 мг / день в течение менее 30 недель у взрослых.[20] Стоит отметить, что средняя диетическая потребность взрослых в витамине B6 составляет 1,75 мг / день. [18]
Не сообщалось о побочных эффектах, вызванных диетическими концентрациями или регулярными дополнительными дозами витамина B6, в то время как более высокие дозы ниже уровня токсичности могут вызвать расстройство желудка, тошноту, болезненность груди, светочувствительность и везикулярные дерматозы. [20]
Противопоказания
Единственными двумя противопоказаниями для приема витамина B6 являются гипервитаминоз B6, поскольку токсические уровни могут вызывать сенсорную невропатию и гиперчувствительность к пиридоксину.
Мониторинг
Терапевтический индекс B6 варьируется между людьми, поскольку отмечается индивидуальная восприимчивость к токсическим побочным эффектам, но в некоторых исследованиях указывается пороговое значение 100 граммов в течение 20 месяцев, ниже которого невропатия, связанная с токсичностью, не возникает [30]. ] [20]
Витамин B6 хорошо усваивается из пищи и лекарств, и его высокая концентрация может быть быстро достигнута; однако человеческий организм выводит избыток с мочой в виде 4-пиридоксической кислоты, и она также выводится в неизменном виде при приеме очень высоких доз.[31] Контроль количества витамина B6 в организме осуществляется по трем причинам; для подтверждения истощения, токсичности и в исследованиях, связанных с витамином B6.
Мониторинг витамина B6 делится на прямые и функциональные методы. Прямые методы — это измерение концентрации витамина в плазме, клетках крови или моче. Концентрация PLP в плазме — лучший метод мониторинга, поскольку она отражает запасы B6 во всем организме. [32]
Функциональные методы, такие как нагрузочный тест триптофана, уровни гомоцистеина в плазме и активность трансаминаз в крови, также используются для выявления дефицита B6.Тесты на стимуляцию аспартатаминотрансферазы эритроцитов и аланинаминотрансферазы позволяют оценить долгосрочный статус витамина B6, и их значения увеличиваются с истощением B6. [32]
Токсичность
Витамин B6 может быть токсичным, если его концентрация в организме слишком высока, вызывая сенсорную невропатию, механизм которой неизвестен. Дегенерация сенсорных волокон периферических нервов и их миелина, а также дорсальных столбов спинного мозга вызывает двустороннюю потерю периферической чувствительности или гиперестезию, сопровождающуюся болью в конечностях, атаксией и потерей равновесия.Состояние постепенно регрессирует после прекращения приема добавки до восстановления нормальной активности. [13] Более высокие дозы могут вызвать атрофию яичек и снижение подвижности сперматозоидов [33].
Исследования по данному вопросу показали, что продолжительность приема витамина прямо пропорциональна риску клинически очевидной токсичности по отношению к общей введенной дозе. [20]
Улучшение результатов команды здравоохранения
Адекватное питание необходимо для любой витаминной профилактики.Медицинские работники должны посоветовать пациентам употреблять в пищу продукты, богатые витамином B6, такие как нут, печень, птица и обогащенные готовые к употреблению злаки. Дефицит B6 обычно встречается редко из-за несоответствия питания.
Гинекологам, акушерам, неврологам, гематологам и дерматологам часто требуется диагностировать, лечить и сотрудничать с пациентами с дефицитом или избытком витамина B6. Клиническая картина, сопровождающая дефицит витамина B6, не является уникальной характеристикой дефицита B6, поэтому для выявления проблемы необходимы тщательный анализ и хорошие навыки наблюдения.Уязвимые группы населения, такие как пациенты с хроническими заболеваниями и некачественным питанием, должны выявляться и управляться соответствующим образом.
Клиническое использование витамина B6 при некоторых заболеваниях вызывает споры, поскольку нет определенных доказательств его использования в этих условиях. Но из-за относительной безопасности высоких доз водорастворимых витаминов строгий контроль за пациентами не требуется. Некоторые состояния требуют гораздо более высоких доз, чем обычно необходимо, например синдромы зависимости, и необходимо наблюдение за побочными эффектами.
Независимо от того, используется ли витамин B6 для лечения заболевания или просто в качестве пищевой добавки, все члены межпрофессиональной команды, включая клиницистов, практикующих среднего звена, медсестер, фармацевтов и диетологов / диетологов, должны работать как единое целое и иметь доступ к той же клинической информации, чтобы они могли внедрять вмешательства, которые оптимизируют результаты лечения пациентов и минимизируют нежелательные явления. [Уровень 5]
Ссылки
- 1.
- SNELL EE. Химическая структура относительно биологической активности витамина B6.Vitam Horm. 1958; 16: 77-125. [PubMed: 13625598]
- 2.
- RABINOWITZ JC, SNELL EE. Группа витаминов B6; микробиологическое и естественное происхождение пиридоксаминфосфата. J Biol Chem. 1947 Август; 169 (3): 643-50. [PubMed: 20259097]
- 3.
- SNELL EE. Резюме известных метаболических функций никотиновой кислоты, рибофлавина и витамина B6. Physiol Rev.1953, октябрь; 33 (4): 509-24. [PubMed: 13100067]
- 4.
- Эбади М. Регулирование и функция пиридоксальфосфата в ЦНС.Neurochem Int. 1981; 3 (3-4): 181-205. [PubMed: 1
- 63]
- 5.
- Wibowo N, Purwosunu Y, Sekizawa A, Farina A, Tambunan V, Bardosono S. Добавление витамина B₆ беременным женщинам с тошнотой и рвотой. Int J Gynaecol Obstet. 2012 Март; 116 (3): 206-10. [PubMed: 22189065]
- 6.
- Мэтьюз А., Хаас Д.П., О’Матуна Д.П., Доусвелл Т., Дойл М. Вмешательства при тошноте и рвоте на ранних сроках беременности. Кокрановская база данных Syst Rev.2014, 21 марта; (3): CD007575. [PubMed: 24659261]
- 7.
- Vech RL, Lumeng L, Li TK. Метаболизм витамина B6 при хроническом злоупотреблении алкоголем Влияние окисления этанола на метаболизм пиридоксаль-5′-фосфата в печени. J Clin Invest. 1975 Май; 55 (5): 1026-32. [Бесплатная статья PMC: PMC301849] [PubMed: 1168205]
- 8.
- Snider DE. Добавки пиридоксина во время терапии изониазидом. Бугорок. 1980 декабрь; 61 (4): 191-6. [PubMed: 6269259]
- 9.
- Раскин Н.Х., Фишман Р.А. Пиридоксин-дефицитная нейропатия, вызванная гидралазином. N Engl J Med.1965 25 ноября; 273 (22): 1182-5. [PubMed: 5847557]
- 10.
- Наир С., Магуайр В., Барон Х., Имбрус Р. Влияние циклосерина на пиридоксин-зависимый метаболизм при туберкулезе. J Clin Pharmacol. 1976 август-сентябрь; 16 (8-9): 439-43. [PubMed: 972198]
- 11.
- Clayton PT. B6-ответные расстройства: модель витаминной зависимости. J Inherit Metab Dis. 2006 апрель-июнь; 29 (2-3): 317-26. [PubMed: 16763894]
- 12.
- Апеланд Т., Фрейланд ЭС, Кристенсен О., Странджорд Р. Э., Мансур Массачусетс.Лекарственное нарушение окислительно-восстановительного статуса аминотиола у пациентов с эпилепсией: улучшение за счет витаминов группы В. Epilepsy Res. 2008 ноя; 82 (1): 1-6. [PubMed: 18644700]
- 13.
- Lheureux P, Penaloza A, Gris M. Пиридоксин в клинической токсикологии: обзор. Eur J Emerg Med. 2005 Апрель; 12 (2): 78-85. [PubMed: 15756083]
- 14.
- MUELLER JF, VILTER RW. Дефицит пиридоксина у людей вызван дезоксипиридоксином. J Clin Invest. 1950 Февраль; 29 (2): 193-201. [Бесплатная статья PMC: PMC439740] [PubMed: 15403983]
- 15.
- Хокинс В.В., Барски Дж. Эксперимент по лишению человека витамина B6. Наука. 1948 10 сентября; 108 (2802): 284-6. [PubMed: 17842719]
- 16.
- Salam RA, Zuberi NF, Bhutta ZA. Пиридоксин (витамин B6) во время беременности или родов для исходов у матери и новорожденного. Кокрановская база данных Syst Rev.2015, 3 июня; (6): CD000179. [PubMed: 26039815]
- 17.
- Рииконен Р., Манкинен К., Гейли Э. Долгосрочный исход пиридоксин-зависимой детской эпилепсии.Eur J Paediatr Neurol. 2015 ноя; 19 (6): 647-51. [PubMed: 26310861]
- 18.
- Frimpter GW, Andelman RJ, George WF. Синдромы зависимости от витамина B6. Новые горизонты в питании. Am J Clin Nutr. 1969 июн; 22 (6): 794-805. [PubMed: 48]
- 19.
- Бендер Д.А. Использование витамина B6 в непищевых целях. Br J Nutr. 1999 Янв; 81 (1): 7-20. [PubMed: 10341670]
- 20.
- Бендич А., Коэн М. Проблемы безопасности витамина B6. Ann N Y Acad Sci. 1990; 585: 321-30. [PubMed: 21]
- 21.
- Larsson SC, Orsini N, Wolk A. Витамин B6 и риск колоректального рака: метаанализ проспективных исследований. ДЖАМА. 17 марта 2010 г .; 303 (11): 1077-83. [PubMed: 20233826]
- 22.
- Tryfiates GP. Влияние пиридоксина на экспрессию сывороточного белка у крыс с гепатомой. J Natl Cancer Inst. 1981 Февраль; 66 (2): 339-44. [PubMed: 6
- 23.
- Хаяши Х, Вада Х, Йошимура Т., Эсаки Н., Сода К. Последние темы в исследованиях пиридоксаль-5′-фосфатного фермента. Анну Рев Биохим.1990; 59: 87-110. [PubMed: 2197992]
- 24.
- Hamm MW, Mehansho H, Henderson LM. Транспорт и метаболизм пиридоксамина и пиридоксаминфосфата в тонком кишечнике крысы. J Nutr. 1979 сентябрь; 109 (9): 1552-9. [PubMed: 479950]
- 25.
- Бусс Д.Д., Хамм М.В., Механшо Х., Хендерсон Л.М. Транспорт и метаболизм пиридоксина в перфузируемой тонкой кишке и задних конечностях крысы. J Nutr. 1980 августа; 110 (8): 1655-63. [PubMed: 7400856]
- 26.
- Цудзи Т., Ямада Р., Нос Ю.Всасывание витамина B6 в кишечнике. I. Поглощение пиридоксола тканью кишечника крыс. J Nutr Sci Vitaminol (Токио). 1973 Октябрь; 19 (5): 401-17. [PubMed: 47
] - 27.
- Механшо Х., Бусс Д.Д., Хамм М.В., Хендерсон Л.М. Транспорт и метаболизм пиридоксина в печени крыс. Biochim Biophys Acta. 1980, 1 августа; 631 (1): 112-23. [PubMed: 7397240]
- 28.
- Mehansho H, Henderson LM. Транспорт и накопление пиридоксина и пиридоксаля эритроцитами. J Biol Chem. 1980 25 декабря; 255 (24): 11901-7.[PubMed: 7440576]
- 29.
- Li TK, Lumeng L, Veitch RL. Регуляция метаболизма пиридоксаль-5′-фосфата в печени. Biochem Biophys Res Commun. 1974, 27 ноября; 61 (2): 677-84. [PubMed: 4375996]
- 30.
- Сенсорная невропатия от злоупотребления пиридоксином. N Engl J Med. 19 января 1984; 310 (3): 197-8. [PubMed: 6318110]
- 31.
- Ink SL, Henderson LM. Метаболизм витамина B6. Анну Рев Нутр. 1984; 4: 455-70. [PubMed: 6380540]
- 32.
- Ueland PM, Ulvik A, Rios-Avila L, Midttun Ø, Gregory JF.Прямые и функциональные биомаркеры статуса витамина B6. Анну Рев Нутр. 2015; 35: 33-70. [Бесплатная статья PMC: PMC5988249] [PubMed: 25974692]
- 33.
- Цуцуми С., Танака Т., Гото К., Акаике М. Влияние пиридоксина на мужскую фертильность. J Toxicol Sci. 1995 августа; 20 (3): 351-65. [PubMed: 8667459]
Пиридоксин — обзор | ScienceDirect Topics
ДЕФИЦИТ ИЛИ ЗАВИСИМОСТЬ ПИРИДОКСИНА
Пиридоксин (витамин B 6 ) важен для церебрального метаболизма.Если младенцы получают диету с дефицитом пиридоксина, у небольшой части из них разовьются симптомы задержки роста, анемии и судорог. Эти симптомы исчезнут после приема нескольких миллиграммов пиридоксина в день. Если этот дефицит пиридоксина не исправить, церебральное повреждение становится необратимым, и у ребенка могут возникать повторяющиеся судороги, которые не реагируют на пиридоксин.
Пиридоксиновая зависимость, вероятно, связана с ферментативным дефектом, унаследованным как аутосомно-рецессивный признак.Симптомы начинаются с трудноизлечимых судорог в течение первой недели жизни, часто в первые часы, и иногда мать может наблюдать судороги плода. Клинически и электроэнцефалографически они реагируют в течение 10-15 минут на 100 мг пиридоксина, вводимого внутримышечно; они повторяются через несколько часов, а затем снова исчезают после следующей инъекции. Длительное лечение — пиридоксин перорально в дозе 10–200 мг в день, что как минимум в 10–100 раз превышает базовую суточную потребность пиридоксина.Согласно имеющимся данным, этот курс терапии должен продолжаться бесконечно. Если единственной терапией является симптоматическое противоэпилептическое лечение в острой ситуации, младенец может выжить с необратимым тяжелым повреждением головного мозга, тогда как младенцы, получавшие пиридоксин на ранней стадии, по-видимому, развиваются нормально. Лучший способ установить диагноз — понаблюдать за реакцией на пиридоксин.
Более расплывчатая группа состоит из детей с пиридоксин-зависимыми припадками. В эту группу входят дети всех возрастов с устойчивыми к терапии судорогами, часто с атаксией и ухудшением психического состояния, у которых эмпирически установлено, что они реагируют на пиридоксин в произвольно выбранной дозе 100–350 мг в день.Потребность в этих высоких дозах пиридоксина, по-видимому, сохраняется в течение переменного периода времени, от нескольких месяцев у одних пациентов до нескольких лет у других. Этот синдром, вероятно, не является однородным заболеванием, но может содержать несколько различных метаболических нарушений.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Антагонист витамина B-6 из льняного семени нарушает метаболизм аминокислот у самцов крыс с умеренным дефицитом витамина B-6 | Журнал питания
Аннотация
Предпосылки: Пиридоксаль-5′-фосфат (PLP) играет решающую роль в качестве кофактора в метаболизме аминокислот.Среди населения широко распространен умеренный дефицит витамина B-6, который может усугубляться из-за приема внутрь 1-амино D-пролина (1ADP), антагониста витамина B-6, обнаруженного в семенах льна.
Цель: Учитывая предварительные данные о влиянии синтетического 1АДФ на показатели метаболизма пиридоксина, настоящее исследование было разработано для изучения влияния 1АДФ, полученного из льняного семени, на метаболизм аминокислот у крыс с умеренным дефицитом витамина B-6.
Методы: Самцы крыс-отъемышей ( n = 8 / лечение) потребляли полуочищенный рацион, содержащий либо 7 мг гидрохлорида пиридоксина / кг рациона [оптимальный витамин B-6 (OB)], либо 0.7 мг гидрохлорида пиридоксина / кг диеты [умеренный дефицит витамина B-6 (MB)], каждый с 0 или 10 мг антагониста витамина B-6 / кг диеты, либо в синтетической форме (1ADP), либо в виде экстракта льняного семени (FE) , в течение 5 нед. В конце эксперимента были проанализированы концентрации витамина B-6 и аминокислот в плазме, а также активность печеночных PLP-зависимых ферментов.
Результаты: По сравнению с контрольной группой MB, концентрации PLP в плазме были на 26% и 69% ниже, соответственно, у крыс MB + FE и MB + 1ADP ( P ≤ 0.001). В группе MB + FE концентрация цистатионина в плазме была на 100% больше, а концентрации α-аминомасляной кислоты и глутаминовой кислоты в плазме были на 59% и 30% ниже, соответственно, чем в контрольной группе MB. Как синтетический 1ADP, так и FE значительно ( P <0,001) ингибировали in vitro печеночную активность 2 PLP-зависимых ферментов, цистатионин-β-синтазы (до 44%) и цистатионин-γ-лиазы (до 60%), независимо от концентрации витамина B-6. Из-за воздействия антагонистов витамина B-6 наблюдаемые нарушения биомаркеров плазмы и активности печеночных ферментов не были очевидными или имели меньшую степень у крыс, потребляющих достаточное количество витамина B-6.
Заключение: Текущие данные модели на крысах свидетельствуют о том, что антагонист витамина B-6, преобладающий в настоящее время в пищевых продуктах человека, может создавать проблемы для людей с умеренным статусом витамина B-6.
Введение
Витамин B-6 известен своей биологической ролью кофактора в бесчисленных метаболических реакциях из-за его способности связывать различные ферментативные реакции углерода и азота и его участия в биосинтезе биогенных аминов и одноуглеродных единиц (1, 2).Обычно пиридоксаль-5′-фосфат (PLP) 7 , активная форма витамина B-6, связывается с ε-аминогруппой активных остатков лизина, содержащихся в витамин B-6-зависимых ферментах, образуя таким образом основание Шиффа / внешний альдимин. Последний вид затем действует как общий центральный промежуточный продукт для всех реакций, катализируемых PLP, включая декарбоксилирование, рацемизацию, трансаминирование, β-элиминирование и альдольное расщепление, и, таким образом, служит для выполнения различных функций в метаболизме аминокислот, сахаров и липидов (2 , 3).В некоторых метаболических путях аминокислот, включая пути транс-сульфирования и реметилирования метаболизма метионина, витамин B-6 необходим в качестве кофактора (4–6). В пути транс-сульфирования PLP действует как кофермент для цистатионин-β-синтазы (CBS), который конденсирует гомоцистеин с серином с образованием цистатионина и цистатионин-γ-лиазы (CGL), которая превращает цистатионин в цистеин, высвобождая α-аминомасляную кислоту в виде побочный продукт. В пути реметилирования гомоцистеин снова превращается в метионин путем связывания нескольких ферментов, включая серингидроксиметилтрансферазу (SHMT).Этот PLP-зависимый фермент участвует в обратимой реакции по переносу группы -CH 2 — от серина к тетрагидрофолату с образованием 5,10-метилентетрагидрофолата, причем последний также образуется через систему расщепления глицина (4, 5, 7, 8).
Статус витамина B-6 в организме в основном определяется его диетическим питанием и может нарушаться приемом антагониста витамина B-6 (9). Некоторые препараты (изониазид, циклосерин, пеницилламин и местранол), а также природные вещества (гиромитрин, канаванин, агаритин, тиофиллин, кофеин и линатин) действуют как антагонисты витамина B-6 в организме, уменьшая свободный PLP и / или ингибируя активность ферментов пиридоксалькиназы (PLK) и пиридоксинфосфатоксидазы (PNPOx) (9–11).Линатин, встречающийся в природе дипептид глутаминовой кислоты и 1-амино D-пролина (1ADP), является антагонистом витамина B-6, присутствующим в льняном семени. Химически это 1 — [(n-γ-L-глутамил) амино] -D-пролин. После гидролиза соляной кислотой линатин высвобождает 1ADP, активную форму этого антагониста витамина B-6 (12). Предыдущие исследования документально подтвердили, что общее содержание антагонистов витамина B-6, выраженное в эквивалентах 1-амино-D-пролина (1АДФЭ; равно 1/2 линатина + 1АДФ), составляло 177–437 мкг / г цельного льняного семени в зависимости от сорта. выборка (12, 13).1ADP связывается с PLP с образованием комплексов гидразона, и эти комплексы могут уменьшать пул свободного PLP in vivo или вызывать токсичность гидразона в организме (12, 14). Ранее мы показали, что токсичность синтетического 1АДФ была гораздо более очевидной у животных, у которых был умеренный дефицит витамина B-6, по сравнению с животными, у которых был избыток. Пероральный прием синтетического 1АДФ в концентрации 10 мг / кг диеты вызвал серьезные нарушения метаболизма гомоцистеина у крыс с умеренным дефицитом витамина B-6 (15).
Потребление льняного семени растет из-за его предполагаемой пользы для здоровья, включая снижение факторов риска, связанных с диабетом, раком и сердечно-сосудистыми заболеваниями (16–18). Одновременный прием антинутриентов, включая антагонист витамина B-6 1ADP, присутствующий в льняном семени, населением в целом, особенно тем, у кого умеренный дефицит витамина B-6, может вызывать беспокойство. Поскольку явный дефицит витамина B-6 встречается редко и преобладает умеренный дефицит (19, 20), настоящее исследование было разработано для оценки влияния антагониста витамина B-6 из льняного семени на метаболизм аминокислот на модели грызунов с умеренным содержанием витамина B. -6 дефицит.
Методы
Приготовление экстракта льняного семени.
Льняное семя было приобретено на коммерческом рынке и обезжирено с использованием аппарата Сокслета с гексаном в качестве растворителя. Обезжиренное льняное семя повторно измельчали до получения тонкого порошка. Антагонист витамина B-6 из молотого обезжиренного льняного семени был экстрагирован с использованием метода ультразвуковой обработки, описанного ранее, с небольшими модификациями, включая использование 40% изопропанола при 25 ° C с соотношением растворителя к твердому веществу 10: 1. на 30 мин (13).Экстракт концентрировали при пониженном давлении и сушили вымораживанием. Затем его тонко измельчили и количество общего содержания антагониста витамина B-6 было определено количественно с использованием сверхвысокопроизводительной жидкостной хроматографии / масс-спектрометрии с синтетическим 1ADP (Santa Cruz Biotechnology) и собственным линатином в качестве стандартов ( 13). Экстракт льняного семени (FE), содержащий концентрированный антагонист витамина B-6, хранили при -20 ° C до использования.
Животные и диета.
Сорок восемь крыс-самцов Sprague-Dawley массой 112 ± 9 г были приобретены в Центре ухода за животными Университета Манитобы.Их по отдельности помещали в полипропиленовые клетки в комнате, в которой поддерживалась температура 20 ± 2 ° C с 12-часовым ритмом света / темноты при относительной влажности 50–70%. После акклиматизации в течение 1 недели крыс случайным образом разделили на 6 групп ( n = 8) и кормили полуочищенным рационом (AIN-93G, на основе безвитаминного казеина), содержащим гидрохлорид пиридоксина (PN⋅HCl) в дозе 7 мг / кг. [оптимальный витамин B-6 (OB)] или 0,7 мг / кг диеты [умеренный дефицит витамина B-6 (MB)], используя модель умеренного дефицита витамина B-6, как описано ранее (15).Каждая группа крыс также потребляла ab libitum 10 мг / кг антагониста витамина B-6 либо в синтетической форме (1ADP) (Santa Cruz Biotechnology), либо без FE (контроль) в течение 5 недель ( Supplemental Table 1 ). Прием пищи контролировали ежедневно, а массу тела измеряли каждую неделю. В конце эксперимента образцы плазмы и тканей были собраны после 12 часов голодания для биохимических анализов.
Биохимические анализы плазмы.
Витамеры B-6 в плазме, включая PLP, пиридоксаль, пиридоксин и 4-пиридоксиновую кислоту (4-PA), были измерены как их семикарбазидные производные с использованием ВЭЖХ и детекции флуоресценции, как описано ранее (15).Общие тиолы в плазме, включая гомоцистеин и цистеин, были количественно определены с использованием 7-фторбензо-2-окса-1,3-диазол-4-сульфоната аммония методом ВЭЖХ с детектированием флуоресценции (21). Анализ профиля аминокислот в плазме выполняли с использованием имеющегося в продаже набора (EZ: faast kit, Phenomenex) с использованием пары Varian 450-GC с Varian 240-MS IT.
Активность печеночных PLP-зависимых ферментов.
Образцы печени (0,5 г) гомогенизировали с 5 мл ледяного 50 ммоль / л калий-фосфатного буфера (pH 6.8) и центрифугировали при 15000 × g и 4 ° C для сбора супернатанта (15). Активность печеночного фермента CBS определяли с использованием ранее описанного метода с некоторыми модификациями. Образец супернатанта инкубировали в реакционной смеси, содержащей радиоактивный материал, 25 ммоль / л L- [U- 14 C] серина (~ 78 000 dpm / мкмоль) (PerkinElmer) и L-цистатионин (0,15 ммоль / L), DL-гомоцистеин (41,67 ммоль / л), S -аденозилметионин (0,32 ммоль / л), DL-пропаргилглицин (2.08 ммоль / л), Трис (125 ммоль / л) и ЭДТА (2,08 ммоль / л). После инкубации при 37 ° C подсчитывали радиоактивность новообразованного 14 C-цистатионина для определения активности фермента CBS (22). Печеночную активность CGL определяли с помощью ферментативного анализа с использованием ранее описанного спектрофотометрического метода (23).
Статистический анализ.
Данные были разрезаны на основе концентрации PN⋅HCl в рационе (OB и MB), чтобы определить простые эффекты воздействия антагонистов независимо от воздействия витамина B-6 с пищей, статистическая процедура, использованная в предыдущей работе (15).Затем был проведен статистический анализ с использованием SPSS 16.0. Нормальность данных проверяли перед анализом с помощью теста Шапиро-Уилка, и, при необходимости, данные нормализовали преобразованием log 10 . Общая линейная модель была использована для сравнения эффектов лечения в той же группе с витамином B-6 с использованием теста Бонферрони, установив значимость на уровне P <0,05. Для всех биохимических аналитов плазмы мы использовали ANCOVA, взяв потребление корма в качестве ковариаты для контроля, учета и выравнивания несоответствий, которые могли возникнуть из-за различий в потреблении корма.В противном случае мы использовали однофакторный дисперсионный анализ для сравнения эффектов лечения.
Результаты
Приготовление ИП.
При количественном определении с помощью жидкостной хроматографии высокого разрешения / масс-спектрометрии количество антагониста витамина B-6 в лиофилизированных ФЭ оказалось равным 305 мкг линатина и 17 мкг 1АДФ на 50 мг образца. Согласно молярному расчету, как упоминалось в нашем предыдущем исследовании (13), общее количество антагониста витамина B-6, выраженное как 1ADPE, присутствующее в образце 50 мг, составляло 169 мкг, и это значение использовалось при приготовлении FE рационы, содержащие 10 мг 1АДФЭ / кг рациона.
Рабочие характеристики.
У крыс, получавших OB-рационы, те, которые подвергались воздействию 1ADP или FE, не показали каких-либо значительных различий в потреблении корма, конечной массе тела, коэффициенте эффективности корма (FER) или общем приросте веса по сравнению с теми, кто получал контрольный OB-рацион. (Рисунок 1 и Таблица 1). Однако у крыс, получавших диету с MB, у крыс из группы MB + 1ADP было более низкое потребление корма, FER и общий прирост массы тела, чем у крыс, получавших контрольную диету с MB ( P <0.001). В результате окончательная масса тела также была значительно снижена ( P <0,001). Тем не менее крысы в группе MB + FE не отличались от контрольных крыс с точки зрения маркеров показателей роста. Кроме того, кормление 1ADP, независимо от источника, не изменяло относительный вес печени крыс, потребляющих рационы с оптимальными или умеренно недостаточными концентрациями PN⋅HCl (таблица 1). В течение исследования наблюдалась одна летальность в группе OB + 1ADP.Смерть наступила внезапно, и у крысы не наблюдалось анорексии или снижения веса; однако патологоанатомическое исследование не выявило причину смерти.
РИСУНОК 1
Влияние FE и 1ADP на рост крыс, получавших рационы, содержащие 7 мг или 0,7 мг PN⋅HCl / кг рациона в течение 5 недель. Значения — это средние значения ± SEM; n = 8. В группе витамина B-6 обозначенные без общей буквы различаются, P <0,05. FE, экстракт льняного семени; МБ, умеренный дефицит витамина B-6; OB, оптимальный витамин B-6; PN⋅HCl, гидрохлорид пиридоксина; 1АДФ, 1-амино D-пролин.
РИСУНОК 1
Влияние FE и 1ADP на рост крыс, получавших рационы, содержащие 7 мг или 0,7 мг PN⋅HCl / кг рациона в течение 5 недель. Значения — это средние значения ± SEM; n = 8. В группе витамина B-6 обозначенные без общей буквы различаются, P <0,05. FE, экстракт льняного семени; МБ, умеренный дефицит витамина B-6; OB, оптимальный витамин B-6; PN⋅HCl, гидрохлорид пиридоксина; 1АДФ, 1-амино D-пролин.
ТАБЛИЦА 1Влияние FE и 1ADP на массу тела, потребление корма и коэффициент эффективности корма у крыс, получавших рационы, содержащие PN⋅HCl либо в дозе 7 мг / кг, либо в дозе 0.7 мг / кг диеты в течение 5 недель 1
Группа витамина B-6 (PN⋅HCl) и лечение . Начальная масса тела, г . Конечная масса тела, г . Общая прибавка в весе, г . RLW . Потребление корма, г . FER . OB диета (7 мг / кг диеты) OB 112 ± 6 456 ± 9 .49 ± 0,13 930 ± 15,3 0,37 ± 0,01 OB + FE 113 ± 3 456 ± 14 343 ± 16 3,49 ± 0,06 918 ± 24,7 OB + 1ADP 114 ± 3 430 ± 12 316 ± 12 3,57 ± 0,07 869 ± 24,8 0,37 ± 0,01 0,97 ± 0 .26 0,2 0,79 0,29 0,56 MB диета (0,7 мг / кг диеты) 270 ± 10 a 3,44 ± 0,08 780 ± 15,8 a 0,35 ± 0,01 a MB + FE 112 ± 7 a 260 ± 7 a 3.35 ± 0,09 770 ± 18,8 a 0,34 ± 0,01 a MB + 1ADP 114 ± 2 255 ± 8 b 141 ± 8 b ± 0,14 514 ± 19,0 b 0,28 ± 0,02 b P 0,98 <0,001 <0,001 0,72 0001
ТАБЛИЦА 1Группа витамина B-6 (PN⋅HCl) и лечение . Начальная масса тела, г . Конечная масса тела, г . Общая прибавка в весе, г . RLW . Потребление корма, г . FER . OB-диета (7 мг / кг диеты) OB 112 ± 6 456 ± 9 .49 ± 0,13 930 ± 15,3 0,37 ± 0,01 OB + FE 113 ± 3 456 ± 14 343 ± 16 3,49 ± 0,06 918 ± 24,7 OB + 1ADP 114 ± 3 430 ± 12 316 ± 12 3,57 ± 0,07 869 ± 24,8 0,37 ± 0,01 0,97 ± 0 .26 0,2 0,79 0,29 0,56 MB диета (0,7 мг / кг диеты) 270 ± 10 a 3,44 ± 0,08 780 ± 15,8 a 0,35 ± 0,01 a MB + FE 112 ± 7 a 260 ± 7 a 3.35 ± 0,09 770 ± 18,8 a 0,34 ± 0,01 a MB + 1ADP 114 ± 2 255 ± 8 b 141 ± 8 b ± 0,14 514 ± 19,0 b 0,28 ± 0,02 b P 0,98 <0,001 <0,001 0,72 0001Влияние FE и 1ADP на массу тела, потребление корма и коэффициент эффективности корма у крыс, получавших рационы, содержащие PN⋅HCl в дозе 7 мг / кг рациона или 0,7 мг / кг рациона в течение 5 недель 1
Группа витаминов B-6 (PN⋅HCl) и лечение . Начальная масса тела, г . Конечная масса тела, г . Общая прибавка в весе, г . RLW . Потребление корма, г . FER . OB диета (7 мг / кг диеты) OB 112 ± 6 456 ± 9 3,4 ± 0,13 930 ± 15,3 0,37 ± 0,01 OB + FE 113 ± 3 456 ± 14 343 ± 16 3.49 ± 0,06 918 ± 24,7 0,39 ± 0,03 OB + 1ADP 114 ± 3 430 ± 12 316 ± 12 3,57 ± 0,07 869 ± 2422,8 3869 ± 2422,8 3P 0,92 0,26 0,2 0,79 0,29 0,56 MB диета (0,7 мг / кг диета) 9067 MB 113 ± 3 383 ± 8 a 270 ± 10 a 3.44 ± 0,08 780 ± 15,8 a 0,35 ± 0,01 a MB + FE 112 ± 2 373 ± 7 a 260 ± 7 3 2 ± 0,09 770 ± 18,8 a 0,34 ± 0,01 a MB + 1ADP 114 ± 2 255 ± 8 b 141 ± 8 3 141 ± 8 3 0,14 514 ± 19.0 b 0,28 ± 0,02 b P 0,98 <0,001 <0,001 0,72 <0,001 6 9065 9065 9065 9065 908 -6 группа (PN⋅HCl) и лечение . Начальная масса тела, г . Конечная масса тела, г . Общая прибавка в весе, г . RLW . Потребление корма, г . FER . OB диета (7 мг / кг диеты) OB 112 ± 6 456 ± 9 3,4 ± 0,13 930 ± 15,3 0,37 ± 0,01 OB + FE 113 ± 3 456 ± 14 343 ± 16 3.49 ± 0,06 918 ± 24,7 0,39 ± 0,03 OB + 1ADP 114 ± 3 430 ± 12 316 ± 12 3,57 ± 0,07 869 ± 2422,8 3869 ± 2422,8 3P 0,92 0,26 0,2 0,79 0,29 0,56 MB диета (0,7 мг / кг диета) 9067 MB 113 ± 3 383 ± 8 a 270 ± 10 a 3.44 ± 0,08 780 ± 15,8 a 0,35 ± 0,01 a MB + FE 112 ± 2 373 ± 7 a 260 ± 7 3 2 ± 0,09 770 ± 18,8 a 0,34 ± 0,01 a MB + 1ADP 114 ± 2 255 ± 8 b 141 ± 8 3 141 ± 8 3 0,14 514 ± 19.0 b 0,28 ± 0,02 b P 0,98 <0,001 <0,001 0,72 <0,00173 6 0,001 . У крыс, получавших диету с MB, концентрации PLP в плазме были снижены на 26% и 69% ( P ≤ 0,001) у крыс, потребляющих диеты с MB + FE и MB + 1ADP, соответственно, по сравнению с контрольной группой с MB.Однако скармливание антагониста витамина B-6 крысам в группах OB-диеты не оказало значительного ( P = 0,61) влияния на концентрации PLP в плазме. Напротив, у крыс, потреблявших OB + 1ADP и MB + 1ADP, наблюдалось значительное снижение концентраций пиридоксаля в плазме по сравнению с их соответствующими контролями (таблица 2). Несмотря на пониженные концентрации пиридоксина в плазме у крыс, получавших антагонист витамина B-6, по сравнению с контрольными крысами, не было значительных различий между обработками ( P = 0.15) из-за мешающего эффекта приема пищи. Аналогичным образом, плазменный 4-PA, побочный продукт катаболизма витамина B-6, не подвергался влиянию, когда крыс кормили либо FE, либо 1ADP, и его стратифицировали в соответствии с диетическим содержанием витамина B-6.
ТАБЛИЦА 2Влияние FE и 1ADP на витамеры B-6 в плазме у крыс, получавших рацион, содержащий PN⋅HCl в дозе 7 мг / кг рациона или 0,7 мг / кг рациона в течение 5 недель 1
. Витамеры В-6, нмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . PN . PLP . 4-ПА . PL . OB-диета (7 мг / кг диеты) OB 320 ± 41,4 731 ± 62,2 649,5 ± 4,3 OB + FE 278 ± 38.4 721 ± 50,8 29,9 ± 4,2 566 ± 58,9 a OB + 1ADP 266 ± 47,4 663 ± 26,5 25,1 ± 2,6 3 P 0,65 0,61 0,64 0,012 MB диета (0,7 мг / кг диеты) 4 63,4 ± 3,0 a 2,6 ± 0,9 39,3 ± 3,2 a MB + FE 112 ± 6,6 47,1 ± 3,0 b 2,4 ± 0,5 2,4 ± 0,5 ± 2,3 a MB + 1ADP 72,3 ± 9,4 19,8 ± 2,0 b 3,6 ± 1,3 9,8 ± 1,0 b - P 0.001
0,62 0,003 . Витамеры В-6, нмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . PN . PLP . 4-ПА . PL . OB диета (7 мг / кг диеты) OB 320 ± 41.4 731 ± 62,2 29,5 ± 4,3 571 ± 64,9 a OB + FE 278 ± 38,4 721 ± 50,8 29,9 ± 4,2 58,91566 a OB + 1ADP 266 ± 47,4 663 ± 26,5 25,1 ± 2,6 397 ± 42,6 b P 0,65 - 9022 0,67012
MB диета (0,7 мг / кг диеты) MB 164 ± 21,4 63,4 ± 3,0 a 90 2,6 a MB + FE 112 ± 6,6 47,1 ± 3,0 b 2,4 ± 0,5 29,7 ± 2,3 a MB + 1ADP 72,3 ± 9. 419,8 ± 2,0 b 3,6 ± 1,3 9,8 ± 1,0 b P 0,15 0,001 2 0,62 6 0,002 6 0,002 FE и 1ADP на витаминах B-6 в плазме у крыс, получавших рационы, содержащие PN⋅HCl либо в дозе 7 мг / кг, либо в дозе 0,7 мг / кг в течение 5 недель 1 . Витамеры В-6, нмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . PN . PLP . 4-ПА . PL . OB-диета (7 мг / кг диеты) OB 320 ± 41,4 731 ± 62,2 649,5 ± 4,3 OB + FE 278 ± 38.4 721 ± 50,8 29,9 ± 4,2 566 ± 58,9 a OB + 1ADP 266 ± 47,4 663 ± 26,5 25,1 ± 2,6 3 P 0,65 0,61 0,64 0,012 MB диета (0,7 мг / кг диеты) 4 63,4 ± 3,0 a 2,6 ± 0,9 39,3 ± 3,2 a MB + FE 112 ± 6,6 47,1 ± 3,0 b 2,4 ± 0,5 2,4 ± 0,5 ± 2,3 a MB + 1ADP 72,3 ± 9,4 19,8 ± 2,0 b 3,6 ± 1,3 9,8 ± 1,0 b 9022 P 0.001 0,62 0,003 . Витамеры В-6, нмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . PN . PLP . 4-ПА . PL . OB диета (7 мг / кг диеты) OB 320 ± 41.4 731 ± 62,2 29,5 ± 4,3 571 ± 64,9 a OB + FE 278 ± 38,4 721 ± 50,8 29,9 ± 4,2 58,91566 a OB + 1ADP 266 ± 47,4 663 ± 26,5 25,1 ± 2,6 397 ± 42,6 b P 0,65 - 9022 0,67012
MB диета (0,7 мг / кг диеты) MB 164 ± 21,4 63,4 ± 3,0 a 90 2,6 a MB + FE 112 ± 6,6 47,1 ± 3,0 b 2,4 ± 0,5 29,7 ± 2,3 a MB + 1ADP 72,3 ± 9. 419,8 ± 2,0 b 3,6 ± 1,3 9,8 ± 1,0 b P 0,15 0,001 0,62 6asmin 9017 кислоты. Помимо витаминов B-6, важными биомаркерами дефицита витамина B-6 являются концентрации гомоцистеина и цистатионина в плазме (24, 25). В текущем исследовании мы обнаружили увеличение концентраций гомоцистеина и цистатионина в плазме из-за воздействия 1ADP ( P <0.001). Концентрация гомоцистеина в плазме была повышена на 744% у крыс MB + 1ADP по сравнению с контрольной группой MB, но у крыс MB + FE изменений не наблюдалось (таблица 3). Однако на концентрацию гомоцистеина в плазме не оказывало значительного влияния воздействие антагониста витамина B-6 (либо FE, либо 1ADP) в группах OB-диеты. В группах, получавших диету с MB, наблюдалось значительное увеличение концентрации цистатионина в плазме у крыс, потребляющих MB + FE (100%) или MB + 1ADP (1300%). Аналогичная картина наблюдалась и у крыс, получавших OB диеты (таблица 3).Несколько неожиданно значительное снижение ( P = 0,005) концентрации цистеина в плазме наблюдалось у крыс в группе OB + 1ADP по сравнению с контролем, но этого не наблюдалось в группах с диетой MB. Не наблюдалось значительного влияния воздействия антагониста витамина B-6 на концентрацию метионина в плазме (таблица 3).
ТАБЛИЦА 3Влияние FE и 1ADP на концентрации серосодержащих аминокислот в плазме у крыс, получавших рационы, содержащие PN⋅HCl либо в дозе 7 мг / кг рациона, либо 0.7 мг / кг диеты в течение 5 недель 1
ТАБЛИЦА 3. Серосодержащие аминокислоты в плазме крови, мкмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . Мет . Cys . Hcy . Cth . OB диета (7 мг / кг диеты) OB 49.9 ± 1,3 282 ± 6,0 a 10,2 ± 0,7 1,7 ± 0,0 c OB + FE 49,9 ± 1,8 284 ± 6,9 a 11 2,2 ± 0,1 b OB + 1ADP 46,3 ± 1,2 256 ± 5,0 b 12,0 ± 0,5 3,4 ± 0,2 a 9055 9055 9055 0.009 0,09 <0,001 MB диета (0,7 мг / кг диеты) MB 47,6 ± 0,8 907 22280 ± 6,2 b 2,3 ± 0,1 c MB + FE 48,4 ± 1,0 263 ± 6,1 9,5 ± 0,6 b 4,6 ± 0,9 b 48.0 ± 1,9 249 ± 4,5 71,7 ± 15,7 a 32,2 ± 5,9 a P 0,9 0,08 <0,001 9065. Серосодержащие аминокислоты в плазме крови, мкмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . Мет . Cys . Hcy . Cth . OB диета (7 мг / кг диеты) OB 49.9 ± 1.3 282 ± 6.0 a 90.2722 907 0,0 c OB + FE 49,9 ± 1,8 284 ± 6,9 a 11.4 ± 0,3 2,2 ± 0,1 b OB + 1ADP 46,3 ± 1,2 256 ± 5,0 b 12,0 ± 0,5 3,4 ± 0,2 a 0,19 0,009 0,09 <0,001 диета MB (0,7 мг / кг диеты) MB 47672 90.6 ± 0,8 280 ± 6,2 8,5 ± 0,5 b 2,3 ± 0,1 c MB + FE 48,4 ± 1,0 263 ± 6,1 9,5 ± 0,6 3 b
4,6 ± 0,9 b MB + 1ADP 48,0 ± 1,9 249 ± 4,5 71,7 ± 15,7 а 32,2 ± 5,9 a 0.08 <0,001 <0,001 Влияние FE и 1ADP на концентрации серосодержащих аминокислот в плазме крови у крыс, получавших рационы, содержащие PN⋅HCl в дозе 7 мг / кг или 0,7 мг / кг рациона в течение 5 недель 1
. Серосодержащие аминокислоты в плазме крови, мкмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . Мет . Cys . Hcy . Cth . OB диета (7 мг / кг диеты) OB 49,9 ± 1,3 282 ± 6,0 a 90,27 ± 0,7 0,0 c OB + FE 49,9 ± 1,8 284 ± 6,9 a 11.4 ± 0,3 2,2 ± 0,1 b OB + 1ADP 46,3 ± 1,2 256 ± 5,0 b 12,0 ± 0,5 3,4 ± 0,2 a 0,19 0,009 0,09 <0,001 диета MB (0,7 мг / кг диеты) MB 47672 90.6 ± 0,8 280 ± 6,2 8,5 ± 0,5 b 2,3 ± 0,1 c MB + FE 48,4 ± 1,0 263 ± 6,1 9,5 ± 0,6 3 b
4,6 ± 0,9 b MB + 1ADP 48,0 ± 1,9 249 ± 4,5 71,7 ± 15,7 а 32,2 ± 5,9 a 0.08 <0,001 <0,001 . Серосодержащие аминокислоты в плазме крови, мкмоль / л . Группа витамина B-6 (PN⋅HCl) и лечение . Мет . Cys . Hcy . Cth . OB диета (7 мг / кг диеты) OB 49.9 ± 1,3 282 ± 6,0 a 10,2 ± 0,7 1,7 ± 0,0 c OB + FE 49,9 ± 1,8 284 ± 6,9 a 11 2,2 ± 0,1 b OB + 1ADP 46,3 ± 1,2 256 ± 5,0 b 12,0 ± 0,5 3,4 ± 0,2 a 9055 9055 9055 0.009 0,09 <0,001 MB диета (0,7 мг / кг диеты) MB 47,6 ± 0,8 907 22280 ± 6,2 b 2,3 ± 0,1 c MB + FE 48,4 ± 1,0 263 ± 6,1 9,5 ± 0,6 b 4,6 ± 0,9 b 48.0 ± 1,9 249 ± 4,5 71,7 ± 15,7 a 32,2 ± 5,9 a P 0,9 0,08 <0,001 <0,001 9068 Другие аминокислоты плазмы. Концентрации других свободных аминокислот в плазме приведены в Таблице 4. В группах диеты с МБ — α-аминомасляная кислота в плазме (59%; P <0,001) и глутаминовая кислота (30%; P = 0.017) были значительно снижены у крыс MB + FE по сравнению с контролем, причем больший эффект наблюдался у крыс MB + 1ADP. Кроме того, концентрация глицина в плазме ( P = 0,02) была повышена, а концентрации серина в плазме ( P = 0,013) и аспарагина ( P = 0,016) были снижены у крыс MB + 1ADP. Мы также обнаружили значительное снижение ( P ≤ 0,013) концентраций α-аминомасляной кислоты в плазме у крыс OB + 1ADP. На другие аминокислоты плазмы, приведенные в таблице 4, пероральный прием FE или 1ADP не влиял.
ТАБЛИЦА 4Влияние FE и 1ADP на основные свободные аминокислоты плазмы у крыс, получавших рационы, содержащие PN⋅HCl в дозе 7 мг / кг рациона или 0,7 мг / кг рациона в течение 5 недель 1
. OB диета (PN⋅HCl: 7 мг / кг диеты), мкмоль / л . MB диета (PN⋅HCl: 0,7 мг / кг диеты), мкмоль / л . Аминокислота в плазме . OB . OB + FE . OB + 1ADP . п. . МБ . МБ + FE . МБ + 1ADP . п. . Аланин 619 ± 27,1 706 ± 25,2 619 ± 39,5 0,08 565 ± 16,2 542 ± 29,8 494 ± 30.5 0,25 Саркозин 10,8 ± 0,1 10,9 ± 0,1 10,9 ± 0,1 0,33 10,8 ± 0,1 10,9 ± 0,1 11,1 ± 0,1 901 285 ± 22,2 297 ± 19,4 289 ± 15,5 0,8 442 ± 24,2 b 511 ± 38,5 b 899 ± 74,4 a 21 02α-аминомасляная кислота 56,1 ± 4,4 a 44,3 ± 4,4 a, b 33,0 ± 3,3 b 0,013 45,9 ± 4,0 1 3
45,9 ± 4,0 1 1,9 b
13,8 ± 1,1 b <0,001 Валин 184 ± 9,4 198 ± 8,8 177 ± 6,0 0,26 907 8,31 151,5 ± 8,7 0,19 Лейцин 148 ± 7,8 158 ± 8,2 143 ± 6,2 0,42 147 ± 6,5 0,42 147 ± 6,5 ,89 147 ± 6,4 ,89 147 ± 6,4 Изолейцин 92,7 ± 5,2 96,0 ± 5,2 86,1 ± 4,5 0,46 90,6 ± 4,2 92,4 ± 4,7 82,9 ± 6,0 0,23 71.7590 ± 39,9 444 ± 38,2 0,05 766 ± 90,6 648 ± 64,9 486 ± 43,2 0,35 Серин 902 9022 907,13 ± 45,1 0,2 585 ± 49,9 a 469 ± 23,5 a, b 353 ± 32,4 b 0,013 Пролин 7,14,14 162 ± 6,6 0,33 183 ± 8,5 188 ± 4,2 186 ± 10,6 0,89 Аспарагин 96,1 ± 5,6 94,8 ± 3,1 94,8 ± 3,1 99,3 ± 4,7 a 87,3 ± 5,8 a, b 79,1 ± 4,4 b 0,013 4-гидроксипролин 64,9 ± 622,7 659,7 ± 6,3 0,56 65,1 ± 6,2 59,9 ± 6,3 51,4 ± 5,6 0,87 Глутаминовая кислота 206 ± 10,6 3 207 2 0,63 197 ± 14,0 a 152 ± 8,6 b 129 ± 6,0 b 0,017 Фенилаланин 64,1 ± 1,8 169,24 65,0 ± 1,7 0,09 62,4 ± 1,0 61,6 ± 2,2 57,7 ± 1,4 0,21 α-аминоадипиновая кислота 2,0 ± 0,2 2,3 ± 0,2 0,65 2,5 ± 0,1 2,9 ± 0,3 2,5 ± 0,2 0,38 Глутамин 956 ± 97,2 778 ± 93,4 867 ± 114,2 797 ± 92.8 759 ± 81,8 0,26 Орнитин 60,5 ± 2,6 66,1 ± 4,2 62,4 ± 2,6 0,48 86,5 ± 7,4 91,6 ± 22 91,6 ± 22 Лизин 303 ± 13,7 271 ± 7,9 273 ± 12,9 0,2 272 ± 16,1 257 ± 13,2 210 ± 13,3 906,16 9067ti 8 ± 5,1 59,4 ± 5,9 60,3 ± 4,5 0,92 62,7 ± 5,3 65,7 ± 6,5 84,0 ± 8,6 0,4 Тирозин 2,19067 1,9 ± 22 52,6 ± 1,9 0,29 51,3 ± 1,5 52,0 ± 1,9 49,1 ± 2,3 0,31 Пролин-гидроксипролин 23,1 ± 1,3 20,3 ± 0,1 90.5 ± 0,3 0,05 21,1 ± 0,3 20,3 ± 0,2 20,5 ± 0,3 0,05 Триптофан 82,3 ± 7,2 67,7 ± 6,2 78,4 ± 22 90,4 ± 6,9 71,1 ± 5,0 72,3 ± 6,6 0,33 . OB диета (PN⋅HCl: 7 мг / кг диеты), мкмоль / л . MB диета (PN⋅HCl: 0.7 мг / кг рациона), мкмоль / л . Аминокислота в плазме . OB . OB + FE . OB + 1ADP . п. . МБ . МБ + FE . МБ + 1ADP . п. . Аланин 619 ± 27.1 706 ± 25,2 619 ± 39,5 0,08 565 ± 16,2 542 ± 29,8 494 ± 30,5 0,25 10673 10,8 ± 0,1 0,33 10,8 ± 0,1 10,9 ± 0,1 11,1 ± 0,1 0,71 Глицин 285 ± 22,2 297 ± 19,4 9022 ± 1578 442 ± 24,2 b 511 ± 38,5 b 899 ± 74,4 a 0,02 α-аминомасляная кислота 56,1 ± 4,4 а, б
33,0 ± 3,3 б 0,013 45,9 ± 4,0 а 19,0 ± 1,9 б 13,8 ± 1,1 б <0,001 906 184 ± 9.4198 ± 8,8 177 ± 6,0 0,26 188 ± 8,3 190 ± 7,1 151,5 ± 8,7 0,19 Лейцин 148 148 1422 158673 148 142 7,83 ± 6,2 0,42 147 ± 6,5 147 ± 6,4 136 ± 9,8 0,26 Изолейцин 92,7 ± 5,2 96,0 ± 5,2 86,1 ± 4,5 4690,6 ± 4,2 92,4 ± 4,7 82,9 ± 6,0 0,23 Треонин 682 ± 71,7 590 ± 39,9 444 ± 38,2 9022 0,05 ± 64,9 486 ± 43,2 0,35 Серин 603 ± 60,1 472 ± 38,9 497 ± 45,1 0,2 585 ± 49,9 ± 23 469673 1 25 а, б 353 ± 32,4 б 0,013 Пролин 171 ± 7,1 168 ± 4,4 162 ± 6,6 0,33 8,5867 ± 183 4,2186 ± 10,6 0,89 Аспарагин 96,1 ± 5,6 94,8 ± 3,1 97,0 ± 4,3 0,94 99,3 ± 4,7 a b- 70
79.1 ± 4,4 b 0,013 4-гидроксипролин 64,9 ± 6,6 55,7 ± 4,6 59,7 ± 6,3 0,56 65,1 ± 6,2 2 59,9 ± 6,3 59,9 ± 6,3 0,87 Глутаминовая кислота 206 ± 10,6 213 ± 4,9 201 ± 20,2 0,63 197 ± 14,0 a 152 ± 8,6 3 1 21 21 1 900 b 0,017 Фенилаланин 64,1 ± 1,8 69,2 ± 1,4 65,0 ± 1,7 0,09 62,4 ± 1,0 61,6 ± 2,2 1,4α-аминоадипиновая кислота 2,0 ± 0,2 2,3 ± 0,2 2,3 ± 0,2 0,65 2,5 ± 0,1 2,9 ± 0,3 2,5 ± 0,2 0,38 778 ± 93,4 867 ± 114,2 0,49 962 ± 119 797 ± 92,8 759 ± 81,8 0,26 Орнитин 2,6 66722 60,57 ± 2,60,48 86,5 ± 7,4 91,6 ± 8,2 87,1 ± 5,9 0,88 Лизин 303 ± 13,7 271 ± 7,9 .2 272 ± 16,1 257 ± 13,2 210 ± 13,3 0,16 Гистидин 61,8 ± 5,1 59,4 ± 5,9 5,360,3 ± 4,5 0,9 ± 6,5 84,0 ± 8,6 0,4 Тирозин 58,7 ± 1,9 56,5 ± 2,1 52,6 ± 1,9 0,29 51,3 ± 1,5 52,0 ± 1,9 90 .6731 ± 2,3 0,31 Пролин-гидроксипролин 23,1 ± 1,3 20,3 ± 0,1 20,5 ± 0,3 0,05 21,1 ± 0,3 20,3 ± 0,2 20,3 ± 0,2 Триптофан 82,3 ± 7,2 67,7 ± 6,2 78,4 ± 8,2 0,34 84,4 ± 6,9 71,1 ± 5,0 72,3 ± 6,6 60 0,33 Эффект FEABLE и 1ADP на основные свободные аминокислоты плазмы у крыс, получавших рацион, содержащий PN⋅HCl либо в дозе 7 мг / кг рациона, либо 0.7 мг / кг диеты в течение 5 недель 1 . OB диета (PN⋅HCl: 7 мг / кг диеты), мкмоль / л . MB диета (PN⋅HCl: 0,7 мг / кг диеты), мкмоль / л . Аминокислота в плазме . OB . OB + FE . OB + 1ADP . п. . МБ . МБ + FE . МБ + 1ADP . п. . Аланин 619 ± 27,1 706 ± 25,2 619 ± 39,5 0,08 565 ± 16,2 542 ± 29,8 493 542 ± 29,8 493 9022 906 0,2 494 9022 906 0,2 494 9022 9067 10,8 ± 0,1 10,9 ± 0,1 10,9 ± 0,1 0,33 10.8 ± 0,1 10,9 ± 0,1 11,1 ± 0,1 0,71 Глицин 285 ± 22,2 297 ± 19,4 289 ± 15,5 0,8 442 b ± 38,5 b 899 ± 74,4 a 0,02 α-аминомасляная кислота 56,1 ± 4,4 a 44,3 ± 4,4 a, b 0 330673 9057
0.013 45,9 ± 4,0 a 19,0 ± 1,9 b 13,8 ± 1,1 b <0,001 Валин 184 ± 9,4 2184 ± 9,4 3 198 ± 8220,26 188 ± 8,3 190 ± 7,1 151,5 ± 8,7 0,19 Лейцин 148 ± 7,8 158 ± 8,2 143 ± 6,2 5 147 ± 6,4 136 ± 9,8 0,26 Изолейцин 92,7 ± 5,2 96,0 ± 5,2 86,1 ± 4,5 0,46 90,6 ± 4,2 ± 6,00,23 Треонин 682 ± 71,7 590 ± 39,9 444 ± 38,2 0,05 766 ± 90,6 648 ± 64,9 43722 4872220,35 Серин 603 ± 60,1 472 ± 38,9 497 ± 45,1 0,2 585 ± 49,9 a 469 ± 23,5 a b 0,013 Пролин 171 ± 7,1 168 ± 4,4 162 ± 6,6 0,33 183 ± 8,5 188 ± 4,2 183 ± 8,5188 ± 4,2 9067 ± 067289Аспарагин 96,1 ± 5,6 94,8 ± 3,1 97,0 ± 4,3 0,94 99,3 ± 4,7 a 87,3 ± 5,8 a, b 79,17 ± 4,4 0,013 4-гидроксипролин 64,9 ± 6,6 55,7 ± 4,6 59,7 ± 6,3 0,56 65,1 ± 6,2 59,9 ± 6,3 51,4 ± 6,3 2 51,4 ± 6,3 51,4 ± 6,387 Глутаминовая кислота 206 ± 10,6 213 ± 4,9 201 ± 20,2 0,63 197 ± 14,0 a 152 ± 8,6 b 152 ± 8,6 b 0,017 Фенилаланин 64,1 ± 1,8 69,2 ± 1,4 65,0 ± 1,7 0,09 62,4 ± 1,0 61,6 ± 2,2 57,7 ± 1,4 21 α-аминоадипиновая кислота 2,0 ± 0,2 2,3 ± 0,2 2,3 ± 0,2 0,65 2,5 ± 0,1 2,9 ± 0,3 2,5 ± 0,2 6 0,38 6 0,38 956 ± 97,2 778 ± 93,4 867 ± 114,2 0,49 962 ± 119 797 ± 92,8 759 ± 81,8 0,26 Орнитин5 ± 2,6 66,1 ± 4,2 62,4 ± 2,6 0,48 86,5 ± 7,4 91,6 ± 8,2 87,1 ± 5,9 0,88 Лизин 303 722 ± 13,7 273 ± 12,9 0,2 272 ± 16,1 257 ± 13,2 210 ± 13,3 0,16 Гистидин 61,8 ± 5,1 59,4 ± 5,9 60673 50,92 62,7 ± 5,3 65,7 ± 6,5 84,0 ± 8,6 0,4 Тирозин 58,7 ± 1,9 56,5 ± 2,1 52,6 ± 22 1,9 52,6 ± 22 1,9 52,0 ± 1,9 49,1 ± 2,3 0,31 Пролин-гидроксипролин 23,1 ± 1,3 20,3 ± 0,1 20,5 ± 0,3 0,05 21.1 ± 0,3 20,3 ± 0,2 20,5 ± 0,3 0,05 Триптофан 82,3 ± 7,2 67,7 ± 6,2 78,4 ± 8,2 0,34 84,4 ± 6,9 71 72,3 ± 6,6 0,33 . OB диета (PN⋅HCl: 7 мг / кг диеты), мкмоль / л . MB диета (PN⋅HCl: 0,7 мг / кг диеты), мкмоль / л . Аминокислота в плазме . OB . OB + FE . OB + 1ADP . п. . МБ . МБ + FE . МБ + 1ADP . п. . Аланин 619 ± 27,1 706 ± 25,2 619 ± 39.5 0,08 565 ± 16,2 542 ± 29,8 494 ± 30,5 0,25 Саркозин 10,8 ± 0,1 10,9 ± 0,1 3 10,9 ± 0,110,9 ± 0,1 11,1 ± 0,1 0,71 Глицин 285 ± 22,2 297 ± 19,4 289 ± 15,5 0,8 67 ± 15,5 0,8 442 9011 59011 - 5 b
899 ± 74,4 a 0,02 α-аминомасляная кислота 56,1 ± 4,4 a 44,3 ± 4,4 a, b 70 a, b 70 0,013 45,9 ± 4,0 a 19,0 ± 1,9 b 13,8 ± 1,1 b <0,001 Валин 184 ± 9,4 3 .0 0,26 188 ± 8,3 190 ± 7,1 151,5 ± 8,7 0,19 Лейцин 148 ± 7,8 158 ± 8,2 143 ± 6,2 143 ± 6,2 147 ± 6,4 136 ± 9,8 0,26 Изолейцин 92,7 ± 5,2 96,0 ± 5,2 86,1 ± 4,5 0,46 90,6 ± 4,2 4 ± 4,782,9 ± 6,0 0,23 Треонин 682 ± 71,7 590 ± 39,9 444 ± 38,2 0,05 766 ± 90,6 64,9664673 0,35 Серин 603 ± 60,1 472 ± 38,9 497 ± 45,1 0,2 585 ± 49,9 a 469 ± 23,5 3 a, b 24 b0,013 Пролин 171 ± 7,1 168 ± 4,4 162 ± 6,6 0,33 183 ± 8,5 188 ± 4,2 0,863 3 Аспарагин 96,1 ± 5,6 94,8 ± 3,1 97,0 ± 4,3 0,94 99,3 ± 4,7 a 87,3 ± 5,8 а, б 79,1 ± 4,4 905 .013 4-гидроксипролин 64,9 ± 6,6 55,7 ± 4,6 59,7 ± 6,3 0,56 65,1 ± 6,2 59,9 ± 6,3 51,4 ± 5,6 51,4 ± 5,6 206 ± 10,6 213 ± 4,9 201 ± 20,2 0,63 197 ± 14,0 a 152 ± 8,6 b 129 ± 6,0 b 0.017 Фенилаланин 64,1 ± 1,8 69,2 ± 1,4 65,0 ± 1,7 0,09 62,4 ± 1,0 61,6 ± 2,2 57,7 ± 1,4 6 0,21 57,7 ± 1,4 6 0,21 2,0 ± 0,2 2,3 ± 0,2 2,3 ± 0,2 0,65 2,5 ± 0,1 2,9 ± 0,3 2,5 ± 0,2 0,38 Глютамин 956 ± 97.2 778 ± 93,4 867 ± 114,2 0,49 962 ± 119 797 ± 92,8 759 ± 81,8 0,26 Орнитин 2,6 66722 90,4 ± 2,60,48 86,5 ± 7,4 91,6 ± 8,2 87,1 ± 5,9 0,88 Лизин 303 ± 13,7 271 ± 7,9 .2 272 ± 16,1 257 ± 13,2 210 ± 13,3 0,16 Гистидин 61,8 ± 5,1 59,4 ± 5,9 5,360,3 ± 4,5 0,9 ± 6,5 84,0 ± 8,6 0,4 Тирозин 58,7 ± 1,9 56,5 ± 2,1 52,6 ± 1,9 0,29 51,3 ± 1,5 52,0 ± 1,9 90 .6731 ± 2,3 0,31 Пролин-гидроксипролин 23,1 ± 1,3 20,3 ± 0,1 20,5 ± 0,3 0,05 21,1 ± 0,3 20,3 ± 0,2 20,3 ± 0,2 20,3 ± 0,2 20,3 Триптофан 82,3 ± 7,2 67,7 ± 6,2 78,4 ± 8,2 0,34 84,4 ± 6,9 71,1 ± 5,0 72,3 ± 6,6 0,33 90p6 виды деятельности.В текущем исследовании мы обнаружили значительное снижение ( P <0,001) активности печеночных ферментов CBS и CGL (рис. 2) при лечении FE или 1ADP по сравнению с соответствующими контролями. Активность печеночного фермента CGL была снижена по сравнению с группой MB на ~ 48% у крыс MB + FE и MB + 1ADP, тогда как снижение составило 26% и 60% для крыс OB + FE и OB + 1ADP, соответственно, в рационе OB. группа. В случае активности печеночного фермента CBS крысы MB + 1ADP имели более высокую степень ингибирования фермента (44% снижение), чем крысы MB + FE (26% снижение).Однако в группах с OB-диетой снижение было аналогичной величины, уменьшившись на ~ 31% для крыс OB + FE и OB + 1ADP.
РИСУНОК 2
Влияние FE и 1ADP на активность ферментов CBS (A) и CGL (B) в печени у крыс, получавших рационы, содержащие 7 мг или 0,7 мг PN⋅HCl / кг рациона в течение 5 недель. Значения — это средние значения ± SEM; n = 8. Внутри группы витамина B-6 обозначенные без общей буквы различаются, P <0,05. CBS, цистатионин-β-синтаза; CGL, цистатионин-γ-лиаза; FE, экстракт льняного семени; МБ, умеренный дефицит витамина B-6; OB, оптимальный витамин B-6; PN⋅HCl, гидрохлорид пиридоксина; 1АДФ, 1-амино D-пролин.
РИСУНОК 2
Влияние FE и 1ADP на активность ферментов CBS (A) и CGL (B) в печени у крыс, получавших рационы, содержащие 7 мг или 0,7 мг PN⋅HCl / кг рациона в течение 5 недель. Значения — это средние значения ± SEM; n = 8. Внутри группы витамина B-6 обозначенные без общей буквы различаются, P <0,05. CBS, цистатионин-β-синтаза; CGL, цистатионин-γ-лиаза; FE, экстракт льняного семени; МБ, умеренный дефицит витамина B-6; OB, оптимальный витамин B-6; PN⋅HCl, гидрохлорид пиридоксина; 1АДФ, 1-амино D-пролин.
Обсуждение
Диетический витамин B-6 оказывает существенное влияние на концентрацию PLP в плазме (9, 26). У людей концентрация PLP в плазме 20–30 нмоль / л или потребление 0,7 мг / сут витамина B-6 указывает на маргинальный статус витамина B-6 (4, 27). Среди населения в целом нехватка витамина B-6 характерна для 24% населения США и 21% пожилого населения Канады (> 50 лет) (19, 28). Неадекватный статус витамина B-6 также вовлечен в развитие многих распространенных заболеваний, включая хроническое воспаление, колоректальный рак и сердечно-сосудистые заболевания (29, 30).Следовательно, потребление соединений, обладающих антагонистической активностью витамина B-6, одновременно с маргинальным дефицитом витамина B-6, может увеличить риск развития метаболических дефектов или заболеваний, связанных с низким статусом витамина B-6 (14, 31). Таким образом, настоящее исследование было разработано для изучения потенциальных ответов на биомаркеры, вызванных дополнительными питательными веществами при пероральном потреблении компонента, полученного из льняного семени, в модели умеренного дефицита витамина B-6.
Дефицит витамина B-6 обычно вызывает снижение потребления пищи, прибавку в весе и FER у растущих животных, что указывает на явные дефекты промежуточного метаболизма, а также задержку азота при субоптимальном статусе витамина B-6 (15, 32, 33).В настоящем исследовании крысы в группе MB + 1ADP продемонстрировали значительное снижение FER, а также прибавку в весе по сравнению с другими группами. Эти данные подтверждают предыдущие результаты исследования, в котором изучалось влияние кормления антагонистом витамина B-6, 4-дезоксипиридоксином, которое привело к значительному снижению массы тела у крыс с низким статусом витамина B-6, чем у их коллег, получавших парное вскармливание (34 ).
Концентрации классических маркеров витамина B-6 в тканях, включая PLP, пиридоксаль, пиридоксин и 4-PA, в первую очередь отражают питательную ценность пиридоксина, но могут зависеть от приема внутрь ингибиторов витамина B-6 (9, 10 , 35).В текущем исследовании значительное изменение основных маркеров витамина B-6, возникшее в результате введения антагониста витамина B-6, согласуется с результатами предыдущих исследований (15, 31, 36). Наши данные показали, что FE снижает концентрацию PLP в плазме со значительными доказательствами у крыс из групп, получавших диету MB, что указывает на потенциальную способность связывания природного 1ADP с эндогенными витаминами B-6. Кроме того, синтетический 1ADP показал более сильное и широкое сродство к витаминам B-6 по сравнению с естественными, поскольку он значительно снизил концентрации PLP и пиридоксаля в плазме.Таким образом, текущее исследование предоставило доказательства того, что пероральный прием антагониста витамина B-6, либо в форме синтетического 1ADP, либо в виде FE, снижает общий пул витаминов B-6 в организме. Одна из основных причин снижения in vivo витаминов B-6 в текущем исследовании может быть результатом образования гидразоновых комплексов 1ADP со свободно доступными эндогенными PLP и пиридоксалем. Эти результаты, также предложенные другими, были более выражены при низком витаминном статусе B-6 (10, 14). Другие потенциальные механизмы включают индуцированную антагонистом витамина B-6 инактивацию ферментов-спасателей витамина B-6, таких как PLK и PNPOx (11), и повышенную экскрецию с мочой витаминов B-6 во время воздействия антагониста витамина B-6 (37).Хорошо известно, что ферменты PLK и PNPOx играют решающую роль в поддержании гомеостаза in vivo витаминов B-6 посредством их фосфорилирования и взаимопревращения (11, 38). Интересно, что их активность, как было показано, подавляется несколькими антагонистами витамина B-6, такими как изониазид, циклосерин и дофамин, которые имеют такой же механизм действия, как 1ADP, вызывая дефицит PLP in vivo (11). Однако необходимы дальнейшие исследования, чтобы охарактеризовать влияние этого антагониста витамина B-6 на гомеостаз витамина B-6 и его катаболизм in vivo.
Дефицит витамина B-6 изменяет профиль аминокислот в плазме из-за участия этого кофактора в многочисленных PLP-зависимых ферментах, особенно тех, которые участвуют в реакциях трансаминирования, транс-сульфирования и декарбоксилирования (6). Например, введение антагонистов витамина B-6 DL-пеницилламина, тиосемикарбазида и семикарбазида-HCl значительно снижало содержание γ-аминомасляной кислоты в мозге мышей (39). Кроме того, внутрибрюшинная инъекция 1ADP крысам приводила к значительному увеличению плазменных концентраций α-аминоадипиновой кислоты, цитруллина и цистатионина (14), тогда как перфузия 1ADP в изолированную печень крысы значительно снижала синтез карнитина из остатков лизина (40). ), что означает серьезные нарушения метаболизма аминокислот.Несколько исследований продемонстрировали значительно более высокие концентрации гомоцистеина и цистатионина в плазме как у животных, так и у людей при соблюдении диеты с ограничением витамина B-6 (15, 24, 25, 26). В текущем исследовании значительное повышение уровня гомоцистеина в плазме, которое наблюдалось в ответ на пероральное воздействие 1ADP, вероятно, было связано с ингибированием активности CBS в печени в пути транссульфурации, состояние, которое было более выражено при низком статусе витамина B-6. . Последний механизм подтверждается данными о том, что концентрация гомоцистеина в плазме выше (в 40 раз) у мышей, лишенных активности CBS, чем у мышей дикого типа (41).Кроме того, активность печеночного фермента CGL также подавлялась из-за подачи антагониста витамина B-6 либо из льняного семени, либо из синтетического 1ADP, что приводило к увеличению содержания цистатионина в плазме и значительному снижению концентраций α-аминомасляной кислоты в плазме. Подобный паттерн ингибирования активности ферментов CBS и CGL был зарегистрирован в печени животных с дефицитом витамина B-6 (24, 26, 42). Текущие результаты подтверждают утверждение о том, что умеренный дефицит витамина B-6, а также пероральное воздействие антагонистов витамина B-6 были способны независимо ингибировать активность PLP-зависимых ферментов, включая печеночные CBS и CGL, у крыс.
Декарбоксилирование глицина через систему расщепления глицина и превращение глицина в серин с помощью SHMT в одноуглеродном метаболизме также требует PLP. Предполагается, что ингибирование SHMT и / или системы расщепления глицина является механизмом, объясняющим сдвиги в соотношении глицина к серину в плазме при низком статусе витамина B-6 (25, 26, 43). Следовательно, одной из причин повышения уровня глицина в плазме и снижения концентрации серина в плазме в текущем исследовании может быть нарушение этих 2 ферментов, что привело к снижению превращения глицина in vivo в серин.Кроме того, снижение концентраций аспарагина и глутаминовой кислоты в плазме в результате кормления 1ADP при низком статусе витамина B-6 может быть связано с нарушением других PLP-зависимых ферментов, участвующих в трансаминировании и взаимном превращении аминокислот. Наши данные подтверждаются предыдущим исследованием Swendseid et al. (43), которые обнаружили более высокие концентрации цистатионина и глицина и более низкие концентрации серина и общего глутамина и аспарагина в плазме крыс с дефицитом витамина B-6.
Ответы, вызванные диетическим дефицитом витамина B-6 или воздействием антагонистов витамина B-6 на аминокислотный профиль, могут проявлять изменчивость, вероятно, связанную с продолжительностью или серьезностью навязанного дефицита (4, 14, 44). Грегори и др. (4) недавно показали, что предельный дефицит витамина B-6 сам по себе может вызывать незначительные нарушения метаболических индексов, в том числе аминокислотных профилей in vivo, а одновременное воздействие синтетического антагониста витамина B-6 еще больше усугубляет статус витамина B-6 (15).Интересно, что текущие данные свидетельствуют о нарушении определенных маркеров витамина B-6 из-за сопутствующего воздействия антагониста витамина B-6, полученного из льняного семени, во время умеренного дефицита витамина B-6 при введении в дозе 0,5 мг 1АДФЭ ⋅ кг −1 масса тела ⋅ d −1 . Потребление 25–30 г / день льняного семени, размер порции, рекомендуемый некоторыми (45–47), приведет к потреблению 0,15 мг 1АДФЭ кг −1 массы тела ⋅ d −1 (при условии, что тело вес 65 кг), концентрация в том же порядке, что и в текущем исследовании.Таким образом, наши данные служат для того, чтобы подчеркнуть потенциальные пагубные последствия перорального воздействия антагониста витамина B-6, связанного с льняным семеном, на популяцию с умеренным дефицитом витамина B-6. Однако биоэффективность природных биологически активных соединений во многом зависит от их биодоступности. Например, синтетические лекарства, как правило, лучше высвобождают, всасываются, распределяют и метаболизм, чем природные биоактивные компоненты (48). Основным антагонистическим фактором витамина B-6, присутствующим в льняном семени, является дипептид линатин, который должен высвобождать свободный 1ADP посредством гидролиза γ-глутамиловой связи, присоединенной к глутаминовой кислоте в желудочно-кишечном тракте, чтобы вызвать in vivo токсичность антагониста витамина B-6. .Неполный гидролиз и / или снижение всасывания и метаболизма линатина, содержащегося в FE, может быть причиной пониженной активности 1ADP, полученного из льняного семени, по сравнению с синтетическим 1ADP. Тем не менее, 1АДФ, полученный из льняного семени, действительно продемонстрировал способность нарушать определенные маркеры метаболизма аминокислот и витамина B-6 в текущем исследовании.
В заключение, настоящее исследование предоставило доказательства того, что пероральный прием антагониста витамина B-6, либо из семян льна, либо из синтетического источника, снижает количество свободных витамеров B-6 in vivo, потенциально из-за образования гидразона, тем самым нарушая метаболизм аминокислот.Наиболее интригующим открытием этого исследования была способность FE ингибировать активность PLP-зависимых ферментов. Однако необходимы дальнейшие исследования, чтобы лучше понять механизм действия 1ADP и защитную роль витамина B-6 при токсичности антагониста витамина B-6. Существуют также дополнительные возможности для изучения долгосрочного воздействия этого природного антагониста витамина B-6, связанного с льняным семенем, на другие метаболические пути.
Благодарности
Благодарим Haifeng Yang за техническую помощь.SM и JDH разработали исследование; SM и SR провели исследование и проанализировали данные; С.М. написал рукопись; MA и JDH рассмотрели рукопись; и JDH несла основную ответственность за окончательный контент. Все авторы прочитали и одобрили окончательную рукопись.
Список литературы
1Christen
P
,Mehta
PK
.От кофактора до ферментов. Молекулярная эволюция пиридоксаль-5′-фосфатзависимых ферментов
.Chem Rec
2001
;1
:436
—47
,2Hellmann
H
,Mooney
S
.Витамин B6: молекула для здоровья человека?
Молекулы
2010
;15
:442
—59
,3Тони
MD
.Специфичность реакции пиридоксальфосфатных ферментов
.Arch Biochem Biophys
2005
;433
:279
—87
.4Грегори
IIIJF
,Парк
Y
,Ламерс
Y
,Bandyopadhyay
N
,Chi
YY
,KIM
KIM
KIM
,da Silva
V
,Hove
N
,Ranka
S
и др.Метаболомический анализ показывает расширенные метаболические последствия маргинального дефицита витамина B-6 у здоровых людей
.PLoS One
2013
;8
:e63544
.5Stipanuk
MH
.Метаболизм серных аминокислот: пути производства и удаления гомоцистеина и цистеина
.Annu Rev Nutr
2004
;24
:539
—77
,6Боулинг
FG
.Предложение пиридоксина в человеческом развитии
.Semin Cell Dev Biol
2011
;22
:611
—8
.7Medici
V
,Peerson
JM
,Stabler
SP
,French
SW
,Gregory
, 3-йJF
,Virata4000 MC A
,Bowlus
CL
,Devaraj
S
,Panacek
EA
и др.Нарушение транссульфурации гомоцистеина является индикатором алкогольной болезни печени
.J Hepatol
2010
;53
:551
—7
,8Дом
JD
,Jacobs
RL
,Stead
LM
,Brosnan
ME
0005ME
ME
Регуляция метаболизма гомоцистеина
.Adv Enzyme Regul
1999
;39
:69
—91
.9Spinneker
A
,Sola
R
,Lemmen
V
,Castillo
9000z4000000 Pietr Гонсалес-ГроссM
.Статус витамина B6, дефицит и его последствия — обзор
.Nutr Hosp
2007
;22
:7
—24
.10Клостерман
JH
.Антагонисты витамина B6 природного происхождения
.Журнал сельскохозяйственной и пищевой химии.
1974
;22–1
:13
—6
.11di Salvo
ML
,Contestabile
R
,Safo
MK
.Ферменты-спасатели витамина B6: механизм, структура и регуляция
.Biochim Biophys Acta
2011
;1814
:1597
—608
.12Klosterman
HJ
,Lamoureux
GL
,Parsons
JL
.Выделение, характеристика и синтез линатина. Антагонист витамина B6 из льняного семени (Linum usitatissimum)
.Biochemistry
1967
;6
:170
—7
.13Mayengbam
S
,Yang
H
,Barthet
V
,Aliani
M
,House
JD
.Идентификация, характеристика и количественная оценка антипиридоксинового фактора из льняного семени с использованием сверхвысокопроизводительной жидкостной хроматографии-масс-спектрометрии
.J Agric Food Chem
2014
;62
:419
—26
.14Sasaoka
K
,Ogawa
T
,Moritoki
K
,Kimoto
M
Антивитамин В6 действие 1 аминопролина на крыс
.Biochim Biophys Acta
1976
;428
:396
—402
.15Майенгбам
S
,Raposo
S
,Алиани
M
,Дом
JD
.Пероральное воздействие антипиридоксинового соединения 1-амино D-пролин дополнительно нарушает метаболизм гомоцистеина через путь транссульфурации у крыс с умеренным дефицитом витамина B 6 -дефицитных крыс
.J Nutr Biochem
2015
;26
:241
—9
.16Карраро
JCC
,де Соуза Дантас
MI
,Espeschit
ACR
,004 SMI
Мартино
Мартино
.Льняное семя и здоровье человека: обзор преимуществ и побочных эффектов
.Food Rev Int
2012
;28
:203
—30
.17Прасад
К
.Льняное семя и здоровье сердечно-сосудистой системы
.J Cardiovasc Pharmacol
2009
;54
:369
—77
. 18Холл
, 3-йC
,Tulbek
MC
,Xu
Y
.Льняное семя
.Adv Food Nutr Res
2006
;51
:1
—97
.19Morris
MS
,Picciano
MF
,Jacques
PF
,Selhub
J
.Пиридоксаль-5′-фосфат в плазме у населения США: Национальное исследование здоровья и питания, 2003–2004 гг.
.Am J Clin Nutr
2008
;87
:1446
—54
.20Haller
J
,Lowik
MR
,Ferry
M
,Ferro-Luzzi
A
.Состояние питания: витамины в крови A, E, B6, B12, фолиевая кислота и каротин. Следователи Euronut SENECA
.евро J Clin Nutr
1991
;45
Suppl 3
:63
—82
,21Pfeiffer
CM
,Huff
DL
,Gunter
EW
.Быстрый и точный анализ ВЭЖХ общего гомоцистеина и цистеина в плазме в условиях клинической лаборатории
.Clin Chem
1999
;45
:290
—2
.22Taoka
S
,Ohja
S
,Shan
X
,Kruger
0004 WDДоказательства опосредованной гемом окислительно-восстановительной регуляции активности цистатионин-β-синтазы человека
.J Biol Chem
1998
;273
:25179
—84
,23Стипанук
MH
.Влияние избытка метионина в рационе на катаболизм цистеина у крыс
.J Nutr
1979
;109
:2126
—39
.24Zhang
Z
,Kebreab
E
,Jing
M
,Rodriguez-Lecompte 9000 9000
Rodriguez-Lecompte 9000
,
Flintoft
M
,House
JD
.Нарушения пиридоксин-зависимого метаболизма серных аминокислот очень чувствительны к степени дефицита и восполнения витамина B6 у свиней
.Животное
2009
;3
:826
—37
,25Ламеры
Y
,Williamson
J
,Ralat
M
,Quinlivan
EP
EP Килинг
C
,Стивенс
RD
,Newgard
CB
,Ueland
PM
,Meyer
K
и др.Умеренное ограничение витамина B-6 в рационе повышает концентрацию глицина и цистатионина в плазме, минимально влияя на скорость обмена и расщепления глицина у здоровых мужчин и женщин
.J Nutr
2009
;139
:452
—60
0,26Мартинес
M
,Cuskelly
GJ
,Williamson
J
,Toth
JR
,Gregory III .
Дефицит витамина B-6 у крыс снижает активность серин-гидроксиметилтрансферазы и цистатионин-β-синтазы в печени и скорость белкового обмена in vivo, реметилирования гомоцистеина и транссульфурации
.J Nutr
2000
;130
:1115
—23
.27Машияма
ST
,Hansen
CM
,Roitman
E
,Sarmiento
000 J
S
S Шульц
TD
,Эймс
BN
.Анализ урацила в ДНК человека на исходном уровне: влияние предельного дефицита витамина B6
.Анал Биохим
2008
;372
:21
—31
,28.
Статистическое управление Канады
.Витамин B6: Обычное поступление с пищей
.2004
. .29Lotto
V
,Choi
SW
,Friso
S
.Витамин B6: сложная связь между питанием и воспалением при сердечно-сосудистых заболеваниях
.Br J Nutr
2011
;106
:183
—95
.30Larsson
SC
,Orsini
N
,Wolk
A
.Витамин B6 и риск колоректального рака: метаанализ проспективных исследований
.JAMA
2010
;303
:1077
—83
.31Чанг
SJ
.Антагонисты витамина B6 изменяют функцию и ультраструктуру эндотелиальных клеток мышей
.J Nutr Sci Vitaminol (Токио)
2000
;46
:149
—53
.32Wolfson
M
,Kopple
JD
.Влияние дефицита витамина B6 на потребление пищи, рост и функцию почек у крыс с хронической азотемией
.JPEN J Parenter Enteral Nutr
1987
;11
:398
—402
.33Кирхгесснер
M
,Костерс
WW
.Влияние дефицита витамина B 6 у поросят на раннем отъеме на усвояемость и преобразование белка и энергии
.Arch Tierernahr
1977
;27
:299
—308
.34Coburn
SP
,Mahuren
JD
,Schaltenbrand
WE
,0005000500050004 Wostmann 9000 Mad5senВлияние дефицита витамина B-6 и 4′-дезоксипиридоксина на концентрацию пиридоксальфосфата, пиридоксинкиназу и другие аспекты метаболизма у крыс
.J Nutr
1981
;111
:391
—8
.35Люмен
L
,Лю
A
,Li
TK
.Содержание витаминов B6 в плазме и его связь с метаболизмом витамина B6 в печени
.J Clin Invest
1980
;66
:688
—95
,36Jaffe
IA
.Антивитамин В6 действие D-пеницилламина
.Ann N Y Acad Sci
1969
;166
:57
—60
.37Кадзивара
T
,Мацуда
M
.Влияние пеницилламина на распределение витаминов B6 в моче крыс
.J Nutr Sci Vitaminol (Токио)
1978
;24
:1
—7
.38McCormick
DB
,Chen
H
.Обновленная информация о взаимопревращениях витамина B-6 с его коферментом
.J Nutr
1999
;129
:325
—7
.39Abe
M
,Matsuda
M
.Влияние антивитамина B6 на региональный метаболизм ГАМК в головном мозге мышей и его связь с судорогами
.J Nutr Sci Vitaminol (Токио)
1979
;25
:459
—68
.40Dunn
WA
,Aronson
NN
Jr.,Englard
S
.Влияние 1-амино-D-пролина на продукцию карнитина из триметиллизина, связанного с экзогенным белком, перфузированной печенью крысы
.J Biol Chem
1982
;257
:7948
—51
.41Watanabe
M
,Osada
J
,Aratani
Y
,Kluckman
Kluckman
K4000 Malinow
MR
,Maeda
N
.Мыши с дефицитом цистатионин бета-синтазы: животные модели легкой и тяжелой гомоцистной (е) инемии
.Proc Natl Acad Sci USA
1995
;92
:1585
—9
.42Финкельштейн
JD
,Чалмерс
FT
.Влияние пиридоксина на цистатионинсинтазу в печени крыс
.J Nutr
1970
;100
:467
—9
.43Swendseid ME
.Вильялобос Дж., Фридрих Б. Свободные аминокислоты в плазме и тканях крыс, получавших диету с дефицитом витамина В6
.J Nutr
1964
;82
:206
—8
.44da Silva
VR
,Rios-Avila
L
,Ламеры
Y
,Ralat
MA4
,Quinlivan
EP
,Garrett
TJ
,Coats
B
,Shankar
MN
,Percival
SS
и др.Анализ профиля метаболитов выявляет функциональные эффекты 28-дневного ограничения витамина B-6 на одноуглеродный метаболизм и катаболические пути триптофана у здоровых мужчин и женщин
.J Nutr
2013
;143
:1719
—27
.45Edel
AL
,Алиани
M
,Pierce
GN
.Поддерживаемая жидкостная экстракция для количественного определения энтеролигнанов плазмы с использованием изотопного разведения ГХ / МС с применением для потребления льняного семени здоровыми взрослыми
.J Chromatogr B Analyt Technol Biomed Life Sci
2013
;912
:24
—32
.46Калиджури
SP
,Аукема
HM
,Ravandi
A
,Guzman
Ravandi
Пирс
GN
.Употребление льняного семени снижает артериальное давление у пациентов с гипертонией за счет изменения циркулирующих оксилипинов посредством ингибирования растворимой эпоксидгидролазы, индуцированного альфа-линоленовой кислотой.
.Гипертония
2014
;64
:53
—9
.47Wu
H
,Pan
A
,Yu
Z
,Qi
Q
,L
L 9000 Zhang
G
,Yu
D
,Zong
G
,Zhou
Y
,Chen
X
и др.Консультации по образу жизни и добавка льняного семени или грецких орехов влияют на лечение метаболического синдрома
.J Nutr
2010
;140
:1937
—42
, 48Рейн
MJ
,Renouf
M
,Cruz-Hernandez
C
,Actis-Goretta
000000
Actis-Goretta 9000 SK
,да Силва Пинто
M
.Биодоступность биоактивных пищевых соединений: сложный путь к биоэффективности
.Br J Clin Pharmacol
2013
;75
:588
—602
.Сокращения
CBS
цистатионин β-синтаза
CGL
FE
FER
MB
умеренно витамин B-6 с дефицитом
PLP
PN⋅HCl
PNPOx
пиридоксинфосфатоксидаза
SHMT
серингидроксиметилтрансфераза
- DADP11
4-АП
PL
© Американское общество питания, 2016 г.
Блокаторы дофаминергических рецепторов D2, используемые для лечения шизофрении, могут привести к развитию двигательных расстройств, вызванных лекарственными препаратами, таких как паркинсонизм, дистония, дискинезия и т. акатизия.Похоже, они связаны с окислительным стрессом в результате увеличения количества свободных радикалов, образующихся в результате метаболизма дофамина. Доклиническое исследование показало, что витамины B6 (пиридоксин) и B12 (кобаламин), по отдельности или в комбинации, предотвращали развитие дискинезии ротовой полости, вызванной галоперидолом, на животной модели шизофрении.
Конкретная цель 1: провести проспективное рандомизированное двойное слепое плацебо-контролируемое исследование для оценки эффективности 12-недельного адъювантного лечения 200 мг пиридоксина (B6) или 2 мг кобаламина (B12) для лечения двигательных расстройств, вызванных лекарственными средствами. пациентов с шизофренией, шизоаффективным или биполярным расстройством.Исследователи случайным образом разделят 45 пациентов на три группы: плацебо, B6 или B12 и проверит, снижает ли введение витамина B6 (пиридоксин) или B12 (кобаламин) лекарственные двигательные расстройства (IDDM) у пациентов с диагнозом шизофрения, шизоаффективность или биполярность. беспорядок.
Конкретная цель 2: количественно оценить изменения сывороточных маркеров воспаления и биомаркеров окислительного стресса в ответ на дополнительное лечение B6 или B12. Гипотеза состоит в том, что изменения этих биомаркеров опосредуют клинический ответ на них.
План исследования: Исследователи проведут 12-недельное проспективное рандомизированное двойное слепое контролируемое исследование витамина B6 и B12 в дозах 200 мг / день и 2 мг / день, соответственно, или идентичных таблеток плацебо. , добавлен к текущим антипсихотическим средствам у 45 стабильных пациентов (возраст 18-60 лет, 15 пациентов в группе) с диагнозом шизофрения, шизоаффективное или биполярное расстройство. Исследование будет проводиться в Центре исследований и разработок лекарственных средств (NPDM) Федерального университета до Сеара, Форталеза, Бразилия.Этот центр имеет долгую историю проведения контролируемых плацебо испытаний в клинической медицине (http://www.npdm.ufc.br/) и имеет необходимую инфраструктуру для успешного завершения предложенного протокола исследования. Все участники дадут письменное информированное согласие до включения в исследование.
Границы | Структурная динамика и перспективы ферментов биосинтеза витамина B6 в плазмодиях: достижения и открытые вопросы
Введение
Согласно отчету Всемирной организации здравоохранения (ВОЗ) о малярии за 2020 год (Всемирная организация здравоохранения, 2020), в общей сложности было зарегистрировано 229 миллионов случаев малярии. сообщалось в 2019 году в 87 эндемичных странах, большинство из которых находятся в Африке к югу от Сахары.Несмотря на недавние достижения в лечении, ок. В 2019 году по-прежнему было зарегистрировано 409000 смертей от малярии и, к сожалению, прибл. 65% этих смертей приходится на детей в возрасте до 5 лет (Всемирная организация здравоохранения, 2020 г.). Для сравнения, пандемия COVID-19 вызвала 450 000 смертей с апреля 2020 г. по середину января 2021 г. в Южной Америке и Африке вместе, что позволяет предположить, что малярия по количеству смертей эквивалентна пандемии COVID-19 для этих регионов. Хотя уровень смертности от малярии снижается во всем мире, очевидно, что для более эффективного лечения малярии в эндемичных районах требуется значительно больше усилий.
Об устойчивости основного возбудителя малярии Plasmodium falciparum к хлорохину и широко используемому сульфадоксин-пириметамину сообщалось с 50-х и 60-х годов прошлого века. Даже для комбинированной терапии на основе артемизинина, рекомендованной ВОЗ для лечения малярии (Всемирная организация здравоохранения, 2015 г.), в эндемичных районах наблюдалось повышение устойчивости, что привело ВОЗ к запуску программы Emergency Response to Artemisinin Resistance (ERAR) в 2013.Кроме того, устойчивые к противомикробным препаратам инфекции вызывают прибл. Ежегодно во всем мире умирает 700 000 человек, а к 2050 году, по оценкам, вырастет до 10 миллионов (IACG, 2019). Что касается серьезности этой ситуации, то на форуме более 20 ведущих мировых фармацевтических компаний в 2020 году было объявлено о создании «Фонда действий против AMR» с инвестиционной целью — вывести на рынок 2-4 новых препарата к 2030 году (Clancy and Нгуен, 2020). В целом, научное сообщество приложило огромные усилия для определения новых молекулярных мишеней и, возможно, для предложения новых лекарственных препаратов-кандидатов, которые можно было бы использовать в эндемичных по малярии районах.
Интересный подход и потенциальная лекарственная мишень включают биосинтез витаминов de novo в Plasmodium . В этом контексте Чан с соавторами показали, что ингибирование тиаминпирофосфокиназы плазмодий с использованием аналога окситиамина приводит к ингибированию пролиферации паразитов (Chan et al., 2013). Аналогичный подход был также оценен для других важных путей. Ренджер и соавторы идентифицировали гены ферментов Pdx1, Pdx2 и PdxK в Plasmodium falciparum , ответственных за биосинтез и утилизацию пиридоксаль-5’-фосфата (PLP) (Wrenger et al., 2005; Мюллер и др., 2010). В отличие от пути биосинтеза тиамина, для биосинтеза de novo PLP (витамин B 6 ) требуется только два фермента (Pdx1 и Pdx2) для образования комплекса (Pdx1-Pdx2 или комплекс синтазы PLP) (Barra et al. ., 2020). Реакция, катализируемая комплексом PLP-синтазы, показана на дополнительном рисунке S1, в то время как отдельные реакции, катализируемые Pdx1 и Pdx2, показаны на рисунках 1A, 3A. В Plasmodium профиль экспрессии генов pdx1 и pdx2 , кодирующих Pdx1 и Pdx2, указывает на то, что оба белка локализованы в цитозоле (Wrenger et al., 2005).
Рисунок 1 (A) Схема ферментативной реакции, катализируемой Pdx1. (B, C) Два ортогональных вида структурного выравнивания одной репрезентативной структуры каждого организма, как доступно в PDB для P. berghei (PDB ID: 4ADU), A . thaliana (5LNR), T. maritima (2ISS), T. thermophilus (2ZBT), G . kaustophilus (4WY0), G . stearothermophilus (1ZNN), B.subtilis (2NV1), S. cerevisae (3FEM), M. tuberculosis (4JDY), M. jannaschii (2YZR) и P. horikoshii (4FIQ). (D) Сравнение кристаллической структуры P. berghei Pdx1 в отсутствие (красный рисунок, PDB ID 4ADU) и присутствие (синий рисунок, PDB ID 4ADS) Pdx2. (E, F) Два ортогональных вида собранного додекамера Pdx1. Нижний гексамер показан в (E) в виде мультфильмов и прозрачных поверхностей. (G, H) Различные ступени в A . thaliana Pdx1 катализ: (G) Pdx1, ковалентно присоединенный к R5P; (H) Pdx1 промежуточный I 320 ; (I) Pdx1 промежуточный I 320 -G3P; (J) Pdx1 ковалентно связывается с продуктом PLP. Каталитические лизины показаны в виде палочек и показаны на рисунке. Рисунок был подготовлен с помощью программы UCSF Chimera (Pettersen et al., 2004).
Plasmodium зависит от de novo синтеза витамина B6, а также от поглощения нефосфорилированного витамина из окружающей среды.Этот вывод подтверждается выводом о том, что P. berghei pdx1 необходим для оптимального развития паразита на стадии крови, хотя и не важен для выживания. Кроме того, не было обнаружено, что PdxK, фермент, ответственный за спасение витамина B6, является незаменимым (Derrer, 2010). Однако нокаут генов pdx1 , pdx2 и pdxk так и не был получен, что позволяет предположить, что de novo и пути спасения совместно необходимы для выживания паразитов.В контексте инфекции человека спасательный путь кажется менее необходимым, поскольку доступные питательные вещества в основном фосфорилируются, и синтез витамина de novo становится более актуальным.
Витамин B6 играет двойную роль в P. falciparum . Классическая роль PLP заключается в его электрофильном стабилизирующем эффекте карбаниона в нескольких ферментативных реакциях. PLP-зависимые ферменты можно разделить на семь групп в зависимости от активности фермента: ( i ) аминотрансферазы и декарбоксилазы аминокислот, такие как сериногидроксиметилтрансферазы и аспартатаминотрансферазы; ( ii ) активность по замене и элиминации Cβ-групп, таких как серин- и треониндегидратазы; ( iii ) активность по взаимному превращению L- и D-аминокислот с общей укладкой (α / β) 8 , такой как аланинрацемаза; ( iv ) аланинаминотрансфераза; ( v ) гликогенфосфорилаза; ( vi ) 5,6-аминомутаза; и ( vii ) 2,3-аминомутаза (Kronenberger et al., 2014). В Plasmodium большинство PLP-зависимых ферментов классифицировано в группы 1 и 2, что подчеркивает их значимость в метаболизме аминокислот (Kappes et al., 2011; Kronenberger et al., 2014). Вторая роль PLP в Plasmodium заключается в защите паразита от синглетного кислорода ( 1 O 2 ). Knöckel и соавторы показали, что уровни транскрипции генов pdx1 и pdx2 активируются в присутствии церкоспорина в ответ на окислительный стресс (Knöckel et al., 2012). Авт. Также показали защитный эффект сверхэкспрессии Pdx1 и Pdx2, приводящий к увеличению выживаемости паразитов в окислительной среде (Knöckel et al., 2012).
Ключевым аспектом биосинтеза de novo PLP является то, можно ли рассматривать этот путь в качестве мишени для открытия лекарств для лечения малярии. Reeksting и соавторы сообщили, что гидразидный аналог D-эритрозо-4-фосфата, 4PEHz, ингибировал P. falciparum Pdx1-Pdx2 с IC 50 , равным 16 мкМ (Reeksting et al., 2013). Соединение также тестировали на его действие на пролиферацию паразитов во внутриэритроцитарных культурах с IC 50 10,4 мкМ. Также интересно отметить, что эффект 4PEHz наблюдался даже в культуральной среде, содержащей 5 мкМ пиридоксина, что позволяет предположить, что ингибирующий эффект может преодолеть путь спасения (Reeksting et al., 2013). Это подтверждающее концептуальное исследование убедительно свидетельствует о том, что ферменты, участвующие в пути биосинтеза PLP, должны быть дополнительно изучены и рассмотрены в качестве потенциальных мишеней для лекарств.
Идеальные случаи новых стратегий разработки лекарств включают специфическое ингибирование лекарственных мишеней патогена с минимальной или почти нулевой токсичностью для человека-хозяина (Lewis, 2012). Следовательно, выбранные лекарственные мишени должны явно отличаться от метаболических процессов хозяина или даже отсутствовать в организме хозяина (Begum et al., 2013). В этом контексте присутствие ферментов синтеза PLP в метаболических путях большинства организмов, включая бактерии, грибы, простейшие и растения, и их отсутствие у людей (Barra et al., 2020) позволяет избежать нецелевого связывания и потенциальных побочных эффектов.
В этом обзоре мы суммируем текущее состояние продолжающихся исследований по характеристике пути биосинтеза PLP у видов Plasmodium и результаты, полученные до настоящего времени. Кроме того, мы кратко пересматриваем перспективы медицинской химии для этого пути и резюмируем некоторые оставшиеся вопросы.
Структура-функция и динамика PDX1
Дезоксилулозо-5-фосфат (DXP) -независимый (R5P-зависимый) путь, впервые идентифицированный в 1999 г. (Ehrenshaft et al., 1999), состоит из двух белков Pdx1 и Pdx2, которые динамически собираются с образованием временного 24-мерного комплекса Pdx1-Pdx2. Комплекс Pdx состоит из додекамерного ядра Pdx1, собранных в два независимых функциональных D6-симметричных гексамера, сложенных вместе (Figure 1) (Strohmeier et al., 2006). Внутренняя часть додекамерного Pdx1 выстлана активными центрами 12 субъединиц мономера Pdx1, а в насыщенном комплексе 12 субъединиц Pdx2 расположены во внешней области додекамера Pdx1, а их активные центры расположены в интерфейсных областях Pdx1-Pdx2.
Ферментная складка Pdx1 напоминает классическую бочкообразную складку (β / α) 8 или TIM (триозофосфат-изомераза) с 8 параллельными β-цепями, составляющими внутреннее ядро, которое чередуется с 8 основными α-спиралями и их вставками вокруг β-цепей. (Чжу и др., 2005). Он катализирует превращение D-рибозо-5-фосфата (R5P), D-глицеральдегид-3-фосфата (G3P) и аммиака в пиридоксаль-5-фосфат, воду и фосфат (рис. 1A), все в серии прибл. 20 или более ферментативных стадий. Механизм ферментативной реакции довольно сложен и включает раскрытие кольца R5P, образование ковалентного иминного промежуточного звена через остаток лизина в активном центре, несколько реакций отщепления и таутомеризации, а также образование новых ковалентных промежуточных продуктов с одним из стабильный хромофорный промежуточный продукт (I 320 ) (Hanes et al., 2008). Такой механизм довольно необычен для метаболических путей и открывает новый путь для исследований дизайна лекарств, нацеленных на конкретный Pdx1 ферментного комплекса PLP.
На сегодняшний день сообщается о ряде кристаллических структур Pdx1 как у прокариот, так и у эукариот, с олигомерными структурами в основном в додекамерной форме и несколькими гексамерами Pdx1. Додекамерные структуры Pdx1 описаны для Plasmodium berghei , PDB ID 4ADT (Guédez et al., 2012), Arabidopsis thaliana (5LNS, 6HX3) (Robinson et al., 2016; Родригес и др., 2017; Robinson et al., 2019), Thermotoga maritima (2ISS) (Zein et al., 2006), Geobacillus kaustophilus (4WXZ) (Smith et al., 2015), G. staerothermophilus (1ZNN) (Zhu et al., 2005), Bacillus subtilis (2NV1) (Strohmeier et al., 2006) и Mycobacterium tuberculosis (4JDY) (Kim and Kim, 2013). С другой стороны, гексамерный олигомер Pdx1 описан для Saccharomyces cerevisiae (3006 и 3FEM) (Neuwirth et al., 2009; Zhang et al., 2010) и археи Pyrococcus horikoshii (4FIQ) (Matsuura et al., 2012). При сравнении их тройных структур с использованием онлайн-сервера DALI (Holm and Rosenström, 2010), вышеупомянутые гомологи дают значения Z-score в диапазоне от 47 до 36 со значениями среднеквадратичного отклонения от 0,5 до 1,3 Å, что свидетельствует о замечательной структурной консервации. у разных организмов, от бактерий до растений, включая дрожжи и Plasmodium , и средняя идентичность последовательностей прибл.60% относительно эталонной структуры Pb Pdx1. Структурная консервация показана структурным выравниванием 10 кристаллических структур на рисунках 1B, C.
Что касается олигомерного состояния Pdx1, плазмодийный фермент спонтанно образует додекамерные олигомеры в растворе (рисунки 1E, F), что также подтверждается электронной микроскопией. для Pf Pdx1 (Knöckel et al., 2009; Derrer et al., 2010; Guédez et al., 2012). Ullah et al. также сообщили о состоянии додекамерного раствора P.vivax Pdx1, используя дополнительные биофизические, биоаналитические методы и методы рассеяния рентгеновских лучей в растворе (SAXS), подчеркивая, что форма додекамерного раствора является функциональной предпосылкой для плазмодиальных белков Pdx1 (Ullah et al., 2020). Додекамерная форма плазмодия Pdx1 также была подтверждена через кристаллическую структуру из Plasmodium berghei (Guédez et al., 2012).
Эти результаты согласуются с наблюдениями, согласно которым большинство бактериальных белков Pdx1 являются додекамерными (Strohmeier et al., 2006). Исключением является Pdx1 из Pyrococcus horikoshii , который оказался гексамером в растворе, а также в кристаллическом состоянии. Дальнейшие подробные структурные исследования показали, что вставка 37 остатков в последовательность P. horikoshii Pdx1 (Matsuura et al., 2012) изменила это равновесие в сторону гексамерной формы. Saccharomyces cerevisae Pdx1 также был обнаружен в гексамерной форме, как в растворе, так и в кристаллическом состоянии, и это наблюдение было приписано вставке остатка лизина (Lys177), пространственно расположенного в области интерфейса гексамера (Neuwirth et al., 2009).
Сравнение природной кристаллической структуры Pdx1 P. berghei и его комплекса с ковалентным промежуточным соединением и с Pdx2 обнаруживает тонкие структурные различия, которые имеют отношение к функции Pdx1 (Guédez et al., 2012). В отсутствие лиганда / субстрата и Pdx2 короткая спираль α2 ’(расположенная рядом с каталитическим центром Pdx1) оказывается неупорядоченной в структуре плазмодия Pdx1. После входа и ковалентного связывания субстрата R5P с остатком активного сайта лизином спираль упорядочивается и ориентируется в соответствии с предлагаемым «закрытым подтверждением» (рис. 1D) (Guédez et al., 2012). Предполагается, что эта закрытая конформация защищает промежуточные соединения субстрата в активном центре Pdx1 от модификации растворителем и позволяет ферменту принимать нейтральный аммиак, переносимый из Pdx2.
Подобная структурная перестройка наблюдалась также в плазмодийном комплексе Pdx1-Pdx2, где присоединение фермента Pdx2 выравнивает спираль α2 ’Pdx1 в« открытую конформацию ». Положение спирали в этой конформации отличается от того, что наблюдалось для связывания субстрата, и не покрывает сайт связывания фосфата Pdx1 (P1) (Guédez et al., 2012). Открытая конформация позволяет ферменту принимать вход аммиака в активный центр Pdx1 через гидрофобный аммиачный туннель. Эти конформационные изменения приводят к предположению, что связывание Pdx2 индуцирует адаптивный эффект на Pdx1, позволяя связываться с субстратом (Raschle et al., 2009).
Структурная схема каталитического механизма и отдельных промежуточных продуктов синтеза Pdx1 PLP была представлена через шести кристаллических структур фермента A. thaliana Pdx1 на различных стадиях катализа (Rodrigues et al., 2017). Авторы сообщили об иминном промежуточном соединении между лизином 98 (Lys84 в PbPdx1) и C1 в R5P (рис. 1G). Промежуточное соединение I 320 образуется впоследствии при добавлении хлорида аммония, вызывая замещение фосфата и образование второго имина лизином 166 (Lys152 в PbPdx1, рис. 1H). Кроме того, изменение положения Lys166 вводит тонкие конформационные изменения в β-цепь β6, где расположен этот остаток. После этого добавление G3P привело к образованию промежуточного соединения I 320 -G3P с фосфатной группой G3P, занимающей тот же сайт связывания фосфата, что и для R5P, в сайте связывания P1 (рис. 1I).Следующим шагом в каталитическом механизме является фактическое превращение R5P и G3P в PLP, ковалентно связанный с Pdx1 через Lys166. В этом случае он создает второй сайт связывания, называемый сайтом связывания P2, аналогично P1, с фосфатным ионом, занимающим сайт в отсутствие продукта PLP (Rodrigues et al., 2017). Каталитический цикл включает изменения конформации боковых цепей Lys98 и Lys166, а также изменение положения β-цепи β6 и небольшой α-спирали α2 ’(рис. 1J). Конформационные изменения, наблюдаемые в цикле, лучше визуализируются в видеоанимации, подготовленной с помощью « трансформации » шести A.thaliana кристаллических структур. Видео доступно как дополнительный материал.
Сайты связывания P1 (участвующие в аккомодации субстратов) и P2 (участвующие в образовании и аккомодации PLP продукта) наблюдаются и сообщаются в мономере Pdx1 для нескольких прокариот и эукариот: эти сайты заняты анионами буферной соли в отсутствие субстрата или продукта (Zhu et al., 2005). Что касается расположения в цилиндре мономера, сайт P1 с характерной петлей GTG ( 156 GTG в PbPdx1, рис.2) расположен в пространственном расположении, близком к C-концевой стороне (Zhu et al., 2005). Этот сайт обычно занят ионами хлорида (Guédez et al., 2012), связанными с другими анионами и имитирующими субстрат рибозы. Участок P2, далекий ок. 15-20 Å от сайта P1 обычно заняты ионами хлорида или фосфата в отсутствие ферментных лигандов (Strohmeier et al., 2006; Rodrigues et al., 2017).
Анализ додекамера Pdx1 из P. berghei показывает, что несколько остатков, участвующих во взаимодействии протомеров Pdx1, расположены в консервативных мотивах у разных видов.Эти мотивы включают 61 VxR, 86 RIGHFVE, 111 TxADx, 140 RRISE, 156 GTG и 181 DESE (нумерация PbPdx1), как показано на рис. Это наблюдение, Knöckel и соавторы показали, что мутация G155A в Pf Pdx1 (Gly156 в Pb Pdx1, из мотива GTG 156 ) снижает равновесную концентрацию додекамера и приводит к образованию гексамера в растворе (Knöckel et al., 2009). Любопытно, что этот мутант был неспособен синтезировать PLP, но был способен рекрутировать и активировать Pdx2 (Knöckel et al., 2009). Lys151 в Pf Pdx1 (K152 в Pb Pdx1), часть активного центра и играющий активную роль в катализе, также показал аналогичное поведение: мутант PfPdx1 K151A был в основном гексамерным и неактивным, но был способен рекрутировать и активировать Pf Pdx2 (Müller et al., 2008). Наконец, C-конец Pdx1 также непосредственно участвует в олигомеризации как часть поверхности взаимодействия, хотя последовательность этой области не сохраняется.На сегодняшний день опубликованные данные показывают, что С-конец образует протяженную петлю с пространственным положением, смежным с петлей α2´-α2 интерфейсного мономера, устанавливая межцепочечные контакты для образования гексамера Pdx1 (Neuwirth et al., 2009 ). Это наблюдение также согласуется с предыдущим наблюдением Derrer и соавторов, которые показали участие C-концевой и предшествующей спирали α8 ’’ в додекамере Pdx1 (Derrer et al., 2010).
Виды олигомеров высокого порядка, наблюдаемые в комплексе PLP, могут указывать на потенциальную кооперативность в синтезе PLP.Однако это не похоже на тот случай, когда Pdx1 анализируется в отсутствие Pdx2. Наблюдаются типичные гиперболические кривые, которые, по-видимому, хорошо согласуются с классической кинетической моделью Michaelis-Menten (Wrenger et al., 2005), а сигмоидальная кривая не наблюдается в кинетике ферментов для большинства ферментов Pdx1, как можно было бы ожидать от кооперативности Хилла. Более того, похоже, что на активность PLP-синтазы P. falciparum не влияет присутствие или отсутствие Pdx2. Удельная активность PfPdx1 была определена как 746 пмоль мин -1 мг -1 при использовании хлорида аммония в качестве источника аммиака и 662 пмоль мин -1 мг -1 в присутствии Pdx2 и L- глутамин (Müller et al., 2008). Любопытно, что это отличается от того, что наблюдалось для фермента Mycobacterium tuberculosis Pdx1, где замена Pdx2 хлоридом аммония приводила к трехкратному снижению удельной активности (Dick et al., 2010).
Структура-функция и динамика Pdx2
Pdx2 — это фермент глутаминаза, ответственный за превращение глутамина в глутамат и аммиак, последний позже доставляется в Pdx1 для синтеза PLP (рисунок 3A и дополнительный рисунок S1).У P. falciparum гены pdx1 и pdx2 расположены в хромосомах 11 и 6 соответственно (Wrenger et al., 2005). Было замечено, что Pdx2 был неактивен, когда экспрессировался отдельно, но проявлял активность глутаминазы при смешивании с Pdx1 в соотношении 1: 1 (Wrenger et al., 2005; Gengenbacher et al., 2006). Удельная активность фермента была определена как 209 нмоль мин -1 мг -1 , с константой Михаэлиса-Ментена K M = 1,3 мМ для глутамина, согласно Wrenger и соавторам (Wrenger et al., 2005), или K M = 0,56 мМ и k cat 0,11 с -1 , согласно Gengenbacher и соавторам (Gengenbacher et al., 2006). Синтазный комплекс PfPLP принимает в качестве субстратов пятиуглеродный сахар R5P или рибулозо-5-фосфат и трехуглеродный сахар G3P или дигидроксиацетонфосфат (DHAP) с сопоставимой активностью. Однако обеспечение хлорида аммония в буфере вместо Pdx2 в качестве источника аммиака делает Pdx1 селективным для G3P как триозного сахара (Gengenbacher et al., 2006).
Рисунок 3 (A) Схема ферментативной реакции, катализируемой Pdx2. (B) Структурная суперпозиция кристаллических структур, доступная в PDB для P. falciparum Pdx2 (PDB ID 2ABW), T. maritima (2ISS), G . kaustophilus (4WXY), B. stearothermophilus (1Q7R), B. subtilis (2NV0), M. jannaschii (2YWJ). (C) Слева, структурный вид Pdx1 (показан синим рисунком и поверхностью) и Pdx2 (показан коричнево-розовым рисунком).Петля, связывающая β-нити β6-β7, указана на рисунке и является частью взаимодействующего интерфейса. Справа: наложение PfPdx2 в отсутствие (коричневый) и присутствие (розовый) Pdx1. (D) Два ортогональных вида взаимодействия Pdx1-Pdx2. Некоторые трещины в комплексе показаны желтым цветом на поверхности, что указывает на предполагаемый путь для туннеля аммиака. Рисунок был подготовлен с помощью UCSF Chimera (Pettersen et al., 2004) и программы PyMol.
Причины активации Pdx2 на основе Pdx1 были, по крайней мере, частично объяснены в недавнем отчете Уллаха и его коллег (Ullah et al., 2020). Авторы показали с помощью исследований динамического рассеяния света (DLS) и рассеяния рентгеновских лучей в растворе (SAXS), что P. vivax Pdx2 обладает внутренними гибкими характеристиками для образования различных олигомеров с течением времени. Кроме того, они наблюдали с помощью DLS с временным разрешением и электронной микроскопии (EM), изучающих интересное поведение обратимой олигомеризации Pdx2 после смешивания мультимерного / олигомерного Pdx2 с монодисперсным додекамерным Pdx1. Это указывает на стабилизирующий эффект фермента Pdx1 при связывании с Pdx2 и в этом контексте для комплекса Pdx (Ullah et al., 2020).
Pdx2 собирается с Pdx1 с образованием комплекса PLP-синтазы спонтанно даже в отсутствие субстратов фермента. Gengenbacher и соавторы описали, что совместная экспрессия обоих ферментов P. falciparum приводит к спонтанному образованию комплекса Pdx (Gengenbacher et al., 2006). Образование комплекса плазмодий PLP-синтазы также наблюдалось с помощью исследований EM и SAXS (Guédez et al., 2012; Ullah et al., 2020). Однако насыщение ферментов Pdx1 Pdx2 обеспечивается только в присутствии субстрата (Guédez et al., 2012), показывая, что активация субстратом увеличивает сродство и поддерживает взаимодействие между Pdx1 и Pdx2. Кроме того, они также наблюдали, что мутация активного сайта в субъединице Pdx2 (h296N) нарушает способность метаболизировать глутамин, приводя к насыщенному и полностью декорированному комплексу Pdx1-Pdx2 (Guédez et al., 2012). В другом структурном исследовании белков Pdx из Saccharomyces cerevisiae субъединица Pdx2 образовывала комплекс без мутаций активного сайта в присутствии аналога глутамина ацивицина.Аналог ацивицина был обнаружен в ковалентно связанном состоянии с каталитическим остатком цистеина (Chaudhuri et al., 2001), что указывает на ингибирование Pdx2. Эти наблюдения предоставляют структурные детали для поддержки дизайна ингибиторов в контексте исследований по открытию лекарств, чтобы приблизиться к PLP синтазному комплексу с акцентом на нативное состояние Pdx2.
Кристаллические структуры некоторых ферментов Pdx2, отдельно или в комплексе с Pdx1, находятся на разных эволюционных уровнях i.е. из P. falciparum (код PDB: 2ABW) (Gengenbacher et al., 2006; Guédez et al., 2012), Thermotoga maritima (код PDB: 2ISS) (Zein et al., 2006), Geobacillus kautophilus (код PDB: 4WXY) (Smith et al., 2015), Bacillus subtilis (код PDB: 1R9G, 2NV0) (Bauer et al., 2004; Strohmeier et al., 2006) и M. jannaschii , со значительными различиями между структурами плазмодий и бактерий Pdx2 в их функциональных структурных элементах.Структура Pdx2 классифицируется как складка Россмана, с β-тяжами, образующими протяженное центральное ядро β-листа, и α-спиралями, окружающими архитектуру листа, образуя трехслойную многослойную структуру, типичную для домена глутамин амидотрансферазы I класса (Strohmeier и др., 2006).
Поиск с помощью сервера DALI показывает, что сравниваемые RMSD между Pf Pdx2 и упомянутыми выше ферментами находятся в диапазоне от 1,1 до 2,1 Å с Z-оценкой, варьирующейся от 28 до 24. Интересно, что типичная идентичность последовательностей между ферментами составляет ок.38%, что указывает на структурную консервацию, несмотря на расхождение в идентичности последовательностей (Фигуры 3B и 4).
Сравнение нативного Pf Pdx2 и кристаллической структуры фермента в комплексе с Pb Pdx1 показывает структурные адаптации Pdx2 при связывании с его партнером. Основная перестройка — это стабилизация петли с участием остатков 123-128 (нумерация Pf Pdx2), соединяющих β6 и β7. Эта петля отсутствует в структуре PfPdx2 с более высоким разрешением и стабилизирована в синтазном комплексе PLP, как показано на рисунке 3C.Эта стабилизация петли обычно наблюдается в других глутамин амидотрансферазах (Mouilleron and Golinelli-Pimpaneau, 2007). Не удивительно, что петля расположена в области интерфейса между Pdx1 и Pdx2, взаимодействуя с N-концевой спиралью Pdx1. Другая важная функция перестройки петли — формирование туннеля без растворителя, соединяющего активный центр Pdx2 с гидрофобным β-бочонком Pdx1, используемым возникающей генерируемой нейтральной молекулой аммиака, которая диффундирует к активному центру Pdx1.Этот аммиачный туннель состоит из гидрофобных остатков (Guédez et al., 2012), соединяющих активные центры синтазы и глутаминазы комплекса Pdx, причем оба активных центра расположены на расстоянии прибл. 25 Å (Рисунок 3D).
Вторая структурная перестройка, наблюдаемая в Pdx2 при связывании с Pdx1, наблюдается в петле, соединяющей β3-α3, внутри консервативного мотива 50 PGGEST и N-концевой области спирали α1 (рис. 4). N-концевая часть спирали α1 искажена, неконсервативный остаток Asp14 перемещен в значительной степени для более тесного пространственного контакта с остатками активного центра каталитической триады.Расстояние между атомами Cδ в Asp14 и Glu198 изменяется от 9 Å в нативной структуре Pdx2 до 4 Å в трехмерной структуре комплекса Pdx1-Pdx2, предполагая, что Asp14 может действовать как вспомогательный остаток во время ферментативного катализа. Кроме того, в петле в мотиве 50 PGGEST вводится перегиб, как показано на фиг. 3C. Этот излом возникает из-за изменения положения Gly51, который перемещается примерно на 2 Å, когда положение атома азота основной цепи сравнивается в связанном и несвязанном состояниях.Этот остаток вместе с Ala88 образует оксианионную дырку через амидные атомы азота основной цепи. Петля с оксианионной дыркой (предпосылка активности глутаминазы) участвует в стабилизации временного отрицательного заряда во время гидролиза глутамина (Gengenbacher et al., 2006; Mouilleron and Golinelli-Pimpaneau, 2007).
От структуры-функции к разработке лекарств
Как мы упоминали ранее, примеры конкретных основных соединений, разработанных для нацеливания на комплекс PLP-синтазы, все еще отсутствуют, насколько известно авторам.На данный момент известно, что аналоги субстрата могут ингибировать фермент и, следовательно, рост паразитов (Chaudhuri et al., 2001; Reeksting et al., 2013), хотя дальнейшая оптимизация соединений не проводилась после этого доказательства. концепция. В этом контексте можно спросить: «Является ли PLP-синтаза жизнеспособной мишенью для лекарств?»?
Инструмент DoGSiteScorer (Volkamer et al., 2012b; Volkamer et al., 2012a) соответствует карману связывания, который охватывает активный сайт (сайт связывания субстрата), но также расширен за счет включения интерфейса взаимодействия со следующим мономером в гексамере. сборка (рисунок 5).Этот карман занимает объем ок. 1,800 Å 3 и индекс DrugScore 0,81, что свидетельствует о наиболее подходящей лекарственной форме этого сайта. DrugStore представляет собой индекс в диапазоне от 0 до 1 и оценивается по базе данных из 1069 структур, где DoGSiteScorer указал точность 88% (Volkamer et al., 2012b). Интересно, что анализ сайтов с наивысшими индексами DrugScore с использованием SIENA (Bietz and Rarey, 2016) не выявил какого-либо известного подобного кармана с уже известным лигандом, сопоставимого со структурными особенностями комплекса PLP-синтазы.
Рисунок 5 Карманы, картированные на Plasmodial PLP синтазном комплексе с помощью DoGSiteScorer (Volkamer et al., 2012b). Идентифицированные карманы большего размера показаны как поверхности. (слева) Общий вид комплекса PLP-синтазы. Второй гексамер Pdx1 и присоединенные ферменты Pdx2 были опущены для ясности. (справа) Подробный вид лузы с лучшим рейтингом. Для сравнения также показан субстрат, связанный с каталитическим лизином 84 (вручную состыкованный из кристаллической структуры A. thaliana , PDB ID 5LNS).Поверхность этого сайта включает карман связывания субстрата, а также простирается до поверхности, где фермент взаимодействует с партнером, показанным голубой лентой. Подобные карманы также идентифицируются для других мономеров, как показано на розовых и желтых прозрачных поверхностях.
Некоторые элементы, необходимые для дальнейшего продвижения предложения о пути биосинтеза пиридоксина в качестве лекарственной мишени, суммированы в этом специализированном обзоре. В дополнительных таблицах 1, 2 перечислены кристаллические структуры Pdx1 и Pdx2, доступные на момент написания этой статьи в базе данных белков.Отметим, что существуют две плазмодиальные кристаллические структуры Pdx1 с разрешением лучше 2,5 Å и по крайней мере три кристаллические структуры неплазмодиальных кристаллических структур Pdx1 с разрешением лучше 1,7 Å (дополнительная таблица 1). Для Pdx2 кристаллическая структура плазмодиального фермента доступна в PDB с разрешением 1,62 Å, обеспечивая точные атомные детали структуры фермента. Эти существующие экспериментальные данные обеспечивают необходимую основу для структурного дизайна и оптимизации лигандов-кандидатов.Другая часть связана с in vivo активностью аналогов субстрата в отношении пролиферации Plasmodium . Эти данные дополнительно дополняются анализом лекарственной способности сайта связывания фермента. Сложив части вместе, можно легко представить сценарий, в котором моделирование на основе структуры применяется для оптимизации аналогов субстрата и для предложения новых соединений, которые могли бы служить в качестве химических проб при оценке пути витамина B6 в качестве реального лекарственного средства. цель.
Аналоги субстратовPLP могут быть очень интересными соединениями в этом контексте. Поскольку механизм PLP-синтазы включает несколько ковалентных промежуточных соединений, эти соединения могут служить суицидными ингибиторами , как ранее использовалось в других важных путях (Drebes et al., 2014). Дополнительным преимуществом этого подхода является то, что он может быть полезен для других патогенов человека, поскольку активный сайт фермента высококонсервативен.
Необходимость оптимизации существующего соединения-ингибитора становится очевидной при анализе сходства между 4PEHz и известными лигандами мишеней CHEMBL, полученными с помощью подхода ансамбля сходства (SEA) (Keizer et al., 2007). Анализ показывает, что по крайней мере пять человеческих мишеней имеют высокую вероятность взаимодействия с 4PEHz ( p — значение менее 1E -27 ), включая 6-фосфоглюконатдегидрогеназу, рецептор 6 лизофосфатидной кислоты, триозофосфатизомеразу и рецептор лизофосфатидной кислоты. 4 и 3. Таким образом, оптимизация на основе структуры для этого аналога может быть необходима, чтобы избежать отклонений от цели.
Обсуждение
Прибл. 4% всех ферментных реакций, перечисленных Комиссией по ферментам (EC), зависят от PLP, что подчеркивает важность витамина B6 для общего гомеостаза (Percudani and Peracchi, 2009).Понимание биосинтеза плазмодий PLP de novo значительно продвинулось за последние 15 лет, и в настоящее время известны многие механистические аспекты ферментной олигомеризации и реакции. Однако чего еще не хватает? Конечно, более полная проверка Pdx1 и Pdx2 как молекулярных мишеней с точки зрения открытия лекарств все еще необходима, и очень желательно больше химических зондов (Gregori-Puigjané et al., 2012). Как мы уже отмечали, PLP-синтаза, и особенно фермент Pdx1, могут быть высоко оценены как лекарственная мишень в соответствии с химиоинформатическими инструментами, но все еще требуются дальнейшие усилия и исследования.
Остающиеся нерешенными вопросы включают в себя: ( i ) Можно ли воздействовать на сайт взаимодействия между Pdx1 и Pdx2? ( ii ) Может ли активность PLP-синтазы быть нарушена Pdx2-специфическим ингибированием? Частью доказательства в этом контексте является ковалентное ингибирование ацивицином Pdx2, которое приводит к ингибированию роста паразитов (Gengenbacher et al., 2006). Однако ацивицин является известным ковалентным ингибитором глутаминаз в целом, и вопрос о специфическом ингибировании все еще требует дополнительных и окончательных исследований.( iii ) Ингибиторы суицида были предложены в контексте биосинтеза витамина de novo (Drebes et al., 2014), однако этот подход еще не оценивается для пути синтазы PLP. Для преодоления вышеупомянутых проблем и соответствующих вопросов потребуется синергетическое сотрудничество различных дисциплин, таких как биохимия, структурная и вычислительная биология, паразитология и медицинская химия.
Вклад авторов
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее для публикации.
Финансирование
Авторы выражают признательность Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) за финансовую поддержку в виде грантов 2015 / 26722-8, 2015 / 13684-0, 2020 / 03983-9, 2019 / 26428- 3, 2019 / 20219-3, 2018 / 21213-6, 2017 / 03966-4 и Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPQ) через грант № 303165 / 2018-9 и Кластер передового опыта «Advanced Imaging of Matter» Deutsche Forschungsgemeinschaft (DFG) — EXC 2056 — проект 3994, BMBF через гранты проекта 05K19GU4, 05K20GUB и 05K16GUA.Авторы также выражают признательность за поддержку гранта от HEC, Пакистан, в рамках проекта «Программа развития профессорско-преподавательского состава BZU Multan (стипендии на 100 докторов наук) (распоряжение премьер-министра)».
Конфликт интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу: https: // www.frontiersin.org/articles/10.3389/fcimb.2021.688380/full#supplementary-material
Ссылки
Barra, ALC, Dantas, L., de, OC, Morão, LG, Gutierrez, RF, Polikarpov, I., et al. . (2020). Основные метаболические пути как путь к ESKAPE от устойчивости к антибиотикам. Фронт. Публичное исцеление. 8, 26. doi: 10.3389 / fpubh.2020.00026
CrossRef Полный текст | Google Scholar
Бауэр, Дж. А., Беннет, Э. М., Бегли, Т. П., Иалик, С. Е. (2004). Трехмерная структура YaaE из Bacillus Subtilis, глутаминазы, участвующей в биосинтезе пиридоксаль-5′-фосфата. J. Biol. Chem. 279, 2704–2711. doi: 10.1074 / jbc.M310311200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Begum, A., Drebes, J., Kikhney, A., Müller, I. B., Perbandt, M., Svergun, D., et al. (2013). Тиаминаза II Staphylococcus Aureus: олигомеризация гарантирует протеолитическую защиту от сериновых протеаз. Acta Crystallogr. Разд. D Biol. Кристаллогр. 69, 2320–2329. doi: 10.1107 / S0
4 CrossRef Полный текст | Google Scholar
Чан, X.W. A., Wrenger, C., Stahl, K., Bergmann, B., Winterberg, M., Müller, I. B., et al. (2013). Химическая и генетическая проверка использования тиамина в качестве мишени противомалярийного препарата. Нат. Commun. 4 (2013), 2060. doi: 10.1038 / ncomms3060
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чаудхури, Б. Н., Ланге, С. К., Майерс, Р. С., Читтур, С. В., Дэвиссон, В. Дж., Смит, Дж. Л. (2001). Кристаллическая структура имидазолглицеринфосфатсинтазы. Структура 9, 987–997.DOI: 10.1016 / S0969-2126 (01) 00661-X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Клэнси, К. Дж., Нгуен, М. Х. (2020). Время покупки: Фонд действий против УПП и состояние разработки антибиотиков в США в 2020 г. Open Forum Infect. Дис. 7, 1–5. doi: 10.1093 / ofid / ofaa464
CrossRef Полный текст | Google Scholar
Derrer, B., Windeisen, V., Guédez Rodríguez, G., Seidler, J., Gengenbacher, M., Lehmann, W. D., et al. (2010). Определение структурных требований для связывания рибозо-5-фосфата и межсубъединичного перекрестного взаимодействия малярийной пиридоксаль-5-фосфат-синтазы. FEBS Lett. 584, 4169–4174. doi: 10.1016 / j.febslet.2010.09.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Dick, T., Manjunatha, U., Kappes, B., Gengenbacher, M. (2010). Биосинтез витамина B6 необходим для выживания и вирулентности Mycobacterium Tuberculosis. Мол. Microbiol. 78, 980–988. doi: 10.1111 / j.1365-2958.2010.07381.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дребес, Дж., Кунц, М., Перейра, К., Бецель, К., Ренджер, К. (2014). Инфекции MRSA: от классического лечения до суицидальных препаратов. Curr. Med. Chem. 21, 1809–1819. DOI: 10.2174 / 0
732066613111 20PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ehrenshaft, M., Bilski, P., Li, M., Chignell, C.F., Daub, M.E. (1999). Высококонсервативная последовательность представляет собой новый ген, участвующий в биосинтезе витамина B6 De Novo . Proc. Natl. Акад. Sci. США. 96, 9374–9378. DOI: 10.1073 / pnas.96.16.9374
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Gengenbacher, M., Fitzpatrick, T. B., Raschle, T., Flicker, K., Sinning, I., Müller, S., et al. (2006). Биосинтез витамина B6 малярийным паразитом Plasmodium Falciparum: биохимические и структурные исследования. J. Biol. Chem. 281, 3633–3641. doi: 10.1074 / jbc.M5086
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Gregori-Puigjané, E., Setola, V., Hert, J., Crews, B.A., Irwin, J.J., Lounkine, E., et al. (2012). Определение целевых механизмов действия для лекарств и зондов. Proc. Natl. Акад. Sci. США. 109, 11178–11183. DOI: 10.1073 / pnas.1204524109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Guédez, G., Hipp, K., Windeisen, V., Derrer, B., Gengenbacher, M., Böttcher, B., et al. (2012). Сборка эукариотического комплекса PLP-синтаза из плазмодия и активация фермента Pdx1. Строение 20, 172–184.doi: 10.1016 / j.str.2011.11.015
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Hanes, J. W., Keresztes, I., Begley, T. P. (2008). Захват хромофорного промежуточного соединения в катализируемом Pdx1 биосинтезе пиридоксаль-5′-фосфата. Angew. Chemie — Int. Эд. 47, 2102–2105. doi: 10.1002 / anie.200704390
CrossRef Полный текст | Google Scholar
IACG (2019). Не время ждать: защита будущего от лекарственно-устойчивых инфекций .(Межведомственная координационная группа по устойчивости к противомикробным препаратам).
Google Scholar
Каппес, Б., Тьюс, И., Бинтер, А., Macheroux, P. (2011). PLP-зависимые ферменты как потенциальные мишени для лекарств от простейших заболеваний. Biochim. Биофиз. Acta — Proteins Proteomics 1814, 1567–1576. doi: 10.1016 / j.bbapap.2011.07.018
CrossRef Полный текст | Google Scholar
Кейзер, М. Дж., Рот, Б. Л., Армбрустер, Б. Н., Эрнсбергер, П., Ирвин, Дж. Дж., Шойхет, Б. К. (2007).Связь белковой фармакологии с химией лигандов. Нат. Biotechnol. 25, 197–206. doi: 10.1038 / nbt1284
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ким, С., Ким, К. Дж. (2013). Кристаллическая структура Mycobacterium Tuberculosis Rv2606c: пиридоксальная лиаза биосинтеза. Biochem. Биофиз. Res. Commun. 435, 255–259. doi: 10.1016 / j.bbrc.2013.04.068
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Knöckel, J., Jordanova, R., Мюллер, И. Б., Ренгер, К., Гровс, М. Р. (2009). Подвижность консервативного глицина 155 необходима для образования активного плазмодийного додекамера Pdx1. Biochim. Биофиз. Acta — Gen. Subj. 1790, 347–350. doi: 10.1016 / j.bbagen.2009.02.016
CrossRef Полный текст | Google Scholar
Knöckel, J., Müller, I. B., Butzloff, S., Bergmann, B., Walter, R. D., Wrenger, C. (2012). Антиоксидантный эффект витамина B 6, продуцируемого De Novo, в Plasmodium Falciparum, подтвержденный белковыми интерференциями. Biochem. J. 443, 397–405. doi: 10.1042 / BJ20111542
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кроненбергер, Т., Линднер, Дж., Мейснер, К. А., Зимбрес, Ф. М., Коронадо, М. А., Зауэр, Ф. М. и др. (2014). Витамин B6-зависимые ферменты у малярийного паразита человека Plasmodium Falciparum: лекарственная мишень? BioMed. Res. Int. 2014 (2014), 1–11. doi: 10.1155 / 2014/108516
CrossRef Полный текст | Google Scholar
Мацуура, А., Юн, Дж. Й., Юн, Х.-Дж., Ли, Х. Х., Сух, С. У. (2012). Кристаллическая структура пиридоксальной биосинтезированной лиазы PdxS из Pyrococcus Horikoshii. Мол. Ячейки 34, 407–412. doi: 10.1007 / s10059-012-0198-8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Mouilleron, S., Golinelli-Pimpaneau, B. (2007). Конформационные изменения в аммиачно-канальных глютамин-амидотрансферазах. Curr. Opin. Struct. Биол. 17, 653–664. doi: 10.1016 / j.sbi.2007.09.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Müller, I.Б., Хайд, Дж. Э., Ренджер, К. (2010). Метаболизм витамина B в Plasmodium Falciparum как источник мишеней для лекарств. Trends Parasitol. 26, 35–43. DOI: 10.1016 / j.pt.2009.10.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Müller, I. B., Knöckel, J., Groves, M. R., Jordanova, R., Ealick, S. E., Walter, R. D., et al. (2008). Сборка синтазного комплекса плазмодий PLP следует определенному курсу. PloS One 3 (2008), e1815. DOI: 10,1371 / журнал.pone.0001815
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Neuwirth, M., Strohmeier, M., Windeisen, V., Wallner, S., Deller, S., Rippe, K., et al. (2009). Рентгеновская кристаллическая структура Saccharomyces Cerevisiae Pdx1 дает представление об олигомерной природе синтаз PLP. FEBS Lett. 583, 2179–2186. doi: 10.1016 / j.febslet.2009.06.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Percudani, R., Peracchi, A. (2009).База данных B6: инструмент для описания и классификации витамин B6-зависимой ферментативной активности и соответствующих семейств белков. BMC Bioinf. 10, 273. doi: 10.1186 / 1471-2105-10-273
CrossRef Полный текст | Google Scholar
Петтерсен, Э. Ф., Годдард, Т. Д., Хуанг, К. К., Коуч, Г. С., Гринблатт, Д. М., Мэн, Э. С. и др. (2004). UCSF Chimera? Система визуализации для поисковых исследований и анализа. J. Comput. Chem. 25, 1605–1612.doi: 10.1002 / jcc.20084
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Raschle, T., Speziga, D., Kress, W., Moccand, C., Gehrig, P., Amrhein, N., et al. (2009). Межсубъединичные перекрестные помехи в пиридоксаль-5′-фосфат-синтазе, координируемые С-концом синтазной субъединицы. J. Biol. Chem. 284, 7706–7718. doi: 10.1074 / jbc.M804728200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Reeksting, S. B., Müller, I. B., Burger, P.Б., Бургос, Э. С., Салмон, Л., Лоу, А. И. и др. (2013). Изучение ингибирования Pdx1, компонента синтазного комплекса PLP малярийного паразита человека Plasmodium Falciparum. Biochem. J. 449, 175–187. doi: 10.1042 / BJ20120925
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Робинсон, Г. К., Кауфманн, М., Ру, К., Фицпатрик, Т. Б. (2016). Структурное определение колебаний лизина в Arabidopsis Thaliana PDX1: промежуточный канал, способствующий биосинтезу витамина B 6. Proc. Natl. Акад. Sci. 113, E5821 – E5829. doi: 10.1073 / pnas.1608125113
CrossRef Полный текст | Google Scholar
Робинсон, Г. К., Кауфманн, М., Ру, К., Мартинес-Фонт, Дж., Хотхорн, М., Тор, С. и др. (2019). Кристаллическая структура псевдофермента PDX1.2 в комплексе с его когнитивным ферментом PDX1.3: полное затмение. Acta Crystallogr. Разд. D Struct. Биол. 75, 400–415. doi: 10.1107 / S205979831 12
CrossRef Полный текст | Google Scholar
Rodrigues, M.J., Windeisen, V., Zhang, Y., Guédez, G., Weber, S., Strohmeier, M., et al. (2017). Механизм ретрансляции лизина координирует промежуточный перенос в биосинтезе витамина B6. Нат. Chem. Биол. 13, 290–294. doi: 10.1038 / nchembio.2273
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Смит, А. М., Браун, В. К., Хармс, Э., Смит, Дж. Л. (2015). Кристаллические структуры захватывают три состояния в каталитическом цикле пиридоксальфосфатной (PLP) синтазы. J. Biol.Chem. 290, 5226–5239. doi: 10.1074 / jbc.M114.626382
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Strohmeier, M., Raschle, T., Mazurkiewicz, J., Rippe, K., Sinning, I., Fitzpatrick, T. B., et al. (2006). Структура бактериального пиридоксаль-5’-фосфат-синтазного комплекса. Proc. Natl. Акад. Sci. 103, 19284–19289. doi: 10.1073 / pnas.0604
3CrossRef Полный текст | Google Scholar
Ullah, N., Andaleeb, H., Mudogo, C. N., Falke, S., Бецель, К., Ренджер, К. (2020). Структуры решений и динамическая сборка 24-мерного плазмодиального комплекса Pdx1 – Pdx2. Внутр. J. Mol. Sci. 21, 1–15. doi: 10.3390 / ijms21175971
CrossRef Полный текст | Google Scholar
Volkamer, A., Kuhn, D., Grombacher, T., Rippmann, F., Rarey, M. (2012a). Комбинирование глобальных и локальных показателей для прогнозирования наркомании на основе структуры. J. Chem. Инф. Модель. 52, 360–372. doi: 10.1021 / ci200454v
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Volkamer, A., Кун, Д., Риппманн, Ф., Рэри, М. (2012b). Dogsitescorer: веб-сервер для автоматического прогнозирования, анализа и оценки возможности связывания сайтов. Биоинформатика 28, 2074–2075. doi: 10.1093 / биоинформатика / bts310
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Всемирная организация здравоохранения (2015 г.). Руководство по лечению малярии . (Всемирная организация здравоохранения).
Google Scholar
Всемирная организация здравоохранения (2020 г.). Всемирный доклад о малярии 2020: 20 лет глобального прогресса и вызовов . (Всемирная организация здравоохранения).
Google Scholar
Ренгер, К., Эшбах, М. Л., Мюллер, И. Б., Варнеке, Д., Вальтер, Р. Д. (2005). Анализ пути биосинтеза витамина B6 у малярийного паразита человека Plasmodium Falciparum. J. Biol. Chem. 280, 5242–5248. doi: 10.1074 / jbc.M412475200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Zein, F., Чжан, Ю., Кан, Ю. Н., Бернс, К., Бегли, Т. П., Иалик, С. Е. (2006). Структурные представления о механизме холофермента PLP-синтазы из Thermotoga Maritima. Биохимия 45, 14609–14620. doi: 10.1021 / bi061464y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Zhang, X., Teng, Y., Liu, J., He, Y., Zhou, K., Chen, Y., et al. (2010). Структурные представления о каталитическом механизме дрожжевой пиридоксаль-5-фосфат-синтазы Snz1. Biochem.J. 432, 445–454. doi: 10.1042 / BJ20101241
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжу, Дж., Бургнер, Дж. У., Хармс, Э., Белицкий, Б. Р., Смит, Дж. Л. (2005). Новое расположение (β / α) 8 стволов в синтазной субъединице PLP-синтазы. J. Biol. Chem. 280, 27914–27923. doi: 10.1074 / jbc.M503642200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
.

 Вспомогательное вещество: вода для инъекций — до 1 мл.
Вспомогательное вещество: вода для инъекций — до 1 мл.
 В составе комплексной терапии: При гипо- и авитаминозе В6, в неврологии — взрослым 50-100 мг/сут 1-2 раза в сутки. Курс лечения — 1 месяц. Детям — 20 мг/сут, курс лечения — 2 недели.
При паркинсонизме назначают по 100 мг/сут раствора в сутки внутримышечно, подкожно. Курс лечения — 20-25 инъекций. Через 2-3 месяца курс лечения повторяют.
При лечении туберкулеза гидразидом изоникотиновой кислоты (ГИНК) и ее производными (изониазидом, фтивазидом и др.) на 1 г введенного препарата необходимо назначать 100 мг пиридоксина (для предупреждения нарушений функций центральной нервной системы).
При лечении нейротоксичности, вызываемой ГИНК и ее производными — внутривенно 500-750 мг/сут раствора препарата.
При лечении пиридоксинзависимого судорожного синдрома у новорожденных — внутримышечно или внутривенно 100 мг пиридоксина.
В составе комплексной терапии: При гипо- и авитаминозе В6, в неврологии — взрослым 50-100 мг/сут 1-2 раза в сутки. Курс лечения — 1 месяц. Детям — 20 мг/сут, курс лечения — 2 недели.
При паркинсонизме назначают по 100 мг/сут раствора в сутки внутримышечно, подкожно. Курс лечения — 20-25 инъекций. Через 2-3 месяца курс лечения повторяют.
При лечении туберкулеза гидразидом изоникотиновой кислоты (ГИНК) и ее производными (изониазидом, фтивазидом и др.) на 1 г введенного препарата необходимо назначать 100 мг пиридоксина (для предупреждения нарушений функций центральной нервной системы).
При лечении нейротоксичности, вызываемой ГИНК и ее производными — внутривенно 500-750 мг/сут раствора препарата.
При лечении пиридоксинзависимого судорожного синдрома у новорожденных — внутримышечно или внутривенно 100 мг пиридоксина.
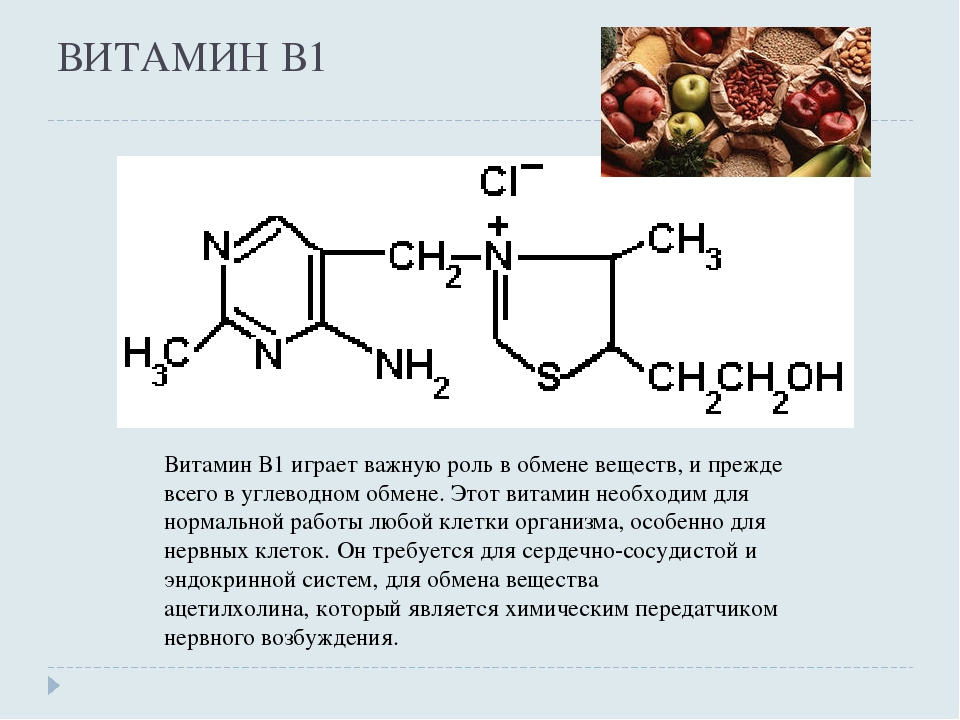 С осторожностью:
язвенная болезнь желудка и двенадцатиперстной кишки (в связи с возможным повышением кислотности желудочного сока), ишемическая болезнь сердца, тяжелые поражения печени.
Применение при беременности н в период грудного вскармливания. При беременности применение возможно только под контролем врача и только в случае, когда ожидаемый терапевтический эффект для матери превышает потенциальный риск для плода. Пиридоксин проникает через плаценту и выделяется в материнское молоко. Длительное использование пиридоксина в высоких дозах в период беременности и в период грудного вскармливания может приводить к развитию у детей «пиридоксиновой зависимости». Не рекомендуется превышать нормы физиологической потребности в пиридоксине в период беременности (2 мг/сут). Пиридоксин усиливает синтез дофамина (который выполняет роль пролакгостатина) и подавляет лактацию, вплоть до ее полного прекращения. При необходимости применение препарата в период лактации грудное вскармливание следует прекратить.
С осторожностью:
язвенная болезнь желудка и двенадцатиперстной кишки (в связи с возможным повышением кислотности желудочного сока), ишемическая болезнь сердца, тяжелые поражения печени.
Применение при беременности н в период грудного вскармливания. При беременности применение возможно только под контролем врача и только в случае, когда ожидаемый терапевтический эффект для матери превышает потенциальный риск для плода. Пиридоксин проникает через плаценту и выделяется в материнское молоко. Длительное использование пиридоксина в высоких дозах в период беременности и в период грудного вскармливания может приводить к развитию у детей «пиридоксиновой зависимости». Не рекомендуется превышать нормы физиологической потребности в пиридоксине в период беременности (2 мг/сут). Пиридоксин усиливает синтез дофамина (который выполняет роль пролакгостатина) и подавляет лактацию, вплоть до ее полного прекращения. При необходимости применение препарата в период лактации грудное вскармливание следует прекратить.


 Лечение: препарат отменяют. Лечение симптоматическое. Специального антидота нет. Симптомы передозировки быстро проходят после отмены препарата.
Лечение: препарат отменяют. Лечение симптоматическое. Специального антидота нет. Симптомы передозировки быстро проходят после отмены препарата.
 Фармацевтически несовместим с тиамином (B1|) и цианокобаламином (В12). Комбинируется с сердечными гликозидами, глутаминовой кислотой и калия и магния аспарагинатом.
Фармацевтически несовместим с тиамином (B1|) и цианокобаламином (В12). Комбинируется с сердечными гликозидами, глутаминовой кислотой и калия и магния аспарагинатом.
